Natura della luce. Qualsiasi tipo di onda è caratterizzato da:
|
|
|
- Mario Molinari
- 8 anni fa
- Visualizzazioni
Transcript
1 Natura della luce James C. Maxwell ( ) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica A una particella carica che oscilla è associato un campo elettrico e un campo magnetico che oscillano in direzioni perpendicolari. Qualsiasi tipo di onda è caratterizzato da: ampiezza (A): altezza di un massimo (o profondità di un minimo) lunghezza d onda (λ): distanza tra due massimi o minimi consecutivi frequenza (ν): numero di cicli d onda che passano per un determinato punto nell unità di tempo. Unità di frequenza è l hertz (Hz = 1/s = s -1 ) La velocità alla quale un onda si muove attraverso lo spazio è definita dalla relazione: v = λ ν L energia per unità di volume posseduta da un onda è proporzionale a A 2
2 Campo elettrico della radiazione elettromagnetica Il campo elettrico della radiazione elettromagnetica oscilla nello spazio e nel tempo. La figura rappresenta un istantanea dell onda elettromagnetica in un dato momento. La lunghezza della freccia in un punto qualsiasi rappresenta la forza che il campo esercita in quel punto su una particella carica Per la luce la velocità (c) nel vuoto è costante: c = 3, m s -1 (1072 milioni di km/h)
3 La radiazione di lunghezza d onda corta presenta frequenza più alta e viceversa a) La freccia verticale mostra come il campo elettrico cambi marcatamente in cinque istanti successivi. b)negli stessi cinque istanti il campo elettrico di una radiazione di lunghezza d onda maggiore cambia molto meno. La freccia orizzontale mostra che in entrambi i casi l onda ha percorso lo stesso cammino
4 Lo spettro elettromagnetico: insieme di tutte le onde elettromagnetiche Figura 5-12 Dispersione della luce visibile in un prisma. La luce visibile è solo una piccola parte dello spettro della radiazione elettromagnetica
5 Dispersione della luce visibile in un prisma
6 Interferenza e diffrazione proprietà della luce che suggeriscono un comportamento ondulatorio Se nel loro cammino le onde incontrano un ostacolo, esse modificano il loro percorso. Questa proprietà è nota come diffrazione Le creste dell onda elettromagnetica sono rappresentate da linee. L onda lineare che incide su due fenditure poco distanti genera onde circolari Nei punti in cui l interferenza è costruttiva lo schermo posto dietro la fenditura mostra una riga luminosa. Dove è distruttiva lo schermo appare scuro
7 Interferenza costruttiva e interferenza negativa a) Se due onde sono in concordanza di fase, ovvero i loro picchi arrivano nello stesso punto allo stesso istante, l ampiezza dell onda risultante è la somma delle due ampiezze: la lunghezza d onda non cambia b) Se le onde che arrivano sullo stesso punto sono in opposizione di fase l intensità della radiazione sarà minore (o nulla)
8 La quantizzazione dell energia: equazione di Planck Un metallo riscaldato emette radiazione elettromagnetica con lunghezze d onda (λ) che dipendono dalla temperatura (T) Spettro della radiazione elettromagnetica emessa da un corpo riscaldato. Ins. Fig pag 293 Kotz La linea tratteggiata rappresenta lo spettro del corpo riscaldato al calor rosso perché la λ che corrispondente alla massima intensità è nella regione del rosso. Aumentando la T il colore della luce emessa dall oggetto diventa più arancio e poi giallo. A temperature molto alte (corrispondenti al calor bianco ) l oggetto emette radiazioni luminose in tutte le regioni dello spettro visibile: tutte le radiazioni visibili hanno intensità dello stesso ordine di grandezza.
9 Alla fine del secolo XIX si pensava che gli atomi dell oggetto riscaldato vibrassero (oscillatore armonico) emettendo in tal modo radiazioni elettromagnetiche (onde luminose) aventi qualsiasi frequenza. Max Planck ( ) propose un idea rivoluzionaria: quando un oggetto emette una radiazione, ci deve essere una quantità minima di energia che può essere emessa ad ogni dato istante. Ciò significa che esiste un pacchetto di energia tale che quantità ad esso inferiori non possano essere emesse. (In analogia al concetto di atomo, che è il pacchetto più piccolo di ogni elemento) Plank (1900) chiamò quanto il suo pacchetto di energia (plurale: quanti) e stabilì che l energia di un quanto dipende dalla frequenza della radiazione secondo la relazione: E quanto = h ν radiazione h = costante di Planck (6, J s) Energia di un quanto di radiazione = (costante di Plank) (frequenza della radiazione) Tutta l energia ceduta o acquistata da un atomo, a una certa frequenza, deve corrispondere ad un multiplo di quel minimo per un numero intero n. Cioè: Energia = n (h ν) Nel 1918 M. Planck fu insignito del Nobel per la fisica
10 NATURA CORPUSCOLARE DELLA LUCE Il fenomeno che non si accorda con la natura ondulatoria della luce è l effetto fotoeletrico (Hertz, 1888). Quando una radiazione elettromagnetica sufficientemente energetica colpisce la superficie di un metallo (elettrodo negativo) posto in un tubo sottovuoto, alcuni elettroni sono emessi dal metallo e creano una corrente elettrica 1. Per ogni metallo esiste una frequenza della luce ν al di sotto della quale non si ha emissione di elettroni (gli elettroni emessi sono chiamati fotoelettroni) 2. Usando frequenze ν maggiori di ν l energia cinetica degli elettroni emessi è proporzionale a ν - ν 3. Il numero di elettroni emessi è proporzionale all intensità della luce ma la loro energia cinetica non dipende dall intensità della luce 4. Gli elettroni sono emessi dalla superficie del metallo quasi istantaneamente, anche quando la luce ha intensità molto bassa.
11 Dualismo onda-particella della luce Secondo la fisica classica, poiché l energia di un onda elettromagnetica dipende dalla sua ampiezza ma non dalla sua frequenza, l energia cinetica degli elettroni emessi dovrebbe essere indipendente dalla frequenza e la luce di qualsiasi frequenza dovrebbe provocare emissione di elettroni: La teoria ondulatoria della luce non spiega quindi i fatti osservati nell effetto fotoelettrico Einstein decise che tutte le osservazioni sperimentali potevano essere spiegate combinando la teoria di Planck dei quanti di energia con la nozione che la luce possieda non soltanto proprietà tipiche delle onde ma anche proprietà tipiche delle particelle Einstein assunse che queste particelle prive di massa, oggi chiamate fotoni, trasportassero l energia che può essere calcolata dall equazione di Plank: questo significa che l energia di ogni fotone in una corrente di fotoni è proporzionale alla frequenza della sua onda
12 Spiegazione dell effetto fotoelettrico: Einstein (1905) Un raggio di luce consiste di piccoli pacchetti di energia chiamati quanti di luce o fotoni L energia di un fotone è proporzionale alla sua frequenza secondo la relazione: E = hνh h costante di Planck (6, J s) Quando un fotone colpisce la superficie del metallo trasferisce tutta la sua energia ad un elettrone Parte di tale energia, indicata con φ (phi), viene utilizzata dall elettrone per vincere le forze che lo tengono legato al metallo, quella rimanente costituisce l energia cinetica. Energia del fotone = (energia necessaria all elettrone per lasciare il metallo) + (energia cinetica dell elettrone) ½ m e v 2 = hν - φ Quando la frequenza della luce è minore del valore critico ν l energia assorbita da un elettrone è minore dell energia φ necessaria all elettrone per lasciare la superficie e quindi non si ha emissione di elettroni Quando il fotone ha il valore critico ν si ha: ½ m e v 2 = h ν - φ = h ν - h ν = 0 L elettrone viene emesso con energia cinetica nulla
13 Effetto fotoelettrico Aumentando la frequenza della luce gli elettroni che vengono emessi hanno energie cinetiche maggiori: ½ m e v 2 = h ν - φ = h ν - h ν = h (ν( - ν ) L energia cinetica degli elettroni espulsi varia linearmente con la frequenza della radiazione incidente I metalli che cedono più facilmente elettroni sono i metalli alcalini (I gruppo). La luce rossa, avendo elevata lunghezza d onda (bassa frequenza) produce effetto fotoelettrico nel rubidio (Rb) ma non nel sodio (Na).
14 Spettri di righe degli atomi e Niels BOHR Un ruolo importante nello sviluppo delle teorie moderne sulla struttura degli atomi è l osservazione delle luce emessa dagli atomi che hanno assorbito energia dall esterno. Lo spettro della luce bianca, come quella emessa dal sole o da una lampada a incandescenza, consiste in una sequenza di colori (arcobaleno) Questo spettro che contiene tutte le lunghezze d onda è detto spettro continuo
15 Spettri a righe Se si applica una differenza di potenziale elevata a un elemento in fase gassosa a bassa pressione, gli atomi assorbono energia: assumono un stato eccitato Gli atomi eccitati emettono luce. Ad es. il neo (a sinistra), l argo (al centro) o il mercurio (a destra) emettono luce nella regione del visibile che, osservata attraverso un prisma si osserva come uno spettro a righe
16 SPETTRI ATOMICI Un ottimo esempio che illustra la quantizzazione dell energia è fornito dai fenomeni di emissione e di assorbimento di radiazione elettromagnetica da parte di atomi isolati. a) Spettri di emissione (insieme delle radiazioni emesse) nella regione del visibile per alcuni elementi b) Spettro di assorbimento dell idrogeno
17 Spettro atomico dell idrogeno a) Spettro di emissione: la luce emessa da un campione di atomi di idrogeno eccitati (o di qualsiasi altro elemento) può essere fatta passare attraverso un prisma e separata in ben precise lunghezze d onda. Si ottiene uno spettro a righe. b) Spettro di assorbimento: quando la luce bianca passa attraverso degli atomi di idrogeno non eccitati e successivamente attraverso una fenditura e un prisma, la radiazione trasmessa manca di alcune lunghezze d onda che sono le stesse emesse eccitando la sostanza.
18 Spettro dell idrogeno Facendo passare luce bianca attraverso atomi di idrogeno, tutta la luce viene trasmessa tranne quella avente lunghezza d onda 3835 Å, 3889 Å 3970Å, 4101 Å, 4340 Å (blu), 4861 Å (verde), 6563 Å (rosso) Johann Balmer (insegnante di musica svizzero, 1855) fu in grado di calcolare le lunghezze d onda delle tre righe più brillanti della parte visibile dello spettro dell idrogeno (riga rossa, verde e azzurra).
19 Successivamente Rydberg ( ) espresse la relazione nella forma: 1/λ = R( 1/2 2 1/n 2 ) n = 3, 4, 5. R = 1,097x10 7 m -1 (cost. di Rydberg) Niels Bohr ( ) fu il primo a trovare una relazione tra gli spettri di emissione degli atomi eccitati e le idee quantistiche di Planck e Einstein Dal lavoro di Rutherford si sapeva che gli elettroni negli atomi sono disposti al di fuori del nucleo: Bohr propose che, per l atomo più semplice, l elettrone si muovesse in un orbita circolare intorno al nucleo Inoltre, per risolvere il problema della stabilità dell atomo, egli introdusse il concetto che l elettrone nell atomo di H può occupare solo certe orbite o livelli energetici (o stati stazionari) Combinando questo postulato di quantizzazione con le leggi del moto della fisica classica Bohr mostrò che l energia posseduta dall elettrone dell atomo di H, nel suo n stato stazionario, è data dalla relazione molto semplice: Energia = E n = - Rhc/n 2 R è una costante di proporzionalità che riproduce con molta accuratezza la costante di Rydberg, h è la costante di Planck, e c è la velocità della luce
20 Livelli energetici nell atomo di idrogeno Il fatto che si osservino righe spettrali distinte lascia intendere che nell atomo un elettrone può avere solo certe energie. Quando l elettrone subisce una transizione da un livello energetico superiore a uno inferiore, l atomo perde energia. Questa energia viene emessa sotto forma di fotoni hν = E sup - E inf Condizione della frequenza di Bohr Ciascuna riga spettrale deriva da una specifica transizione Quanto maggiore è la perdita di energia tanto maggiore è la frequenza della radiazione emessa
21 Livelli energetici nell atomo di idrogeno Tutte le righe dello spettro dell idrogeno possono essere calcolate con la formula: 1/λ = R(1/n 12-1/n 22 ) n 1 = 1, 2, ; n 2 = n 1 + 1, n 1 + 2, R è una costante determinata sperimentalmente (costante di Rydberg = 3,29x10 15 Hz ovvero 1,0974x10 7 m) I livelli energetici dell atomo di idrogeno sono descritti dalla relazione: E n = - Rhc/n 2 Lo zero dell energia corrisponde a una situazione in cui l elettrone e il protone sono a distanza infinita (energia potenziale nulla)
22 Il modello atomico di Bohr In diagramma sono riportati i valori dell energia (espressa in J/atomo) in funzione di n E = -Rhc/n 2 La differenza fra due livelli successivi dell energia diventa sempre più piccola all aumentare di n Bohr (premio Nobel 1922) ebbe il merito di collegare l invisibile (l interno dell atomo) con il visibile (le righe che si osservano nello spettro dell idrogeno). Tuttavia il suo modello di atomo è scorretto!!
23 Livelli energetici dell elettrone nell atomo di idrogeno L energia dell elettrone in un atomo di idrogeno dipende dal valore del numero quantico n L energia è espressa in J/atomo La differenza fra i diversi livelli energetici diventa sempre più piccola all aumentare di n
24 L atomo descritto per mezzo della meccanica ondulatoria I fotoni sono privi di massa propria, ma possono essere visti come corpuscoli di cui si può calcolare la quantità di moto ricorrendo alla relazione dell equivalenza tra massa ed energia di Einstein: E = mc 2 ; E = hν mc 2 = hν mc = hν/c = h/λ Questa equazione correla la quantità di moto con la frequenza o con la lunghezza d onda della radiazione elettromagnetica Se la luce può essere descritta tanto in termini ondulatori che in termini particellari, perché il resto della materia non dovrebbe comportarsi nello stesso modo? Luis Victor de Broglie (1925) ipotizzò anche per i corpi materiali un comportamento ondulatorio: hν = mv 2 ; ν = v/λ; λ = h/mv = h/p la lunghezza d onda associata ad una particella, avente massa m e velocità v è inversamente proporzionale alla quantità di moto del corpo. (Il prodotto di una massa per la velocità si chiama momento lineare: mv = p)
25 Dualismo onda-corpuscolo della materia La materia può avere proprietà ondulatorie? (Louis de Broglie, 1925) La massa di un elettrone è 9,11x10-31 kg. La lunghezza d onda di un elettrone che si muove alla velocità di 6, m s -1 è 1,19x10-10 m = 119 pm Questa lunghezza d onda è confrontabile con quella dei raggi X G.P.Thomson (figlio dello scopritore dell elettrone) dimostrò che gli elettroni producono una figura di diffrazione attraversando una lamina sottile di oro Gli elettroni (e la materia in generale) possiedono proprietà ondulatorie!! L ipotesi formulata da de Broglie che gli elettroni posseggano anche caratteristiche ondulatorie ha portato alla tecnica della microscopia elettronica
26 Principio di indeterminazione di Heisemberg (1927) La posizione e il momento di una particella sono complementari, cioè risulta impossibile conoscere simultaneamente con precisione il momento e la posizione di una particella Se si conosce la posizione di una particella con una incertezza pari a x, il momento lineare parallelo all asse x si può conoscere solo con incertezza p tale per cui: x p h/4π a) Se la posizione della particella è mal definita il momento(freccia) è noto con accettabile precisione b) Se la posizione è ben definita, non è possibile specificare il momento con grande precisione
27 Principio di indeterminazione e probabilità Come può un elettrone essere contemporaneamente descritto come particella e come onda? In nessun modo!! Se si decide di conoscere l energia di un elettrone in un atomo con solamente una piccola incertezza, allora si deve accettare una incertezza molto elevata nella sua posizione nello spazio intorno al nucleo. In pratica, ciò che ci è permesso di fare è calcolare la probabilità di trovare un elettrone di un certo contenuto energetico in una certa regione di spazio
28 La visione quantomeccanica dell atomo Gli elettroni negli atomi possono essere più efficacemente trattati come onde piuttosto che come particelle compatte che si muovono lungo orbite circolari o ellittiche Gli atomi e le molecole possono esistere solo in certi stati energetici. In ciascuno di questi stati, l atomo o la molecola possiede una determinata energia. Quando l atomo o la molecola cambia il suo stato energetico deve emettere od assorbire la quantità esatta di energia per passare al nuovo stato. Quando gli atomi (o molecole) emettono od assorbono radiazione elettromagnetica (luce), essi variano il loro stato energetico. La variazione di energia subita è correlata alla frequenza o alla lunghezza d onda della luce emessa o assorbita secondo l equazione: E = hν ovvero E = hc/λ L energia persa (o guadagnata) da un atomo quando passa da un livello energetico superiore ad uno inferiore (o viceversa) è uguale all energia del fotone emesso o assorbito durante la transizione I livelli energetici permessi per gli atomi e le molecole possono essere descritti da un insieme di numeri definiti numeri quantici
29 Onde stazionarie ristrette entro una dimensione Quando una corda fissata alle due estremità (come in una chitarra) viene pizzicata, essa mostra parecchie vibrazioni (modi normali). Essendo fissi, i punti estremi non possono muoversi. Ogni possibile differente vibrazione è un onda stazionaria e può essere descritta da una funzione d onda. Le sole onde possibili sono quelle nelle quali si può formare lungo la corda un numero intero di mezze lunghezze d onda. Queste onde costituiscono una serie armonica L insieme delle vibrazioni possibili obbediscono alla relazione: L = n λ/2 in cui L è la lunghezza della corda ed n è un numero intero (numero quantico) Per n = 1 si ha la vibrazione a più bassa energia
30 Non sono permesse altre vibrazioni. Per esempio, nel caso di una vibrazione in cui L = 1,25 λ, l onda risultante non sarebbe stazionaria. Nel tempo darebbe interferenza con distruzione della vibrazione!
31 Onde stazionarie ristrette ad una superficie La percussione al centro della superficie (es. un tamburo) genera una vibrazione senza nodi a bassa energia (n = 1). La superficie si alza (o si abbassa) tutta. La percussione centrale può generare anche una vibrazione a energia più alta (n = 2) che presenta un nodo (la superficie è sollevata al centro e abbassata alla periferia Quando la percussione avviene alla periferia della superficie si possono avere altri tipi di vibrazioni In questo caso esistono 2 numeri quantici indicati con n e l. Per n = 1 l vale 0; per n = 2 l può assumere i valori 0 e 1
32 Modello quanto-meccanico dell atomo L energia cinetica di un elettrone è inversamente correlata al volume della regione in cui è confinato Quando l elettrone si avvicina al nucleo l energia elettrostatica diminuisce; cioè essa diventa sempre più negativa. Contemporaneamente l energia cinetica aumenta in quanto l elettrone si muove all interno di un volume sempre più piccolo. I due effetti si oppongono tra loro: l atomo risulta stabile Non è possibile indicare l esatta posizione di un elettrone in un atomo in un dato istante e non è possibile descrivere con esattezza la traiettoria che l elettrone compie attorno al nucleo: il massimo che possiamo fare è stimare la probabilità di trovare l elettrone all interno di una particolare regione
33 Equazione d onda di Schröedinger Secondo la meccanica ondulatoria il comportamento di una particella, quale l elettrone, è definito da un equazione matematica (nota come equazione d onda di Schröedinger), le cui soluzioni, dette funzioni d onda, ψ, descrivono gli stati possibili della particella. ψ (psi) rappresenta una delle infinite funzioni d onda che sono soluzioni dell equazione d onda: 2 ψ/ x ψ/ y ψ/ z π 2 m /h 2 (E-V) ψ = 0 E è il valore di energia (E 1, E 2, ecc.) dello stato descritto dalla particolare funzione d onda e V è l energia potenziale della particella. ψ non ha un significato fisico definito ma il suo quadrato (ψ 2 ), calcolato in un dato punto di coordinate x,y,z, misura la probabilità che ha l elettrone di trovarsi in un elemento infinitesimo di volume dv centrato sul punto medesimo.
34 Funzioni d onda Le funzioni d onda caratterizzano l elettrone come un onda di materia L elettrone è descritto da onde stazionarie Soltanto alcune funzioni d onda sono permesse: esse sono chiamate orbitali Ad ogni funzione d onda ψ corrisponde a un energia permessa per l elettrone: l energia dell elettrone è quantizzata Ogni funzione d onda (o orbitale) è caratterizzato da tre numeri quantici: n, l, m l Il numero quantico principale n determina l energia dell elettrone attraverso la relazione: E n = - Rhc/n 2 R, h e c sono costanti, quindi l energia dell elettrone nell atomo di idrogeno varia solo con il valore di n
35 Tre dimensioni, tre numeri quantici Le soluzioni delle equazioni di Schrödinger (1926) per l atomo di idrogeno sono funzioni d onda che descrivono gli stati possibili per il singolo elettrone 1. Numero quantico principale, n, definisce il livello di energia. Può assumere tutti i valori interi positivi: n = 1, 2, 3, Numero quantico azimutale (o numero quantico di momento angolare) l. Descrive la forma della regione di spazio che un elettrone può occupare. Può assumere tutti i valori interi e positivi tra 0 e (n 1). 3. Numero quantico magnetico, m l, dal quale dipende l orientazione spaziale dell orbitale. Può assumere ogni valore intero tra l e +l. Esso impone la quantizzazione della direzione
36 Per ogni valore di n esistono n 2 orbitali Nell atomo di H (e in tutti gli atomi idrogenoidi, cioè che hanno un solo elettrone come in He +, Li 2+ ) tutti gli orbitali che hanno lo stesso valore di n formano un guscio, così identificato: n K L M N.. Per es. i 4 orbitali del guscio con n = 2 formano il guscio L dell atomo Orbitali con lo stesso valore di n ma differenti valori di l appartengono a differenti sottogusci dello stesso guscio: questi sono indicati con le lettere s, p,. usando la seguente corrispondenza: l s p d f.. Ogni sottoguscio contiene 2l + 1 orbitali Un orbitale con l = 0 è chiamato orbitale s; il sottoguscio p (con l = 1) consiste di tre orbitali p
37 Orbitali atomici
38 Nube elettronica nell orbitale 1s La nube elettronica tridimensionale che corrisponde a un elettrone nell orbitale 1s dell idrogeno La densità dell ombreggiatura rappresenta la probabilità di trovare l elettrone nei vari punti Il grafico sovrapposto mostra come varia la probabilità al variare della distanza del punto dal nucleo lungo un raggio qualunque A una distanza di 250 pm dal nucleo la probabilità di trovare l elettrone è praticamente nulla
39 La distribuzione radiale Densità di probabilità radiale o funzione di distribuzione radiale, 4πr 2 ψ 2, diagrammata in funzione di r (distanza dell elettrone dal nucleo). Il massimo della funzione si ha a 53 pm
40 I tre orbitali s di minore energia Funzione di distribuzione radiale Superficie sferica entro la quale sussiste una probabilità elevata (90%) di trovare l elettrone
41 Orbitali p Superficie dei contorni e variazione radiale dell orbitale 2p lungo l asse z (verticale)
42 Figura 5-23 Le orientazioni relative di un insieme di orbitali p.
43 Orbitali d
44 Orbitali f
45 Il numero quantico magnetico di spin m s L elettrone possiede la proprietà dello spin: essa è descritta dal numero quantico m s che può assumere i valori +1/2 e 1/2 I due stati di spin si possono rappresentare con una rotazione oraria o antioraria intorno ad un asse passante per l elettrone
46 Atomi multielettronici Dato che gli elettroni in differenti tipi di orbitali hanno un diverso potere schermante della carica nucleare, negli atomi polielettronici l ordine dell energia degli orbitali di un determinato strato risulta di norma s <p < d < f Energia relativa di strati, sottostrati e orbitali in un atomo multielettronico. Ciascun quadratino può contenere al massimo due elettroni
Da Newton a Planck. La struttura dell atomo. Da Newton a Planck. Da Newton a Planck. Meccanica classica (Newton): insieme
 Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Struttura Elettronica degli Atomi
 Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
May 5, 2013. Fisica Quantistica. Monica Sambo. Sommario
 May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
IL MODELLO ATOMICO DI BOHR
 IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
La propagazione delle onde luminose può essere studiata per mezzo delle equazioni di Maxwell. Tuttavia, nella maggior parte dei casi è possibile
 Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Fisica II - CdL Chimica. La natura della luce Ottica geometrica Velocità della luce Dispersione Fibre ottiche
 La natura della luce Ottica geometrica Velocità della luce Dispersione Fibre ottiche La natura della luce Teoria corpuscolare (Newton) Teoria ondulatoria: proposta già al tempo di Newton, ma scartata perchè
La natura della luce Ottica geometrica Velocità della luce Dispersione Fibre ottiche La natura della luce Teoria corpuscolare (Newton) Teoria ondulatoria: proposta già al tempo di Newton, ma scartata perchè
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione
 Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
Capitolo 4 Le spettroscopie. 1. Lo spettro elettromagnetico
 Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Il fotone. Emanuele Pugliese, Lorenzo Santi URDF Udine
 Il fotone Emanuele Pugliese, Lorenzo Santi URDF Udine Interpretazione di Einstein dell effetto fotoelettrico Esistono «particelle»* di luce: i fotoni! La luce è composta da quantità indivisibili di energia
Il fotone Emanuele Pugliese, Lorenzo Santi URDF Udine Interpretazione di Einstein dell effetto fotoelettrico Esistono «particelle»* di luce: i fotoni! La luce è composta da quantità indivisibili di energia
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
LE PARTICELLE ELEMENTARI: loro scoperta
 LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
Gli orbitali: modello atomico probabilistico
 1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
19 Il campo elettrico - 3. Le linee del campo elettrico
 Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Il metodo scientifico
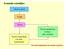 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
ENERGIA. Energia e Lavoro Potenza Energia cinetica Energia potenziale Principio di conservazione dell energia meccanica
 1 ENERGIA Energia e Lavoro Potenza Energia cinetica Energia potenziale Principio di conservazione dell energia meccanica 2 Energia L energia è ciò che ci permette all uomo di compiere uno sforzo o meglio
1 ENERGIA Energia e Lavoro Potenza Energia cinetica Energia potenziale Principio di conservazione dell energia meccanica 2 Energia L energia è ciò che ci permette all uomo di compiere uno sforzo o meglio
Tutte le tecniche spettroscopiche si basano sulla interazione tra radiazione elettromagnetica e materia.
 G. Digilio - principi_v10 versione 6.0 LA SPETTROSCOPIA Tutte le tecniche spettroscopiche si basano sulla interazione tra radiazione elettromagnetica e materia. La Spettroscopia di risonanza magnetica
G. Digilio - principi_v10 versione 6.0 LA SPETTROSCOPIA Tutte le tecniche spettroscopiche si basano sulla interazione tra radiazione elettromagnetica e materia. La Spettroscopia di risonanza magnetica
Einstein ci dice che la luce è costituita da unità elementari chiamate fotoni. Cosa sono questi fotoni?
 La natura della luce Einstein ci dice che la luce è costituita da unità elementari chiamate fotoni. Cosa sono questi fotoni? Se si potesse fotografare un fotone in un certo istante vedremmo una deformazione
La natura della luce Einstein ci dice che la luce è costituita da unità elementari chiamate fotoni. Cosa sono questi fotoni? Se si potesse fotografare un fotone in un certo istante vedremmo una deformazione
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
Prova scritta intercorso 2 31/5/2002
 Prova scritta intercorso 3/5/ Diploma in Scienza e Ingegneria dei Materiali anno accademico - Istituzioni di Fisica della Materia - Prof. Lorenzo Marrucci Tempo a disposizione ora e 45 minuti ) Un elettrone
Prova scritta intercorso 3/5/ Diploma in Scienza e Ingegneria dei Materiali anno accademico - Istituzioni di Fisica della Materia - Prof. Lorenzo Marrucci Tempo a disposizione ora e 45 minuti ) Un elettrone
13. Campi vettoriali
 13. Campi vettoriali 1 Il campo di velocità di un fluido Il concetto di campo in fisica non è limitato ai fenomeni elettrici. In generale il valore di una grandezza fisica assegnato per ogni punto dello
13. Campi vettoriali 1 Il campo di velocità di un fluido Il concetto di campo in fisica non è limitato ai fenomeni elettrici. In generale il valore di una grandezza fisica assegnato per ogni punto dello
I modelli atomici da Dalton a Bohr
 1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA MATERIA MATERIA. COMPOSIZIONE (struttura) Atomi che la compongono
 LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
PARTICELLE SUBATOMICHE
 MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose.
 Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
Istituzioni di fisica della materia I Lezione 3. S. Solimeno lezione 3 1
 Istituzioni di fisica della materia I Lezione 3 S. Solimeno lezione 3 1 S. Solimeno lezione 3 2 S. Solimeno lezione 3 3 S. Solimeno lezione 3 4 S. Solimeno lezione 3 5 spettroscopia gamma di colori che
Istituzioni di fisica della materia I Lezione 3 S. Solimeno lezione 3 1 S. Solimeno lezione 3 2 S. Solimeno lezione 3 3 S. Solimeno lezione 3 4 S. Solimeno lezione 3 5 spettroscopia gamma di colori che
La corrente elettrica
 PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR
 LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR LIMITI DEL MODELLO ATOMICO DI RUTHERFORD Il modello atomico planetario di Ernest Rutherford, seppure rappresentava un grande passo avanti rispetto al modello
LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR LIMITI DEL MODELLO ATOMICO DI RUTHERFORD Il modello atomico planetario di Ernest Rutherford, seppure rappresentava un grande passo avanti rispetto al modello
V= R*I. LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro.
 LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
Università degli studi di Messina facoltà di Scienze mm ff nn. Progetto Lauree Scientifiche (FISICA) Prisma ottico
 Università degli studi di Messina facoltà di Scienze mm ff nn Progetto Lauree Scientifiche (FISICA) Prisma ottico Parte teorica Fenomenologia di base La luce che attraversa una finestra, un foro, una fenditura,
Università degli studi di Messina facoltà di Scienze mm ff nn Progetto Lauree Scientifiche (FISICA) Prisma ottico Parte teorica Fenomenologia di base La luce che attraversa una finestra, un foro, una fenditura,
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
IL FOTOVOLTAICO E L ARCHITETTURA
 IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Induzione magnetica. Corrente indotta. Corrente indotta. Esempio. Definizione di flusso magnetico INDUZIONE MAGNETICA E ONDE ELETTROMAGNETICHE
 Induzione magnetica INDUZIONE MAGNETICA E ONDE ELETTROMAGNETICHE Che cos è l induzione magnetica? Si parla di induzione magnetica quando si misura una intensità di corrente diversa da zero che attraversa
Induzione magnetica INDUZIONE MAGNETICA E ONDE ELETTROMAGNETICHE Che cos è l induzione magnetica? Si parla di induzione magnetica quando si misura una intensità di corrente diversa da zero che attraversa
Nome..Cognome.. Classe 4G 4 dicembre 2008. VERIFICA DI FISICA: lavoro ed energia
 Nome..Cognome.. Classe 4G 4 dicembre 8 VERIFIC DI FISIC: lavoro ed energia Domande ) Energia cinetica: (punti:.5) a) fornisci la definizione più generale possibile di energia cinetica, specificando l equazione
Nome..Cognome.. Classe 4G 4 dicembre 8 VERIFIC DI FISIC: lavoro ed energia Domande ) Energia cinetica: (punti:.5) a) fornisci la definizione più generale possibile di energia cinetica, specificando l equazione
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Campione sciolto in un solvente (deuterato) e. posto in un tubo. di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm
 posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia. Francesco Nobili
 Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
APPUNTI DI RISONANZA MAGNETICA NUCLEARE Dr. Claudio Santi. CAPITOLO 1 NMR Risonanza Magnetica Nucleare
 APPUNTI DI RISONANZA MAGNETICA NUCLEARE Dr. Claudio Santi CAPITOLO 1 NMR Risonanza Magnetica Nucleare INTRODUZIONE Nel 1946 due ricercatori, F. Block ed E.M.Purcell, hanno indipendentemente osservato per
APPUNTI DI RISONANZA MAGNETICA NUCLEARE Dr. Claudio Santi CAPITOLO 1 NMR Risonanza Magnetica Nucleare INTRODUZIONE Nel 1946 due ricercatori, F. Block ed E.M.Purcell, hanno indipendentemente osservato per
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
L osservazione in luce bianca è, per così dire, l osservazione del Sole al naturale ovviamente dopo averne attenuato la fortissima emissione di luce.
 L osservazione in luce bianca è, per così dire, l osservazione del Sole al naturale ovviamente dopo averne attenuato la fortissima emissione di luce. Questa attenuazione si ottiene mediante l uso di un
L osservazione in luce bianca è, per così dire, l osservazione del Sole al naturale ovviamente dopo averne attenuato la fortissima emissione di luce. Questa attenuazione si ottiene mediante l uso di un
1 3 STRUTTURA ATOMICA
 1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
MOTO DI UNA CARICA IN UN CAMPO ELETTRICO UNIFORME
 6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
CORRENTE ELETTRICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V 2 isolati tra loro V 2 > V 1 V 2
 COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
Spettrometria. Introduzione.
 Spettrometria. Introduzione. Lo studio degli spettri di emissione e di assorbimento è stato sicuramente uno degli aspetti che hanno maggiormente contribuito alla crisi della meccanica classica a cavallo
Spettrometria. Introduzione. Lo studio degli spettri di emissione e di assorbimento è stato sicuramente uno degli aspetti che hanno maggiormente contribuito alla crisi della meccanica classica a cavallo
Misureremo e analizzeremo la distribuzione di intensità luminosa di diverse figure di diffrazione in funzione della posizione acquisite on- line.
 4 IV Giornata Oggi termineremo questo percorso sulla luce misurando l intensità luminosa della distribuzione di massimi e minimi delle figure di diffrazione e di interferenza. In particolare confronteremo
4 IV Giornata Oggi termineremo questo percorso sulla luce misurando l intensità luminosa della distribuzione di massimi e minimi delle figure di diffrazione e di interferenza. In particolare confronteremo
GIROSCOPIO. Scopo dell esperienza: Teoria fisica. Verificare la relazione: ω p = bmg/iω
 GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
Introduzione all analisi dei segnali digitali.
 Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
Il magnetismo nella materia
 Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Ottica fisica e ottica ondulatoria Lezione 12
 Ottica fisica e ottica ondulatoria Lezione La luce è un onda elettromagnetica; ne studiamo le proprietà principali, tra cui quelle non dipendenti direttamente dalla natura ondulatoria (ottica geometrica
Ottica fisica e ottica ondulatoria Lezione La luce è un onda elettromagnetica; ne studiamo le proprietà principali, tra cui quelle non dipendenti direttamente dalla natura ondulatoria (ottica geometrica
Interferenza e diffrazione
 Interferenza e diffrazione La radiazione elettromagnetica proveniente da diverse sorgenti si sovrappongono in ogni punto combinando l intensita INTERFERENZA Quando la radiazione elettromagnetica passa
Interferenza e diffrazione La radiazione elettromagnetica proveniente da diverse sorgenti si sovrappongono in ogni punto combinando l intensita INTERFERENZA Quando la radiazione elettromagnetica passa
La diffrazione. Lezioni d'autore
 La diffrazione Lezioni d'autore Figure di diffrazione VIDEO Il potere risolutivo di un sistema ottico (I) Un esperienza classica sulle capacità di una persona di distinguere due oggetti vicini si realizza
La diffrazione Lezioni d'autore Figure di diffrazione VIDEO Il potere risolutivo di un sistema ottico (I) Un esperienza classica sulle capacità di una persona di distinguere due oggetti vicini si realizza
Capitolo 13: L offerta dell impresa e il surplus del produttore
 Capitolo 13: L offerta dell impresa e il surplus del produttore 13.1: Introduzione L analisi dei due capitoli precedenti ha fornito tutti i concetti necessari per affrontare l argomento di questo capitolo:
Capitolo 13: L offerta dell impresa e il surplus del produttore 13.1: Introduzione L analisi dei due capitoli precedenti ha fornito tutti i concetti necessari per affrontare l argomento di questo capitolo:
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.6 ENERGIE DI IONIZZAZIONE E DISTRIBUZIONE DEGLI ELETTRONI 4.C OBIETTIVI
 LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
Radiazione atmosferica
 Radiazione atmosferica Fondamenti di meteorologia e climatologia Trento, 28 Aprile 2015 Radiazione elettromagnetica La radiazione elettromagnetica puó essere vista come un insieme di onde che si propagano
Radiazione atmosferica Fondamenti di meteorologia e climatologia Trento, 28 Aprile 2015 Radiazione elettromagnetica La radiazione elettromagnetica puó essere vista come un insieme di onde che si propagano
L EQUILIBRIO UNIVERSALE dalla meccanica celeste alla fisica nucleare
 L EQUILIBRIO UNIVERSALE dalla meccanica celeste alla fisica nucleare Cap.4 giroscopio, magnetismo e forza di Lorentz teoria del giroscopio Abbiamo finora preso in considerazione le condizionidi equilibrio
L EQUILIBRIO UNIVERSALE dalla meccanica celeste alla fisica nucleare Cap.4 giroscopio, magnetismo e forza di Lorentz teoria del giroscopio Abbiamo finora preso in considerazione le condizionidi equilibrio
Tesina di scienze. L Elettricità. Le forze elettriche
 Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
LA TERMOGRAFIA SPETTRO ONDE ELETTROMAGNETICHE
 SPETTRO ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è un mezzo di trasmissione dell energia sotto forma di onde aventi entrambe le componenti elettriche e magnetiche. La sequenza ordinata delle
SPETTRO ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è un mezzo di trasmissione dell energia sotto forma di onde aventi entrambe le componenti elettriche e magnetiche. La sequenza ordinata delle
Campi elettrici, magnetici ed elettromagnetici
 Campi elettrici, magnetici ed elettromagnetici Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Campo Elettrico: si definisce campo elettrico il fenomeno fisico che conferisce
Campi elettrici, magnetici ed elettromagnetici Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Campo Elettrico: si definisce campo elettrico il fenomeno fisico che conferisce
Campi elettrici, magnetici ed elettromagnetici. Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo
 Campi elettrici, magnetici ed elettromagnetici Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Campo Elettrico: si definisce campo elettrico il fenomeno fisico che conferisce
Campi elettrici, magnetici ed elettromagnetici Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Campo Elettrico: si definisce campo elettrico il fenomeno fisico che conferisce
Corrente elettrica. Esempio LA CORRENTE ELETTRICA CONTINUA. Cos è la corrente elettrica? Definizione di intensità di corrente elettrica
 Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Pressione. Esempio. Definizione di pressione. Legge di Stevino. Pressione nei fluidi EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI
 Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
GEOMETRIA DELLE MASSE
 1 DISPENSA N 2 GEOMETRIA DELLE MASSE Si prende in considerazione un sistema piano, ossia giacente nel pian x-y. Un insieme di masse posizionato nel piano X-Y, rappresentato da punti individuati dalle loro
1 DISPENSA N 2 GEOMETRIA DELLE MASSE Si prende in considerazione un sistema piano, ossia giacente nel pian x-y. Un insieme di masse posizionato nel piano X-Y, rappresentato da punti individuati dalle loro
Generatore radiologico
 Generatore radiologico Radiazioni artificiali alimentazione: corrente elettrica www.med.unipg.it/ac/rad/ www.etsrm.it oscar fiorucci. laurea.tecn.radiol@ospedale.perugia.it Impianto radiologico trasformatore
Generatore radiologico Radiazioni artificiali alimentazione: corrente elettrica www.med.unipg.it/ac/rad/ www.etsrm.it oscar fiorucci. laurea.tecn.radiol@ospedale.perugia.it Impianto radiologico trasformatore
ENERGIA SOLARE: Centrali fotovoltaiche e termosolari. Istituto Paritario Scuole Pie Napoletane - Anno Scolastico 2012-13 -
 ENERGIA SOLARE: Centrali fotovoltaiche e termosolari L A V E R A N A T U R A D E L L A L U C E La luce, sia naturale sia artificiale, è una forma di energia fondamentale per la nostra esistenza e per quella
ENERGIA SOLARE: Centrali fotovoltaiche e termosolari L A V E R A N A T U R A D E L L A L U C E La luce, sia naturale sia artificiale, è una forma di energia fondamentale per la nostra esistenza e per quella
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ
 Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
1 Giochi d ombra [Punti 10] 2 Riscaldatore elettrico [Punti 10] AIF Olimpiadi di Fisica 2015 Gara di 2 Livello 13 Febbraio 2015
![1 Giochi d ombra [Punti 10] 2 Riscaldatore elettrico [Punti 10] AIF Olimpiadi di Fisica 2015 Gara di 2 Livello 13 Febbraio 2015 1 Giochi d ombra [Punti 10] 2 Riscaldatore elettrico [Punti 10] AIF Olimpiadi di Fisica 2015 Gara di 2 Livello 13 Febbraio 2015](/thumbs/24/2276739.jpg) 1 Giochi d ombra [Punti 10] Una sorgente di luce rettangolare, di lati b e c con b > c, è fissata al soffitto di una stanza di altezza L = 3.00 m. Uno schermo opaco quadrato di lato a = 10cm, disposto
1 Giochi d ombra [Punti 10] Una sorgente di luce rettangolare, di lati b e c con b > c, è fissata al soffitto di una stanza di altezza L = 3.00 m. Uno schermo opaco quadrato di lato a = 10cm, disposto
quale agisce una forza e viceversa. situazioni. applicate a due corpi che interagiscono. Determinare la forza centripeta di un
 CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
FISICA DELLA BICICLETTA
 FISICA DELLA BICICLETTA Con immagini scelte dalla 3 SB PREMESSA: LEGGI FISICHE Velocità periferica (tangenziale) del moto circolare uniforme : v = 2πr / T = 2πrf Velocità angolare: ω = θ / t ; per un giro
FISICA DELLA BICICLETTA Con immagini scelte dalla 3 SB PREMESSA: LEGGI FISICHE Velocità periferica (tangenziale) del moto circolare uniforme : v = 2πr / T = 2πrf Velocità angolare: ω = θ / t ; per un giro
All interno dei colori primari e secondari, abbiamo tre coppie di colori detti COMPLEMENTARI.
 Teoria del colore La teoria dei colori Gli oggetti e gli ambienti che ci circondano sono in gran parte colorati. Ciò dipende dal fatto che la luce si diffonde attraverso onde di diversa lunghezza: ad ogni
Teoria del colore La teoria dei colori Gli oggetti e gli ambienti che ci circondano sono in gran parte colorati. Ciò dipende dal fatto che la luce si diffonde attraverso onde di diversa lunghezza: ad ogni
FISICA E LABORATORIO
 Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
Transitori del primo ordine
 Università di Ferrara Corso di Elettrotecnica Transitori del primo ordine Si consideri il circuito in figura, composto da un generatore ideale di tensione, una resistenza ed una capacità. I tre bipoli
Università di Ferrara Corso di Elettrotecnica Transitori del primo ordine Si consideri il circuito in figura, composto da un generatore ideale di tensione, una resistenza ed una capacità. I tre bipoli
I COLORI DEL CIELO: COME SI FORMANO LE IMMAGINI ASTRONOMICHE
 I COLORI DEL CIELO: COME SI FORMANO LE IMMAGINI ASTRONOMICHE Nell ultima notte di osservazione abbiamo visto bellissime immagini della Galassia, delle sue stelle e delle nubi di gas che la compongono.
I COLORI DEL CIELO: COME SI FORMANO LE IMMAGINI ASTRONOMICHE Nell ultima notte di osservazione abbiamo visto bellissime immagini della Galassia, delle sue stelle e delle nubi di gas che la compongono.
Aprile (recupero) tra una variazione di velocità e l intervallo di tempo in cui ha luogo.
 Febbraio 1. Un aereo in volo orizzontale, alla velocità costante di 360 km/h, lascia cadere delle provviste per un accampamento da un altezza di 200 metri. Determina a quale distanza dall accampamento
Febbraio 1. Un aereo in volo orizzontale, alla velocità costante di 360 km/h, lascia cadere delle provviste per un accampamento da un altezza di 200 metri. Determina a quale distanza dall accampamento
Radiazione elettromagnetica
 Radiazione elettromagnetica Un onda e.m. e un onda trasversa cioe si propaga in direzione ortogonale alle perturbazioni ( campo elettrico e magnetico) che l hanno generata. Nel vuoto la velocita di propagazione
Radiazione elettromagnetica Un onda e.m. e un onda trasversa cioe si propaga in direzione ortogonale alle perturbazioni ( campo elettrico e magnetico) che l hanno generata. Nel vuoto la velocita di propagazione
Capitolo 7 Le particelle dell atomo
 Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
LE ONDE. Le onde Fisica Medica Lauree triennali nelle Professioni Sanitarie. P.Montagna gen-08. pag.1
 LE ONDE Fenomeni ondulatori Periodo e frequenza Lunghezza d onda e velocità Legge di propagazione Energia trasportata Onde meccaniche: il suono Onde elettromagnetiche Velocità della luce Spettro elettromagnetico
LE ONDE Fenomeni ondulatori Periodo e frequenza Lunghezza d onda e velocità Legge di propagazione Energia trasportata Onde meccaniche: il suono Onde elettromagnetiche Velocità della luce Spettro elettromagnetico
Queste note non vogliono essere esaustive, ma solo servire come linee guida per le lezioni
 Alessandro Farini: note per le lezioni di ottica del sistema visivo Queste note non vogliono essere esaustive, ma solo servire come linee guida per le lezioni 1 Lo spettro elettromagnetico La radiazione
Alessandro Farini: note per le lezioni di ottica del sistema visivo Queste note non vogliono essere esaustive, ma solo servire come linee guida per le lezioni 1 Lo spettro elettromagnetico La radiazione
Appunti sulla Macchina di Turing. Macchina di Turing
 Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
Elettricità e magnetismo
 E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
Introduzione alla Meccanica Quantistica. Fausto Borgonovi
 Introduzione alla Meccanica Quantistica Fausto Borgonovi Dipartimento di Matematica e Fisica e i.l.a.m.p. Universitá Cattolica, via Musei 41, BRESCIA Istituto Nazionale di Fisica Nucleare, PAVIA fausto.borgonovi@unicatt.it
Introduzione alla Meccanica Quantistica Fausto Borgonovi Dipartimento di Matematica e Fisica e i.l.a.m.p. Universitá Cattolica, via Musei 41, BRESCIA Istituto Nazionale di Fisica Nucleare, PAVIA fausto.borgonovi@unicatt.it
LA MASSIMIZZAZIONE DEL PROFITTO ATTRAVERSO LA FISSAZIONE DEL PREZZO IN FUNZIONE DELLE QUANTITÀ
 LA MASSIMIZZAZIONE DEL PROFITTO ATTRAVERSO LA FISSAZIONE DEL PREZZO IN FUNZIONE DELLE QUANTITÀ In questa Appendice mostreremo come trovare la tariffa in due parti che massimizza i profitti di Clearvoice,
LA MASSIMIZZAZIONE DEL PROFITTO ATTRAVERSO LA FISSAZIONE DEL PREZZO IN FUNZIONE DELLE QUANTITÀ In questa Appendice mostreremo come trovare la tariffa in due parti che massimizza i profitti di Clearvoice,
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
Corso di Laboratorio di Fisica prof. Mauro Casalboni dott. Giovanni Casini
 SSIS indirizzo Fisico - Informatico - Matematico 2 anno - a.a.. 2006/2007 Corso di Laboratorio di Fisica prof. Mauro Casalboni dott. Giovanni Casini LA LUCE La luce è un onda elettromagnetica Il principio
SSIS indirizzo Fisico - Informatico - Matematico 2 anno - a.a.. 2006/2007 Corso di Laboratorio di Fisica prof. Mauro Casalboni dott. Giovanni Casini LA LUCE La luce è un onda elettromagnetica Il principio
Relazioni statistiche: regressione e correlazione
 Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Basi di matematica per il corso di micro
 Basi di matematica per il corso di micro Microeconomia (anno accademico 2006-2007) Lezione del 21 Marzo 2007 Marianna Belloc 1 Le funzioni 1.1 Definizione Una funzione è una regola che descrive una relazione
Basi di matematica per il corso di micro Microeconomia (anno accademico 2006-2007) Lezione del 21 Marzo 2007 Marianna Belloc 1 Le funzioni 1.1 Definizione Una funzione è una regola che descrive una relazione
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
Unità Didattica 1. La radiazione di Corpo Nero
 Diapositiva 1 Unità Didattica 1 La radiazione di Corpo Nero Questa unità contiene informazioni sulle proprietà del corpo nero, fondamentali per la comprensione dei meccanismi di emissione delle sorgenti
Diapositiva 1 Unità Didattica 1 La radiazione di Corpo Nero Questa unità contiene informazioni sulle proprietà del corpo nero, fondamentali per la comprensione dei meccanismi di emissione delle sorgenti
Effetto fotoelettrico
 Effetto fotoelettrico Introduzione. Verso la seconda metà del XIX secolo c era la convinzione che la meccanica "classica" (Newton e sviluppi successivi), l elettromagnetismo (sostanzialmente riassunto
Effetto fotoelettrico Introduzione. Verso la seconda metà del XIX secolo c era la convinzione che la meccanica "classica" (Newton e sviluppi successivi), l elettromagnetismo (sostanzialmente riassunto
Proprieta meccaniche dei fluidi
 Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
1-LA FISICA DEI CAMPI ELETTRICI E MAGNETICI.
 1-LA FISICA DEI CAMPI ELETTRICI E MAGNETICI. Tutti i fenomeni elettrici e magnetici hanno origine da cariche elettriche. Per comprendere a fondo la definizione di carica elettrica occorre risalire alla
1-LA FISICA DEI CAMPI ELETTRICI E MAGNETICI. Tutti i fenomeni elettrici e magnetici hanno origine da cariche elettriche. Per comprendere a fondo la definizione di carica elettrica occorre risalire alla
Moto circolare uniforme
 Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
