STRUTTURA E FUNZIONE DELLE PROTEINE
|
|
|
- Cesarina Riccio
- 6 anni fa
- Visualizzazioni
Transcript
1 STRUTTURA E FUNZIONE DELLE PROTEINE
2 PROTEINE Sono le macromolecole più abbondanti della cellula,50% del peso secco di una cellula
3 Le proteine sono le macromolecole più abbondanti e sono presenti in tutti i compartimenti cellulari
4 The Main Functions of the Membrane-bounded Compartments of a Eukaryotic Cell Compartment Main Function Cytosol Nucleus Endoplasmic reticulum (ER) Golgi apparatus Lysosomes Endosomes Mitochondria Chloroplasts (in plant cells) Peroxisomes contains many metabolic pathways protein synthesis contains main genome DNA and RNA synthesis synthesis of most lipids synthesis of proteins for distribution to many organelles and plasma membrane modification, sorting, and packaging of proteins and lipids for either secretion or delivery to another organelle intracellular degradation sorting of endocytosed material ATP synthesis by oxidative phosphorylation ATP synthesis and carbon fixation by photosynthesis oxidation of toxic molecules
5 PROTEINE Sono le macromolecole più abbondanti della cellula, 50% del peso secco di una cellula Sono presenti in tutti i compartimenti cellulari Sono presenti nella matrice extracellulare Sono presenti nel plasma (60-80 gr/l) e in altri fluidi biologici
6 Quante proteine Genoma umano: circa geni splicing alternativo modificazioni post-traduzionali 1 milione di proteine diverse circa proteine diverse espresse simultaneamente in una cellula umana
7 PROTEINE Le proteine sono biopolimeri lineari, costituite da unita monomeriche, gli aminoacidi Le proteine contengono una vasta gamma di gruppi funzionali, gruppi alcolici, tiolici, carbossilici, amidici. Tali gruppi si combinano in diverse sequenze, responsabili dell ampio spettro di strutture proteiche e di funzioni ad esse associate Le proteine possono interagire tra loro e con altre macromolecole biologiche, formando complessi funzionali Alcune proteine sono rigide, altre presentano un elevato grado di flessibilita, possono funzionare come leve, cerniere o molle Sono polimeri funzionalmente molto versatili
8 Le proteine sono molecole dinamiche In almost every case, the function depends on its ability to recognize and bind to some other molecule. For example, antibodies bind to particular foreign substances (antigen) that fit their binding sites. Enzyme recognize and bind to specific substrates, facilitating a chemical reaction. Neurotransmitters pass signals from one cell to another by binding to receptor sites on proteins in the membrane of the receiving cell.
9 La struttura delle proteine ne determina la funzione Subunita β della DNA polimerai III in E. coli Nelson & Cox I principi di Biochimica di Lehninger- Zanichelli 6 ed. La struttura della subunità β permette la replicazione del DNA senza che si dissoci la «macchina» del processo replicativo.
10 Flessibilità e funzione le modificazioni conformazionali sono essenziali per la funzione di una proteina Il legame del ferro alla lattoferrina: cambi conformazionali che permettono ad altre proteine di distinguere la forma legata da quella non legata
11 Proteine- funzioni (1) Enzimi Proteine strutturali Catalizzano le reazioni chimiche Costituiscono parte delle strutture extracellulari: collageno, elastina, cheratina, fibronectina e della «impalcatura» interna (citoscheletro): spettrina, desmina, distrofina
12 Proteine- funzioni (2) Proteine contrattili Responsabili della contrazione muscolare e di diverse forme di locomozione cellulare (flagelli, cilia, fuso mitotico) Es. actina, miosina, tubulina Proteine di difesa Riconoscono/ inattivano sostanze estranee, proteggono l organismo dalle infezioni batteriche e virali Es. immunoglobuline (anticorpi), interferone, cascata del complemento Proteggono l organismo dalla perdita di sangue dovuta a lesioni vascolari Es. proteine (fattori) della coagulazione
13 Proteine- funzioni (3) Proteine regolatrici Regolano diverse processi cellulari Es.ormoni, fattori di crescita, fattori di trascrizione. Recettori Pompe e canali ionici Legano ormoni, fattori di crescita, neurotrasmettitori Assicurano il trasporto di ioni e composti organici attraverso le membrane sulle quali sono organizzate.
14 Proteine- funzioni (4) Proteine di trasporto Assicurano il trasporto nei liquidi biologici di molecole altrimenti insolubili. Es.emoglobina, albumina, lipoproteine, transferrina Proteine di deposito Rappresentano un deposito di energia o di particolari molecole/composti. Es. caseina, mioglobina, ferritina
15 Proteine- funzioni (5) Funzione tampone Funzione ormonale
16 Classificazione delle proteine in base alla loro composizione PROTEINE SEMPLICI: contengono solo amminoacidi (ad es. ribonucleasi e chimotripsina) PROTEINE CONIUGATE: sono composte da amminoacidi e da una parte non amminoacidica (gruppo prostetico)
17 Classe Gruppo prostetico Esempio Glicoproteine Carboidrati Immunoglobulina G Fosfoproteine Gruppi fosforici Caseina del latte Emeproteine Proteine coniugate Eme (ferroporfirina) Emoglobina citocromi Mioglobina Flavoproteine Nucleotidi flavinici Succinato deidrogenasi Ferro Ferritina Metalloproteine Zinco Calcio Rame Zinco Alcol deidrogenasi Calmodulina Ceruloplasmina Anidrasi carbonica
18 S T R U C T U R E Biology/Chemistry of Protein Structure Primary Assembly Secondary Tertiary Folding Packing P R O C E S S Quaternary Interaction
19 occurs at the ribosome involves polymerization of amino acids attached to trna thermodynamically unfavorable, thus coupled to reactions that act as sources of free energy Protein Assembly the precise primary structure of a protein is determined by inherited genetic information. -
20 Struttura Primaria = peculiare sequenza amminoacidica di una catena polipeptidica linear (1 dimensional) sequence of amino acid polymer by convention, written from amino end to carboxyl end a perfectly linear amino acid polymer is neither functional nor energetically favorable folding!
21 Struttura secondaria Si riferisce alla conformazione locale della catena polipeptidica. E determinata da interazioni di tipo legame idrogeno fra l ossigeno di un gruppo carbonilico del legame peptidico e l idrogeno del gruppo ammidico di un altro legame peptidico. Esistono due tipi di strutture secondarie: l a-elica ed il foglietto b.
22 Proteine: struttura secondaria strutture dovute ad interazioni locali di tipo ponte-h ad intervalli regolari a-elica ponte-h ogni 3,6 aminoacidi Il legame H si instaura tra l H dell azoto amidico e l O del gruppo carbonilico residui esterni alla spirale b-foglietto legami idrogeno fra aminoacidi di porzioni diverse della catena polipeptidica foglietto piegato
23 Struttura secondaria non ripetitive motivi strutturali non ripetitivi: forma meno regolare rispetto all a-elica ed al foglietto b. La catena polipeptidica assume una conformazione ad anse ed avvolgimenti. Ferritina
24 Proteine-La struttura terziaria La struttura terziaria è la conformazione tridimensionale assunta da una proteina.
25 Tertiary structure is stabilized by a variety of interactions among R groups and between R groups and the polypeptide backbone. hydrogen bonds among polar and/or charged areas; ionic bonds between charged R groups; hydrophobic interactions and van der Waals interactions among hydrophobic R groups. disulfide bridges, strong covalent bonds that form between the sulfhydryl groups (SH) of cysteine monomers, stabilize the structure.
26 La struttura terziaria è stabilizzata da 4 tipi di interazioni Interazioni idrofobiche: gli amminoacidi con catene laterali non polari tendono a localizzarsi all interno della molecola dove si associano con altri residui idrofobici. Interazioni ioniche: i gruppi con carica negativa (-COO - ) possono interagire con gruppi carichi positivamente (-NH 3+ ) Legami a idrogeno Legami disolfuro
27 Struttura terziaria (i domini) Le catene polipeptidiche formate da più di 200 amminoacidi in genere comprendono 2 o più domini, piccole unità compatte. I domini sono le unità strutturali e funzionali di una proteina. Ciascun dominio è una regione globulare, compatta, che si forma per la combinazione di più elementi strutturali secondari (a-eliche, foglietti b, sequenze non ripetitive), strutturalmente, indipendente da altri domini. La struttura terziaria riguarda sia il ripiegamento di ciascun dominio sia la disposizione reciproca finale dei domini di un polipeptide.
28 Struttura terziaria di una proteina chinasi dominio proteico: parte di una catena polipeptidica che si può ripiegare indipendentemente in una struttura compatta stabile 2 domini con funzioni regolatorie Src 2 domini con funzioni catalitiche
29 Spesso, domini simili ricorrono in proteine diverse che hanno funzioni diverse e sequenza amminoacidica completamente diversa.
30 Struttura tridimensionale delle proteine Alcune proteine o segmenti di proteine sono intrinsecamente disordinati, privi di una struttura ordinata, definita. Hanno composizioni amminoacidiche caratteristiche, ricche in amminoacidi carichi e in Pro. Struttura piu flessibile. Funzioni di: - molecole spaziatrici e isolanti all interno di strutture complesse - agenti detossificanti, che funzionano da «scavenger» - componenti delle reti di interazione delle proteine
31 Quarternary structure results from the aggregation of two or more polypeptide subunits Collagen is a fibrous protein of three polypeptides that are supercoiled like a rope. This provides the structural strength for their role in connective tissue. Hemoglobin is a globular protein with two copies of two kinds of polypeptides.
32 Proteina Chinasi AMP ciclico dipendente esempio di domini funzionali modificazioni conformazionali indotte Nelson & Cox I principi di Biochimica di Lehninger- Zanichelli 6 ed.
33 Proteina molecole composte da una o più catene polipeptidiche Proteine monomeriche Proteine multimeriche omomultimeriche (stesso tipo di polipeptide) eteromultimeriche (diversi tipi di polipeptidi)
34 Complessi proteici Poliovirus Virus del mosaico del tabacco Nelson & Cox I principi di Biochimica di Lehninger- Zanichelli 6 ed.
35 Complex protein assembly Poro nucleare circa 30 nucleoproteine diverse, in copie di 8 o multipli di 8
36 Complessi proteici Le molecole proteiche sono presenti nell ambiente cellulare principalmente come complessi proteici contenenti numerose proteine. I complessi sono funzionalmente essenziali per la maggior parte dei processi cellulari, quali segnalazione cellulare trascrizione genica, splicing e maturazione RNA traduzione dell RNA metabolismo cellulare
37 Proteine Fibrose e Globulari Le proteine possono essere divise in due classi: Proteine Globulari Proteine fibrose
38 Proteine globulari Le catene polipeptidiche sono ripiegate ed assumono forma compatta, sferica o globulare. Generalmente contengono più tipi di struttura secondaria. Sono solubili in acqua Comprendono: Enzimi Ormoni Proteine di trasporto Proteine di deposito Proteine regolatrici lisozima
39 Champe et al., Le basi della biochimica, Ed. Zanichelli In soluzione acquosa le proteine globulari hanno una struttura compatta: le catene laterali idrofobiche si trovano nella parte interna della molecola mentre i gruppi idrofilici in genere si trovano in superficie.
40 In un ambiente non polare (lipidico), per esempio una membrana, la disposizione è opposta: catene laterali idrofiliche all interno, amminoacidi idrofobici sulla superficie della molecola.
41 Proteine Fibrose Hanno catene polipeptidiche disposte in lunghi fasci o in foglietti. In genere presentano un unico tipo di struttura secondaria. Sono insolubili in H 2 O per la presenza di elevate [ ] di AA idrofobici. Le catene polipeptidiche si associano in complessi sopramolecolari in modo da nascondere al solvente le superfici idrofobiche. Sono adatte a ruoli strutturali (p.es. a-cheratina, collageno).
42 Cheratine e collageni hanno strutture ad elica Le Proteine Fibrose Gruppi apolari e ponti disolfuro tendono a conferire rigidità e insolubilità alle proteine fibrose.
43 Protein Folding In spite of the knowledge of the three-dimensional shapes of over 10,000 proteins, it is still difficult to predict the conformation of a protein from its primary structure alone. Most proteins appear to undergo several intermediate stages before reaching their mature conformation.
44 Ripiegamento di una proteina Il meccanismo del folding è probabilmente un processo progressivo. Interazioni non covalenti a breve raggio: le strutture secondarie (α-eliche e strutture β) si formano piuttosto rapidamente Interazioni a breve e lungo raggio ed interazioni con il solvente Champe et al., Le basi della biochimica, Ed. Zanichelli
45 Ripiegamento di una proteina puo essere un processo spontaneo grazie all informazione contenuta nella sequenza primaria della proteina; molto spesso viene acquisito tramite molecole assistenti, chiamate chaperoni molecolari : -heat shock proteins (Hsps) -chaperonine (complessi proteici)
46 Ripiegamento delle proteine e proteine da stress i chaperoni avrebbero il compito di occupare le regioni idrofobiche, ancora esposte nella proteina, in modo da impedire che per effetto di interazioni idrofobiche essa possa aggregarsi e precipitare
47 Le proteine da stress possono essere indotte da: Fattori ambientali Shock termico Metalli pesanti di transizione Agenti chemioterapici Stati patologici Infezioni virali Febbre Infiammazione Ischemia Lesioni da ossidanti Neoplasie Fattori cellulari normali Ciclo di divisione cellulare Fattori di crescita Sviluppo e differenziamento
48 Destino della proteina sintetizzata e ruolo degli chaperones molecolari
49 Molte malattie sono dovute al ripiegamento difettoso «misfolding» di proteine Alcune patologie hanno in comune un non corretto avvolgimento di proteine. Le proteine non correttamente ripiegate e parzialmente ripiegate, secrete dalla cellula tendono a formare grossi aggregati insolubili (fibrille o placche amiloidi). Esempi: Alzheimer, Parkinson, encefalopatia spongiforme, diabete di tipo II, la sclerosi laterale amiotrofica
50 malattia di Alzheimer- peptide b- amiloide Il peptide b- amiloide deriva per taglio ad opera di proteasi da una proteina di transmembrana (APP= proteina precursore della proteina amiloide). Il peptide b è instabile e perde la struttura ad alpha elica depositi amorfi extracellulari di peptide b-amiloide (Ab) sotto forma di placche amiloidi
51 Proteina a-sinucleina - Morbo di Parkinson Corpi di Lewy: aggregati proteici all interno di cellule nervose. Gli aggregati contengono fibrille di a-sinucleina insolubili La proteina alfa-sinucleina interagisce direttamente con la membrana dei mitocondri, danneggiandola e causandone la frammentazione. La riduzione della produzione di energia determina la morte delle cellule nervose. (Nakamura K, J Biol Chem, 2011)
52 Proteina amilina - Diabete di tipo II L amilina o IAPP (Polipeptide Amiloide Insulare), un polipeptide di 37 amminoacidi che viene, anche in soggetti sani, prodotto dalle cellule β pancreatiche, immagazzinato nei granuli di tali cellule e co-secreto insieme all'insulina. La formazione di aggregati contenenti amilina è causa di necrosi delle cellule β del pancreas.
53 Molte malattie sono dovute al difettoso ripiegamento di una proteina Mutazioni puntiformi possono generare proteine che non raggiungono la loro localizzazione finale Es Fibrosi cistica: difetto nella proteina transmembrana che agisce come un canale degli ioni cloro nelle cellule epiteliali (CFTR: 1480 amminoacidi). La mutazione più comune è la delezione di un amminoacido (Phe 508) e la proteina mutata non si avvolge correttamente e non raggiunge la sua destinazione finale.
54 Canale degli ioni cloro nelle cellule epiteliali Regolatore della Conduttanza transmembrana (CFTR) Proteina multi-dominio N Engl J Med 2005;352:
55 Denaturazione delle proteine
56 Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere definito come la tendenza a mantenere la conformazione nativa Denaturazione: perdita della struttura secondaria, terziaria e/o quaternaria, parziale o totale srotolamento Lo stato denaturato è sempre correlato alla perdita della funzione, viceversa la perdita di funzione non è necessariamente correlata alla perdita della struttura nativa (es. Sostituzioni aa in sito attivo di un enzima)
57 Denaturazione reversibile ed irreversibile Denaturazione: perdita della struttura tridimensionale Reversibile: la rimozione dell agente denaturante permette di riprendere spontaneamente la struttura nativa Nell ambiente intracellulare, la proteina può riacquistare la sua struttura tridimensionale corretta per la presenza di proteine chaperonine
58 Denaturazione Active protein Irreversibile: la proteina non ritorna più alla condizione originale: danno permanente. Denatured protein
59 Protein Inactivation What factors may cause inactivation or unfolding? Temperature Oxidation Heavy metals Radiation Extremes of ph Detergents Chelating agents Mechanical forces
60 Protein Inactivation High temperature Increase of mobility of protein segments Exposure of hydrophobic groups Formation of non-native disulfide bridges Scrambled structures Aggregation Precipitation
61 Transition: folded to unfolded
62 Protein Inactivation Thermostable enzymes Hyperthermophilic microorganisms Many different structural reasons for increased thermostability Compact (multimeric) proteins Increase of number of salt bridges
63 Protein Inactivation Oxidation Oxygen, hydrogen peroxide, oxygen radicals Tyr, Phe, Trp, Cys, Met UV-radiation Cys, Trp, His
64 Protein Inactivation Mechanical forces Stirring and mixing: shear forces Ultrasound, high pressure, shaking Deformation and exposure of hydrophobic residues aggregation Adsorption to the vessel wall
65 Proteine- aspetti nutrizionali Le proteine alimentari: si trovano in quasi tutti gli alimenti, ne sono privi oli, zucchero e bevande alcoliche. Sono nutrizionalmente importanti: -proteine di masse muscolari (carne e pesce) per l 80% costituite da actina e miosina e -proteine di deposito (uovo, latte, cereali e legumi).
66 Best Sources of Protein
67 Protein Quality Complete proteins Contain all nine essential amino acids Usually animal source are complete proteins Are considered higher quality Incomplete proteins Low in one or more essential amino acid Usually plant sources are incomplete
68 Proprietà nutrizionali delle proteine Forniscono all organismo amminoacidi essenziali e non, che hanno funzioni: Plastica per la costruzione di proteine umane Energetica mediante ossidazione nel ciclo di Krebs o conversione a glucosio nella gluconeogenesi
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Fondamentali in ogni organismo, hanno molteplici ruoli:
 Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Le Biomolecole II parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
STRUTTURAZIONE DELLE PROTEINE
 STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Macromolecole biologiche
 MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
I PROTIDI. Aspetti generali
 I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
LE MEMBRANE CELLULARI
 LE MEMBRANE CELLULARI Sono strutture sovramolecolari che racchiudono e delimitano l ambiente intracellulare e negli eucarioti anche gli organuli citoplasmatici. Hanno funzione di Protezione. Sostegno.
LE MEMBRANE CELLULARI Sono strutture sovramolecolari che racchiudono e delimitano l ambiente intracellulare e negli eucarioti anche gli organuli citoplasmatici. Hanno funzione di Protezione. Sostegno.
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Di cosa è fatta una cellula?
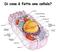 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
Plasma membrane. Endoplasmic reticulum. Nucleus. Golgi apparatus. Mitochondrion Lysosome. Ribosome
 Endoplasmic reticulum Plasma membrane Nucleus Golgi apparatus Ribosome Mitochondrion Lysosome Funzioni 1- Compartimentazione 2- Localizzazione per attività biochimiche 3- Barriera selettiva 4- Trasporto
Endoplasmic reticulum Plasma membrane Nucleus Golgi apparatus Ribosome Mitochondrion Lysosome Funzioni 1- Compartimentazione 2- Localizzazione per attività biochimiche 3- Barriera selettiva 4- Trasporto
Struttura e funzione delle proteine
 Proteine Struttura e funzione delle proteine Le cellule viventi contengono un corredo estremamente diversificato di molecole proteiche, ciascuna costituita da una catena lineare di aminoacidi uniti da
Proteine Struttura e funzione delle proteine Le cellule viventi contengono un corredo estremamente diversificato di molecole proteiche, ciascuna costituita da una catena lineare di aminoacidi uniti da
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
Acquisizione e Stabilità della struttura terziaria delle proteine
 Acquisizione e Stabilità della struttura terziaria delle proteine FORZE CHE STABILIZZANO LA STRUTTURA TERZIARIA DELLE PROTEINE 1. Legame covalente S-S (forte): non è presente in tutte le proteine che,
Acquisizione e Stabilità della struttura terziaria delle proteine FORZE CHE STABILIZZANO LA STRUTTURA TERZIARIA DELLE PROTEINE 1. Legame covalente S-S (forte): non è presente in tutte le proteine che,
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Il legame peptidico è polare
 Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Introduzione al Citoscheletro
 http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Le molecole biologiche. Le proteine
 Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine:
 La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
Macromolecole Biologiche. La struttura secondaria (III)
 La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
Riepilogo 1^ lezione
 Riepilogo 1^ lezione I 20 amminoacidi che si trovano comunemente nelle proteine sono uniti l uno all altro da legami peptidici. La sequenza lineare degli amminoacidi legati contiene l informazione necessaria
Riepilogo 1^ lezione I 20 amminoacidi che si trovano comunemente nelle proteine sono uniti l uno all altro da legami peptidici. La sequenza lineare degli amminoacidi legati contiene l informazione necessaria
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Di cosa è fatta una cellula?
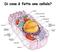 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
Membrane Biologiche. Barriere per confinare sostanze o attività in ambienti specifici. Costituite da lipidi e proteine. Confini Cellulari Organelli
 Membrane Biologiche Membrane Biologiche Barriere per confinare sostanze o attività in ambienti specifici. Confini Cellulari Organelli Costituite da lipidi e proteine. Sistema di Endomembrane Delimitano
Membrane Biologiche Membrane Biologiche Barriere per confinare sostanze o attività in ambienti specifici. Confini Cellulari Organelli Costituite da lipidi e proteine. Sistema di Endomembrane Delimitano
 8 ER membrane ribosomi lume RER and SER Trasporto di proteine nei mitocondri Traduzione In vitro su polisomi liberi : NH2 Signal peptide Leader peptide: 20-25 hydrophobic amino acids Traduzione In vivo
8 ER membrane ribosomi lume RER and SER Trasporto di proteine nei mitocondri Traduzione In vitro su polisomi liberi : NH2 Signal peptide Leader peptide: 20-25 hydrophobic amino acids Traduzione In vivo
20/12/ tipi di amino acidi: parecchie combinazioni
 20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
Riconoscimento dell antigene
 Riconoscimento dell antigene Risposta immune adattativa La risposta immune innata è molto efficiente ma non sempre riesce ad impedire il diffondersi dell infezione È essenziale quindi che subentri la risposta
Riconoscimento dell antigene Risposta immune adattativa La risposta immune innata è molto efficiente ma non sempre riesce ad impedire il diffondersi dell infezione È essenziale quindi che subentri la risposta
CHIMICA BIOLOGICA. Università degli Studi della Campania Luigi Vanvitelli. Antimo Di Maro. Lezione 0. Corso di Laurea in Scienze Biologiche
 Università degli Studi della Campania Luigi Vanvitelli Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 0 Chimica Biologica o Biochimica
Università degli Studi della Campania Luigi Vanvitelli Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 0 Chimica Biologica o Biochimica
LE PROTEINE. Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O)
 LE PROTEINE Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O) Sono costituite dall'unione di tante unità di base dette amminoacidi Protidi negli alimenti Copyright
LE PROTEINE Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O) Sono costituite dall'unione di tante unità di base dette amminoacidi Protidi negli alimenti Copyright
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 5
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
INDICE PARTE I CHIMICA. Autori Introduzione
 INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Classificazione dell Architettura Proteica
 Classificazione dell Architettura Proteica struttura Primaria struttura Secondaria Super-secondaria Domini struttura Terziaria: folding struttura Quaternaria Proteine globulari Il ripiegamento della catena
Classificazione dell Architettura Proteica struttura Primaria struttura Secondaria Super-secondaria Domini struttura Terziaria: folding struttura Quaternaria Proteine globulari Il ripiegamento della catena
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
La struttura delle proteine e e descritta da quattro livelli di organizzazione
 La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
