CEFPAS 24 Marzo 2015 Silvana Mansueto
|
|
|
- Arrigo Fiorini
- 6 anni fa
- Visualizzazioni
Transcript
1 CENTRO DI FARMACOVIGILANZA Centro di consulenza ed informazione sugli effetti tossici da farmaci in gravide e neonati da erbe medicinali e dai prodotti da esse derivati A.O.U. "Policlinico - Vittorio Emanuele" Catania La segnalazione, completezza del dato e follow-up CEFPAS 24 Marzo 2015 Silvana Mansueto
2
3
4
5 Andamento sospette reazioni avverse Sicilia Italia nel triennio SICILIA ITALIA
6 Distribuzione segnalazioni per regione Anno 2014
7
8 Obblighi dei responsabili di farmacovigilanza secondo la nuova normativa Il Responsabile di Fv è parte integrante di un sistema nazionale che fa capo all AIFA e pertanto è tenuto a fornire il proprio contributo nei modi e nei tempi richiesti. Le attività che un responsabile di farmacovigilanza deve garantire sono le seguenti: Inserimento e gestione delle schede di sospetta reazione avversa a farmaci e vaccini Follow-up Feedback ai segnalatori Risposte alle richieste da parte delle Aziende Farmaceutiche Diffusione delle informazioni agli operatori sanitari
9 Importanza della validazione e della completezza delle schede di segnalazione - 1 Il sistema nazionale di farmacovigilanza deve garantire elevati standard qualitativi perché le segnalazioni non restano isolate a livello nazionale, vengono trasmesse ad Eudravigilance ed al centro WHO di Uppsala Va tenuto presente che Schede errate o incomplete possono portare ad elaborazioni non corrette a livello internazionale con impatto sulle decisioni regolatorie e conseguenze non prevedibili
10 Importanza della validazione e della completezza delle schede di segnalazione - 2 Mensilmente, tutte le segnalazioni sono inviate al Centro WHO di Uppsala. Le segnalazioni gravi sono trasferite nel data base di Eudravigilance ogni 10 giorni, quelle non gravi sono riversate ogni 60 giorni. Le reazioni in cui il campo della gravità non è definito, rispettano la tempistica di quelle non gravi. Considerata la differenza tra le gravi e le non gravi, laddove il campo gravità non fosse definito, sarebbe opportuno chiedere conferma al segnalatore prima del caricamento.
11 Completezza della segnalazione La segnalazione è una sorta di comunicazione relativa all insorgenza di una reazione avversa che si sospetta sia correlata all assunzione di un farmaco. La qualità e la completezza delle informazioni riportate sono fondamentali. Ogni sezione della scheda ha una sua ragione di esistere e dovrebbe essere debitamente compilata.
12 Validità della scheda di segnalazione Vanno inserite nella rete nazionale di farmacovigilanza, soltanto le segnalazioni ritenute valide. Per essere considerata valida la scheda deve riportare contemporeanemente 4 elementi fondamentali Segnalatore Identificabile Un paziente Un farmaco sospetto Una reazione avversa Questi 4 elementi sono necessari ma da solo non sufficienti a consentire un adeguata valutazione del caso. Informazioni aggiuntive vanno acquisite ed inserite in rete
13 Compilazione della scheda in rete L inserimento in rete viene effettuato attraverso la compilazione delle cartelle di seguito indicate Possono sussistere alcune discrepanze tra la compilazione della scheda in rete rispetto alla scheda cartacea; in quest'ultima, per esigenze di spazio, non è possibile riportare tutte le singole voci come appaiono invece nelle cartelle in rete. In generale risulta importante ricordare che l inserimento dei dati deve essere fatto in modo strutturato e secondo formati ben definiti per permettere il recupero delle informazioni in fase di analisi e la trasferibilità del dato stesso ad altri database (EV e WHO).
14 Paziente I dati riportati in questa sezione servono per I dati riportati in questa sezione servono per l identificazione di eventuali duplicati. Nel caso di vaccini può essere utile inserire la data di nascita. Iniziali e data di nascita consentono di distinguere più facilmente i casi (soprattutto se ci sono cluster di segnalazioni da vaccino provenienti dalla stessa struttura).
15
16 Reazione avversa La descrizione della reazione deve essere molto chiara per potere effettuare una codifica fedele. Nel caso di segnalazioni da vaccino bisogna riportare anche l ora della somministrazione. C è la possibilità di indicare gli eventuali esami diagnostici effettuati con la data relativa. E importante inoltre descrivere dettagliatamente le azioni intraprese
17 GRAVITA Viene stabilita secondo criteri precisi ed inequivocabili. Se il Responsabile di Fv ravvisa che è presente uno dei criteri di gravità, deve caricare la segnalazione come grave anche se il segnalatore non lo ha indicato sulla scheda. Biffa quindi altra condizione clinicamente rilevante ed espone le moptivazioni del cambiamento nel campo Commento ESITO Valutatore (sezione Condizioni concomitanti o predisponenti ) Va ricordato che le voci selezionabili a proposito della relazione ADR decesso si riferiscono sempre a un decesso, pertanto vanno selezionate solo per un esito fatale.
18 GRAVITA ESITO
19 Farmac co Sospetto È importante riportare il nome commerciale del farmaco e non soltanto il principio attivo (in caso di farmaci generici aggiungere il nome dell azienda). Deve essere riportato il dosaggio e non solo l unità posologica. Nel caso di vaccini è necessario riportare anche l ora della somministrazione e il numero di dose (I, II, III o richiamo), lotto e data di scadenza e sito d inoculo; È importante fornire anche le informazioni relative al miglioramento della reazione avversa dopo la sospensione del farmaco dechallange e, quando disponibili, anche le informazioni relative al rechallenge.
20 Tra le informazioni riportate nella scheda, non compare la data di scadenza che molto spesso però viene richiesta dalle Aziende farmaceutiche. In questo caso il responsabile valuta se l informazione è rilevante e decide se contattare il segnalatore. Farmaco Sospetto Se le date non sono indicate con precisione (per esempio si dispone soltanto del mese e dell anno) si indica il primo del mese e si biffa il campo attribuzione d ufficio della scheda in rete. La data d insorgenza deve essere definita con certezza. Qualora la data di scadenza del vaccino fosse indicata con mese ed anno, per convenzione si riporta l ultimo giorno del mese.
21 Farmaco Sospetto
22 Si ricorda che in presenza di una segnalazione in cui sono riportati più medicinali indicati come sospetti va inserita un'unica scheda in rete e non deve essere compilata una scheda per ogni farmaco sospetto (moltiplicherebbe i casi di reazione avversa).
23 Farmaci concomitanti Campo fondamentale poiché alcune ADR potrebbero essere il frutto di un interazione. Se si tratta di vaccini, bisogna indicare quelli somministrati fino a 4 settimane prima della somministrazione. Va specificato inoltre se c è un uso concomitante di integratori alimentari o prodotti erboristici
24 Farmaci concomitanti Altre sostanze utilizzate
25 Condizioni concomitanti o predisponenti La compilazione delle cartelle Farmaci concomitanti e Condizioni concomitanti predisponenti fornisce informazioni utili per la valutazione del caso, ad esempio presenza di una insufficienza d organo, e per la valutazione del nesso di causalità in quanto possono indicare la presenza di cause alternative al farmaco sospetto nel determinare la reazione avversa.
26 Informazioni sul segnalatore La nuova scheda di segnalazione prevede il campo con la firma del segnalatore. Considerato, tuttavia, che la scheda può essere inviata in formato elettronico, la firma non è di fatto considerata vincolante per l inserimento. Il segnalatore deve comunque essere identificabile (Nome, cognome, indirizzo, etc.) per poter essere contattato in caso di chiarimenti o per informazioni aggiuntive, inoltre non sono accettabili schede anonime. E obbligatorio compilare il campo relativo alla data di ricezione.
27 Follow-Up 1 La sezione Follow-up è destinata a tutte le informazioni aggiuntive che si hanno in merito al contenuto della scheda inserita. Tali informazioni possono essere inserite a seguito di specifiche richieste da parte delle Aziende o di AIFA oppure su iniziativa del Responsabile di FV.
28 Follow-Up 2 Spesso come follow-up è richiesta una relazione clinica. I dati o la relazione clinica acquisiti vanno quindi inseriti in questa cartella evitando di inviare solo o fax all Azienda richiedente o all AIFA: in questa maniera tutti gli utenti coinvolti in RNF avranno la possibilità di visualizzare le informazioni aggiunte. E importante documentare quando sono stati richiesti gli aggiornamenti al segnalatore e gli eventuali solleciti (es. in data 05/10/2012 è stato contattato il segnalatore per richiedere il risultato dell esame di laboratorio; in data 15/10/2012: inviata di sollecito al segnalatore in merito all informazione richiesta).si ricorda che nell inserire le informazioni è importante rispettare le norme della privacy. Negli allegati vanno ben anneriti preventivamente tutti i campi sensibili (es. nome e cognome del paziente, indirizzo, codice fiscale, nome del medico, etc.). Quando si allega la relazione in formato pdf o word, bisogna fare attenzione a non allegare file troppo pesanti e nella denominazione, non bisogna lasciare alcuno spazio vuoto es. scrivere Relazione_clinica1 piuttosto che Relazione clinica 1
29 Follow-Up 3 Se dal follow-up emerge una diversa descrizione della reazione avversa o comunque qualche elemento differente rispetto a ciò che era stato inserito in precedenza, le informazioni già inserite (inclusa l eventuale codifica) vanno modificate. Ogni variazione confluirà in EV nell ambito della quale sarà valutato sempre l ultimo aggiornamento disponibile. Le informazioni di follow-up vanno inserite in Rete il prima possibile, in particolare entro 7 giorni dal ricevimento nel caso di reazioni gravi. Il follow up deve essere proattivo e non visto come un semplice riscontro.
30 Richieste di integrazione da parte delle Aziende Molto spesso le richieste delle Aziende farmaceutiche possono essere ridodanti. In questo caso il responsabile deve valutare la completezza della scheda e valutare se le informazioni richieste, sono utili o meno alla valutazione del caso. Il follow up è richiesto per le reazioni gravi. Nel caso in cui il Responsabile di farmacovigilanza decida di non dare seguito alla richiesta dell Azienda per non stressare il segnalatore, è opportuno comunque che risponda motivando la propria decisione
31
32
33 Follow-Up 4 Il seguente esempio di follow up, mostra il tipo di attività che va svolta quando si caricano in rete, segnalazioni provenienti dai cittadini. Il responsabile locale ha il compito di attivarsi per il recupero delle informazioni cliniche
34 Caso clinico 1
35 Caso clinico 1
36 Caso clinico 1
37 Caso clinico 2
38 Grazie per l attenzione!
Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa
 Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa Vengono di seguito riportate alcune precisazioni, tratte dalle linee guida presenti nel sito dell'aifa relativamente
Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa Vengono di seguito riportate alcune precisazioni, tratte dalle linee guida presenti nel sito dell'aifa relativamente
Ministero della Salute
 Ministero della Salute DECRETO: NUOVO MODELLO DI SEGNALAZIONE DI REAZIONE AVVERSA A FARMACI E VACCINI IL MINISTRO DELLA SALUTE VISTO il decreto legislativo. 18 febbraio 1997, n. 44; VISTO il decreto legislativo
Ministero della Salute DECRETO: NUOVO MODELLO DI SEGNALAZIONE DI REAZIONE AVVERSA A FARMACI E VACCINI IL MINISTRO DELLA SALUTE VISTO il decreto legislativo. 18 febbraio 1997, n. 44; VISTO il decreto legislativo
La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di
 La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di individuare precocemente possibili segnali di allarme correlati
La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di individuare precocemente possibili segnali di allarme correlati
CASO CLINICO. Arianna Deidda
 CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari CASO CLINICO Arianna Deidda Vaccini & Vaccinovigilanza Cagliari,
CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari CASO CLINICO Arianna Deidda Vaccini & Vaccinovigilanza Cagliari,
La nuova normativa in breve
 La nuova normativa in breve Le nuove disposizioni di legge in tema di sicurezza dei medicinali promettono di cambiare significativamente la farmacovigilanza Nel luglio 2012 sono entrate in vigore due nuove
La nuova normativa in breve Le nuove disposizioni di legge in tema di sicurezza dei medicinali promettono di cambiare significativamente la farmacovigilanza Nel luglio 2012 sono entrate in vigore due nuove
Scheda unica di segnalazione di sospetta reazione avversa
 DIPARTIMENTO ASSISTENZA FARMACEUTICA Scheda unica di segnalazione di sospetta reazione avversa Dott.ssa Elisa Iori Responsabile di farmacovigilanza Assicura la qualità dei dati delle schede Gestisce il
DIPARTIMENTO ASSISTENZA FARMACEUTICA Scheda unica di segnalazione di sospetta reazione avversa Dott.ssa Elisa Iori Responsabile di farmacovigilanza Assicura la qualità dei dati delle schede Gestisce il
LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE: VIGIFARMACO
 CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE:
CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE:
-Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio
 Centro Regionale di Farmacovigilanza -Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio Seminario multi-tematico
Centro Regionale di Farmacovigilanza -Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio Seminario multi-tematico
Dipartimento Interaziendale Farmaceutico UO Farmacia Ospedaliera. La gestione delle segnalazione di reazione avversa (ADR) a farmaco
 Pag. 1/6 La gestione delle segnalazione di reazione avversa (ADR) a farmaco 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...2 6. Definizioni...2
Pag. 1/6 La gestione delle segnalazione di reazione avversa (ADR) a farmaco 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...2 6. Definizioni...2
La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce
![La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce](/thumbs/65/53226195.jpg) La normativa europea in materia di farmacovigilanza è stata modificata con l adozione nel 2010, del Regolamento UE 1235/2010, la cui applicazione è operativa dal 2 luglio 2012, e della Direttiva 2010/84/UE,
La normativa europea in materia di farmacovigilanza è stata modificata con l adozione nel 2010, del Regolamento UE 1235/2010, la cui applicazione è operativa dal 2 luglio 2012, e della Direttiva 2010/84/UE,
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013
 Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Servizio FV Interno OEI : dott.ssa MT Calcagno, dott.ssa M.Torsegno Indice - Definizioni di Farmacovigilanza
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Servizio FV Interno OEI : dott.ssa MT Calcagno, dott.ssa M.Torsegno Indice - Definizioni di Farmacovigilanza
La gestione degli eventi avversi e dei SAE
 Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi
 La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Andrea Marchi Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali Regione Emilia Romagna Bologna 26 gennaio e 2, 9,
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Andrea Marchi Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali Regione Emilia Romagna Bologna 26 gennaio e 2, 9,
Elementi di vigilanza nella gestione dei gas medicinali
 La gestione sanitaria dei gas medicinali Corso per formatori delle Aziende sanitarie 15 novembre 2012 e 17 gennaio 2013 Elementi di vigilanza nella gestione dei gas medicinali Elisa SANGIORGI Servizio
La gestione sanitaria dei gas medicinali Corso per formatori delle Aziende sanitarie 15 novembre 2012 e 17 gennaio 2013 Elementi di vigilanza nella gestione dei gas medicinali Elisa SANGIORGI Servizio
IL FARMACISTA COME SEGNALATORE:
 Direzione Generale Sanità e Servizi Sociali IL FARMACISTA COME SEGNALATORE: la scheda, la corretta compilazione, esempi di segnalazioni di ADR CORSO PER FARMACISTI CONVENZIONATI: LA CULTURA DELLA FARMACOVIGILANZA
Direzione Generale Sanità e Servizi Sociali IL FARMACISTA COME SEGNALATORE: la scheda, la corretta compilazione, esempi di segnalazioni di ADR CORSO PER FARMACISTI CONVENZIONATI: LA CULTURA DELLA FARMACOVIGILANZA
SEGNALAZIONE DELLE SOSPETTE REAZIONI AVVERSE DA FARMACI. Un impegno etico per la. sicurezza del farmaco. Prevenire è meglio che curare
 Azienda U.S.L. 5 Spezzino U.O. Farmaceutica Territoriale Direttore Dr. Alessandro Sarteschi Prevenire è meglio che curare Le segnalazioni devono essere inviate a: Servizio Farmacovigilanza e Centro Documentazione
Azienda U.S.L. 5 Spezzino U.O. Farmaceutica Territoriale Direttore Dr. Alessandro Sarteschi Prevenire è meglio che curare Le segnalazioni devono essere inviate a: Servizio Farmacovigilanza e Centro Documentazione
Corso di aggiornamento in FARMACOVIGILANZA. Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013
 Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Farmacovigilanza La scienza e le attività collegate alla identificazione, valutazione, conoscenza
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Farmacovigilanza La scienza e le attività collegate alla identificazione, valutazione, conoscenza
La nuova legislazione sulla Farmacovigilanza. Il nuovo flusso delle segnalazioni. Carmela Santuccio. Roma, 13 settembre 2012
 La nuova legislazione sulla Farmacovigilanza Il nuovo flusso delle segnalazioni Carmela Santuccio Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione
La nuova legislazione sulla Farmacovigilanza Il nuovo flusso delle segnalazioni Carmela Santuccio Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione
Prot. Az.Osp. n e Prot.Az.USL n Ferrara, Rif.: I, L 1/12
 Dipartimento Farmaceutico Interaziendale Università degli Studi di Ferrara COORDINAMENTO DI FARMACOVIGILANZA INTERAZIENDALE Prot. Az.Osp. n. 12175 e Prot.Az.USL n. 24666 Ferrara, 18.03.2008. Rif.: I, 3.5
Dipartimento Farmaceutico Interaziendale Università degli Studi di Ferrara COORDINAMENTO DI FARMACOVIGILANZA INTERAZIENDALE Prot. Az.Osp. n. 12175 e Prot.Az.USL n. 24666 Ferrara, 18.03.2008. Rif.: I, 3.5
FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE LA SICUREZZA DEI FARMACI
 Sede legale: Via G. Cusmano, 24 90141 PALERMO C.F. e P. I.V.A.: 05841760829 Dipartimento Farmaceutico Via Pindemonte 88 90128 PALERMO dipfarmaco@asppalermo.org FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE
Sede legale: Via G. Cusmano, 24 90141 PALERMO C.F. e P. I.V.A.: 05841760829 Dipartimento Farmaceutico Via Pindemonte 88 90128 PALERMO dipfarmaco@asppalermo.org FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE
La segnalazione via web con la piattaforma Vigifarmaco. Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona
 La segnalazione via web con la piattaforma Vigifarmaco Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra
La segnalazione via web con la piattaforma Vigifarmaco Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra
VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE
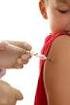 VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE Il concetto di farmacovigilanza si fonda sull assunto che nessun farmaco può essere considerato completamente sicuro ma risulta tale solo quando il rischio
VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE Il concetto di farmacovigilanza si fonda sull assunto che nessun farmaco può essere considerato completamente sicuro ma risulta tale solo quando il rischio
Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza. AIFA - Agenzia Italiana del Farmaco
 Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza AIFA - Agenzia Italiana del Farmaco Informazione di ritorno Nel 2012 l AIFA ha attivato un progetto ad hoc per la predisposizione
Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza AIFA - Agenzia Italiana del Farmaco Informazione di ritorno Nel 2012 l AIFA ha attivato un progetto ad hoc per la predisposizione
Il ruolo del Responsabile aziendale di Farmacovigilanza
 Il ruolo del Responsabile aziendale di Farmacovigilanza Bologna, 8 novembre 2013 Dott.ssa Mirna Magnani La farmacovigilanza ha 4 obiettivi principali: 1. riconoscere, il pi rapidamente possibile, nuove
Il ruolo del Responsabile aziendale di Farmacovigilanza Bologna, 8 novembre 2013 Dott.ssa Mirna Magnani La farmacovigilanza ha 4 obiettivi principali: 1. riconoscere, il pi rapidamente possibile, nuove
Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione
 Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione La cultura della farmacovigilanza per la sicurezza del paziente Bologna 26 gennaio, 2, 9 e 16
Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione La cultura della farmacovigilanza per la sicurezza del paziente Bologna 26 gennaio, 2, 9 e 16
REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA
 REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA Dati sulla segnalazione spontanea delle reazioni avverse a farmaci (ADR) in Regione Puglia nell anno 2016 Nella presente relazione vengono illustrati
REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA Dati sulla segnalazione spontanea delle reazioni avverse a farmaci (ADR) in Regione Puglia nell anno 2016 Nella presente relazione vengono illustrati
VIGER LA FARMACOVIGILANZA IN GERIATRIA. Progetto Regionale Farmacovigilanza
 VIGER LA FARMACOVIGILANZA IN GERIATRIA Progetto Regionale Farmacovigilanza COS È IL PROGETTO VIGER Il progetto VIGER (Vigilanza in Geriatria) è un progetto di farmacovigilanza finalizzato alla valutazione
VIGER LA FARMACOVIGILANZA IN GERIATRIA Progetto Regionale Farmacovigilanza COS È IL PROGETTO VIGER Il progetto VIGER (Vigilanza in Geriatria) è un progetto di farmacovigilanza finalizzato alla valutazione
Normativa Regolamento UE 1235/2010 Direttiva 2010/84/UE
 Implementazione delle nuove linee guida dell AIFA e principali modifiche introdotte dalla nuova normativa europea di Farmacovigilanza CEFPAS 24 marzo 2015 Claudia La Cavera Normativa Regolamento UE 1235/2010
Implementazione delle nuove linee guida dell AIFA e principali modifiche introdotte dalla nuova normativa europea di Farmacovigilanza CEFPAS 24 marzo 2015 Claudia La Cavera Normativa Regolamento UE 1235/2010
FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI.
 Caf Latium - Professione & Sviluppo Marzo 2006. FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI. I farmacisti (come operatori sanitari, oltre ai medici) sono tenuti
Caf Latium - Professione & Sviluppo Marzo 2006. FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI. I farmacisti (come operatori sanitari, oltre ai medici) sono tenuti
LA RETE NAZIONALE DI FARMACOVIGILANZA
 Primo Corso Regionale di Farmacovigilanza LA RETE NAZIONALE DI FARMACOVIGILANZA Dott.ssa Carmela Santuccio AIFA - Ufficio Farmacovigilanza Bologna 21 Febbraio 2008 Rete Nazionale di Farmacovigilanza: sistema
Primo Corso Regionale di Farmacovigilanza LA RETE NAZIONALE DI FARMACOVIGILANZA Dott.ssa Carmela Santuccio AIFA - Ufficio Farmacovigilanza Bologna 21 Febbraio 2008 Rete Nazionale di Farmacovigilanza: sistema
GUIDA ALLE PRATICHE ONLINE
 GUIDA ALLE PRATICHE ONLINE A cura del Settore Sistema informativo integrato SOMMARIO SCELTA E CREAZIONE DEL TIPO DI PRATICA 3 DETTAGLIO DELLA PRATICA 5 COMPILAZIONE DELLE SEZIONI 6 INSERIMENTO (E CANCELLAZIONE)
GUIDA ALLE PRATICHE ONLINE A cura del Settore Sistema informativo integrato SOMMARIO SCELTA E CREAZIONE DEL TIPO DI PRATICA 3 DETTAGLIO DELLA PRATICA 5 COMPILAZIONE DELLE SEZIONI 6 INSERIMENTO (E CANCELLAZIONE)
COMPILAZIONE DOMANDA
 COMPILAZIONE DOMANDA Alcuni campi dell istanza saranno già pre-compilati dal sistema con i dati inseriti all atto della registrazione (N.B. i valori sono comunque modificabili da parte dell utente). I
COMPILAZIONE DOMANDA Alcuni campi dell istanza saranno già pre-compilati dal sistema con i dati inseriti all atto della registrazione (N.B. i valori sono comunque modificabili da parte dell utente). I
Casi clinici. Esempi dalla realtà di Rimini. Presentazione di alcuni casi clinici (esempi dalla realtà di Rimini)
 Casi clinici Università di Bologna CReVIF Dipartimento di Farmacologia Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia- Romagna AUSL Piacenza
Casi clinici Università di Bologna CReVIF Dipartimento di Farmacologia Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia- Romagna AUSL Piacenza
L area pubblica è costituita da un portale informativo attraverso il quale è possibile effettuare la diffusione dell informazione.
 Area web Pubblica L area pubblica è costituita da un portale informativo attraverso il quale è possibile effettuare la diffusione dell informazione. L informazione contenuta nel portale può essere di tipo
Area web Pubblica L area pubblica è costituita da un portale informativo attraverso il quale è possibile effettuare la diffusione dell informazione. L informazione contenuta nel portale può essere di tipo
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria
 Corso di formazione sul campo a cura della sezione regionale SIFO Liguria DIPARTIMENTO DEL FARMACO S.C. FARMACEUTICA Settore Assistenza Farmaceutica Pec : farmacia@pec.asl4.liguria.it Email :farm.terr@asl4.liguria.it
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria DIPARTIMENTO DEL FARMACO S.C. FARMACEUTICA Settore Assistenza Farmaceutica Pec : farmacia@pec.asl4.liguria.it Email :farm.terr@asl4.liguria.it
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica
 Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci.
 VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci. Azienda Ulss n.13 Mirano (Ve) Servizio farmaceutico territoriale Settembre 2015 https://vigifarmaco.it
VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci. Azienda Ulss n.13 Mirano (Ve) Servizio farmaceutico territoriale Settembre 2015 https://vigifarmaco.it
Farmacovigilanza e Vigilanza Dispositivi medici
 Farmacovigilanza e Vigilanza Dispositivi medici Vigilanza Pre e post market Farmacovigilanza e Vigilanza Dispositivi Medici Partecipanti Pazienti ed utilizzatori, segnalatori, promotori commerciali e non
Farmacovigilanza e Vigilanza Dispositivi medici Vigilanza Pre e post market Farmacovigilanza e Vigilanza Dispositivi Medici Partecipanti Pazienti ed utilizzatori, segnalatori, promotori commerciali e non
Elementi di farmacovigilanza
 Elementi di farmacovigilanza Il Coordinamento della Ricerca 1 Corso ISG di Formazione per la Ricerca Clinica 28-Set-2015 Farmacovigilanza La sicurezza dei prodotti sperimentali (IMP) rappresenta un punto
Elementi di farmacovigilanza Il Coordinamento della Ricerca 1 Corso ISG di Formazione per la Ricerca Clinica 28-Set-2015 Farmacovigilanza La sicurezza dei prodotti sperimentali (IMP) rappresenta un punto
Gestione delle schede di segnalazione e nuove modifiche della Rete Nazionale di Farmacovigilanza (RNF) Paola Cutroneo
 Gestione delle schede di segnalazione e nuove modifiche della Rete Nazionale di Farmacovigilanza (RNF) Paola Cutroneo Centro Referente Regionale per la Segnalazione Spontanea, AOU Policlinico di Messina
Gestione delle schede di segnalazione e nuove modifiche della Rete Nazionale di Farmacovigilanza (RNF) Paola Cutroneo Centro Referente Regionale per la Segnalazione Spontanea, AOU Policlinico di Messina
Regione Puglia Ufficio Politiche del Farmaco e dell Emergenza/Urgenza dott.ssa Maria Cristina Carbonara BARI Giugno 2014
 Regione Puglia Ufficio Politiche del Farmaco e dell Emergenza/Urgenza dott.ssa Maria Cristina Carbonara BARI Giugno 2014 Definizione di Farmacovigilanza Normativa e obiettivi Le reazioni avverse Gli attori
Regione Puglia Ufficio Politiche del Farmaco e dell Emergenza/Urgenza dott.ssa Maria Cristina Carbonara BARI Giugno 2014 Definizione di Farmacovigilanza Normativa e obiettivi Le reazioni avverse Gli attori
RAPPORTO DI FARMACOVIGILANZA REGIONE PIEMONTE
 RAPPORTO DI FARMACOVIGILANZA REGIONE PIEMONTE A cura di Settore Assistenza Farmaceutica, Integrativa e Protesica Assessorato alla Sanità della Regione Piemonte Centro Regionale di Farmacovigilanza della
RAPPORTO DI FARMACOVIGILANZA REGIONE PIEMONTE A cura di Settore Assistenza Farmaceutica, Integrativa e Protesica Assessorato alla Sanità della Regione Piemonte Centro Regionale di Farmacovigilanza della
Novita portale fornitori Eni Aggiornamento del 02/10/2017
 Novità portale fornitori Eni - Aggiornamento del 02 ottobre 2017 Pagina 1 di 6 INDICE 1. Obiettivi del documento... 3 2. Visualizzazione fatture... 3 3. Comunicazioni e richieste informazioni... 3 4. Avvisi
Novità portale fornitori Eni - Aggiornamento del 02 ottobre 2017 Pagina 1 di 6 INDICE 1. Obiettivi del documento... 3 2. Visualizzazione fatture... 3 3. Comunicazioni e richieste informazioni... 3 4. Avvisi
Prot. n Frosinone,31/01/2018 FARMAINFORMA. Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018
 Prot. n. 10373 Frosinone,31/01/2018 FARMAINFORMA Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018 La numerosità delle segnalazioni di ADR è un criterio cardine per definire un
Prot. n. 10373 Frosinone,31/01/2018 FARMAINFORMA Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018 La numerosità delle segnalazioni di ADR è un criterio cardine per definire un
Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica)
 Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica) Versione 1.0 Giugno 2012 1 Indice Suggerimenti per il management del computer...3 Sospette reazioni avverse...5 Report Sospette Reazioni
Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica) Versione 1.0 Giugno 2012 1 Indice Suggerimenti per il management del computer...3 Sospette reazioni avverse...5 Report Sospette Reazioni
Manuale Utente Terapia farmacologica
 Manuale Utente Terapia farmacologica 1 Introduzione... 2 2 Prescrizione di una terapia somministrata... 2 3 Prescrizione di una terapia distribuita... 5 4 Visualizzazione di una terapia... 6 5 Somministrazione/distribuzione
Manuale Utente Terapia farmacologica 1 Introduzione... 2 2 Prescrizione di una terapia somministrata... 2 3 Prescrizione di una terapia distribuita... 5 4 Visualizzazione di una terapia... 6 5 Somministrazione/distribuzione
ISTRUZIONI - Bandi per l attribuzione di attività didattiche A.A
 ISTRUZIONI - Bandi per l attribuzione di attività didattiche A.A. 2016-2017 1. Per visionare i bandi o per presentare le domande occorre preliminarmente registrarsi come candidato. Per effettuare la registrazione
ISTRUZIONI - Bandi per l attribuzione di attività didattiche A.A. 2016-2017 1. Per visionare i bandi o per presentare le domande occorre preliminarmente registrarsi come candidato. Per effettuare la registrazione
Manuale Utente Questionario GEI-FTV
 Guida alla compilazione del questionario GEI-FTV per comunicazioni relative a interventi di manutenzione e ammodernamento tecnologico su impianti fotovoltaici in esercizio Procedure ai sensi del D.M. 23
Guida alla compilazione del questionario GEI-FTV per comunicazioni relative a interventi di manutenzione e ammodernamento tecnologico su impianti fotovoltaici in esercizio Procedure ai sensi del D.M. 23
LA FARMACOVIGILANZA in Liguria Rete e Centro regionale di farmacovigilanza ed indipendente sulfarmaco(criff)
 LA LEGISLAZIONE SUL FARMACO IN MEDICINA VETERINARIA E FARMACOVIGILANZA 23 GIUGNO 2012 GENOVA, SALA QUADRIVIUM P.ZZA Santa Marta 2 LA FARMACOVIGILANZA in Liguria Rete e Centro regionale di farmacovigilanza
LA LEGISLAZIONE SUL FARMACO IN MEDICINA VETERINARIA E FARMACOVIGILANZA 23 GIUGNO 2012 GENOVA, SALA QUADRIVIUM P.ZZA Santa Marta 2 LA FARMACOVIGILANZA in Liguria Rete e Centro regionale di farmacovigilanza
FONTUR MANUALE UTENTE
 FONTUR MANUALE UTENTE Si accede all Area riservata aziende del portale istituzionale del fondo www.fontur.it attraverso lo username e la password inviati via mail. Fig.1 Se non si è ancora in possesso
FONTUR MANUALE UTENTE Si accede all Area riservata aziende del portale istituzionale del fondo www.fontur.it attraverso lo username e la password inviati via mail. Fig.1 Se non si è ancora in possesso
Nota Informativa Importante. Guida alla Terapia per i Paziente. Guida alla Contraccezione. Modulo d'informazione e Consenso Informato
 AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
A39 - Patentini Fitosanitari. Manuale Utente
 A39 - Patentini Fitosanitari Manuale Utente Versione 1.0 Modello documento MU_A39_ManualeUtente_PatentiniFitosanitari_UtenteRichiedente_v1.0.docx SOMMARIO 1INTRODUZIONE...2 1.1CONTESTO...2 1.2PROFILI E
A39 - Patentini Fitosanitari Manuale Utente Versione 1.0 Modello documento MU_A39_ManualeUtente_PatentiniFitosanitari_UtenteRichiedente_v1.0.docx SOMMARIO 1INTRODUZIONE...2 1.1CONTESTO...2 1.2PROFILI E
Centro Regionale di documentazione e informazione sul farmaco
 La segnalazione di Reazioni Avverse in Calabria: Resoconto del 2011. Introduzione L obiettivo principale della Farmacovigilanza è l incremento della segnalazione spontanea delle reazioni avverse ai farmaci.
La segnalazione di Reazioni Avverse in Calabria: Resoconto del 2011. Introduzione L obiettivo principale della Farmacovigilanza è l incremento della segnalazione spontanea delle reazioni avverse ai farmaci.
ALLEGATO TECNICO PER PROGETTI DI FARMACOVIGILANZA ATTIVA FINANZIABILI ATTRAVERSO I FONDI FV 2010/11
 Allegato B ALLEGATO TECNICO PER PROGETTI DI FARMACOVIGILANZA ATTIVA FINANZIABILI ATTRAVERSO I FONDI FV 2010/11 REGIONE: Sardegna RESPONSABILI TECNICO-SCIENTIFICO DEL PROGETTO nome: Michela cognome: Pellecchia
Allegato B ALLEGATO TECNICO PER PROGETTI DI FARMACOVIGILANZA ATTIVA FINANZIABILI ATTRAVERSO I FONDI FV 2010/11 REGIONE: Sardegna RESPONSABILI TECNICO-SCIENTIFICO DEL PROGETTO nome: Michela cognome: Pellecchia
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
PROCEDURA DI ACCESSO IN CONDIZIONI ORDINARIE
 MODELLO DI PERCORSO REGIONALE UNIFICATO PER L ACCESSO ALL UTILIZZO TERAPEUTICO DI MEDICINALI SOTTOPOSTI A SPERIMENTAZIONE CLINICA (EXPANDED-ACCESS/USO COMPASSIONEVOLE) Il protocollo da sottoporre all impresa
MODELLO DI PERCORSO REGIONALE UNIFICATO PER L ACCESSO ALL UTILIZZO TERAPEUTICO DI MEDICINALI SOTTOPOSTI A SPERIMENTAZIONE CLINICA (EXPANDED-ACCESS/USO COMPASSIONEVOLE) Il protocollo da sottoporre all impresa
Manuale d uso del Sistema di e-procurement. Guida alla pre-abilitazione ai nuovi Bandi del Mercato Elettronico della PA
 Manuale d uso del Sistema di e-procurement Guida alla pre-abilitazione ai nuovi Bandi del Mercato Elettronico della PA Data ultimo aggiornamento: 12 giugno 2017 Soggetti ammessi... 3 1. Passo 1- Forma
Manuale d uso del Sistema di e-procurement Guida alla pre-abilitazione ai nuovi Bandi del Mercato Elettronico della PA Data ultimo aggiornamento: 12 giugno 2017 Soggetti ammessi... 3 1. Passo 1- Forma
Sorveglianza sulle reazioni avverse da vaccino: il progetto interregionale. Ugo Moretti Università di Verona
 Sorveglianza sulle reazioni avverse da vaccino: il progetto interregionale Ugo Moretti Università di Verona quando un tedesco non sa una cosa... la impara quando un americano non sa una cosa... paga per
Sorveglianza sulle reazioni avverse da vaccino: il progetto interregionale Ugo Moretti Università di Verona quando un tedesco non sa una cosa... la impara quando un americano non sa una cosa... paga per
Segnaliamo le sospette reazioni avverse! Come fare?
 La Farmacovigilanza. Perché, quando e come segnalare le Reazioni Avverse da Farmaci Segnaliamo le sospette reazioni avverse! Come fare? Dr. Michele Conti Regione Lazio Farmacista collaboratore di Farmacovigilanza
La Farmacovigilanza. Perché, quando e come segnalare le Reazioni Avverse da Farmaci Segnaliamo le sospette reazioni avverse! Come fare? Dr. Michele Conti Regione Lazio Farmacista collaboratore di Farmacovigilanza
Guida per il cittadino
 DOMANDA ONLINE PER L ISCRIZIONE ALLA SCUOLA DELL INFANZIA CAPITOLINA ANNO SCOLASTICO 2014/15 Guida per il Pagina 1 di 22 SOMMARIO Premessa 3 Domanda online - iscrizione scuola dell infanzia capitolina
DOMANDA ONLINE PER L ISCRIZIONE ALLA SCUOLA DELL INFANZIA CAPITOLINA ANNO SCOLASTICO 2014/15 Guida per il Pagina 1 di 22 SOMMARIO Premessa 3 Domanda online - iscrizione scuola dell infanzia capitolina
Il processo della logistica farmaceutica, prospettive e sfide per il farmacista SSN LA DOSE UNITARIA Teresa Cocquio Farmacia Ospedale di Forlì
 Il processo della logistica farmaceutica, prospettive e sfide per il farmacista SSN LA DOSE UNITARIA Teresa Cocquio Farmacia Ospedale di Forlì Contenuti della Presentazione o Premessa sul sistema Dose
Il processo della logistica farmaceutica, prospettive e sfide per il farmacista SSN LA DOSE UNITARIA Teresa Cocquio Farmacia Ospedale di Forlì Contenuti della Presentazione o Premessa sul sistema Dose
Istruzioni per l inserimento online delle richieste di sovvenzione:
 : ciascun socio può, attraverso il link servizi per i soci che trova all interno del sito della cassa di mutuo soccorso, inserire online la richiesta di sovvenzione. La richiesta dovrà essere compilata
: ciascun socio può, attraverso il link servizi per i soci che trova all interno del sito della cassa di mutuo soccorso, inserire online la richiesta di sovvenzione. La richiesta dovrà essere compilata
La nuova legislazione sulla Farmacovigilanza
 La nuova legislazione sulla Farmacovigilanza Responsabilità e compiti dell Azienda Farmaceutica Alessandra Del Porto MSD Italia S.r.l., GdL Farmacovigilanza Farmindustria Auditorium Confindustria Roma,
La nuova legislazione sulla Farmacovigilanza Responsabilità e compiti dell Azienda Farmaceutica Alessandra Del Porto MSD Italia S.r.l., GdL Farmacovigilanza Farmindustria Auditorium Confindustria Roma,
Guida per i docenti della piattaforma elearning
 Guida per i docenti della piattaforma elearning http://elearning.cinfor.it Cinfor 1 Modificare le impostazioni di un corso Effettuare il login con le proprie credenziali all indirizzo web http://elearning.cinfor.it
Guida per i docenti della piattaforma elearning http://elearning.cinfor.it Cinfor 1 Modificare le impostazioni di un corso Effettuare il login con le proprie credenziali all indirizzo web http://elearning.cinfor.it
Procedura per la richiesta di Borse di Studio
 Procedura per la richiesta di Borse di Studio Prima di accedere alla procedura che consente l invio della richiesta di borsa di studio per i figli dei dipendenti, occorre tenere presente che il figlio
Procedura per la richiesta di Borse di Studio Prima di accedere alla procedura che consente l invio della richiesta di borsa di studio per i figli dei dipendenti, occorre tenere presente che il figlio
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi FARMACOVIGILANZA
 La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza 20 e 22 novembre
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza 20 e 22 novembre
Manuale Operativo ASTE ELETTRONICHE GUIDA PER GLI OPERATORI ECONOMICI
 ASTE ELETTRONICHE GUIDA PER GLI OPERATORI ECONOMICI Roma, 25 Gennaio 2016 1 9 È possibile che le maschere inserite nel presente manuale siano differenti da quelle effettivamente utilizzate dall applicativo.
ASTE ELETTRONICHE GUIDA PER GLI OPERATORI ECONOMICI Roma, 25 Gennaio 2016 1 9 È possibile che le maschere inserite nel presente manuale siano differenti da quelle effettivamente utilizzate dall applicativo.
La segnalazione delle padr con il nuovo applicativo per il progetto Mereafaps5
 La segnalazione delle padr con il nuovo applicativo per il progetto Mereafaps5 G. Muti Centro Regionale di Farmacovigilanza 27 marzo 2015 Errore Terapeutico padr Schumock? Campo 7 ADR Cosa e come segnalare
La segnalazione delle padr con il nuovo applicativo per il progetto Mereafaps5 G. Muti Centro Regionale di Farmacovigilanza 27 marzo 2015 Errore Terapeutico padr Schumock? Campo 7 ADR Cosa e come segnalare
Oggetto : Sicurezza d uso di Olimel (aminoacidi elettroliti glucosio anidro lipidi)
 Regione Lombardia - Giunta DIREZIONE GENERALE SALUTE GOVERNO DEI DATI, DELLE STRATEGIE E PIANI DEL SISTEMA SANITARIO FARMACEUTICA, PROTESICA E DISPOSITIVI MEDICI Piazza Città di Lombardia n.1 20124 Milano
Regione Lombardia - Giunta DIREZIONE GENERALE SALUTE GOVERNO DEI DATI, DELLE STRATEGIE E PIANI DEL SISTEMA SANITARIO FARMACEUTICA, PROTESICA E DISPOSITIVI MEDICI Piazza Città di Lombardia n.1 20124 Milano
La nuova legislazione sulla Farmacovigilanza. Il sistema di qualità di farmacovigilanza in AIFA. Pietro Erba. Roma, 13 settembre 2012
 La nuova legislazione sulla Farmacovigilanza Il sistema di qualità di farmacovigilanza in AIFA Pietro Erba Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa
La nuova legislazione sulla Farmacovigilanza Il sistema di qualità di farmacovigilanza in AIFA Pietro Erba Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa
GUIDA OPERATIVA. Gestione richieste Assegni per il Nucleo. (norme/processi attinenti ad aree sensibili relative al D.Lgs 231/01)
 GUIDA OPERATIVA Gestione richieste Assegni per il Nucleo Familiare (norme/processi attinenti ad aree sensibili relative al D.Lgs 231/01) Percorso Destinatari Gestione risorse Gestione risorse umane Amministrazione
GUIDA OPERATIVA Gestione richieste Assegni per il Nucleo Familiare (norme/processi attinenti ad aree sensibili relative al D.Lgs 231/01) Percorso Destinatari Gestione risorse Gestione risorse umane Amministrazione
Il registro dei CE: aggiornamento e consultazione
 Corso sull Osservatorio Nazionale sulla Sperimentazione Clinica dei Medicinali (OsSC) rivolto ai Comitati Etici Bologna, 12,13, 19, 20, 26, 27 febbraio 2009 Il registro dei CE: aggiornamento e consultazione
Corso sull Osservatorio Nazionale sulla Sperimentazione Clinica dei Medicinali (OsSC) rivolto ai Comitati Etici Bologna, 12,13, 19, 20, 26, 27 febbraio 2009 Il registro dei CE: aggiornamento e consultazione
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI
 ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
La creazione di una Richiesta di Offerta semplificata. Aprile 2011
 La creazione di una Richiesta di Offerta semplificata Aprile 2011 Accesso all Area Personale 1/ Per procedere con la predisposizione di una RdO semplificata è necessario inserire la propria Utenza e Password
La creazione di una Richiesta di Offerta semplificata Aprile 2011 Accesso all Area Personale 1/ Per procedere con la predisposizione di una RdO semplificata è necessario inserire la propria Utenza e Password
AZIENDA OSPEDALIERA UNIVERSITARIA Policlinico Gaetano Martino di Messina
 AZIENDA OSPEDALIERA UNIVERSITARIA Policlinico Gaetano Martino di Messina Deliberazione del Commissario Straordinario n 103 del 30/01/2014 A seguito di Proposta n 74 del 27/01/2014 U.O.C. Settore Affari
AZIENDA OSPEDALIERA UNIVERSITARIA Policlinico Gaetano Martino di Messina Deliberazione del Commissario Straordinario n 103 del 30/01/2014 A seguito di Proposta n 74 del 27/01/2014 U.O.C. Settore Affari
CISOA Cassa Integrazione Salariale Operai Agricoli
 CISOA Cassa Integrazione Salariale Operai Agricoli Manuale Operativo per le aziende ed i consulenti pag. 1 di 22 Indice 1 GENERALITÀ...3 2 ACCESSO ALLA PROCEDURA...3 3 INTRODUZIONE...7 4 COMPILAZIONE...9
CISOA Cassa Integrazione Salariale Operai Agricoli Manuale Operativo per le aziende ed i consulenti pag. 1 di 22 Indice 1 GENERALITÀ...3 2 ACCESSO ALLA PROCEDURA...3 3 INTRODUZIONE...7 4 COMPILAZIONE...9
Rapporto Farmacovigilanza 2011 in Regione Piemonte
 Rapporto Farmacovigilanza 2011 in Regione Piemonte In Italia nel 2011 ci sono state 21.274 segnalazioni di sospette reazioni avverse da farmaci (ADRs), pari a 302 segnalazioni per milione di abitante,
Rapporto Farmacovigilanza 2011 in Regione Piemonte In Italia nel 2011 ci sono state 21.274 segnalazioni di sospette reazioni avverse da farmaci (ADRs), pari a 302 segnalazioni per milione di abitante,
Premessa. Responsabilità La responsabilità associata alla gestione della presente procedura è precisata nella Tabella 1 ( allegato 1)
 Premessa La somministrazione inappropriata endovenosa di sali di Potassio può comportare grave rischio per il paziente ed è una delle principali cause di incidenti ad effetto letale nelle unità operative
Premessa La somministrazione inappropriata endovenosa di sali di Potassio può comportare grave rischio per il paziente ed è una delle principali cause di incidenti ad effetto letale nelle unità operative
REGIONE TOSCANA SISTEMA INFORMATIVO CULTURA GLI EVENTI NELLE BIBLIOTECHE
 REGIONE TOSCANA SISTEMA INFORMATIVO CULTURA GLI EVENTI NELLE BIBLIOTECHE Il sistema informativo cultura raccoglie le informazioni sui luoghi della cultura: musei, biblioteche, archivi e luoghi dello spettacolo.
REGIONE TOSCANA SISTEMA INFORMATIVO CULTURA GLI EVENTI NELLE BIBLIOTECHE Il sistema informativo cultura raccoglie le informazioni sui luoghi della cultura: musei, biblioteche, archivi e luoghi dello spettacolo.
Regione Lazio. DIREZIONE SALUTE E POLITICHE SOCIALI Atti dirigenziali di Gestione 14/02/ BOLLETTINO UFFICIALE DELLA REGIONE LAZIO - N.
 Regione Lazio DIREZIONE SALUTE E POLITICHE SOCIALI Atti dirigenziali di Gestione Determinazione 2 febbraio 2017, n. G01055 Approvazione Avviso pubblico e fac-simile di domanda per la Manifestazione di
Regione Lazio DIREZIONE SALUTE E POLITICHE SOCIALI Atti dirigenziali di Gestione Determinazione 2 febbraio 2017, n. G01055 Approvazione Avviso pubblico e fac-simile di domanda per la Manifestazione di
Farmacovigilanza. Aggiornamenti sulla nuova normativa Settembre 2012
 Farmacovigilanza Aggiornamenti sulla nuova normativa Settembre 2012 Due nuove disposizioni in materia di farmacovigilanza Pubblicazione sulla Gazzetta ufficiale Europea L 348 del 31 Dic 2010: Regolamento
Farmacovigilanza Aggiornamenti sulla nuova normativa Settembre 2012 Due nuove disposizioni in materia di farmacovigilanza Pubblicazione sulla Gazzetta ufficiale Europea L 348 del 31 Dic 2010: Regolamento
Istruzioni per la Compilazione Online Domanda Servizio Civile
 Istruzioni per la Compilazione Online Domanda Servizio Civile Sommario 1 Generalità...2 1.1 Scopo...2 1.2 Validità...2 1.3 Riferimenti...2 2 Presentazione...2 3 Funzionalità...2 3.1 Modalità compilazione
Istruzioni per la Compilazione Online Domanda Servizio Civile Sommario 1 Generalità...2 1.1 Scopo...2 1.2 Validità...2 1.3 Riferimenti...2 2 Presentazione...2 3 Funzionalità...2 3.1 Modalità compilazione
Portale Acquisti RAI. Guida all iscrizione all Albo Fornitori
 Portale Acquisti RAI Guida all iscrizione all Albo Fornitori Registrazione al Portale Acquisti RAI Effettuare l accesso alla pagina web del Portale Acquisti RAI al seguente indirizzo: https://www.portaleacquisti.rai.it
Portale Acquisti RAI Guida all iscrizione all Albo Fornitori Registrazione al Portale Acquisti RAI Effettuare l accesso alla pagina web del Portale Acquisti RAI al seguente indirizzo: https://www.portaleacquisti.rai.it
Farmacovigilanza e Risk Management per la gestione dell errore terapeutico
 Farmacovigilanza e Risk Management per la gestione dell errore terapeutico Centro Regionale di Farmacovigilanza & Coordinamento Regionale per il Risk Management 20 marzo 2014 Un percorso integrato per
Farmacovigilanza e Risk Management per la gestione dell errore terapeutico Centro Regionale di Farmacovigilanza & Coordinamento Regionale per il Risk Management 20 marzo 2014 Un percorso integrato per
VADEMECUM PIATTAFORMA COSTRUTTORI
 VADEMECUM PIATTAFORMA COSTRUTTORI PRIMA FASE ISCRIZIONE ALLA PIATTAFORMA Le aziende interessate ad accedere alla piattaforma costruttori dovranno compilare il modulo di iscrizione collegandosi al sito
VADEMECUM PIATTAFORMA COSTRUTTORI PRIMA FASE ISCRIZIONE ALLA PIATTAFORMA Le aziende interessate ad accedere alla piattaforma costruttori dovranno compilare il modulo di iscrizione collegandosi al sito
Guida alla registrazione al Sistema di Gestione dell Albo Fornitori di REALE GROUP
 Guida alla registrazione al Sistema di Gestione dell Albo Fornitori di REALE GROUP A CHI SI RIVOLGE: a tutti i Fornitori Candidati al Sistema di Gestione dell Albo Fornitori di REALE GROUP, con un distinguo
Guida alla registrazione al Sistema di Gestione dell Albo Fornitori di REALE GROUP A CHI SI RIVOLGE: a tutti i Fornitori Candidati al Sistema di Gestione dell Albo Fornitori di REALE GROUP, con un distinguo
Il protocollo nazionale degli eventi sentinella
 La gestione del rischio clinico e della sicurezza del paziente Il protocollo nazionale degli eventi sentinella 1 Agenzia sanitaria e e Il Ministero della Salute 2003 Commissione tecnica Rischio clinico
La gestione del rischio clinico e della sicurezza del paziente Il protocollo nazionale degli eventi sentinella 1 Agenzia sanitaria e e Il Ministero della Salute 2003 Commissione tecnica Rischio clinico
Dote Lavoro Ambito persone con disabilità psichica
 Profilazione della Cooperativa Dote Lavoro Ambito persone con disabilità psichica Per poter accedere alla prenotazione della dote, è necessario che la Cooperativa si sia profilata. E sufficiente pertanto
Profilazione della Cooperativa Dote Lavoro Ambito persone con disabilità psichica Per poter accedere alla prenotazione della dote, è necessario che la Cooperativa si sia profilata. E sufficiente pertanto
GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI
 PA.DF.01 0 1 di 33 PROCEDURA AZIENDALE GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI PA.DF.01 0 2 di 33 INDICE PREMESSA
PA.DF.01 0 1 di 33 PROCEDURA AZIENDALE GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI PA.DF.01 0 2 di 33 INDICE PREMESSA
Guida rapida per l utilizzatore Browser
 ANticoagulant THEraphy MAnagement Guida rapida per l utilizzatore Browser Copyright 2010 Instrumentation Laboratory SpA Le informazioni contenute in questo documento sono proprietà di Instrumentation Laboratory
ANticoagulant THEraphy MAnagement Guida rapida per l utilizzatore Browser Copyright 2010 Instrumentation Laboratory SpA Le informazioni contenute in questo documento sono proprietà di Instrumentation Laboratory
GUIDA AIFA PER I RESPONSABILI DI FV ALLA GESTIONE DELLE SEGNALAZIONI NELLA RNF
 FV/CS /LP UFFICIO DI FARMACOVIGILANZA GUIDA AIFA PER I RESPONSABILI DI FV ALLA GESTIONE DELLE SEGNALAZIONI NELLA RNF Versione 2 Aggiornamento Febbraio 2015 Guida AIFA per i Responsabili di FV Aggiornamento
FV/CS /LP UFFICIO DI FARMACOVIGILANZA GUIDA AIFA PER I RESPONSABILI DI FV ALLA GESTIONE DELLE SEGNALAZIONI NELLA RNF Versione 2 Aggiornamento Febbraio 2015 Guida AIFA per i Responsabili di FV Aggiornamento
GUIDA ALLA REGISTRAZIONE
 GUIDA ALLA REGISTRAZIONE 1. Collegarsi al sito internet www.apservice.it/pslatina 2. Cliccare su registrati (fig. a) e nella nuova finestra inserire i dati richiesti e cliccare sul bottone REGISTRATI per
GUIDA ALLA REGISTRAZIONE 1. Collegarsi al sito internet www.apservice.it/pslatina 2. Cliccare su registrati (fig. a) e nella nuova finestra inserire i dati richiesti e cliccare sul bottone REGISTRATI per
Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore)
 1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
Cartella personale integrata e foglio unico di terapia. Nasce nell ambito del governo clinico, qualita e sicurezza delle cure
 Cartella personale integrata e foglio unico di terapia Nasce nell ambito del governo clinico, qualita e sicurezza delle cure Raccomandazione per la prevenzione della morte,coma o grave danno derivati da
Cartella personale integrata e foglio unico di terapia Nasce nell ambito del governo clinico, qualita e sicurezza delle cure Raccomandazione per la prevenzione della morte,coma o grave danno derivati da
Dr.ssa Laura Sottosanti AIFA - Ufficio Farmacovigilanza
 OSTEONECROSI DEI MASCELLARI (ONJ): PREVENZIONE, DIAGNOSI, TRATTAMENTO UPDATE 009 Alessandria, martedì 3 giugno 009 LE SEGNALAZIONI ALL AIFA I dati della Rete Nazionale di Farmacovigilanza (RNF) sui Bifosfonati
OSTEONECROSI DEI MASCELLARI (ONJ): PREVENZIONE, DIAGNOSI, TRATTAMENTO UPDATE 009 Alessandria, martedì 3 giugno 009 LE SEGNALAZIONI ALL AIFA I dati della Rete Nazionale di Farmacovigilanza (RNF) sui Bifosfonati
Arsenàl.IT. Centro Veneto Ricerca e Innovazione per la Sanità Digitale. GDL-O Documenti Clinici
 GDL-O Documenti Clinici Linee guida funzionali sulla Lettera di Dimissione Ospedaliera (LDO) Arsenàl.IT Centro Veneto Ricerca e Innovazione per la Sanità Digitale pag. 1 di 22 pag. 2 di 22 5 Informazioni
GDL-O Documenti Clinici Linee guida funzionali sulla Lettera di Dimissione Ospedaliera (LDO) Arsenàl.IT Centro Veneto Ricerca e Innovazione per la Sanità Digitale pag. 1 di 22 pag. 2 di 22 5 Informazioni
ASILI NIDO. Per il primo inserimento della domanda cliccare su Aggiungi. Sarà presentata la mappa per l inserimento dei dati della domanda :
 ASILI NIDO Prima di accedere alla procedura che consente l invio della richiesta di contributo per l asilo nido per i figli dei dipendenti, occorre tenere presente che il figlio o figli per cui viene inserita
ASILI NIDO Prima di accedere alla procedura che consente l invio della richiesta di contributo per l asilo nido per i figli dei dipendenti, occorre tenere presente che il figlio o figli per cui viene inserita
AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO
 AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante
AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante
Guida alla domanda di valutazione preventiva di crediti formativi universitari
 Guida alla domanda di valutazione preventiva di crediti formativi universitari La domanda di valutazione preventiva di crediti formativi universitari serve a conoscere quali esami o attività formative
Guida alla domanda di valutazione preventiva di crediti formativi universitari La domanda di valutazione preventiva di crediti formativi universitari serve a conoscere quali esami o attività formative
E stata pubblicata dall USR la circolare Prot. MIUR AOODRLO R.U n Milano, 09 giugno 2016 reperibile con l Intesa approvata su
 Como, 30 giugno 2016 Prot. n. 185/16 CB Circ. 7/16 C AI PRESIDENTI E COORDINATRICI DELLE SCUOLE DELL INFANZIA PARITARIE FISM DELLA PROVINCIA DI COMO Loro Sedi OGGETTO: DOMANDA CONTRIBUTO SEZIONI PRIMAVERA:
Como, 30 giugno 2016 Prot. n. 185/16 CB Circ. 7/16 C AI PRESIDENTI E COORDINATRICI DELLE SCUOLE DELL INFANZIA PARITARIE FISM DELLA PROVINCIA DI COMO Loro Sedi OGGETTO: DOMANDA CONTRIBUTO SEZIONI PRIMAVERA:
