Approssimativamente 20 sperimentatori (oncologi o pneumologi). Approssimativamente 20 centri in tutto il mondo.
|
|
|
- Margherita Luigina Maggio
- 6 anni fa
- Visualizzazioni
Transcript
1 SINOSSI Nome dello sponsor/azienda: Eisai Inc. Riservato alle Autorità Titolo dello studio: N. di protocollo: Sperimentatori: Centri dello studio: Studio in aperto, multicentrico, randomizzato, di fase Ib/II su eribulin mesilato somministrato in associazione con pemetrexed rispetto a pemetrexed in monoterapia nella seconda linea di trattamento di pazienti con carcinoma polmonare non a piccole cellule non squamocellulare di stadio IIIB o IV. Approssimativamente 20 sperimentatori (oncologi o pneumologi). Approssimativamente 20 centri in tutto il mondo. Durata dello studio: i pazienti saranno sottoposti al trattamento dello studio (eribulin mesilato in associazione con pemetrexed o pemetrexed in monoterapia) per circa sei cicli di 21 giorni (18 settimane) fino a progressione di malattia, tossicità inaccettabile, ritiro del consenso, ritiro dallo studio da parte dello sperimentatore, perdita al follow up o decesso, a seconda di quale evento si verifichi per primo. Obiettivi: Primari: Fase: Ib/II Fase Ib: definire la massima dose tollerata (MTD)/dose raccomandata di fase II di eribulin mesilato, d'ora in poi detto semplicemente eribulin, in ciascuno dei due regimi posologici, somministrato in associazione con pemetrexed a pazienti con carcinoma polmonare non a piccole cellule (NSCLC) non squamocellulare, trattati in precedenza con 1 regime chemioterapico citotossico per la malattia allo stadio IIIB o IV. Fase II: valutare la sicurezza e la tollerabilità di più dosi di eribulin somministrato in associazione con pemetrexed, rispetto a pemetrexed in monoterapia, a pazienti con NSCLC non squamocellulare, trattati in precedenza con 1 regime chemioterapico citotossico per la malattia allo stadio IIIB o IV. Secondario Fase II: effettuare una valutazione preliminare dell'efficacia di eribulin somministrato in associazione con pemetrexed, rispetto a pemetrexed in monoterapia, a pazienti con NSCLC non squamocellulare, trattati in precedenza con 1 regime chemioterapico citotossico per la malattia allo stadio IIIB o IV. Metodologia: Questo studio in aperto, multicentrico, randomizzato sarà costituito da una parte relativa alla fase Ib: un periodo preliminare di sicurezza con 3 dosi incrementali di eribulin in ciascuno dei due bracci paralleli di regimi posologici e da una parte relativa alla fase II: un disegno randomizzato a 3 bracci. I pazienti parteciperanno a una sola delle due parti relative alle fasi Ib o II e potranno continuare il trattamento fino alla progressione. Fase Ib I pazienti saranno reclutati in coorti, in uno di due bracci paralleli Eisai Inc. 1
2 Metodologia (segue): Numero di pazienti: che valutano diversi regimi posologici di eribulin (braccio 1: eribulin il giorno 1; braccio 2: eribulin i giorni 1 e 8), con un minimo di 3 e un massimo di 6 pazienti per coorte. Tutti i pazienti saranno trattati con pemetrexed (500 mg/m 2 ) in associazione con eribulin. Tutti i pazienti della stessa coorte saranno trattati con lo stesso livello di dose di eribulin e la dose non verrà aumentata tra un paziente e l'altro. Il livello di dose di eribulin sarà aumentato per le altre coorti in ciascuno dei due bracci a meno che non vengano segnalate 2 tossicità dose-limitanti (DLT) ai livelli di dose inferiori prima dell'arruolamento del livello di dose successivo. Per tossicità dose-limitanti si intendono eventi avversi (EA) clinicamente significativi che si manifestino 21 giorni dall'inizio del trattamento dello studio e che lo sperimentatore consideri potenzialmente o probabilmente correlati al trattamento dello studio. Se si verifica 1 DLT a qualsiasi livello di dose, la coorte verrà ampliata per includere fino a 6 pazienti. Se si verificano 2 DLT a qualsiasi livello di dose, la MTD sarà fissata alla dose precedente o a una dose intermedia. Per valutare una dose intermedia, è possibile aggiungere un'altra coorte di dose per definire la MTD in modo più accurato. Un comitato responsabile dell'aumento della dose determinerà quando non è più appropriato aumentare ulteriormente la dose e se la MTD deve essere fissata alla dose precedente o a una dose intermedia. Fase II I pazienti saranno randomizzati in rapporto 1:1:1 al trattamento con eribulin in associazione con pemetrexed, in ciascuno dei due regimi posologici (braccio 1 e 2), o al trattamento con pemetrexed in monoterapia (braccio 3). La dose di eribulin costituirà la MTD per eribulin quando somministrato in associazione con pemetrexed, come determinato nella parte dello studio relativa alla fase Ib. Per entrambe le fasi, Ib e II, 1 ciclo di terapia durerà 21 giorni, con un numero stimato di 6 cicli. Durante il periodo di screening e successivamente ogni 2 cicli fino a progressione di malattia, saranno eseguiti esami radiologici, compresa una TAC del torace, dell'addome e della pelvi, a seconda della situazione [e TAC o risonanza magnetica (RM) a seconda della situazione]. Le valutazioni radiologiche devono essere ripetute al ritiro dallo studio se l'ultimo esame è stato eseguito >3 settimane dalla sospensione della terapia. Fase Ib: approssimativamente pazienti. Fase II: approssimativamente 120 pazienti. Criteri di inclusione inclusione: I pazienti possono essere arruolati nello studio solo se Eisai Inc. 2
3 inclusione (segue): soddisfano tutti i seguenti criteri: 1. Pazienti di sesso maschile o femminile di età 18 anni. 2. NSCLC non squamocellulare di stadio IIIb istologicamente o citologicamente confermato con versamento pleurico maligno o malattia di stadio IV non assoggettabile a terapia curativa. Sono idonei anche i pazienti con anamnesi di malattia di stadio III con recidiva dopo chemio e radioterapia. 3. Almeno 1 sito di malattia misurabile secondo la versione 1.1 dei criteri RECIST (Response Evaluation Criteria in Solid Tumors, Criteri di valutazione della risposta nei tumori solidi). 4. Fallimento di 1 regime chemioterapico precedente con doppietta a base di platino per NSCLS non squamocellulare di stadio IIIB con versamento pleurico maligno o di stadio IV. È consentito un regime citotossico aggiuntivo per la terapia neoadiuvante, adiuvante o neoadiuvante più adiuvante per i pazienti nella fase II. Per i pazienti arruolati nella parte dello studio relativa alla fase Ib, è consentito un massimo di tre regimi precedenti in totale. Definizione di un regime chemioterapico: è considerato 1 regime qualsiasi chemioterapia con doppietta a base di platino, che può includere anche farmaci biologici o mirati e/o anticorpi umanizzati, somministrati in concomitanza, in sequenza o entrambi. Se, a causa della tossicità, è necessario ridurre o omettere 1 o più dei componenti del regime oppure sostituirli con altri farmaci simili, la versione modificata del regime originale non è considerata un nuovo regime. Tuttavia, se si aggiunge al regime un nuovo componente, dissimile dai componenti originali, la nuova associazione è considerata un nuovo regime. Un trattamento che venga interrotto per un intervento chirurgico o per la radioterapia e quindi prosegua con schema e componenti immutati, è considerato un regime nonostante l'interruzione. 5. Aspettativa di vita 3 mesi. 6. Performance status secondo l Eastern Cooperative Oncology Group (ECOG) I pazienti devono presentare un'adeguata funzionalità renale mostrata dalla clearance della creatinina 45 ml/min calcolata secondo la formula di Cockcroft e Gault. 8. I pazienti sottoposti a trattamento giornaliero con farmaci antinfiammatori non steroidei (FANS) sono idonei. I pazienti con clearance della creatinina ml/min devono essere in grado di interrompere i FANS 2 giorni prima della somministrazione (5 giorni per i FANS a rilascio prolungato), il giorno della somministrazione e 2 giorni dopo la somministrazione di pemetrexed. 9. I pazienti devono presentare un'adeguata funzionalità del midollo osseo mostrata dalla conta dei neutrofili (ANC) 1,5 X 10 9 /l, emoglobina 9,0 g/dl (emoglobina <9,0 g/dl allo Eisai Inc. 3
4 inclusione (segue): screening è accettabile se è corretta a 9 g/dl da fattore di crescita o trasfusione prima della prima dose) e conta delle piastrine 100 X 10 9 /l. 10. I pazienti devono presentare un'adeguata funzionalità epatica mostrata da bilirubina 1,5 volte il limite superiore della norma (ULN) e fosfatasi alcalina, alanina aminotransferasi (ALT) e aspartato aminotransferasi (AST) 3 X ULN (in caso di metastasi epatiche 5 X ULN). In presenza di metastasi ossee, la fosfatasi alcalina specifica del fegato può essere separata da quella totale e utilizzata per valutare la funzionalità epatica al posto della fosfatasi alcalina totale. 11. I pazienti fertili di entrambi i sessi devono accettare di utilizzare un metodo anticoncezionale a doppia barriera, anticoncezionali orali o misure per evitare la gravidanza durante lo studio e per 90 giorni dopo l'ultimo giorno di trattamento. 12. Le donne fertili devono presentare un test di gravidanza negativo eseguito sul siero. 13. Le donne non devono allattare al seno. 14. I pazienti devono essere in grado di comprendere e disposti a firmare un consenso informato scritto. Criteri di esclusione I pazienti non verranno arruolati nello studio per uno qualsiasi dei seguenti motivi: 1. Trattamento precedente con pemetrexed, epotilone, ixabepilone, patupilone, alicondrina B o composti simili all'alicondrina B. 2. Trattamento con chemioterapia, terapia mirata, radioterapia, chirurgia o immunoterapia nei 30 giorni precedenti all'inizio del trattamento dello studio o mancato recupero da tutte le tossicità correlate al trattamento fino al grado 1, ad eccezione dell'alopecia. 3. Anamnesi di altre neoplasie maligne ad eccezione di: (1) carcinoma cutaneo basocellulare o squamocellulare adeguatamente trattato; (2) a) carcinoma in situ delle cervice uterina, b) cancro della prostata o c) cancro superficiale della vescica trattati in modo curativo; o (3) altro tumore solido trattato in modo curativo senza evidenza di malattia per 5 anni. 4. Presenza di metastasi cerebrale, a meno che il paziente sia stato sottoposto a trattamento adeguato almeno 4 settimane prima della randomizzazione, sia stabile e asintomatico e abbia sospeso gli steroidi da almeno 4 settimane prima della randomizzazione. 5. Trattamento in un altro studio clinico nei 30 giorni precedenti all'inizio del trattamento dello studio o pazienti che non si sono ripresi dagli effetti collaterali di un farmaco sperimentale Eisai Inc. 4
5 inclusione (segue): fino al grado 1, fatta eccezione per l'alopecia. 6. Qualsiasi altro trattamento in corso del tumore, compresa radioterapia palliativa, ad eccezione delle terapie per il controllo dei sintomi. 7. Neuropatia periferica di grado 3 secondo i criteri comuni di tossicità (CTC). 8. Necessità di dosi terapeutiche di antagonisti della vitamina K. 9. Versamenti pleurici, asciti o altri accumuli di fluidi nel terzo spazio non controllati. 10. Diabete mellito di tipo 1 o 2 non controllato. Dose e via di somministrazione del prodotto oggetto di studio: Dose e via di somministrazione della terapia di riferimento: 11. Compromissione cardiovascolare significativa [anamnesi di insufficienza cardiaca congestizia grado >II secondo NYHA (New York Heart Association), angina instabile o infarto miocardico negli ultimi 6 mesi oppure aritmia cardiaca seria]. 12. Pazienti con allotrapianto di organo che richiedano immunosoppressione. 13. Positività accertata al virus dell'immunodeficienza umana (HIV), all'antigene di superficie del virus dell'epatite B o al virus dell'epatite C. 14. Ipersensibilità all'alicondrina B e/o ai derivati chimici dell'alicondrina B. o 15. Qualsiasi altra condizione clinica che interferisca con la conduzione dello studio. (eribulin; E7389) somministrato in bolo endovenoso (EV) nell'arco di 2-5 minuti in uno di due regimi posologici per entrambe le parti dello studio relative alle fasi Ib e II: i giorni 1 e 8 di un ciclo di 21 giorni in dosi incrementali di 0,7, 1,1 o 1,4 mg/m 2 o il giorno 1 del ciclo di 21 giorni in dosi incrementali di 0,9, 1,4 o 2,0 mg/m 2. Per la parte dello studio relativa alla fase II, la dose sarà la MTD determinata durante la parte dello studio relativa alla fase Ib. Pemetrexed somministrato a una dose di 500 mg/m 2 come infusione EV il giorno 1 di un ciclo di 21 giorni. I pazienti saranno inoltre trattati con desametasone e integratori vitaminici come raccomandato nelle informazioni per la prescrizione di pemetrexed. Criteri di valutazione: Fase Ib La MTD di eribulin somministrato in associazione con pemetrexed in ciascuno dei due bracci paralleli di dosaggio sarà determinata come indicato di seguito: se si verificano 2 DLT a qualsiasi livello di dose, la MTD sarà fissata alla dose precedente o a una dose intermedia. Per valutare una dose intermedia, è possibile aggiungere un'altra coorte di dose per definire la MTD in modo più accurato. Eisai Inc. 5
6 Fase II Sicurezza: I parametri di sicurezza includeranno: eventi avversi (EA), segni vitali, PS ECOG, valutazioni cliniche di laboratorio, esami obiettivi ed elettrocardiogrammi (ECG) a 12 derivazioni. Tutti i dati degli EA saranno raccolti a ogni visita utilizzando la versione 4.0 dei criteri comuni di tossicità (CTCAE v.4.0). Efficacia preliminare: L'endpoint esplorativo primario di efficacia sarà la sopravvivenza libera da progressione (PFS) mediana, nello stesso gruppo di trattamento, definita come il tempo trascorso dalla data di randomizzazione di un paziente fino alla prima delle due seguenti date: (1) data della prima progressione documentata della malattia del paziente in base alla valutazione dello sperimentatore secondo i criteri RECIST o (2) data del decesso del paziente per qualsiasi causa. Efficacia secondaria: Gli endpoint esplorativi secondari di efficacia comprendono il tasso di PFS alla settimana 12, il tempo alla progressione (TTP) mediano, la sopravvivenza globale (OS) e il tasso di risposta obiettiva (ORR), nello stesso gruppo di trattamento. Metodi statistici: Determinazione della dimensione del campione: Non è stata specificata alcuna ipotesi statistica formale. Il numero di pazienti arruolati nello studio è considerato adeguato per una valutazione preliminare della sicurezza e della tollerabilità di E7389 in associazione con terapia standard. Popolazioni di analisi: Fase Ib Popolazione di sicurezza: tutti i pazienti arruolati nella parte dello studio relativa alla fase Ib, ad eccezione di chi (i) si è ritirato dallo studio prima di essere trattato con il farmaco dello studio o (ii) non dispone di valutazione di sicurezza dopo la prima dose del farmaco dello studio. Fase II Popolazione di sicurezza: tutti i pazienti arruolati e randomizzati al trattamento nella parte dello studio relativa alla fase II, ad eccezione di chi (i) si è ritirato dallo studio prima di essere trattato con il farmaco dello studio o (ii) non dispone di valutazione di sicurezza dopo la prima dose del farmaco dello studio. Popolazione Intent-to-Treat modificata (MITT): tutti i pazienti randomizzati nel braccio applicabile dello studio, fatta eccezione per i pazienti che si ritirino da tale braccio prima di essere trattati con il farmaco di confronto o sperimentale. I pazienti saranno analizzati in base al farmaco effettivamente assunto. Per entrambe le parti dello studio relative alle fasi Ib e II, tutti i dati di tutte le visite dei pazienti, che si verificano prima della chiusura del database, saranno inclusi nel database per l'analisi iniziale. Gli endpoint di sicurezza saranno basati sulla popolazione di sicurezza. Gli endpoint di efficacia saranno basati sulla popolazione MITT. Inoltre, i dati per i pazienti della popolazione di sicurezza della fase Ib, trattati con la dose di Eisai Inc. 6
7 eribulin mesilato scelta per la parte dello studio relativa alla fase II, saranno raggruppati insieme ai dati dei pazienti della popolazione di sicurezza della fase II per riepiloghi di sicurezza separati. Metodi analitici: In generale, verranno presentati riepiloghi descrittivi per le variabili di sicurezza e di efficacia raccolte. Le variabili continue saranno riassunte utilizzando media, deviazione standard, valore minimo, valore mediano e valore massimo. Le variabili categoriche saranno riassunte utilizzando valori numerici e percentuali della frequenza. Per le variabili di tempo all'evento, verranno presentati grafici di Kaplan-Meier, tempo mediano all'evento e altri percentili. Gli eventi avversi saranno codificati secondo MedDRA (Medical Dictionary for Regulatory Activities, Dizionario medico per le attività di regolamentazione) e saranno riassunti per classificazione organo-sistemica e termine preferito. Saranno inoltre presentati riepiloghi di EA per gravità e relazione con il farmaco dello studio. Eisai Inc. 7
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO
 Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
SINOSSI Protocollo MO19390 SAIL
 SINOSSI Protocollo MO19390 SAIL TITOLO INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO Studio in aperto con bevacizumab (Avastin ) in combinazione con un regime chemioterapico contenente platino per il trattamento
SINOSSI Protocollo MO19390 SAIL TITOLO INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO Studio in aperto con bevacizumab (Avastin ) in combinazione con un regime chemioterapico contenente platino per il trattamento
II GOIM Prof. Giuseppe Colucci Direttore Dipartimento Oncologia Medica Istituto Tumori G.PaoloII, Bari
 1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
SINOSSI DEL PROTOCOLLO ML21868
 TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
Sinossi Protocollo Sperimentale GOIM 21002
 1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
Sinossi Protocollo LEGA Versione No. 1 Finale, 11 Novembre 2011
 1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
SINOSSI. Studio di Fase II: Obiettivo primario Determinare l attività antitumorale della combinazione in termini di tempo alla progressione
 SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
RIASSUNTO IN ITALIANO DEL PROTOCOLLO H3E-EW-S124
 RIASSUNTO IN ITALIANO DEL PROTOCOLLO H3E-EW-S124 STUDIO DI FASE III RANDOMIZZATO, IN DOPPIO CIECO, CON PEMETREXED PIÙ BEST SUPPORTIVE CARE (BSC) VERSO PLACEBO PIÙ BEST SUPPORTIVE CARE COME TERAPIA DI MANTENIMENTO
RIASSUNTO IN ITALIANO DEL PROTOCOLLO H3E-EW-S124 STUDIO DI FASE III RANDOMIZZATO, IN DOPPIO CIECO, CON PEMETREXED PIÙ BEST SUPPORTIVE CARE (BSC) VERSO PLACEBO PIÙ BEST SUPPORTIVE CARE COME TERAPIA DI MANTENIMENTO
Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy. Studio di fase II randomizzato, open-label. Carcinoma Colorettale (CCR) Metastatico
 VERS. PROTOCOLLO 3.0 25 Novembre 2013 SPONSOR FASE STUO INCAZIONE RAZIONALE DELLO STUO Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy Studio di fase II randomizzato, open-label Carcinoma Colorettale (CCR)
VERS. PROTOCOLLO 3.0 25 Novembre 2013 SPONSOR FASE STUO INCAZIONE RAZIONALE DELLO STUO Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy Studio di fase II randomizzato, open-label Carcinoma Colorettale (CCR)
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs
 Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
SINOSSI. EudraCT number Versione del protocollo Version Octobre 2013
 SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
Versione PROTOCOLLO DI STUDIO
 Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
1 Sinossi. Numero dello studio EMR Merck KGaA, Darmstadt, Germania. Fase di studio
 1 Sinossi Titolo dello studio Uno studio aperto, randomizzato, di Fare II in soggetti affetti da carcinoma polmonare a piccole cellule malattia estesa (ED-SCLC), dopo una risposta iniziale (risposta completa
1 Sinossi Titolo dello studio Uno studio aperto, randomizzato, di Fare II in soggetti affetti da carcinoma polmonare a piccole cellule malattia estesa (ED-SCLC), dopo una risposta iniziale (risposta completa
SINOSSI protocollo 2903 [v. 13 settembre 2009]
![SINOSSI protocollo 2903 [v. 13 settembre 2009] SINOSSI protocollo 2903 [v. 13 settembre 2009]](/thumbs/69/60075672.jpg) GOIM 2903 Titolo dello studio: Cisplatino e Pemetrexed seguita da pemetrexed in mantenimento vs Carboplatino- Paclitaxel e Bevacizumab seguita da Bevacizumab in mantenimento: studio multicentrico randomizzato
GOIM 2903 Titolo dello studio: Cisplatino e Pemetrexed seguita da pemetrexed in mantenimento vs Carboplatino- Paclitaxel e Bevacizumab seguita da Bevacizumab in mantenimento: studio multicentrico randomizzato
STUDIO PANDA. Sinossi
 Titolo Studio di fase II randomizzato di prima linea con FOLFO/panitumumab e 5FU/panitumumab in pazienti anziani con carcinoma colorettale metastatico RAS e BRAF wild-type. Versione 2.2 del 18.04.2016
Titolo Studio di fase II randomizzato di prima linea con FOLFO/panitumumab e 5FU/panitumumab in pazienti anziani con carcinoma colorettale metastatico RAS e BRAF wild-type. Versione 2.2 del 18.04.2016
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI
 ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ZACTIMA è un marchio commerciale del gruppo di società AstraZeneca.
 Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
STUDIO GRUPPO ITALIANO PANCREAS GIP-2
 STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
ALGORITMI E PERCORSI TERAPEUTICI CARCINOMI DEL POLMONE NON-MICROCITOMA (NSCLC)
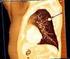 ALGORITMI E PERCORSI TERAPEUTICI CARCINOMI DEL POLMONE NON-MICROCITOMA (NSCLC) Data di aggiornamento: Luglio 2014 Indicazione a supporto cure palliative senza terapia oncologica specifica in pazienti con
ALGORITMI E PERCORSI TERAPEUTICI CARCINOMI DEL POLMONE NON-MICROCITOMA (NSCLC) Data di aggiornamento: Luglio 2014 Indicazione a supporto cure palliative senza terapia oncologica specifica in pazienti con
Dott. Francesco Fiorica
 Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Protocollo clinico. Codice dello studio: FIL R2-B Fase II Numero EudraCT: VERSIONE N MARZO 2012
 Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
(CRICKET) - EUDRACT Gruppo Oncologico Nord-Ovest (G.O.N.O.)
 APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017)
 POLMONE PROTOCOLLO TS-IRST PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017) Protocollo Descrizione protocollo Breve Sinossi Studio HighTySy randomizzato, di fase II, in aperto, disegnato per confrontare
POLMONE PROTOCOLLO TS-IRST PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017) Protocollo Descrizione protocollo Breve Sinossi Studio HighTySy randomizzato, di fase II, in aperto, disegnato per confrontare
SINOSSI STUDIO IRST ITACa: Italian Trial in Advanced Colorectal Cancer
 SINOSSI STUDIO IRST 153 01 - ITACa: Italian Trial in Advanced Colorectal Cancer Titolo Responsabile dello studio Centri partecipanti Background e razionale Strategia di terapia sistemica nel carcinoma
SINOSSI STUDIO IRST 153 01 - ITACa: Italian Trial in Advanced Colorectal Cancer Titolo Responsabile dello studio Centri partecipanti Background e razionale Strategia di terapia sistemica nel carcinoma
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO Titolo Numero di protocollo Studio multicentrico, in aperto, randomizzato e adattivo di palifosfamide-tris, un nuovo DNA crosslinker, in combinazione con chemioterapia con carboplatino
SINOSSI DEL PROTOCOLLO Titolo Numero di protocollo Studio multicentrico, in aperto, randomizzato e adattivo di palifosfamide-tris, un nuovo DNA crosslinker, in combinazione con chemioterapia con carboplatino
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
TERAPIA MEDICA. Federica Grosso
 Federica Grosso # 230 nuovi casi/anno ~ 60 90 Provincia di Alessandria 33/100.000 anno CPO Piemonte Federica Grosso 2 INCIDENZA IN ITALIA 1.400 nuovi casi/anno UOMINI: 3,84/100.000 anno DONNE: 1,45/100.000
Federica Grosso # 230 nuovi casi/anno ~ 60 90 Provincia di Alessandria 33/100.000 anno CPO Piemonte Federica Grosso 2 INCIDENZA IN ITALIA 1.400 nuovi casi/anno UOMINI: 3,84/100.000 anno DONNE: 1,45/100.000
ERLOTINIB ( )
 ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
Sinossi Prot.GOIM 2802
 1 Sinossi Prot.GOIM 2802 TRATTAMENTO DI I LINEA CON BEVACIZUMAB + FOLFOX4 O XELOX2 NEL CARCINOMA COLORETTALE. STUDIO DI FASE II RANDOMIZZATO Ricercatore responsabile: Evaristo Maiello Dipartimento di Oncoematologia
1 Sinossi Prot.GOIM 2802 TRATTAMENTO DI I LINEA CON BEVACIZUMAB + FOLFOX4 O XELOX2 NEL CARCINOMA COLORETTALE. STUDIO DI FASE II RANDOMIZZATO Ricercatore responsabile: Evaristo Maiello Dipartimento di Oncoematologia
SINOSSI DEL PROTOCOLLO NUMERO BO25460
 SINOSSI DEL PROTOCOLLO NUMERO BO25460 TITOLO Studio di fase III randomizzato, in doppio cieco, controllato con placebo, diretto a confrontare la terapia di mantenimento di prima linea con Tarceva e la
SINOSSI DEL PROTOCOLLO NUMERO BO25460 TITOLO Studio di fase III randomizzato, in doppio cieco, controllato con placebo, diretto a confrontare la terapia di mantenimento di prima linea con Tarceva e la
TRASTUZUMAB ( )
 TRASTUZUMAB (13-09-2006) Specialità: Herceptin (Roche) Forma farmaceutica: 1fl ev 150 mg - Prezzo: euro 1.1004 ATC: L01XC03 Categoria terapeutica: altri antineoplastici: anticorpi monoclonali Fascia di
TRASTUZUMAB (13-09-2006) Specialità: Herceptin (Roche) Forma farmaceutica: 1fl ev 150 mg - Prezzo: euro 1.1004 ATC: L01XC03 Categoria terapeutica: altri antineoplastici: anticorpi monoclonali Fascia di
STUDY ID: FIL_RENOIR12 EUDRACT NUMBER
 Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
I numeri del cancro in Italia Sandro Barni
 I numeri del cancro in Italia 2017 Sandro Barni I quesiti in Sanità Pubblica nel 2017 Quale è l impatto della patologia neoplastica in Italia? Come si è modificato l andamento per le diverse neoplasie
I numeri del cancro in Italia 2017 Sandro Barni I quesiti in Sanità Pubblica nel 2017 Quale è l impatto della patologia neoplastica in Italia? Come si è modificato l andamento per le diverse neoplasie
Studio ID: FIL_FOLL12 VERSIONE E DATA: VERSIONE LUGLIO 2012 EUDRACT NUMBER:
 Studio multicentrico, randomizzato di fase III per valutare l efficacia di una strategia di mantenimento modulata sulla base della risposta al trattamento di induzione con chemioimmunoterapia standard
Studio multicentrico, randomizzato di fase III per valutare l efficacia di una strategia di mantenimento modulata sulla base della risposta al trattamento di induzione con chemioimmunoterapia standard
SINOSSI. Istituto Clinico Humanitas - Humanitas Cancer Center Dr.ssa Monica Balzarotti. Versione 2.0 / 11 Novembre 2013
 SINOSSI Title Investigator Sponsor Coordinatore dello studio Numero identificativo Versione del protocollo Razionale Fase Popolazione in studio e selezione dei pazienti Ofatumumab-Bendamustina nei linfomi
SINOSSI Title Investigator Sponsor Coordinatore dello studio Numero identificativo Versione del protocollo Razionale Fase Popolazione in studio e selezione dei pazienti Ofatumumab-Bendamustina nei linfomi
Il protocollo di ricerca
 Infermiere di ricerca Il protocollo di ricerca Dr. Monica Turazza Negrar, 17 maggio 2017 Cosa rappresenta: percorso da seguire in qualsiasi forma di sperimentazione pianificata che riguardi prevenzione,
Infermiere di ricerca Il protocollo di ricerca Dr. Monica Turazza Negrar, 17 maggio 2017 Cosa rappresenta: percorso da seguire in qualsiasi forma di sperimentazione pianificata che riguardi prevenzione,
Metastasi cerebrali: Trattamento. Jennifer Foglietta Oncologia Medica - Perugia
 Metastasi cerebrali: Trattamento Jennifer Foglietta Oncologia Medica - Perugia Controllare i sintomi neurologici Trattamento delle metastasi cerebrali 1. Locale Radioterapia panencefalica (WBRT) Chirurgia
Metastasi cerebrali: Trattamento Jennifer Foglietta Oncologia Medica - Perugia Controllare i sintomi neurologici Trattamento delle metastasi cerebrali 1. Locale Radioterapia panencefalica (WBRT) Chirurgia
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Ruolo della chemioterapia nel trattamento dei pazienti affetti da carcinoma del canale anale T1-2 N0: Analisi retrospettiva di 140 pazienti
 Ruolo della chemioterapia nel trattamento dei pazienti affetti da carcinoma del canale anale T- N: Analisi retrospettiva di 4 pazienti Dr.ssa Laëtitia Lestrade Background Studi clinici randomizzati (anni
Ruolo della chemioterapia nel trattamento dei pazienti affetti da carcinoma del canale anale T- N: Analisi retrospettiva di 4 pazienti Dr.ssa Laëtitia Lestrade Background Studi clinici randomizzati (anni
Boehringer Ingelheim Sinossi del Protocollo - Versione 1.0 del 05 Febbraio 2010 Studio N di 11 SINOSSI DEL PROTOCOLLO
 1 di 11 SINOSSI DEL PROTOCOLLO Titolo dello : Studio randomizzato di fase III con con aggiunta di paclitaxel settimanale verso monochemioterapia a scelta in seguito a monoterapia con in pazienti con tumore
1 di 11 SINOSSI DEL PROTOCOLLO Titolo dello : Studio randomizzato di fase III con con aggiunta di paclitaxel settimanale verso monochemioterapia a scelta in seguito a monoterapia con in pazienti con tumore
Innovatività per i pazienti
 Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR)
 Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/09/2017)
 PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/09/2017) Protocollo Descrizione protocollo Breve Sinossi POLMONE Studio EDEN IN CORSO DI ATTIVAZIONE Studio randomizzato di fase III, in aperto, di Nivolumab
PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/09/2017) Protocollo Descrizione protocollo Breve Sinossi POLMONE Studio EDEN IN CORSO DI ATTIVAZIONE Studio randomizzato di fase III, in aperto, di Nivolumab
IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI
 IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI CAGLIARI CAESAR S HOTEL 10 OTTOBRE 2015 Alessio Cubeddu Manuela Dettori CASO CLINICO N 1 PAZIENTE RAS WT NON
IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI CAGLIARI CAESAR S HOTEL 10 OTTOBRE 2015 Alessio Cubeddu Manuela Dettori CASO CLINICO N 1 PAZIENTE RAS WT NON
SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE
 SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE Studio prospettico, non interventistico, di coorte, sul rischio di tromboembolismo venoso (TEV) in pazienti sottoposti a un nuovo trattamento chemioterapico per
SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE Studio prospettico, non interventistico, di coorte, sul rischio di tromboembolismo venoso (TEV) in pazienti sottoposti a un nuovo trattamento chemioterapico per
N cartella N ricovero Cognome Nome Data di nascita DICHIARAZIONE DI AVVENUTA INFORMAZIONE ED ESPRESSIONE DEL CONSENSO A TRATTAMENTO CHEMIOTERAPICO
 Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Fondazione Italia Fondazione It alia Linf omi Linf ONLUS
 Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
LGH447. Sinossi del protocollo dello studio CLGH447X2102
 LGH447 Sinossi del protocollo dello studio CLGH447X2102 Studio di Fase I, multicentrico, in aperto, con LGH447 somministrato per via orale in pazienti con leucemia mieloide acuta o sindrome mielodisplastica
LGH447 Sinossi del protocollo dello studio CLGH447X2102 Studio di Fase I, multicentrico, in aperto, con LGH447 somministrato per via orale in pazienti con leucemia mieloide acuta o sindrome mielodisplastica
SINOSSI DEL PROTOCCOLO
 Protocollo GO27821, versione 2 SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II, RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA
Protocollo GO27821, versione 2 SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II, RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA
AMPHOTERICIN B (AMBISOME
 SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
LINEE GUIDA TERAPEUTICHE TUMORE DELLA PROSTATA
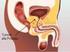 LINEE GUIDA TERAPEUTICHE TUMORE DELLA PROSTATA Data di aggiornamento: novembre 2013 TERAPIA PRIMARIA RISCHIO MOLTO BASSO: (previa biopsia) T1a Follow-up urologico Chirurgia RISCHIO MOLTO BASSO: T1c e Gleason
LINEE GUIDA TERAPEUTICHE TUMORE DELLA PROSTATA Data di aggiornamento: novembre 2013 TERAPIA PRIMARIA RISCHIO MOLTO BASSO: (previa biopsia) T1a Follow-up urologico Chirurgia RISCHIO MOLTO BASSO: T1c e Gleason
INduction chemotherapy followed by CEtuximab Plus definitive radiotherapy versus radiation plus cisplatin N EUDRACT:
 Gruppo Oncologico Nord Ovest Azienda Ospedaliera S. Croce e Carle di Cuneo INduction chemotherapy followed by CEtuximab Plus definitive radiotherapy versus radiation plus cisplatin Chemioterapia di induzione
Gruppo Oncologico Nord Ovest Azienda Ospedaliera S. Croce e Carle di Cuneo INduction chemotherapy followed by CEtuximab Plus definitive radiotherapy versus radiation plus cisplatin Chemioterapia di induzione
Sinossi del protocollo I4T-MC-JVBA
 I4T-MC-JVBA (IMCL CP12-1027) Protocollo clinico (17 Agosto 2010) Pagina 1 Razionale dello studio Sinossi del protocollo I4T-MC-JVBA Un approccio promettente alla cura del tumore è rappresentato dall'inibizione
I4T-MC-JVBA (IMCL CP12-1027) Protocollo clinico (17 Agosto 2010) Pagina 1 Razionale dello studio Sinossi del protocollo I4T-MC-JVBA Un approccio promettente alla cura del tumore è rappresentato dall'inibizione
STUDIO TRIBE 2 EUDRACT SINOSSI
 EUDRACT 2014-004436-19 Titolo Studio di fase III randomizzato di prima linea con FOLFOXIRI/bevacizumab seguito da reintroduzione di FOLFOXIRI/bevacizumab alla progressione versus prima linea con FOLFOX/bevacizumab
EUDRACT 2014-004436-19 Titolo Studio di fase III randomizzato di prima linea con FOLFOXIRI/bevacizumab seguito da reintroduzione di FOLFOXIRI/bevacizumab alla progressione versus prima linea con FOLFOX/bevacizumab
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO
 RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
Studio SeBA. Salute. e Benessere nell Anziano. nziano. Niccolò Marchionni. Presidente Società Italiana di Gerontologia e Geriatria
 Studio SeBA Salute e Benessere nell Anziano nziano Niccolò Marchionni Presidente Società Italiana di Gerontologia e Geriatria Con il supporto tecnico di: Obiettivi Descrivere, attraverso l analisi di database
Studio SeBA Salute e Benessere nell Anziano nziano Niccolò Marchionni Presidente Società Italiana di Gerontologia e Geriatria Con il supporto tecnico di: Obiettivi Descrivere, attraverso l analisi di database
CLASSI DI PRIORITÀ CLINICA PER L ESECUZIONE DEL TRATTAMENTO RADIOTERAPICO
 giunta regionale Allegato A al Decreto n. 0018 del 13 GIU 2016 pag. 1/6 CLASSI DI PRIORITÀ CLINICA PER L ESECUZIONE DEL TRATTAMENTO RADIOTERAPICO L'erogazione di trattamenti radioterapici in regime di
giunta regionale Allegato A al Decreto n. 0018 del 13 GIU 2016 pag. 1/6 CLASSI DI PRIORITÀ CLINICA PER L ESECUZIONE DEL TRATTAMENTO RADIOTERAPICO L'erogazione di trattamenti radioterapici in regime di
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI
 PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE. Reggio Emilia 4 giugno 2008
 O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
SCHEDA DI SEGNALAZIONE DI CASO PER ESPOSIZIONE IN OPERATORE SANITARIO
 Le schede per la segnalazione di caso di profilassi post.-esposizione (PPE) ad HIV sono due; una per le esposizioni occupazionali in operatore sanitario, l altra per le esposizioni occupazionali in non
Le schede per la segnalazione di caso di profilassi post.-esposizione (PPE) ad HIV sono due; una per le esposizioni occupazionali in operatore sanitario, l altra per le esposizioni occupazionali in non
Produttività, capacità di attrarre risorse e trasferibilità
 Produttività, capacità di attrarre Trials clinici Anno 2008 Studio Gisas: aripiprazolo, olanzapina e aloperidolo nel trattamento a lungo termine della schizofrenia Lo studio si propone di valutare l utilità
Produttività, capacità di attrarre Trials clinici Anno 2008 Studio Gisas: aripiprazolo, olanzapina e aloperidolo nel trattamento a lungo termine della schizofrenia Lo studio si propone di valutare l utilità
PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA
 PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA Unità destinatarie e competenze Urologia (prevenzione, diagnosi e stadiazione), trattamento, riabilitazione,
PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA Unità destinatarie e competenze Urologia (prevenzione, diagnosi e stadiazione), trattamento, riabilitazione,
Domande relative alla specializzazione in: Radioterapia
 Domande relative alla specializzazione in: Radioterapia Domanda #1 (codice domanda: n.611) : Rispetto a un tessuto ipossico, in un tessuto molto ossigenato gli effetti dannosi delle radiazioni sono: A:
Domande relative alla specializzazione in: Radioterapia Domanda #1 (codice domanda: n.611) : Rispetto a un tessuto ipossico, in un tessuto molto ossigenato gli effetti dannosi delle radiazioni sono: A:
Autori: Pierandrea De Iaco, Anna Myriam Perrone. Documento: Protocollo. Versione: Finale del 24 Dicembre 2012. Numero di pagine: 7
 Codice dello studio: SIRENA (Studio Ipertermia REtrospettivo NAzionale) Studio osservazionale multicentrico retrospettivo sulla Chemioterapia Ipertermica Intraperitoneale nel carcinoma avanzato dell ovaio
Codice dello studio: SIRENA (Studio Ipertermia REtrospettivo NAzionale) Studio osservazionale multicentrico retrospettivo sulla Chemioterapia Ipertermica Intraperitoneale nel carcinoma avanzato dell ovaio
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO TITOLO DELLO STUDIO: CODICE DEL PROTOCOLLO: SPONSOR: FASE DELLO STUDIO: CENTRI PARTECIPANTI ALLO STUDIO: PERIODO DI STUDIO PIANIFICATO (PRIMO ARRUOLAMENTO ULTIMO PAZIENTE USCITO
SINOSSI DEL PROTOCOLLO TITOLO DELLO STUDIO: CODICE DEL PROTOCOLLO: SPONSOR: FASE DELLO STUDIO: CENTRI PARTECIPANTI ALLO STUDIO: PERIODO DI STUDIO PIANIFICATO (PRIMO ARRUOLAMENTO ULTIMO PAZIENTE USCITO
Oncology Division, Breats Unit Ospedale Perrino, Brindisi, Italy Phone: Fax: Versione n.
 A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
Lezione 2 Come leggere l articolo scientifico
 Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine
 Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
PROTOCOLLO DELLO STUDIO
 PROTOCOLLO DELLO STUDIO TITOLO DELLO STUDIO TRATTAMENTO CON IMMUNOGLOBULINE NELLA SINDROME POST-POLIO DISEGNO DELLO STUDIO Studio clinico randomizzato, in doppio cieco, a due bracci (trattamento vs placebo)
PROTOCOLLO DELLO STUDIO TITOLO DELLO STUDIO TRATTAMENTO CON IMMUNOGLOBULINE NELLA SINDROME POST-POLIO DISEGNO DELLO STUDIO Studio clinico randomizzato, in doppio cieco, a due bracci (trattamento vs placebo)
BAY 43-9006/13266 - SINOSSI DEL PROTOCOLLO
 BAY 43-9006/13266 - SINOSSI DEL PROTOCOLLO Nome dello sponsor Nome del prodotto finito Nome del principio attivo Titolo dello studio Sperimentatore Principale Centri dello studio pianificati Periodo di
BAY 43-9006/13266 - SINOSSI DEL PROTOCOLLO Nome dello sponsor Nome del prodotto finito Nome del principio attivo Titolo dello studio Sperimentatore Principale Centri dello studio pianificati Periodo di
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti
 Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
Popolazione in studio: Analisi descrittiva delle tre regioni
 Popolazione in studio: Analisi descrittiva delle tre regioni Silvia Cascini, Claudio Voci, Lisa Bauleo Roma, 13 giugno 2014 Fonti dei dati Costruzione dataset Definizione di caso Caratterizzazione paziente,
Popolazione in studio: Analisi descrittiva delle tre regioni Silvia Cascini, Claudio Voci, Lisa Bauleo Roma, 13 giugno 2014 Fonti dei dati Costruzione dataset Definizione di caso Caratterizzazione paziente,
Schema dello studio clinico di Fase 2b
 Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO
 MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
LA TERAPIA DELLA MALATTIA METASTATICA
 IL TUMORE DELLA MAMMELLA: CONOSCERE PER DECIDERE LA TERAPIA DELLA MALATTIA METASTATICA Chiara Saggia SCDU Oncologia AOU Maggiore della Carità, Novara Torino, 8 marzo 2011 IL CARCINOMA MAMMARIO METASTATICO
IL TUMORE DELLA MAMMELLA: CONOSCERE PER DECIDERE LA TERAPIA DELLA MALATTIA METASTATICA Chiara Saggia SCDU Oncologia AOU Maggiore della Carità, Novara Torino, 8 marzo 2011 IL CARCINOMA MAMMARIO METASTATICO
epidemiologia del melanoma
 epidemiologia del melanoma Il Melanoma metastatico: tra efficacia delle terapie e governance Palace Hotel Como 17 dicembre 2013 UO Registro Tumori e Screening dr.ssa Gemma Gola Prevenzione Primaria Prima
epidemiologia del melanoma Il Melanoma metastatico: tra efficacia delle terapie e governance Palace Hotel Como 17 dicembre 2013 UO Registro Tumori e Screening dr.ssa Gemma Gola Prevenzione Primaria Prima
PROTOCOLLI GOIRC-SPONSORED FARM6PMFJM
 PROTOCOLLI -SPONSORED FARM6PMFJM Multicenter phase III randomized study of cisplatin and etoposide with or without bevacizumab as first-line treatment in extensive stage (ED) small cell lung cancer (SCLC).
PROTOCOLLI -SPONSORED FARM6PMFJM Multicenter phase III randomized study of cisplatin and etoposide with or without bevacizumab as first-line treatment in extensive stage (ED) small cell lung cancer (SCLC).
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione
 Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
LA GESTIONE DEL FALLIMENTO DOPO TERAPIA RADICALE
 LA GESTIONE DEL FALLIMENTO DOPO TERAPIA RADICALE Dr.ssa Nice Bedini S.C. Radioterapia 1 Milano, 28.11.2009 Indice Definizione di recidiva biochimica dopo chirurgia Definizione di recidiva biochimica dopo
LA GESTIONE DEL FALLIMENTO DOPO TERAPIA RADICALE Dr.ssa Nice Bedini S.C. Radioterapia 1 Milano, 28.11.2009 Indice Definizione di recidiva biochimica dopo chirurgia Definizione di recidiva biochimica dopo
La gestione degli eventi avversi e dei SAE
 Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE III PROSPETTICO, A DUE COORTI, NON RANDOMIZZATO, MULTICENTRICO, INTERNAZIONALE, IN APERTO, VOLTO A VALUTARE LA SICUREZZA DI TRASTUZUMAB
SINOSSI DEL PROTOCOLLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE III PROSPETTICO, A DUE COORTI, NON RANDOMIZZATO, MULTICENTRICO, INTERNAZIONALE, IN APERTO, VOLTO A VALUTARE LA SICUREZZA DI TRASTUZUMAB
VALUTAZIONE E DIGIUNO
 POLO UNICO OSPEDALIERO UNIVERSITARIO DI PERUGIA Sezione di Anestesia, Analgesia e Terapia Intensiva Scuola di Specializzazione in Anestesia e Rianimazione Struttura Complessa di Anestesia e Rianimazione
POLO UNICO OSPEDALIERO UNIVERSITARIO DI PERUGIA Sezione di Anestesia, Analgesia e Terapia Intensiva Scuola di Specializzazione in Anestesia e Rianimazione Struttura Complessa di Anestesia e Rianimazione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE ALIMTA 100 mg polvere per concentrato per soluzione per infusione ALIMTA 500 mg polvere per concentrato per soluzione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE ALIMTA 100 mg polvere per concentrato per soluzione per infusione ALIMTA 500 mg polvere per concentrato per soluzione
La strategia terapeutica adiuvante
 I tumori del corpo dell utero: strategie terapeutiche in evoluzione La strategia terapeutica adiuvante Renato Maggi - Maria Paola Odorizzi Anna Tusei Ospedale S. Anna Como Torino 26 Febbraio 2010 PAZIENTE
I tumori del corpo dell utero: strategie terapeutiche in evoluzione La strategia terapeutica adiuvante Renato Maggi - Maria Paola Odorizzi Anna Tusei Ospedale S. Anna Como Torino 26 Febbraio 2010 PAZIENTE
STUDI CLINICI IN CORSO nella MIELOFIBROSI
 Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA. Istruzioni per la compilazione delle schede pazienti
 LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA Istruzioni per la compilazione delle schede pazienti COME SI COLLABORA Lo studio ha l obiettivo di analizzare le terapie ormonali in pazienti con carcinoma
LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA Istruzioni per la compilazione delle schede pazienti COME SI COLLABORA Lo studio ha l obiettivo di analizzare le terapie ormonali in pazienti con carcinoma
Indicatori di qualità nei carcinomi genitali femminili"
 Indicatori di qualità nei carcinomi genitali femminili" Corso DAS Oncologia 19.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in Selva 24 6600 Locarno Indicatori di qualità Introduzione"
Indicatori di qualità nei carcinomi genitali femminili" Corso DAS Oncologia 19.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in Selva 24 6600 Locarno Indicatori di qualità Introduzione"
Allo stato attuale la casistica consta di 60 casi trattati con peritonectomia e chemioipetermia intraoperatoria.
 I dati sintetizzati nella tabella sopra riportata nel contesto delle esperienze internazionali sono relativi alla casistica di 47 casi relativa al periodo 2000-20007 analizzata nell articolo: Cytoreductive
I dati sintetizzati nella tabella sopra riportata nel contesto delle esperienze internazionali sono relativi alla casistica di 47 casi relativa al periodo 2000-20007 analizzata nell articolo: Cytoreductive
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR ERLOTINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
Minaccia di parto pretermine e/o rottura pretermine delle membrane: Protocollo di Trasporto
 Protocollo V11 - Procedure di Trasporto PATOLOGIE Minaccia di parto pretermine e/o rottura pretermine delle membrane: Protocollo di Trasporto Diagnosi di minaccia di parto pretermine (MPP): 1. attività
Protocollo V11 - Procedure di Trasporto PATOLOGIE Minaccia di parto pretermine e/o rottura pretermine delle membrane: Protocollo di Trasporto Diagnosi di minaccia di parto pretermine (MPP): 1. attività
AULA GIALLA STUDI CLINICI IN CORSO
 Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA GIALLA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA GIALLA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
Evidenze cliniche: punto d incontro fra ricercatore e clinico. 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1
 Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
Regorafenib nella recidiva di glioblastoma Studio REGOMA RIASSUNTO PROTOCOLLO
 ISTITUTO ONCOLOGICO VENETO IRCCS Regorafenib nella recidiva di glioblastoma Studio REGOMA Studio clinico di fase II, controllato, randomizzato, in aperto RIASSUNTO PROTOCOLLO Identificativo studio: IOV-GB-1-2014
ISTITUTO ONCOLOGICO VENETO IRCCS Regorafenib nella recidiva di glioblastoma Studio REGOMA Studio clinico di fase II, controllato, randomizzato, in aperto RIASSUNTO PROTOCOLLO Identificativo studio: IOV-GB-1-2014
Storia naturale del tumore della mammella. diagnosi. +/-trattamento/i. preclinica. nascita del tumore. diagnosi. exitus. clinica
 Storia naturale del tumore della mammella diagnosi preclinica +/-trattamento/i? nascita del tumore diagnosi clinica exitus Trattamento carcinoma della mammella chirurgia radioterapia terapia medica MASSIMO
Storia naturale del tumore della mammella diagnosi preclinica +/-trattamento/i? nascita del tumore diagnosi clinica exitus Trattamento carcinoma della mammella chirurgia radioterapia terapia medica MASSIMO
