CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
|
|
|
- Lorenza Marrone
- 6 anni fa
- Visualizzazioni
Transcript
1 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio ibridato sp3, che presenta quattro sostituenti diversi tra loro, costituisce un centro stereogenico ed è privo di elementi di simmetria, perciò viene definito chirale. O b. C2C2I 19 a. CC2 C2 CI O 24 a. (5 isomeri) 1. C2C2C2C2 2. C2C2C cis 3. C2CC2 trans trans cis 20 a. C2C2O C2O b. C2C2C2O C2OC2 21 C2C2C2C2O O O C2C2C C2C2C O O C2CC2 C2CC2 22 C2=C 4. CC 5. C2C b. (9 isomeri) 1. C2C2C2C2C2 2. C2C2C2C 3. C2C2CC2 4. C2CC C2 C 2 18 a. C2C2 C2C2C2 C2C2CCOO OOCCC2C2 17 anno centri stereogeni i composti a., c. e f. b. 16 a. chirale b. achirale c. achirale 23 C2 5. CC2C 6. C2C2C David Sadava, David M. illis,. Craig eller, May R. Berenbaum, Francesco C 19
2 5. CC2C 27 a. CC2C2 CC2C2 2C2 CC O O b. O C2CC2C2 C2CC2C2 C2CC2C2 c. 2C CCC2 CCC2 2C CCC2 2C d. C C CC 2C2C2 3 2 C2CC2C2C2 1g C2C 28 cc 2 =3C2CC =20,01 g/ml 100 ml 6. C2C2C 7. C2CC2 8. CC C2 9. CC2 α 1,33 [α] = = = 66,5 l c 2 0,01 29 Nelle forme meso che presenta, per esempio, l acido tartarico esiste un piano di simmetria che permette di ruotare la molecola di 180 per ottenere la sua immagine speculare; in tal modo non viene rispettata la condizione di chiralità e la molecola è otticamente inattiva. 25 (6 isomeri) 1. C2C2C2O 2. C2C O 30 Si chiamano enantiomeri quegli stereoisomeri che sono l uno l immagine speculare dell altro, ma non sono sovrapponibili. I diasteroisomeri, invece, sono stereoisomeri che non sono immagini speculari l uno dell altro. 3. C 6. OC 26 OC 2CON O O C COO acido (+) tartarico I COO COO COO COO C O O C O C C O O C COO C O C 3 COO 32 Nella convenzione relativa d,l le molecole vengono osservate nella loro struttura proiettata sul piano; invece, nella convenzione assoluta R,S, le molecole vengono osservate nella loro reale struttura tridimensionale. 33 C 3 N S COO O C acido ( ) tartarico II III L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato in base al numero atomico dell atomo legato direttamente al centro stereogenico: all atomo con numero atomico maggiore viene data priorità maggiore. 5. OC2C2 O 4. C2OC2 COO acido meso-tartarico David Sadava, David M. illis,. Craig eller, May R. Berenbaum, Francesco IV
3 eraldeide b. F > O > O > C2O 44 a. La convenzione Fischer-Rosanoff prende come molecola di riferimento la gliceraldeide e la rappresenta in base alle proiezioni di Fischer. Lo stereodescrittore d viene assegnato alla configurazione in cui il gruppo O del centro stereogenico è a destra, mentre l viene assegnato a quella con il gruppo O a sinistra. c. O > O > N > C2N2 37 a priorità più alta il gruppo vinile. 38 S; C O C2O a. glicerolo CO 2N C O C2O c. L-serina CO C2O 40 O C C2O b. L-gliceraldeide CO C O O C C O C O C2O d. D-glucosio 41 Nessuna delle tre proiezioni di Fischer ha la stessa configurazione di A. Sono tutte proiezioni di Fischer dell enantiomero di A. 42 a. Se un fascio di luce attraversa un materiale cosiddetto polarizzante, la luce trasmessa vibra in un solo piano, quello parallelo alla direzione di polarizzazione. Si ottiene così un raggio di luce polarizzata che oscilla in un unico piano di vibrazione. b. Il potere rotatorio è l entità della rotazione del piano della luce polarizzata. c. L attività ottica è la proprietà di una molecola di ruotare di un certo angolo il piano dove vibra un fascio di luce linearmente polarizzato. 43 a. Le proiezioni di Fischer stabiliscono delle convenzioni che permettono di rappresentare la struttura tridimensionale di una molecola nelle due dimensioni in modo inequivocabile. David Sadava, David M. illis,. Craig eller, May R. Berenbaum, Francesco 39 No; sì; no; no; sì. b. La convenzione assoluta R,S di Cahn, Ingold e Prelog considera la molecola nella sua reale struttura tridimensionale e si basa sull ordine di priorità CIP. Rispetto alla gliceraldeide, in base CO alla priorità CIP, sico ha per primo il gruppo O, per secondo il gruppo CO, per terzo il grup C 2N C O O Si orienta la molecola. po C2O,infine in modo che il sostituente a priorità CIP minore C2O O C rispetto all osservatore; sia dalla parte opposta sono rivolti verso l osservac. L-serinagli altri tre sostituenti C O tore. Considerando questi tre sostituenti, se per procedere dal sostituente C O a priorità maggiore fino a quello a priorità minore si gira in senso orario, si assegna allo stereocentro la configurazione R C2O (rectus); altrimenti, se si ruota in senso antiorario, -glucosio gli si assegnad.ladconfigurazione S (sinister). c. Quando ci si riferisce alla simmetria di una molecola, si devono considerare gli elementi di simmetria, fra cui si distinguono quelli di primo e di secondo ordine. L elemento di simmetria di primo ordine è la presenza di un asse di rotazione. Gli elementi di simmetria di secondo ordine sono il piano di simmetria, il centro di simmetria e l asse di roto-riflessione. Se non è rispettato neanche l elemento di simmetria di primo ordine, la molecola è asimmetrica: una molecola asimmetrica è chirale. C2O c. I diastereoisomeri sono stereoisomeri che non sono immagini speculari l uno dell altro. 36 a. N2 > C()2 > > C b. Gli enantiomeri sono due stereoisomeri che sono l uno l immagine speculare dell altro, ma non sono sovrapponibili. 35 > C2 > > CO 34 l-gliceraldeide o S-gliceraldeide; acido l-lattico o acido S-lattico; d-serina o R-serina. d. Nell isomeria strutturale gli isomeri sono composti dagli stessi atomi, ma differiscono per il rapporto che essi hanno tra loro all interno della molecola e quindi per la struttura. Si distinguono l isomeria strutturale di catena, l isomeria strutturale di posizione e l isomeria strutturale funzionale. La stereoisomeria, invece, si riferisce a molecole che, pur mantenendo lo stesso rapporto tra gli atomi all interno della molecola, differiscono tra loro per la diversa disposizione degli atomi o dei gruppi di atomi nello spazio. Si distinguono la stereoisomeria conformazionale e la stereoisomeria configurazionale, la quale a sua volta è suddivisa in isomeria cis/trans, detta anche isomeria geometrica, ed enantiomeria, detta anche stereoisomeria ottica. 21
4 45 a. Esistono molti casi in cui la convenzione relativa d,l non può essere applicata: per esempio, quello in cui la molecola non ha un estremità più ossidata dell altra nella catena carboniosa e non può essere orientata in modo inequivocabile, per cui non ha senso definire gruppi disposti a destra o a sinistra. In tali casi si ricorre alla convenzione assoluta R,S che può essere applicata a ogni stereoisomero ma, nel caso di composti organici come amminoacidi e monosaccaridi, si preferisce la convenzione d,l per la sua maggiore semplicità. b. La convenzione relativa d,l viene preferibilmente utilizzata in campo biochimico in composti organici come gli amminoacidi e i monosaccaridi. Negli amminoacidi, scritta la molecola in base alla convenzione Fischer-Rosanoff, si guarda la posizione del gruppo N2 rispetto alla catena verticale di atomi di carbonio; si prende come riferimento la serina, data la sua somiglianza con l aldeide glicerica. Per quanto riguarda i monosaccaridi, che invece presentano più di uno stereocentro, il modo più rigoroso di assegnare uno stereodescrittore sarebbe quello di indicare la configurazione di ogni atomo di carbonio in base alla convenzione assoluta R,S. c. Un centro chirale è un atomo che è legato a quattro sostituenti diversi tra loro; viene definito centro stereogenico o stereocentro. L attività ottica è una proprietà fisica che permette di distinguere due enantiomeri tra loro e consiste nella proprietà di una molecola di ruotare di un certo angolo il piano dove vibra un fascio di luce linearmente polarizzato. Una forma meso è una molecola che presenta un piano di simmetria. TEST YOURSELF 46 D 47 Enantiomers are stereoisomers which are mirror images of each other but they are not superimposable upon one another. Diastereomers are stereoisomers which are not superimposable and also are not mirror images of each other. 48 Epimers are stereoisomers which differ in configuration of only one stereogenic centre. 49 3C propene cyclopropane VERSO L UNIVERSITÀ 50 A 51 C VERSO L ESAME DEFINISCI 53 a. Uno stereocentro è rappresentato da un atomo di carbonio con ibridazione sp3, in cui i quattro sostituenti legati a esso sono tutti diversi tra loro. b. Gli enantiomeri sono due stereoisomeri che sono l uno l immagine speculare dell altro, ma non sono sovrapponibili. c. Se un fascio di luce attraversa un materiale cosiddetto polarizzante, la luce trasmessa vibra in un solo piano, quello parallelo alla direzione di polarizzazione. Si ottiene così un raggio di luce polarizzata che oscilla in un unico piano di vibrazione. 22 e. I diasteroisomeri sono stereoisomeri che non sono immagini speculari l uno dell altro. f. Una molecola chirale è una molecola asimmetrica in cui non viene rispettato neanche l elemento di simmetria di primo ordine. OSSERVA E CLASSIFICA 54 Coltello e forchetta non sono l uno l immagine speculare dell altro; le altre coppie sono immagini speculari ma la saliera e la pepiera e le lenti a contatto destra e sinistra sono sovrapponibili, per cui sono oggetti chirali solo gli occhi, le ali di farfalla e il paio di scarpe. d. L entità della rotazione del piano della luce polarizzata è detta potere rotatorio e si definisce potere rotatorio specifico la rotazione osservata con un campione di concentrazione di 1 g/ml, con un cammino ottico di 1 dm, alla temperatura di 20 C, utilizzando una luce con lunghezza d onda di circa 589 nm. ANALIZZA E IPOTIZZA David Sadava, David M. illis,. Craig eller, May R. Berenbaum, Francesco 55 Miscele: a. 50% A + 50% B: nessuna attività ottica (racemo); b. 25% A + 75% B: levogira; c. 25% B + 75% A: destrogira.
5 SPIEGA 56 a. Le molecole A e B sembrano isomeri perché i due atomi di cloro (o i due atomi di idrogeno) in A sono orientati in direzioni opposte e formano un angolo di 180, mentre in B formano un angolo di 90. b. In realtà il cloruro di metilene è un unica molecola a geometria tetraedrica in cui l atomo di carbonio è centrale e i due atomi di cloro e i due atomi di idrogeno sono disposti ai vertici del tetraedro, come nella molecola di metano. C C IPOTIZZA E RAPPRESENTA O C25 C 58 a. Considerando l ordine di priorità CIP si ha: CO2 > C65 > >, per cui si tratta dell enantiomero S. b. Semplicemente osservando una struttura disegnata su un foglio, non è possibile prevedere se ruoterà il piano della luce polarizzata verso destra o sinistra; la proprietà può essere determinata solo per via sperimentale. SPIEGA c. Come si può notare, le due molecole non presentano enantiomeria, poiché sono immagini speculari sovrapponibili. 57 ANALIZZA E DEDUCI David Sadava, David M. illis,. Craig eller, May R. Berenbaum, Francesco 59 a. La notazione l deriva dalla convenzione d,l, relativa, in cui lo stereodescrittore l viene assegnato alla formula di proiezione dell acido lattico che presenta l ossidrile a sinistra. La notazione S deriva dalla convenzione assoluta R,S; in cui si assegna allo stereocentro la configurazione S perché, in base all ordine di priorità CIP, si ruota in senso antiorario. b. È preferibile utilizzare la convenzione assoluta, poiché nella convenzione relativa d,l le molecole vengono osservate nella loro struttura proiettata su un piano, invece nella convenzione assoluta R,S le molecole vengono osservate nella loro reale struttura tridimensionale. Il 2-butanolo è otticamente attivo perché presenta uno stereocentro in cui l atomo di carbonio è legato a quattro sostituenti diversi e quindi è chirale. 23
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
Stereochimica. Molecole nello spazio
 Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
7.9 Reazioni che introducono un centro Stereogenico
 7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
STEREOISOMERIA carbonio ibridizzato sp3 è legato a quattro atomi o gruppi tutti diversi fra loro
 STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
7.4 Proprietà delle Molecole Chirali: Attvità Ottica
 7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
Polarimetria. Polarimetria
 Polarimetria Polarimetria La radiazione elettromagnetica viene considerata come una forma di energia radiante dotata di una doppia natura, ondulatoria e corpuscolare. In ogni momento il vettore campo elettrico
Polarimetria Polarimetria La radiazione elettromagnetica viene considerata come una forma di energia radiante dotata di una doppia natura, ondulatoria e corpuscolare. In ogni momento il vettore campo elettrico
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI
 L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
 La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Chimica organica. Biomolecole. Tessuti biologici. Polimeri proprietà funzioni
 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni 1 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni C O N 1 Chimica organica Biomolecole Tessuti biologici
Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni 1 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni C O N 1 Chimica organica Biomolecole Tessuti biologici
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
5.5 Il piano di simmetria divide la molecola in due metà identiche.
 opyright 009 The McGraw-ill ompanies srl Soluzioni ai problemi proposti nel libro apitolo 5 5.1 5. Gli isomeri costituzionali hanno atomi legati d atomi diversi. Gli stereoisomeri differiscono nella disposizione
opyright 009 The McGraw-ill ompanies srl Soluzioni ai problemi proposti nel libro apitolo 5 5.1 5. Gli isomeri costituzionali hanno atomi legati d atomi diversi. Gli stereoisomeri differiscono nella disposizione
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
La composizione di isometrie
 La composizione di isometrie Quello che è più interessante in una trasformazione geometrica è studiare quali effetti ha sulle figure e soprattutto valutare quali proprietà delle figure di partenza si conservano
La composizione di isometrie Quello che è più interessante in una trasformazione geometrica è studiare quali effetti ha sulle figure e soprattutto valutare quali proprietà delle figure di partenza si conservano
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Introduzione ai fenomeni di polarizzazione. Lezioni d'autore di Claudio Cigognetti
 Introduzione ai fenomeni di polarizzazione Lezioni d'autore di Claudio Cigognetti VIDEO POLARIZZAZIONE IN UN IPAD, RICAPITOLANDO Impiegando occhiali aventi lenti polaroid e un display a cristalli liquidi
Introduzione ai fenomeni di polarizzazione Lezioni d'autore di Claudio Cigognetti VIDEO POLARIZZAZIONE IN UN IPAD, RICAPITOLANDO Impiegando occhiali aventi lenti polaroid e un display a cristalli liquidi
CHIMICA ORGANICA I. Corso di laurea in CHIMICA
 IMIA RGANIA I orso di laurea in IMIA Esercitazione n. 6 - Esercitazione sulla stereoisomeria ottica. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Molecole simmetriche e dissimmetriche.
IMIA RGANIA I orso di laurea in IMIA Esercitazione n. 6 - Esercitazione sulla stereoisomeria ottica. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Molecole simmetriche e dissimmetriche.
STEREOCHIMICA C OH CH 2 CH 3. 180 in questo caso nessuna rotazione è in grado di far sovrapporre perfettamente le due strutture
 TEEIMIA TEEIMEI Due stereoisomeri sono sostanze diverse che hanno in comune sia la formula bruta che la formula di costituzione. osa li rende diversi allora? Una differente orientazione tridimensionale
TEEIMIA TEEIMEI Due stereoisomeri sono sostanze diverse che hanno in comune sia la formula bruta che la formula di costituzione. osa li rende diversi allora? Una differente orientazione tridimensionale
Idrocarburi insaturi. Alcheni
 Idrocarburi insaturi Alcheni Idrocarburi insaturi Un idrocarburo si dice insaturo quando possiede un numero di atomi di idrogeno minore al numero massimo possibile per un dato numero di atomi di carbonio.
Idrocarburi insaturi Alcheni Idrocarburi insaturi Un idrocarburo si dice insaturo quando possiede un numero di atomi di idrogeno minore al numero massimo possibile per un dato numero di atomi di carbonio.
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
CARBOIDRATI. Perché? Chi sfrutta questo lavoro?
 CARBOIDRATI I carboidrati, detti anche glucidi (dal greco "glucos" = dolce) sono sostanze formate da carbonio ed acqua. Hanno forma molecolare Cn(H2O)n e sono contenuti principalmente negli alimenti di
CARBOIDRATI I carboidrati, detti anche glucidi (dal greco "glucos" = dolce) sono sostanze formate da carbonio ed acqua. Hanno forma molecolare Cn(H2O)n e sono contenuti principalmente negli alimenti di
Funzioni Pari e Dispari
 Una funzione f : R R si dice Funzioni Pari e Dispari PARI: se f( ) = f() R In questo caso il grafico della funzione è simmetrico rispetto all asse DISPARI: se f( ) = f() R In questo caso il grafico della
Una funzione f : R R si dice Funzioni Pari e Dispari PARI: se f( ) = f() R In questo caso il grafico della funzione è simmetrico rispetto all asse DISPARI: se f( ) = f() R In questo caso il grafico della
ESPERIENZE CON GLI SPECCHI PIANI
 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine riflessa del cilindro
1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine riflessa del cilindro
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
Misure di fenomeni di aberrazione di una lente
 Padova, gennaio 00 Misure di fenomeni di aberrazione di una lente Indicare il numero identificativo e le caratteristiche geometriche della lente utilizzata: Lente num. =... Spessore =... Spigolo =... Indice
Padova, gennaio 00 Misure di fenomeni di aberrazione di una lente Indicare il numero identificativo e le caratteristiche geometriche della lente utilizzata: Lente num. =... Spessore =... Spigolo =... Indice
quadrilatero generico parallelogramma rombo rettangolo quadrato
 Pavimentare 1. Quali forme di quadrilateri puoi costruire? Schizza tutte le forme possibili e scrivi il loro nome. 2. Cosa rappresentano i piccoli punti rossi sui lati del quadrilatero? 3. a) Costruisci
Pavimentare 1. Quali forme di quadrilateri puoi costruire? Schizza tutte le forme possibili e scrivi il loro nome. 2. Cosa rappresentano i piccoli punti rossi sui lati del quadrilatero? 3. a) Costruisci
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
QUOTATURA. Affinché un qualsiasi oggetto disegnato possa essere esattamente realizzato deve essere perfettamente individuato in forma e dimensioni
 QUOTATURA Affinché un qualsiasi oggetto disegnato possa essere esattamente realizzato deve essere perfettamente individuato in forma e dimensioni Il disegno di un oggetto è quindi completo se descrive
QUOTATURA Affinché un qualsiasi oggetto disegnato possa essere esattamente realizzato deve essere perfettamente individuato in forma e dimensioni Il disegno di un oggetto è quindi completo se descrive
1. CALCOLO DELLA QUANTITÀ D'ARIA NECESSARIA ALLA COMBUSTIONE DI UN DATO COMBUSTIBILE
 1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
valore di a: verso l alto (ordinate crescenti) se a>0, verso il basso (ordinate decrescenti) se a<0;
 La parabola è una particolare conica definita come è una curva aperta, nel senso che non può essere contenuta in alcuna superficie finita del piano; è simmetrica rispetto ad una retta, detta ASSE della
La parabola è una particolare conica definita come è una curva aperta, nel senso che non può essere contenuta in alcuna superficie finita del piano; è simmetrica rispetto ad una retta, detta ASSE della
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: H 2 O 2(aq) + MnO 4
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA
 ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
DISEGNO PROSPETTICO CAPITOLO 1 METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE PROIEZIONI ORTOGRAFICHE PROIEZIONI ASSONOMETRICHE
 CAPITOLO DISEGNO PROSPETTICO METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE La norma UNI EN ISO 0209-2 raccoglie i principali metodi di rappresentazione raccomandati per il disegno
CAPITOLO DISEGNO PROSPETTICO METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE La norma UNI EN ISO 0209-2 raccoglie i principali metodi di rappresentazione raccomandati per il disegno
La Polarizzazione della luce
 La Polarizzazione della luce Applet Java sulle OEM Le Onde Elettromagnetiche Sono onde trasversali costituite dalle vibrazioni del vuoto quantistico. Hanno velocità c=3.0 10 8 m/s. In ogni istante E è
La Polarizzazione della luce Applet Java sulle OEM Le Onde Elettromagnetiche Sono onde trasversali costituite dalle vibrazioni del vuoto quantistico. Hanno velocità c=3.0 10 8 m/s. In ogni istante E è
REALTÀ E MODELLI SCHEDA DI LAVORO
 LE TRSFRINI GEETRICHE RELTÀ E DELLI SCHED DI LVR Il televisore La forma rettangolare di uno schermo televisivo è differente a seconda del rapporto tra la larghezza e l altezza. I televisori di vecchio
LE TRSFRINI GEETRICHE RELTÀ E DELLI SCHED DI LVR Il televisore La forma rettangolare di uno schermo televisivo è differente a seconda del rapporto tra la larghezza e l altezza. I televisori di vecchio
Logica figurale. 1 Quanti quadrati contengono la stella? A. 1 B. 2 C. 5 D. 6 E. 9. 2 Quanti triangoli sono rappresentati nella figura?
 Logica figurale 1 Quanti quadrati contengono la stella? A. 1 B. 2 C. 5 D. 6 E. 9 2 Quanti triangoli sono rappresentati nella figura? A. 6 B. 8 C. 9 D. 10 E. 12 3 Quanti sono i quadrati presenti nella seguente
Logica figurale 1 Quanti quadrati contengono la stella? A. 1 B. 2 C. 5 D. 6 E. 9 2 Quanti triangoli sono rappresentati nella figura? A. 6 B. 8 C. 9 D. 10 E. 12 3 Quanti sono i quadrati presenti nella seguente
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Tensioni e corrente variabili
 Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
UNIVERSITÀ DEGLI STUDI DI PADOVA Facoltà di Ingegneria A.A. 2009/10
 UNIVERSITÀ DEGLI STUDI DI PDOV Facoltà di Ingegneria Corso di Disegno Tecnico Industriale per i Corsi di Laurea triennale in Ingegneria Meccanica e in Ingegneria dell Energia Costruzioni geometriche in
UNIVERSITÀ DEGLI STUDI DI PDOV Facoltà di Ingegneria Corso di Disegno Tecnico Industriale per i Corsi di Laurea triennale in Ingegneria Meccanica e in Ingegneria dell Energia Costruzioni geometriche in
ESPONENZIALI E LOGARITMI. chiameremo logaritmica (e si legge il logaritmo in base a di c è uguale a b ).
 ESPONENZIALI E LOGARITMI Data una espressione del tipo a b = c, che chiameremo notazione esponenziale (e dove a>0), stabiliamo di scriverla anche in un modo diverso: log a c = b che chiameremo logaritmica
ESPONENZIALI E LOGARITMI Data una espressione del tipo a b = c, che chiameremo notazione esponenziale (e dove a>0), stabiliamo di scriverla anche in un modo diverso: log a c = b che chiameremo logaritmica
Nomenclatura IUPAC e struttura di alcheni e alchini
 Imparare la chimica con l aiuto del computer Nomenclatura IUPAC e struttura di alcheni e alchini Aggiornata alla nuova nomenclatura IUPAC 2009. Con questa esercitazione imparerete a disegnare semplici
Imparare la chimica con l aiuto del computer Nomenclatura IUPAC e struttura di alcheni e alchini Aggiornata alla nuova nomenclatura IUPAC 2009. Con questa esercitazione imparerete a disegnare semplici
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Quadro riassuntivo di geometria analitica
 Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
Rappresentazione grafica delle ombre delle figure disegnate
 Rappresentazione grafica delle ombre delle figure disegnate BERTOLDO T. E., Tecnica grafica. I - II tomo. Istituto Italiano Edizioni Atlas (Biblioteca Architettura ) Teoria delle ombre applicata alle proiezioni
Rappresentazione grafica delle ombre delle figure disegnate BERTOLDO T. E., Tecnica grafica. I - II tomo. Istituto Italiano Edizioni Atlas (Biblioteca Architettura ) Teoria delle ombre applicata alle proiezioni
3 Geometria delle masse e momento di 2 ordine 3.3 Ellisse centrale d inerzia e nocciolo centrale d inerzia
 3 Geometria delle masse e momento di ordine ESERCIZI SVOLTI Considerata la sezione rappresentata in figura, calcolare i raggi d inerzia massimo e minimo, tracciare l ellisse d inerzia e il nocciolo centrale
3 Geometria delle masse e momento di ordine ESERCIZI SVOLTI Considerata la sezione rappresentata in figura, calcolare i raggi d inerzia massimo e minimo, tracciare l ellisse d inerzia e il nocciolo centrale
APPUNTI DI MATEMATICA ALGEBRA \ CALCOLO LETTERALE \ MONOMI (1)
 LGEBR \ CLCOLO LETTERLE \ MONOMI (1) Un monomio è un prodotto di numeri e lettere; gli (eventuali) esponenti delle lettere sono numeri naturali (0 incluso). Ogni numero (reale) può essere considerato come
LGEBR \ CLCOLO LETTERLE \ MONOMI (1) Un monomio è un prodotto di numeri e lettere; gli (eventuali) esponenti delle lettere sono numeri naturali (0 incluso). Ogni numero (reale) può essere considerato come
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Punti nel piano cartesiano
 Punti nel piano cartesiano In un piano consideriamo due rette perpendicolari che chiamiamo x e. Solitamente, disegniamo la retta x (ascisse) orizzontalmente e orientata da sinistra a destra, la retta e
Punti nel piano cartesiano In un piano consideriamo due rette perpendicolari che chiamiamo x e. Solitamente, disegniamo la retta x (ascisse) orizzontalmente e orientata da sinistra a destra, la retta e
Funzioni goniometriche
 Funzioni goniometriche In questa dispensa vengono introdotte le definizioni delle funzioni goniometriche. Preliminarmente si introducono le convenzioni sull orientazione degli angoli e sulla loro rappresentazione
Funzioni goniometriche In questa dispensa vengono introdotte le definizioni delle funzioni goniometriche. Preliminarmente si introducono le convenzioni sull orientazione degli angoli e sulla loro rappresentazione
Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA. Parte 3. Lo spazio. Prof. Gianfranco Ciaschetti
 Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA Parte 3 Lo spazio Prof. Gianfranco Ciaschetti Solitamente, per spazio intendiamo un volume in tre dimensioni di estensione illimitata. In grafica,
Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA Parte 3 Lo spazio Prof. Gianfranco Ciaschetti Solitamente, per spazio intendiamo un volume in tre dimensioni di estensione illimitata. In grafica,
Retta di calibrazione del polarimetro
 INDICE Generalità Caratteristiche tecniche Componenti dello strumento Metodo operativo Manutenzione Retta di calibrazione del polarimetro Realizzazione Home Caratteristiche tecniche del nostro polarimetro
INDICE Generalità Caratteristiche tecniche Componenti dello strumento Metodo operativo Manutenzione Retta di calibrazione del polarimetro Realizzazione Home Caratteristiche tecniche del nostro polarimetro
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
ANALISI CHIMICO FARMACEUTICA I
 Prof. Gianluca Sbardella : 089 969770 : gsbardella@unisa.it L INCERTEZZA E LE CIFRE SIGNIFICATIVE Tutte le misure sono affette da un certo grado di incertezza la cui entità può dipendere sia dall operatore
Prof. Gianluca Sbardella : 089 969770 : gsbardella@unisa.it L INCERTEZZA E LE CIFRE SIGNIFICATIVE Tutte le misure sono affette da un certo grado di incertezza la cui entità può dipendere sia dall operatore
Le coordinate di mappatura
 Informatica Grafica per le arti Le coordinate di mappatura Per assegnare ad un oggetto tridimensionale una texture 2D, occorre specificare un insieme di coordinate di mappatura. Le coordinate di mappatura
Informatica Grafica per le arti Le coordinate di mappatura Per assegnare ad un oggetto tridimensionale una texture 2D, occorre specificare un insieme di coordinate di mappatura. Le coordinate di mappatura
Serie completa di Modelli Molecolari per la Chimica Organica
 EdiSES Istruzioni per l utilizzo dei modelli molecolari Serie completa di Modelli Molecolari per la Chimica Organica allegati ai seguenti volumi: Chimica Organica - Paula Y. Bruice Elementi di Chimica
EdiSES Istruzioni per l utilizzo dei modelli molecolari Serie completa di Modelli Molecolari per la Chimica Organica allegati ai seguenti volumi: Chimica Organica - Paula Y. Bruice Elementi di Chimica
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Massa assoluta e relativa e mole
 Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
ITIS G.C.FACCIO VERCELLI DIPARTIMENTO DI CHIMICA. ITIS G.C.FACCIO VERCELLI DIPARTIMENTO DI CHIMICA ----------- Prof. Paolo Rosso
 ITIS G.C.FACCIO VERCELLI DIPARTIMENTO DI CHIMICA ----------- Prof. Paolo Rosso GLI ZUCCHERI Introduzione Gli zuccheri sono composti naturali costituiti dai seguenti atomi carbonio, idrogeno ed ossigeno.
ITIS G.C.FACCIO VERCELLI DIPARTIMENTO DI CHIMICA ----------- Prof. Paolo Rosso GLI ZUCCHERI Introduzione Gli zuccheri sono composti naturali costituiti dai seguenti atomi carbonio, idrogeno ed ossigeno.
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
Lezione 4. Sommario. L artimetica binaria: I numeri relativi e frazionari. I numeri relativi I numeri frazionari
 Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Sistemi di equazioni di secondo grado
 1 Sistemi di equazioni di secondo grado Risoluzione algebrica Riprendiamo alcune nozioni che abbiamo già trattato in seconda, parlando dei sistemi di equazioni di primo grado: Una soluzione di un'equazione
1 Sistemi di equazioni di secondo grado Risoluzione algebrica Riprendiamo alcune nozioni che abbiamo già trattato in seconda, parlando dei sistemi di equazioni di primo grado: Una soluzione di un'equazione
I vertici e i lati di ogni poligono vengono detti rispettivamente vertici e spigoli del poliedro.
 1 I poliedri diagonale DEFINIZIONE. Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due di essi. I poligoni che delimitano il poliedro
1 I poliedri diagonale DEFINIZIONE. Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due di essi. I poligoni che delimitano il poliedro
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica. Lezione del 7 Marzo 2016
 C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
Funzioni di secondo grado
 Definizione della funzione di secondo grado 1 Funzioni di secondo grado 1 Definizione della funzione di secondo grado f: R R, = a +b +c dove a, b, c ǫ R e a definisce una funzione di secondo grado. A seconda
Definizione della funzione di secondo grado 1 Funzioni di secondo grado 1 Definizione della funzione di secondo grado f: R R, = a +b +c dove a, b, c ǫ R e a definisce una funzione di secondo grado. A seconda
Le Tolleranze Geometriche
 Le Tolleranze Geometriche Ing. Alessandro Carandina A.A. 2014/2015 Disegno Tecnico Industriale per Ingegneria Meccanica 2 Tolleranze geometriche Le tolleranze geometriche consentono di controllare lo scostamento
Le Tolleranze Geometriche Ing. Alessandro Carandina A.A. 2014/2015 Disegno Tecnico Industriale per Ingegneria Meccanica 2 Tolleranze geometriche Le tolleranze geometriche consentono di controllare lo scostamento
Università di Cassino. Esercitazioni di Statistica 1 del 29 Gennaio 2010. Dott. Mirko Bevilacqua
 Università di Cassino Esercitazioni di Statistica del 29 Gennaio 200 Dott. Mirko Bevilacqua DATASET STUDENTI N SESSO ALTEZZA PESO CORSO NUMERO COLORE COLORE (cm) (kg) LAUREA SCARPA OCCHI CAPELLI M 79 65
Università di Cassino Esercitazioni di Statistica del 29 Gennaio 200 Dott. Mirko Bevilacqua DATASET STUDENTI N SESSO ALTEZZA PESO CORSO NUMERO COLORE COLORE (cm) (kg) LAUREA SCARPA OCCHI CAPELLI M 79 65
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI
 I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
IIS Moro Dipartimento di matematica e fisica
 IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
Appunti ed esercizi sulle coniche
 1 LA CIRCONFERENZA 1 Appunti ed esercizi sulle coniche Versione del 1 Marzo 011 1 La circonferenza Nel piano R, fissati un punto O = (a, b) e un numero r > 0, la circonferenza (o cerchio) C di centro O
1 LA CIRCONFERENZA 1 Appunti ed esercizi sulle coniche Versione del 1 Marzo 011 1 La circonferenza Nel piano R, fissati un punto O = (a, b) e un numero r > 0, la circonferenza (o cerchio) C di centro O
CORSO DI LAUREA IN INGEGNERIA CIVILE A.A. 2008-2009 Prova scritta del corso di Chimica A-K Compito prova
 CORSO DI LAUREA IN INGEGNERIA CIVILE A.A. 2008-2009 Prova scritta del corso di Chimica A-K Compito prova Cognome e nome.... n di matricola Nei quesiti a risposta multipla, verranno ANNULLATI i quesiti
CORSO DI LAUREA IN INGEGNERIA CIVILE A.A. 2008-2009 Prova scritta del corso di Chimica A-K Compito prova Cognome e nome.... n di matricola Nei quesiti a risposta multipla, verranno ANNULLATI i quesiti
DISEGNO E RAPPRESENTAZIONE
 29. Osservando la sezione longitudinale dell Auditorium di Ibirapuera costruito da Oscar Niemeyer a San Paolo nel 2005, qual è la corretta disposizione dei piani verticali per ottenere le sezioni trasversali
29. Osservando la sezione longitudinale dell Auditorium di Ibirapuera costruito da Oscar Niemeyer a San Paolo nel 2005, qual è la corretta disposizione dei piani verticali per ottenere le sezioni trasversali
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
MEMBRANE. struttura: fosfolipidi e proteine
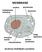 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
+ ε (deschermo) ε (schermo) α β α. B o
 Il fenomeno dell accoppiamento di spin Nuclei non equivalenti possono interagire attraverso i loro momenti di spin Ai fini della indagine strutturale di molecole incognite è necessario sario non solo considerare
Il fenomeno dell accoppiamento di spin Nuclei non equivalenti possono interagire attraverso i loro momenti di spin Ai fini della indagine strutturale di molecole incognite è necessario sario non solo considerare
Definizione: Dato un sottoinsieme non vuoti di. Si chiama funzione identica o identità di in sé la funzione tale che.
 Esercitazioni di Analisi Matematica Prof.ssa Chiara Broggi Materiale disponibile su www.istitutodefilippi.it/claro Lezione 2: Funzioni reali e loro proprietà Definizione: Siano e due sottoinsiemi non vuoti
Esercitazioni di Analisi Matematica Prof.ssa Chiara Broggi Materiale disponibile su www.istitutodefilippi.it/claro Lezione 2: Funzioni reali e loro proprietà Definizione: Siano e due sottoinsiemi non vuoti
Geogebra. a. La lancetta è ruotata? SI NO. Se sì attorno a quale punto?
 Geogebra L ANGOLO 1. Nel programma Geogebra, fai doppio clic sull icona e scegli Circonferenza dati centro e raggio. 2. Posizionati al centro della finestra di geometria e fai clic. Nella finestra che
Geogebra L ANGOLO 1. Nel programma Geogebra, fai doppio clic sull icona e scegli Circonferenza dati centro e raggio. 2. Posizionati al centro della finestra di geometria e fai clic. Nella finestra che
CHIMICA QUANTITATIVA. Massa atomica. Unità di massa atomica. Massa molare
 CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
ARROTONDANDO FIGURE CON TRIANGOLI EQUILATERI
 ARROTONDANDO Cosa succede ad accostare figure identiche una all altra? Le figure ottenute che proprietà presentano? Posso trovare un qualche tipo di legge generale? Per rispondere a questa ed altre domande
ARROTONDANDO Cosa succede ad accostare figure identiche una all altra? Le figure ottenute che proprietà presentano? Posso trovare un qualche tipo di legge generale? Per rispondere a questa ed altre domande
SUPERFICI CONICHE. Rappresentazione di coni e cilindri
 SUPERFICI CONICHE Rappresentazione di coni e cilindri Si definisce CONO la superficie che si ottiene proiettando tutti i punti di una curva, detta DIRETTRICE, da un punto proprio, non appartenente al piano
SUPERFICI CONICHE Rappresentazione di coni e cilindri Si definisce CONO la superficie che si ottiene proiettando tutti i punti di una curva, detta DIRETTRICE, da un punto proprio, non appartenente al piano
Lo scopo del posizionamento
 Lo scopo del posizionamento Stimare posizioni di punti con le osservazioni disponibili: il problema è intrinsecamente deficiente di rango per stimare posizioni è necessario vincolare i gradi di libertà
Lo scopo del posizionamento Stimare posizioni di punti con le osservazioni disponibili: il problema è intrinsecamente deficiente di rango per stimare posizioni è necessario vincolare i gradi di libertà
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza?
 Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
EQUAZIONE DELLA RETTA
 EQUAZIONE DELLA RETTA EQUAZIONE DEGLI ASSI L equazione dell asse x è 0. L equazione dell asse y è 0. EQUAZIONE DELLE RETTE PARALLELE AGLI ASSI L equazione di una retta r parallela all asse x è cioè è uguale
EQUAZIONE DELLA RETTA EQUAZIONE DEGLI ASSI L equazione dell asse x è 0. L equazione dell asse y è 0. EQUAZIONE DELLE RETTE PARALLELE AGLI ASSI L equazione di una retta r parallela all asse x è cioè è uguale
Introduzione alla probabilità
 Introduzione alla probabilità Osservazione e studio dei fenomeni naturali: a. Caso deterministico: l osservazione fornisce sempre lo stesso risultato. b. Caso stocastico o aleatorio: l osservazione fornisce
Introduzione alla probabilità Osservazione e studio dei fenomeni naturali: a. Caso deterministico: l osservazione fornisce sempre lo stesso risultato. b. Caso stocastico o aleatorio: l osservazione fornisce
LA CHIMICA DEI GLUCIDI
 1.1 La classificazione chimica dei glucidi LA CHIMICA DEI GLUCIDI GLUCIDI (sono comunemente chiamati zuccheri) Si dividono in: SEMPLICI Sono chiamati MONOSACCARIDI Sono formati da una sola molecola di
1.1 La classificazione chimica dei glucidi LA CHIMICA DEI GLUCIDI GLUCIDI (sono comunemente chiamati zuccheri) Si dividono in: SEMPLICI Sono chiamati MONOSACCARIDI Sono formati da una sola molecola di
CORSO DI DISEGNO TECNICO EDILE LEZIONE 2 TEORIA DELLE OMBRE
 PERCORSI ABILITANTI SPECIALI (PAS) - A.A. 2013-2014 UNIVERSITÀ DI PISA DIPARTIMENTO DI INGEGNERIA CIVILE E INDUSTRIALE (DICI) CORSO DI DISEGNO TECNICO EDILE LEZIONE 2 TEORIA DELLE OMBRE 1 non abbiate mai
PERCORSI ABILITANTI SPECIALI (PAS) - A.A. 2013-2014 UNIVERSITÀ DI PISA DIPARTIMENTO DI INGEGNERIA CIVILE E INDUSTRIALE (DICI) CORSO DI DISEGNO TECNICO EDILE LEZIONE 2 TEORIA DELLE OMBRE 1 non abbiate mai
1 I solidi a superficie curva
 1 I solidi a superficie curva PROPRIETÀ. Un punto che ruota attorno ad un asse determina una circonferenza. PROPRIETÀ. Una linea, un segmento o una retta che ruotano attorno ad un asse determinano una
1 I solidi a superficie curva PROPRIETÀ. Un punto che ruota attorno ad un asse determina una circonferenza. PROPRIETÀ. Una linea, un segmento o una retta che ruotano attorno ad un asse determinano una
determinare le coordinate di P ricordando la relazione che permette di calcolare le coordinate del punto medio di un segmento si
 PROBLEMA Determinare il punto simmetrico di P( ;) rispetto alla retta x y =0 Soluzione Il simmetrico di P rispetto ad una retta r è il punto P che appartiene alla retta passante per P, perpendicolare ad
PROBLEMA Determinare il punto simmetrico di P( ;) rispetto alla retta x y =0 Soluzione Il simmetrico di P rispetto ad una retta r è il punto P che appartiene alla retta passante per P, perpendicolare ad
