- Φ e ψ Presenta 3,6 residui per spira -HB between C=O n residue n and NH n+4. - α-helix
|
|
|
- Daniela Ferrario
- 6 anni fa
- Visualizzazioni
Transcript
1 Structure
2 Basic elements
3 - Φ e ψ Presenta 3,6 residui per spira -HB between C=O n residue n and NH n+4. - α-helix
4 Β-sheet Red oxygen Blu nitrogen white hydrogen black Cα Violet lateral chain -at least two strands
5 antiparallel strands are very stable Antiparallel β sheet parallel β sheet
6 topology diagrams links between secondary structure elements aspartate carbamiltransferase flavodoxin plastocyanine
7 STRUCTURAL MOTIF Made by secondary structure elements Combination of di structural motifs form domains
8 4 frequent structural motifs helix-loop-helix β-hairpin greek key β-α-β
9 helix-loop-helix DNA binding Calcium binding protein (parvalbuina,calmodulina, troponinac)
10 EF hand -the loop between the two helices binds the calcium: consensus Sequence (orange aa involved in Ca binding ; green hydrophobic aa
11 troponine C -E4 EF hand motifs) -Asp (D9), Asn (N11) e Asp (D13), Glu (E20),. -
12 helix-loop-helix + DNA
13 β hairpin alone In a β sheet
14 Greek key -. Useful to link strands that are In the opposite side of a barrel
15 β-α-β -a simple way to link beta parallel strands. --the loop linking the carboxy terminal of the beta strand with the Amino terminal of the helix is oftn involved in the formation of the Active site
16 Motivo β-α-β The helix is always over the plane ( a )
17 DOMAINS alfa alfa-beta supercoiled helix 4 helix bundle globine TIM barrel alfa- beta open sheet horseshoe antiparallel beta Beta barrel greek key Up-and-down Jelly roll Parallel beta beta helix with 2 sheets beta helix with 3 sheets
18 Supercoiled helix 3.5 residue per coil
19 Electrostatic interactions a e and g are charged residues.
20 4 helix bundle -two pairs of antiparellel helices -
21 It is found in a single protein or in a dimeric protein
22 The globine folding 8 helices Connected by short loops To form an hydrophobic pocket
23 alfa-beta (
24 β-α-β 2 β-α-β motifs are connected in 2 different ways: a) alfa helices are on a single side of the plane formed by the beta sheet (TIM barrel and horseshoe); b) The helices are on both sides
25 TIM Barrel
26 The open alfa-beta sheet
27 Esempi di tipi diversi di strutture α/β aperta flavodossina e adenilato chinasi esochinasi e fosfoglicerato mutasi
28 The horseshoe Ribonuclease hinibitor, 17 β strands and 16 α helices. The conserved leucines
29 β barrel up and down Greek key jelly roll
30 greek key SOD 8 antiparallel β strands
31 Retinol binding protein up and down
32 neuraminidase tetramer each subunit 470 aa each monomer forms a barrel with 24 β Strands building 6 structural motifs each containing 4 strands
33 neuraminidase Tetramero Monomer () The basic motif: Topology of Each monomer
34 Structural and active region are well separated
35 L emoagglutinina si ripiega a formare un motivo strutturale a jelly roll Formata da 3 subunità, ognuna delle quali è ancorata alla membrana pericapsidica del virus dell influenza. Le teste globulari contengono i siti per i recettori che legano i residui di acido sialico presenti alla superficie delle cellule eucariotiche Singola subunità dell emoagglutinina del virus dell influenza
36 Il sito di legame per il recettore è formato dal dominio jelly roll La testa globulare di ogni subunità dell emoagglutinina ha una struttura a botte jelly roll distorta. Il sito di legame è localizzato all apice della subunità, all interno della struttura a botte jelly roll.
37 Domini ad eliche β parallele Scoperta nel 1993 in California Presente in molte proteasi batteriche extracellulari e nella proteina della coda del batteriofago P22 La catena polipeptidica risulta ripiegata a formare un ampio superavvolgimento ad elica formato da filamenti β separati da regioni loop I filamenti β si allineano a formare 2 o 3 foglietti β paralleli che racchiudono un core riempito dagli atomi delle catene laterali.
38 Eliche beta parallele a 2 foglietti Elica β a 2 foglietti dove sono mostrati 3 superavvolgimenti completi dell elica. - Ogni unità strutturale è costituita da 18 residui che formano una struttura β-loop-β. - Ogni regione loop contiene sei residui di sequenza Gly-Gly-X-Gly-X-Asp-H-U-X dove U è un aminoacido con catena ingombrante e idrofobica, spesso una leucina. - Ioni calcio sono legati ad entrambe le regioni loop, stabilizzandole.
39 Eliche beta parallele a 3 foglietti - 2 dei foglietti β sono paralleli l un l altro e perpendicolari al terzo. - Ogni giro dell elica contiene 3 brevi filamenti β ognuno di 3-5 residui collegati da 3 regioni loop. - Uno dei loop è sempre costiuito solo da 2 residui, mentre gli altri 2 sono più lunghi e variano in dimensioni. -Quindi l elica β comprende comprende 3 foglietti β paralleli grossolanamente disposti come le tre facce di un prisma
40 Struttura della pectato liasi C
La funzione delle proteine dipende dalla loro struttura tridimensionale
 La funzione delle proteine dipende dalla loro struttura tridimensionale La struttura dipende dal ripiegamento di particolari sequenze aminoacidiche La sequenza aminoacidica della catena polipeptidica è
La funzione delle proteine dipende dalla loro struttura tridimensionale La struttura dipende dal ripiegamento di particolari sequenze aminoacidiche La sequenza aminoacidica della catena polipeptidica è
Macromolecole Biologiche. La struttura secondaria (III)
 La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
Il legame peptidico. Il legame che ne risulta è il legame peptidico. Nelle cellule il legame viene creato nei ribosomi, catalizzato da enzimi.
 Il legame peptidico Il legame peptidico La polimerizzazione di AA viene raggiunta per eliminazione di una molecola d acqua tra il gruppo carbossilico di un AA e il gruppo amminico del successivo. Il legame
Il legame peptidico Il legame peptidico La polimerizzazione di AA viene raggiunta per eliminazione di una molecola d acqua tra il gruppo carbossilico di un AA e il gruppo amminico del successivo. Il legame
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Il gruppo peptidico ha una struttura rigida e planare, dovuta al parziale. legame peptidico. O O - N N + H H
 Il legame peptidico Il gruppo peptidico ha una struttura rigida e planare, dovuta al parziale (~40 %) carattere di doppio legame del legame peptidico. O O - C C N N + H H Il legame peptidico pp Il legame
Il legame peptidico Il gruppo peptidico ha una struttura rigida e planare, dovuta al parziale (~40 %) carattere di doppio legame del legame peptidico. O O - C C N N + H H Il legame peptidico pp Il legame
Macromolecole Biologiche. La struttura secondaria (II)
 La struttura secondaria (II) Nello stesso anno (1951) in cui proposero l α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo l α elica,
La struttura secondaria (II) Nello stesso anno (1951) in cui proposero l α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo l α elica,
La battaglia contro l influenza
 La battaglia contro l influenza Il contributo della biologia strutturale allo sviluppo di inibitori della sialidasi Prof. Elena Luraschi Virus dell influenza I virus dell influenza sono virus a RNA, con
La battaglia contro l influenza Il contributo della biologia strutturale allo sviluppo di inibitori della sialidasi Prof. Elena Luraschi Virus dell influenza I virus dell influenza sono virus a RNA, con
Proteine. Struttura tridimensionale Parte II
 Proteine Struttura tridimensionale Parte II (D.L. Nelson, M.M. Cox, Lehninger Principles of Biochemistry, 4th ed., W.H. Freeman & Co., 2005) Plot di Ramachandran Una situazione opposta a quella della glicina
Proteine Struttura tridimensionale Parte II (D.L. Nelson, M.M. Cox, Lehninger Principles of Biochemistry, 4th ed., W.H. Freeman & Co., 2005) Plot di Ramachandran Una situazione opposta a quella della glicina
20/12/ tipi di amino acidi: parecchie combinazioni
 20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
INTERAZIONI INTERMOLECOLARI NELLE PROTEINE
 INTERAZIONI INTERMOLECOLARI NELLE PROTEINE 1 RICHIAMI DI TERMODINAMICA 2 Entalpia Entropia Energia Libera di Gibbs ENERGIA INTERNA (U) L energia interna riassume tutti i contributi cinetici e potenziali
INTERAZIONI INTERMOLECOLARI NELLE PROTEINE 1 RICHIAMI DI TERMODINAMICA 2 Entalpia Entropia Energia Libera di Gibbs ENERGIA INTERNA (U) L energia interna riassume tutti i contributi cinetici e potenziali
formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini.
 Idomini(I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini. I domini sono definiti come parte
Idomini(I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini. I domini sono definiti come parte
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Macromolecole Biologiche. La struttura secondaria (I)
 La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
La struttura delle proteine e e descritta da quattro livelli di organizzazione
 La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
GLI ELEMENTI STRUTTURALI DELLE PROTEINE
 CAPITOLO 3 GLI ELEMENTI STRUTTURALI DELLE PROTEINE Gli elementi di struttura secondaria si possono ricondurre sostanzialmente a tre diverse tipologie (Fig. 1): - α-elica - filamenti β - anse o ripiegamenti
CAPITOLO 3 GLI ELEMENTI STRUTTURALI DELLE PROTEINE Gli elementi di struttura secondaria si possono ricondurre sostanzialmente a tre diverse tipologie (Fig. 1): - α-elica - filamenti β - anse o ripiegamenti
Struttura secondaria
 Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA
 Il Codice Genetico The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine)
Il Codice Genetico The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine)
Predizione di Struttura Secondaria di Proteine
 Laboratorio di Bioinformatica I Predizione di Struttura Secondaria di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Struttura delle proteine Struttura Secondaria Elementi non strutturati (Non hanno
Laboratorio di Bioinformatica I Predizione di Struttura Secondaria di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Struttura delle proteine Struttura Secondaria Elementi non strutturati (Non hanno
MOTIVI, DOMINI E MODULI
 Proteine della matrice MOTIVI, DOMINI E MODULI Seminario https://upload.wikimedia.org/wikipedia/commons/7/75/solenoid domain examples.png http://images.slideplayer.com/23/6899540/slides/slide_14.jpg PROTEINE:
Proteine della matrice MOTIVI, DOMINI E MODULI Seminario https://upload.wikimedia.org/wikipedia/commons/7/75/solenoid domain examples.png http://images.slideplayer.com/23/6899540/slides/slide_14.jpg PROTEINE:
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Struttura secondaria, Motivi e Domini nelle Proteine
 Struttura secondaria, Motivi e Domini nelle Proteine Proprietà generali Le forme ioniche degli aminoacidi, senza considerare alcuna ionizzazione delle catene laterali. Proprietà generali Tutti gli aminoacidi
Struttura secondaria, Motivi e Domini nelle Proteine Proprietà generali Le forme ioniche degli aminoacidi, senza considerare alcuna ionizzazione delle catene laterali. Proprietà generali Tutti gli aminoacidi
Il legame peptidico è polare
 Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
Amminoacidi/peptidi/proteine. Chimica Organica II
 Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
CONTROLLO DELL ESPRESSIONE GENICA NEI PROCARIOTI
 CONTROLLO DELL ESPRESSIONE GENICA NEI PROCARIOTI Unità trascrizionale E. Coli possiede diversi fattori sigma generale shock da calore carenza di azoto sintesi flagellare stress calore e sali Fattori sigma
CONTROLLO DELL ESPRESSIONE GENICA NEI PROCARIOTI Unità trascrizionale E. Coli possiede diversi fattori sigma generale shock da calore carenza di azoto sintesi flagellare stress calore e sali Fattori sigma
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
MIOSINA. Motori molecolari. II Strutture per il movimento Miosina, Kinesina e Dineina. Una struttura per il movimento. Prof.
 Prof. Giorgio Sartor Motori molecolari II Strutture per il movimento Miosina, Kinesina e Dineina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P02 - Versione 2.0 oct 2013 MIOSINA Una struttura
Prof. Giorgio Sartor Motori molecolari II Strutture per il movimento Miosina, Kinesina e Dineina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P02 - Versione 2.0 oct 2013 MIOSINA Una struttura
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Il Codice Genetico. La decodifica della sequenza nucleotidica in. sequenza aminoacidica
 Il Codice Genetico La decodifica della sequenza nucleotidica in sequenza aminoacidica La sequenza del mrna viene letta a gruppi di 3 nucleotidi, senza interruzioni e senza sovrapposizioni; 4 3 = 64 ---------64
Il Codice Genetico La decodifica della sequenza nucleotidica in sequenza aminoacidica La sequenza del mrna viene letta a gruppi di 3 nucleotidi, senza interruzioni e senza sovrapposizioni; 4 3 = 64 ---------64
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
10/03/ Proteine di membrana
 Proteine di membrana http://www.nfsdsystems.com/w3bio315/; http://www.ncbi.nlm.nih.gov/books/nbk28193/figure/a105/?report=objectonly Proteine di membrana 1 I domini transmembrana delle proteine integrali
Proteine di membrana http://www.nfsdsystems.com/w3bio315/; http://www.ncbi.nlm.nih.gov/books/nbk28193/figure/a105/?report=objectonly Proteine di membrana 1 I domini transmembrana delle proteine integrali
Schema'c drawing of the polypep'de backbone of ribonuclease S (bovine pancrea'c ribonuclease A, cleaved by sub'lisin between residues 20 and 21).
 Schema'c drawing of the polypep'de backbone of ribonuclease S (bovine pancrea'c ribonuclease A, cleaved by sub'lisin between residues 20 and 21). Spiral ribbons represent α- helices and arrows represent
Schema'c drawing of the polypep'de backbone of ribonuclease S (bovine pancrea'c ribonuclease A, cleaved by sub'lisin between residues 20 and 21). Spiral ribbons represent α- helices and arrows represent
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Domini nelle Proteine
 Struttura secondaria, Motivi e Domini nelle Proteine Proprietà generali Le forme ioniche degli aminoacidi, senza considerare alcuna ionizzazione delle catene laterali. Proprietà generali Tutti gli aminoacidi
Struttura secondaria, Motivi e Domini nelle Proteine Proprietà generali Le forme ioniche degli aminoacidi, senza considerare alcuna ionizzazione delle catene laterali. Proprietà generali Tutti gli aminoacidi
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
STRUTTURA E FUNZIONI
 STRUTTURA E FUNZIONI Typical Cell Membrana plasmatica Chiamata anche membrana cellulare Circonda ogni cellula Separa il contenuto cellulare dal cio che la circonda Separa il LIC dal LEC Controlla il movimento
STRUTTURA E FUNZIONI Typical Cell Membrana plasmatica Chiamata anche membrana cellulare Circonda ogni cellula Separa il contenuto cellulare dal cio che la circonda Separa il LIC dal LEC Controlla il movimento
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Struttura delle Proteine
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari
Fattori di crescita. Membrana citoplasmatica. Recettori di fattori di crescita. Proteine trasduttrici del segnale. Nucleo. Fattori trascrizionali
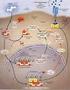 Fattori di crescita Recettori di fattori di crescita Membrana citoplasmatica roteine trasduttrici del segnale Nucleo Fattori trascrizionali roteine del ciclo cellulare Ciclo di divisione cellulare Fattori
Fattori di crescita Recettori di fattori di crescita Membrana citoplasmatica roteine trasduttrici del segnale Nucleo Fattori trascrizionali roteine del ciclo cellulare Ciclo di divisione cellulare Fattori
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 5
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 6
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
F. Fogolari Milano, Marzo
 Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Fondamentali in ogni organismo, hanno molteplici ruoli:
 Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
RELAZIONE TRA STRUTTURA E FUNZIONE
 RELAZIONE TRA STRUTTURA E FUNZIONE 1) Classi strutturali e funzione enzimatica 2) Fold delle proteine e funzione 3) Famiglie di proteine omologhe e funzione Struttura primaria (sequenza) Struttura secondaria
RELAZIONE TRA STRUTTURA E FUNZIONE 1) Classi strutturali e funzione enzimatica 2) Fold delle proteine e funzione 3) Famiglie di proteine omologhe e funzione Struttura primaria (sequenza) Struttura secondaria
Metodi predittivi 1D
 Metodi predittivi 1D Introduzione Data la sequenza di una proteina ci sono tutta una serie di predizioni che si possono fare. Queste utilizzano i metodi di predizione che abbiamo visto in precedenza, in
Metodi predittivi 1D Introduzione Data la sequenza di una proteina ci sono tutta una serie di predizioni che si possono fare. Queste utilizzano i metodi di predizione che abbiamo visto in precedenza, in
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
Lipidi. Funzioni biologiche
 Lipidi Funzioni biologiche -I lipidi che contengono catene di idrocarburi fungono da riserva di energia. -Le molecole lipidiche, sotto forma di doppi strati, sono componenti essenziali delle membrane biologiche.
Lipidi Funzioni biologiche -I lipidi che contengono catene di idrocarburi fungono da riserva di energia. -Le molecole lipidiche, sotto forma di doppi strati, sono componenti essenziali delle membrane biologiche.
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Gli angoli diedri (φ, ψ) della catena polipeptidica in conformazione foglietto β cadono nella. (quadrante in alto a sinistra).
 Strutture secondarie (b) Foglietto β Nello stesso anno (1951) in cui proposero l α α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo
Strutture secondarie (b) Foglietto β Nello stesso anno (1951) in cui proposero l α α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo
La struttura delle proteine e. organizzazione. ramificati di aminoacidi
 La struttura delle proteine e descritta da quattro livelli di organizzazione Struttura Primaria- la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e descritta da quattro livelli di organizzazione Struttura Primaria- la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Principi di Citologia e Istologia. Prof. Pucci, La Matrice Extracellulare
 Principi di Citologia e Istologia. Prof. Pucci, 2003 La Matrice Extracellulare La matrice extracellulare è composta da quattro classi di macromolecole Collageni Proteoglicani Elastina Glicoproteine Essa
Principi di Citologia e Istologia. Prof. Pucci, 2003 La Matrice Extracellulare La matrice extracellulare è composta da quattro classi di macromolecole Collageni Proteoglicani Elastina Glicoproteine Essa
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
6.5 RNA Secondary Structure. 18 novembre 2014
 6.5 RNA Secondary Structure 18 novembre 2014 Calendario Oggi è la lezione 17/24: ultima lezione su Programmazione dinamica Metodo greedy: 18, 19 Grafi: 20, 21, 22, 23 Reti di flusso: 23, 24 (=mercoledì
6.5 RNA Secondary Structure 18 novembre 2014 Calendario Oggi è la lezione 17/24: ultima lezione su Programmazione dinamica Metodo greedy: 18, 19 Grafi: 20, 21, 22, 23 Reti di flusso: 23, 24 (=mercoledì
RUOLI BIOLOGICI DELLE PROTEINE. Biochimica
 RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
Tirosin chinasi senza o con funzione recettoriale
 Tirosin chinasi senza o con funzione recettoriale elica di poliprolina Il dominio chinasico di Src è mantenuto nello stato inattivo mediante due distinte interazioni intramolecolari: il legame del dominio
Tirosin chinasi senza o con funzione recettoriale elica di poliprolina Il dominio chinasico di Src è mantenuto nello stato inattivo mediante due distinte interazioni intramolecolari: il legame del dominio
Macromolecole Biologiche. Chimica Biologica A.A. 2010-2011. Struttura Terziaria
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura Terziaria Domini e struttura terziaria Struttura terziaria L arrangiamento spaziale degli amminoacidi di una singola catena polipeptidica
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura Terziaria Domini e struttura terziaria Struttura terziaria L arrangiamento spaziale degli amminoacidi di una singola catena polipeptidica
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
strutture di Proteine
 Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
I sistemi muscolare e scheletrico
 I sistemi muscolare e scheletrico Il sistema muscolare Esistono tre tipi di muscoli con caratteristiche strutturali e funzionali diverse: o il muscolo striato o scheletrico; o il muscolo liscio; o il muscolo
I sistemi muscolare e scheletrico Il sistema muscolare Esistono tre tipi di muscoli con caratteristiche strutturali e funzionali diverse: o il muscolo striato o scheletrico; o il muscolo liscio; o il muscolo
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
L icona posta all estrema sinistra consente di portare la proteina al centro dello schermo.
 Deep View Deep View è un potente programma di grafica, ottenibile da Expert Protein Analysis System (ExPASy) Molecular Biology Server di Ginevra. Deep View è semplice da usare e consente di vedere la struttura
Deep View Deep View è un potente programma di grafica, ottenibile da Expert Protein Analysis System (ExPASy) Molecular Biology Server di Ginevra. Deep View è semplice da usare e consente di vedere la struttura
DOGMA CENTRALE DELLA BIOLOGIA. Secondo il dogma centrale della biologia, il DNA dirige la. sintesi del RNA che a sua volta guida la sintesi delle
 DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Formazione di una fibra muscolare scheletrica
 Formazione di una fibra muscolare scheletrica I mioblasti derivano da cellule del midollo osseo. Queste in determinate condizioni di necessità (stress chimico, traumatico etc.) vengono mobilizzate dalla
Formazione di una fibra muscolare scheletrica I mioblasti derivano da cellule del midollo osseo. Queste in determinate condizioni di necessità (stress chimico, traumatico etc.) vengono mobilizzate dalla
SINTESI DELLE PROTEINE
 SINTESI DELLE PROTEINE IN UN GIORNO DI UN INDIVIDUO ADULTO NORMALE: -100 grammi vengono introdotti con la dieta -400 grammi vengono degradati -400 grammi vengono sintetizzati -100 grammi vengono consumati
SINTESI DELLE PROTEINE IN UN GIORNO DI UN INDIVIDUO ADULTO NORMALE: -100 grammi vengono introdotti con la dieta -400 grammi vengono degradati -400 grammi vengono sintetizzati -100 grammi vengono consumati
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
