ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
|
|
|
- Anna Valle
- 6 anni fa
- Visualizzazioni
Transcript
1 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni blande di Temperatura e ph Hanno pesi molecolari >> dei substrati o gruppi funzionali su cui agiscono Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
2 I COFATTORI possono essere Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Nucleotidi : NAD +, FAD + Alcuni Cofattori sono associati solo temporaneamente COSUBSTRATI o COENZIMI Alcuni Cofattori sono associati in modo permanente con la proteina, anche mediante legami covalenti: GRUPPI PROSTETICI : il gruppo eme dei citocromi Il complesso La proteina enzima-cofattore cataliticamente attivo = oloenzima cataliticamente inattiva = apoenzima Apoenzima (inattivo) + cofattore oloenzima ( attivo)
3 Ioni inorganici che svolgono funzione di cofattori per alcuni enzimi, molti sono micronutrienti
4 I coenzimi vengono modificati chimicamente durante le reazioni : NADH, FADH 2 (nucleotidi) Per completare il ciclo catalitico, il coenzima deve tornare al suo stato originale: reazione di rigenerazione anche a carico di un E. diverso Alcune vitamine idrosolubili sono precursori di coenzimi le VITAMINE devono. essere presenti nella dieta
5 La reazione dell enzima (catalisi) avviene nel SITO ATTIVO = Tasca o fenditura sulla superficie dell E. sito di legame per il substrato gruppi catalitici Gr. COOH o NH 2 di catene laterali di a.a -S- di cisteina Cofattori che garantiscono la rottura e formazione di legami
6 Il legame del substrato con sito attivo coinvolge interazioni non covalenti La forma e la polarità del sito di legame sono responsabili della specificità enzimatica Esiste complementarietà fra la forma e la polarità del substrato con quelle del sito attivo Meccanismo della catalisi enzimatica Nel 1894 teoria di Emil Fischer Modello chiave-serratura contatto rigido fra E e S Tale adattamento non consentirebbe una reazione reversibile essendo P diverso da S Nel 1958: ipotesi dello Adattamento indotto La vicinanza di S o P all Enzima provoca modificazioni della conformazione del sito attivo dell E Migliore combinazione E-S e E-P
7
8 L'enzima esochinasi è un buon esempio del modello dell'adattamento indotto: quando il glucosio si avvicina al sito attivo, l'enzima cambia conformazione, avvolgendosi attorno al substrato
9 Come agisce un enzima? Modifica la VELOCITà DI UNA REAZIONE Gli enzimi non influiscono sul rapporto dell equilibrio fra reagenti e prodotti: - Le velocità delle reazioni, in entrambe le direzioni, vengono aumentate della stessa entità - Non sono in grado di fare avvenire una reazione non spontanea, ( ΔG>0 energicamente in salita )
10 Consideriamo la reazione di I ordine : A P A= reagente P= prodotto A temperatura costante, la velocità di reazione è proporzionale alla frequenza con cui le molecole di A si incontrano La velocità è proporzionale alla concentrazione di A La velocità di reazione : intesa come comparsa del prodotto P o scomparsa V = d P = - d A = K A dt dt del reagente A K = cost. di velocità è una costante di proporzionalità
11 E una reazione bimolecolare di II ordine : 2 tipi di reagenti A reagisce con B, dando origine a P e Q. 2 molecole di reagenti diversi devono incontrarsi simultaneamente Collisione formazione di P e Q Le concentrazioni di A e B diminuiscono mentre quelle di P e Q aumentano. Esprimiamo la velocità in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un reagente o di un prodotto e l intervallo di tempo considerato v = K A B il segno - indica la variazione negativa della concentrazione dei reagenti
12 Alcune molecole di A e B devono possedere + energia rispetto alle altre STATO ATTIVATO raggiungimento dello STATO DI TRANSIZIONE Punto + alto della barriera energetica E uno stato instabile, le molecole possono: o trasformarsi nei prodotti o tornare allo stato non eccitato con emissione di energia (calore, luce) La probabilità che una reazione avvenga in una direzione dipende dal ΔG fra reagenti e prodotti ΔG < 0 ΔG > 0 la reazione procede spontaneamente verso i prodotti è la reazione inversa a procedere spontaneamente
13
14 Nello stato di transizione i reagenti sono parzialmente convertiti in prodotti Energia di attivazione = energia (calorie) richiesta per portare 1 mole di reagente allo stato di transizione La velocità di una reazione chimica è proporzionale alla concentrazione delle molecole allo stato di transizione
15 Vi sono 2 vie per aumentare la velocità di reazione 1. Incremento della Temperatura aumento dei moti termici delle molecole aumento del numero di molecole con en. interna sufficiente a raggiungere lo stato di transizione La vel. quasi si raddoppia per ogni aumento di T=10 C Q 10 è il rapporto tra vel di reazione a una data temp. e la vel della reaz ad una temp inferiore di 10 C Q 10 = 2 2. Impiego di un catalizzatore abbassamento della barriera energetica Il catalizzatore si combina transitoriamente con A e B in un complesso con uno stato di transizione energeticamente + basso
16 Abbassamento dell energia di attivazione Maggior numero di molecole nell unità di tempo in grado di reagire rispetto al numero che reagirebbero in assenza di catalizzatore Alla fine della reazione il catalizzatore viene rilasciato e può combinarsi con altre molecole di A e B
17 Reazione chimica a 2 tappe 2 stati di transizione 2 diverse energie di attivazione
18 La velocità di reazione diminuisce con il passare del tempo: Il substrato si consuma La reazione è reversibile e la formazione del prodotto innesca la reazione contraria Il prodotto di reazione può inibire l attività dell enzima L enzima può andare incontro a denaturazione Per misurare la velocità di una reazione enzimatica conviene misurare la velocità iniziale (V 0 )
19 Se la concentrazione del substrato S è maggiore dell Enzima S >> E Se il tempo di analisi è ridotto misurando la velocità iniziale (V 0 ) La quantità di S trasformato è trascurabile e può essere considerata costante nel tempo
20 Cinetica di reazioni enzimatiche ad un substrato. La prima equazione generale di velocità per una reazione enzimatica fu derivata nel 1903 da Victor Henri. la velocità iniziale della reazione è direttamente proporzionale alla concentrazione dell'enzima, ma cresce in modo non lineare al crescere della concentrazione del substrato fino ad un valore limite massimo Gli studi di Henri furono ripresi ed ampliati da Michaelis e Menten (1913) che hanno dato il nome alla equazione generale di velocità di reazioni enzimatiche ad un substrato.
21 Il meccanismo di reazione proposto prevede: La prima assunzione è nota come del "quasi equilibrio" o dello "equilibrio rapido" la formazione del complesso ES è una reazione molto veloce ed è reversibile : Il complesso enzima-substrato è in equilibrio con l'enzima libero ed il substrato questa situazione di equilibrio non è disturbata dalla formazione del prodotto: la velocità di formazione del prodotto a partire da ES è molto piccola rispetto alla velocità con cui ES si scinde a dare E+S k3 <<k2
22 L E si combina reversibilmente con S in una reazione veloce Il complesso ES si scinde in una reazione lenta che rappresenta la tappa limitante Briggs e Haldane (1925) introdussero l assunzione dello "stato stazionario" [ES] rimane costante la concentrazione di ES è costante quando la sua velocità di formazione di ES eguaglia la sola velocità di decomposizione in E+S (K1=K2) Questo si verifica assumendo k3 <<k2 la velocità di trasformazione di ES in E+P sia trascurabile
23 Stato stazionario: La conc di ES resta costante: Velocità di sintesi = Vel di consumo quando tutto S viene consumato l E torna ad essere libero conversione max in P l'equazione di velocità di formazione del prodotto si può esprimere come funzione della concentrazione di ES:
24 In ogni istante l Enzima è presente in 2 forme Forma libera E Forma legata ES Equazione di conservazione di massa per l'enzima La velocità della reazione sarà max quando tutto sarà come complesso ES e la concentrazione di enzima libero E sarà minima Questa condizione si verifica quando [S] >> [E] la concentrazione del substrato è molto più grande della concentrazione dell'enzima [S] è elevata l E reagirà velocemente con S e sarà sempre saturo con il substrato Forma ES stato stazionario
25 Le cinetiche enzimatiche vengono di solito determinate in condizioni di Stato stazionario L'assunzione [S] >> [E tot ] garantisce che tutto l'enzima sia presente in forma di complesso con il substrato, per cui potremo scrivere Espressione della massima velocità ottenibile per una data quantità di enzima in condizioni di saturazione del substrato.
26 RIASSUMENDO
27
28
29 RIASSUMENDO : 3 FASI NEL RAPPORTO E-S
30 RAPPRESENTAZIONE GRAFICA
31 l'equazione di velocità delle reazioni enzimatiche viene descritta con l equazione di Michaelis-Menten: la velocità iniziale di una reazione enzimatica ad un substrato è in relazione tramite due costanti (Vmax e Km) con la sola concentrazione del substrato, che La concentrazione del substrato per la assunzione [S] >> [Etot ] è assimilabile sempre alla concentrazione iniziale di substrato.
32 La Vmax indica la saturazione dell enzima a [S] infinita La Km è una costante - dipende dal sistema enzimatico considerato, - correlata alla costante di dissociazione di ES. La Km rappresenta la concentrazione di S richiesta perché la vel di reazione sia V = ½ della Vmax
33 Minore è il valore di Km Solitamente maggiore sarà il legame (affinità) fra E e S 1 μm < Km < 1 mm Conoscendo la Vmax e la Km di un enzima si può calcolare la velocità di reazione ad una data concentrazione di S Un E. che catalizza una reazione fra 2 o + substrati diversi avrà una diversa Km per ciascun substrato
34 Importanza della Km: Rappresenta una misura inversa dell affinità dell E per un dato S: Minore è la Km + stabile è il complesso ES Se lo stesso E catalizza una reazione con 2 substrati simili Es: Glucosio e Fruttosio Il substrato su cui agirà + di frequente è quello con Km minore La Km dà informazioni sulla concentrazione di un substrato nel comparto cellulare dove avviene la reazione: Enzimi che catalizzano reazioni a concentrazioni elevate di substrato (saccarosio) avranno Km elevate Enzimi che catalizzano reazioni con substrati presenti a concentrazioni molto basse (ormoni) Km piccole
35 Kcat = COSTANTE CATALITICA di un enzima viene anche definita numero di turnover Rappresenta il numero di volte che l enzima turnover, cioè reinizia la sua attività nell unità di tempo Rappresenta il numero massimo di molecole di substrato convertito in prodotto nell unità di tempo Kcat = V max E TOT
36 EQUAZIONE DI LINEWEAVER BURK O DIAGRAMMA DEI DOPPI RECIPROCI È il metodo migliore per calcolare Km e Vmax è il reciproco dell equazione di Michaelis-Menten:
37 E l equazione di una retta
38 le variabili sono 1/v e 1/[S] 1/Vmax è l' intercetta sull' asse y -1/Km è l' intercetta sull' asse x.
39 E l equazione di una retta che occupa il I e II quadrante A concentrazioni crescenti di S la retta assume valori decrescenti e si può calcolare 1/Vmax Migliore situazione nell intervallo 0,5 Km < S < 5 Km Quando la S è elevata i punti tendono ad affollarsi Uno svantaggio è che per molti valori di S si va nel quadrante sinistro del grafico
40 INIBIZIONE ENZIMATICA INIBITORE= qualsiasi agente in grado di diminuire la velocità di una reazione catalizzata INATTIVATORE quando l inibizione è irreversibile Inibitori IRREVERSIBILI formano legami covalenti con gli enzimi denaturano gli Enzimi Inibitori REVERSIBILI formano legami deboli e non covalenti 3 tipi di inibizione reversibile: Inibizione COMPETITIVA Aumenta la Km e non ha nessun effetto sulla Vmax Inibizione NON COMPETITIVA Diminuisce Vmax, la Km resta inalterata Inibizione INCOMPETITIVA Diminuiscono Km e Vmax
41 Inibizione competitiva L inibitore competitivo compete con S per il sito catalitico È una molecola molto simile a S Può adattarsi e legarsi al sito dell E ma non può reagire con l E Es. inibizione competitiva: L'acido malonico è in grado di legarsi nel sito attivo dell' enzima, ma non può essere ossidato avendo un solo gruppo CH 2
42 per l assunzione dell equilibrio rapido K I = E I EI e diminuzione dell affinità per S aumento della Km + basso è il valore di KI, maggiore è l inibizione Molto E è presente come EI Km apparente
43 Aumento della Km di un fattore α = (1 + [ I ] / KI) La velocità massima della reazione non è influenzata dalla presenza dell'inibitore ad elevate concentrazioni di substrato tutto l'enzima viene complessato in forma di ES. la reazione è rallentata la Vmax è raggiunta + tardi
44 La Vmax è raggiunta con una quantità maggiore di S K m I Km 2 Enzima non inibito Enzima inibito K m I < Km 2
45 Km Vmax Aumento del coefficiente angolare (pendenza) il valore aumentato di Km ci dice che più substrato è necessario per raggiungere la stessa Vmax / 2 che si avrebbe in assenza dell'inibitore Km app> Km La Km apparente non è costante è in funzione del fattore α che considera I
46 Inibizione non competitiva Un inibitore non competitivo è una sostanza che si lega sia all'enzima libero che al complesso ES La presenza di I non impedisce ad S di legarsi ( e viceversa) l'inibitore non ha alcun effetto sul legame del substrato con l' enzima, ed il substrato non ha alcun effetto sulla formazione del legame tra inibitore ed enzima, in quanto entrambi si legano reversibilmente all' enzima in síti differenti. ES ed ESI hanno le stesse costanti di dissociazione E ed EI hanno quindi uguale affinità per S
47 I si lega tanto ad E che a ES S si lega sia ad E che a EI. La presenza di uno di essi non ha alcun effetto sulla costante di dissociazione dell'altro, ma il complesso ESI è inattivo in presenza di I, anche ad infinite concentrazioni di S, l'enzima non potrà essere tutto sotto forma di ES, ma parte rimarrà come complesso non-produttivo ESI. La presenza di un inibitore non competitivo fa sembrare che meno enzima sia presente
48 Vmax 1 Vmax 2 Vmax 2 < Vmax 1 Gli inibitori si legano reversibilmente in un sito diverso dal sito attivo. Una parte dell enzima resta inattivo L inibizione non è influenzata dalla concentrazione del substrato S
49 Vmax sarà più bassa in presenza dell'inibitore; la Km non sarà variata in quanto i complessi ES ed ESI hanno le stesse costanti di dissociazione E ed EI hanno quindi uguale affinità per S
50 Strutturalmente gli inibitori non competitivi sono meno simili a S rispetto a quelli competitivi Sono metalli pesanti, fluoruri Es: l eccesso di O 2 può provocare l ossidazione di gruppi -SH vicini : - rimozione di H - formazione di ponti S S Modificazione della struttura dell Enzima Il sito attivo non può + combinarsi con S Anche gli agenti denaturanti per le proteine: Acidi e basi forti, detergenti, urea Rottura legami H Inibizione non competitiva
51 Inibizione incompetitiva o Acompetitiva Un inibitore incompetitivo è una sostanza che si lega reversibilmente solo al complesso ES dando origine al complesso non produttivo ESI i rispettivi valori all'equilibrio: La causa può essere: o il substrato sia direttamente coinvolto nel legare l'inibitore, o il substrato produca dei cambiamenti conformazionali nel sito dell'inibitore da permettergli di entrare. In presenza di una qualsiasi concentrazione di I, per quanto elevata possa essere la concentrazione di S, l'enzima non può essere presente solo come ES
52
53 presenza di rette parallele: - la Vmax e la Km sono diminuite dello stesso fattore. La Vmax raggiunta è inferiore a quella dell E non inibito il valore della Km apparente sarà più basso: il complesso ESI non può liberare il substrato, mostrando per esso una affinità infinita, L inibizione aumenta con l aumento della concentrazione di S in quanto l'inibitore incompetitivo si lega al solo complesso ES, e la [ES] cresce al crescere di [ S ]. Gli inibitori incompetitivi sono poco rappresentati
54 ph Ogni enzima ha il suo valore ottimale di ph In genere 6 > ph ottimale < 8 I diagrammi delle attività enzimatiche in Funzione del ph possono essere: 1. Curve a campana 2. Curve quasi piatte - a valori estremi di ph Denaturazione dell enzima - Il ph influenza anche la ionizzazione dei Gruppi COOH e NH 2 importanti per l attività catilitica
55 Temperatura Le piante non possono regolare la loro temperatura la velocità delle reazioni enzimatiche aumenta da 0 a C Aumento dell energia cinetica delle molecole - La temperatura può agire modificando la conformazione dell enzima Effetto sulla Km e Vmax - Enzimi diversi, ma della stessa famiglia possono rispondere in modo diverso alla temperatura A temp > C o Temp basse : Denaturazione = Inattivazione dell enzima
56 Le temperature ottimali dipendono dall habitat delle piante : - Nelle piante alpine e artiche : Enzimi fotosintetici con una temp ottimale di C - Nelle piante dei climi temperati ( mais ) la temperatura ottimale per gli stessi enzimi è 30 C ISOZIMI enzimi in grado di agire sullo stesso substrato e di convertirlo nello stesso prodotto, sono molto simili hanno piccole differenze nella sequenza degli a.a Differenze codificate a livello genetico, traduzionale Una pianta con isozimi differenti in grado di catalizzare la stessa reazione Gli isozimi differiscono nella risposta a fattori ambientali
57 Le ISOFORME degli enzimi sono modificazioni post-traduzionali : Gli E. dopo la sintesi subiscono modificazioni chimiche che possono influenzare la loro attività catalitica Le isoforme sono codificate dallo stesso gene stessa sequenza di a.a. Le modificazioni successive sono dovute a: - Fosforilazione di un OH di un a.a. - Glicosilazione attacco di 1 o + zuccheri - Metilazione attacco di CH 3 Tali modificazioni che possono avvenire nella stessa cellula e in diversi stadi di sviluppo Es: La luce induce segnali nelle piante che si traducono in meccanismi di fosforilazione o defosforilazione di certe proteine enzimatiche L enzima modificato risponde meglio all ambiente
58 L azione di enzimi può essere inibita da - ioni o molecole estranei alterazione della configurazione mancata formazione del complesso ES - normali costituenti cellulari, prodotti del metabolismo attivazione o inibizione dell attività enzimatica INIBIZIONE da feedback o da prodotto finale È l inibizione a carico di un metabolita non correlato chimicamente al normale substrato su cui agisce l enzima inibito È un importante meccanismo di regolazione metabolica gli organismi producono solo quantità adeguate dei composti che utilizzano
59 INIBIZIONE da feedback o da prodotto finale si verifica solo quando f è in concentrazione elevata ATTIVAZIONE a è il substrato di 2 enzimi con 2 diverse vie e 2 diversi prodotti finali: Una sintesi eccessiva di k viene impedita dall attivazione di k sull E della I reazione nella sequenza che porta alla formazione di e
60 ENZIMI ALLOSTERICI Sono proteine con maggiore complessità (+ subunità) e contengono due o più siti di legame : siti allosterici (diversi e distinti dal sito catalitico) Il termine allosteria deriva dal greco allos, cioè "altro", e stereos, "struttura, solido", in riferimento alla separazione del sito allosterico di una proteina dal suo sito attivo la regolazione allosterica (o allosteria) è la regolazione di un enzima mediata da una molecola detta effettore, che si lega al sito allosterico. Gli effettori che intensificano l'attivazione della proteina vengono detti attivatori allosterici, quelli che al contrario diminuiscono l'attivazione sono gli inibitori allosterici
61 L effettore può essere anche il substrato quando si lega al sito allosterico allosteria omotropica l'effettore coincide con il suo substrato, è tipicamente un attivatore, allosteria eterotropica l'effettore è diverso dal suo substrato, può essere un attivatore o un inibitore A volte la regolazione allosterica può fungere da controllo retroattivo ( feedback negativo) quando l'effettore allosterico inibitore è il prodotto della reazione enzimatica.
62 Il legame dell'effettore presso il sito allosterico è in grado di modificare leggermente la struttura terziaria dell'enzima quindi di variare la sua affinità per il substrato, consentendo di incrementare o di ridurre l'attività catalitica a seconda delle esigenze della cellula. Il legame è reversibile, non covalente : modificazione transitoria e reversibile della conformazione dell enzima Il legame di un effettore al suo enzima è un legame cooperativo Si parla di COOPERATIVITA o EFFETTO COOPERATIVO
63 Cooperatività = il legame di 1 molecola del modulatore (o S) all E aumenterà o diminuirà la capacità dell enzima di legare una II A molecola di modulatore ( o S). cooperatività positiva Se la modificazione aumenta la capacità di legame (o affinità) cooperatività negativa Se questa capacità di legame viene diminuita cambiamento della costante di legame della proteina La costante di legame è analoga al Ks per il substrato e alla Ki per l'inibitore.
64 Il meccanismo allosterico nelle proteine multimeriche può essere spiegato tramite 2 teorie: modello simmetrico o d'insieme o concertato o MWC proposto da Jacques Monod, Jeffries Wyman e Jean-Pierre Changeux nel 1965 modello sequenziale descritto da Daniel Koshland e dai suoi collaboratori George Némethy e David Filmer nel 1966 Entrambi ipotizzano che 1.le subunità di un enzima esistano in una delle due conformazioni: Tesa (T) o Rilassata (R), 2. le subunità rilassate leghino i substrati molto più prontamente di quelle nello stato teso. I due modelli differiscono soprattutto per le interazione tra subunità.
65 Ipotesi simmetrica o concertata o d insieme Le subunità possono esistere solo in due differenti conformazioni: 1. stato R, forma attiva, ad alta affinità (Conformazione Rilassata) 2. stato T, forma inattiva a bassa affinità (Conformazione Tesa) Se avviene un cambiamento di conformazione in un solo protomero, la stessa trasformazione è indotta negli altri in maniera concertata. Di conseguenza, tutte le subunità devono esistere nella stessa conformazione. L'assenza del modulatore sposta l'equilibrio verso lo stato T, l'attacco del modulatore lo sposta verso R.
66 il substrato è il modulatore È più probabile che si leghi alla conformazione R data la maggiore affinità. Spostamento dell equilibrio: diminuisce la concentrazione della forma T e aumenta quella della forma R. Aumento della probabilità di transizione dalla forma inattiva a quella attiva cooperatività positiva
67 L'ipotesi sequenziale: possono trovarsi enzimi misti, contenenti cioè entrambe le subunità. Le forme pure R e T rappresentano gli estremi di questo equilibrio. l effettore ha un'influenza più diretta sulla forma dell'enzima. adattamento indotto = la subunità a cui si è legato il substrato viene convertita nella conformazione R (cooperatività positiva). non propaga il cambiamento di conformazione alle subunità adiacenti, ma provoca una lieve alterazione nella loro struttura in modo che i loro siti leganti siano più recettivi per i substrati (maggiore affinità).
68 L effettore non propaga il cambiamento di conformazione alle subunità adiacenti: provoca una lieve alterazione nella loro struttura in modo che i loro siti leganti siano più recettivi per i substrati (maggiore affinità). il cambiamento di forma tende a spingere le altre subunità verso la forma R cooperatività positiva più unità si potranno trovare nello stato a maggiore affinità.
69 Gli enzimi allosterici spesso non seguono la cinetica di M.M. forma sigmoidale della curva: a basse concentrazioni di substrato un aumento di concentrazione del substrato lieve incremento della velocità Interazione di tipo cooperativo fra le subunità dell Enzima Ad alti livelli di substrato il grafico è molto simile all'iperbolico Il legame con effettori allosterici positivi o negativi possono influenzare il legame con S (Km, Vmax)
70 L'inibitore esalta la forma sigmoidale allungando il piede della curva, mentre l'attivatore ha l'effetto opposto fino alla completa scomparsa del piede. per alte concentrazioni di attivatore si giunge ad una curva iperbolica Tutte le curve tendono allo stesso valore di Vmax. Gli effettori operano sulla capacità di legare il substrato cioè sulla Km.
71
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Coenzimi : NAD +, FAD + COSUBSTRATI GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Coenzimi : NAD +, FAD + COSUBSTRATI GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA
 TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Inibizione Enzimatica
 Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio
 Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Fondamenti di Chimica Farmaceutica. Recettori come bersagli dei farmaci
 Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Energia di attivazione
 Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Cine%ca enzima%ca. Copyright 2013 Zanichelli editore S.p.A.
 Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Le reazioni chimiche
 Le reazioni chimiche Reazioni di sintesi Reazioni di sintesi o di combinazione diretta: A + B à AB. Nelle reazioni di sintesi due o più atomi o molecole reagiscono tra loro per dare un unico composto come
Le reazioni chimiche Reazioni di sintesi Reazioni di sintesi o di combinazione diretta: A + B à AB. Nelle reazioni di sintesi due o più atomi o molecole reagiscono tra loro per dare un unico composto come
La via per accelerare i processi biologici
 La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Enzimi. 1. Definizione 2. Numero di Turn-over 3. Nomenclatura 4. Cofattori 5. Sito attivo
 Enzimi 1. Definizione 2. Numero di Turn-over 3. Nomenclatura 4. Cofattori 5. Sito attivo 6. Specificità o Modello di Fischer (chiave-serratura) o Modello dell adattamento indotto 7. Cinetica enzimatica
Enzimi 1. Definizione 2. Numero di Turn-over 3. Nomenclatura 4. Cofattori 5. Sito attivo 6. Specificità o Modello di Fischer (chiave-serratura) o Modello dell adattamento indotto 7. Cinetica enzimatica
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe.
 INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Velocità di reazione Una trasformazione chimica modifica completamente la natura delle sostanze iniziali ( i reagenti), formando altre specie (i prodo
 Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
FARMACODINAMICA. La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci.
 FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi
 Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Cr Mn Fe Co Ni Cu Zn. Chimica Inorganica Biologica Vita ed Energia
 Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Fonte diretta di Energia è l ATP.
 Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA
 REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA Reazione chimica in condizione di equilibrio: concentrazioni costanti che obbediscono al vincolo determinato dalla costante
REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA Reazione chimica in condizione di equilibrio: concentrazioni costanti che obbediscono al vincolo determinato dalla costante
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed.
 Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Gli ENZIMI sono proteine (eccezioni: RIBOZIMI = RNA con attività catalitica) che sono strutturalmente suddivise in due classi:
 ENZIMI Gli ENZIMI sono proteine (eccezioni: RIBOZIMI = RNA con attività catalitica) che sono strutturalmente suddivise in due classi: PROTEINE SEMPLICI (costituite solo dalla parte di natura proteica)
ENZIMI Gli ENZIMI sono proteine (eccezioni: RIBOZIMI = RNA con attività catalitica) che sono strutturalmente suddivise in due classi: PROTEINE SEMPLICI (costituite solo dalla parte di natura proteica)
Regolazione della Glicolisi
 Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A
 1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
La cinetica chimica. Velocità media di reazione
 La cinetica chimica 1. Velocità di reazione. Leggi cinetiche semplici 3. Meccanismi di reazione 4. Effetto della temperatura: legge di Arrhenius e teoria del complesso attivato 5. Catalizzatori Velocità
La cinetica chimica 1. Velocità di reazione. Leggi cinetiche semplici 3. Meccanismi di reazione 4. Effetto della temperatura: legge di Arrhenius e teoria del complesso attivato 5. Catalizzatori Velocità
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
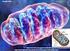 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Utilizzo del glucosio: la glicolisi
 Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Capitolo 5 L energia e il trasporto
 Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
Affinità ed efficacia
 Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
CINETICA CHIMICA. ChimicaGenerale_lezione21 1
 CINETICA CHIMICA La cinetica chimica è lo studio della velocità delle reazioni chimiche, cioè della variazione delle concentrazione dei reagenti (o dei prodotti) in funzione del tempo. ChimicaGenerale_lezione21
CINETICA CHIMICA La cinetica chimica è lo studio della velocità delle reazioni chimiche, cioè della variazione delle concentrazione dei reagenti (o dei prodotti) in funzione del tempo. ChimicaGenerale_lezione21
delle curve isoterme dell anidride carbonica
 COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Introduzione al Metabolismo
 Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
relazioni tra il calore e le altre forme di energia.
 Termodinamica i Termodinamica: ramo della scienza che studia le relazioni tra il calore e le altre forme di energia. Sistema e ambiente sistema: zona dello spazio all interno della quale studiamo i fenomeni
Termodinamica i Termodinamica: ramo della scienza che studia le relazioni tra il calore e le altre forme di energia. Sistema e ambiente sistema: zona dello spazio all interno della quale studiamo i fenomeni
Il metabolismo cellulare
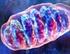 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO
 L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A
 Università di Roma Tor Vergata Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A. 2012-2013 1 Composizione chimica dell atmosfera Oltre ad O 2 e N
Università di Roma Tor Vergata Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A. 2012-2013 1 Composizione chimica dell atmosfera Oltre ad O 2 e N
Legge dell azione di massa. Misura sperimentale della costante di equilibrio. Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Legge dell azione di massa Il caso dei gas: utilizziamo le pressioni parziali Lezione 7-8 1 Per definizione le concentrazioni
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Legge dell azione di massa Il caso dei gas: utilizziamo le pressioni parziali Lezione 7-8 1 Per definizione le concentrazioni
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Appendice cap. 29: applicazioni
 2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
La quantità di glu presente nei liquidi extracellulari è di circa 20g, 80kcal.
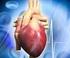 I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Le reazioni chimiche biologiche e gli enzimi
 Le reazioni chimiche biologiche e gli enzimi LEZIONE NR. 6 - PSICOBIOLOGIA Le reazioni chimiche consistono in interazioni interatomiche che si svolgono a livello dei loro orbitali, e quindi differenti
Le reazioni chimiche biologiche e gli enzimi LEZIONE NR. 6 - PSICOBIOLOGIA Le reazioni chimiche consistono in interazioni interatomiche che si svolgono a livello dei loro orbitali, e quindi differenti
L elasticità e le sue applicazioni in economia Introduzione
 L elasticità e le sue applicazioni in economia Introduzione Fino ad ora l analisi su domanda, offerta ed equilibrio di mercato è stata di tipo qualitativo. Se vogliamo avere una misura quantitativa degli
L elasticità e le sue applicazioni in economia Introduzione Fino ad ora l analisi su domanda, offerta ed equilibrio di mercato è stata di tipo qualitativo. Se vogliamo avere una misura quantitativa degli
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici
 La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
- Equilibri omogenei: tutte le sostanze che partecipano alla reazione fanno parte della stessa fase:
 ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
Equilibri chimici. Consideriamo la seg. reazione chimica in fase omogenea: aa + bb î cc + dd Definiamo, in ogni istante della reazione:
 Equilibri chimici Consideriamo la seg. reazione chimica in fase omogenea: aa + bb î cc + dd Definiamo, in ogni istante della reazione: con A, B, C, D espressi come concentrazioni molari. Il sistema si
Equilibri chimici Consideriamo la seg. reazione chimica in fase omogenea: aa + bb î cc + dd Definiamo, in ogni istante della reazione: con A, B, C, D espressi come concentrazioni molari. Il sistema si
