Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
|
|
|
- Giorgia Monti
- 6 anni fa
- Visualizzazioni
Transcript
1 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi) Aria. E costituita dal 78% di N2 solvente gas e dal 21% di O2 soluto gas Esempio ottone (rame e zinco); oppure acciaio (ferro e carbonio, come anche la ghisa). L acciaio è più resistente del ferro. Il soluto può essere gassoso (CO2 acqua minerale), liquido (soluzioni alcoliche), solido (sale o zucchero). Soluto e solvente non sono riconoscibili tra loro, nemmeno al microscopio. Al contrario, quando sono riconoscibili, si parla di sospensioni, in cui il soluto ha dimensioni maggiori a 1000nm. In tal caso soluto e solvente si possono separare per semplice filtrazione. Una soluzione colloidale, invece, è caratterizzata da una grandezza intermedia delle particelle di soluto (tra 1 e 1000 nm), come la panna, le polveri, il fumo. Si riconoscono per l effetto Tyndall (deviazioni laterali dei raggi di luce che le attraversano). CRITERI DI SOLUBILITA : il simile scioglie il simile SOLUTO è il componente presente in quantità minore. Può essere ionico, come il sale da cucina; polare, come l alcool o l acido fluoridrico oppure apolare, come il grasso. SOLVENTE è il componente presente in quantità maggiore. Può essere polare, come l acqua o apolare, come la benzina. La legge di solubilità afferma che il simile scioglie il simile, dunque soluti ionici o polari sono solubili nei solventi polari come l acqua. In effetti in acqua è possibile sciogliere sali o zuccheri. Soluti apolari come l olio sono solubili nei solventi apolari come la benzina. La solubilità delle diverse sostanze, inoltre, aumenta con l aumentare della temperatura. Una soluzione si dice satura quando contiene la quantità massima di soluto, una soluzione è soprassatura quando il soluto è presente come corpo di fondo. Pag. 1
2 SOLUTI IONICI (sale) POLARI (saccarosio) APOLARI (olio) SOLVENTI POLARI (acqua) POLARI (acqua) APOLARI (benzina) SOLUTI IONICI-SOLVENTI POLARI Lo ione Na + quando viene sciolto in acqua viene circondato da molecole d acqua con la parte negativa della molecola d acqua rivolto vero lo ione Na + e la parte positiva della molecola rivolta verso lo ione Cl -. Le interazioni che si creano sono di tipo ione-dipolo (collegamento-legami). SOLUTI IONICI-SOLVENTI POLARI Nella figura in 3D si osserva lo ione Cl - in verde, circondato da molecole di acqua rivolte con la parte positiva (H + ) verso lo ione negativo (Cl - ). Lo ione Na +, in grigio (sopra), appare invece circondato da molecole d acqua rivolte con l ossigeno (parte negativa del dipolo) verso di esso. Le interazioni che si creano sono di tipo ione-dipolo (collegamento-legami). SOLUTI POLARI DISCIOLTI IN SOLVENTI POLARI Anche l alcol è solubile in H2O, poiché si creano interazioni dipolo- dipolo. Si tratta sempre di attrazioni tra cariche opposte simili a quelle dei poli magnetici. Nella figura l atomo verde è di fluoro (parte negativa), l atomo bianco di idrogeno (parte positiva) e si affacciano sempre come in figura. Si creano interazioni dipolodipolo (legami di van der Waals: collegamento-legami). Pag. 2
3 SOLUTI APOLARI Essendo gli idrocarburi, come i grassi, costituiti in gran parte da molecole apolari, non si possono stabilire con l acqua delle interazioni elettrostatiche e i due componenti restano separati. La figura mostra un idrocarburo, costituito solo da carbonio (azzurro) e idrogeno (bianco) e fa vedere che non ci sono interazioni con l acqua. Solubilità: quantità di soluto che può essere sciolta in 100 g di sovente (a temp=20 C e pressione=1 atm) Solventi polari (H2O) Solubili Insolubili Ossidi (sia acidi che basici) Acidi (tutti HA-> H + +A - ) Idrossidi (quasi tutti MeOH->Me + +OH - ) Idrossidi di metalli pesanti e di Ca 2+, Sr 2+ Sali (CA->C + +A - ) Eccezioni Alogenuri di Ag +, Hg ++, Pb ++ Solfuri _S 2- Carbonati _CO 3 2- Fosfati _PO 4 3- Cromati_CrO 4 - Sali di ammonio NH 4 + Solfati (SO 4 2- ) di Ca 2+, Ba 2+, Sr 2+, Pb 2+ Pag. 3
4 METODI PER ESPRIMERE LA CONCENTRAZIONE DELLE SOLUZIONI Alcune caratteristiche delle soluzioni sono diverse da quelle del solvente puro e dipendono dalla concentrazione di esse (proprietà colligative). Tra queste sono molto importanti l innalzamanto ebullioscopico (ATe= K eb m, dove K eb = dipende dal solvente, per l acqua è pari a 0,51kg/moli e m= molalità) e l abbassamento del punto crioscopico (A T= K c m, dove m= molalità e k c dipende dal solvente, per l acqua è 1,86). Pertanto è fondamentale saper esprimere la concentrazione delle soluzioni. Metodi Fisici Per prepararle occorre la bilancia. %P = 100 Per prepararle occorre il cilindro graduato %V = = 100 %P/V = 100 D = Per prepararle occorrono sia il contenitore graduato che la bilancia Massa e volume si riferiscono solo alla soluzione e non al soluto Dalla percentuale del peso, riesco a trovare la percentuale P/V della soluzione con la sola formula %P D = % P/V Metodi Chimici M = = l -1 N = = M = l -1 Mol = = Kg -1 Pag. 4
5 X = X = frazione molare Altre formule risolutive M= = mol = DILUIZIONI: Nelle diluizioni con solo acqua il numero di moli di soluto non varia, poiché in effetti aggiungo solo il solvente. La nuova concentrazione molari sarà dunque data dal M=numero di moli della soluzione concentrata/ volume totale (V1+V2) Vale comunque la regola che Ma Va = Mb Vb Se invece mescolo due soluzioni a concentrazione diversa la concentrazione molare sarà data dal rapporto tra la somma delle moli e la somma dei volumi (n1+n2/v1+v2. Se ho le molarità anziche il numero di moli, si può applicare la formula M= ESERCIZI: A)Ho a disposizione 125ml una soluzione di NaOH 0,25M. Calcolare la molarità se porto il volume a 200 ml. V a = 125 ml M a = 0,25 l V b = 200 ml M b =? M a V a = M b V b Pag. 5
6 M b = formula risolutiva M b = = 0,156 l -1 B) Calcola la molarità di una soluzione in cui 25 g H 2 SO 4 sono stati sciolti in 300 ml di soluzione. m H 2 SO 4 = 25,5 g V S = 300 ml M=? M = = = 0,87 l -1 formula risolutiva C)Una soluzione viene ottenuta solubilizzando 1,005g di acido citrico in 50 ml m C 6 H 8 O 7 = 1,005 g VS = 50 ml %P/V=? M =? % p/v = 100 = formula risolutiva M = = 0,1 l -1 formula risolutiva Pag. 6
Soluzioni unità 3, modulo D del libro
 Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti
 LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
Le soluzioni e la loro concentrazione
 Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Le soluzioni e il loro comportamento
 A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Esercizi Concentrazioni e diluizioni
 Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei
 Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
Espressioni di concentrazione di una soluzione
 SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
Le soluzioni. A cura della Prof. ssa Barone Antonina
 Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Classificazione della materia
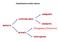 Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
solvente soluto concentrazione
 Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
LA FORMAZIONE DELLE SOLUZIONI.
 LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 41 2009 Solubilità Diapositiva della prof. Nadia Lotti Solubilità Stabilite le condizioni di equilibrio di una soluzione
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 41 2009 Solubilità Diapositiva della prof. Nadia Lotti Solubilità Stabilite le condizioni di equilibrio di una soluzione
Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea.
 Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE
 SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
Calcoli stechiometrici in soluzione (Cap. 12)
 Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
ESERCIZI sulle SOLUZIONI
 ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
solvente soluto concentrazione
 Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
STATO LIQUIDO. Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso
 STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
Soluzioni e Concentrazione
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione Prof. Dipartimento CMIC Giulio Natta https://corsi.chem.polimi.it/citterio/default.htm
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione Prof. Dipartimento CMIC Giulio Natta https://corsi.chem.polimi.it/citterio/default.htm
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 12 Aprile 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
Soluzioni semplici. Soluzioni liquide
 Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ
 LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
N.B. Indicare i passaggi dei calcoli
 Corso Corso di di Laurea Laurea in in Fisica ca COMPITO N 3 DA CONSEGNARE ENTRO IL 11/12/09 Cognome Nome(*)....N di Matricola (*) scrivere in stampatello N.B. Indicare i passaggi dei calcoli 1. Il cloro
Corso Corso di di Laurea Laurea in in Fisica ca COMPITO N 3 DA CONSEGNARE ENTRO IL 11/12/09 Cognome Nome(*)....N di Matricola (*) scrivere in stampatello N.B. Indicare i passaggi dei calcoli 1. Il cloro
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato liquido
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni
 2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
Chimica: Studio della materia e delle sue interazioni.
 Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Capitolo 15 Le proprietà delle soluzioni
 Capitolo 15 Le proprietà delle soluzioni Hai capito? pag. 354 Alle forze di London presenti fra le molecole di soluto se ne sostituiscono di nuove fra le molecole di soluto e solvente. pag. 356 A 0,4%
Capitolo 15 Le proprietà delle soluzioni Hai capito? pag. 354 Alle forze di London presenti fra le molecole di soluto se ne sostituiscono di nuove fra le molecole di soluto e solvente. pag. 356 A 0,4%
CARATTERISTICHE. In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee.
 In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
dispersioni omogenee di due o più specie chimiche l una nell altra
 Soluzioni : dispersioni omogenee di due o più specie chimiche l una nell altra Solvente : componente che si trova nel medesimo stato fisico della soluzione componente che si trova in quantità maggiore
Soluzioni : dispersioni omogenee di due o più specie chimiche l una nell altra Solvente : componente che si trova nel medesimo stato fisico della soluzione componente che si trova in quantità maggiore
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
-SOLUZIONE- In una soluzione liquida si possono distinguere un solvente (il componente liquido più abbondante) e uno o più soluti.
 -SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
-SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
ESERCIZI ESERCIZI. del componente i-esimo di un miscela è definita come: a. χ i. 1) La frazione molare χ i. /n t b. χ i. = n i. /m t c. χ i. /V d.
 1) La frazione molare χ i del componente i-esimo di un miscela è definita come: a. χ i = n i /n t b. χ i = n i /m t c. χ i = n i /V d. χ i = m i /m t con n i = numero di moli del componente i-esimo n t
1) La frazione molare χ i del componente i-esimo di un miscela è definita come: a. χ i = n i /n t b. χ i = n i /m t c. χ i = n i /V d. χ i = m i /m t con n i = numero di moli del componente i-esimo n t
Relazione giorno 4 Febbraio 2011
 Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Proprietà colligative
 Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
PROPRIETÁ DEI LIQUIDI
 PROPRIETÁ DEI LIQUIDI Viscosità: resistenza di un fluido al flusso, ossia scorrimento relativo delle molecole Una semplice misura (indiretta) è il tempo di efflusso di un dato volume di liquido attraverso
PROPRIETÁ DEI LIQUIDI Viscosità: resistenza di un fluido al flusso, ossia scorrimento relativo delle molecole Una semplice misura (indiretta) è il tempo di efflusso di un dato volume di liquido attraverso
REGISTRO DELLE LEZIONI 2004/2005. Tipologia. Addì Tipologia. Addì Tipologia
 Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
LE PROPRIETÀ DELLE SOLUZIONI
 LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
PROVA 1. Dati i composti con formula HI e NaNO 2 :
 PROVA 1 Dati i composti con formula HI e NaNO 2 : 1) Denominare i composti 2) Determinare le valenze o i numeri di ossidazione di tutti gli elementi nei due composti 3) Indicare quale legame esiste per
PROVA 1 Dati i composti con formula HI e NaNO 2 : 1) Denominare i composti 2) Determinare le valenze o i numeri di ossidazione di tutti gli elementi nei due composti 3) Indicare quale legame esiste per
satura SOLUZIONE concentrata diluita MISCUGLIO ETEROGENEO Sospensione (acqua e polvere di marmo) Miscuglio solido (es. sabbia)
 MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
Esame (0) classei - Codice Prova:
 1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
ESERCIZI SU. le soluzioni e la loro composizione
 ESERCIZI SU le soluzioni e la loro composizione martedì 15 dicembre 2015 Composizione delle soluzioni definita da grandezze di primario interesse fisico Composizione percentuale in massa % di A = (m A
ESERCIZI SU le soluzioni e la loro composizione martedì 15 dicembre 2015 Composizione delle soluzioni definita da grandezze di primario interesse fisico Composizione percentuale in massa % di A = (m A
Stechiometria delle soluzioni
 www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
LEGAMI INTERMOLECOLARI LEGAMI INTERMOLECOLARI
 I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
I MISCUGLI OMOGENEI ED ETEROGENEI
 I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
 DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
NELLA LEZIONE DI OGGI:
 ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
PROPRIETÀ TIPICHE DEI LIQUIDI
 STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
Esercizi su Cambiamenti di Stato
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi su Cambiamenti di Stato Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi su Cambiamenti di Stato Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
soluzione acquosa di HCl al 37% in peso è una soluzione contenente 37g di HCl ogni 100g di soluzione. ESERCIZIO 1 soluzione.
 SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti SOLVENTE componente presente in maggiore quantità SOLUTO componente presente in minore quantità DENSITA di una soluzione:
SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti SOLVENTE componente presente in maggiore quantità SOLUTO componente presente in minore quantità DENSITA di una soluzione:
CONCENTRAZIONE. Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono.
 1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
Classificazione chimica della materia
 Classificazione chimica della materia sostanze (o specie chimiche) sistemi ad un componente specie elementari costituite da atomi dello stesso elemento argento, zolfo, ossigeno, idrogeno composti costituiti
Classificazione chimica della materia sostanze (o specie chimiche) sistemi ad un componente specie elementari costituite da atomi dello stesso elemento argento, zolfo, ossigeno, idrogeno composti costituiti
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Soluzioni, Acidi e Basi
 Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Soluzione Per una miscela di due liquidi
 Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
La Concentrazione. C i = m i / M,
 La Concentrazione La concentrazione, C i, di un composto chimico i all interno di un sistema a più componenti, definisce il rapporto C i = m i / M, dove m i è la massa di i e M = ( i m i ) è la massa totale
La Concentrazione La concentrazione, C i, di un composto chimico i all interno di un sistema a più componenti, definisce il rapporto C i = m i / M, dove m i è la massa di i e M = ( i m i ) è la massa totale
Miscela di gas 1, 2 e 3. P 1 = n1 R T P 2 = n2 R T P 3 = n3 R T V V V. Pressioni parziali dei gas P 1 P 2 P 3
 Miscele di gas Pressione parziale di un gas in una miscela gassosa: pressione esercitata da un componente della miscela se occupasse da solo l intero volume a disposizione della miscela.(legge di DALTON)
Miscele di gas Pressione parziale di un gas in una miscela gassosa: pressione esercitata da un componente della miscela se occupasse da solo l intero volume a disposizione della miscela.(legge di DALTON)
Il binomio di van t Hoff Le proprietà colligative dipendono dal numero di particelle effettivamente presenti nella soluzione. Nel caso in cui il solut
 Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Miscibilità parziale
 Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
Chimica: Studio della materia e delle sue interazioni.
 Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Concentrazione delle Soluzioni
 Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
2. La concentrazione La quantità di soluto contenuto in una determinata quantità di soluzione (o in alcuni casi di
 LE SOLUZIONI E LA CONCENTRAZIONE 1. Generalità e concetto di solubilità Una soluzione è un sistema omogeneo costituito da due o più componenti. Le soluzioni possono essere solide, liquide o gassose. Sono
LE SOLUZIONI E LA CONCENTRAZIONE 1. Generalità e concetto di solubilità Una soluzione è un sistema omogeneo costituito da due o più componenti. Le soluzioni possono essere solide, liquide o gassose. Sono
-PROPRIETA COLLIGATIVE-
 -PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
-PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
Rapporto tra soluto e solvente o soluzione
 Rapporto tra soluto e solvente o soluzione Dissoluzione delle sostanze Concentrazione espressa in unità chimiche : Molarità Frazione molare Concentrazione espressa in unità fisiche : Percentuale in
Rapporto tra soluto e solvente o soluzione Dissoluzione delle sostanze Concentrazione espressa in unità chimiche : Molarità Frazione molare Concentrazione espressa in unità fisiche : Percentuale in
Test di approfondimento
 Test di approfondimento 1 In 100 ml di una soluzione 2 M sono presenti 6 grammi di soluto. Qual è il peso molecolare del soluto in u.m.a.? A 3 B 12 30 D 120 E 60 2 Attraverso una membrana semipermeabile
Test di approfondimento 1 In 100 ml di una soluzione 2 M sono presenti 6 grammi di soluto. Qual è il peso molecolare del soluto in u.m.a.? A 3 B 12 30 D 120 E 60 2 Attraverso una membrana semipermeabile
1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)?
 1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)? A. ai legami ad idrogeno tra gli atomi di mercurio B. alle interazioni tipo London tra gli atomi di mercurio C.
1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)? A. ai legami ad idrogeno tra gli atomi di mercurio B. alle interazioni tipo London tra gli atomi di mercurio C.
Soluzioni e Concentrazione (cap. 4)
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione (cap. 4) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione (cap. 4) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Esame di Chimica Generale 20 Aprile 2011
 Esame di Chimica Generale 20 Aprile 2011 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 20 Aprile 2011 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
PROPRIETA DELLE SOLUZIONI ACQUOSE. Prof.ssa Patrizia Gallucci
 PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
Undicesima unità didattica. I liquidi e le soluzioni
 Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
LICEO SCIENTIFICO STATALE Nicola Sensale NOCERA INFERIORE (SA)
 1. 14,0 g di azoto puro (N 2) sono costituiti da un numero di molecole uguale a: A) 6,02 10 23 B) 3,01 10 23 C) 1,20 10 24 D) lo stesso numero di particelle contenute in 12,0 g di 12 C 2 Un recipiente
1. 14,0 g di azoto puro (N 2) sono costituiti da un numero di molecole uguale a: A) 6,02 10 23 B) 3,01 10 23 C) 1,20 10 24 D) lo stesso numero di particelle contenute in 12,0 g di 12 C 2 Un recipiente
ATTIVITA' ESTIVA 3ASA
 ATTIVITA' ESTIVA 3ASA PROBLEMI STECHIOMETRIA 1) Nella reazione chimica AsF 3 + C 2 Cl 6 AsCl 3 + C 2 Cl 2 F 4 la resa teorica di C 2 Cl 2 F 4 è stata calcolata in 1,86 mol. Se la resa in percentuale della
ATTIVITA' ESTIVA 3ASA PROBLEMI STECHIOMETRIA 1) Nella reazione chimica AsF 3 + C 2 Cl 6 AsCl 3 + C 2 Cl 2 F 4 la resa teorica di C 2 Cl 2 F 4 è stata calcolata in 1,86 mol. Se la resa in percentuale della
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: H 2 S (aq) + NO 3
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 (aq) + N 3 (aq) + + (aq) (s) + N (g) + 2 (l). Calcolare i grammi di (s) ed il volume di N (g) a 25 C ed 1
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 (aq) + N 3 (aq) + + (aq) (s) + N (g) + 2 (l). Calcolare i grammi di (s) ed il volume di N (g) a 25 C ed 1
