REPORT HTA REGIONALE. Decisioni CTR Data riunione: 20/02/2012 Decisione: Inserito fd CARATTERISTICHE DEL PRODOTTO
|
|
|
- Gildo Ippolito
- 8 anni fa
- Visualizzazioni
Transcript
1 REPORT HTA REGIONALE Decisioni CTR Data riunione: 20/02/2012 Decisione: Inserito fd CARATTERISTICHE DEL PRODOTTO PRINCIPIO ATTIVO: PLERIXAFOR NOME COMMERCIALE: MOZOBIL DITTA PRODUTTRICE: GENZYME FORMULAZIONE: 1 flaconcino 24mg/1,2 ml Prezzo: ,03 ATC: L03AX16 CATEGORIA TERPAEUTICA: Altri immunostimolanti CLASSE: H osp REGISTRO AIFA: SI ONCOLOGICI Criteri di eleggibilità: diagnosi di linfoma / mieloma multiplo paziente candidato a trapianto di cellule staminali ematopoietiche che ha fallito almeno un tentativo di mobilizzazione efficace con adeguato dosaggio di GCSF somministrato dopo pretrattamento con G-CSF (10 µg/kg una volta al giorno per almeno 4 giorni consecutivi MODALITA PRESCRITTIVE: farmaco ospedaliero INDICAZIONE MINISTERIALE: in combinazione con G-CSF per incrementare la mobilizzazione delle cellule staminali ematopoietiche al sangue periferico per la raccolta e il conseguente trapianto autologo in pazienti con linfoma e mieloma multiplo con una scarsa mobilizzazione cellulare DATA REGISTRAZIONE EMA: 31/07/2009 NOTE: farmaco orfano. Incluso nell elenco farmaci rimborsati dal SSN secondo la legge 648/ 96 (escluso da tale lista da gennaio 2012). Incluso nell elenco dei farmaci innovativi dell AIFA (secondo l accordo stato-regioni 28 novembre 2010) REGISTRAZIONE FDA: si DATA REGISTRAZIONE FDA : 15/12/2008 DATA AIC: 25/11/2010 1
2 MECCANISMO D AZIONE E POSOLOGIA Plerixafor è un derivato del biciclam, un antagonista reversibile selettivo del recettore di chemochine CXCR4 in grado di bloccare il legame del suo legante affine, il fattore derivato dalle cellule stromali 1α (SDF-1α), definito anche CXCL12 [1]. La leucocitosi e gli incrementi nei livelli di cellule progenitrici ematopoietiche in circolazione indotti dal plerixafor si ritengono un risultato della rottura del legame del CXCR4 con il suo legante affine, con la conseguente comparsa di cellule pluripotenti e mature nella circolazione sistemica. Le cellule CD34+ mobilizzate dal plerixafor sono funzionali e in grado di attecchire con una capacità di ripopolamento a lungo termine. La terapia con plerixafor deve essere iniziata e supervisionata da un medico esperto in oncologia e/o ematologia. Le procedure di mobilizzazione e aferesi devono essere eseguite in collaborazione con un centro oncologico-ematologico con un esperienza soddisfacente in questo campo e in cui il monitoraggio delle cellule progenitrici ematopoietiche possa essere realizzato correttamente. La dose raccomandata è 0,24 mg/kg di peso corporeo/die. Deve essere somministrato mediante iniezione sottocutanea da 6 a 11 ore prima dell inizio dell aferesi dopo 4 giorni di pretrattamento con il fattore stimolante le colonie dei granulociti (G-CSF). Negli studi clinici, plerixafor è stato comunemente utilizzato per un periodo compreso tra 2 e 4 giorni consecutivi (e fino a 7). ALTERNATIVE DISPONIBILI Si tratta di un farmaco orfano che non presenta alternative della medesima classe terapeutica. Per la mobilizzazione delle cellule staminali ematopoietiche vengono utilizzati i fattori stimolanti le colonie (G- CSF: filgrastim, pegfilgrastim e lenograstim) da soli o in associazione a chemioterapia (generalmente ciclofosfamide), tuttavia il plerixafor non può considerarsi un alternativa ai G-CSF in quanto viene utilizzato in associazione agli stessi e nei pazienti che abbiano già fallito almeno un tentativo di mobilizzazione con un dosaggio adeguato di G-CSF. INQUADRAMENTO DELLA PATOLOGIA I pazienti con linfoma non-hodgkin (LNH) o con mieloma multiplo (MM) possono essere trattati con chemioterapia ad alte dosi, che è mielosoppressiva o mieloablativa e richiede reinfusione di cellule staminali ematopoietiche (CSE) per ripopolare il midollo osseo e rigenerare le cellule del sangue (globuli rossi, piastrine, neutrofili) [2]. Le CSE utilizzate per il trapianto possono essere raccolte dal midollo osseo, dal sangue del cordone ombelicale o dal sangue periferico, e il trapianto può essere autologo (dal paziente) o allogenico (da donatore). Nel caso di trapianto autologo, l'uso di sangue periferico come fonte di CSE è preferito rispetto al midollo osseo a causa della facilità di raccolta e della minore probabilità di contaminazione con cellule tumorali. Durante lo steady-state i livelli omeostatici di cellule staminali nella circolazione periferica sono bassi, con una conta di CD cellule / ml e pertanto, le cellule hanno bisogno di essere "mobilizzate" dal midollo osseo, dove normalmente risiedono, nel sangue periferico. Tale mobilizzazione può essere realizzata mediante il trattamento con citochine (di solito G-CSF), o chemochine, da sole o in combinazione a chemioterapia. Il numero minimo di cellule CD34 + necessarie per il successo del trapianto autologo è considerato cellule / kg. Il picco di mobilizzazione dopo il G-CSF da solo si presenta solitamente 4 o 5 giorni dopo l'inizio della terapia, mentre la mobilitazione in seguito di diversi regimi di chemioterapia generalmente si verifica da 7 a 14 giorni dopo la somministrazione dell'ultima dose di chemioterapia. Una significativa percentuale di pazienti può non essere in grado di mobilizzare un 2
3 numero sufficiente di cellule bersaglio per il trapianto con gli attuali regimi di mobilizzazione e questi pazienti richiedono più mobilizzazioni, aumentando così i costi associati ed il rischio di progressione della malattia tra i tentativi di mobilitazione. LINEE GUIDA DI TRATTAMENTO ESISTENTI Una review del 2009 [3] fa un excursus sulle strategie per il miglioramento della mobilizzazione delle cellule staminali nel trapianto autologo. Da tale pubblicazione emerge che la mobilizzazione con sole citochine, generalmente G-CSF, è generalmente ben tollerata, ma che tuttavia tale approccio è limitato dalla quantità di cellule CD34+ raccolte, che risulta spesso insufficiente per il trapianto, con necessità quindi di numerose sessioni di aferesi. Un ulteriore approccio è rappresentato dalla combinazione di citochine e agenti chemioterapici (es. ciclofosfamide, paclitaxel, etoposide): questa strategia incrementa il numero di cellule raccolte a discapito però di un aumento della tossicità e delle risorse utilizzate. Secondo gli autori non esiste una strategia di mobilizzazione che possa considerarsi standard, anche se risulta preferibile considerare come primo approccio l utilizzo di G-CSF da solo, che, soprattutto nei pazienti con MM, si è dimostrato spesso sufficiente. Nei pazienti con LNH e LH la mobilizzazione con solo G-CSF si è dimostrata fallimentare nel 23% dei casi e per questi pazienti si rende necessario regimi che includano agenti chemioterapici o nuovi farmaci tra cui il plerixafor. Tuttavia una percentuale di pazienti variabile tra il 5% e il 30% fallisce tutte le strategie di mobilizzazione. Nella revisione vengono descritti anche gli studi registrativi e i programmi di uso compassionevole di plerixafor e gli autori concludono affermando che si tratta di una nuova strategia che può incrementare la percentuale di successo soprattutto nei pazienti cattivi mobilizzatori. Le linee guida sulla raccolta delle cellule staminali del gruppo di lavoro internazionale sul mieloma [4] descrivono i vantaggi e i limiti delle strategie ad oggi utilizzate per la mobilizzazione. Secondo tali linee guida l obiettivo della mobilizzazione è la raccolta di almeno 2 milioni di cellule CD34+ / kg, anche se la dose ottimale sarebbe di 4-6 milioni CD34+/kg. Le strategie raccomandate sono le seguenti: filgrastim come agente singolo: i vantaggi sono rappresentati dalla facilità di utilizzo, dai costi relativamente bassi, da una percentuale di successo >80% e dalla buona tollerabilità. Lo svantaggio è il basso numero di CD34+ raccolte. Si tratta del gold standard corrente. Filgrastim + ciclofosfamide: si tratta della più comune strategia di chemiomobilizzazione, con risultati prevedibili e ben tollerata. Tuttavia la ciclofosfamide presenta problemi di tossicità ai dosaggi >4g/m 2, con rischio di citopenia e infezioni. Inoltre i costi aumentano. Filgrastim + chemioterapia di combinazione: questa strategia può essere praticata solo in alcuni centri specializzati e per pazienti con malattia in stato molto avanzato, vi è infatti un elevato rischio di tossicità, un aumento dei costi e possibili ritardi dell eventuale trapianto. Le linee guida individuano dei fattori di rischio che consentono di prevedere quali possono essere i pazienti cattivi mobilizzatori e suggeriscono delle strategie terapeutiche per questi pazienti: Pazienti di età superiore a 60 anni: la raccomandazione è di considerare la mobilizzazione con plerixafor. Esposizione a melphalan: considerare anticipatamente la chemiomobilizzazione o plerixafor. 3
4 Precedenti fallimenti terapeutici: considerare anticipatamente la chemiomobilizzazione o plerixafor. Pazienti che hanno subito numerose sessioni di radioterapia al midollo osseo: considerare anticipatamente la chemiomobilizzazione o plerixafor. Relativamente a plerixafor le linee guida suggeriscono la necessità di ulteriori studi che permettano di definire meglio il suo ruolo nel trattamento del MM. Questi studi dovrebbero prevedere anche endpoint farmacoeconomici e di consumo di risorse. ANALISI DEGLI STUDI CLINICI DATI DI EFFICACIA Due RCT in doppio cieco di fase III hanno confrontato l'efficacia di plerixafor versus placebo in 298 pazienti con linfoma non Hodgkin (LNH) [5] e 302 pazienti con mieloma multiplo (MM) [6]. In entrambi gli studi, i pazienti di età >18 anni, avevano una diagnosi confermata da biopsia, ECOG performance status di 0 o 1. Sono stati invece esclusi i pazienti che avevano già ricevuto un trapianto autologo o allogenico precedente e quelli che avevano avuto precedenti tentativi di raccolta di cellule staminali. Pertanto gli studi registrativi hanno arruolato pazienti con caratteristiche diverse rispetto a quelle per le quali AIFA lo ha limitati (solo pazienti che abbiano già fallito almeno un tentativo di mobilizzazione con G-CSF). Il trattamento è stato iniziato con G-CSF 10mcg/kg/die per un massimo di otto giorni. Dopo quattro giorni, i pazienti randomizzati hanno ricevuto plerixafor sottocute 240 mcg / kg oppure placebo, la sera prima di ogni giornata di aferesi. I pazienti hanno continuato l aferesi per un massimo di quattro giorni fino alla raccolta di 5 x 10 6 cellule CD34 + / kg nello studio che ha arruolato pazienti con LNH e fino alla raccolta di 6 x 10 6 cellule CD34 + / kg per un massimo di 2 giorni nello studio che ha arruolato pazienti con MM. Era previsto un protocollo di salvataggio in entrambi gli studi per i pazienti che avevano fallito la mobilizzazione di sufficienti cellule CD34 +. Dopo un periodo di riposo di almeno sette giorni, i pazienti sono stati trattati in aperto con plerixafor e G-CSF per un massimo di quattro giorni o fino a quando erano state raccolte 5 x 10 6 cellule CD34 + / kg. L'endpoint primario era la proporzione di pazienti che raggiungevano l'obiettivo numerico di cellule CD34 + entro il numero predefinito di sessioni aferesi per ogni studio (massimo 4 giorni nello studio su pazienti con LNH e 2 giorni nello studio MM). Un obiettivo specifico per l EMA [2] era un endpoint composito che comprendeva l'obiettivo numerico di cellule CD34+ (raccolta di almeno 6X10 6 CD34+ nei pazienti con MM e di 2X10 6 CD34+ nei pazienti con LNH) e la riuscita dell attecchimento delle cellule polimorfonucleate (PMN) e delle piastrine (PLT). Nello studio su pazienti con LNH, una percentuale significativamente maggiore di pazienti del gruppo plerixafor, il 59.3% (89/150), rispetto al gruppo placebo, 19.6% (29/148), ha raggiunto l'endpoint primario (raccolta di almeno 5 x 10 6 cellule CD34 +/ kg in 4 giorni di aferesi). Inoltre una percentuale significativamente maggiore di pazienti nel gruppo plerixafor ha raggiunto anche l'endpoint specifico per EMA: l attecchimento dei PMN e PLT è stato raggiunto rispettivamente nell'84% e 57% dei pazienti trattati con plerixafor verso rispettivamente il 43% e il 19% dei pazienti del braccio di controllo. Nel gruppo plerixafor, il 90% dei pazienti è stato sottoposto a trapianto contro il 55% dei pazienti trattati con placebo. Dei 62 pazienti che sono stati inclusi nella procedura di salvataggio, 4 pazienti sui 10 del gruppo plerixafor hanno raggiunto l obiettivo di 2 x 10 6 cellule CD34 + / kg nei quattro giorni di aferesi, rispetto a 33 pazienti sui 52 del gruppo placebo. Nello studio su pazienti con MM, l'endpoint primario (raccolta di almeno 6 x 10 6 cellule CD34 + / kg in 2 giorni di aferesi), è stato raggiunto da una percentuale di pazienti significativamente maggiore nel gruppo plerixafor rispetto al placebo (71.6% e il 34.4% rispettivamente, p<0.001). Una percentuale significativamente maggiore di pazienti nel gruppo plerixafor ha raggiunto anche l'endpoint specifico per l EMA: il 70.3% dei pazienti del gruppo plerixafor verso il 34.4% del gruppo di 4
5 controllo. Il numero mediano di giorni di aferesi per la raccolta di 6 x 10 6 cellule CD34 + / kg è stato di 1 giorno nel gruppo plerixafor rispetto a 4 giorni nel gruppo di controllo (p<0.001). Nel gruppo plerixafor, il 95.9% dei pazienti ha proceduto al trapianto rispetto a 88.3% dei pazienti trattati con placebo. Il tempo medio all attecchimento è risultato simile nei gruppi placebo e plerixafor in entrambi gli studi, così come le percentuali di pazienti che ha mantenuto l attecchimento a 100 giorni, 6 e 12 mesi. Non c'è stata differenza tra i gruppi nella sopravvivenza globale. Sono stati pubblicati i risultati di due programmi di uso compassionevole (CUP) di plerixafor, uno svoltosi negli USA [7] e l altro, successivo al primo, in Europa [8]. I risultati di questi studi ci forniscono dati di efficacia importanti nel sottogruppo di pazienti per il farmaco è stato registrato in Europa, ossia coloro i quali abbiano fallito almeno un tentativo di mobilizzazione con G-CSF. La prima pubblicazione presenta i risultati di una coorte di 115 pazienti affetti da neoplasie ematologiche (mieloma multiplo, linfoma non Hodgkin e linfoma di Hodgkin), che non avevano risposto a mobilizzazione con chemioterapia o con G-CSF. In oltre il 66% dei pazienti trattati con G-CSF più plerixafor sono state raccolte almeno 2 x 10 6 CD34+/kg (60,3% dei pazienti con LNH, 71,4% dei pazienti con MM e il 76,6% dei pz con HL). Il tempo medio all attecchimento dei neutrofili è stato di 8 giorni e 11 giorni quello delle piastrine. Il CUP svoltosi in Europa ha permesso di raccogliere i dati di 56 pazienti arruolati in Spagna e UK: 32 affetti da mieloma multiplo e 24 da linfoma. I pazienti avevano fallito almeno un precedente tentativo di mobilizzazione, il 59% con chemioterapia e il restante 49% con G-CSF. L obiettivo primario era la raccolta di almeno 2 x 10 6 CD34+/kg, che è stato raggiunto dal 84% dei pazienti con MM e dal 63% dei pazienti con linfoma. Il tempo medio all attecchimento dei neutrofili è stato di 13.4 giorni e 18,5 giorni quello delle piastrine. Tabella 1(Appendice) DATI DI SICUREZZA Negli studi di fase III, l'incidenza di eventi avversi correlati al trattamento è stata più elevata nel gruppo plerixafor rispetto al placebo, il 65% versus il 41% nello studio su pazienti con LNH e il 65% versus il 45% nello studio su pazienti con MM [2]. Nello studio su pazienti con linfoma, tre pazienti hanno avuto un evento avverso grave correlato al trattamento, due nel gruppo plerixafor (un paziente con ipotensione e vertigini ed un paziente con trombocitopenia post-aferesi). I più comuni eventi avversi correlati al trattamento sono stati disturbi gastrointestinali (diarrea, rispettivamente nel 32% e 18% nei gruppi plerixafor rispetto al 4,1% e 5,3% nel gruppo placebo, nausea, nel 17% e 16% nei gruppi plerixafor e il 5,5% e 7,3% nel gruppo placebo) e reazioni al sito di iniezione (eritema, 29% e 20% nei gruppi plerixafor e il 6,9% e 3,3% nel gruppo placebo). Nella scientific discussion il CHMP dell EMA ha sottolineato che esiste un rischio teorico di mobilizzazione delle cellule tumorali nei pazienti con MM e linfoma. Al fine di valutare la rilevanza clinica di questo rischio l EMA ha richiesto i risultati del follow-up dei due studi di fase lll che sono stati estesi a cinque anni con la valutazione delle ricadute, della PFS e della sopravvivenza globale. Inoltre è stata richiesta la compilazione di un registro a lungo termine. STUDI IN CORSO Dal registro governativo americano [9] risultano 3 studi in corso di fase III o IV con plerixafor. Oltre ad uno studio di farmacocinetica, che intende confrontare il dosaggio fisso del farmaco rispetto al dosaggio variabile in base al peso corporeo in pazienti con LNH di peso inferiore a 70 kg, da segnalare un RCT di fase 5
6 III, in aperto, che vuole confrontare l efficacia di plerixafor + G-CSF verso solo G-CSF, in pazienti con MM nel raggiungimento della raccolta di almeno 5 X 10 6 CD34+, dopo un precedente trattamento con lenalidomide. Infine uno studio di fase IV, a singolo braccio, con l obiettivo di valutare l efficacia di plerixafor utilizzato come prima linea di trattamento in pazienti considerati potenziali cattivi mobilizzatori e l eventuale impatto economico di questa strategia, calcolato nel confronto con controlli storici. ALTRI REPORT DI HTA Il report dello Scottish Medicine Consortium [10] esprime parere favorevole al rimborso di plerixafor in Scozia in quanto il farmaco, in associazione a G-CSF, ha permesso che una percentuale significativamente maggiore di pazienti rispetto al placebo, raggiungesse il target di raccolta di cellule CD34+, sufficienti a consentire il trapianto autologo di cellule staminali. La ditta nella sua sottomissione ha proposto che l utilizzo del farmaco venga limitato in seconda linea di trattamento o successive. Il report riporta un analisi costo utilità sviluppata dalla ditta, in cui plerixafor è stato confrontato a G-CSF da solo o in associazione a ciclofosamide, in pazienti che avessero fallito almeno un tentativo di mobilizzazione. Nel base-case, nei pazienti con MM è stato calcolato un ICER di / QALY rispetto a G-CSF e di rispetto a G-CSF + ciclofosfamide. Nei pazienti con LNH l ICER è di / QALY nel confronto con G-CSF e di / QALY nel confronto con l associazione G-CSF e ciclofosfamide. Il rapporto costo-beneficio è stato considerato positivo nei pazienti con LNH, mentre nei pazienti con MM è stato considerato elevato ma comunque accettabile, trattandosi di un farmaco orfano che permette ad una percentuale superiore di pazienti di essere sottoposti ad un trattamento risolutivo come lo è il trapianto di cellule staminali. Il report dell HAS francese [11] esprime parere positivo al farmaco ed indica un miglioramento del beneficio clinico aggiuntivo (ASMR) di grado III (moderato). ANALISI ECONOMICHE STUDI DISPONIBILI In letteratura sono presenti diversi studi [12-15] ben sintetizzati da un review del 2011 [16] che hanno confrontato plerixafor vs le terapie standard. I lavori hanno mostrato una sostanziale uguaglianza tra il costo dei percorsi terapeutici, in quanto l utilizzo di plerixafor se da una parte comporta inevitabilmente un aumento del costo della terapia, d altra parte consente un risparmio della spesa sanitaria in virtù di un minor numero di fallimenti terapeutici e della minor durata delle ospedalizzazioni. I setting di questi studi sono diversi dal nostro e i pazienti presi in esame, visto anche il ristretto ambito terapeutico sono troppo poco numerosi per poter generalizzare i risultati e poter estenderli a diversi setting; inoltre anche gli autori della review evidenziano che i risultati non sono necessariamente traslabili a quelli che si avrebbero con la normale pratica clinica In tabella si sintetizzano solo gli studi pubblicati come articolo e non quelli presentati solo come abstract. Tabella 2(Appendice) 6
7 COSTO DEL PRODOTTO E DELLE ALTERNATIVE ED IMPATTO ORGANIZZATIVO Tabella prezzi farmaco e alternative: FARMACO PREZZO ALL OSPEDALE ( ) NOTE Plerixafor 1 flacone 24mg/1,2ml Filgrastim (Nivestim ) 1 sir 30 MU (300 mcg/0,5ml) Filgrastim (Granulokine ) 1 sir 30 MU (300 mcg/0,5ml) 5.649,44* 9,50 77,53 Payment by result: rimborso del costo di plerixafor in caso di fallimento terapeutico dopo almeno 2 somministrazioni. Solo il biosimilare presenta il prezzo da gara regionale (Nivestim prodotto aggiudicatario) mentre si considera l ex factory per l originator (non ha presentato offerte in sede di gara regionale) Lenograstim (Myelostim, Granocyte ) 1 sir 33,6 MU 63,00 Ciclofosfsamide fl da 500 mg fl da 1 g Citarabina 1 fl 1g 1 fl 2 g 2,27 5,99 14,32 28,03 FARMACO PREZZO ALL OSPEDALE ( ) NOTE Ifosfamide 11,92 1 fl 1g Epirubicina 1fl 50 mg 20,80 Etoposide 1 fl 10 ml, 20mg/ml 1 fl 50 ml, 20mg/ml 4,3 17,00 *prezzo ex factory + ulteriore sconto del 9.1% previsto dagli accordi con AIFA prezzo da gara regionale Costi comparativi: Le alternative a plerixafor sono i regimi di associazione di chemioterapia e G-CSF. Dal confronto con i clinici è risultato che i regimi chemioterapici utilizzati sono molto variabili, in tabella vengono riportati i costi di 7
8 alcuni di questi regimi, i dosaggi sono quelli suggeritici dagli stessi clinici. La durata della terapia con plerixafor è stata considerata variabile da 2 a 4 giorni (come da scheda tecnica). Il costo del trattamento con plerixafor è molto superiore rispetto alle alternative considerate: il trattamento con plerixafor varia infatti da circa ,00, qualora si consideri l associazione di plerixafor per due giorni di trattamento e filgrastim biosimilare, ad un massimo di ,00, quando si consideri l associazione di plerixafor per 4 giorni di trattameno associato a filgrastim originator. Le alternative variano da un costo di 215,00 dell associazione ciclofosfamide + filgrastim biosimilare ad un massimo di 1.732,00 dell associazione citarabina al dosaggio più alto e filgrastim originator. Da sottolineare che attualmente il DRG 404 relativo alla rimobilizzazione ha un valore in Veneto 1.682,28 e quindi non copre il costo di plerixafor (una sola somministrazione costa più di 5.000,00). Se la somministrazione avvenisse il regime ambulatoriale sarebbe auspicabile, qualora si decidesse di inserire il farmaco in PTORV, includerlo all interno della lista dei farmaci che possono essere messi in mobilità alle ASL di appartenenza del paziente, in caso contrario l intero costo del farmaco sarebbe a carico della struttura erogante. Tabella costi del trattamento con plerixafor: Farmaci Dosaggio Costo trattamento Note Plerixafor 0,24 mg/kg/die per 2 4 gg , ,00 Payment by result: rimborso del costo di plerixafor in caso di fallimento terapeutico dopo almeno 2 somministrazioni.. Al costo del trattamento con plerixafor si deve sommare il costo del trattamento con lenograstim o filgrastim. Lenograstim 150 µg/m 2 /die per 6-8 gg 378,00 504,00 Filgrastim biosimil. 171,00 273,00 Filgrastim originator 10 µg/kg/die per 6-8 giorni 1.396, ,00 Il costo del trattamento varia a seconda che si utilizzi il filgrastim biosimilare o l originator. Tabella costi del trattamento con alcuni schemi di chemioterapia, a cui va sempre aggiunto il costo della terapia con G-CSF (filgrastim o lenograstim): Farmaci Dosaggio Costo trattamento Note Ciclofosfamide 4 7 g/ m 2 per 1 gg 44,00 74,00 Citarabina 2 g/m 2 per 4-6 gg 224,00-336,00 Secondo l opinione dei clinici, nei regimi di mobilizzazione con chemioterapia, la durata della terapia con G-CSF, difficilmente prosegue per 8 giorni 8
9 Ifosfamide + etoposide + epirubicina 3000 mg/m 2 da 1 a 3 gg 200 mg/m 2 da 1 a 3 gg 50 mg/m 2 per 1 gg 101,00 261,00 Secondo l opinione dei clinici, nei regimi di mobilizzazione con chemioterapia, la durata della terapia con G-CSF, difficilmente prosegue per 8 giorni ANALISI DI IMPATTO SUL BUDGET Popolazione Target: Il report dell HAS France [11] individua in 983 pazienti l anno in Francia i possibili eleggibili alla terapia; queste stime riportandole alla popolazione Veneta individuerebbero in 75 il numero degli eleggibili in Regione. Questa stima sembra molto alta, in quanto non tiene conto dei diversi percorsi clinici terapeutici. La ditta utilizzando i dati del rapporto GITMO 2011 riporta che in Italia dei 2645 trapianti autologhi circa 82% sono da correlare a linfomi e mieloma multiplo. Per cui applicando questa percentuale alla casistica del Veneto (106 trapianti autologhi) si possono stimare in 86 i trapianti in soggetti con linfomi e mieloma multiplo. Di questi solo una parte sarà eleggibile al trattamento, in quanto scarsi mobilizzatore i cioè tra il 3-23% di quelli con mieloma e 11-53% di quelli con linfoma [17].La ditta considera quindi una percentuale di scarsi mobilizzatori del 20% per un totale di 22 pazienti. Queste stime, in generale sono state confermate dal confronto con alcuni clinici, ma gli stessi hanno sottolineato che soprattutto nei primi anni si pensa di trattarne circa 10 per anno. Analisi di impatto sul budget: La ditta sulla base dei dati GITMO ha presentato un analisi di budget considerando sia i costi dei farmaci che quelli sanitari più generali (costi del ricovero e dell aferesi, gestione della neutropenia febbrile, gestione dei fallimenti terapeutici ed eventuali rimobilizzazioni). In questa analisi si confronta uno Scenario iniziale (Anno 0) in cui plerixafor presente in regime di 648 viene somministrato al 25% dei pazienti (6 su 22) con 3 scenari (Anno 1-3) in cui la percentuale di somministrazione di plerixafor varia dal 50% al 85% (da 11 a 19 su 22 pazienti). La Spesa Sanitaria potrebbe aumentare tra euro. Per completezza si riporta una tabella semplificata dell analisi della ditta. Tabella A. Analisi della ditta su 22 pazienti scarsi mobilizzatori in Veneto. Anno 0 Anno 1 Anno 2 Anno 3 PZ G-CSF +/- chemio (%) 75% 50% 35% 15% PZ G-CSF +/- chemio (n)
10 Costo G-CSF +/- chemio (9 giorni) Costo Aferesi (4 accessi) Costo neutropenia febb Costo Rimobilizzazioni TOTALE Costo G-CSF +/- chemio PZ G-CSF + plerixafor (%) 25% 50% 65% 85% PZ G-CSF + plerixafor (n) Costo G-CSF (4 giorni) Costo plerixafor Costo Aferesi (4 accessi) TOTALE Costo G-CSF + plerixafor TOTALE Spesa Incrementi Spesa rispetto all Anno L analisi sopra descritta presenta degli spunti sicuramente interessanti mettendo in luce oltre ai costi incrementali anche i possibili risparmi legati ad una migliore gestione terapeutica del paziente (minor neutropenia febbrile causata della chemioterapia) e possibili minor accessi ospedalieri a seguito di fallimenti terapeutici e di ulteriori mobilizzazioni. UVEF ritiene però che queste voci di spesa non sono così facilmente quantificabili, soprattutto a causa della mancanza di evidenze sulla reale insorgenza degli eventi, e ritiene inoltre che la ditta ne abbia sovrastimato i costi utilizzando dei valori per le tariffe DRG (vecchio tariffario nazionale) molto più alte di quelle vigenti in Regione Veneto. Nello specifico la ditta: 1) Per stimare il costo della rimobilizzazione ha utilizzato il DRG 404 ad un valore di invece di 1.682,28. 2) Per stimare il costo della neutropenia febbrile il DRG 403 ad un valore di invece di 3.588,96. UVEF sottolinea inoltre che sentiti i clinici, la stima della ditta, nel gruppo di pazienti non trattati con plerixafor, di 9 giorni di trattamento con GCSF +/- chemioterapia è un periodo eccessivo; i clinici infatti hanno indicato il periodo medio di trattamento di circa 6 giorni. UVEF individuando tutte queste criticità 10
11 preferisce presentare un analisi molto conservativa che tenga conto della sola spesa farmaceutica e quindi del costo dei trattamenti. Per entrambi i gruppi di pazienti si è utilizzato un periodo medio di trattamento con G-CSF di 6 giorni; per il costo del trattamento si è considerato l utilizzo del filgrastim originator cioè a paziente; nel gruppo di confronto si è ipotizzato che la chemioterapia venga utilizzata in tutti i pazienti e che venga utilizzata la citarabina per una durata di 6 giorni ed un costo medio di 336 (si è utilizzata la citarabina in quanto risultava essere la più costosa tra le alternative). Nel gruppo trattato con plerixafor si è ipotizzato un utilizzo dello stesso per 2 giorni con un costo medio di Queste ipotesi sono le più conservative ed in particolare quella sul costo del plerixafor. Le stime di UVEF sono presentate in tabella. Tabella B. Analisi UVEF su 22 pazienti scarsi mobilizzatori in Veneto. Anno 0 Anno 1 Anno 2 Anno 3 PZ G-CSF +/- chemio (%) 75% 50% 35% 15% PZ G-CSF +/- chemio (n) Costo G-CSF + chemio (6 giorni) PZ G-CSF + plerixafor (%) 25% 50% 65% 85% PZ G-CSF + plerixafor (n) Costo G-CSF (6 giorni) Costo plerixafor (2 giorni) TOTALE Costo G-CSF + plerixafor TOTALE Spesa Incrementi Spesa rispetto all Anno Considerando quindi attendibili i dati presentati sui possibili pazienti scarsi mobilizzatori e le percentuali di penetrazione di plerixafor, la Spesa Farmaceutica potrebbe aumentare, rispetto allo scenario attuale, da fino a UVEF per il 2012 ha previsto un incremento di circa pari a 7 pazienti. Questi incrementi sulla Spesa Farmaceutica in parte potrebbero essere bilanciati da una migliore gestione terapeutica e da un minor numero di ricoveri e nuove mobilizzazioni. Questi risparmi potrebbero essere significativi, ma in misura minore rispetto a quanto presentato dalla ditta. L analisi è comunque molto influenzata dall ipotesi che plerixafor venga utilizzato solo per 2 giorni; nello scenario molto pessimistico in 11
12 cui venga utilizzato per tutti i pazienti fino a 4 giorni, la spesa avrebbe un incremento (in ogni singolo anno) quasi doppio tra il primo anno fino a il terzo. UVEF Sottolinea infine che sentiti i clinici regionali, almeno nei primi anni di introduzione del farmaco sembra verosimile che i pazienti trattati annualmente in regione possano essere circa 10 e quindi che gli incrementi potrebbero essere vicini a quello presentato (in tabella) per l Anno 1, cioè circa di BIBLIOGRAFIA 1. Riassunto delle caratteristiche del prodotto. 2. Epar Mozobil. EMEA/CHMP/303556/ (accesso del ). 3. Bensinger W. Et al, Bone Marrow Transplant 2009, 43: Giralt S. et al, Leukemia 2009; 23: DiPersio J.F. et al, J. Clin. Oncol. 2009, 27(28): DiPersio J.F. et al, Blood 2009; 113: Calandra G. et al, Bone Marrow Transplan 2008; 41: Duarte R.F. et al, Bone Marrow Transplan 2011; 46: (accesso del 7/02/2012) (accesso del 06/02/2011) (accesso del 06/02/2011) 12. Shaughnessyet al. Biol Blood Marrow Transplant (5): Vishnu et al. Transfusion : Li J, et al.. Transfusion : Costa et al, Bone Marrow Transplantation 2011; 46:
13 16. Keating et al Drugs (12): Olivieri et al, Bone Marrow Transplant May 30. [Epub ahead of print] SINTESI Plerixafor è un derivato del biciclam, un antagonista reversibile selettivo del recettore di chemochine CXCR4. Deve essere somministrato mediante iniezione sottocutanea da 6 a 11 ore prima dell inizio dell aferesi dopo 4 giorni di pretrattamento con G-CSF. Si tratta di un farmaco orfano che non presenta alternative della medesima classe terapeutica. Per la mobilizzazione delle cellule staminali ematopoietiche vengono utilizzati i fattori stimolanti le colonie (G-CSF) da soli o in associazione a chemioterapia (generalmente ciclofosfamide), tuttavia il plerixafor non può considerarsi un alternativa ai G-CSF in quanto viene utilizzato in associazione agli stessi e nei pazienti che abbiano già fallito almeno un tentativo di mobilizzazione con un dosaggio adeguato di G-CSF. Due RCT in doppio cieco di fase III hanno confrontato l'efficacia di plerixafor versus placebo in 298 pazienti con linfoma non Hodgkin (LNH) e 302 pazienti con mieloma multiplo (MM). In entrambi gli studi sono stati esclusi i pazienti che avevano avuto precedenti tentativi di raccolta di cellule staminali, pertanto sono stati inclusi pazienti con caratteristiche diverse rispetto a quelle per le quali AIFA ha limitato il farmaco (solo pazienti che abbiano già fallito almeno un tentativo di mobilizzazione con G-CSF). Il trattamento è stato iniziato con G-CSF e dopo quattro giorni, i pazienti randomizzati hanno ricevuto plerixafor sottocute 240 mcg / kg oppure placebo. L'endpoint primario era la proporzione di pazienti che raggiungevano l'obiettivo numerico di cellule CD34 + entro il numero predefinito di sessioni aferesi per ogni studio (massimo 4 giorni nello studio su pazienti con LNH e 2 giorni nello studio MM). Nello studio su pazienti con LNH, una percentuale significativamente maggiore di pazienti del gruppo plerixafor, il 59.3% (89/150), rispetto al gruppo placebo, 19.6% (29/148), ha raggiunto l'endpoint primario (raccolta di almeno 5 x 10 6 cellule CD34 +/ kg). Anche nello studio su pazienti con MM, l'endpoint primario (raccolta di almeno 6 x 10 6 cellule CD34 + / kg), è stato raggiunto da una percentuale di pazienti significativamente maggiore nel gruppo plerixafor rispetto al placebo (71.6% e il 34.4% rispettivamente, p<0.001). Sono stati pubblicati i risultati di due programmi di uso compassionevole (CUP) di plerixafor, uno svoltosi negli USA e l altro in Europa. I risultati di questi studi ci forniscono dati di efficacia importanti nel sottogruppo di pazienti per il farmaco è stato registrato in Europa, ossia coloro i quali abbiano fallito almeno un tentativo di mobilizzazione con G-CSF. La prima pubblicazione presenta i risultati di una coorte di 115 pazienti affetti da neoplasie ematologiche, che non avevano risposto a mobilizzazione con chemioterapia o con G-CSF. In oltre il 66% dei pazienti trattati con G-CSF più plerixafor sono state raccolte almeno 2 x 106 CD34+/kg. Il CUP svoltosi in Europa ha permesso di raccogliere i dati di 56 pazienti con MM e LNH che avevano fallito almeno un precedente tentativo di mobilizzazione. La raccolta di almeno 2 x 106 CD34+/kg è stata raggiunta dal 84% dei pazienti con MM e dal 63% dei pazienti con linfoma. Negli studi di fase III, l'incidenza di eventi avversi correlati al trattamento è stata più elevata nel gruppo plerixafor rispetto al placebo, il 65% versus il 41% nello studio su pazienti con LNH e il 65% versus il 45% nello studio su pazienti con MM. I più comuni eventi avversi correlati al trattamento sono stati disturbi gastrointestinali e reazioni al sito di iniezione. Nella scientific discussion il CHMP dell EMA ha sottolineato che esiste un rischio teorico di mobilizzazione delle cellule tumorali nei pazienti con MM e linfoma. Al fine di valutare la rilevanza clinica di questo rischio l EMA ha richiesto i risultati del follow-up dei due studi di fase lll che sono stati estesi a cinque anni. Inoltre è stata richiesta la compilazione di un registro a lungo termine. Il report dello SMC esprime parere favorevole al rimborso di plerixafor in Scozia. La ditta nella sua sottomissione ha proposto che l utilizzo del farmaco venga limitato in seconda linea di trattamento o successive. Il report 13
14 dell HAS francese esprime parere positivo al farmaco ed indica un ASMR di grado III (moderato). Il costo del trattamento con plerixafor è molto superiore rispetto alle alternative considerate: il trattamento con plerixafor in associazione a G-CSF varia infatti da circa ,00, ad un massimo di ,00. Le alternative (diversi regimi di chemioterapia indicateci dai clinici + G-CSF) variano da un costo di 215,00 ad un massimo di 1.732,00. Da sottolineare che attualmente il DRG 404 relativo alla rimobilizzazione ha un valore in Veneto 1.682,28 e quindi non copre il costo di plerixafor (una sola somministrazione costa più di 5.000). Se la somministrazione avvenisse il regime ambulatoriale sarebbe auspicabile, qualora si decidesse di inserire il farmaco in PTORV, includerlo all interno della lista dei farmaci in mobilità, in caso contrario l intero costo del farmaco sarebbe a carico della struttura erogante. La ditta utilizzando i dati del rapporto GITMO 2011 riporta che in Italia dei 2645 trapianti autologhi circa 82% sono da correlare a LNH e MM. Per cui applicando questa percentuale alla casistica del Veneto si possono stimare in 86 i trapianti in soggetti con LNH e MM. La ditta considera quindi una percentuale di scarsi mobilizzatori del 20% per un totale di 22 pazienti. Queste stime sono state confermate dal confronto con alcuni clinici i quali evidenziano però che in regione Veneto, soprattutto nei primi anni i pazienti trattati saranno di circa 10 l anno. La ditta sulla base dei dati GITMO ha presentato un analisi di budget considerando sia i costi dei farmaci che quelli sanitari più generali (costi del ricovero e dell aferesi, gestione della neutropenia febbrile, gestione dei fallimenti terapeutici ed eventuali rimobilizzazioni). L analisi presenta secondo UVEF numerose criticità:la ditta ha utilizzato dei valori di DRG molto più alti rispetto a quelli vigenti in Vento, inoltre, sentiti i clinici, la stima della ditta di 9 giorni di trattamento con GCSF +/- chemioterapia si ritiene essere un periodo eccessivo; i clinici infatti hanno indicato il periodo medio di trattamento di circa 6 giorni. UVEF preferisce presentare un analisi molto conservativa che tenga conto della sola spesa farmaceutica e quindi del costo dei trattamenti per una terapia della durata media di 6 giorni. Considerando quindi attendibili i dati presentati sui possibili pazienti scarsi mobilizzatori e le percentuali di penetrazione di plerixafor, UVEF per il 2012 ha previsto un incremento di circa pari a 7 pazienti. Questi incrementi sulla Spesa Farmaceutica in parte potrebbero essere bilanciati da una migliore gestione terapeutica e da un minor numero di ricoveri e nuove mobilizzazioni. L analisi è comunque molto influenzata dall ipotesi che plerixafor venga utilizzato solo per 2 giorni; nello scenario molto pessimistico in cui venga utilizzato per tutti i pazienti fino a 4 giorni, la spesa avrebbe un incremento quasi doppio. UVEF Sottolinea infine che sentiti i clinici regionali, almeno nei primi anni di introduzione del farmaco sembra verosimile che i pazienti trattati annualmente in regione possano essere circa 10 e quindi che gli incrementi potrebbero essere vicini a quello presentato (in tabella) per l Anno 1, cioè circa di
15 APPENDICE Tabella 1 Referenza n. pazienti, patologia, trattamenti Disegno/Fase Misura di esito primario Risultati su outcome primario DiPersio J.F. et al, Blood 2009 [6] DiPersio J.F. et al, J. Clin. Oncol [5] 302 pz dai 18 ai 78 anni, con MM che non avevano ricevuto un precedente tentativo di mobilizzazione. Trattamento: - G-CSF 10 µg/kg + plerixafor 0.24 mg/kg [N=148] - G-CSF 10 µg/kg + placebo [N=154] Trattamento fino al raggiungimento di almeno 6 X 10 6 CD34+/kg, massimo 4 giorni. 298 pz dai 18 ai 78 anni, con LNH che non avevano ricevuto un precedente tentativo di mobilizzazione. Trattamento: - G-CSF 10 µg/kg + plerixafor 0.24 mg/kg [N=150] - G-CSF 10 µg/kg + placebo [N=148] Trattamento fino al raggiungimento di almeno 5 X 10 6 CD34+/kg, massimo 4 giorni. RCT, doppio cieco, controllato con placebo, di superiorità, analisi ITT / III RCT, doppio cieco, controllato con placebo, di superiorità, analisi ITT / III 1 ) % di pazienti con raccolta di almeno 6 X 10 6 CD34+/kg, in al massimo 2 giorni di aferesi. 1 EMA) endpoint composito: % di pazienti con raccolta di almeno 6 X 10 6 CD34+/kg, in <2 giorni di aferesi + successo nell attecchimento di PMN e PLT 1 ) % di pazienti con raccolta di almeno 5 X 10 6 CD34+/kg, in al massimo 4 giorni di aferesi. 1 EMA) endpoint composito: % di pazienti con raccolta di almeno 2 X 10 6 CD34+/kg, in <4 giorni di aferesi + successo nell attecchimento di PMN e PLT 1 ) 71.6% plerixafor vs 34.4% placebo, p< EMA) 70.3% plerixafor vs 34.4% placebo, p< ) 59.3% plerixafor vs 19.6% placebo, p< EMA) 84.0% plerixafor vs 43.2% placebo, p<0.001 Jadad score* 3 Calandra G. et al, 115 pz di età dai 18 ai 70 anni, con MM o Studio prospettico 1) % di pazienti con raccolta 1) Globale: 66.1%. -- Bone Marrow LNH o LH, che avevano fallito almeno un di coorte di almeno 2 X 10 6 CD34+/kg LNH: 60.3%, MM: 71.4%, LH: Trasplan 2008 [7] precedente tentativo di mobilizzazione. (programma di uso 2) Tempo all attecchimento 76.5% Trattamento: compassionevole di neutrofili e PLT dopo il 2) tempo all attecchimento - plerixafor 0.24 mg/kg + G-CSF 10 µg/kg USA) trapianto dei neutrofili: 11 gg; tempo all attecchimento PLT: 8 gg. 15 3
16 Referenza n. pazienti, patologia, trattamenti Disegno/Fase Misura di esito primario Risultati su outcome primario Duarte R.F. et al, Bone Marrow Trasplan 2011 [8] 56 pz di età compresa tra 18 e 78 anni, con MM o linfoma, che avevano fallito almeno un precedente tentativo di mobilizzazione. Trattamento: - plerixafor 0.24 mg/kg + G-CSF 10 µg/kg Studio prospettico di coorte (programma di uso compassionevole EU) 1) % di pazienti con raccolta di almeno 2 X 10 6 CD34+/kg 2) Tempo all attecchimento di neutrofili e PLT dopo il trapianto 1) Globale: 75%. Linfoma: 63%, MM: 84% 2) tempo all attecchimento dei neutrofili: 13.4 gg; tempo all attecchimento PLT: 18.5 gg. Jadad score* --- *Jadad Scale: strumento per la verifica della qualità della pubblicazione; si basa sulla considerazione che i tre elementi principali che devono essere riportati per avere maggiori garanzie sulla buona qualità di uno studio clinico siano la randomizzazione, la condizione di doppia cecità, e la gestione dei drop-out. Si considerano buone le pubblicazioni che ottengono almeno 3 punti, mentre si considerano di scarsa qualità quelle che raggiungono un punteggio uguale o inferiore a due. 16
17 Tabella 2 Referenza Tipo di analisi e confronti Nazione/ Punto di Vista Pazienti e Time Horizon Misura di efficacia Misura di costo Risultati Shaughnessyet al [12] Vishnu et al [13] Analisi Costo- Conseguenze. Plerixafor + G-CSF vs Chemioterapia + GCSF Confronto tra i risultati di un programma di expanded access (33 pazienti visti in maniera prospettica) vs un gruppo di controllo (33 pazienti visti in maniera retrospettiva, cioè controllo con lo storico). Analisi costo beneficio Modello di Simulazione con 100 Pazienti per gruppo di confronto. Plerixafor + filgrastim vs filgrastim USA / Terzo Pagante Pazienti eleggibili al trapianto autologo, naive alla mobilizzazione, al trapianto allo genico o al trapianto autologo, con o linfoma di Hodgkin o mieloma multiplo o linfoma di non Hodgkin. / 6 mesi. USA / Terzo Pagante Utilizzo di plerixafor come terapia preventiva in pazienti con linfoma non Hodgkin e mieloma multiplo / Non specificato Conta delle cellule CD34+ 1) Conta delle cellule CD34, 2) Giorni per raggiungere livelli ottimali di CD34. 3) Eventi avversi, attecchimento delle cellule dopo trapianto Costi diretti sanitari Costo mediano torale nel gruppo plerixafor + G-CSF = $ Costo mediano totale nel gruppo chemioterapia + G-CSF = $ Questa differenza non è però significativa. I pazienti trattati con plerixafor hanno avuto minori ospedalizzazioni, minor numero di trasfusioni durante l aferesi. Costi diretti sanitari L utilizzo di plerixafor si traduce in un risparmio di $ per paziente trattato. 17
18 Li et al [14] Costa et al [15] Analisi dei costi. Plerixafor + GCSF vs GCSF Analisi Costo Conseguenze Plerixafor + GCS-F vs Chemioterapia di condizionamento + GCS-F USA / Terzo Pagante USA / Terzo Pagante Pazienti eleggibili al trapianto autologo con linfoma o mieloma multiplo / da un giorno prima dell aferesi fino all ultimo giorno di aferesi Pazienti eleggibili al trapianto autologo con linfoma o mieloma multiplo. / giorni Conta delle cellule CD34. Conta delle cellule CD34 Costi diretti sanitari. Non si sono considerati i costi di re-mobilizzazione Complessivamente nel paziente medio la strategia con plerixafor si è mostrata più costosa cioè $ vs $ Gli autori evidenziano però che nei pazienti con alto rischio di fallimento della mobilizzazione CD34) plerixafor prene Costi diretti sanitari Considerando il minor numero di ricadute e quindi di remobilizzazioni il gruppo con plerixafor si è mostrato meno costoso cioè $ vs $
Trials clinici. Disegni di studio
 Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
16th World Conference on Lung Cancer (WCLC): highlights
 16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA
 IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
La neutropenia è definita in gradi a seconda del valore raggiunta dai neutrofili al Nadir ( tabella 1)
 TRATTAMENTO DELLA NEUTROPENIA CON G-CSF Introduzione La neutropenia e le complicanze ad essa correlate rappresentano la principale tossicità dose limitante della chemioterapia, per il rischio di infezioni
TRATTAMENTO DELLA NEUTROPENIA CON G-CSF Introduzione La neutropenia e le complicanze ad essa correlate rappresentano la principale tossicità dose limitante della chemioterapia, per il rischio di infezioni
La cellula staminale emopoietica: utilizzo nel trapianto autologo e allogenico e metodiche di raccolta in età adulta e pediatrica.
 La cellula staminale emopoietica: utilizzo nel trapianto autologo e allogenico e metodiche di raccolta in età adulta e pediatrica Valter Tassi La cellula staminale La cellula staminale è una cellula IMMATURA
La cellula staminale emopoietica: utilizzo nel trapianto autologo e allogenico e metodiche di raccolta in età adulta e pediatrica Valter Tassi La cellula staminale La cellula staminale è una cellula IMMATURA
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA
 Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA FARMACI ONCOLOGICI Genova, Palazzo della Regione Liguria 4 Dicembre 2014 Dr.ssa Alida Rota farmacista Ospedale
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA FARMACI ONCOLOGICI Genova, Palazzo della Regione Liguria 4 Dicembre 2014 Dr.ssa Alida Rota farmacista Ospedale
autologo: nuove strategie di
 Bergamo, 15-16 aprile 2012 Cellule staminali e trapianto autologo: nuove strategie di mobilizzazione Coordinamento Scientifico Alberto Bosi Direttore Locale Alessandro Rambaldi sezione di ematologia OBIETTIVI
Bergamo, 15-16 aprile 2012 Cellule staminali e trapianto autologo: nuove strategie di mobilizzazione Coordinamento Scientifico Alberto Bosi Direttore Locale Alessandro Rambaldi sezione di ematologia OBIETTIVI
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Diagnosi precoce delle neoplasie del collo dell utero
 Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE
 Genova, 24 maggio 2013 L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE Dott.ssa Simona Genta FATTORI CHE INFLUISCONO SULLA SPESA FARMACEUTICA ANALISI DEI CONSUMI FATTORI CHE RIDUCONO LA SPESA
Genova, 24 maggio 2013 L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE Dott.ssa Simona Genta FATTORI CHE INFLUISCONO SULLA SPESA FARMACEUTICA ANALISI DEI CONSUMI FATTORI CHE RIDUCONO LA SPESA
QUESTIONARIO SODDISFAZIONE FAMIGLIA. Nome del bambino: Sesso: F M
 QUESTIONARIO SODDISFAZIONE FAMIGLIA Ministero della Salute - Centro Nazionale per la Prevenzione delle Malattie (CCM) Progetti applicativi al programma CCM 2009 Presa in carico precoce nel primo anno di
QUESTIONARIO SODDISFAZIONE FAMIGLIA Ministero della Salute - Centro Nazionale per la Prevenzione delle Malattie (CCM) Progetti applicativi al programma CCM 2009 Presa in carico precoce nel primo anno di
Il mieloma multiplo La terapia
 MIELOMA MULTIPLO Il mieloma multiplo è una malattia neoplastica caratterizzata dalla proliferazione e accumulo nel midollo osseo di linfociti e di plasmacellule che, direttamente o indirettamente, possono
MIELOMA MULTIPLO Il mieloma multiplo è una malattia neoplastica caratterizzata dalla proliferazione e accumulo nel midollo osseo di linfociti e di plasmacellule che, direttamente o indirettamente, possono
Segnaliamo le sospette reazioni avverse! Come fare?
 La Farmacovigilanza. Perché, quando e come segnalare le Reazioni Avverse da Farmaci Segnaliamo le sospette reazioni avverse! Come fare? Dr. Michele Conti Regione Lazio Farmacista collaboratore di Farmacovigilanza
La Farmacovigilanza. Perché, quando e come segnalare le Reazioni Avverse da Farmaci Segnaliamo le sospette reazioni avverse! Come fare? Dr. Michele Conti Regione Lazio Farmacista collaboratore di Farmacovigilanza
Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria
 Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria Christopher N. Sciamanna, Scott P. Novak, Bess H. Marcus. International Journal of
Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria Christopher N. Sciamanna, Scott P. Novak, Bess H. Marcus. International Journal of
CARTA INTESTATA DEL CENTRO CLINICO
 CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA
 COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA METODOLOGIA DI VALUTAZIONE DELLA PERFORMANCE Approvato con atto G.C. n. 492 del 07.12.2011 1
COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA METODOLOGIA DI VALUTAZIONE DELLA PERFORMANCE Approvato con atto G.C. n. 492 del 07.12.2011 1
COMUNE DI ZERO BRANCO Provincia di Treviso
 COMUNE DI ZERO BRANCO Provincia di Treviso SISTEMA DI VALUTAZIONE PERMANENTE DELLA PERFORMANCE INDIVIDUALE E DELLE PERFORMANCE ORGANIZZATIVE APPROVATO CON DELIBERAZIONE DI G.C. N. 15 DEL 9.2.2012 E MODIFICATO
COMUNE DI ZERO BRANCO Provincia di Treviso SISTEMA DI VALUTAZIONE PERMANENTE DELLA PERFORMANCE INDIVIDUALE E DELLE PERFORMANCE ORGANIZZATIVE APPROVATO CON DELIBERAZIONE DI G.C. N. 15 DEL 9.2.2012 E MODIFICATO
10 VALUTAZIONE DELLE ANALISI
 10 VALUTAZIONE DELLE ANALISI ECONOMICHE Questa valutazione economica può aiutarvi? 1 Esistono prove valide che gli interventi sono efficaci? 2 Di quale tipo di analisi economica si tratta? Studio costo-conseguenze
10 VALUTAZIONE DELLE ANALISI ECONOMICHE Questa valutazione economica può aiutarvi? 1 Esistono prove valide che gli interventi sono efficaci? 2 Di quale tipo di analisi economica si tratta? Studio costo-conseguenze
PASQUALE FREGA Assobiotec
 ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI
 ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI INTRODUZIONE Le Infezioni da Pneumococco (PNU) rappresentano un problema sanitario grave, soprattutto a causa
ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI INTRODUZIONE Le Infezioni da Pneumococco (PNU) rappresentano un problema sanitario grave, soprattutto a causa
LA REVISIONE LEGALE DEI CONTI La comprensione
 LA REVISIONE LEGALE DEI CONTI La comprensione dell impresa e del suo contesto e la valutazione dei rischi di errori significativi Ottobre 2013 Indice 1. La comprensione dell impresa e del suo contesto
LA REVISIONE LEGALE DEI CONTI La comprensione dell impresa e del suo contesto e la valutazione dei rischi di errori significativi Ottobre 2013 Indice 1. La comprensione dell impresa e del suo contesto
STUDI SU MATERIALE GENETICO
 Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Indagine qualita percepita
 Sistema di Gestione per la Qualità - Ospedale M. G. Vannini Report sulla qualità percepita OSPEDALE M. G. VANNINI Direttore Sanitario Dott.ssa Maura Moreschini Sistema qualità certificato UNI EN ISO 9001:2008
Sistema di Gestione per la Qualità - Ospedale M. G. Vannini Report sulla qualità percepita OSPEDALE M. G. VANNINI Direttore Sanitario Dott.ssa Maura Moreschini Sistema qualità certificato UNI EN ISO 9001:2008
L EFFICACIA DELLE MISURE DI POLITICA ATTIVA DEL LAVORO REALIZZATE IN PROVINCIA DI TORINO NEL 2007-08
 1 La valutazione L EFFICACIA DELLE MISURE DI POLITICA ATTIVA DEL LAVORO REALIZZATE IN PROVINCIA DI TORINO NEL 2007-08 Esiti occupazionali a 24 dalla partecipazione Vengono qui riassunti i risultati della
1 La valutazione L EFFICACIA DELLE MISURE DI POLITICA ATTIVA DEL LAVORO REALIZZATE IN PROVINCIA DI TORINO NEL 2007-08 Esiti occupazionali a 24 dalla partecipazione Vengono qui riassunti i risultati della
AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune)
 AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
Statistica. Lezione 6
 Università degli Studi del Piemonte Orientale Corso di Laurea in Infermieristica Corso integrato in Scienze della Prevenzione e dei Servizi sanitari Statistica Lezione 6 a.a 011-01 Dott.ssa Daniela Ferrante
Università degli Studi del Piemonte Orientale Corso di Laurea in Infermieristica Corso integrato in Scienze della Prevenzione e dei Servizi sanitari Statistica Lezione 6 a.a 011-01 Dott.ssa Daniela Ferrante
PROCEDURA OPERATIVA DI VALUTAZIONE DEI DIPENDENTI
 PROCEDURA OPERATIVA DI VALUTAZIONE DEI DIPENDENTI A fini dell erogazione della produttività individuale e di gruppo ( art 17 comma 1 lettera a) dell Accordo nazionale e ai fini della progressione economica
PROCEDURA OPERATIVA DI VALUTAZIONE DEI DIPENDENTI A fini dell erogazione della produttività individuale e di gruppo ( art 17 comma 1 lettera a) dell Accordo nazionale e ai fini della progressione economica
A.A. 2015/2016. Statistica Medica. Corso di. CdL in Fisioterapia CdL in Podologia
 A.A. 2015/2016 Corso di Statistica Medica CdL in Fisioterapia CdL in Podologia La statistica è la scienza che ha come fine lo studio quantitativo e qualitativo di un "collettivo". Studia i modi in cui
A.A. 2015/2016 Corso di Statistica Medica CdL in Fisioterapia CdL in Podologia La statistica è la scienza che ha come fine lo studio quantitativo e qualitativo di un "collettivo". Studia i modi in cui
Rapporto dal Questionari Insegnanti
 Rapporto dal Questionari Insegnanti SCUOLA CHIC81400N N. Docenti che hanno compilato il questionario: 60 Anno Scolastico 2014/15 Le Aree Indagate Il Questionario Insegnanti ha l obiettivo di rilevare la
Rapporto dal Questionari Insegnanti SCUOLA CHIC81400N N. Docenti che hanno compilato il questionario: 60 Anno Scolastico 2014/15 Le Aree Indagate Il Questionario Insegnanti ha l obiettivo di rilevare la
Governo del Farmaco. Azienda Ospedaliera di Verona
 Governo del Farmaco Elementi organizzativi e tecnologie: Esperienze a confronto Venezia 23 Febbraio 2009 Giovanna Scroccaro Azienda Ospedaliera di Verona Governo del Farmaco Elementi organizzativi e tecnologie:
Governo del Farmaco Elementi organizzativi e tecnologie: Esperienze a confronto Venezia 23 Febbraio 2009 Giovanna Scroccaro Azienda Ospedaliera di Verona Governo del Farmaco Elementi organizzativi e tecnologie:
Comparabilità fra le somministrazioni successive effetto di trascinamento ( carry-over ) effetto di periodo
 Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
Sviluppo del Sistema Cure Intermedie al fine dell utilizzo corretto delle risorse ex DGR 1235/2012
 Pagina 1 di 6 Sviluppo del Sistema Cure Intermedie al fine dell utilizzo corretto delle risorse ex DGR 1235/2012 Il presente documento è inteso a suggerire una allocazione ottimale dei pazienti che non
Pagina 1 di 6 Sviluppo del Sistema Cure Intermedie al fine dell utilizzo corretto delle risorse ex DGR 1235/2012 Il presente documento è inteso a suggerire una allocazione ottimale dei pazienti che non
HTA e farmaci: il ruolo dell AIFA
 HTA e farmaci: il ruolo dell AIFA Simona Montilla 12 luglio 2013 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA
HTA e farmaci: il ruolo dell AIFA Simona Montilla 12 luglio 2013 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA
Accesso ai farmaci innovativi e controllo della spesa a livello regionale
 FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
BANDO. Premi di Ricerca SIOMMMS per giovani ricercatori
 BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2014/2016 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2014/2016 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
Potenza dello studio e dimensione campionaria. Laurea in Medicina e Chirurgia - Statistica medica 1
 Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009
 ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009 A cura di: Dr.ssa M. Gambino, Dr.ssa Ass. San. L. Balconi, Dr. S. Pisani U. O. S. Sorveglianza
ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009 A cura di: Dr.ssa M. Gambino, Dr.ssa Ass. San. L. Balconi, Dr. S. Pisani U. O. S. Sorveglianza
Osservatorio SosTariffe.it Telefonia Mobile
 Osservatorio SosTariffe.it Telefonia Mobile TARIFFE IN PORTABILITA DEL NUMERO: ANALISI SUL RISPARMIO CHE SI OTTIENE EFFETTUANDO IL PASSAGGIO DEL NUMERO AD UN ALTRO OPERATORE SIA PER ABBONAMENTI CHE PER
Osservatorio SosTariffe.it Telefonia Mobile TARIFFE IN PORTABILITA DEL NUMERO: ANALISI SUL RISPARMIO CHE SI OTTIENE EFFETTUANDO IL PASSAGGIO DEL NUMERO AD UN ALTRO OPERATORE SIA PER ABBONAMENTI CHE PER
GUIDA ALLA RILEVANZA
 GUIDA ALLA RILEVANZA Posizionamento per Rilevanza Suggerimenti per una migliore visibilità su ebay www.egolden.it Vers. 1.1 Questa guida puo essere ridistribuita con l obbligo di non modificarne contenuto
GUIDA ALLA RILEVANZA Posizionamento per Rilevanza Suggerimenti per una migliore visibilità su ebay www.egolden.it Vers. 1.1 Questa guida puo essere ridistribuita con l obbligo di non modificarne contenuto
PREVENZIONE POLMONITE
 fiammaz o l m o n a r e struzione br avità pleuri Streptococcus p n e u m o n i a Infezione Mal Respiratorio PREVENZIONE POLMONITE Vaccino Pneumococcico Polisaccaridico Coniugato, (13Valente Adsorbito)
fiammaz o l m o n a r e struzione br avità pleuri Streptococcus p n e u m o n i a Infezione Mal Respiratorio PREVENZIONE POLMONITE Vaccino Pneumococcico Polisaccaridico Coniugato, (13Valente Adsorbito)
Risultati dell indagine sul benessere dei dipendenti 2014
 Risultati dell indagine sul benessere dei dipendenti 2014 (art. 14 comma 5 - d.lgs 150/2009) sintesi dati Generali, per Area e tipologia di dipendente Le Amministrazioni pubbliche, nella prospettiva di
Risultati dell indagine sul benessere dei dipendenti 2014 (art. 14 comma 5 - d.lgs 150/2009) sintesi dati Generali, per Area e tipologia di dipendente Le Amministrazioni pubbliche, nella prospettiva di
CONVENZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO, 2006 1
 Convenzione 187 CONVENZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO, 2006 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio
Convenzione 187 CONVENZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO, 2006 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio
Principi generali. Vercelli 9-10 dicembre 2005. G. Bartolozzi - Firenze. Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli
 Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli Principi generali Carlo Federico Gauss Matematico tedesco 1777-1855 G. Bartolozzi - Firenze Vercelli 9-10 dicembre 2005 Oggi il nostro lavoro
Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli Principi generali Carlo Federico Gauss Matematico tedesco 1777-1855 G. Bartolozzi - Firenze Vercelli 9-10 dicembre 2005 Oggi il nostro lavoro
PROCEDURE - GENERALITA
 PROCEDURE - GENERALITA Le PROCEDURE sono regole scritte, utili strumenti di buona qualità organizzativa, con le quali lo svolgimento delle attività viene reso il più possibile oggettivo, sistematico, verificabile,
PROCEDURE - GENERALITA Le PROCEDURE sono regole scritte, utili strumenti di buona qualità organizzativa, con le quali lo svolgimento delle attività viene reso il più possibile oggettivo, sistematico, verificabile,
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI
 UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO
 LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO Accuratezza degli studi Miettinen, nel 1985, afferma che : la accuratezza di uno studio epidemiologico consiste nel grado di - assenza di errori
LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO Accuratezza degli studi Miettinen, nel 1985, afferma che : la accuratezza di uno studio epidemiologico consiste nel grado di - assenza di errori
Attuali proposte di finanziamento di progetti in discussione in gruppo V nel 2014
 Attuali proposte di finanziamento di progetti in discussione in gruppo V nel 2014 - Progetti a call - Progetti bottom-up - Progetti simil-firb La metodologia di sottomissione attuale Storicamente, da quando
Attuali proposte di finanziamento di progetti in discussione in gruppo V nel 2014 - Progetti a call - Progetti bottom-up - Progetti simil-firb La metodologia di sottomissione attuale Storicamente, da quando
STUDIO Co.Mi.M. - Costo sociale del Mieloma Multiplo
 STUDIO Co.Mi.M. - Costo sociale del Mieloma Multiplo Dott.ssa Maria Teresa Petrucci, Policlinico Umberto I, Roma Premessa Il presente project work si distingue per la visione di insieme che caratterizza
STUDIO Co.Mi.M. - Costo sociale del Mieloma Multiplo Dott.ssa Maria Teresa Petrucci, Policlinico Umberto I, Roma Premessa Il presente project work si distingue per la visione di insieme che caratterizza
La donazione di sangue: una scelta libera e consapevole. XVII Assemblea Annuale Soci Avis Comunale Cariati. 2 Aprile 2011 Dott. Domenico Lorenzo Urso
 La donazione di sangue: una scelta libera e consapevole XVII Assemblea Annuale Soci Avis Comunale Cariati 2 Aprile 2011 Dott. Domenico Lorenzo Urso Nella relazione vengono esposti gli aspetti legislativi
La donazione di sangue: una scelta libera e consapevole XVII Assemblea Annuale Soci Avis Comunale Cariati 2 Aprile 2011 Dott. Domenico Lorenzo Urso Nella relazione vengono esposti gli aspetti legislativi
PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA)
 PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA) Il presente documento descrive le modalità di coordinamento tra gestori
PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA) Il presente documento descrive le modalità di coordinamento tra gestori
1. Introduzione e finalità delle Linee guida
 LINEE GUIDA PER L ACQUISTO DI TRATTAMENTI ALL ESTERO - Versione finale, 09.11.2005 1. Introduzione e finalità delle Linee guida Il Gruppo ad alto livello sui servizi sanitari e l'assistenza medica ha deciso
LINEE GUIDA PER L ACQUISTO DI TRATTAMENTI ALL ESTERO - Versione finale, 09.11.2005 1. Introduzione e finalità delle Linee guida Il Gruppo ad alto livello sui servizi sanitari e l'assistenza medica ha deciso
Migliorare la gestione del paziente con BPCO in Medicina Generale.
 Progetto di audit clinico. Migliorare la gestione del paziente con BPCO in Medicina Generale. Razionale. Numerose esperienze hanno dimostrato che la gestione del paziente con BPCO è subottimale. La diagnosi
Progetto di audit clinico. Migliorare la gestione del paziente con BPCO in Medicina Generale. Razionale. Numerose esperienze hanno dimostrato che la gestione del paziente con BPCO è subottimale. La diagnosi
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? 2. Come nasce la sperimentazione clinica e che tipi di studi esistono?
 STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
16/05/2012. La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino. Roma, 10 Maggio 2012
 La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI
 BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI SCHEMA DI PRESENTAZIONE DELLA LETTERA DI INTENTI La presentazione della lettera di intenti dovrà avvenire entro le ore 12.00 del 23 aprile 2012,
BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI SCHEMA DI PRESENTAZIONE DELLA LETTERA DI INTENTI La presentazione della lettera di intenti dovrà avvenire entro le ore 12.00 del 23 aprile 2012,
Informazioni per potenziali partecipanti. Possiamo sciogliere l'amiloidosi AL?
 Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
BANDO. Premi di Ricerca SIOMMMS per giovani ricercatori
 BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2015/2017 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2015/2017 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
Sistema Informativo per il monitoraggio dell Assistenza Domiciliare (SIAD)
 Sistema Informativo per il monitoraggio dell Assistenza Domiciliare (SIAD) INDICATORI SIAD - SISTEMA ASSISTENZA DOMICILIARE Schede descrittive degli Indicatori per la lettura integrata dei fenomeni sanitari
Sistema Informativo per il monitoraggio dell Assistenza Domiciliare (SIAD) INDICATORI SIAD - SISTEMA ASSISTENZA DOMICILIARE Schede descrittive degli Indicatori per la lettura integrata dei fenomeni sanitari
 Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
Capitolo 13: L offerta dell impresa e il surplus del produttore
 Capitolo 13: L offerta dell impresa e il surplus del produttore 13.1: Introduzione L analisi dei due capitoli precedenti ha fornito tutti i concetti necessari per affrontare l argomento di questo capitolo:
Capitolo 13: L offerta dell impresa e il surplus del produttore 13.1: Introduzione L analisi dei due capitoli precedenti ha fornito tutti i concetti necessari per affrontare l argomento di questo capitolo:
CHI DONA SANGUE HA CUORE.
 Tel. e Fax Tel. e Fax Tel. e Fax Tel. e Fax IL E I SUOI COMPONENTI. LE DIVERSE FORME DI DONAZIONE. Il sangue è un tessuto fluido che circola nei vasi sanguigni, rappresenta l 8% del peso corporeo ed è
Tel. e Fax Tel. e Fax Tel. e Fax Tel. e Fax IL E I SUOI COMPONENTI. LE DIVERSE FORME DI DONAZIONE. Il sangue è un tessuto fluido che circola nei vasi sanguigni, rappresenta l 8% del peso corporeo ed è
La valutazione del rischio chimico
 La valutazione del rischio chimico Introduzione Per sua stessa definizione, l agente chimico è una sostanza o un preparato di natura chimica. L agente chimico può presentarsi sotto forma di gas, vapore,
La valutazione del rischio chimico Introduzione Per sua stessa definizione, l agente chimico è una sostanza o un preparato di natura chimica. L agente chimico può presentarsi sotto forma di gas, vapore,
Grazie dell attenzione
 Grazie dell attenzione http://www.registri-tumori.it/pdf/aiom2012/i_numeri_del_cancro_2012.pdf In Italia circa 2.250mila persone (4% del totale della popolazione) vivono avendo avuto una precedente
Grazie dell attenzione http://www.registri-tumori.it/pdf/aiom2012/i_numeri_del_cancro_2012.pdf In Italia circa 2.250mila persone (4% del totale della popolazione) vivono avendo avuto una precedente
IL diabetico. Gestione condivisa. Claudio Marengo Marco Comoglio Andrea Pizzini
 IL diabetico anziano Gestione condivisa Claudio Marengo Marco Comoglio Andrea Pizzini SEEd srl C.so Vigevano, 35-10152 Torino Tel. 011.566.02.58 - Fax 011.518.68.92 www.edizioniseed.it info@seed-online.it
IL diabetico anziano Gestione condivisa Claudio Marengo Marco Comoglio Andrea Pizzini SEEd srl C.so Vigevano, 35-10152 Torino Tel. 011.566.02.58 - Fax 011.518.68.92 www.edizioniseed.it info@seed-online.it
INDICAZIONI OPERATIVE PER VALUTARE E PROMUOVERE L ORGANIZZAZIONE AZIENDALE DELLA SICUREZZA
 INDICAZIONI OPERATIVE PER VALUTARE E PROMUOVERE L ORGANIZZAZIONE AZIENDALE DELLA SICUREZZA Con il presente documento si precisano le modalità di intervento da adottare da parte degli Spisal per valutare
INDICAZIONI OPERATIVE PER VALUTARE E PROMUOVERE L ORGANIZZAZIONE AZIENDALE DELLA SICUREZZA Con il presente documento si precisano le modalità di intervento da adottare da parte degli Spisal per valutare
PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO
 PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO L indagine si è svolta nel periodo dal 26 agosto al 16 settembre 2014 con l obiettivo di conoscere l opinione dei residenti
PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO L indagine si è svolta nel periodo dal 26 agosto al 16 settembre 2014 con l obiettivo di conoscere l opinione dei residenti
Atrial Fibrillation Study - Italy Study conducted by Opinion Health
 Atrial Fibrillation Study - Italy Study conducted by Opinion Health Obiettivi Valutare il livello di awareness della FA e dei sintomi Comprendere l impatto della FA e del trattamento sulla qualità di vita
Atrial Fibrillation Study - Italy Study conducted by Opinion Health Obiettivi Valutare il livello di awareness della FA e dei sintomi Comprendere l impatto della FA e del trattamento sulla qualità di vita
Fornitura dell apparecchio acustico a carico del Servizio Sanitario Nazionale
 Fornitura dell apparecchio acustico a carico del Servizio Sanitario Nazionale Lo sapevi che la sanità italiana eroga un contributo a favore dei cittadini italiani con particolari problemi di udito? In
Fornitura dell apparecchio acustico a carico del Servizio Sanitario Nazionale Lo sapevi che la sanità italiana eroga un contributo a favore dei cittadini italiani con particolari problemi di udito? In
A cura di Giorgio Mezzasalma
 GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
Specificare quale ospedale, dipartimento e/o soggetti inoltrano la proposta
 1. Chi è il proponente? - l ospedale - il dipartimento - un singolo soggetto Specificare quale ospedale, dipartimento e/o soggetti inoltrano la proposta 2. Chi sono i soggetti coinvolti nella proposta?
1. Chi è il proponente? - l ospedale - il dipartimento - un singolo soggetto Specificare quale ospedale, dipartimento e/o soggetti inoltrano la proposta 2. Chi sono i soggetti coinvolti nella proposta?
Migliorare la gestione del paziente con BPCO in Medicina Generale.
 Progetto di audit clinico. Migliorare la gestione del paziente con BPCO in. Razionale. Numerose esperienze hanno dimostrato che la gestione del paziente con BPCO è subottimale. La diagnosi spesso non è
Progetto di audit clinico. Migliorare la gestione del paziente con BPCO in. Razionale. Numerose esperienze hanno dimostrato che la gestione del paziente con BPCO è subottimale. La diagnosi spesso non è
Metodologia di calcolo del pay-back 5% - 2013
 Metodologia di calcolo del pay-back 5% - 2013 Vista la proroga al 31 dicembre 2013 emanata ai sensi del D.P.C.M. 26 giugno 2013, dei termini previsti all art.9, comma 1, del D.L. 31 dicembre 2007, n.248,
Metodologia di calcolo del pay-back 5% - 2013 Vista la proroga al 31 dicembre 2013 emanata ai sensi del D.P.C.M. 26 giugno 2013, dei termini previsti all art.9, comma 1, del D.L. 31 dicembre 2007, n.248,
Medici a laboratori clinici: quale rapporto e livello di comunicazione?
 RILEVAZIONI Medici a laboratori clinici: quale rapporto e livello di comunicazione? I risultati da un indagine condotta in Puglia su un campione di medici di base Francesca Di Serio * I dati raccolti negli
RILEVAZIONI Medici a laboratori clinici: quale rapporto e livello di comunicazione? I risultati da un indagine condotta in Puglia su un campione di medici di base Francesca Di Serio * I dati raccolti negli
La riforma del servizio di distribuzione del
 CReSV Via Röntgen, 1 Centro Ricerche su Sostenibilità e Valore 20136 Milano tel +39 025836.3626 La riforma del servizio di distribuzione del 2013 gas naturale In collaborazione con ASSOGAS Gli ambiti territoriali
CReSV Via Röntgen, 1 Centro Ricerche su Sostenibilità e Valore 20136 Milano tel +39 025836.3626 La riforma del servizio di distribuzione del 2013 gas naturale In collaborazione con ASSOGAS Gli ambiti territoriali
RISULTATI DELLA RILEVAZIONE SULLE COMMISSIONI APPLICATE DALLE BANCHE SU AFFIDAMENTI E SCOPERTI DI CONTO
 RISULTATI DELLA RILEVAZIONE SULLE COMMISSIONI APPLICATE DALLE BANCHE SU AFFIDAMENTI E SCOPERTI DI CONTO 1. Premessa La legge n. 2 del 28 gennaio 2009 ha vietato la commissione di massimo scoperto (CMS)
RISULTATI DELLA RILEVAZIONE SULLE COMMISSIONI APPLICATE DALLE BANCHE SU AFFIDAMENTI E SCOPERTI DI CONTO 1. Premessa La legge n. 2 del 28 gennaio 2009 ha vietato la commissione di massimo scoperto (CMS)
ANALISI DI RISCHIO SEMIQUANTITATIVA IN SUPPORTO ALLE VALUTAZIONI IN PRESENZA DI ATMOSFERE ESPLOSIVE (ATEX)
 ANALISI DI RISCHIO SEMIQUANTITATIVA IN SUPPORTO ALLE VALUTAZIONI IN PRESENZA DI ATMOSFERE ESPLOSIVE (ATEX) T. Pezzo *, D. Vannucci *, G. Uguccioni + * D Appolonia SpA, Genova + D Appolonia SpA, San Donato
ANALISI DI RISCHIO SEMIQUANTITATIVA IN SUPPORTO ALLE VALUTAZIONI IN PRESENZA DI ATMOSFERE ESPLOSIVE (ATEX) T. Pezzo *, D. Vannucci *, G. Uguccioni + * D Appolonia SpA, Genova + D Appolonia SpA, San Donato
Tariffari e politiche di rimborsi regionali
 L attività di day surgery nella Regione Lombardia è praticata sin dagli anni 70 in diverse strutture ospedaliere della Regione; dove venivano trattate in day hospital alcune patologie ortopediche pediatriche
L attività di day surgery nella Regione Lombardia è praticata sin dagli anni 70 in diverse strutture ospedaliere della Regione; dove venivano trattate in day hospital alcune patologie ortopediche pediatriche
STORE MANAGER.. LE COMPETENZE CARATTERISTICHE E I BISOGNI DI FORMAZIONE
 STORE MANAGER.. LE COMPETENZE CARATTERISTICHE E I BISOGNI DI FORMAZIONE 1 Indice 1. Premessa 2. Obiettivo 3. Le competenze del profilo ideale Competenze 3.1. Età ed esperienza 3.2. Le reali competenze
STORE MANAGER.. LE COMPETENZE CARATTERISTICHE E I BISOGNI DI FORMAZIONE 1 Indice 1. Premessa 2. Obiettivo 3. Le competenze del profilo ideale Competenze 3.1. Età ed esperienza 3.2. Le reali competenze
IL TRAPIANTO DI CELLULE STAMINALI
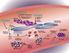 IL TRAPIANTO DI CELLULE STAMINALI Maria Teresa Petrucci (Roma) La terapia (orale, endovenosa, sottocutanea) ha un ruolo fondamentalenellaterapia nella terapia delmielomamultiploche Multiplo è una malattia
IL TRAPIANTO DI CELLULE STAMINALI Maria Teresa Petrucci (Roma) La terapia (orale, endovenosa, sottocutanea) ha un ruolo fondamentalenellaterapia nella terapia delmielomamultiploche Multiplo è una malattia
COMUNE DI RAVENNA GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI)
 COMUNE DI RAVENNA Il sistema di valutazione delle posizioni del personale dirigente GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI) Ravenna, Settembre 2004 SCHEMA DI SINTESI PER LA
COMUNE DI RAVENNA Il sistema di valutazione delle posizioni del personale dirigente GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI) Ravenna, Settembre 2004 SCHEMA DI SINTESI PER LA
PROGETTO SIMULTANEOUS HOME CARE. Dr Mauro Bandera Oncologo
 PROGETTO SIMULTANEOUS HOME CARE Dr Mauro Bandera Oncologo I progressi nella terapia dei tumori hanno portato ad una sopravvivenza a 5 anni dei 2/3 dei pazienti e di circa la metà a 10 anni dalla diagnosi.
PROGETTO SIMULTANEOUS HOME CARE Dr Mauro Bandera Oncologo I progressi nella terapia dei tumori hanno portato ad una sopravvivenza a 5 anni dei 2/3 dei pazienti e di circa la metà a 10 anni dalla diagnosi.
Quando il dolore è ancora un problema. XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013
 Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Il Direttore della Direzione Regionale Programmazione Sanitaria -Risorse Umane e Sanitarie
 Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015
 IL DOVERE E IL DIRITTO DI DARE VOCE E CURA AL DOLORE DELLA PERSONA NON IN GRADO DI RIFERIRLO Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015 Il dolore è il più soggettivo tra
IL DOVERE E IL DIRITTO DI DARE VOCE E CURA AL DOLORE DELLA PERSONA NON IN GRADO DI RIFERIRLO Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015 Il dolore è il più soggettivo tra
Le Scelte Finanziarie. S. Corsaro Matematica Finanziaria a.a. 2007/08
 Le Scelte Finanziarie 1 Tasso Interno di Rendimento Consideriamo un operazione finanziaria (t 0 =0): 0 x 0 t 1 t 2 t m...... x 1 x 2 x m Posto: x = x0, x1,, xm { } si definisce tasso interno di rendimento
Le Scelte Finanziarie 1 Tasso Interno di Rendimento Consideriamo un operazione finanziaria (t 0 =0): 0 x 0 t 1 t 2 t m...... x 1 x 2 x m Posto: x = x0, x1,, xm { } si definisce tasso interno di rendimento
CONSIGLIO NAZIONALE RAGIONIERI 00198 Roma Via G. Paisiello, 24 - www.consrag.it
 Norme di attuazione sull applicazione delle tecnologie di e-learning agli eventi formativi previsti nei programmi di formazione professionale continua per i ragionieri commercialisti Indice 1. Definizioni..3
Norme di attuazione sull applicazione delle tecnologie di e-learning agli eventi formativi previsti nei programmi di formazione professionale continua per i ragionieri commercialisti Indice 1. Definizioni..3
PROGRAMMA DI PREVENZIONE CARDIOVASCOLARE nella REGIONE VENETO
 PROGRAMMA DI PREVENZIONE CARDIOVASCOLARE nella REGIONE VENETO Il programma di prevenzione cardiovascolare è stato attivato nella Regione Veneto nel corso del 2008, dopo una fase di preparazione durata
PROGRAMMA DI PREVENZIONE CARDIOVASCOLARE nella REGIONE VENETO Il programma di prevenzione cardiovascolare è stato attivato nella Regione Veneto nel corso del 2008, dopo una fase di preparazione durata
MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO.
 ALLEGATO A MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO. il sistema organizzativo che governa le modalità di erogazione delle cure non è ancora rivolto al controllo in modo sistemico
ALLEGATO A MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO. il sistema organizzativo che governa le modalità di erogazione delle cure non è ancora rivolto al controllo in modo sistemico
PROPOSTE DI SPENDING REVIEW E SOSTENIBILITÀ DEL SERVIZIO SANITARIO NAZIONALE
 PROPOSTE DI SPENDING REVIEW E SOSTENIBILITÀ DEL SERVIZIO SANITARIO NAZIONALE NOTA A CURA DELLA DIVISIONE SALUTE, ORGANIZZAZIONE PER LA COOPERAZIONE E LO SVILUPPO ECONOMICO (OCSE), A SEGUITO DI RICHIESTA
PROPOSTE DI SPENDING REVIEW E SOSTENIBILITÀ DEL SERVIZIO SANITARIO NAZIONALE NOTA A CURA DELLA DIVISIONE SALUTE, ORGANIZZAZIONE PER LA COOPERAZIONE E LO SVILUPPO ECONOMICO (OCSE), A SEGUITO DI RICHIESTA
Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo
 Nota congiunturale Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo L indagine congiunturale di previsione per il primo trimestre 2016 di Confindustria Cuneo evidenzia
Nota congiunturale Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo L indagine congiunturale di previsione per il primo trimestre 2016 di Confindustria Cuneo evidenzia
Schema metodologico per la valutazione del personale del comparto addetto agli uffici di diretta collaborazione
 Schema metodologico per la valutazione del personale del comparto addetto agli uffici di diretta collaborazione Sommario Premessa... 2 1. Introduzione... 3 2. Criteri generali della metodologia di valutazione...
Schema metodologico per la valutazione del personale del comparto addetto agli uffici di diretta collaborazione Sommario Premessa... 2 1. Introduzione... 3 2. Criteri generali della metodologia di valutazione...
Studio di ricerca clinica sul dolore da endometriosi. Il dolore che Lei sente è reale... anche se gli altri non possono vederlo.
 Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Report di valutazione studiolegalebraggio.it
 Roma, li 15/01/2013 Report di valutazione studiolegalebraggio.it Il presente documento è redatto allo scopo di mostrare e analizzare le performance del sito web a due mesi e mezzo dalla pubblicazione online,
Roma, li 15/01/2013 Report di valutazione studiolegalebraggio.it Il presente documento è redatto allo scopo di mostrare e analizzare le performance del sito web a due mesi e mezzo dalla pubblicazione online,
LA RICERCA INFERMIERISTICA
 Prof. ssa Eufemia Renzi LA RICERCA INFERMIERISTICA DIAPOSITIVA N. 2 IL SIGNIFICATO DI RICERCA INFERMIERISTICA La ricerca infermieristica opera su due grandi aree interdipendenti: quella teorica nursing
Prof. ssa Eufemia Renzi LA RICERCA INFERMIERISTICA DIAPOSITIVA N. 2 IL SIGNIFICATO DI RICERCA INFERMIERISTICA La ricerca infermieristica opera su due grandi aree interdipendenti: quella teorica nursing
BANCA ALETTI & C. S.p.A.
 BANCA ALETTI & C. S.p.A. in qualità di Emittente e responsabile del collocamento del Programma di offerta al pubblico e/o quotazione dei certificates BORSA PROTETTA e BORSA PROTETTA con CAP e BORSA PROTETTA
BANCA ALETTI & C. S.p.A. in qualità di Emittente e responsabile del collocamento del Programma di offerta al pubblico e/o quotazione dei certificates BORSA PROTETTA e BORSA PROTETTA con CAP e BORSA PROTETTA
Economia Internazionale e Politiche Commerciali (a.a. 12/13)
 Economia Internazionale e Politiche Commerciali (a.a. 12/13) Soluzione Esame (11 gennaio 2013) Prima Parte 1. (9 p.) (a) Ipotizzate che in un mondo a due paesi, Brasile e Germania, e due prodotti, farina
Economia Internazionale e Politiche Commerciali (a.a. 12/13) Soluzione Esame (11 gennaio 2013) Prima Parte 1. (9 p.) (a) Ipotizzate che in un mondo a due paesi, Brasile e Germania, e due prodotti, farina
LA DONAZIONE DI MIDOLLO OSSEO Italian bone marrow donor registry (I.B.M.D.R.)
 LA DONAZIONE DI MIDOLLO OSSEO Italian bone marrow donor registry (I.B.M.D.R.) Donazione di midollo osseo o di cellule staminali emopoietiche da sangue periferico? Un tempo esisteva soltanto la donazione
LA DONAZIONE DI MIDOLLO OSSEO Italian bone marrow donor registry (I.B.M.D.R.) Donazione di midollo osseo o di cellule staminali emopoietiche da sangue periferico? Un tempo esisteva soltanto la donazione
Indice di rischio globale
 Indice di rischio globale Di Pietro Bottani Dottore Commercialista in Prato Introduzione Con tale studio abbiamo cercato di creare un indice generale capace di valutare il rischio economico-finanziario
Indice di rischio globale Di Pietro Bottani Dottore Commercialista in Prato Introduzione Con tale studio abbiamo cercato di creare un indice generale capace di valutare il rischio economico-finanziario
Allegato A Guida ai Diritti Guida al sito dell Autorità
 Criteri per la selezione e il finanziamento di progetti da realizzare nell ambito del Protocollo di intesa tra l Autorità per l energia elettrica e il gas e il Consiglio nazionale dei consumatori e degli
Criteri per la selezione e il finanziamento di progetti da realizzare nell ambito del Protocollo di intesa tra l Autorità per l energia elettrica e il gas e il Consiglio nazionale dei consumatori e degli
SVILUPPO, CERTIFICAZIONE E MIGLIORAMENTO DEL SISTEMA DI GESTIONE PER LA SICUREZZA SECONDO LA NORMA BS OHSAS 18001:2007
 Progettazione ed erogazione di servizi di consulenza e formazione M&IT Consulting s.r.l. Via Longhi 14/a 40128 Bologna tel. 051 6313773 - fax. 051 4154298 www.mitconsulting.it info@mitconsulting.it SVILUPPO,
Progettazione ed erogazione di servizi di consulenza e formazione M&IT Consulting s.r.l. Via Longhi 14/a 40128 Bologna tel. 051 6313773 - fax. 051 4154298 www.mitconsulting.it info@mitconsulting.it SVILUPPO,
