CINETICA ENZIMATICA - velocità di reazione
|
|
|
- Ottaviano Alessandro Montanari
- 5 anni fa
- Visualizzazioni
Transcript
1 [P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t
2 CINETICA ENZIMATICA: Condizioni iniziali e stato stazionario CONDIZIONI INIZIALI: t 0 [P] 0, k 4 0 VELOCITÀ DI CATALISI: v = k 3 [ES] eq. 1 CONDIZIONI SATURANTI: [S] è alta, tutti i siti attivi sono occupati, [ES] [E] tot v V max = k 3 [E] tot {k 3 k cat } eq. 2 CONDIZIONI SUBSATURANTI: i siti attivi sono solo parzialmente occupati k 1 E + S ES E + P k 2 d[es]/dt = k 1 [E][S] - (k 2 + k 3) [ES] (velocità formazione velocità rimozione) k 3 k 4 STATO STAZIONARIO: all inizio della reazione d[es] = 0, k 1 [E][S] = (k 2 + k 3 ) [ES] [E][S] k 1 [E][S] k 1 [E][S] ES] = (k 2 + k 3 ) = (k 2 + k 3 ) /k 1 = K M eq. 3 M
3 CINETICA ENZIMATICA: L equazione di Michaelis-Menten La K M indica l affinità dell enzima per il substrato affinità K M Se k 1 (costante di velocità di associazione) >> k 2 e k 3 (costanti di velocità di dissociazione e reazione) K M = (k 2 + k 3 )/k 1 k 1 K M La K M indica la [S] alla quale l attività dell enzima diventa significativa in natura K M varia da 10-1 a 10-7 M Il V max è raggiunto quando [ES] [E] tot, (tutto l enzima è complessato), poiché la velocità di formazione di P è proporzionale a [ES] (eq.1) (questa è una situazione avvicinabile ma non raggiungibile). Derivazione di V max In condizioni fisiologiche: se [S] >> [E] ne deriva che [S] >> [ES] e quindi [S] [S] tot (nelle condizioni iniziali)
4 [E] tot = [E] + [ES] [E] = [E] tot - [ES] (eq. 3) [ES] = [E][S] = ([E] tot - [ES])[S] = [E] tot [S] [ES] [S] K M K M K M K M [ES] K M = [E] tot [S] [ES] [S] [ES] K M + [ES] [S] = [E] tot [S] [ES] (K M + [S]) = [E] tot [S] [ES] = [E] tot [S] eq. 4 (K M + [S]) (eq. 1) Sostituendo in v = k 3 [ES] si ha v = k 3 [E] tot [S] eq. 5 (K M + [S]) siccome k3 [E] tot = Vmax (eq. 2), si ottiene Questa è l equazione di Michaelis-Menten M eq. 6 v = velocità iniziale; V max = velocità massima; [S] = conc. substrat.; K M = costante di Michaelis
5
6 L equazione di Michaelis Menten è valida per enzimi non-allosterici È valida se: 1) [E] << [S] i ; 2) [P] i 0 ; 3) d[es]/dt 0 (stato stazionario); 4) T, ph, ecc. sono costanti V max non è raggiungibile, ma alla [S] che v = V max 2 ½V max quindi K M = [S] alla quale v = ½V max In altre parole, K M = [S] alla quale metà dei siti attivi dell enzima sono occupati
7 In condizioni saturanti [S] >> K M ; (K M + [S]) [S] v V max in modo asintotico e la velocità diventa indipendente da [S] In condizioni subsaturanti, se [S] << K M V max [S] v K M ed è proporzionale alla [S] V max v L equazione di Lineweaver-Burk se consideriamo il reciproco di v eq. 7 1 V max Questa equazione descrive una relazione lineare e ci permette di determinare V max e K M -1 K M
8 Possiamo ora considerare alcuni casi che corrispondono a diverse condizioni di reazione: Caso 1 : k 1, k 2 >> k 3 cioè, l associazione e la dissociazione sono i passi limitanti K M = (k 2 + k 3 )/k 1 k 2 / k 1 K D la costante di dissociazione Caso 2 : k 2 << k 3 e siamo in condizioni subsaturanti ([S] < K M ; [ES]<< [E] [E] tot ) (enzima efficiente) [E][S] [E][S] [E] tot [S] dalle eq. 1 v = k 3 [ES] e 3 [ES] = v = k 3 v = k 3 K M K M K M k 3 / K M = k 3 k 1 /(k 2 + k 3 ) k 3 k 1 /(k 3 ) = k 1 v = k 1 [E] tot [S] Per un enzima molto efficiente il prodotto si forma immediatamente dopo la formazione del compleso ES (avviene ad ogni incontro) e P la velocità di reazione è limitata solo dalla velocità di diffusione ( M -1 s -1 in soluzioni acquose). L enzima ha raggiunto la perfezione cinetica. La velocità di diffusione può essere superata solo in complessi enzimatici multifunzionali S 3 S 2 S
9 ATTIVITÀ ENZIMATICA unità di attività L attività dell enzima (E) è una misura della sua capacità di promuovere la trasformazione del Substato a Prodotto DIVERSE UNITÀ DI ATTIVITÀ ENZIMATICA IU (International Unit): 1 IU = quantità di enzima che promuove la trasformazione di 1 mole di S in 1 min. a T ambiente. Attività specifica: Katal: = N di IU/mg di proteina (in condizioni definite) 1 katal = 1 mol/sec (normalmente espresso in nkatal) N di turnover: = moli di S trasformati per minuto per moli di enzima FATTORI CHE INFLUISCONO SULL ATTIVITÀ ENZIMATICA Temperatura ph [substrato] Inibitori/attivatori [enzima]
10 Saggi di attività Per determinare la velocità di reazione in presenza di un enzima, è necessario misurare la variazione di un determinato parametro correlato con [S] o [P] (es. assorbanza, intensità di fluorescenza, radioattività ecc ) con il tempo. v 0 [S] = 1 mm MM V MAX v 0 [S] = 0.5 mm v 0 [S] = 0.2 mm v 0 [S] mm LB 1/v 0 1/V max -1/K M 1 2 1/[S] 5 mm -1
11 Esempio di un saggio enzimatico Determinazione del K M per l alcol deidrogenasi (AD) di lievito utilizzando il metodo di Lineweaver-Burk AD CH 3 CH 2 OH + NAD + CH 3 CHO + NADH + H + Si segue la produzione di NADH spettrofotometricamente ( A = c l ; A [P] ) A = [ NADH ] 1 da/dt d[ NADH ]/dt v [S] 1/[S] v 1/v (mm) (mm -1 ) (mm/s) (mm -1 s) NB: Scegliere gli assi correttamente Fare attenzione alle unità di misura Fare attenzione all ordine di grandezza 1/K M = K M = 8.2 mm /v 60 mm -1 s -1 Rendersi conto che i dati sperimentali normalmente non sono esatti /V max = 16.5 mm -1 s 1/[S] 0.1 mm
12 Cinetica enzimatica in presenza di inibitori Inibitori REVERSIBILI: - interazione non-covalente; gli inibitori COMPETITIVI diminuiscono k 1 gli inibitori NONCOMPETITIVI diminuiscono k 3 k 1 S ES P k 2 k 3 k 4 Inibitori IRREVERSIBILI: interazione covalente o non-covalente ma molto forte
13 Inibizione competitiva E ES E + P k 6 k 5 k 1 S k 2 k 3 k 4 EI Allo stato stazionario: k 5 [E][ I ] = k 6 [ EI ] K i = k 5 /k 6 eq. 3 [ES] = [E] [S] analogamente [EI] = [E] [I] eq. 8 K M K I [E] tot = [E] + [ES] + [EI] e quindi sostituendo in eq. 3 ed eq. 8 e riarrangiando [E] = K I K M [E] tot (K I K M + K I [S] + K M [I]) eq. 9
14 Inibizione competitiva (cont.) Dalle equazioni v = k 3 [ES] (eq.1) V max = k 3 [E] tot (eq.2) e [ES] = [E][S] (eq.3) K M troviamo che v = k 3 [E][S] e sostituendo per [E] usando eq. 9 K M v = k 3 K I K M [E] tot [S] = V max K I [S] K M (K I K M + K I [S] + K M [ I ]) (K I K M + K I [S] + K M [ I ]) riarrangiando v = V max [S] una variante dell eq. MM con [S] + K M ( 1 + [ I ]/K I ) K M modificata in base a [I] e K I Trovando l inverso di V si ottiene una variante dell equazione di LB : 1 1 K M 1 [ I ] = v V max V max [S] K I
15 Inibizione noncompetitiva S E ES E + P I I EI S ESI In questo caso si può formare un complesso enzima/substrato/inibitore Più che diminuire l accesso del substrato al sito catalitico diminuisce l efficienza di catalisi stessa 1 1 K M [ I ] = v V max V max [S] K I una variante dell eq. LB con tutta l ed. modificata in base a [I] e K I
16 INIBITORI COMPETITIVI INIBITORI NONCOMPETITIVI 1 1 K M [ I ] = v V max V max [S] K I
17 prodotto saggi di inibizione enzimatica [S] costante v 0 v 0 v 0 [ I ] = 0 mm [ I ] = 0.01 mm [ I ] = 0.05 mm v 0 V 0 2 IC 50 = [ I ] che dimezza la velocità iniziale [ I ] = 0.1 mm tempo IC [ I ] 0.1 mm per inibitori COMPETITIVI che legano strettamente all enzima, l IC 50 è correlato alla costante di inibizione K i dall equazione: [S] IC 50 = ½ [E] + K i 1 + K m K i è universale, IC 50 è relativo, dipende dalle condizioni e soprattutto da [E] Per calcolare Ki : Diversi tipi di inibitori e condizioni:
18 PURIFICAZIONE DI ENZIMI PARAMETRI IMPORTANTI: Qualità, Quantità, Costo Si procede frazionando mediante opportuni metodi di purificazione. L'enzima dovrebbe concentrarsi in una sola frazione (dove la quantità di enzima aumenta rispetto ad altre proteine). Ogni successivo passaggio di purificazione dovrebbe tenere in considerazione i seguenti criteri: 1) Resa più alta possibile: resa = 2) Il grado di purificazione grado = 3) l'attività specifica attività = attività dell enzima nella frazione purificata attività dell enzima nella preparato originale attività specifica della frazione attività specifica della preparazione originale unità di enzima nella frazione quantità totale di proteina nella frazione Passaggio Proteina totale (mg) Attività totale (nmol/min) Attività specifica [(nmol/min)/mg] Grado di purificazine Resa (%) (come attività) prelievo siero (NH 4 ) 2 SO 4 (ppt) LC Scambio ionico LC Hydroph.Int LC Gel permeazione LC Fase inversa
v = Δ[P] = _ Δ[S] S P
![v = Δ[P] = _ Δ[S] S P v = Δ[P] = _ Δ[S] S P](/thumbs/98/137173050.jpg) CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
Fondamenti di Chimica Farmaceutica. Inibizione enzimatica
 Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
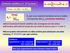 Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione -
 Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio
 Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe. Substrato
 Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA
 TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
ENZIMI. Catalizzatori delle reazioni biologiche
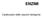 ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
Casi più complicati. inibizione mista (competitiva e non competitiva)
 Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
A = εlc c = A/εl c = 0.2/38000 M -1 cm -1 1 cm c = M = 5 μm
 COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
TARGETS DEI FARMACI ATTUALMENTE IN USO
 TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
Inibizione Enzimatica
 Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari
 Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
La cinetica enzimatica
 La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Cine%ca enzima%ca. Copyright 2013 Zanichelli editore S.p.A.
 Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Velocità di reazione
 1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
La via per accelerare i processi biologici
 La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
La cinetica enzimatica: Calcolo della K m e V max
 La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI. 1) Aumentano la velocità di reazione. 2) Non modificano l equilibrio della reazione
 PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
ENZIMI. Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle
 ENZIMI Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle condizioni fisiologiche Aumentano la velocità delle reazioni senza alterarne l equilibrio
ENZIMI Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle condizioni fisiologiche Aumentano la velocità delle reazioni senza alterarne l equilibrio
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Scaricato da 1
 A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
Determinazione dell attività enzimatica
 Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Fondamenti di Chimica Farmaceutica. Recettori come bersagli dei farmaci
 Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
In questo caso parliamo di un processo entalpico. Si tratta di un processo entalpico.
 LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
A B d A d B v dt dt A 2 B C 3 D d D 1 d C d A 1 d B v dt 3 dt dt 2 dt
 Cinetica chimica A B d A d B v A 2 B 3C D d D 1 d C d A 1 d B v 3 2 1 d[ J ] v j v f ([ A][ B]...) v k[ A] [ B]... a b k costante cinetica a, b non sono i coefficienti stechiometrici non sono necessariamente
Cinetica chimica A B d A d B v A 2 B 3C D d D 1 d C d A 1 d B v 3 2 1 d[ J ] v j v f ([ A][ B]...) v k[ A] [ B]... a b k costante cinetica a, b non sono i coefficienti stechiometrici non sono necessariamente
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Cinetica chimica. studia l influenza di variabili quali T, concentrazione dei reattivi, natura solvente, pressione...
 Cinetica chimica la cinetica chimica studia la velocità delle reazioni chimiche e i meccanismi attraverso cui i reagenti si trasformano in prodotti studia l influenza di variabili quali T, concentrazione
Cinetica chimica la cinetica chimica studia la velocità delle reazioni chimiche e i meccanismi attraverso cui i reagenti si trasformano in prodotti studia l influenza di variabili quali T, concentrazione
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
Cinetica chimica. Istantanea. Cinetica chimica : studio della velocita delle reazioni chimiche
 Cinetica chimica Cinetica chimica : studio della velocita delle reazioni chimiche La termodinamica ci dice se una reazione è possibile (termodinamicamente) ma non se è lenta o veloce. C diamante O g CO
Cinetica chimica Cinetica chimica : studio della velocita delle reazioni chimiche La termodinamica ci dice se una reazione è possibile (termodinamicamente) ma non se è lenta o veloce. C diamante O g CO
INIBIZIONE ENZIMATICA REVERSIBILE
 INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Coenzimi : NAD +, FAD + COSUBSTRATI GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Equilibri chimici. Chimica
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata Equilibri chimici Equilibrio Chimico Studio
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata Equilibri chimici Equilibrio Chimico Studio
Equilibri e Principio di Le Chatelier
 Equilibri e Principio di Le Chatelier Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY
Equilibri e Principio di Le Chatelier Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY
FOCUS SU EQUILIBRI ACIDO-BASE
 1 Ci sono varie definizioni di acidi e basi, tra le quali meritano di essere ricordate quella di Bronsted e quella di Lewis. Per i nostri fini pratici, ovvero gli esercizi, ci basta però ricordare le definizioni
1 Ci sono varie definizioni di acidi e basi, tra le quali meritano di essere ricordate quella di Bronsted e quella di Lewis. Per i nostri fini pratici, ovvero gli esercizi, ci basta però ricordare le definizioni
Amminoacidi/peptidi/proteine. Chimica Organica II
 Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Alcuni Cofattori sono associati in modo permanente con la proteina, anche mediante legami covalenti: GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Reazioni chimiche reversibili
 Reazioni chimiche reversibili In accordo all esperienza, la maggior parte delle reazioni chimiche possono procedere sia nel verso dai reagenti ai prodotti che nel verso opposto, cioè dai prodotti ai reagenti,
Reazioni chimiche reversibili In accordo all esperienza, la maggior parte delle reazioni chimiche possono procedere sia nel verso dai reagenti ai prodotti che nel verso opposto, cioè dai prodotti ai reagenti,
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Appendice cap. 29: applicazioni
 2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
I catalizzatori della cellula: gli ENZIMI
 I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
ENZIMI. Catalizzatori delle reazioni biologiche
 ENZIMI Catalizzatori delle reazioni biologiche Le tre proprietà distintive degli enzimi sono A capacità catalitica B specificità C regolazione NOMENCLATURA Gli enzimi sono classificati in base alle reazioni
ENZIMI Catalizzatori delle reazioni biologiche Le tre proprietà distintive degli enzimi sono A capacità catalitica B specificità C regolazione NOMENCLATURA Gli enzimi sono classificati in base alle reazioni
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
ESERCITAZIONI CHIMICA-FISICA I a.a. 2012/2013. Metodo differenziale. Problema
 ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
2 febbraio con 10 Pa, Pa, K, 1760 J mol e m mol. Con questi dati si ricava la temperatura finale. exp 422.
 febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Coenzimi : NAD +, FAD + COSUBSTRATI GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
GRUPPI PROSTETICI : il gruppo eme dei citocromi
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
Cinetica chimica MECCANISMO <<Lo studio CINETICO fornisce invece queste informazioni>>
 Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Per la stessa reazione possono essere utilizzati catalizzatori diversi. es. HCOOH H 2 + CO 2 viene catalizzata da Ni, Cd, Pt, Cu.
 CATALISI L'uso di un catalizzatore, sostanza capace di accelerare una reazione senza intervenire sulla T, è di enorme importanza in alcuni tipi di reazione. Ad esempio le proteine reagiscono velocemente
CATALISI L'uso di un catalizzatore, sostanza capace di accelerare una reazione senza intervenire sulla T, è di enorme importanza in alcuni tipi di reazione. Ad esempio le proteine reagiscono velocemente
Affinità ed efficacia
 Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
Comportamento di un acido forte monoprotico in soluzione (acquosa)
 Comportamento di un acido forte monoprotico in soluzione (acquosa) Acido forte monoprotico Un acido forte monoprotico in acqua si dissocia completamente secondo la reazione: HA + H 2 O H 3 O + + A (1)
Comportamento di un acido forte monoprotico in soluzione (acquosa) Acido forte monoprotico Un acido forte monoprotico in acqua si dissocia completamente secondo la reazione: HA + H 2 O H 3 O + + A (1)
2015 /2016. scaricato da
 Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Cinetica Chimica. Cinetica chimica
 Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Corso di Chimica e Propedeutica Biochimica Cinetica chimica ed enzimatica
 Corso di Chimica e Propedeutica Biochimica Cinetica chimica ed enzimatica 2 H 2 (g) + 2 (g) 2 H 2 (g) 1 Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007,
Corso di Chimica e Propedeutica Biochimica Cinetica chimica ed enzimatica 2 H 2 (g) + 2 (g) 2 H 2 (g) 1 Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007,
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%.
 Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza
 PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza Come tutti sanno, gli enzimi sono proteine semplici o coniugate capaci
PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza Come tutti sanno, gli enzimi sono proteine semplici o coniugate capaci
NOTE DI CINETICA ENZIMATICA
 NOTE DI CINETICA ENZIMATICA - 1 - Sommario Cinetica chimica... 5 Velocità di reazione.... 5 Cinetica di reazioni enzimatiche ad un substrato.... 7 Le equazioni di Michaelis-Menten e di Briggs-Haldane....
NOTE DI CINETICA ENZIMATICA - 1 - Sommario Cinetica chimica... 5 Velocità di reazione.... 5 Cinetica di reazioni enzimatiche ad un substrato.... 7 Le equazioni di Michaelis-Menten e di Briggs-Haldane....
Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]
![Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH] Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]](/thumbs/103/157927484.jpg) SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Alcuni Cofattori sono associati in modo permanente con la proteina, anche mediante legami covalenti: GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Reazioni lente e reazioni veloci
 CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
PRINCIPI DI INGEGNERIA BIOCHIMICA ESERCITAZIONI NUMERICHE A.A
 Cinetica enzimatica applicata 1) Progettare un protocollo di prove sperimentali che, impiegando un reattore CSTR a membrana ultrafiltrante, consentano la determinazione dei parametri cinetici di un enzima
Cinetica enzimatica applicata 1) Progettare un protocollo di prove sperimentali che, impiegando un reattore CSTR a membrana ultrafiltrante, consentano la determinazione dei parametri cinetici di un enzima
Reversibilità delle Reazioni Chimiche
 Reversibilità delle Reazioni Chimiche Pioggia ricca in CO 2 Terreno carsico, ricco in carbonato di calcio CaCO 3 CO 2(aq) + H 2 O (l) + CaCO 3(s) Ca 2+ (aq) + 2 HCO 3 - (aq) Nel Sottosuolo: Acqua ricca
Reversibilità delle Reazioni Chimiche Pioggia ricca in CO 2 Terreno carsico, ricco in carbonato di calcio CaCO 3 CO 2(aq) + H 2 O (l) + CaCO 3(s) Ca 2+ (aq) + 2 HCO 3 - (aq) Nel Sottosuolo: Acqua ricca
