Lowenstein Jensen Medium Selective medium for the isolation and cultivation of mycobacteria.
|
|
|
- Raffaella Anna Maria Locatelli
- 5 anni fa
- Visualizzazioni
Transcript
1 Lowenstein Jensen Medium Selective medium for the isolation and cultivation of mycobacteria. Instructions For Use ENGLISH DESCRIPTION Lowenstein Jensen Medium is a solid medium used for the selective isolation of Mycobacterium spp, especially Mycobacterium tuberculosis, from clinical specimens as well as for the cultivation of pure cultures of mycobacteria. TYPICAL FORMULA (per 600 ml purified water) L-Asparagine 3.6 g Monopotassium Phosphate 2.5 g Magnesium Sulfate 0.24 g Sodium Citrate 0.6 g Potato Flour 30.0 g Malachite Green 0.4 g Glycerol 12 ml Whole Egg Suspension 1000 ml Final ph 7.0 ± 0.2 at 25 C METHOD PRINCIPLE Asparagine and potato flour are sources of nitrogen and vitamins. Monopotassium phosphate and magnesium sulfate enhance organisms growth and act as buffers. Glycerol and whole egg suspension provide fatty acids and amino acids required for the metabolism of mycobacteria. The coagulation of the egg albumin during sterilization makes the medium solid. Sodium citrate is converted to citric acid which holds inorganic cations in solution. Malachite green is the selective agent inhibiting the contaminant microbial flora. Malachite green serves as ph indicator as well. TEST PROCEDURE Inoculate the medium according to test procedures recommended by the Centers for Disease Control and Prevention (CDC) or consult appropriate references. Protect tubes from light and incubate at 35 ± 2 C for a minimum of 8 weeks in aerobic atmosphere enriched with 5-10% carbon dioxide. To permit the circulation of CO 2 for the initiation of growth, keep caps loosened for the first week of incubation at least. Thereafter, to prevent dehydration, tighten caps; loosen briefly once a week. INTERPRETING RESULTS Examine weekly for growth, pigment production and colony morphology. Carry out identification tests according to established laboratory procedures. N.B. Negative culture results do not rule-out active infection by mycobacteria. Some factors that may lead to unsuccessful cultures are: The specimen was not representative of the infectious materials; i.e. saliva instead of sputum. The mycobacteria were destroyed during digestion and decontamination of the specimen. Gross contamination interfered with the growth of mycobacteria. Proper aerobic conditions and increased CO 2 tension were not provided during incubation. APPEARANCE Opalescent, viscous, dark blue to green. STORAGE Store at 2-8 C away from light. Do not use the product beyond its expiry date on the label or if product shows any evidence of contamination or any sign of deterioration. SHELF LIFE 1 year. Page 1 of 2
2 QUALITY CONTROL Tubes are inoculated with the microbial strains indicated in the QC table. Inoculum for productivity: CFU. Inoculum for selectivity: CFU. Incubation conditions: aerobic atmosphere with 5-10%CO 2 at 35 ± 2 C for up to 21 days. QC Table. Microorganism Growth Mycobacterium intracellulare ATCC Good Mycobacterium scrofulaceum ATCC Good Escherichia coli ATCC Partially to completely inhibited WARNING AND PRECAUTIONS The product does not contain hazardous substances in concentrations exceeding the limits set by current legislation and therefore is not classified as dangerous. It is nevertheless recommended to consult the safety data sheet for its correct use. The product is intended for in vitro diagnostic use and must be used only by properly trained operators. DISPOSAL OF WASTE Disposal of waste must be carried out according to national and local regulations in force. BIBLIOGRAPHY 1. Murray, P.R., E.J. Baron, J.H. Jorgensen, M.L. Landry, and M.A. Pfaller (2007) Manual of Clinical Microbiology. 9 th ed. ASM Press, Washington, D.C. 2. Clinical and Laboratory Standards Institute (2004) Quality Control for Commercially Prepared Microbiological Culture Media; Approved Standard, 3 rd ed. M22-A3. CLSI, Wayne, PA 3. Koneman, E.W., S.D. Allen, W.M. Janda, P.C. Schreckenberger, and W.C. Winn, Jr. (1997) Color Atlas and Textbook of Diagnostic Microbiology. 5 th ed. Lippincott Williams and Wilkins, Philadelphia, PA. 4. Kent, P.T. and G.P. Kubica (1985) Public Health Mycobacteriology, A Guide for the Level III Laboratory. Dept. of H.H.S. and Centers for Disease Control (CDC), Atlanta, GA. 5. Jensen, K.A. (1932) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 125: Lowenstein, E. (1931) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 120: PRESENTATION Contents Ref. Lowenstein Jensen Medium Flat bottom slant tubes 10 x 9 ml tubes Lowenstein Jensen Medium Round bottom slant tubes 10 x 8 ml tubes TABLE OF SYMBOLS LOT Batch code IVD In vitro Diagnostic Medical Device Manufacturer Use by Fragile, handle with care REF Catalogue number Temperature limitation Contains sufficient for <n> tests Caution, consult Instruction For Use Do not reuse LIOFILCHEM s.r.l. Via Scozia zona ind.le, Roseto degli Abruzzi (Te) Italy Tel Fax liofilchem@liofilchem.net Page 2 of 2
3 Lowenstein Jensen Medium Terreno selettivo per l isolamento e la coltivazione dei micobatteri. Istruzioni per l uso ITALIANO DESCRIZIONE Lowenstein Jensen Medium è un terreno solido utilizzato per l isolamento selettivo di Mycobacterium spp, in particolare di Mycobacterium tuberculosis, da campioni clinici ma anche per la coltivazione di colture pure di micobatteri. FORMULA TIPICA (per 600 ml di acqua purificata) L-Asparagina 3.6 g Potassio Fosfato Monobasico 2.5 g Magnesio Solfato 0.24 g Sodio Citrato 0.6 g Farina di Patate 30.0 g Verde Malachite 0.4 g Glicerolo 12 ml Emulsione d Uovo 1000 ml ph Finale 7.0 ± 0.2 a 25 C PRINCIPIO DEL METODO Asparagina e farina di patate sono fonti di azoto e vitamine. Potassio fosfato e magnesio solfato stimolano la crescita dei microrganismi ed agiscono come tamponi. Il glicerolo e l emulsione d uovo forniscono acidi grassi ed aminoacidi necessari per il metabolismo dei micobatteri. La coagulazione dell albumina d uovo durante la sterilizzazione rende il terreno solido. Il sodio citrato viene convertito in acido citrico il quale mantiene in soluzione i cationi inorganici. Il verde di malachite è l agente selettivo che inibisce la flora microbica contaminante. Il verde malachite serve anche come indicatore di ph. PROCEDURA DEL TEST Inoculare il terreno secondo le procedure raccomandate dal Centers for Disease Control and Prevention (CDC) o consultare riferimenti opportuni. Tenere le provette al riparo dalla luce ed incubare a 35 ± 2 C per un minimo di 8 settimane in atmosfera aerobica arricchita con 5-10% di anidride carbonica. Per permettere la circolazione di CO 2 e promuovere la crescita, tenere i tappi svitati almeno durante la prima settimana di incubazione. Dopo di che, avvitare i tappi una volta a settimana per prevenire la disidratazione. INTERPRETAZIONE DEI RISULTATI Esaminare settimanalmente crescita, produzione del pigmento e morfologia delle colonie. Eseguire test identificativi secondo le procedure di laboratorio previste. N.B. Risultati negativi non escludono la presenza di un infezione attiva ad opera di micobatteri. Alcuni fattori che possono condurre a colture negative sono: Il campione non era rappresentativo del materiale infetto; es. saliva invece che sputo. I micobatteri sono stati distrutti durante la digestione e decontaminazione del campione. Una contaminazione importante ha interferito con la crescita dei micobatteri. Condizioni adeguate di aerobiosi ed aumento della tensione di CO 2 non sono state rispettate durante l incubazione. ASPETTO Da blu scuro a verde, opalescente, viscoso. CONSERVAZIONE Conservare a 2-8 C al riparo dalla luce. Non usare il prodotto dopo la sua data di scadenza indicata sull etichetta o se il prodotto mostra segni di contaminazione o deterioramento. DURATA 1 anno. Pagina 1di 2
4 CONTROLLO DI QUALITÀ Le provette vengono inoculate con i ceppi microbici indicati nella tabella CQ. Inoculo per produttività: UFC. Inoculo per selettività: UFC. Condizioni di incubazione: ambiente aerobico con 5-10%CO 2 a 35 ± 2 C fino a 21 giorni. Tabella CQ. Microrganismo Crescita Mycobacterium intracellulare ATCC Buona Mycobacterium scrofulaceum ATCC Buona Escherichia coli ATCC Da parzialmente a completamente inibita AVVERTENZE E PRECAUZIONI Il prodotto non contiene sostanza nocive in concentrazioni superiori ai limiti fissati dall attuale legislazione e perciò non è classificato come pericoloso. Ciononostante si raccomanda di consultare la scheda di sicurezza per il suo corretto uso. Il prodotto è da intendersi per uso diagnostico in vitro e deve essere utilizzato esclusivamente da operatori adeguatamente addestrati. SMALTIMENTO DEI RIFIUTI Lo smaltimento dei rifiuti deve essere effettuato in conformità alle normative nazionali e locali in vigore. BIBLIOGRAFIA 1. Murray, P.R., E.J. Baron, J.H. Jorgensen, M.L. Landry, and M.A. Pfaller (2007) Manual of Clinical Microbiology. 9 th ed. ASM Press, Washington, D.C. 2. Clinical and Laboratory Standards Institute (2004) Quality Control for Commercially Prepared Microbiological Culture Media; Approved Standard, 3 rd ed. M22-A3. CLSI, Wayne, PA 3. Koneman, E.W., S.D. Allen, W.M. Janda, P.C. Schreckenberger, and W.C. Winn, Jr. (1997) Color Atlas and Textbook of Diagnostic Microbiology. 5 th ed. Lippincott Williams and Wilkins, Philadelphia, PA. 4. Kent, P.T. and G.P. Kubica (1985) Public Health Mycobacteriology, A Guide for the Level III Laboratory. Dept. of H.H.S. and Centers for Disease Control (CDC), Atlanta, GA. 5. Jensen, K.A. (1932) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 125: Lowenstein, E. (1931) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 120: PRESENTAZIONE Contenuto Ref. Lowenstein Jensen Medium Provette a becco di clarino fondo piatto 10 x 9 ml tubes Lowenstein Jensen Medium Provette a becco di clarino fondo tondo 10 x 8 ml tubes TABELLA DEI SIMBOLI LOT Codice del lotto IVD Dispositivo Medico Diagnostico in vitro Fabbricante Utilizzare entro Fragile, maneggiare con cura REF Numero di catalogo Limiti di temperatura Contenuto sufficiente per <n> saggi Attenzione, Consultare le istruzioni per l uso Non riutilizzare LIOFILCHEM s.r.l. Via Scozia zona ind.le, Roseto degli Abruzzi (Te) Italy Tel Fax liofilchem@liofilchem.net Pagina 2di 2
5 Lowenstein Jensen Medium Milieu sélectif pour l'isolement et la culture des mycobactéries. Mode d emploi FRANÇAIS DESCRIPTION Lowenstein Jensen Medium est un support solide utilisé pour l'isolement sélectif de Mycobacterium spp, en particulier Mycobacterium tuberculosis, à partir d'échantillons cliniques, ainsi que pour la culture des cultures pures de mycobactéries. FORMULE TYPQUE (per 600 ml eau purifiée) L-Asparagine 3.6 g Phosphate Monopotassique 2.5 g Sulfate de Magnésium 0.24 g Citrate de Sodium 0.6 g Potato Flour 30.0 g Vert Malachite 0.4 g Glycérol 12 ml Suspension d'oeuf Entier 1000 ml ph Final 7.0 ± 0.2 à 25 C PRINCIPE DE LA METHODE L'asparagine et de la farine de pomme de terre sont des sources d'azote et de vitamines. Phosphate monopotassique et du sulfate de magnésium améliorent la croissance des organismes et à agir comme des tampons. Le glycérol et la suspension d'œuf entier fournissent des acides gras et les acides aminés nécessaires pour le métabolisme des mycobactéries. La coagulation de l'albumine de l'œuf lors de la stérilisation rend le milieu solide. Le citrate de sodium est converti en acide citrique qui contient des cations inorganiques en solution. Le vert de malachite est l'agent sélectif inhibition de la flore microbienne de contaminants. Le vert de malachite sert indicateur de ph ainsi. PROCÉDURE DE TEST Inoculer le milieu selon les procédures de test recommandées par les Centres de Contrôle Maladies et Prévention ou consulter les références appropriées. Protéger de la lumière et incuber les tubes à 35 ± 2 C pendant au moins 8 semaines à l'atmosphère aérobie enrichie avec 5 à 10% de dioxyde de carbone. Pour permettre la circulation de CO2 pour l'initiation de la croissance, garder bouchons desserrés pour la première semaine d'incubation au moins. Par la suite, pour éviter la déshydratation, serrer casquettes; desserrer brièvement une fois par semaine. INTERPRÉTATION DES RÉSULTATS Examinez hebdomadaire pour la croissance, la production de pigments et de la morphologie des colonies. Effectuer des tests d'identification selon les procédures établies pour le laboratoire. N.B. Les résultats de culture négatifs ne excluent-out infection active par des mycobactéries. Certains facteurs qui peuvent conduire à des cultures infructueuses: L'échantillon était pas représentatif des matières infectieuses; salive à-dire au lieu de crachats. Les mycobactéries ont été détruites au cours de la digestion et décontamination de l'échantillon. Contamination brut interféré avec la croissance des mycobactéries. Des conditions aérobies appropriées et la tension de l'augmentation du CO2 n ont pas été fournies pendant l'incubation. APPARENCE Opalescente, visqueuse, bleu foncé au vert. STOCKAGE ET CONSERVATION Conserver à 2-8 C loin de la lumière. Ne pas utiliser le produit au-delà de sa date d'expiration sur l'étiquette ou si le produit montre des signes de contamination ou de tout signe de détérioration. DURÉE DE VIE 1 an. Page 1 sur 2
6 CONTRÔLE DE QUALITÉ Les tubes sont inoculés avec les souches microbiennes indiquées dans le tableau CQ. Inoculum pour la productivité: CFU. Inoculum de sélectivité: CFU. Les conditions d'incubation: atmosphère aérobie avec 5-10% de CO 2 à 35 ± 2 C pendant jusqu'à 21 jours. Tableau CQ. Microorganisme Croissance Mycobacterium intracellulare ATCC Bonne Mycobacterium scrofulaceum ATCC Bonne Escherichia coli ATCC Partièllement à complètement inhibée AVERTISSEMENT ET PRECAUTIONS Le produit ne contient pas de substances dangereuses à des concentrations dépassant les limites fixées par la législation en vigueur et est donc pas classée comme dangereuse. Il est néanmoins recommandé de consulter la fiche de données de sécurité pour leur utilisation correcte. Le produit est destiné à une utilisation diagnostique in vitro et doit être utilisé que par des opérateurs dûment formés. ÉLIMINATION DES DÉCHETS L'élimination des déchets doit être effectuée conformément aux réglementations nationales et locales en vigueur. BIBLIOGRAPHIE 1. Murray, P.R., E.J. Baron, J.H. Jorgensen, M.L. Landry, and M.A. Pfaller (2007) Manual of Clinical Microbiology. 9 th ed. ASM Press, Washington, D.C. 2. Clinical and Laboratory Standards Institute (2004) Quality Control for Commercially Prepared Microbiological Culture Media; Approved Standard, 3 rd ed. M22-A3. CLSI, Wayne, PA 3. Koneman, E.W., S.D. Allen, W.M. Janda, P.C. Schreckenberger, and W.C. Winn, Jr. (1997) Color Atlas and Textbook of Diagnostic Microbiology. 5 th ed. Lippincott Williams and Wilkins, Philadelphia, PA. 4. Kent, P.T. and G.P. Kubica (1985) Public Health Mycobacteriology, A Guide for the Level III Laboratory. Dept. of H.H.S. and Centers for Disease Control (CDC), Atlanta, GA. 5. Jensen, K.A. (1932) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 125: Lowenstein, E. (1931) Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. 1 Orig. 120: PRESENTATION Contents Ref. Lowenstein Jensen Medium Tubes à fond Plat 10 x 9 ml tubes Lowenstein Jensen Medium Tubes à fond Rond 10 x 8 ml tubes TABLE DES SYMBOLES LOT N de lot IVD A usage de Diagnostique in vitro Fabricant Utiliser par Fragile, manipuler avec soin REF Référence Température de conservation Contenu suffisant pour <n> Tests Attention, consultez Notice d'emploi Ne pas réutiliser LIOFILCHEM s.r.l. Via Scozia zona ind.le, Roseto degli Abruzzi (Te) Italy Tel Fax liofilchem@liofilchem.net Page 2 sur 2
Chromatic TM MRSA Chromogenic selective medium for the isolation of methicillin-resistant Staphylococcus aureus.
 Chromatic TM MRSA Chromogenic selective medium for the isolation of methicillin-resistant Staphylococcus aureus. Instructions For Use ENGLISH DESCRIPTION Chromatic TM MRSA is a chromogenic selective medium
Chromatic TM MRSA Chromogenic selective medium for the isolation of methicillin-resistant Staphylococcus aureus. Instructions For Use ENGLISH DESCRIPTION Chromatic TM MRSA is a chromogenic selective medium
Lowenstein Jensen + Antibiotic Media for the cultivation and susceptibility testing of mycobacteria.
 Liofilchem - Lowenstein Jensen + Antibiotic - Rev.0 / 24.04.2018 Lowenstein Jensen + Antibiotic Media for the cultivation and susceptibility testing of mycobacteria. Instructions For Use ENGLISH DESCRIPTION
Liofilchem - Lowenstein Jensen + Antibiotic - Rev.0 / 24.04.2018 Lowenstein Jensen + Antibiotic Media for the cultivation and susceptibility testing of mycobacteria. Instructions For Use ENGLISH DESCRIPTION
TEST PROCEDURE Inoculate the plates by streaking directly the sample onto the agar surface. Incubate aerobically at 37 C for hours.
 Chromatic TM Staph aureus Chromogenic selective medium for the isolation and differentiation of Staphylococcus aureus directly from clinical and nonclinical specimens. ENGLISH DESCRIPTION Chromatic TM
Chromatic TM Staph aureus Chromogenic selective medium for the isolation and differentiation of Staphylococcus aureus directly from clinical and nonclinical specimens. ENGLISH DESCRIPTION Chromatic TM
Chromatic TM ESBL Chromogenic medium for detection of ESBLs in Enterobacteriaceae directly from clinical specimens.
 Liofilchem - Chromatic TM ESBL - Rev.1 / 08.05.2014 Chromatic TM ESBL Chromogenic medium for detection of ESBLs in Enterobacteriaceae directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM
Liofilchem - Chromatic TM ESBL - Rev.1 / 08.05.2014 Chromatic TM ESBL Chromogenic medium for detection of ESBLs in Enterobacteriaceae directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM
TYPICAL FORMULA. Cronobacter sakazakii. Green to blue-green. See pictures in Appendix I.
 Enterobacter (Cronobacter) sakazakii Isolation Agar Chromogenic medium for detection of Cronobacter spp (formerly E. sakazakii), according to ISO 22964. DESCRIPTION Enterobacter (Cronobacter) sakazakii
Enterobacter (Cronobacter) sakazakii Isolation Agar Chromogenic medium for detection of Cronobacter spp (formerly E. sakazakii), according to ISO 22964. DESCRIPTION Enterobacter (Cronobacter) sakazakii
TECHNIQUE Inoculate the plates by streaking the sample onto the agar surface. Incubate at 36+/-1 for hours.
 TECHNICAL SHEET TS11058 Rev. 1 of 12.02.2009 Page 1 of 3 Selective medium for fecal streptococci enumeration and isolation, according to the formulation reported by ISO 7899-2:2000. TYPICAL FORMULA (g/l)
TECHNICAL SHEET TS11058 Rev. 1 of 12.02.2009 Page 1 of 3 Selective medium for fecal streptococci enumeration and isolation, according to the formulation reported by ISO 7899-2:2000. TYPICAL FORMULA (g/l)
PLATE COUNT AGAR Terreno per la determinazione della carica batterica totale delle superfici e dell aria
 SCHEDA TECNICA Rev.3 08.02.2012 Pagina 1 di 2 Terreno per la determinazione della carica batterica totale delle superfici e dell aria FORMULA TIPICA (g/l) Triptone 5.0 Glucosio 1.0 Estratto di lievito
SCHEDA TECNICA Rev.3 08.02.2012 Pagina 1 di 2 Terreno per la determinazione della carica batterica totale delle superfici e dell aria FORMULA TIPICA (g/l) Triptone 5.0 Glucosio 1.0 Estratto di lievito
LIOFILCHEM s.r.l. TECHNICAL SHEET TS Rev. 0 of Pag. 1 of 2
 TECHNICAL SHEET TS 34071 Rev. 0 of 04.06.2008 Pag. 1 of 2 Semi-solid basal medium used with added carbohydrates in differentiating microorganisms on fermentation reactions and motility. TYPICAL FORMULA
TECHNICAL SHEET TS 34071 Rev. 0 of 04.06.2008 Pag. 1 of 2 Semi-solid basal medium used with added carbohydrates in differentiating microorganisms on fermentation reactions and motility. TYPICAL FORMULA
For the detection of coliform bacteria in milk and milk products, with MPN technique, proceed according to ISO
 TECHNICAL SHEET TS 20102 Rev. 0 of 15.11.2007 Pag. 1 of 2 Selective medium for coliforms and faecal coliforms detection according to ISO 4832. TYPICAL FORMULA (g/l) Oxbile...... 20.0 Lactose............
TECHNICAL SHEET TS 20102 Rev. 0 of 15.11.2007 Pag. 1 of 2 Selective medium for coliforms and faecal coliforms detection according to ISO 4832. TYPICAL FORMULA (g/l) Oxbile...... 20.0 Lactose............
Chromatic TM Detection Chromogenic medium for the enumeration and identification of microorganisms directly from clinical and nonclinical specimens.
 Chromatic TM Detection Chromogenic medium for the enumeration and identification of microorganisms directly from clinical and nonclinical specimens. Instructions For Use ENGLISH DESCRIPTION Chromatic TM
Chromatic TM Detection Chromogenic medium for the enumeration and identification of microorganisms directly from clinical and nonclinical specimens. Instructions For Use ENGLISH DESCRIPTION Chromatic TM
Chromatic Bacillus cereus Chromogenic medium for detection of Bacillus cereus in food and environmental samples.
 Chromogenic medium for detection of Bacillus cereus in food and environmental samples. Instructions For Use ENGLISH DESCRIPTION Chromatic TM Bacillus cereus is a chromogenic medium used with supplements
Chromogenic medium for detection of Bacillus cereus in food and environmental samples. Instructions For Use ENGLISH DESCRIPTION Chromatic TM Bacillus cereus is a chromogenic medium used with supplements
20x SSC Solution. For use in in situ hybridization procedures. For Research Use Only. Not for use in diagnostic procedures.
 20x SSC Solution WB-0003-50 14 (50 ml) For use in in situ hybridization procedures For Research Use Only. Not for use in diagnostic procedures. 1. Scope of Application This product is designed for research
20x SSC Solution WB-0003-50 14 (50 ml) For use in in situ hybridization procedures For Research Use Only. Not for use in diagnostic procedures. 1. Scope of Application This product is designed for research
Chromatic TM VRE Chromogenic medium for the detection of Vancomycin Resistant Enterococci (VRE) directly from clinical specimens.
 Chromatic TM VRE Chromogenic medium for the detection of Vancomycin Resistant Enterococci (VRE) directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM VRE is a chromogenic medium used for the
Chromatic TM VRE Chromogenic medium for the detection of Vancomycin Resistant Enterococci (VRE) directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM VRE is a chromogenic medium used for the
MANUALE DI ISTRUZIONI
 MANUALE DI ISTRUZIONI INSTRUCTION MANUAL BEDIENUNGSANLEITUNG MANUEL D INSTRUCTION MANUAL DE INSTRUCCIONES IDE002341NOC 2 3 4 5 6 7 TRATTAMENTO DEL DISPOSITIVO ELETTRICO ED ELETTRONICO A FINE VITA Informazione
MANUALE DI ISTRUZIONI INSTRUCTION MANUAL BEDIENUNGSANLEITUNG MANUEL D INSTRUCTION MANUAL DE INSTRUCCIONES IDE002341NOC 2 3 4 5 6 7 TRATTAMENTO DEL DISPOSITIVO ELETTRICO ED ELETTRONICO A FINE VITA Informazione
Pseudomonas Agar Base Selective medium for detection and enumeration of Pseudomonas spp, according to ISO 13720, ISO/TS and ISO
 TECHNICAL SHEET Page 1 of 3 Selective medium for detection and enumeration of Pseudomonas spp, according to ISO 13720, ISO/TS 11059 and ISO 16266. TYPICAL FORMULA (g/l) Gelatin Peptone 16.0 Casein Hydrolysate
TECHNICAL SHEET Page 1 of 3 Selective medium for detection and enumeration of Pseudomonas spp, according to ISO 13720, ISO/TS 11059 and ISO 16266. TYPICAL FORMULA (g/l) Gelatin Peptone 16.0 Casein Hydrolysate
Chromatic TM ESBL Chromatic TM ESBL+AmpC Chromogenic media for detection of ESBLs and AmpC in Enterobacteriaceae directly from clinical specimens.
 Chromatic TM ESBL Chromatic TM ESBL+AmpC Chromogenic media for detection of ESBLs and AmpC in Enterobacteriaceae directly from clinical specimens. DESCRIPTION Chromatic TM ESBL is a chromogenic medium
Chromatic TM ESBL Chromatic TM ESBL+AmpC Chromogenic media for detection of ESBLs and AmpC in Enterobacteriaceae directly from clinical specimens. DESCRIPTION Chromatic TM ESBL is a chromogenic medium
MULLER HINTON AGAR Medium for susceptibility test (Kirby-Bauer method)
 TECHNICAL SHEET TS402250-412250-470070 Rev. 0 of 29.03.2007 Pag.1 of 2 MULLER HINTON AGAR Medium for susceptibility test (Kirby-Bauer method) TIPICAL FORMULA (g/l) Meat Extract.... 2.0 Casamino Acids,
TECHNICAL SHEET TS402250-412250-470070 Rev. 0 of 29.03.2007 Pag.1 of 2 MULLER HINTON AGAR Medium for susceptibility test (Kirby-Bauer method) TIPICAL FORMULA (g/l) Meat Extract.... 2.0 Casamino Acids,
Terreni BBL in flacone e in provetta pronti per l uso per la coltivazione selettiva di funghi
 Terreni BBL in flacone e in provetta pronti per l uso per la coltivazione selettiva di funghi 8806361JAA 2004/06 Italiano BBL Sabouraud Dextrose Agar, Emmons, with Gentamicin Vedere il glossario dei simboli
Terreni BBL in flacone e in provetta pronti per l uso per la coltivazione selettiva di funghi 8806361JAA 2004/06 Italiano BBL Sabouraud Dextrose Agar, Emmons, with Gentamicin Vedere il glossario dei simboli
BBL Middlebrook 7H9 Broth with Glycerol
 BBL Middlebrook 7H9 Broth with Glycerol Rev. 12 ottobre 2015 PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) I II INTRODUZIONE Middlebrook 7H9 Broth with Glycerol è un terreno di coltura non selettivo
BBL Middlebrook 7H9 Broth with Glycerol Rev. 12 ottobre 2015 PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) I II INTRODUZIONE Middlebrook 7H9 Broth with Glycerol è un terreno di coltura non selettivo
Liofilchem - Tryptic Soy Broth - Rev.0.1 / Instructions For Use ENGLISH
 Liofilchem - - Rev.0.1 / 27.01.2017 Casein Soya Bean Digest Broth Liquid medium for the isolation and cultivation of a wide variety of organisms, according to USP/EP/JP. Instructions For Use ENGLISH DESCRIPTION
Liofilchem - - Rev.0.1 / 27.01.2017 Casein Soya Bean Digest Broth Liquid medium for the isolation and cultivation of a wide variety of organisms, according to USP/EP/JP. Instructions For Use ENGLISH DESCRIPTION
DICHIARAZIONE DI PRESTAZIONE 2015/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2015/552 1. Codice di identificazione unico del prodotto-tipo: BETONPRIMER 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
DICHIARAZIONE DI PRESTAZIONE N 2015/552 1. Codice di identificazione unico del prodotto-tipo: BETONPRIMER 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
Chromatic TM Coliform Agar ISO Chromogenic medium for detection and enumeration of E. coli and coliform bacteria in water, according to ISO 9308-1.
 Liofilchem - Chromatic TM Coliform Agar ISO- Rev.0.2 / 24.04.2015 Chromatic TM Coliform Agar ISO Chromogenic medium for detection and enumeration of E. coli and coliform bacteria in water, according to
Liofilchem - Chromatic TM Coliform Agar ISO- Rev.0.2 / 24.04.2015 Chromatic TM Coliform Agar ISO Chromogenic medium for detection and enumeration of E. coli and coliform bacteria in water, according to
BBL Lowenstein-Jensen Medium BBL Lowenstein-Jensen Medium with 5% Sodium Chloride
 BBL Lowenstein-Jensen Medium BBL Lowenstein-Jensen Medium with 5% Sodium Chloride Rev. 11 Ottobre 2015 I PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) INTRODUZIONE Lowenstein-Jensen Medium viene utilizzato
BBL Lowenstein-Jensen Medium BBL Lowenstein-Jensen Medium with 5% Sodium Chloride Rev. 11 Ottobre 2015 I PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) INTRODUZIONE Lowenstein-Jensen Medium viene utilizzato
SensiQuattro Gram-negative
 SensiQuattro Gram-negative System for determination of the Minimum Inhibitory Concentration (MIC) of gram-negative bacteria with the broth microdilution method. Ref. 76031-79031 Contents Page Italiano
SensiQuattro Gram-negative System for determination of the Minimum Inhibitory Concentration (MIC) of gram-negative bacteria with the broth microdilution method. Ref. 76031-79031 Contents Page Italiano
DICHIARAZIONE DI PRESTAZIONE 2015/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2015/449 1. Codice di identificazione unico del prodotto-tipo: FLESSCOAT GRAFF.S MEDIO 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi
DICHIARAZIONE DI PRESTAZIONE N 2015/449 1. Codice di identificazione unico del prodotto-tipo: FLESSCOAT GRAFF.S MEDIO 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi
DICHIARAZIONE DI PRESTAZIONE 2014/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2014/234 1. Codice di identificazione unico del prodotto-tipo : ANCORALL G C.A. KG 24,25 BASE 9 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione
DICHIARAZIONE DI PRESTAZIONE N 2014/234 1. Codice di identificazione unico del prodotto-tipo : ANCORALL G C.A. KG 24,25 BASE 9 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione
DICHIARAZIONE DI PRESTAZIONE N 2013/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2013/089 1. Codice di identificazione unico del prodotto-tipo : BETON PRIMER 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
DICHIARAZIONE DI PRESTAZIONE N 2013/089 1. Codice di identificazione unico del prodotto-tipo : BETON PRIMER 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
!" " " " """""""""""""""""""""""""""""""""" """""""""""""""""""""" JAA 2005/07 Italiano
 !" " " " """""""""""""""""""""""""""""""""" """""""""""""""""""""" 8814091JAA 2005/07 Italiano #" Terreno BBL in flacone e in provetta pronto per l uso, per la rilevazione e l identificazione presuntiva
!" " " " """""""""""""""""""""""""""""""""" """""""""""""""""""""" 8814091JAA 2005/07 Italiano #" Terreno BBL in flacone e in provetta pronto per l uso, per la rilevazione e l identificazione presuntiva
BBL Seven H11 Agar. L Rev. 11 Aprile 2015 PROCEDURE DI CONTROLLO DI QUALITÀ
 BBL Seven H11 Agar Rev. 11 Aprile 2015 PROCEDURE DI CONTROLLO DI QUALITÀ I II INTRODUZIONE BBL Seven H11 Agar è un terreno di coltura per l isolamento e la coltivazione di micobatteri. PROCEDURA DEL TEST
BBL Seven H11 Agar Rev. 11 Aprile 2015 PROCEDURE DI CONTROLLO DI QUALITÀ I II INTRODUZIONE BBL Seven H11 Agar è un terreno di coltura per l isolamento e la coltivazione di micobatteri. PROCEDURA DEL TEST
SensiQuattro Gram-positive
 SensiQuattro Gram-positive System for determination of the Minimum Inhibitory Concentration (MIC) of gram-positive bacteria with the broth microdilution method. Ref. 76032-79032 Contents Page Italiano
SensiQuattro Gram-positive System for determination of the Minimum Inhibitory Concentration (MIC) of gram-positive bacteria with the broth microdilution method. Ref. 76032-79032 Contents Page Italiano
Convegno Qualità Microbiologica dei Cosmetici: Aspetti Tecnici e Normativi Milano, 15 maggio Lucia Bonadonna Istituto Superiore di Sanità
 Convegno Qualità Microbiologica dei Cosmetici: Aspetti Tecnici e Normativi Milano, 15 maggio 2015 Lucia Bonadonna Istituto Superiore di Sanità REGOLAMENTO (CE) n. 1223/2009 DEL PARLAMENTO EUROPEO E DEL
Convegno Qualità Microbiologica dei Cosmetici: Aspetti Tecnici e Normativi Milano, 15 maggio 2015 Lucia Bonadonna Istituto Superiore di Sanità REGOLAMENTO (CE) n. 1223/2009 DEL PARLAMENTO EUROPEO E DEL
DICHIARAZIONE DI PRESTAZIONE 2015/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2015/477 1. Codice di identificazione unico del prodotto-tipo: BETONSET MAR 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
DICHIARAZIONE DI PRESTAZIONE N 2015/477 1. Codice di identificazione unico del prodotto-tipo: BETONSET MAR 2. Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
Terreni BBL in flacone e in provetta pronti per l uso - Selective Sabouraud Brain Heart Infusion Agars for Cultivation of Fungi
 8806701 2003/08 Terreni BBL in flacone e in provetta pronti per l uso - Selective Sabouraud Brain Heart Infusion Agars for Cultivation of Fungi BBL Sabouraud Brain Heart Infusion Sheep Blood Agar with
8806701 2003/08 Terreni BBL in flacone e in provetta pronti per l uso - Selective Sabouraud Brain Heart Infusion Agars for Cultivation of Fungi BBL Sabouraud Brain Heart Infusion Sheep Blood Agar with
ELCART ART. 19/ /13275 PAGINA 1 DI 8. servizio automatico documentazione tecnica
 ART. 19/13270-19/13275 PAGINA 1 DI 8 DISTRIBUTION SPA via Michelangelo Buonarroti, 46-20093 Cologno Monzese (Milano) ITALY ART. 19/13270-19/13275 PAGINA 2 DI 8 DISTRIBUTION SPA via Michelangelo Buonarroti,
ART. 19/13270-19/13275 PAGINA 1 DI 8 DISTRIBUTION SPA via Michelangelo Buonarroti, 46-20093 Cologno Monzese (Milano) ITALY ART. 19/13270-19/13275 PAGINA 2 DI 8 DISTRIBUTION SPA via Michelangelo Buonarroti,
AmpC disc kit Disc tests for confirmation of AmpC producing organisms.
 Liofilchem - - Rev.0.1 / 08.09.2015 Disc tests for confirmation of AmpC producing organisms. ENGLISH DESCRIPTION AmpC β-lactamases are enzymes encoded on the chromosome of many Enterobacteriaceae and a
Liofilchem - - Rev.0.1 / 08.09.2015 Disc tests for confirmation of AmpC producing organisms. ENGLISH DESCRIPTION AmpC β-lactamases are enzymes encoded on the chromosome of many Enterobacteriaceae and a
SensiQuattro CANDIDA EU
 SensiQuattro CANDIDA EU Panel for determining the susceptibility testing of Candida spp. with antimycotic agents. Ref. 76033-79033 Contents Page Italiano 1 English 4 Code F00043 Rev.2 / 13.12.2012 SensiQuattro
SensiQuattro CANDIDA EU Panel for determining the susceptibility testing of Candida spp. with antimycotic agents. Ref. 76033-79033 Contents Page Italiano 1 English 4 Code F00043 Rev.2 / 13.12.2012 SensiQuattro
DICHIARAZIONE DI PRESTAZIONE 2015/ Numero di tipo, lotto, serie (identificazione del prodotto da costruzione ai sensi dell art.
 DICHIARAZIONE DI PRESTAZIONE N 2015/443 1. Codice di identificazione unico del prodotto-tipo: ADESAN CPV 22 BIANCO; ADESAN CPV 22 GRIGIO 2. Numero di tipo, lotto, serie (identificazione del prodotto da
DICHIARAZIONE DI PRESTAZIONE N 2015/443 1. Codice di identificazione unico del prodotto-tipo: ADESAN CPV 22 BIANCO; ADESAN CPV 22 GRIGIO 2. Numero di tipo, lotto, serie (identificazione del prodotto da
Sensi Test gram-positive
 Sensi Test gram-positive System for the susceptibility testing of gram-positive bacteria REF.76020 Contents Page Italiano 1 English 4 Code F03913 Rev.1 / 20.04.2006 Sensi Test gram-positive Sistema per
Sensi Test gram-positive System for the susceptibility testing of gram-positive bacteria REF.76020 Contents Page Italiano 1 English 4 Code F03913 Rev.1 / 20.04.2006 Sensi Test gram-positive Sistema per
Foglio Integrativo del manuale Serie Trivalente
 Foglio Integrativo del manuale Serie Trivalente AVVERTENZE GENERALI! Questa apparecchiatura deve essere usata utilizzando esclusivamente gas GPL G0/G (butano/propano) alla pressione di 8-0/7 mbar IT COMANDI!
Foglio Integrativo del manuale Serie Trivalente AVVERTENZE GENERALI! Questa apparecchiatura deve essere usata utilizzando esclusivamente gas GPL G0/G (butano/propano) alla pressione di 8-0/7 mbar IT COMANDI!
istruzioni di montaggio - manutenzione BASI LUMINOSE - BLE
 IS_029_0_0 istruzioni di montaggio - manutenzione prodotto rispondente ai requisiti previsti dalle Direttive Comunitarie Europee BASI LUMINOSE - BLE NOTA BENE: le presenti istruzioni di montaggio informano
IS_029_0_0 istruzioni di montaggio - manutenzione prodotto rispondente ai requisiti previsti dalle Direttive Comunitarie Europee BASI LUMINOSE - BLE NOTA BENE: le presenti istruzioni di montaggio informano
Copyright by Albini & Fontanot spa, prima pubblicazione 4 aprile 2011 Magia70
 STYLE: www.fontanot.it Copyright by Albini & Fontanot spa, prima pubblicazione 4 aprile 0 - - ,5 mm mm 5 mm 1 mm PH 1 mm 0 mm,5 mm mm 4,5 mm 1 x 10 mm x 0 mm - - 1-4 - 1 1 1 4 5 1 1 A1 A7 A 45 x 100 mm
STYLE: www.fontanot.it Copyright by Albini & Fontanot spa, prima pubblicazione 4 aprile 0 - - ,5 mm mm 5 mm 1 mm PH 1 mm 0 mm,5 mm mm 4,5 mm 1 x 10 mm x 0 mm - - 1-4 - 1 1 1 4 5 1 1 A1 A7 A 45 x 100 mm
Instructions For Use ENGLISH
 Chromatic TM MH Chromogenic Mueller Hinton for the microbial differentiation simultaneously with susceptibility testing directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM MH is a chromogenic
Chromatic TM MH Chromogenic Mueller Hinton for the microbial differentiation simultaneously with susceptibility testing directly from clinical specimens. ENGLISH DESCRIPTION Chromatic TM MH is a chromogenic
DAPI/DuraTect-Solution
 DAPI/DuraTect-Solution MT-0007-0.8 20 (0.8 ml) For use in in situ hybridization procedures.... In vitro diagnostic medical device according to EU directive 98/79/EC 1. Scope of Application This product
DAPI/DuraTect-Solution MT-0007-0.8 20 (0.8 ml) For use in in situ hybridization procedures.... In vitro diagnostic medical device according to EU directive 98/79/EC 1. Scope of Application This product
RAPPORTO DI CLASSIFICAZIONE DI RESISTENZA AL N. 2016CS C. RESISTANCE TO FIRE CLASSIFICATION REPORT No. RAPPORTO DI CLASSIFICAZIONE N.
 Pagina 1 di 7 Page 1 of 7 FUOCO IN ACCORDO ALLA NORMA EN 13501-2:2016 CLASSIFICATION OF FIRE RESISTANCE IN ACCORDANCE WITH EN 13501-2:2016 PROPRIETARIO DEL RAPPORTO DI CLASSIFICAZIONE: SPONSOR: DIERRE
Pagina 1 di 7 Page 1 of 7 FUOCO IN ACCORDO ALLA NORMA EN 13501-2:2016 CLASSIFICATION OF FIRE RESISTANCE IN ACCORDANCE WITH EN 13501-2:2016 PROPRIETARIO DEL RAPPORTO DI CLASSIFICAZIONE: SPONSOR: DIERRE
CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR
 CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR Codice CND W050301020180 PROVETTE IN MATERIALE PLASTICO PER ANALISI - ACCESSORI Code 128A on the box side CARATTERISTICHE
CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR Codice CND W050301020180 PROVETTE IN MATERIALE PLASTICO PER ANALISI - ACCESSORI Code 128A on the box side CARATTERISTICHE
BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride
 BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride Rev. 12 Settembre 2014 PROCEDURE DI CONTROLLO DI QUALITÀ I II INTRODUZIONE BBL Brain Heart Infusion (BHI) (infuso cuore-cervello)
BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride Rev. 12 Settembre 2014 PROCEDURE DI CONTROLLO DI QUALITÀ I II INTRODUZIONE BBL Brain Heart Infusion (BHI) (infuso cuore-cervello)
DISC DISPENSER 8. Antibiotic discs dispenser. Ref Italiano 1 English 4
 DISC DISPENSER 8 Antibiotic discs dispenser Ref. 91200 Contents page Italiano 1 English 4 Rev.1 / 03.10.2012 chem chem compan chem - DISC DISPENSER 8 - Rev.1 / 03.10.2012 DISC DISPENSER 8 Dispensatore
DISC DISPENSER 8 Antibiotic discs dispenser Ref. 91200 Contents page Italiano 1 English 4 Rev.1 / 03.10.2012 chem chem compan chem - DISC DISPENSER 8 - Rev.1 / 03.10.2012 DISC DISPENSER 8 Dispensatore
TEST REPORT: VERIFICA DEL POTERE ANTIMICROBICO IN VITRO : METODO IN SUPERFICIE
 DIPARTIMENTO DI MEDICINA SPERIMENTALE E DIAGNOSTICA / DPT. EXP. & DIAGNOSTIC MEDICINE Via LUIGI BORSARI, 46 44100 FERRARA - ITALY TEST REPORT: VERIFICA DEL POTERE ANTIMICROBICO IN VITRO : METODO IN SUPERFICIE
DIPARTIMENTO DI MEDICINA SPERIMENTALE E DIAGNOSTICA / DPT. EXP. & DIAGNOSTIC MEDICINE Via LUIGI BORSARI, 46 44100 FERRARA - ITALY TEST REPORT: VERIFICA DEL POTERE ANTIMICROBICO IN VITRO : METODO IN SUPERFICIE
Sabouraud CAF Agar + Actidione Selective medium for isolation and cultivation of dermatophytes and other fungi.
 Sabouraud CAF Agar + Actidione Selective medium for isolation and cultivation of dermatophytes and other fungi. Instructions For Use ENGLISH DESCRIPTION Sabouraud CAF Agar + Actidione is a selective medium
Sabouraud CAF Agar + Actidione Selective medium for isolation and cultivation of dermatophytes and other fungi. Instructions For Use ENGLISH DESCRIPTION Sabouraud CAF Agar + Actidione is a selective medium
REPORT VERIFICA POTERE ANTIMICROBICO
 UNIVERSITÀ DEGLI STUDI DI FERRARA / UNIVERSITY OF FERRARA DIPARTIMENTO DI MEDICINA SPERIMENTALE E DIAGNOSTICA / DPT. EXP. & DIAGNOSTIC MEDICINE SEZIONE DI MICROBIOLOGIA / SECTION OF MICROBIOLOGY via LUIGI
UNIVERSITÀ DEGLI STUDI DI FERRARA / UNIVERSITY OF FERRARA DIPARTIMENTO DI MEDICINA SPERIMENTALE E DIAGNOSTICA / DPT. EXP. & DIAGNOSTIC MEDICINE SEZIONE DI MICROBIOLOGIA / SECTION OF MICROBIOLOGY via LUIGI
Giulietta BE T ISTRUZIONI DI MONTAGGIO / ASSEMBLY INSTRUCTIONS / INSTRUCTIONS DE MONTAGE / MONTAGEANLEITUNGEN / INSTRUCCIONES DE MONTAJE
 Giulietta BE T table ISTRUZIONI DI MONTAGGIO / ASSEMBLY INSTRUCTIONS / INSTRUCTIONS DE MONTAGE / MONTAGEANLEITUNGEN / INSTRUCCIONES DE MONTAJE www.catellanismith.com AVVERTENZE Si consiglia l utilizzo
Giulietta BE T table ISTRUZIONI DI MONTAGGIO / ASSEMBLY INSTRUCTIONS / INSTRUCTIONS DE MONTAGE / MONTAGEANLEITUNGEN / INSTRUCCIONES DE MONTAJE www.catellanismith.com AVVERTENZE Si consiglia l utilizzo
NGA x 8x x x GR. 2x GR GR GR. 4x GR. 4x GR. 4x GR. 8x
 NEW GENERATION NGA1 NGA1 9001289 9004035 9001289 2x 8x 9004035 55000210 810072GR 810273GR 2x 810009GR 2x 810197GR 8x 810145 810172GR 810198GR 810257GR 810206GR 890002GR 810258GR 810259GR 6x 810025GR 6x
NEW GENERATION NGA1 NGA1 9001289 9004035 9001289 2x 8x 9004035 55000210 810072GR 810273GR 2x 810009GR 2x 810197GR 8x 810145 810172GR 810198GR 810257GR 810206GR 890002GR 810258GR 810259GR 6x 810025GR 6x
Mycoplasma System VET Sistema per conteggio, identificazione ed antibiogramma dei micoplasmi di interesse veterinario.
 Mycoplasma System VET Sistema per conteggio, identificazione ed antibiogramma dei micoplasmi di interesse veterinario. ITALIANO DESCRIZIONE Mycoplasma System VET è un sistema a 24 pozzetti contenente substrati
Mycoplasma System VET Sistema per conteggio, identificazione ed antibiogramma dei micoplasmi di interesse veterinario. ITALIANO DESCRIZIONE Mycoplasma System VET è un sistema a 24 pozzetti contenente substrati
COSTRUZIONI CONSTRUCTION REAZIONE REACTION 0550\DC\REA\12_4 21/09/2012. Product Name. Descrizione : Vedi pagina 2 Description : See page 2
 COSTRUZIONI CONSTRUCTION REAZIONE REACTION 1 Nome commerciale Product Name : K-FLEX SOLAR Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX S.r.l. Indirizzo / Address
COSTRUZIONI CONSTRUCTION REAZIONE REACTION 1 Nome commerciale Product Name : K-FLEX SOLAR Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX S.r.l. Indirizzo / Address
RAPPORTO DI CLASSIFICAZIONE CLASSIFICATION REPORT 0412\DC\REA\12_5
 RAPPORTO DI CLASSIFICAZIONE CLASSIFICATION REPORT 0412\DC\REA\12_5 Rapporto di classificazione di reazione al fuoco del prodotto : Reaction to fire classification report of product BETON COLOR Descrizione
RAPPORTO DI CLASSIFICAZIONE CLASSIFICATION REPORT 0412\DC\REA\12_5 Rapporto di classificazione di reazione al fuoco del prodotto : Reaction to fire classification report of product BETON COLOR Descrizione
Norma Tecnica / Norme Technique: NF D :2006 Regola tecnica /Règle Technique: Arrêté 25 juin 1980 modifié (art. AM 18) arrêté 6 mars 2006
 COSTRUZIONI REAZIONE 1/5 Nome / Object... : SERIE INVENTA CONTRACT Nome / Nome...: INVENTA CONTRACT S.r.l. Indirizzo / Adresse...: Via Antonio Bracci, 6 Città / Ville...: 61122 Pesaro (PU)) - Italia Norma
COSTRUZIONI REAZIONE 1/5 Nome / Object... : SERIE INVENTA CONTRACT Nome / Nome...: INVENTA CONTRACT S.r.l. Indirizzo / Adresse...: Via Antonio Bracci, 6 Città / Ville...: 61122 Pesaro (PU)) - Italia Norma
SonDa acqua SanitaRia
 SonDa acqua SanitaRia IT avvertenze PrelIMINarI questa istruzione è parte integrante del libretto dell apparecchio sul quale viene installato il Kit. a tale libretto si rimanda per le avvertenze GEnERaLi
SonDa acqua SanitaRia IT avvertenze PrelIMINarI questa istruzione è parte integrante del libretto dell apparecchio sul quale viene installato il Kit. a tale libretto si rimanda per le avvertenze GEnERaLi
RAPPORTO DI CLASSIFICAZIONE RAPPORT DE CLASSEMENT 0314\DC\REA\12
 RAPPORTO DI CLASSIFICAZIONE RAPPORT DE CLASSEMENT 0314\DC\REA\12 Rapporto di classificazione di reazione al fuoco del prodotto : Rapport de classement de of product Descrizione : Description : MODULIT
RAPPORTO DI CLASSIFICAZIONE RAPPORT DE CLASSEMENT 0314\DC\REA\12 Rapporto di classificazione di reazione al fuoco del prodotto : Rapport de classement de of product Descrizione : Description : MODULIT
HACCP-SYSTEM Plus. REAZIONI BIOCHIMICHE PER IDENTIFICAZIONE Decarbossilazione della Lisina 5-H 2S Produzione di Idrogeno Solforato 4-LDC
 HACCP-SYSTEM Plus Sistema per la determinazione della carica microbica totale e per la ricerca e l identificazione presuntiva di germi patogeni isolabili da superfici di lavoro ITALIANO DESCRIZIONE HACCP-SYSTEM
HACCP-SYSTEM Plus Sistema per la determinazione della carica microbica totale e per la ricerca e l identificazione presuntiva di germi patogeni isolabili da superfici di lavoro ITALIANO DESCRIZIONE HACCP-SYSTEM
SPECIFICA TECNICA TECHNICAL SPECIFICATION
 CAS EINECS / ELINCS 12209-98-2 234-724-5 SPECIFICA SPECIFICATION METODO METHOD Lim. Inf. - Lim. Sup. Lower Lim. - Upper Lim. u.m. * Descrizione Description Polvere bianco nocciola White hazel powder *
CAS EINECS / ELINCS 12209-98-2 234-724-5 SPECIFICA SPECIFICATION METODO METHOD Lim. Inf. - Lim. Sup. Lower Lim. - Upper Lim. u.m. * Descrizione Description Polvere bianco nocciola White hazel powder *
Manuale di Installazione Installationshandbuch / Manual de Instalación V _E_SmartKEY_160914_v2.2
 SmartKEY Manuale di Installazione Installation manual / Notice technique Installationshandbuch / Manual de Instalación V.. 90050_E_SmartKEY_6094_v. PRINCIPIO DI FUNZIONAMENTO OPERATING PRINCIPLE Centralina
SmartKEY Manuale di Installazione Installation manual / Notice technique Installationshandbuch / Manual de Instalación V.. 90050_E_SmartKEY_6094_v. PRINCIPIO DI FUNZIONAMENTO OPERATING PRINCIPLE Centralina
DICHIARAZIONE DI CONFORMITA ACCESSORI IN PA+ sono conformi
 DICHIARAZIONE DI CONFORMITA ACCESSORI IN PA+ 1 Con la presente si dichiara che gli accessori in PA+ sono composti da: - Materiale Corpo: Poliammide (nylon 6.6) con fibra di vetro sono conformi a tutte
DICHIARAZIONE DI CONFORMITA ACCESSORI IN PA+ 1 Con la presente si dichiara che gli accessori in PA+ sono composti da: - Materiale Corpo: Poliammide (nylon 6.6) con fibra di vetro sono conformi a tutte
CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR
 CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR Codice CND W0503020180 PROVETTE IN MATERIALE PLASTICO PER ANALISI - ACCESSORI Code 128A on the box side CARATTERISTICHE
CryoGen Box1D CON CODICE A BARRE LINEARE IDEALE PER WITH LINEAR BARCODE IDEAL FOR Codice CND W0503020180 PROVETTE IN MATERIALE PLASTICO PER ANALISI - ACCESSORI Code 128A on the box side CARATTERISTICHE
INTERPRETATION OF RESULTS
 TECHNICAL SHEET Page 1 of 3 Clostridium perfringens Agar Base Basal medium for detection of C. perfringens from clinical specimens and other materials according to ISO 7937 and ISO 14189. TYPICAL FORMULA
TECHNICAL SHEET Page 1 of 3 Clostridium perfringens Agar Base Basal medium for detection of C. perfringens from clinical specimens and other materials according to ISO 7937 and ISO 14189. TYPICAL FORMULA
Materiale / Material: PP COLORI / COLORS
 EXTRA IGIENE CON: visit www.microban.com* Melamine FREE BPA FREE 100% Recyclable Microban 3G Silver technology are 99.9% effective against harmful bacteria / Microban 3G Silver TM efficace al 99,9% contro
EXTRA IGIENE CON: visit www.microban.com* Melamine FREE BPA FREE 100% Recyclable Microban 3G Silver technology are 99.9% effective against harmful bacteria / Microban 3G Silver TM efficace al 99,9% contro
BBL Fluid Thioglycollate Medium
 BBL Fluid Thioglycollate Medium Rev. 13 Ottobre 2015 I II PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) INTRODUZIONE BBL Fluid Thioglycollate Medium (terreno tioglicollato fluido BBL) è un terreno universale
BBL Fluid Thioglycollate Medium Rev. 13 Ottobre 2015 I II PROCEDURE DI CONTROLLO DI QUALITÀ (Facoltativo) INTRODUZIONE BBL Fluid Thioglycollate Medium (terreno tioglicollato fluido BBL) è un terreno universale
TEST TUBES AND ACCESSORIES PROVETTE E ACCESSORI
 TEST TUBES AND ACCESSORIES PROVETTE E ACCESSORI 167 TPX CYLINDRICAL TEST TUBES PROVETTE CILINDRICHE IN TPX Transparent, non graduated, with rim, autoclavable, resistant to acids, to concentrated solvents
TEST TUBES AND ACCESSORIES PROVETTE E ACCESSORI 167 TPX CYLINDRICAL TEST TUBES PROVETTE CILINDRICHE IN TPX Transparent, non graduated, with rim, autoclavable, resistant to acids, to concentrated solvents
BD Modified CNA Agar BD Modified CNA Agar with Crystal Violet
 ISTRUZIONI PER L'USO TERRENI SU PIASTRA PRONTI ALL'USO PA-255082.02 Rev.: giugno 2003 BD Modified CNA Agar BD Modified CNA Agar with Crystal Violet USO PREVISTO BD Modified CNA Agar (agar CNA modificato)
ISTRUZIONI PER L'USO TERRENI SU PIASTRA PRONTI ALL'USO PA-255082.02 Rev.: giugno 2003 BD Modified CNA Agar BD Modified CNA Agar with Crystal Violet USO PREVISTO BD Modified CNA Agar (agar CNA modificato)
HALL LED IP65 EASY. // Istruzioni per il montaggio // Assembly instructions
 HALL LED IP65 EASY IP 65 // Istruzioni per il montaggio // Assembly instructions Gli apparecchi non sono idonei ad essere coperti con materiale termoisolante Luminaires not suitable for covering with thermally
HALL LED IP65 EASY IP 65 // Istruzioni per il montaggio // Assembly instructions Gli apparecchi non sono idonei ad essere coperti con materiale termoisolante Luminaires not suitable for covering with thermally
REPORT CHALLENGE TEST METODO ISO 11930:2012
 REPORT CHALLENGE TEST METODO ISO 11930:2012 Valutazione in vitro del sistema preservante di un prodotto cosmetico in base al metodo ISO 11930:2012, secondo il Regolamento 1223/2009 COD. LAB.: 1709052 Data
REPORT CHALLENGE TEST METODO ISO 11930:2012 Valutazione in vitro del sistema preservante di un prodotto cosmetico in base al metodo ISO 11930:2012, secondo il Regolamento 1223/2009 COD. LAB.: 1709052 Data
Pag. 1 di 7 / Page 1 out of 7
 DETERMINAZIONE in vitro DELL ATTIVITÀ BATTERICIDA O BATTERIOSTATICA E DELL ATTIVITÀ FUNGICIDA COD. LAB.: 1805032 Data emissione: 20/06/2018 Rev. 1: 10/11/2018 Efficacia microbica in vitro Committente /
DETERMINAZIONE in vitro DELL ATTIVITÀ BATTERICIDA O BATTERIOSTATICA E DELL ATTIVITÀ FUNGICIDA COD. LAB.: 1805032 Data emissione: 20/06/2018 Rev. 1: 10/11/2018 Efficacia microbica in vitro Committente /
ISTRUZIONI PER L USO
 ISTRUZIONI PER L USO 2797 Prodotti Helix Elite Molecular Standards (pellet inattivato) Chlamydia Cytomegalovirus USO PREVISTO Gli standard molecolari Helix Elite (pellet inattivati) e i set CQ con pannelli
ISTRUZIONI PER L USO 2797 Prodotti Helix Elite Molecular Standards (pellet inattivato) Chlamydia Cytomegalovirus USO PREVISTO Gli standard molecolari Helix Elite (pellet inattivati) e i set CQ con pannelli
ELCART ART. 12/23040 PAGINA 1 DI 6. servizio automatico documentazione tecnica
 ART. 12/23040 PAGINA 1 DI 6 DISTRIBUTION SPA via Michelangelo Buonarroti, 46-20093 Cologno Monzese (Milano) ITALY ART. 12/23040 PAGINA 2 DI 6 Informazioni agli utenti Il simbolo riportato sull apparecchiatura
ART. 12/23040 PAGINA 1 DI 6 DISTRIBUTION SPA via Michelangelo Buonarroti, 46-20093 Cologno Monzese (Milano) ITALY ART. 12/23040 PAGINA 2 DI 6 Informazioni agli utenti Il simbolo riportato sull apparecchiatura
TESTING-CERTIFICAZIONE TESTING & CERTIFICATION. Fisica della Combustione Physics of Combustion 0120\DC\REA\17_6 21/02/2017
 TESTING-CERTIFICAZIONE TESTING & CERTIFICATION Fisica della Combustione Physics of Combustion 1 Nome commerciale... : CLE Product Name Descrizione... : Vedi pag. 2/See pag. 2 Description Nome / Name...
TESTING-CERTIFICAZIONE TESTING & CERTIFICATION Fisica della Combustione Physics of Combustion 1 Nome commerciale... : CLE Product Name Descrizione... : Vedi pag. 2/See pag. 2 Description Nome / Name...
OFPBL Agar è usato nell isolamento selettivo e nella rilevazione di Burkholderia (già Pseudomonas) cepacia da campioni clinici e non clinici.
 Terreni BBL in piastra pronti per l uso per l isolamento di Burkholderia (Pseudomonas) cepacia OFPBL Agar USO PREVISTO 8806561JAA 2007/07 Italiano OFPBL Agar è usato nell isolamento selettivo e nella rilevazione
Terreni BBL in piastra pronti per l uso per l isolamento di Burkholderia (Pseudomonas) cepacia OFPBL Agar USO PREVISTO 8806561JAA 2007/07 Italiano OFPBL Agar è usato nell isolamento selettivo e nella rilevazione
La sottoscritta Carlotta Dodi
 La sottoscritta Carlotta Dodi ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato-Regione del 5 novembre 2009, dichiara che negli ultimi due anni NON ha avuto
La sottoscritta Carlotta Dodi ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato-Regione del 5 novembre 2009, dichiara che negli ultimi due anni NON ha avuto
Associazione Accademia Europea Mozart 9 MASTERCLASS DI MUSICA DA CAMERA - CERVO marzo 28 marzo
 Associazione Accademia Europea Mozart 9 MASTERCLASS DI MUSICA DA CAMERA - CERVO 2016 23 marzo 28 marzo MODULO D ISCRIZIONE da inviare via mail a corsi@accademiamozart.eu le iscrizioni dovranno pervenire
Associazione Accademia Europea Mozart 9 MASTERCLASS DI MUSICA DA CAMERA - CERVO 2016 23 marzo 28 marzo MODULO D ISCRIZIONE da inviare via mail a corsi@accademiamozart.eu le iscrizioni dovranno pervenire
(IT) FILTRO JET A BASSA PRESSIONE Mod.FBP
 (IT) FILTRO JET A BASSA PRESSIONE Mod.FBP (EN) LOW PRESSURE AIR JET FILTER Mod.FBP (FR) FILTRE À JET D AIR À BASSE PRESSURE Mod.FBP IMPIEGO Il Filtro jet a bassa pressione Mod.FBP, viene utilizzato in
(IT) FILTRO JET A BASSA PRESSIONE Mod.FBP (EN) LOW PRESSURE AIR JET FILTER Mod.FBP (FR) FILTRE À JET D AIR À BASSE PRESSURE Mod.FBP IMPIEGO Il Filtro jet a bassa pressione Mod.FBP, viene utilizzato in
1 Descrizione del prodotto. 2 Prima connessione. 3 Collegamento da remoto. 1.1 Pannello anteriore 1.2 Pannello posteriore. 2.1 Configurazione guidata
 it en fr 1 Descrizione del prodotto 1.1 Pannello anteriore 1.2 Pannello posteriore 2 Prima connessione 2.1 Configurazione guidata 2.1.1 Configurazione della rete 2.1.2 Installazione delle telecamere IP
it en fr 1 Descrizione del prodotto 1.1 Pannello anteriore 1.2 Pannello posteriore 2 Prima connessione 2.1 Configurazione guidata 2.1.1 Configurazione della rete 2.1.2 Installazione delle telecamere IP
STREPTOSYSTEM 12R. System for the identification of Streptococci. Ref Italiano 1 English 6
 STREPTOSYSTEM 12R System for the identification of Streptococci. Ref. 72560-79560 Contents Page Italiano 1 English 6 Rev.0 / 02.07.2014 Liofilchem and the Liofilchem company logo are registered trademarks
STREPTOSYSTEM 12R System for the identification of Streptococci. Ref. 72560-79560 Contents Page Italiano 1 English 6 Rev.0 / 02.07.2014 Liofilchem and the Liofilchem company logo are registered trademarks
i-line Apparecchio per interni disponibile nelle versioni a sospensione e a plafone, a luce diretta o diretta-indiretta.
 28 i-line Aluminium body Frosted polycarbonate diffuser Accessories sold separately Includes LED driver and suspensions CRI v80 Class I IP20 i-line 1195, 1495 CODE DESCRIPTION LUMEN DIMENSION ILI.3493.
28 i-line Aluminium body Frosted polycarbonate diffuser Accessories sold separately Includes LED driver and suspensions CRI v80 Class I IP20 i-line 1195, 1495 CODE DESCRIPTION LUMEN DIMENSION ILI.3493.
FICHA TÉCNICA ALICATE DE LA ROSA SIN RANURAS PROCLINIC REFERENCIA FABRICANTE / RESPONSABLE
 TDS_114_1 FICHA TÉCNICA ALICATE DE LA ROSA SIN RANURAS PROCLINIC REFERENCIA FABRICANTE / RESPONSABLE CLASIFICACIÓN DESCRIPCIÓN COMPOSICIÓN ENVASE FINALIDAD PREVISTA VIDA ÚTIL LIMPIEZA Y ESTERILIZACIÓN
TDS_114_1 FICHA TÉCNICA ALICATE DE LA ROSA SIN RANURAS PROCLINIC REFERENCIA FABRICANTE / RESPONSABLE CLASIFICACIÓN DESCRIPCIÓN COMPOSICIÓN ENVASE FINALIDAD PREVISTA VIDA ÚTIL LIMPIEZA Y ESTERILIZACIÓN
Petrifilm Piastre per il conteggio di Enterobacteriaceae
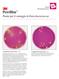 Guida all'interpretazione Petrifilm Piastre per il conteggio di Enterobacteriaceae 1 2 1 2 Conteggio di Enterobacteriaceae = 1 Il conteggio di Enterobacteriaceae è facile utilizzando le piastre Petrifilm
Guida all'interpretazione Petrifilm Piastre per il conteggio di Enterobacteriaceae 1 2 1 2 Conteggio di Enterobacteriaceae = 1 Il conteggio di Enterobacteriaceae è facile utilizzando le piastre Petrifilm
FICHA TÉCNICA ALICATE CORTE LIGADURA PROCLINIC REFERENCIA L8773 FABRICANTE / RESPONSABLE
 TDS_105_1 FICHA TÉCNICA ALICATE CORTE LIGADURA PROCLINIC REFERENCIA FABRICANTE / RESPONSABLE CLASIFICACIÓN DESCRIPCIÓN COMPOSICIÓN ENVASE FINALIDAD PREVISTA VIDA ÚTIL LIMPIEZA Y ESTERILIZACIÓN ALMACENAMIENTO
TDS_105_1 FICHA TÉCNICA ALICATE CORTE LIGADURA PROCLINIC REFERENCIA FABRICANTE / RESPONSABLE CLASIFICACIÓN DESCRIPCIÓN COMPOSICIÓN ENVASE FINALIDAD PREVISTA VIDA ÚTIL LIMPIEZA Y ESTERILIZACIÓN ALMACENAMIENTO
COSTRUZIONI CONSTRUCTION REAZIONE REACTION 0086\DC\REA\15_5 09/02/2015. Product Name. Descrizione : Vedi pagina 2 Description : See page 2
 COSTRUZIONI CONSTRUCTION REAZIONE REACTION 1 0086\DC\REA\1_ 09/02/201 Nome commerciale Product Name : K-Flex SOLAR HT Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX
COSTRUZIONI CONSTRUCTION REAZIONE REACTION 1 0086\DC\REA\1_ 09/02/201 Nome commerciale Product Name : K-Flex SOLAR HT Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX
COSTRUZIONI CONSTRUCTIONS REAZIONE REACTION 0414\DC\REA\15_3 22/05/2015. Product Name. Descrizione : Vedi pagina 2 Description : See page 2
 COSTRUZIONI CONSTRUCTIONS REAZIONE REACTION 1 0414\DC\REA\1_3 Nome commerciale Product Name : K-Flex Solar HT Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX S.p.A.
COSTRUZIONI CONSTRUCTIONS REAZIONE REACTION 1 0414\DC\REA\1_3 Nome commerciale Product Name : K-Flex Solar HT Descrizione : Vedi pagina 2 Description : See page 2 Nome / Name : L'ISOLANTE K-FLEX S.p.A.
BBL CDC Anaerobe 5% Sheep Blood Agar with Phenylethyl Alcohol (PEA)
 BBL CDC Anaerobe 5% Sheep Blood Agar with Phenylethyl Alcohol (PEA) I Rev. 10 Gennaio 2015 PROCEDURE DI CONTROLLO DI QUALITÀ INTRODUZIONE BBL CDC Anaerobe 5% Sheep Blood Agar with Phenylethyl Alcohol (PEA)
BBL CDC Anaerobe 5% Sheep Blood Agar with Phenylethyl Alcohol (PEA) I Rev. 10 Gennaio 2015 PROCEDURE DI CONTROLLO DI QUALITÀ INTRODUZIONE BBL CDC Anaerobe 5% Sheep Blood Agar with Phenylethyl Alcohol (PEA)
: Strada Maestra, 5 - Fraz. Cividale Mantovano : Rivarolo Mantovano (MN)
 TESTING-CERTIFICAZIONE TESTING & CERTIFICATION Fisica della Combustione Physics of Combustion 1 000\DC\REA\17_1 Nome commerciale Product Name : Lastre Sintostamp vetroresina traslucida Descrizione : Vedi
TESTING-CERTIFICAZIONE TESTING & CERTIFICATION Fisica della Combustione Physics of Combustion 1 000\DC\REA\17_1 Nome commerciale Product Name : Lastre Sintostamp vetroresina traslucida Descrizione : Vedi
CESI ESTENSIONE n. 03/11 al Certificato di Esame CE del tipo CESI 06 ATEX 022 Descrizione dell'apparecchiatura Le piastre di terminazione HiCTB08, HiC
 CESI ESTENSIONE n. 03/11 al Certificato di Esame CE del tipo CESI 06 ATEX 022 Descrizione dell'apparecchiatura Le piastre di terminazione HiCTB08, HiCTB16 e HiCTB32 sono dispositivi passivi predisposti
CESI ESTENSIONE n. 03/11 al Certificato di Esame CE del tipo CESI 06 ATEX 022 Descrizione dell'apparecchiatura Le piastre di terminazione HiCTB08, HiCTB16 e HiCTB32 sono dispositivi passivi predisposti
istruzioni di montaggio - manutenzione LIBRA
 istruzioni di montaggio - manutenzione prodotto rispondente ai requisiti previsti dalle Direttive Comunitarie Europee OTA BEE: le presenti istruzioni di montaggio informano l utilizzatore sulle corrette
istruzioni di montaggio - manutenzione prodotto rispondente ai requisiti previsti dalle Direttive Comunitarie Europee OTA BEE: le presenti istruzioni di montaggio informano l utilizzatore sulle corrette
Legend of Nutritional Characteristics / Legende der Nährwertcharakteristika / Légende des caractéristiques nutritionnelles
 Scheda Tecnica di Prodotto / Technical Product Specification / Fiche technique de produit 1000835072 PENNETTE RIGATE 3X5000G Data di stampa: 17-gen-2015 13.34.11 Trade Unit Info TU Code TU Description
Scheda Tecnica di Prodotto / Technical Product Specification / Fiche technique de produit 1000835072 PENNETTE RIGATE 3X5000G Data di stampa: 17-gen-2015 13.34.11 Trade Unit Info TU Code TU Description
L utilizzo non chirurgico di tessuti donati a scopo di trapianto: gli aspetti etici. Lucca, 6 novembre 2010
 L utilizzo non chirurgico di tessuti donati a scopo di trapianto: gli aspetti etici Lucca, 6 novembre 2010 Struttura dell intervento 1. Che vuol dire aspetti etici? 2. Qual è il punto di riferimento della
L utilizzo non chirurgico di tessuti donati a scopo di trapianto: gli aspetti etici Lucca, 6 novembre 2010 Struttura dell intervento 1. Che vuol dire aspetti etici? 2. Qual è il punto di riferimento della
RAPPORTO DI PROVA:
 15.46812 RAPPORTO DI PROVA: 15.46812 Questo rapporto è costituito da 16 pagine, di cui: 3 pagine per il Sommario 2 pagine per il Rapporto di Prova 15.46812a 11 pagine per il Rapporto di Prova 15.46812b
15.46812 RAPPORTO DI PROVA: 15.46812 Questo rapporto è costituito da 16 pagine, di cui: 3 pagine per il Sommario 2 pagine per il Rapporto di Prova 15.46812a 11 pagine per il Rapporto di Prova 15.46812b
, Vers ATEX 94/9/CE. HTP S.r.l. DIN A DIN B. n.a.
 Type : Connector type DIN 43650-A and DIN 43650-B Page 1/8 1 General information Informazioni generali 1.1 Report n : Report n : 1.2 Date of report: Emesso il: 1.3 Prepared by: Preparato da: 1.4 Main reference
Type : Connector type DIN 43650-A and DIN 43650-B Page 1/8 1 General information Informazioni generali 1.1 Report n : Report n : 1.2 Date of report: Emesso il: 1.3 Prepared by: Preparato da: 1.4 Main reference
BD MacConkey II Agar / Columbia CNA Agar Improved II with 5% Sheep Blood (Biplate)
 ISTRUZIONI PER L USO - TERRENI SU PIASTRA PRONTI PER L USO PA-257574.02 Rev.: Sept. 2015 BD MacConkey II Agar / Columbia CNA Agar Improved II with 5% Sheep Blood (Biplate) USO PREVISTO BD MacConkey II
ISTRUZIONI PER L USO - TERRENI SU PIASTRA PRONTI PER L USO PA-257574.02 Rev.: Sept. 2015 BD MacConkey II Agar / Columbia CNA Agar Improved II with 5% Sheep Blood (Biplate) USO PREVISTO BD MacConkey II
WHITE TRUFFLES OIL PRODUCT NAME (Tuber magnatum Pico) WHITE TRUFFLES OIL 55 ml. REVISION 02 de 07/01/2016
 55 ml 1 GENERAL CHARACTERISTIC 1.1 DESCRIPTION 1.2 T.M.C. 1.3 STORAGE 1.4 TREATMENT The olive oil are infused with white truffle, and a special time to obtain the perfect olive oil flavoured. 24 months
55 ml 1 GENERAL CHARACTERISTIC 1.1 DESCRIPTION 1.2 T.M.C. 1.3 STORAGE 1.4 TREATMENT The olive oil are infused with white truffle, and a special time to obtain the perfect olive oil flavoured. 24 months
1.0 GENERAL CHARACTERISTIC. Room temperature max 22 C. Sterilization, min F(0) > 15. Produced in Italy. The product are ogm free
 1.0 GENERAL CHARACTERISTIC 1.1 DESCRIPTION 1.2 T.M.C. 1.3 STORAGE Off summer truffles combined with fresh mushrooms, in a recipe that this one of the oldest and most traditional in Italy. 48 months ( indicated
1.0 GENERAL CHARACTERISTIC 1.1 DESCRIPTION 1.2 T.M.C. 1.3 STORAGE Off summer truffles combined with fresh mushrooms, in a recipe that this one of the oldest and most traditional in Italy. 48 months ( indicated
