n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
|
|
|
- Gabriella Pastore
- 5 anni fa
- Visualizzazioni
Transcript
1 Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari
2
3
4
5 c l n n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] c n = frequenza [1/s] Le onde elettromagnetiche sono quantizzate E hn h c l h = costante di Planck = J s
6
7
8 n n R H l n Johannes Rydberg R H = Costante di Ryberg = m -1 n 1 ed n 2 = numeri interi Spettro dell atomo di Idrogeno
9 Il modello atomico di Rutherford non è in grado di descrivere questo comportamento. Modello atomo di Bohr (1913) L elettrone si muove attorno al nucleo solo su determinate orbite circolari a ciascuna delle quali corrisponde un valore costante dell energia (stato stazionario); Finché l elettrone rimane in uno stato stazionario non assorbe e non cede energia; Il momento angolare (o della quantità di moto) dell elettrone, m v r, è quantizzato. m v r = n h /(2p) n= 1, 2, 3,.,
10 n viene chiamato numero quantico principale ne consegue che r è quantizzato: r = a 0 n 2 (a 0 = m) e l energia totale risulta: n=1 n=2 n=3 n=4 E E 0 Z n Johannes Rydberg 2 2 Z è la carica del nucleo dell atomo idrogenoide. E 1 1 h n 1 E 1 1 n R H 2 2 n1 n l 2 n 1 n2
11 Serie Paschen Serie Balmer Serie Lyman
12 Meccanica quantistica o ondulatoria Le onde elettromagnetiche hanno un comportamento duale (onda-particella) De Broglie (1924) ipotizza un comportamento duale (onda-particella) anche per la materia Un elettrone (o una qualsiasi particella materiale) può essere rappresentato da un onda di lunghezza h l m v Principio di indeterminazione di Heisenberg (1927) x ( m v) h 4p
13
14 necessita di introdurre una nuova equazione per descrivere il comportamento ondulatorio della materia Equazione di Schrödinger Le cui soluzioni rappresentano funzioni d onda (Y ) Y 2 (x,y,z), il quadrato della funzioni d onda rappresenta la densità (di probabilità) di trovare l elettrone in un dato punto (x,y,z). La soluzione dell equazione di Schrödinger per l atomo di Idrogeno evidenzia l esistenza di stati stazionari (o orbitali elettronici) caratterizzati da 3 numeri quantici n = numero quantico principale l = numero quantico angolare (o secondario) m = numero quantico magnetico E E 0 Z n 2 2
15
16 n = 1, 2, 3,., l = 0, 1, 2,, (n-1) m = l, (l 1), (l 2),, 0,, +(l 2), +(l 1), +l m s = ½, +½
17 ogni orbitale viene indicato con un numero corrispondente ad n ed un simbolo (s, p, d, f) in base al numero quantico angolare (l ) l Simbolo s p d f
18
19 Livelli energetici 7d 7f 6f Atomo Idrogenoide Atomo con più elettroni Nucleo carica Z Nucleo carica E Z E Un solo elettrone 0 Z n 2 2
20
21 La configurazione degli atomi poli-elettronici la si determina con un «meccanismo fittizio» chiamato Aufbau (dal tedesco, costruzione). Consiste nell inserire gli elettroni uno ad uno negli orbitali di più bassa energia rispettando il Principio di esclusione di Pauli: in un atomo non vi possono essere due (o più) elettroni con tutti i quattro numeri quantici, n, l, m ed m s, uguali e la Regola di Hund: gli orbitali degeneri vengono dapprima occupati tutti singolarmente da elettroni con spin parallelo e solo successivamente da altri elettroni che si accoppiano con i precedenti
22 Z = 1 un elettrone 2p 2s 1s Idrogeno 1s 1 = [H]
23 Z = 2 due elettroni 2p 2s 1s Elio 1s 2 = [He]
24 Z = 3 tre elettroni 2p 2s 1s Litio 1s 2 2s 1 = [He]2s 1
25 Z = 4 quattro elettroni 2p 2s 1s Berillio 1s 2 2s 2 = [He]2s 2
26 Z = 5 cinque elettroni 2p 2s 1s Boro 1s 2 2s 2 2p 1 = [He]2s 2 2p 1
27 Z = 6 sei elettroni 2p 2s 1s Carbonio 1s 2 2s 2 2p 2 = [He]2s 2 2p 2
28 Z = 7 sette elettroni 2p 2s 1s Azoto 1s 2 2s 2 2p 3 = [He]2s 2 2p 3
29 Z = 8 otto elettroni 2p 2s 1s Ossigeno 1s 2 2s 2 2p 4 = [He]2s 2 2p 4
30 Z = 9 nove elettroni 2p 2s 1s Fluoro 1s 2 2s 2 2p 5 = [He]2s 2 2p 5
31 Z = 10 dieci elettroni 2p 2s 1s Neon 1s 2 2s 2 2p 6 = [He]2s 2 2p 6
32 Z = elettroni 3d 3p 3s 2p 2s 1s Z = 11 Na 1s 2 2s 2 2p 6 3s = [Ne]3s
33 Z = elettroni 3d 3p 3s 2p 2s 1s Z = 17 Cl 1s 2 2s 2 2p 6 3s 2 3p 5 = [Ne]3s 2 3p 5
34 1s 2 2s 2 2p 5 = [He]2s 2 2p 5 1s 2 2s 2 2p 6 3s 2 3p 5 = [Ne]3s 2 3p 5 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5 = [Ar]4s 2 4p 5 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 5 = [Kr]5s 2 5p 5 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 2 6p 5 = [Xe]6s 2 6p 5
35
36
37
38
39
40
41 Energia di ionizzazione L energia di prima ionizzazione (I 1 ), è l energia che occorre fornire ad un atomo gassoso isolato nel suo stato fondamentale, M(g), affinché perda un elettrone e si trasformi in uno ione mono positivo, M + (g), gassoso isolato: M g) I M ( g) e ( 1 L energia di seconda ionizzazione (I 2 ), rappresenta l energia necessaria per allontanare un elettrone da uno ione gassoso mono positivo, M + (g), gassoso e trasformarlo in uno ione bi-positivo isolato: 2 M ( g) I M ( g) e 2
42 II periodo 2p 2p 3p III periodo 2s 1s Z = s 1s Z= =14 =13 =12 = He Li Be C OF Ne Ar Cl PSi Al Mg Na IV periodo
43 Affinità elettronica: A e è l energia che viene liberata da un atomo neutro isolato nel suo stato fondamentale quando acquista un elettrone per dare luogo ad uno ione negativo isolato. Per convenzione, l energia liberata ha segno positivo. II Periodo X( g) e X III Periodo ( g) A e
44 Dai potenziali di ionizzazione e dalle affinità elettroniche si evidenzia che i sistemi con gusci elettronici chiusi sono i più stabili. Elementi con gusci (shell) di elettroni aperti tendono più facilmente a perdere o acquisire elettroni per ottenere una configurazione elettronica con guscio chiuso Regola dell ottetto (W. Kossel; 1916). L aggruppamento di otto elettroni s 2 p 6 prende il nome di ottetto ed è una configurazione di grande stabilità; gli atomi, nella formazione dei legami, tendono a realizzare una tale configurazione elettronica esterna, cedendo, acquistando o mettendo in comune elettroni con altri atomi. (da: P. Silvestroni, Fondamenti di chimica, Ed. Veschi) 2p 2s 1s Z = 10 Ne
45 Simboli di Lewis I II III IV V VI VII 0 H He Li Be B C N O F Ne S Al Si Mg P Cl Ar Na
La Teoria dei Quanti e la Struttura Elettronica degli Atomi. Capitolo 7
 La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
TEORIA QUANTISTICA E STRUTTURA ATOMICA
 TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Il metodo scientifico
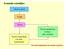 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Struttura Elettronica degli Atomi
 Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Le particelle elementari di interesse in Chimica sono: Particella simbolo massa carica spin
 Le particelle elementari di interesse in Chimica sono: Particella simbolo massa carica spin Elettrone e - 9.11x10-31 kg -1 ½ 5.486x10-4 u Protone p 1.67x10-27 kg +1 ½ 1.0073 u Neutrone n 1.67x10-27 kg
Le particelle elementari di interesse in Chimica sono: Particella simbolo massa carica spin Elettrone e - 9.11x10-31 kg -1 ½ 5.486x10-4 u Protone p 1.67x10-27 kg +1 ½ 1.0073 u Neutrone n 1.67x10-27 kg
LE PARTICELLE ELEMENTARI: loro scoperta
 LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.6 ENERGIE DI IONIZZAZIONE E DISTRIBUZIONE DEGLI ELETTRONI 4.C OBIETTIVI
 LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
Natura della luce. Qualsiasi tipo di onda è caratterizzato da:
 Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
FISICA E LABORATORIO
 Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
I modelli atomici da Dalton a Bohr
 1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
Indice generale. Prefazione
 26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR
 LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR LIMITI DEL MODELLO ATOMICO DI RUTHERFORD Il modello atomico planetario di Ernest Rutherford, seppure rappresentava un grande passo avanti rispetto al modello
LA NATURA DELLA LUCE E IL MODELLO ATOMICO DI BOHR LIMITI DEL MODELLO ATOMICO DI RUTHERFORD Il modello atomico planetario di Ernest Rutherford, seppure rappresentava un grande passo avanti rispetto al modello
Recenti Scoperte Scientifiche in Ottica
 Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
Richiami. Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza
 Parte I Problemi Richiami Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza u ν = 8π hν c 3 ν e βhν 1, dove c è la velocità della luce
Parte I Problemi Richiami Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza u ν = 8π hν c 3 ν e βhν 1, dove c è la velocità della luce
CLASSE 5 A L.S.A. ISTITUTO D ISTRUZIONE SUPERIORE STATALE G. CIGNA ANNO SCOL: 2015/2016 PROGRAMMAZIONE ANNUALE DI FISICA. Docente: Prof.
 ISTITUTO D ISTRUZIONE SUPERIORE STATALE G. CIGNA ANNO SCOL: 2015/2016 PROGRAMMAZIONE ANNUALE DI FISICA CLASSE 5 A L.S.A. Docente: Prof. LINGUA ALDO Libro di testo: CORSO di FISICA: voll. 3 James S. Walker
ISTITUTO D ISTRUZIONE SUPERIORE STATALE G. CIGNA ANNO SCOL: 2015/2016 PROGRAMMAZIONE ANNUALE DI FISICA CLASSE 5 A L.S.A. Docente: Prof. LINGUA ALDO Libro di testo: CORSO di FISICA: voll. 3 James S. Walker
IL MODELLO ATOMICO DI BOHR
 IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
May 5, 2013. Fisica Quantistica. Monica Sambo. Sommario
 May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
MASSE ATOMICHE. 1,000 g di idrogeno reagiscono con 7,9367 g di ossigeno massa atomica ossigeno=2 x 7,9367=15,873 g (relativa all'idrogeno)
 MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
Indice PREFAZIONE. Capitolo 5 LE LEGGI DEL MOTO DI NEWTON 58 5.1 La terza legge di Newton 58
 Indice PREFAZIONE XV Capitolo 1 RICHIAMI DI MATEMATICA 1 1.1 Simboli, notazione scientifica e cifre significative 1 1.2 Algebra 3 1.3 Geometria e trigonometria 5 1.4 Vettori 7 1.5 Sviluppi in serie e approssimazioni
Indice PREFAZIONE XV Capitolo 1 RICHIAMI DI MATEMATICA 1 1.1 Simboli, notazione scientifica e cifre significative 1 1.2 Algebra 3 1.3 Geometria e trigonometria 5 1.4 Vettori 7 1.5 Sviluppi in serie e approssimazioni
Da Newton a Planck. La struttura dell atomo. Da Newton a Planck. Da Newton a Planck. Meccanica classica (Newton): insieme
 Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
LA MOLE LA MOLE 2.A PRE-REQUISITI 2.3 FORMULE E COMPOSIZIONE 2.B PRE-TEST
 LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
Gli orbitali: modello atomico probabilistico
 1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
PARTICELLE SUBATOMICHE
 MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici.
 LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO Vari esperimenti condotti fra la fine del 1800 e l inizio del 1900 dimostrarono che gli atomi non sono indivisibili, ma costituiti da particelle più piccole (elementari). PARTICELLE
STRUTTURA DELL'ATOMO Vari esperimenti condotti fra la fine del 1800 e l inizio del 1900 dimostrarono che gli atomi non sono indivisibili, ma costituiti da particelle più piccole (elementari). PARTICELLE
CORSO DI LAUREA IN SCIENZE FISICHE A.A. 2010/2011
 MANIFESTO DEGLI STUDI CORSO DI LAUREA IN SCIENZE FISICHE A.A. 2010/2011 1. Denominazione - Laurea in SCIENZE FISICHE 2. Classe Il Corso di laurea in Scienze Fisiche appartiene alla classe L-30 - Scienze
MANIFESTO DEGLI STUDI CORSO DI LAUREA IN SCIENZE FISICHE A.A. 2010/2011 1. Denominazione - Laurea in SCIENZE FISICHE 2. Classe Il Corso di laurea in Scienze Fisiche appartiene alla classe L-30 - Scienze
Quesiti e problemi (sul libro da pag. 189)
 Quesiti e problemi (sul libro da pag. 189) 1 La doppia natura della luce 1 Qual è la prova più evidente della natura ondulatoria della luce? la diffrazione 2 Come sono chiamate le particelle che costituiscono
Quesiti e problemi (sul libro da pag. 189) 1 La doppia natura della luce 1 Qual è la prova più evidente della natura ondulatoria della luce? la diffrazione 2 Come sono chiamate le particelle che costituiscono
Introduzione alla fisica quantistica
 Paola Pannuti Liceo Scientifico Ulivi Parma Introduzione alla fisica quantistica http://digilander.libero.it/la_prof_di_fisica/fisicaquantistica.pdf Dalle lezioni del professor Elio Fabri Dip. di fisica
Paola Pannuti Liceo Scientifico Ulivi Parma Introduzione alla fisica quantistica http://digilander.libero.it/la_prof_di_fisica/fisicaquantistica.pdf Dalle lezioni del professor Elio Fabri Dip. di fisica
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia
 Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
I legami. 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1):
 Percorso 3 I legami E S E R C I Z I A Legame covalente omeopolare 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1): 2) Rappresenta la struttura della molecola di ossigeno
Percorso 3 I legami E S E R C I Z I A Legame covalente omeopolare 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1): 2) Rappresenta la struttura della molecola di ossigeno
LA MATERIA MATERIA. COMPOSIZIONE (struttura) Atomi che la compongono
 LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
PROGRAMMA DI SCIENZE Cl. II sez. E A.S. 2014/2015. Testo: S. Passannanti C. Sbriziolo Noi e la chimica Dai fenomeni alle leggi Ed.
 PROGRAMMA DI SCIENZE Cl. II sez. E A.S. 2014/2015 CHIMICA Testo: S. Passannanti C. Sbriziolo Noi e la chimica Dai fenomeni alle leggi Ed. Tramontana S. Passannanti C. Sbriziolo Noi e la chimica agli atomi
PROGRAMMA DI SCIENZE Cl. II sez. E A.S. 2014/2015 CHIMICA Testo: S. Passannanti C. Sbriziolo Noi e la chimica Dai fenomeni alle leggi Ed. Tramontana S. Passannanti C. Sbriziolo Noi e la chimica agli atomi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
Lo sviluppo dei modelli atomici da Thomson alla fisica quantistica. Lavoro di maturità
 Liceo cantonale di Locarno Lo sviluppo dei modelli atomici da Thomson alla fisica quantistica Lavoro di maturità Marco Tognetti 007-008 Professori responsabili: Boffa Gianni e Ferrari Christian Indice
Liceo cantonale di Locarno Lo sviluppo dei modelli atomici da Thomson alla fisica quantistica Lavoro di maturità Marco Tognetti 007-008 Professori responsabili: Boffa Gianni e Ferrari Christian Indice
MODELLI ATOMICI. Dai primi modelli alla teoria moderna
 MODELLI ATOMICI Dai primi modelli alla teoria moderna Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole,
MODELLI ATOMICI Dai primi modelli alla teoria moderna Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole,
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Gruppo 10 Nickel Ni (1751)
 Gruppo 10 ickel i (1751) Proprietà i Pd Pt Z 28 46 78 umero di isotopi 5 6 6 naturali Massa atomica 58.69 106.42 195.08 onfigurazione [Ar]3d 8 4s 2 [Kr]4d 10 [Xe]4f 14 5d 9 6s 1 elettronica Aspetto Metallo
Gruppo 10 ickel i (1751) Proprietà i Pd Pt Z 28 46 78 umero di isotopi 5 6 6 naturali Massa atomica 58.69 106.42 195.08 onfigurazione [Ar]3d 8 4s 2 [Kr]4d 10 [Xe]4f 14 5d 9 6s 1 elettronica Aspetto Metallo
Corso di Laurea in FARMACIA
 Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Inquinamento da Campi Elettromagnetici
 Inquinamento da Campi Elettromagnetici Aspetti Tecnici, Sanitari, Normativi A cura di ECORICERCHE s.r.l. Lo Spettro Elettromagnetico ECORICERCHE s.r.l. 2 Elettrosmog: che cos è? E un termine entrato nell
Inquinamento da Campi Elettromagnetici Aspetti Tecnici, Sanitari, Normativi A cura di ECORICERCHE s.r.l. Lo Spettro Elettromagnetico ECORICERCHE s.r.l. 2 Elettrosmog: che cos è? E un termine entrato nell
La Fisica spiega la Chimica
 La Fisica spiega la Chimica ovvero sulla struttura della materia a cura di Gloria Nobili Docente di Fisica presso Polo liceale Rambaldi-Valeriani Divulgatrice scientifica Presidente Ass.ne culturale SALTO
La Fisica spiega la Chimica ovvero sulla struttura della materia a cura di Gloria Nobili Docente di Fisica presso Polo liceale Rambaldi-Valeriani Divulgatrice scientifica Presidente Ass.ne culturale SALTO
Istituto di Istruzione Superiore L. da Vinci Civitanova Marche. Anno scolastico 2014-2015. Programma svolto. Docente: Silvana Venditti
 Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
SPETTROSCOPIA MOLECOLARE
 SPETTROSCOPIA MOLECOLARE La spettroscopia molecolare studia l assorbimento o l emissione delle radiazioni elettromagnetiche da parte delle molecole. Il dato sperimentale che si ottiene, chiamato rispettivamente
SPETTROSCOPIA MOLECOLARE La spettroscopia molecolare studia l assorbimento o l emissione delle radiazioni elettromagnetiche da parte delle molecole. Il dato sperimentale che si ottiene, chiamato rispettivamente
Prova scritta intercorso 2 31/5/2002
 Prova scritta intercorso 3/5/ Diploma in Scienza e Ingegneria dei Materiali anno accademico - Istituzioni di Fisica della Materia - Prof. Lorenzo Marrucci Tempo a disposizione ora e 45 minuti ) Un elettrone
Prova scritta intercorso 3/5/ Diploma in Scienza e Ingegneria dei Materiali anno accademico - Istituzioni di Fisica della Materia - Prof. Lorenzo Marrucci Tempo a disposizione ora e 45 minuti ) Un elettrone
PROGRAMMAZIONE DIDATTICA
 Pagina 1 di 6 Il profilo educativo, culturale e professionale dello studente liceale: I percorsi liceali forniscono allo studente gli strumenti culturali e metodologici per una comprensione approfondita
Pagina 1 di 6 Il profilo educativo, culturale e professionale dello studente liceale: I percorsi liceali forniscono allo studente gli strumenti culturali e metodologici per una comprensione approfondita
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
PERCHÉ STUDIARE LA CHIMICA. La chimica studia la composizione e le proprietà della materia e i cambiamenti cui quest ultima va incontro.
 1 PERCHÉ STUDIARE LA CHIMICA La chimica studia la composizione e le proprietà della materia e i cambiamenti cui quest ultima va incontro. Cucinare Digestione Chimica: scienza centrale Respirazione Combustione
1 PERCHÉ STUDIARE LA CHIMICA La chimica studia la composizione e le proprietà della materia e i cambiamenti cui quest ultima va incontro. Cucinare Digestione Chimica: scienza centrale Respirazione Combustione
Spettrometria. Introduzione.
 Spettrometria. Introduzione. Lo studio degli spettri di emissione e di assorbimento è stato sicuramente uno degli aspetti che hanno maggiormente contribuito alla crisi della meccanica classica a cavallo
Spettrometria. Introduzione. Lo studio degli spettri di emissione e di assorbimento è stato sicuramente uno degli aspetti che hanno maggiormente contribuito alla crisi della meccanica classica a cavallo
Chimica Fisica II. Prof. Riccardo Basosi
 1 Anno Accademico 2014/2015 Chimica Fisica II Prof. Riccardo Basosi con la collaborazione delle Dr. Adalgisa Sinicropi e Dr. Maria Laura Parisi La Natura della Luce: 2 Dualismo onda-particella Gli studi
1 Anno Accademico 2014/2015 Chimica Fisica II Prof. Riccardo Basosi con la collaborazione delle Dr. Adalgisa Sinicropi e Dr. Maria Laura Parisi La Natura della Luce: 2 Dualismo onda-particella Gli studi
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013
 LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
LICEO SCIENTIFICO VITO VOLTERRA
 LICEO SCIENTIFICO VITO VOLTERRA DIPARTIMENTO DI FISICA ORIETTA DI BIAGIO Penso si possa tranquillamente affermare che nessuno capisce la meccanica quantistica Richard P. Feynman Premio Nobel nel 1963 Quelli
LICEO SCIENTIFICO VITO VOLTERRA DIPARTIMENTO DI FISICA ORIETTA DI BIAGIO Penso si possa tranquillamente affermare che nessuno capisce la meccanica quantistica Richard P. Feynman Premio Nobel nel 1963 Quelli
INDICAZIONI ED ESERCIZI PER LA PREPARAZIONE ALLA PROVA DI VERIFICA DI SETTEMBRE SCIENZE INTEGRATE (CHIMICA)
 ISTITUTO DI ISTRUZIONE SUPERIORE CHINO CHINI Via Pietro Caiani 68-50032 Borgo San Lorenzo (Fi) Tel. 055.8459.268 - Fax 055.8495.131 Sito Web: www.chinochini.it - E-mail: chinochini@tin.it - PEC FIIS02300N@PEC.ISTRUZIONE.IT
ISTITUTO DI ISTRUZIONE SUPERIORE CHINO CHINI Via Pietro Caiani 68-50032 Borgo San Lorenzo (Fi) Tel. 055.8459.268 - Fax 055.8495.131 Sito Web: www.chinochini.it - E-mail: chinochini@tin.it - PEC FIIS02300N@PEC.ISTRUZIONE.IT
Competenze. Riconoscere che una calamita esercita una forza su una seconda calamita. Riconoscere che l ago di una bussola ruota in direzione Sud-Nord.
 Ist.Magistrale G. Comi Tricase ( LE Allegata al verbale del Consiglio di classe del 19/10/2015 PROGRAMMAZIONE DISCIPLINARE della CLASSE 5 AA Anno scolastico 2015/2016 MATERIA Fisica DOCENTE Nicolì Pasquale
Ist.Magistrale G. Comi Tricase ( LE Allegata al verbale del Consiglio di classe del 19/10/2015 PROGRAMMAZIONE DISCIPLINARE della CLASSE 5 AA Anno scolastico 2015/2016 MATERIA Fisica DOCENTE Nicolì Pasquale
PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO: CHIMICA, MATERIALI E BIOTECNOLOGIE
 RE P U B B L I C A I T A L I A N A ISTITUTO DI ISTRUZIONE SECONDARIA SUPERIORE MINERARIO G. ASPRONI E. FERMI DI IGLESIAS PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO:
RE P U B B L I C A I T A L I A N A ISTITUTO DI ISTRUZIONE SECONDARIA SUPERIORE MINERARIO G. ASPRONI E. FERMI DI IGLESIAS PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO:
Formule di Struttura delle Molecole Organiche
 Formule di Struttura delle Molecole Organiche Costituzione L ordine in cui gli atomi di una molecola sono connessi è chiamata costituzione o connettività. La costituzione di una molecola deve essere determinata
Formule di Struttura delle Molecole Organiche Costituzione L ordine in cui gli atomi di una molecola sono connessi è chiamata costituzione o connettività. La costituzione di una molecola deve essere determinata
FÖDELSEN AV KVANTMEKANIK
 Liceo Norberto Rosa Sede associata di Bussoleno Indirizzo Scientifico-tecnologico sperimentazione Brocca Approfondimento personale per l Esame di Stato FÖDELSEN AV KVANTMEKANIK LA NASCITA DELLA MECCANICA
Liceo Norberto Rosa Sede associata di Bussoleno Indirizzo Scientifico-tecnologico sperimentazione Brocca Approfondimento personale per l Esame di Stato FÖDELSEN AV KVANTMEKANIK LA NASCITA DELLA MECCANICA
L ATOMO. Risponde (o almeno ci prova)
 L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia. Francesco Nobili
 Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
1.11.3 Distribuzione di carica piana ed uniforme... 32
 Indice 1 Campo elettrico nel vuoto 1 1.1 Forza elettromagnetica............ 2 1.2 Carica elettrica................ 3 1.3 Fenomeni elettrostatici............ 6 1.4 Legge di Coulomb.............. 9 1.5 Campo
Indice 1 Campo elettrico nel vuoto 1 1.1 Forza elettromagnetica............ 2 1.2 Carica elettrica................ 3 1.3 Fenomeni elettrostatici............ 6 1.4 Legge di Coulomb.............. 9 1.5 Campo
LE COMPETENZE ESSENZIALI DI FISICA
 LE COMPETENZE ESSENZIALI DI FISICA classe prima Liceo scientifico COMPETENZE raccogliere dati attraverso l osservazione diretta dei fenomeni naturali fisici e attraverso l attività di laboratorio OSA comprendere
LE COMPETENZE ESSENZIALI DI FISICA classe prima Liceo scientifico COMPETENZE raccogliere dati attraverso l osservazione diretta dei fenomeni naturali fisici e attraverso l attività di laboratorio OSA comprendere
TEORIA PERTURBATIVA DIPENDENTE DAL TEMPO
 Capitolo 14 EORIA PERURBAIVA DIPENDENE DAL EMPO Nel Cap.11 abbiamo trattato metodi di risoluzione dell equazione di Schrödinger in presenza di perturbazioni indipendenti dal tempo; in questo capitolo trattiamo
Capitolo 14 EORIA PERURBAIVA DIPENDENE DAL EMPO Nel Cap.11 abbiamo trattato metodi di risoluzione dell equazione di Schrödinger in presenza di perturbazioni indipendenti dal tempo; in questo capitolo trattiamo
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
La Meccanica Quantistica
 Alunno: Giovannangelo Dante Liceo Scientifico Tecnologico L. Da Vinci, Lanciano La Meccanica Quantistica La realtà così come non la vediamo Il percorso 1. Storia 2. Fisica 3. Matematica La Meccanica Quantistica
Alunno: Giovannangelo Dante Liceo Scientifico Tecnologico L. Da Vinci, Lanciano La Meccanica Quantistica La realtà così come non la vediamo Il percorso 1. Storia 2. Fisica 3. Matematica La Meccanica Quantistica
PROGRAMMAZIONE DISCIPLINARE E ORGANIZZAZIONE DEI CONTENUTI Anno scolastico 2015 / 16
 PROGRAMMAZIONE DISCIPLINARE E ORGANIZZAZIONE DEI CONTENUTI Anno scolastico 2015 / 16 Docente: Classe: Materia: Indirizzo: Libro di testo: Altri materiali didattici: Alessandro PASQUALI 5ª A Fisica Liceo
PROGRAMMAZIONE DISCIPLINARE E ORGANIZZAZIONE DEI CONTENUTI Anno scolastico 2015 / 16 Docente: Classe: Materia: Indirizzo: Libro di testo: Altri materiali didattici: Alessandro PASQUALI 5ª A Fisica Liceo
LA DUPLICE NATURA DELLA LUCE
 LA DUPLICE NATURA DELLA LUCE Ovvero: Così è, se vi pare La secolare disputa sulla natura della luce è caratterizzata da numerosi rovesciamenti di fronte. Newton sosteneva essere costituita da un flusso
LA DUPLICE NATURA DELLA LUCE Ovvero: Così è, se vi pare La secolare disputa sulla natura della luce è caratterizzata da numerosi rovesciamenti di fronte. Newton sosteneva essere costituita da un flusso
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Programmazione di Scienze A.S. 2013-2014
 Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
Il quanto di luce e la fisica quantistica
 Il quanto di luce e la fisica quantistica motivazioni della scelta ripensare all energia in fisica classica: aspetti corpuscolari e ondulatori dal quanto di azione di Planck al quanto di luce di Einstein
Il quanto di luce e la fisica quantistica motivazioni della scelta ripensare all energia in fisica classica: aspetti corpuscolari e ondulatori dal quanto di azione di Planck al quanto di luce di Einstein
Capitolo 4 Le spettroscopie. 1. Lo spettro elettromagnetico
 Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione
 Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
INTRODUZIONE ALLO STUDIO DELLA CHIMICA
 INTRODUZIONE ALLO STUDIO DELLA CHIMICA La chimica si interessa dello studio della materia, delle sue proprietà, della sua struttura e delle trasformazioni che avvengono in essa. Materia è tutto ciò che
INTRODUZIONE ALLO STUDIO DELLA CHIMICA La chimica si interessa dello studio della materia, delle sue proprietà, della sua struttura e delle trasformazioni che avvengono in essa. Materia è tutto ciò che
NUMERI DI OSSIDAZIONE
 NUMERI DI OSSIDAZIONE Numeri in caratteri romani dotati di segno Tengono conto di uno squilibrio di cariche nelle specie poliatomiche Si ottengono, formalmente, attribuendo tutti gli elettroni di valenza
NUMERI DI OSSIDAZIONE Numeri in caratteri romani dotati di segno Tengono conto di uno squilibrio di cariche nelle specie poliatomiche Si ottengono, formalmente, attribuendo tutti gli elettroni di valenza
ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica
 ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica La prova Il candidato svolga una relazione su uno solo dei seguenti due temi, a sua
ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica La prova Il candidato svolga una relazione su uno solo dei seguenti due temi, a sua
Introduzione alla Meccanica Quantistica. Fausto Borgonovi
 Introduzione alla Meccanica Quantistica Fausto Borgonovi Dipartimento di Matematica e Fisica e i.l.a.m.p. Universitá Cattolica, via Musei 41, BRESCIA Istituto Nazionale di Fisica Nucleare, PAVIA fausto.borgonovi@unicatt.it
Introduzione alla Meccanica Quantistica Fausto Borgonovi Dipartimento di Matematica e Fisica e i.l.a.m.p. Universitá Cattolica, via Musei 41, BRESCIA Istituto Nazionale di Fisica Nucleare, PAVIA fausto.borgonovi@unicatt.it
LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE
 LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE Anno scolastico 2014-2015 RELAZIONE FINALE DEL DOCENTE All. A Classe: 5^DSA Indirizzo: SCIENZE APPLICATE Materia: FISICA
LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE Anno scolastico 2014-2015 RELAZIONE FINALE DEL DOCENTE All. A Classe: 5^DSA Indirizzo: SCIENZE APPLICATE Materia: FISICA
Dai primi modelli atomici alla teoria moderna
 Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
Dipartimento di Chimica
 UNIVERSITA' DEGLI STUDI DI SASSARI Dipartimento di Chimica Mauro Rustici Dipartimento di chimica, Via Vienna 2, 07100 Sassari email rustici@uniss.it Elementi di Chimica Anno Accademico 2011/2012 2 Indice
UNIVERSITA' DEGLI STUDI DI SASSARI Dipartimento di Chimica Mauro Rustici Dipartimento di chimica, Via Vienna 2, 07100 Sassari email rustici@uniss.it Elementi di Chimica Anno Accademico 2011/2012 2 Indice
Unità di misura. Perché servono le unità di misura nella pratica di laboratorio e in corsia? Le unità di misura sono molto importanti
 Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Dalla Chimica Generale
 RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
RADIAZIONI RADIAZIONI IONIZZANTI RADIAZIONI IONIZZANTI
 RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
 LEGAME CHIMICO In natura solo i gas nobili si ritrovano allo stato monoatomico. Gli altri atomi tendono a legarsi spontaneamente fra di loro per formare delle MOLECOLE, raggiungendo una condizione di MAGGIORE
LEGAME CHIMICO In natura solo i gas nobili si ritrovano allo stato monoatomico. Gli altri atomi tendono a legarsi spontaneamente fra di loro per formare delle MOLECOLE, raggiungendo una condizione di MAGGIORE
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI
 Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
SISTEMI MICROSCOPICI meccanica quantistica e spettroscopia
 SISTEMI MICROSCOPICI meccanica quantistica e spettroscopia Le proprietà fisiche e chimiche degli elementi e dei composti dipendono dal comportamento degli elettroni negli atomi e nelle molecole. La meccanica
SISTEMI MICROSCOPICI meccanica quantistica e spettroscopia Le proprietà fisiche e chimiche degli elementi e dei composti dipendono dal comportamento degli elettroni negli atomi e nelle molecole. La meccanica
PERCORSI DIDATTICI. Atom in a box
 di: Isidoro Sciarratta PERCORSI DIDATTICI Atom in a box scuola: Università di Udine area tematica: Scienze pensato per: 15-18 Introduzione La proposta Modelli, scienze e computer nell insegnamento della
di: Isidoro Sciarratta PERCORSI DIDATTICI Atom in a box scuola: Università di Udine area tematica: Scienze pensato per: 15-18 Introduzione La proposta Modelli, scienze e computer nell insegnamento della
Carlo Cosmelli. La visione del mondo della Relatività e della Meccanica Quantistica. Settimana 5. Lezione 5.1 La funzione d onda I parte
 La visione del mondo della Relatività e della Meccanica Quantistica Settimana 5 Lezione 5.1 La funzione d onda I parte Carlo Cosmelli 1 Riassunto al 1924 Quindi: 1900 - Planck: lo scambio di Energia [onda
La visione del mondo della Relatività e della Meccanica Quantistica Settimana 5 Lezione 5.1 La funzione d onda I parte Carlo Cosmelli 1 Riassunto al 1924 Quindi: 1900 - Planck: lo scambio di Energia [onda
Državni izpitni center. Prova d esame 1. Giovedì, 29 agosto 2013 / 90 minuti
 odice del candidato: ržavni izpitni center *M13243121I* SESSIONE UTUNNLE Prova d esame 1 Giovedì, 29 agosto 2013 / 90 minuti l candidato sono consentiti l'uso della penna stilografica o a sfera, matita
odice del candidato: ržavni izpitni center *M13243121I* SESSIONE UTUNNLE Prova d esame 1 Giovedì, 29 agosto 2013 / 90 minuti l candidato sono consentiti l'uso della penna stilografica o a sfera, matita
Energia elettrica. L atomo nel suo complesso è neutro perché ha l equilibrio tra protoni ed elettroni presenti nello stesso numero.
 Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO
 LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO F I S I C A CLASSI NUOVO ORDINAMENTO A. S. 2014/2015 COMPETENZE PRIMO BIENNIO: SC1 SC2 Osservare descrivere ed
LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO F I S I C A CLASSI NUOVO ORDINAMENTO A. S. 2014/2015 COMPETENZE PRIMO BIENNIO: SC1 SC2 Osservare descrivere ed
Poniamo il carbonio al centro, tre idrogeni sono legati al carbonio direttamente e uno attraverso l ossigeno
 Strutture di Lewis E un metodo semplice per ottenere le formule di struttura di composti covalenti nota la formula molecolare, la configurazione elettronica del livello di valenza degli atomi e la connettività
Strutture di Lewis E un metodo semplice per ottenere le formule di struttura di composti covalenti nota la formula molecolare, la configurazione elettronica del livello di valenza degli atomi e la connettività
FISICA Corso di laurea in Informatica e Informatica applicata
 FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
COMPONENTI OTTICI ATTIVI
 COMPONENTI OTTICI ATTIVI Sono quei dispositivi necessari per lo scambio di informazioni su fibra ottica ossia per la trasmissione di impulsi luminosi. Si distinguono in convertitori elettro-ottici, convertitori
COMPONENTI OTTICI ATTIVI Sono quei dispositivi necessari per lo scambio di informazioni su fibra ottica ossia per la trasmissione di impulsi luminosi. Si distinguono in convertitori elettro-ottici, convertitori
