di Johnny E. Brian jr Chiudi
|
|
|
- Cecilia Caputo
- 5 anni fa
- Visualizzazioni
Transcript
1 di Johnny E. Brian jr Chiudi La finestra dell ossigeno. La sottosaturazione interna. Il calo di pressione parziale. Molti subacquei interessati alla decompressione hanno incontrato questi termini. Tutte e tre le espressioni vengono usate per descrivere lo stesso fenomeno fisiologico. Per questo articolo la definizione di finestra dell ossigeno sarà usata nell accezione più comune del termine. Tuttavia i termini sottosaturazione interna e calo di pressione parziale descrivono in modo più corretto il fenomeno fisico. Ossigeno iperbarico e finestra ossigeno Le attuali tecniche di ottimizzazione della decompressione, basate sull uso dell ossigeno, sono stabilite sullo sfruttamento della finestra dell ossigeno. Contrariamente al significato che è comunemente attribuito dai subacquei a quest espressione, questa sembra essere uno dei concetti meno compresi in merito alla decompressione. La comprensione della finestra dell ossigeno richiede la conoscenza della fisiologia del sistema circolatorio e del trasporto dei gas, e il modo migliore per cominciare è quello di affrontare la fisiologia in condizioni normobariche. La vita ad 1 atmosfera La fisiologia non è omogenea. In individui sani in normali condizioni, il flusso di sangue ai polmoni e la ventilazione, così come il flusso di sangue nei tessuti e il metabolismo, variano molto. Il flusso di sangue, la ventilazione e il metabolismo possono variare secondo le zone del corpo e dei momenti. Queste variabili condizionano lo scambio di gas nei polmoni e nei tessuti. Per rendere più semplice la comprensione di questi fenomeni complessi, molti meccanismi fisiologici sono stati ridotti ai minimi termini. Tuttavia, le descrizioni rispecchiano fedelmente i processi complessivi di assorbimento ed eliminazione del gas, e i valori riportati rappresentano i valori medi. Le pressioni parziali sono espresse in millimetri di mercurio (mmhg); 1 ATA equivale a 760 mm Hg. Per i puristi del Sistema Internazionale, dividendo i millimetri di mercurio per 7,5 si ottiene il valore in kilopascal (kpa), la corretta unità di misura della pressione secondo il sistema internazionale (SI). Il movimento del gas dai polmoni ai tessuti e viceversa dipende dalla differenza di pressione parziale (gradiente). Il concetto di pressione parziale di un gas in soluzione è, a volte, ingannevole quando si tratta di un gas disciolto in soluzione in un liquido. Un gas disciolto in soluzione in un liquido, infatti, non esercita una pressione idrostatica come un gas allo stato gassoso poiché le molecole o atomi di gas non sono libere di muoversi come nello stato gassoso. Questo è un concetto molto importante da capire o accettare. Le forze che tengono un gas in soluzione sono le stesse che tengono ogni soluto non ionizzato (gas, liquido o solido) in soluzione. I tessuti sono prevalentemente liquidi, e la pressione parziale di un gas disciolto in un liquido è definita come la pressione parziale che il gas eserciterebbe se la fase gassosa fosse in equilibrio con il tessuto. Le pressioni parziali dei gas nei tessuti sono spesso espresse in mmhg or atmosfere assolute (ATA). La pressione parziale del gas nel tessuto è un indice della quantità totale di gas disciolto nel tessuto. Tale quantitativo è anche condizionato dalla solubilità del gas, che varia secondo i gas ed i tessuti. Un tessuto può assorbire un maggiore quantitativo di un gas molto solubile rispetto ad uno meno solubile, prima di raggiungere una determinata 1 / 6
2 pressione. In altre parole, se un determinato volume di gas si scioglie in un tessuto, la pressione parziale tissutale di un gas molto solubile sarà inferiore rispetto a quella di un gas meno solubile. Il gas in soluzione si muove per diffusione da un area di maggiore pressione parziale ad una a minore pressione parziale. Nonostante la forza che governa la diffusione sia la differenza di pressione parziale (gradiente), non è la pressione in sé che muove il gas. Quando un gas è pressurizzato per riempire una bombola, la differenza di pressione governa il movimento di tale gas e si ha il movimento di una massa di gas. Tuttavia, la diffusione di un gas in soluzione non è il movimento di una massa di gas dovuto alla differenza di pressione del gas quanto piuttosto, il movimento dei singoli atomi o delle molecole dovuto ad un agitazione atomica o molecolare casuale. La diffusione di un gas singolo verso o da un tessuto dipende unicamente dalla differenza di pressione parziale del singolo gas preso in esame (gradiente) e non dagli altri gas presenti nel tessuto. Questo può sembrare paradossale poiché i subacquei spesso concepiscono i gas, presenti nei tessuti, come se esercitassero una pressione che spinge gli altri gas fuori del tessuto. Questa analogia non è corretta. La diffusione dei gas non dipende dal movimento di una massa di gas dovuto alla differenza di pressione del gas ma, piuttosto, dal movimento degli atomi o delle molecole dei singoli gas dovuto alla differenza di pressione parziale dei singoli gas. Le interazioni fra i singoli gas disciolti in soluzione non influenza la diffusione dei gas. Per esempio, la figura 1 mostra la diffusione del gas dal sangue al tessuto. Nella figura 1A, al momento 0, il sangue con pressione di elio (He) di 500 mmhg scorre in un capillare in un tessuto con una PHe pari a zero. A causa del movimento casuale, gli atomi d elio cominciano ad incontrare la membrana interna del capillare. Alcuni atomi d elio attraversano la membrana del capillare e raggiungono il tessuto da dove gli atomi possono diffondere ulteriormente nel tessuto stesso oppure ritornare indietro nel capillare. La direzione del movimento è un evento casuale, ma a questo punto, ci sono molti più atomi che attraversano la membrana del capillare muovendosi verso il tessuto che non viceversa, e la diffusione complessiva dell elio è dal capillare al tessuto. In un determinato momento, intermedio fra la figura 1A e la figura 1B, la PHe nel tessuto raggiungerà il valore di 250 mmhg. A questo punto, gli atomi d elio nel tessuto, incontrerebbero la membrana esterna del capillare, con una frequenza pari alla metà di quella con la quale gli atomi nel sangue incontrerebbero la membrana interna. La diffusione 2 / 6
3 2 Trasporto di gas nel sangue In ogni condizione, il sangue che attraversa i polmoni, cede CO2 e assorbe O2. In condizioni normali, ad 1 ATA, noi siamo saturi di N 2 e tracce d altri gas, così che non vi è differenza di pressione parziale per questi gas fra sangue e polmoni. Per la maggior parte delle funzioni fisiologiche, N 2 e tracce d altri gas, vengono ignorati e non vi è scambio di questi gas. Per i nostri scopi, è utile includere l azoto e tracce d altri gas così che questo ci aiuti ad illustrare come la finestra d ossigeno possa essere allargata. Nel seguito, le tracce di gas (principalmente argon), sono state incluse nell N 2 per semplificare la discussione e le figure. La 2 CO atmosferica è stata ignorata poiché rappresenta solo una frazione minima dell atmosfera. Quando respiriamo aria ad 1 ATA, l aria inspirata si muove giù per le vie aeree fino a raggiungere gli alveoli, le unità di scambio del gas dei polmoni. Quando il gas entra nei nostri polmoni diventa saturo di vapore acqueo che diluisce i gas inspirati. A 37 C la pressione parziale del vapore acqueo è 47 mmhg. La membrana degli alveoli non costituisce una barriera alla diffusione del gas ed i gas alveolari rapidamente raggiungono l equilibrio con il sangue che attraversa i capillari alveolari. Poiché gli alveoli sono spazi in contatto con l atmosfera, la somma delle pressioni parziali dei gas negli alveoli deve essere equivalente alla pressione ambiente. 2dal sangue agli alveoli; L ossigeno entrambi i processi si contribuiscono diffonde ad abbassare dagli alveoli la pressione parziale al sangue, dell ossigeno negli la alveoli CO(PO 2 ). La figura 2 mostra le pressioni parziali dei gas inspirati e dei gas alveolari per l aria. Ad 1 ATA, l aria di 159 secca mmhg; ha una tuttavia, PO raggiungendo l alveolo e equilibrandosi con il sangue, la PO La finestra ossigeno DIR Italia.it complessiva dell elio è ancora diretta verso il tessuto ma, ad una velocità pari alla metà di quella indicata in figura 1A. Al momento 0+X, l equilibrio è raggiunto e la pressione parziale dell elio (PHe) è pari a 500 mm Hg, sia nel tessuto che nel sangue (figura 1B). In condizioni d equilibrio gli atomi d elio continuano ad incontrare la membrana del capillare e diffondono nel tessuto, alla stessa velocità che avevano quando la pressione d elio nel tessuto era pari a zero. Tuttavia la diffusione complessiva dell elio ora è pari a 0, poiché gli atomi d'elio che attraversano la membrana delcapillare in un senso, sono pari a quelli che la attraversano in direzione opposta (contrassegnato dalle frecce della medesima lunghezza). Nella figura 1C è rappresentata una condizione simile alla figura 1A, ad eccezione del fatto che il sangue e il tessuto sono stati saturati con 500 mmhg di pressione parziale d azoto (PN2 ). N2 è in equilibrio e le sue molecole si diffondono, da e verso il sangue, con la stessa velocità. Supponendo che la pressione ambiente sia uguale o maggiore di 1000 mmhg, quando il sangue, con una PN 2 di 500 mm Hg e di He pari a 500 mm Hg scorre nel capillare, l elio si diffonde nel tessuto esattamente come nella figura 1A. Le molecole di N non bloccano la diffusione dell elio dal sangue al tessuto. Il gradiente di diffusione dell elio è 500 mm Hg in entrambe le figure 1A e 1C. Nella figura 1D l elio raggiungerà l equilibrio con il tessuto nello stesso tempo che impiega nel caso rappresentato dalla figura 1B. Quando un gas si diffonde attraverso un liquido, le interazioni delle molecole del gas con le molecole del liquido, prevalgono su ogni interazione gas-gas. Per esempio, se l acqua è satura con N2 a 1 ATA a 37 C, le molecole di N2 sono solo lo 0,01% del totale delle molecole (acqua e N 2 ). Se il quantitativo di N2 viene duplicato (2 ATA) allora le molecole di N2 aumentano solo fino allo 0,02% del totale delle molecole. Nella realtà, la possibilità d interazione fra N 2 e molecole di gas è ancora maggiore di quanto le percentuali riportate possano indicare, rispetto alla possibilità d interazione gas-gas, poiché il diametro delle molecole d acqua è più largo della maggior parte delle molecole di gas. Tuttavia, a causa delle interazioni solvente/soluto (acqua/gas), le molecole di gas disciolte tendono a rimanere circondate da molecole d acqua. Il concetto che le molecole, o gli atomi di gas disciolti, possano spingere le altre molecole di gas fuori del tessuto a causa delle interazioni gas-gas non è corretto. 3 / 6
4 4 / 6
5 5 / 6
6 6 / 6
O2: % 84, N2: % 62, % CO2:
 Diffusione alveolo-capillare dei gas respiratori La quantità di un gas che diffonde nell unità di tempo (velocità di diffusione) dipende dalla sua pressione parziale (p), che, per la Legge di Dalton è
Diffusione alveolo-capillare dei gas respiratori La quantità di un gas che diffonde nell unità di tempo (velocità di diffusione) dipende dalla sua pressione parziale (p), che, per la Legge di Dalton è
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
FISIOLOGIA DELL APPARATO RESPIRATORIO
 FISIOLOGIA DELL APPARATO RESPIRATORIO L APPARATO RESPIRATORIO Il cuore è l organo centrale del sistema circolatorio: funge da pompa capace di produrre una pressione sufficiente a permettere la circolazione
FISIOLOGIA DELL APPARATO RESPIRATORIO L APPARATO RESPIRATORIO Il cuore è l organo centrale del sistema circolatorio: funge da pompa capace di produrre una pressione sufficiente a permettere la circolazione
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
LA DIFFUSIONE. M At 1 A. dm dt
 LA DIFFUSIONE Il trasferimento di massa, all interno di un solido, di un liquido o di un gas o di un altra fase solida è detto diffusione ( trasporto di materiale mediante movimento di atomi). La diffusione
LA DIFFUSIONE Il trasferimento di massa, all interno di un solido, di un liquido o di un gas o di un altra fase solida è detto diffusione ( trasporto di materiale mediante movimento di atomi). La diffusione
Gli scambi gassosi, i gradienti di pressione parziale e la finestra di Ossigeno.
 Gli scambi gassosi, i gradienti di pressione parziale e la finestra di Ossigeno. di Johnny E. Brian Jr. M.D. Professore Associato Dipartimento di Anestesia University of Iowa College of Medicine Traduzione
Gli scambi gassosi, i gradienti di pressione parziale e la finestra di Ossigeno. di Johnny E. Brian Jr. M.D. Professore Associato Dipartimento di Anestesia University of Iowa College of Medicine Traduzione
Fisiologia della Respirazione 9.Scambi gassosi-ventilazione vent/perf. FGE aa
 Fisiologia della Respirazione 9.Scambi gassosi-ventilazione vent/perf FGE aa.2015-16 Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso di sangue nei polmoni, composizione dell aria
Fisiologia della Respirazione 9.Scambi gassosi-ventilazione vent/perf FGE aa.2015-16 Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso di sangue nei polmoni, composizione dell aria
I gas e loro proprietà Cap , 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96
 2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
CdL Professioni Sanitarie A.A. 2012/2013. Unità 9: Gas e processi di diffusione
 L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
Temperatura. Il legame con le grandezze microscopiche è di tipo statistico. Pressione Volume Temperatura
 Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Fisicaa Applicata, Area Tecnica, M. Ruspa Esercizio. Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli. 2) il numero di molecole
 Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
Fisiologia della Respirazione 9.Scambi gassosi-ventilazione 1. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 9.Scambi gassosi-ventilazione 1 Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso
Fisiologia della Respirazione 9.Scambi gassosi-ventilazione 1 Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso
Fisiologia della Respirazione
 Fisiologia della Respirazione Scambi gassosi-ventilazione vent/perf FGE aa.2016-17 Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso di sangue nei polmoni, composizione dell aria ambiente,
Fisiologia della Respirazione Scambi gassosi-ventilazione vent/perf FGE aa.2016-17 Obiettivi Studio delle relazioni quantitative tra ventilazione, flusso di sangue nei polmoni, composizione dell aria ambiente,
Stati d aggregazione della materia
 Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Lo scambio gassoso negli animali
 Lo scambio gassoso negli animali Durante la RESPIRAZIONE CELLULARE (mitocondri) le cellule consumano O2 e producono CO2 L approvvigionamento di O2 e la rimozione della CO2 avvengono tramite SCAMBI GASSOSI
Lo scambio gassoso negli animali Durante la RESPIRAZIONE CELLULARE (mitocondri) le cellule consumano O2 e producono CO2 L approvvigionamento di O2 e la rimozione della CO2 avvengono tramite SCAMBI GASSOSI
po % O % N % CO 2 = 159 mmhg pn 2 = 597 mmhg pco 2 = 0.3 mmhg
 Scambi alveolari L aria che respiriamo è una miscela di gas, principalmente costituita da O 2, N 2 e CO 2. La velocità di diffusione di ciascuno di questi gas (quantità di gas che diffonde nell unità di
Scambi alveolari L aria che respiriamo è una miscela di gas, principalmente costituita da O 2, N 2 e CO 2. La velocità di diffusione di ciascuno di questi gas (quantità di gas che diffonde nell unità di
Dinamica dei fluidi viscosi
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Dinamica dei fluidi viscosi 14/3/2006 Ripartizione del sangue portata totale NQ diametro iniziale D diametro d dei rami secondari
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Dinamica dei fluidi viscosi 14/3/2006 Ripartizione del sangue portata totale NQ diametro iniziale D diametro d dei rami secondari
1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido.
 UNITÀ 8 LA MECCANICA DEI FLUIDI 1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido. 3. La pressione atmosferica. 4. La legge di Stevino. 5. La legge di Pascal. 6. La forza di Archimede.
UNITÀ 8 LA MECCANICA DEI FLUIDI 1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido. 3. La pressione atmosferica. 4. La legge di Stevino. 5. La legge di Pascal. 6. La forza di Archimede.
Sherwood, FISIOLOGIA UMANA. Dalle cellule ai sistemi, Zanichelli editore S.p.A. Copyright
 13 1 13 2 13 3 Le pleure sono costituite da diversi strati di tessuto connettivo elastico e numerosi capillari. Esse contengono il liquido pleurico e hanno due funzioni fondamentali: 1 - creare una superficie
13 1 13 2 13 3 Le pleure sono costituite da diversi strati di tessuto connettivo elastico e numerosi capillari. Esse contengono il liquido pleurico e hanno due funzioni fondamentali: 1 - creare una superficie
Apparato respiratorio
 Apparato respiratorio Anatomia Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre muscolari
Apparato respiratorio Anatomia Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre muscolari
Apparato respiratorio. Anatomia
 Apparato respiratorio Anatomia 1 Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre
Apparato respiratorio Anatomia 1 Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre
LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE
 LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE Un corpo immerso in un fluido riceve una spinta dal basso verso l'alto pari al peso del volume del fluido che sposta. Il GAV è una applicazione pratica
LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE Un corpo immerso in un fluido riceve una spinta dal basso verso l'alto pari al peso del volume del fluido che sposta. Il GAV è una applicazione pratica
il sistema respiratorio
 il sistema respiratorio respirazione cellulare (o interna) e respirazione esterna scambio dei gas regolato dalle leggi della diffusione in alcuni organismi la respirazione avviene attraverso la superficie
il sistema respiratorio respirazione cellulare (o interna) e respirazione esterna scambio dei gas regolato dalle leggi della diffusione in alcuni organismi la respirazione avviene attraverso la superficie
POTENZA METABOLICA. Fisica Applicata, Area Infermieristica, M. Ruspa
 POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
Chimica. Gli stati di aggregazione della materia
 Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
Anatomia del sistema respiratorio
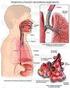 Funzioni del sistema respiratorio 1. Convogliare l aria muovendola verso le vie respiratorie e viceversa. 2. Proteggere le superfici di scambio da danni ambientali e disidratazione. 3. Riscaldare e umidificare
Funzioni del sistema respiratorio 1. Convogliare l aria muovendola verso le vie respiratorie e viceversa. 2. Proteggere le superfici di scambio da danni ambientali e disidratazione. 3. Riscaldare e umidificare
Stati di aggregazione della materia. dal microscopico al macroscopico: struttura. interazioni GASSOSO. proprietà SOLIDO LIQUIDO
 Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della
 Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
INTRODUZIONE ALLA TERMODINAMICA. Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta
 INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
FISIOLOGIA VEGETALE. I movimenti dell acqua e dei soluti
 FISIOLOGIA VEGETALE I movimenti dell acqua e dei soluti MOVIMENTI DELL ACQUA E DEI SOLUTI L acqua si muove seguente delle differenze di potenziali di energia Il potenziale di energia è l energia che viene
FISIOLOGIA VEGETALE I movimenti dell acqua e dei soluti MOVIMENTI DELL ACQUA E DEI SOLUTI L acqua si muove seguente delle differenze di potenziali di energia Il potenziale di energia è l energia che viene
Le soluzioni e il loro comportamento
 A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
FENOMENI DI TRASPORTO DELLA MATERIA
 FENOMENI DI TRASPORTO DELLA MATERIA MOTI BROWNIANI Gli atomi e le molecole che costituiscono la materia non sono mai fermi, se non alla temperatura dello zero assoluto (T 0 K -273 C) In particolare, mentre
FENOMENI DI TRASPORTO DELLA MATERIA MOTI BROWNIANI Gli atomi e le molecole che costituiscono la materia non sono mai fermi, se non alla temperatura dello zero assoluto (T 0 K -273 C) In particolare, mentre
SOLUZIONI. Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto).
 SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
Anatomia del sistema respiratorio
 Funzioni del sistema respiratorio 1. Fornire una vasta area per lo scambio gassoso tra sangue e ambiente esterno (aria) per consentire ingresso di ossigeno ed eliminazione di anidride carbonica. 2. Convogliare
Funzioni del sistema respiratorio 1. Fornire una vasta area per lo scambio gassoso tra sangue e ambiente esterno (aria) per consentire ingresso di ossigeno ed eliminazione di anidride carbonica. 2. Convogliare
. Proprietà degli stati della materia Aeriforme Liquido Solido
 . Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
. Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
Aria e pressione. Enrico Degiuli Classe prima
 Aria e pressione Enrico Degiuli Classe prima Le proprietà dell aria L aria è un miscuglio di gas, è composta da 78% di azoto 21% di ossigeno 1% altri gas (argon, CO2, neon, elio, ) Il nostro pianeta è
Aria e pressione Enrico Degiuli Classe prima Le proprietà dell aria L aria è un miscuglio di gas, è composta da 78% di azoto 21% di ossigeno 1% altri gas (argon, CO2, neon, elio, ) Il nostro pianeta è
Alcuni esempi di ruoli fisiologici. Effetto di trascinamento nei capillari arteriosi e venosi Effetto di trascinamento nel glomerulo renale
 Alcuni esempi di ruoli fisiologici Effetto di trascinamento nei capillari arteriosi e venosi Effetto di trascinamento nel glomerulo renale Formazione e riassorbimento del liquido interstiziale Cellule
Alcuni esempi di ruoli fisiologici Effetto di trascinamento nei capillari arteriosi e venosi Effetto di trascinamento nel glomerulo renale Formazione e riassorbimento del liquido interstiziale Cellule
VENTILAZIONE e PERFUSIONE
 VENTILAZIONE e PERFUSIONE VENTILAZIONE Ven2lazione= VE = f x VC f= frequenza VC= volume corrente (500mL nell adulto) =volume di aria inspirato/espirato in ogni singolo alo respiratorio Composizione dell
VENTILAZIONE e PERFUSIONE VENTILAZIONE Ven2lazione= VE = f x VC f= frequenza VC= volume corrente (500mL nell adulto) =volume di aria inspirato/espirato in ogni singolo alo respiratorio Composizione dell
Esercitazioni Infermieristica
 Esercitazioni Infermieristica Novara: Gruppo A 28/1 9-13 29/1 14-18 Gruppo B 28/1 14-18 29/1 9-13 Alba 7/12/2012 11-13 14-17 25/01/2013 15-18 a Novara Alessandria 18/12/2012 10-13 14-16 14/01/2013 10-13
Esercitazioni Infermieristica Novara: Gruppo A 28/1 9-13 29/1 14-18 Gruppo B 28/1 14-18 29/1 9-13 Alba 7/12/2012 11-13 14-17 25/01/2013 15-18 a Novara Alessandria 18/12/2012 10-13 14-16 14/01/2013 10-13
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
Fisiologia della Respirazione 1.Introduzione-Leggi dei Gas. FGE aa.2015-16
 Fisiologia della Respirazione 1.Introduzione-Leggi dei Gas FGE aa.2015-16 Obiettivi Trasporto ventilatorio convettivo dei gas integrato con trasporto convettivo circolatorio e respirazione cellulare Cenni
Fisiologia della Respirazione 1.Introduzione-Leggi dei Gas FGE aa.2015-16 Obiettivi Trasporto ventilatorio convettivo dei gas integrato con trasporto convettivo circolatorio e respirazione cellulare Cenni
Apparato Respiratorio
 Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia e Biofisica A.A. 2016-2017 Apparato Respiratorio Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unina2.it
Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia e Biofisica A.A. 2016-2017 Apparato Respiratorio Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unina2.it
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
COMPITO: assicurare un continuo ed adeguato apporto di O 2 alle cellule ed eliminare l eccesso di CO 2
 RESPIRAZIONE è l insieme dei meccanismi che permettono lo scambio di gas metabolicamente attivi (O 2 e CO 2 ) tra ambiente esterno e cellule dell organismo vivente COMPITO: assicurare un continuo ed adeguato
RESPIRAZIONE è l insieme dei meccanismi che permettono lo scambio di gas metabolicamente attivi (O 2 e CO 2 ) tra ambiente esterno e cellule dell organismo vivente COMPITO: assicurare un continuo ed adeguato
Azoto. La molecola di azoto e formata da due atomi di azoto, legati insieme con un triplo legame:
 Aria ed atmosfera L aria Questo sottile strato, inodore ed incolore è una miscela di gas: 78 % di azoto; 21 % di ossigeno; 0,03 % di anidride carbonica; 0,97 % altri gas. Azoto La molecola di azoto e formata
Aria ed atmosfera L aria Questo sottile strato, inodore ed incolore è una miscela di gas: 78 % di azoto; 21 % di ossigeno; 0,03 % di anidride carbonica; 0,97 % altri gas. Azoto La molecola di azoto e formata
QUADERNI DIDATTICI L OSSIGENO NEGLI INCIDENTI DECOMPRESSIVI IN COLLABORAZIONE CON
 QUADERNI DIDATTICI L OSSIGENO NEGLI INCIDENTI DECOMPRESSIVI IN COLLABORAZIONE CON DIPARTIMENTO NAZIONALE EMERGENZA MARE 1 NEGLI INCIDENTI DECOMPRESSIVI SOMMINISTRARE OSSIGENO FINO ALL ARRIVO IN CAMERA
QUADERNI DIDATTICI L OSSIGENO NEGLI INCIDENTI DECOMPRESSIVI IN COLLABORAZIONE CON DIPARTIMENTO NAZIONALE EMERGENZA MARE 1 NEGLI INCIDENTI DECOMPRESSIVI SOMMINISTRARE OSSIGENO FINO ALL ARRIVO IN CAMERA
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Chimica generale. Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3
 Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Fisica per scienze ed ingegneria
 Serway, Jewett Fisica per scienze ed ingegneria Capitolo 19 Temperatura e principio zero della termodinamica I nostri sensi non sono affidabili per definire lo stato termico dei corpi. Ocorre un metodo
Serway, Jewett Fisica per scienze ed ingegneria Capitolo 19 Temperatura e principio zero della termodinamica I nostri sensi non sono affidabili per definire lo stato termico dei corpi. Ocorre un metodo
GAS. H 2 N 2 O 2 F 2 Cl 2 CO CO 2 NO 2 SO 2 CH 4
 GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
FISIOLOGIA GENERALE - ESERCITAZIONE n. 5 del 30 Novembre Superficie
 FISIOLOGIA GENERALE - ESERCITAZIONE n. 5 del 30 Novembre 2016 Esercizio n. 1 Respirazione Si prendano in considerazione i diversi fattori che, in combinazione, danno origine alle differenze di velocità
FISIOLOGIA GENERALE - ESERCITAZIONE n. 5 del 30 Novembre 2016 Esercizio n. 1 Respirazione Si prendano in considerazione i diversi fattori che, in combinazione, danno origine alle differenze di velocità
Fisiologia della Respirazione 10.Scambi gassosiventilazione. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 10.Scambi gassosiventilazione 2 Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Distribuzione zonale della ventilazione e della perfusione
Fisiologia della Respirazione 10.Scambi gassosiventilazione 2 Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Distribuzione zonale della ventilazione e della perfusione
Le forze intermolecolari ed i liquidi Brooks/Cole - Cengage
 2018 Le forze intermolecolari ed i liquidi 1 2009 Brooks/Cole - Cengage Forze Intermolecolari 2 Forze intermolecolari sono forze che si esercitano fra molecole, fra ioni, o fra molecole e ioni. Forze intramolecolari
2018 Le forze intermolecolari ed i liquidi 1 2009 Brooks/Cole - Cengage Forze Intermolecolari 2 Forze intermolecolari sono forze che si esercitano fra molecole, fra ioni, o fra molecole e ioni. Forze intramolecolari
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
Lezione 11 Soluzioni. Diffusione ed osmosi.
 Lezione 11 Soluzioni. Diffusione ed osmosi. Soluzioni Una soluzione è formata da un insieme di molecole di uno o più soluti (eventualmente dissociati in ioni), disciolti in un solvente (nei sistemi biologici
Lezione 11 Soluzioni. Diffusione ed osmosi. Soluzioni Una soluzione è formata da un insieme di molecole di uno o più soluti (eventualmente dissociati in ioni), disciolti in un solvente (nei sistemi biologici
Equilibrio chimico. Equilibri dinamici Legge azione di massa, Kc, Kp, Equilibri eterogenei Principio di Le Chatelier
 Equilibrio chimico Equilibri dinamici Legge azione di massa, Kc, Kp, Equilibri eterogenei Principio di Le Chatelier Data la reazione generica: A + B C Seguendo nel tempo le variazioni di concentrazione
Equilibrio chimico Equilibri dinamici Legge azione di massa, Kc, Kp, Equilibri eterogenei Principio di Le Chatelier Data la reazione generica: A + B C Seguendo nel tempo le variazioni di concentrazione
L APPARATO RESPIRATORIO
 Tutte le illustrazioni sono state prese dal seguente testo con l unico proposito di illustrare questi appunti ad uso e consumo degli studenti di Scienze Motorie che a causa del terremoto non hanno potuto
Tutte le illustrazioni sono state prese dal seguente testo con l unico proposito di illustrare questi appunti ad uso e consumo degli studenti di Scienze Motorie che a causa del terremoto non hanno potuto
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Regolazione della pressione arteriosa
 Regolazione della pressione arteriosa Riflesso barocettivo Controllo riflesso Centro di integrazione: bulbo del troncoencefalico Mantenimento flusso sanguigno a cuore e cervello Risposta veloce Regolazione
Regolazione della pressione arteriosa Riflesso barocettivo Controllo riflesso Centro di integrazione: bulbo del troncoencefalico Mantenimento flusso sanguigno a cuore e cervello Risposta veloce Regolazione
Fisiologia della Respirazione 7.Meccanica respiratoria: dinamica. FGE aa
 Fisiologia della Respirazione 7.Meccanica respiratoria: dinamica FGE aa.2015-16 Obiettivi Relazione P-flusso in regime di flusso lineare; resistenze Flusso turbolento e numero di Reynolds Flusso di transizione
Fisiologia della Respirazione 7.Meccanica respiratoria: dinamica FGE aa.2015-16 Obiettivi Relazione P-flusso in regime di flusso lineare; resistenze Flusso turbolento e numero di Reynolds Flusso di transizione
Fisiologia della Respirazione
 Fisiologia della Respirazione 6.Meccanica respiratoria: Statica e fenomeni di superficie 2 FGE aa.2016-17 Obiettivi I fenomeni di superficie principali determinanti dell isteresi polmonare e della pressione
Fisiologia della Respirazione 6.Meccanica respiratoria: Statica e fenomeni di superficie 2 FGE aa.2016-17 Obiettivi I fenomeni di superficie principali determinanti dell isteresi polmonare e della pressione
= cost a p costante V 1 /T 1 =V 2 /T 2 LEGGE DI GAY-LUSSAC: Un sistema allo stato gassoso è definito da 4. mmhg (torr), bar.
 GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
Corso: Chimica Fisica
 Docente: Gianni ROMEO Corso: Chimica Fisica pagina 1 di 6 TEST N. 3 (IL CORRETTORE DEL TEST È A PAGINA 2 ) DATA: 07.01.2010 Argomenti (Moduli 1 e 2): Materia ed Energia; le Unità di Misura e l Analisi
Docente: Gianni ROMEO Corso: Chimica Fisica pagina 1 di 6 TEST N. 3 (IL CORRETTORE DEL TEST È A PAGINA 2 ) DATA: 07.01.2010 Argomenti (Moduli 1 e 2): Materia ed Energia; le Unità di Misura e l Analisi
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Trasformazioni fisiche della materia: i passaggi di stato
 Trasformazioni fisiche della materia: i passaggi di stato Nelle condizioni terrestri la materia può presentarsi in tre differenti stati fisici o stati di aggregazione: solido, liquido e aeriforme. I solidi
Trasformazioni fisiche della materia: i passaggi di stato Nelle condizioni terrestri la materia può presentarsi in tre differenti stati fisici o stati di aggregazione: solido, liquido e aeriforme. I solidi
Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei
 Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
Il cuore tra lo spazio e gli abissi marini F i s i o p a t o l o g i a cardiovascolare in ipergravità, ipobarismo ed ambiente iperbarico
 Umberto Berrettini Angelo Landolfi Il cuore tra lo spazio e gli abissi marini F i s i o p a t o l o g i a cardiovascolare in ipergravità, ipobarismo ed ambiente iperbarico Casa Editrice Scientifica Internazionale
Umberto Berrettini Angelo Landolfi Il cuore tra lo spazio e gli abissi marini F i s i o p a t o l o g i a cardiovascolare in ipergravità, ipobarismo ed ambiente iperbarico Casa Editrice Scientifica Internazionale
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Fisiologia della Respirazione 2.Ventilazione. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 2.Ventilazione Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Muscoli inspiratori ed espiratori coinvolti nella respirazione a riposo,
Fisiologia della Respirazione 2.Ventilazione Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Muscoli inspiratori ed espiratori coinvolti nella respirazione a riposo,
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
STATO GASSOSO. parte I a. - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio
 STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 16 L equilibrio chimico 1. L equilibrio dinamico 2. L equilibrio chimico: anche i prodotti reagiscono
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 16 L equilibrio chimico 1. L equilibrio dinamico 2. L equilibrio chimico: anche i prodotti reagiscono
LA MATERIA E IL MODELLO PARTICELLARE
 LA MATERIA E IL MODELLO PARTICELLARE - Gli oggetti che ci circondano sono costituiti di materia. - Come possiamo definire la materia? La materia è tutto ciò che possiede una massa e occupa un volume. -
LA MATERIA E IL MODELLO PARTICELLARE - Gli oggetti che ci circondano sono costituiti di materia. - Come possiamo definire la materia? La materia è tutto ciò che possiede una massa e occupa un volume. -
Termoscopio di Galileo Sfrutta la dilatazione termica dell aria contenuta al suo interno.
 Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
La meccanica dei fluidi
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La meccanica dei fluidi 7/3/2006 Stati della materia Esistono tre stati della materia Il solido ha volume e forma definita La forma
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La meccanica dei fluidi 7/3/2006 Stati della materia Esistono tre stati della materia Il solido ha volume e forma definita La forma
MEMBRANE. MEMBRANE equilibri gas-liquido. elio giroletti
 UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
Trasporto gas nel sangue
 Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Foto funzioni apparato respiratorio
 RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
ESERCITAZIONE 6. Dr.ssa Valeria Monti Corso di Laurea in Chimica e Tecnologia Farmaceutiche Fisica a.a
 ESERCITAZIONE 6 Dr.ssa Valeria Monti Corso di Laurea in Chimica e Tecnologia Farmaceutiche Fisica a.a. 2016 2017 Fluidi : Esercizio 1 Un arteria di raggio R 1 = 2.5 mm è parzialmente bloccata da una placca.
ESERCITAZIONE 6 Dr.ssa Valeria Monti Corso di Laurea in Chimica e Tecnologia Farmaceutiche Fisica a.a. 2016 2017 Fluidi : Esercizio 1 Un arteria di raggio R 1 = 2.5 mm è parzialmente bloccata da una placca.
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
P aria (livello del mare) = 760 mmhg. Composizione: O 2 : 20.84% N 2 : 78.62% CO 2 : 0.04% po 2 = 159 mmhg. pn 2 = 597mmHg. pco 2 = 0.
 Scambi alveolari Aria atmosferica = miscela di gas (principalmente O 2, N 2, CO 2 ) La velocità di diffusione di un gas (quantità di gas che diffonde nell unità di tempo) è direttamente proporzionale alla
Scambi alveolari Aria atmosferica = miscela di gas (principalmente O 2, N 2, CO 2 ) La velocità di diffusione di un gas (quantità di gas che diffonde nell unità di tempo) è direttamente proporzionale alla
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI)
 1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore.
 Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore. Cambiamenti di stati di aggregazione Gli stati di aggregazione della materia sono: solido, liquido gassoso (e
Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore. Cambiamenti di stati di aggregazione Gli stati di aggregazione della materia sono: solido, liquido gassoso (e
Fisiologia della Respirazione 6.Meccanica respiratoria: Statica e fenomeni di superficie 2. FGE aa
 Fisiologia della Respirazione 6.Meccanica respiratoria: Statica e fenomeni di superficie 2 FGE aa.2015-16 Obiettivi I fenomeni di superficie principali determinanti dell isteresi polmonare e della pressione
Fisiologia della Respirazione 6.Meccanica respiratoria: Statica e fenomeni di superficie 2 FGE aa.2015-16 Obiettivi I fenomeni di superficie principali determinanti dell isteresi polmonare e della pressione
12/03/2013. Aria umida. Proprietà e trasformazioni
 Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
L apparato respiratorio. In movimento Marietti Scuola 2010 De Agostini Scuola S.p.A. Novara
 L apparato respiratorio Fasi della respirazione La ventilazione polmonare (o esterna) La diffusione Il trasporto dei gas La respirazione cellulare (o interna) Le vie aeree Le vie aeree I polmoni Il destro
L apparato respiratorio Fasi della respirazione La ventilazione polmonare (o esterna) La diffusione Il trasporto dei gas La respirazione cellulare (o interna) Le vie aeree Le vie aeree I polmoni Il destro
Fisica Applicata, Area Infermieristica, M. Ruspa REGIMI DI MOTO DI UN FLUIDO REALE
 REGIMI DI MOTO DI UN FLUIDO REALE MOTO LAMINARE O TURBOLENTO? Dipende dalla velocita di scorrimento del fluido! VELOCITA CRITICA La velocita critica per un fluido di viscosita η e di densita d che scorre
REGIMI DI MOTO DI UN FLUIDO REALE MOTO LAMINARE O TURBOLENTO? Dipende dalla velocita di scorrimento del fluido! VELOCITA CRITICA La velocita critica per un fluido di viscosita η e di densita d che scorre
L acqua e la cellule vegetale. Importanza dell acqua per la pianta e meccanismi di movimento
 L acqua e la cellule vegetale Importanza dell acqua per la pianta e meccanismi di movimento Perché l acqua è importante per la pianta? Le cellule vegetali sono costituite per 80-95% di acqua consente il
L acqua e la cellule vegetale Importanza dell acqua per la pianta e meccanismi di movimento Perché l acqua è importante per la pianta? Le cellule vegetali sono costituite per 80-95% di acqua consente il
Stati d aggregazione della materia
 Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
