Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei
|
|
|
- Marisa Castelli
- 5 anni fa
- Visualizzazioni
Transcript
1 Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. Un miscuglio eterogeneo è costituito da più fasi. Le proprietà sono diverse nelle differenti parti. 5 6
2 Soluzioni e miscugli eterogenei Soluzioni e miscugli eterogenei Una soluzione è un sistema formato da più componenti ma in cui è visibile una sola fase, che presenta le stesse proprietà intensive in ogni parte. Una soluzione è un sistema formato da più componenti ma in cui è visibile una sola fase, che presenta le stesse proprietà intensive in ogni parte. Le soluzioni possono essere: liquide; gassose; solide (leghe metalliche). 7 8 Soluto, solvente e soluzione Soluto, solvente e soluzione I componenti di una soluzione sono: solvente: il componente più abbondante; soluti: i componenti presenti in minore quantità. soluto solvente SOLUTO SOLVENTE SOLUZIONE 10 9
3 Solvente, soluto e concentrazione La concentrazione di una soluzione è il rapporto tra la quantità di soluto e la quantità di solvente in cui il soluto è disciolto. Durante il processo fisico di dissoluzione la massa si conserva. Il volume, invece, non sempre si conserva. Solubilità e soluzioni sature Una sostanza che si scioglie facilmente in un solvente è detta solubile, mentre se non si scioglie è detta insolubile. Una soluzione è detta satura se contiene la massima quantità possibile di soluto e si forma il corpo di fondo. Solubilità e soluzioni sature La solubilità di un soluto in un certo solvente è la sua concentrazione nella soluzione satura. La solubilità varia da sostanza a sostanza e dipende dalla temperatura e dalla natura del solvente. corpo di fondo 12
4 Solubilità e soluzioni sature La solubilità di un solido aumenta con la temperatura e dipende dalla natura chimica del soluto. Solubilità e soluzioni sature La velocità del processo di dissoluzione di un solido dipende da: estensione della superficie di contatto; rimescolamento; temperatura Solubilità dei gas nei liquidi La legge di Henry afferma che all aumentare della pressione esercitata sul gas, la quantità di gas che si scioglie in un liquido aumenta. Solubilità dei gas nei liquidi La legge di Henry afferma che la quantità di gas che si scioglie in un liquido è direttamente proporzionale alla pressione esercitata dal gas. P1 P2 La CO 2 disciolta nel vino sotto pressione esce con violenza quando la bottiglia viene stappata a causa della diminuzione di pressione che determina una minore solubilità del gas. conc.1 conc.2 P2 > P1, conc.2 > conc
5 Solubilità dei gas nei liquidi Altri fattori che influenzano la solubilità dei gas sono la temperatura e le caratteristiche chimiche del soluto e del solvente. All aumentare della temperatura, diminuisce la quantità di gas che si scioglie in un liquido. Solubilità dei gas nei liquidi Un aumento della temperatura dell acqua causa una diminuzione della concentrazione dell ossigeno disciolto, a scapito degli esseri viventi subacquei. 19 Le dispersioni colloidali Le dispersioni colloidali, o colloidi, si formano quando le particelle disperse hanno dimensioni comprese tra 1 e 1000 nm. Come esprimere la concentrazione La composizione di una soluzione si esprime tramite la sua concentrazione: molarità = n soluto V soluzione (V espresso in litri) %m / m = m soluto 100 m (m espressa in grammi) soluzione %m / V = m soluto 100 V (m espressa in grammi, V espresso in ml) soluzione %V / V = V soluto 100 V (V espresso in ml) soluzione 20
6 Come esprimere la concentrazione Come esprimere la concentrazione Le due soluzioni hanno lo stesso rapporto tra la quantità di soluto e solvente, cioè hanno la stessa concentrazione. L indicazione Acidità: 6% dell aceto balsamico significa che sono presenti 6 g di acido acetico ogni 100 ml di aceto. Proprietà colligative delle soluzioni Le proprietà colligative delle soluzioni sono proprietà che dipendono dalla concentrazione delle molecole di soluto o degli ioni in soluzione, ma non dalla loro natura. abbassamento della tensione di vapore Le soluzioni hanno una minore tendenza ad evaporare rispetto al solvente puro. Esse sono: abbassamento della tensione di vapore abbassamento crioscopico innalzamento ebulloscopico osmosi
7 abbassamento crioscopico Le soluzioni hanno un punto di solidificazione più basso rispetto al solvente puro. Il soluto interferisce con la formazione del reticolo cristallino del ghiaccio e quindi la fase più stabile è quella liquida. L entità dell abbassamento crioscopico dipende dal numero di molecole o ioni disciolti in acqua, cioè dalla concentrazione. abbassamento crioscopico Supponiamo di avere del ghiaccio a 0 C e di aggiungere del sale. Il ghiaccio tenderà a fondere per dissolvere il sale. Per potersi fondere però il ghiaccio ha bisogno di assorbire calore che viene prelevato dalla miscela stessa che quindi diminuisce la propria temperatura. Con del normale sale da cucina si può arrivare fino a -21,1 C. Qui sotto potete vedere la temperatura raggiunta (-18.4 C) mescolando un poco di neve con del sale fino. innalzamento ebulloscopico L aggiunta di sale all acqua aumenta il suo punto di ebollizione: si parla di innalzamento ebullioscopico. Tuttavia per aumentare di un grado un litro di acqua si debbono aggiungere ben 58 grammi di sale da cucina, quantità ben superiori a quelle utilizzate in cucina (solitamente 5-10 grammi per litro), per cui a tutti gli effetti pratici l aggiunta del sale in cucina non aumenta apprezzabilmente il punto di ebollizione. Questo effetto si può osservare con qualsiasi altra sostanza disciolta, anche se l innalzamento può essere diverso a parità di grammi di sostanza aggiunta. osmosi Il processo dell osmosi rappresenta la diffusione del solvente attraverso una membrana semipermeabile dal compartimento a minore concentrazione di soluto verso quello a concentrazione maggiore. L'osmosi è un processo fisico spontaneo che tende a diluire la soluzione più concentrata e a ridurre la differenza di concentrazione. Il flusso netto di solvente può essere contrastato applicando una pressione (pressione osmotica) al compartimento a concentrazione maggiore.
8 osmosi osmosi in cucina In biologia, interviene in alcuni processi di trasporto passivo attraverso membrane biologiche.
Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea.
 Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni e il loro comportamento
 A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
STATO LIQUIDO. Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso
 STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 12 Aprile 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
 positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni
 1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
Esercizi Concentrazioni e diluizioni
 Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti
 LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 2 Le trasformazioni fisiche della materia 1. La materia e le sue caratteristiche 2. I sistemi omogenei e i sistemi
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 2 Le trasformazioni fisiche della materia 1. La materia e le sue caratteristiche 2. I sistemi omogenei e i sistemi
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
Le soluzioni. A cura della Prof. ssa Barone Antonina
 Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
PROPRIETA DELLE SOLUZIONI ACQUOSE. Prof.ssa Patrizia Gallucci
 PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato liquido
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Proprietà colligative
 Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
solvente soluto concentrazione
 Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
LE SOLUZIONI 07/04/2019
 LE SOLUZIONI Le sostanze tendono spontaneamente a miscelarsi tra loro; tale fenomeno si deve, soprattutto, all agitazione termica delle particelle che le porta a disperdersi disordinatamente. Si definisce
LE SOLUZIONI Le sostanze tendono spontaneamente a miscelarsi tra loro; tale fenomeno si deve, soprattutto, all agitazione termica delle particelle che le porta a disperdersi disordinatamente. Si definisce
Soluzioni unità 3, modulo D del libro
 Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
GLI STATI DELLA MATERIA
 GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
Un sistema è una porzione delimitata di materia.
 1. La materia e le sue caratteristiche Un sistema è una porzione delimitata di materia. 1. La materia e le sue caratteristiche Gli stati fisici in cui la materia si può trovare sono: solido; liquido; aeriforme.
1. La materia e le sue caratteristiche Un sistema è una porzione delimitata di materia. 1. La materia e le sue caratteristiche Gli stati fisici in cui la materia si può trovare sono: solido; liquido; aeriforme.
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Soluzioni semplici. Soluzioni liquide
 Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Soluzioni, Acidi e Basi
 Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI
 EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI Consideriamo un sistema formato da due liquidi A e B miscibili in tutte le proporzioni. Per la legge di Raoult
EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI Consideriamo un sistema formato da due liquidi A e B miscibili in tutte le proporzioni. Per la legge di Raoult
CARATTERISTICHE. In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee.
 In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
Lezione n. 12. Proprietà colligative Variazione del punto crioscopico. Pressione osmotica. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Il binomio di van t Hoff Le proprietà colligative dipendono dal numero di particelle effettivamente presenti nella soluzione. Nel caso in cui il solut
 Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Soluzioni. Un miscuglio eterogeneo è costituito da materia presente in stati omogenei diversi, definiti fasi del sistema eterogeneo.
 Le soluzioni Soluzioni Una soluzione è una miscela omogenea di due o più componenti. Il componente in quantità maggiore viene in genere indicato come solvente, gli altri con il nome di soluto. I componenti
Le soluzioni Soluzioni Una soluzione è una miscela omogenea di due o più componenti. Il componente in quantità maggiore viene in genere indicato come solvente, gli altri con il nome di soluto. I componenti
Espressioni di concentrazione di una soluzione
 SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ
 LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
SOLUZIONI. Soluzioni gassose, liquide e solide
 LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LE SOLUZIONI. 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative
 LE SOLUZIONI 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative 7.1 Le soluzioni Si definisce soluzione una miscela omogenea
LE SOLUZIONI 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative 7.1 Le soluzioni Si definisce soluzione una miscela omogenea
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
Le proprietà colligative
 Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Le Soluzioni Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente - La specie chimica presente nella soluzione in quantità più abbondante viene detta SOLVENTE
Le Soluzioni Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente - La specie chimica presente nella soluzione in quantità più abbondante viene detta SOLVENTE
-PROPRIETA COLLIGATIVE-
 -PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
-PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
Equilibri solido-liquido e proprietà colligative. Termodinamica dell Ingegneria Chimica
 Equilibri solido-liquido e proprietà colligative Termodinamica dell Ingegneria Chimica Equilibrio solido-liquido il diagramma (a P=cost mostrato si riferisce a una miscela di due specie miscibili a l l
Equilibri solido-liquido e proprietà colligative Termodinamica dell Ingegneria Chimica Equilibrio solido-liquido il diagramma (a P=cost mostrato si riferisce a una miscela di due specie miscibili a l l
Esercitazioni di Elementi di Chimica. Modulo 3 Trasformazioni della Materia
 Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
SOLUZIONI. Soluzioni gassose, liquide e solide
 LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LA FORMAZIONE DELLE SOLUZIONI.
 LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
CONCENTRAZIONE. Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono.
 1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE
 SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
PROPRIETÀ TIPICHE DEI LIQUIDI
 STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO
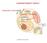 COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO OMEOSTASI Stato di stabilità locale che tende a mantenersi lontano dallo stato di equilibrio EQUILIBRIO Stato di stabilità energetica, massima entropia
COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO OMEOSTASI Stato di stabilità locale che tende a mantenersi lontano dallo stato di equilibrio EQUILIBRIO Stato di stabilità energetica, massima entropia
LA MATERIA E IL MODELLO PARTICELLARE
 LA MATERIA E IL MODELLO PARTICELLARE - Gli oggetti che ci circondano sono costituiti di materia. - Come possiamo definire la materia? La materia è tutto ciò che possiede una massa e occupa un volume. -
LA MATERIA E IL MODELLO PARTICELLARE - Gli oggetti che ci circondano sono costituiti di materia. - Come possiamo definire la materia? La materia è tutto ciò che possiede una massa e occupa un volume. -
Lezione 11 Soluzioni. Diffusione ed osmosi.
 Lezione 11 Soluzioni. Diffusione ed osmosi. Soluzioni Una soluzione è formata da un insieme di molecole di uno o più soluti (eventualmente dissociati in ioni), disciolti in un solvente (nei sistemi biologici
Lezione 11 Soluzioni. Diffusione ed osmosi. Soluzioni Una soluzione è formata da un insieme di molecole di uno o più soluti (eventualmente dissociati in ioni), disciolti in un solvente (nei sistemi biologici
Stato solido. CLASSIFICAZIONE (I) Basata sulla natura delle particelle che costituiscono il solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO
 Stato solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO Stato dotato di forma propria e volume proprio Le particelle (atomi, ioni, molecole) sono fortemente legate tra loro e non si possono allontanare
Stato solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO Stato dotato di forma propria e volume proprio Le particelle (atomi, ioni, molecole) sono fortemente legate tra loro e non si possono allontanare
Cambiamenti di stato. Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti
 Cambiamenti di stato Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti 1 Equilibri tra fasi diverse fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente
Cambiamenti di stato Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti 1 Equilibri tra fasi diverse fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente
GAS. H 2 N 2 O 2 F 2 Cl 2 CO CO 2 NO 2 SO 2 CH 4
 GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
LIQUIDO LIQUIDO LIQUIDO Alcol in acqua. LIQUIDO LIQUIDO SOLIDO Sale in acqua. SOLIDO SOLIDO GAS Idrogeno nell acciaio
 SOLUZIONI Le soluzioni sono miscele omogenee (= stesse proprietà in qualsiasi sua porzione) di due o più sostanze La sostanza presenta in maggior quantità è detta SOLVENTE mentre quelle in quantità inferiore
SOLUZIONI Le soluzioni sono miscele omogenee (= stesse proprietà in qualsiasi sua porzione) di due o più sostanze La sostanza presenta in maggior quantità è detta SOLVENTE mentre quelle in quantità inferiore
Gas. Chimica generale ed Inorganica: Chimica Generale. I palloni ad aria calda
 Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15 Esercizio PAG 340 ES 1 PAG 340 ES 2 PAG 340 ES 3 PAG 340 ES 4 PAG 340 ES 5 PAG 340 ES 6 PAG 340 ES 7 Risposta Il
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15 Esercizio PAG 340 ES 1 PAG 340 ES 2 PAG 340 ES 3 PAG 340 ES 4 PAG 340 ES 5 PAG 340 ES 6 PAG 340 ES 7 Risposta Il
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Stechiometria delle soluzioni
 www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
CONCENTRAZIONE CHIMICA
 CONCENTRAZIONE CHIMICA In una soluzione la specie presente in minore quantità si chiama soluto e quella presente in maggiore quantità solvente. Nelle soluzioni acquose il solvente è l acqua. Concentrazione:
CONCENTRAZIONE CHIMICA In una soluzione la specie presente in minore quantità si chiama soluto e quella presente in maggiore quantità solvente. Nelle soluzioni acquose il solvente è l acqua. Concentrazione:
Cambiamenti di stato Regola delle fasi
 Cambiamenti di stato Regola delle fasi Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti: equilibri tra fasi condensate 1 Equilibri tra fasi diverse fase
Cambiamenti di stato Regola delle fasi Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti: equilibri tra fasi condensate 1 Equilibri tra fasi diverse fase
STRUTTURA DELLA MATERIA. Prof.ssa PATRIZIA GALLUCCI
 STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
-SOLUZIONE- In una soluzione liquida si possono distinguere un solvente (il componente liquido più abbondante) e uno o più soluti.
 -SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
-SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
NELLA LEZIONE DI OGGI:
 ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
Undicesima unità didattica. I liquidi e le soluzioni
 Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
I MISCUGLI OMOGENEI ED ETEROGENEI
 I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
 DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
Cambiamenti di stato
 Cambiamenti di stato Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti 1 Equilibri tra fasi diverse fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente
Cambiamenti di stato Equilibri tra le fasi: diagrammi di stato per un componente puro diagrammi di stato a due componenti 1 Equilibri tra fasi diverse fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente
Test di approfondimento
 Test di approfondimento 1 In 100 ml di una soluzione 2 M sono presenti 6 grammi di soluto. Qual è il peso molecolare del soluto in u.m.a.? A 3 B 12 30 D 120 E 60 2 Attraverso una membrana semipermeabile
Test di approfondimento 1 In 100 ml di una soluzione 2 M sono presenti 6 grammi di soluto. Qual è il peso molecolare del soluto in u.m.a.? A 3 B 12 30 D 120 E 60 2 Attraverso una membrana semipermeabile
Le soluzioni. Lezioni d'autore di Giorgio Benedetti
 Le soluzioni Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) La materia che ci circonda normalmente non è formata da elementi chimici o da composti, ma da miscugli, cioè insiemi di più sostanze
Le soluzioni Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) La materia che ci circonda normalmente non è formata da elementi chimici o da composti, ma da miscugli, cioè insiemi di più sostanze
Miscibilità parziale
 Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
INDICE. Nota dell'autore 9 PARTE PRIMA LE RISORSE MATERIALI ED ENERGETICHE E L'ANALISI DELLE LORO PROPRIETÀ STRUTTURALI E TERMODINAMICHE
 INDICE Nota dell'autore 9 PARTE PRIMA LE RISORSE MATERIALI ED ENERGETICHE E L'ANALISI DELLE LORO PROPRIETÀ STRUTTURALI E TERMODINAMICHE Capitolo I La formazione dell'universo 11 1.1 La storia dell universo
INDICE Nota dell'autore 9 PARTE PRIMA LE RISORSE MATERIALI ED ENERGETICHE E L'ANALISI DELLE LORO PROPRIETÀ STRUTTURALI E TERMODINAMICHE Capitolo I La formazione dell'universo 11 1.1 La storia dell universo
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
L equilibrio si dice omogeneo se la fase dei reagenti è uguale a quella dei prodotti, è eterogeneo in ogni altro caso.
 Chimica Equilibri omogenei ed eterogenei Quando un sistema è in equilibrio dinamico significa che vi sono dei processi ed i loro opposti che evolvono alla stessa velocità. L equilibrio si dice omogeneo
Chimica Equilibri omogenei ed eterogenei Quando un sistema è in equilibrio dinamico significa che vi sono dei processi ed i loro opposti che evolvono alla stessa velocità. L equilibrio si dice omogeneo
LA MATERIA NEI SUOI DIVERSI ASPETTI
 LA MATERIA NEI SUOI DIVERSI ASPETTI Materia è tutto ciò che costituisce i corpi e che, assumendo forme diverse nello spazio, si manifesta ai nostri sensi. La materia è ovunque intorno a noi: il nostro
LA MATERIA NEI SUOI DIVERSI ASPETTI Materia è tutto ciò che costituisce i corpi e che, assumendo forme diverse nello spazio, si manifesta ai nostri sensi. La materia è ovunque intorno a noi: il nostro
Siena, 10 Giugno 2015 Sandra Defazio Serena Fedi
 CLASSE I A Costruzione Ambiente e Territorio omogenei ed eterogenei e curva di riscaldamento di un miscuglio. nobili. Distinzione fra molecole e atomi. Principio di conservazione della massa. Teoria atomica
CLASSE I A Costruzione Ambiente e Territorio omogenei ed eterogenei e curva di riscaldamento di un miscuglio. nobili. Distinzione fra molecole e atomi. Principio di conservazione della massa. Teoria atomica
Richiami di Fisica, Meccanica e Termodinamica Introduzione al Corso Prof. Ing. Giulio Vannucci
 CORSO DI FISICA TECNICA Richiami di Fisica, Meccanica e Termodinamica Introduzione al Corso Prof. Ing. Giulio Vannucci RICHIAMI DI FISICA, MECCANICA E TERMODINAMICA Nozioni di unità di misura Elementi
CORSO DI FISICA TECNICA Richiami di Fisica, Meccanica e Termodinamica Introduzione al Corso Prof. Ing. Giulio Vannucci RICHIAMI DI FISICA, MECCANICA E TERMODINAMICA Nozioni di unità di misura Elementi
Le proprietà colligative delle soluzioni
 Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
REGISTRO DELLE LEZIONI 2004/2005. Tipologia. Addì Tipologia. Addì Tipologia
 Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
PROGRAMMA DEL CORSO DI CHIMICA FISICA 1 CON LABORATORIO a.a
 PROGRAMMA DEL CORSO DI CHIMICA FISICA 1 CON LABORATORIO a.a. 2012-2013 NOTA durante lo svolgimento del corso, sulla base di criteri di opportunita, potrei apportare qualche modifica al programma, che sara
PROGRAMMA DEL CORSO DI CHIMICA FISICA 1 CON LABORATORIO a.a. 2012-2013 NOTA durante lo svolgimento del corso, sulla base di criteri di opportunita, potrei apportare qualche modifica al programma, che sara
POTENZA METABOLICA. Fisica Applicata, Area Infermieristica, M. Ruspa
 POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
