Leggi ricavate da osservazioni sperimentali : mantenendo costante due dei 4 parametri, come variano gli altri due?
|
|
|
- Umberto Sartori
- 5 anni fa
- Visualizzazioni
Transcript
1 Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione (P) Temperatura (T) la quantità (espressa come numero di moli n) Leggi ricavate da osservazioni sperimentali : mantenendo costante due dei 4 parametri, come variano gli altri due? (Quantità costante, n const.) Trasformazione isoterma: T costante, grandezze che variano P & V Il V di una determinata massa di gas è inversamente proporzionale alla P; es. la P diminuisce con l aumentare del V. Il prodotto tra volume e pressione in due stati diversi del gas rimane constante (Legge di Boyle) P1 x V1 = P2 x V2 Trasformazione isòbara : P costante, grandezze che variano V & T Il V di una determinata massa di gas è direttamente proporzionale alla T; es. il V aumente con l aumentare della T. Il rapporto tra V e T in due stati diversi del gas rimane constante (Legge di Charles) V1 T1 = V2 T2 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 1
2 Le leggi dei gas Trasformazione isocòra : V constante, grandezze che variano P & T La P di una determinata massa di gas è direttamente proporzionale alla T. La P aumenta con l aumentare della T. Il rapporto tra P e T in due stati diversi del gas rimane constante(legge di Gay-Lussac) P1 T1 = P2 T2 Boyle P x V = const. P1 x V1 = P2 x V2 Charles Gay Lussac V T = const. P T = const. V1 T1 = V2 T2 P1 T1 = P2 T2 (P const., T const.) Interpretazione della legge di Avogadro: a una temperatura fissa e a una pressione fissa, il volume occupato da un gas è direttamente proporzionale alla quantità di gas (es. numero di moli n). 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 2
3 Equazione di stato dei gas ideali Nel modello del gas ideale, le particelle: 1. sono puntiformi e il loro volume è trascurabile; 2. non si respingono o attraggono reciprocamente; 3. viaggiano in tutte le direzioni con un movimento disordinato dovuto al fatto che il loro moto rettilineo è interrotto dagli urti (detti elastici) con le altre particelle e con le pareti del contenitore. L equazione di stato dei gas ideali è una combinazione delle leggi di Boyle, Gay-Lussac, Charles & Avogadro: P = pressione V = volume T = temperatura assoluta (in K) n = numero di moli R = costante universale dei gas = 0,08206 l atm P V = n R T (per V in litri & P in atm) 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 3
4 Equazione di stato dei gas ideali P V = n R T Attenzione alle unità di misura: Pressione: 1 atm = 760 mm Hg = 760 Torr = Pa Volume: 1 l = 1 dm 3 = 1000 cm 3 1 ml = 1 cm 3 = costante universale dei gas il cui valore dipende dalle unità in cui sono espresse P e V P in atm e V in litri: R = P in Pascal e V in m 3 : R = l atm J Temperatura assoluta: espressa in K = C n = numero di moli 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 4
5 Esercizi Equazione di stato dei gas ideali Una bombola di 80.0 dm 3 contiene 5.60 kg di metano (CH 4 ). La pressione massima che la bombola può sopportare è di 148 atm (limite di sicurezza). Calcolare la temperatura massima che può raggiungere la bombola in condizioni di sicurezza. P = 148 atm V = 80.0 dm 3 = 80.0 l n = massa / MM = 5.60 x 10 3 g / gmol -1 = 3.49 x 10 2 mol R = l atm P V = n R T T = PV / nr = 413 K 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 5
6 Esercizi Equazione di stato dei gas ideali Calcolare la pressione a cui si deve sottoporre una data quantità di gas che occupa un volume di 2.60 x 10 2 l alla Temperatura di 85.6 C ed alla pressione di 4.20 x 10 4 Pa, affinché occupi un volume di 105 l alla temperatura di 341 C. Dati: V 1 = 2.60 x 10 2 L T 1 = 85.6 C = K P 1 = 4.20 x 10 4 Pa V 2 = 105 L T 2 = 341 C = 614 K n 1 = n 2 P 1 V 1 RT 1 = P 2V 2 RT 2 => P 1V 1 T 1 = P 2V 2 T 2 => P 2 = V 1P 1 T 2 V 2 T 1 = 2.60 x 102 l x 4.20 x 10 4 Pa x 614 K 105 l x K = 1.78 x 10 5 Pa 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 6
7 Esercizi Equazione di stato dei gas ideali Un composto contenente C e H ha una densità pari a 1.80 g/l alla pressione di 1.00 atm e alla temperatura di 25.0 C. Determinare la massa molare. n V = P RT = 1.00 atm L atm = mol/l K n (mol) = massa MM n (mol) = mol/l x V = massa MM mol/l = massa V x MM = densità MM MM = 1.80 g/l = 44.0 g/mol mol/l = 1.80 g/l MM n V = P RT m MM x V = P RT mrt MM = VP = drt P 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 7
8 Esercizi Equazione di stato dei gas ideali Un idrocarburo gassoso, C x H y, contiene l 82.66% di carbonio. Un campione di g dell idrocarburo esercita una pressione di 373 mmhg in un recipiente di vetro del volume 185 ml a 23.0 C. Calcolare la formula minima e la formula molecolare dell idrocarburo. 1. Convertire le unità di misura V = l P = 373 mmhg/ 760 mmhg atm -1 = atm T = 23.0 C = K 2. Calcolare la massa molare utilizzando l equazione di stato dei gas ideali (slide n.8) n V = P RT m MM x V = P RT MM = mrt / PV = (0.218 g x l atm x K) / (0.491 atm x l) = 58.3 g/mol 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 8
9 Esercizi Equazione di stato dei gas ideali 3. Calcolare la formula minima 100 g di composto g di C & g di H Moli C = g / gmol -1 = mol Moli H = g / gmol -1 = mol Dividiamo per il numero più piccolo : C 6.882/6.882 = 1 H 17.20/6.882 = 2.5 x2 Formula minima : C 2 H 5 4. Calcolare la formula molecolare Massa molare C 2 H 5 = 2* * = g/mol Coeff. = 58.3 gmol -1 / gmol -1 = 2 formula minima C 2 H 5 ; formula molecolare C 4 H 10 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 9
10 Esercizi Equazione di stato dei gas ideali 2.54 g di Al reagiscono in acqua con 3.02 g di NaOH svolgendo H 2 secondo la reazione: 2NaOH + 2Al + 6H 2 O 2NaAl(OH) 4 + 3H 2 Alla temperatura di 28 C e alla pressione di atm vengono svolti 2.85 l di idrogeno. Calcolare la resa di reazione. 1.Determinazione del reagente limitante Moli Al = 2.54 g / g/mol = mol Moli NaOH = 3.02 g / g/mol = mol Rapporto Al : NaOH 2 : 2 (1:1) NaOH reagente limitante 2. Calcolo delle moli di H 2 teoricamente ottenibili Rapporto molare NaOH : H 2 2 : 3 moli H 2 = x 3/2 = mol 3. Calcolo delle moli ottenute H 2...alla temperatura di 28 C e alla pressione di atm vengono svolti 2.85 l di idrogeno PV = nrt n = PV/RT = atm x 2.85 l / x 301 K = mol 4. Calcolo della resa percentuale η = moli ottenute moli teoricamente ottenibili moli x 100 = x100 = 91.2 % moli 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 10
11 Esercizi Equazione di stato dei gas ideali Un eccesso di HCl reagisce con g di Zn. Calcolare la pressione di H 2 raccolto in un recipiente di volume pari a 50.0 ml a 25.0 C, sapendo che la resa della reazione è del 75.0 %. Zn + 2HCl ZnCl 2 + H 2 1. Calcolo delle moli di H 2 teoricamente ottenibili Moli Zn = g/ MM = g / g/mol = 3.76 x 10-3 mol Moli H 2 = Moli Zn = 3.76 x 10-3 mol 2. Calcolo delle moli di H 2 ottenute Moli ottenute = resa % x moli teoricamente ottenibili = x 3.76 x 10-3 mol = 2.82 x 10-3 mol 3. Calcolo della pressione esercitata (attenzione alle unità di misura) V = 50.0 ml = 5 x 10-2 l T = 25 C = 298 K P = nrt/ V = 1.38 atm n = 2.82 x 10-3 mol 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 11
12 Esercizi Equazione di stato dei gas ideali 5.00 g di un campione impuro di idruro di calcio (CaH 2 ) reagiscono con un eccesso di acqua per produrre una quantità di H 2 che occupa un volume di 3.90 l alla pressione di 750 Torr e alla temperatura di 32 C. Calcolare la percentuale in massa del CaH 2 nel campione. CaH 2 + 2H 2 O Ca(OH) 2 + 2H 2 Moli H 2 prodotte = n = PV RT = 750 Torr 760 Torr atm L atm x 3.90 L x 305 K = mol Rapporto molare CaH 2 : H 2 1 mol : 2 mol Massa CaH 2 x : mol x = mol di CaH 2 (g) = mol x g/mol = 3.24 g % CaH 2 = 3.24 g/ 5 g x 100 = 64.8 % 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 12
13 Pressione parziale e legge di Dalton Data una miscela di tre gas A, B e C che non reagiscono tra di loro posti in un recipente chiuso con volume uguale a V, la pressione parziale è la pressione che eserciterebbe ogni componente della miscela se occupasse da solo l intero V alla stessa temperatura. La pressione totale esercitata da una miscela di gas è uguale alla somma delle pressioni parziali dei singoli componenti della miscela (legge di Dalton). Ptotale = p1 + p2 + p3 + A p = 2.5 atm B p = 1.5 atm A + B p tot = 4 atm 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 13
14 Esercizi miscele di gas Sia data la figura in cui il cilindro A di 400 cm 3 contiene moli i argon, e il cilindro B di 550 cm 3, contiene azoto ad una pressione di 450 torr a 23.0 C e il rubinetto R è inizialmente chiuso. Calcolare le pressioni parziali dei due gas quando il rubinetto R viene aperto (i gas si mescolano) e tutto il sistema viene portato a temperatura di C. 1. Calcolo delle moli di N 2 n = PV RT = atm x L L atm x K = mol Argon 400cm mol R Azoto P= 450 torr V= 550 cm 3 T = 23.0 C 2. Calcolo delle pressioni parziali dei due gas dopo l apertura del rubinetto & riscaldamento T = C = K V tot = L L= L n N2 = mol n Ar = mol n tot = mol P tot = nrt V L atm mol x x K = L = 2.37 atm Frazione molare (Х) i-esimo = moli gas i-esimo / moli miscela Pressione parziale = X x P tot P Ar = mol x 2.37 atm = 1.94 atm P mol mol N 2 = mol x 2.37 atm= atm 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 14
15 Esercizi miscele di gas In un reattore chiuso, del volume di 20.0 dm 3, vengono fatti reagire 80.0 g di biossido di stagno con 8.00 g di idrogeno, a C, che formano stagno e vapore acqueo. Calcolare le pressioni parziali dei componenti del miscuglio gassoso alla fine della reazione. SnO 2 + 2H 2 Sn + 2H 2 O V = 20.0 dm 3 = 20.0 L T = C = K 1. Determinazione del reagente limitante SnO 2 + 2H 2 Sn + 2H 2 O 80.0 g 8.0 g Moli SnO 2 = 80.0 g / gmol -1 = mol Moli H 2 = 8.00 g / gmol -1 = 3.97 mol Moli H 2 necessati per reagire con mol SnO 2 : x 2/1 = 1.06 mol Reagente limitante : SnO 2 alla fine della reazione : H 2 in eccesso + prodotti 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 15
16 Esercizi miscele di gas 2. Calcolo delle pressioni parziali alla fine della reazione Moli H 2 che non hanno reagito = 3.97 mol 1.06 mol = 2.91 mol Moli H 2 O formate SnO 2 : H 2 O 1 : 2 moli H 2 O = mol x 2/1 = 1.06 mol Moli totali = 2.91 mol mol = 3.97 mol Frazione molare (Х) i-esimo = moli gas i-esimo / moli miscela Pressione parziale = X x P tot P tot = nrt V L atm 3.97 mol x x K = 20.0 L = 6.90 atm H 2 X = 2.91 mol / 3.97 mol = P = x 6.90 atm = 5.06 atm H 2 O X = 1.06 mol / 3.97 mol = P = x 6.90 atm = 1.84 atm 17/11/2017 Esercitazioni di Chimica Generale ed Inorganica 16
= cost a p costante V 1 /T 1 =V 2 /T 2 LEGGE DI GAY-LUSSAC: Un sistema allo stato gassoso è definito da 4. mmhg (torr), bar.
 GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Sistemi Gassosi. GAS = specie che occupa tutto lo spazio disponibile. VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 )
 Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
I Gas e Loro Proprietà (II)
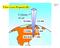 I Gas e Loro Proprietà (II) 2017 10 miles 0.2 atm 4 miles 0.5 atm Sea level 1 atm Dario Bressanini Gas e reazioni chimiche Determinare il volume di CO 2 prodotto a 37 0 C e 1.0 atm quando 5.6 g di glucosio
I Gas e Loro Proprietà (II) 2017 10 miles 0.2 atm 4 miles 0.5 atm Sea level 1 atm Dario Bressanini Gas e reazioni chimiche Determinare il volume di CO 2 prodotto a 37 0 C e 1.0 atm quando 5.6 g di glucosio
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Il Gas Ideale. Il gas ideale é un'astrazione
 Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
UNIVERSITÀ DEGLI STUDI DI TORINO
 UNIVERSITÀ DEGLI STUDI DI TORINO Laurea Triennale in Scienze Biologiche TUTORAGGIO DEL CORSO DI CHIMICA GENERALE ED INORGANICA (CORSO A) AA 2017-2018 GIUSEPPE RICCIO giuseppe.riccio@edu.unito.it REAGENTI
UNIVERSITÀ DEGLI STUDI DI TORINO Laurea Triennale in Scienze Biologiche TUTORAGGIO DEL CORSO DI CHIMICA GENERALE ED INORGANICA (CORSO A) AA 2017-2018 GIUSEPPE RICCIO giuseppe.riccio@edu.unito.it REAGENTI
Legge di stato dei gas ideali
 Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
I gas e loro proprietà Cap , 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96
 2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
Calcolo del numero di moli dei reagenti: P.M. HCl= 36 uma. 36 g/mol. n HCl = 1,9 g = 0,0528 moli
 ESERCIZI DI STECHIOMETRIA IN CUI COMPAIONO SPECIE ALLO STATO GASSOSO Es. ESERCIZIO 1 Nella reazione tra alluminio ed acido cloridrico si sviluppa idrogeno gassoso. Determinare il volume di H 2, misurato
ESERCIZI DI STECHIOMETRIA IN CUI COMPAIONO SPECIE ALLO STATO GASSOSO Es. ESERCIZIO 1 Nella reazione tra alluminio ed acido cloridrico si sviluppa idrogeno gassoso. Determinare il volume di H 2, misurato
H 2 SO 4 : mol : 3 = mol REAGENTE LIMITANTE Ca 3 (PO 4 ) 2 : mol : 1 = mol
 1) Partendo da 100.0 g di H 2 SO 4 e 300.0 g di Ca 3 (PO 4 ) 2, calcolare quanti grammi di prodotti si formano e quanti grammi di reagente in eccesso rimangono non reagiti. 3H 2 SO 4 + Ca 3 (PO 4 ) 2 3CaSO
1) Partendo da 100.0 g di H 2 SO 4 e 300.0 g di Ca 3 (PO 4 ) 2, calcolare quanti grammi di prodotti si formano e quanti grammi di reagente in eccesso rimangono non reagiti. 3H 2 SO 4 + Ca 3 (PO 4 ) 2 3CaSO
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
Esame (0) classei - Codice Prova:
 1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
-GAS IDEALI- Le particelle che costituiscono un gas ideale:
 -GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
-GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
GAS IDEALI (o gas perfetti )
 GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1
 I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
Lo stato gassoso. L atmosfera terrestre è il sistema gassoso in cui siamo immersi
 Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
LEGGI DEI GAS. Gas sono sostanze sprovviste di forma e volume proprio
 LEGGI DEI GAS Gas sono sostanze sprovviste di forma e volume proprio Una grandezza molto significativa per descrivere un gas è la pressione, conseguenza delle collisioni del gas sulla superficie del contenitore.
LEGGI DEI GAS Gas sono sostanze sprovviste di forma e volume proprio Una grandezza molto significativa per descrivere un gas è la pressione, conseguenza delle collisioni del gas sulla superficie del contenitore.
Stati di aggregazione della materia. dal microscopico al macroscopico: struttura. interazioni GASSOSO. proprietà SOLIDO LIQUIDO
 Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
I gas. ChimicaGenerale_lezione10
 I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
ATOMI E MOLECOLE. ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche.
 1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
LA MATERIA ED I SUOI STATI
 LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
Leggi dei gas Equazione di stato dei gas perfetti
 Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Queste proprietà derivano dalla grande distanza che separa le molecole che compongono un gas.
 Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Chimica A.A. 2017/2018
 Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 6 Un gas contenuto in una bombola da 5,0 dm 3 esercita una pressione di 2,6 am. Il gas viene quindi compresso in condizioni isoterme fino ad
Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 6 Un gas contenuto in una bombola da 5,0 dm 3 esercita una pressione di 2,6 am. Il gas viene quindi compresso in condizioni isoterme fino ad
I GAS GAS IDEALI. PV=nRT. Pressione Volume numero di moli Temperatura Costante dei gas. P V n T R. n, T= cost Legge di Boyle
 I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
Diagramma di stato di H 2 O
 Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
Stati di aggregazione della materia
 Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
CorsI di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica. FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti. Esercitazione del 26/10/2010
 CorsI di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti Esercitazione del 6/0/00 ARGOMENTI TRATTATI DURANTE LA LEZIONE Equazione di stato dei
CorsI di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti Esercitazione del 6/0/00 ARGOMENTI TRATTATI DURANTE LA LEZIONE Equazione di stato dei
Esercizi sui Gas. Insegnamento di Chimica Generale CCS CHI e MAT
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 Un
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 Un
STATO GASSOSO. parte I a. - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio
 STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C.
 http://www. I GAS : ESERCIZI 1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C. da quanto espresso si evince che il numero di moli è costante
http://www. I GAS : ESERCIZI 1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C. da quanto espresso si evince che il numero di moli è costante
Termodinamica Chimica
 Universita degli Studi dell Insubria Termodinamica Chimica I Gas Ideali dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini Proprietà di un Gas Può essere compresso facilmente Esercita
Universita degli Studi dell Insubria Termodinamica Chimica I Gas Ideali dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini Proprietà di un Gas Può essere compresso facilmente Esercita
Correzione Parziale del 24/01/2014
 Correzione Parziale del 24/01/2014 Compito A Esercizio 1 L analisi elementare di una sostanza ha dato il seguente risultato: C 52,2%, H 13%, O 34,8%. 3,83 g di questa sostanza vengono introdotti in un
Correzione Parziale del 24/01/2014 Compito A Esercizio 1 L analisi elementare di una sostanza ha dato il seguente risultato: C 52,2%, H 13%, O 34,8%. 3,83 g di questa sostanza vengono introdotti in un
Esercizi sui Gas. Insegnamento di Chimica Generale CCS CHI e MAT. A.A. 2015/2016 (I Semestre)
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio 1 Un campione
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio 1 Un campione
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Massa degli atomi e delle molecole
 Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Esercizi bilanciamento redox
 Esercizi bilanciamento redox Bilanciare la reazione e calcolare la massima quantità (in grammi) di zinco nitrato che si ottiene facendo reagire 2.10 10 3 g di acido nitrico puro al 85.0 % p/p con un eccesso
Esercizi bilanciamento redox Bilanciare la reazione e calcolare la massima quantità (in grammi) di zinco nitrato che si ottiene facendo reagire 2.10 10 3 g di acido nitrico puro al 85.0 % p/p con un eccesso
Se la densità assoluta di un gas a 30 C e a 768 mm di Hg è pari a g/l, trovare la sua densità assoluta nelle condizioni normali.
 Una certa quantità di idrogeno viene posta in una camera di platino a volume costante. Quando la camera viene immersa in un bagno di ghiaccio che sta fondendo, la pressione assoluta del gas è di 1000 mm
Una certa quantità di idrogeno viene posta in una camera di platino a volume costante. Quando la camera viene immersa in un bagno di ghiaccio che sta fondendo, la pressione assoluta del gas è di 1000 mm
In base ai coefficienti stechiometrici posso calcolare quanti grammi di sostanza reagiscono.
 ESERCITAZIONE 6 RAPPORTI PONDERALI E VOLUMETRICI NELLE REAZIONI In base ai coefficienti stechiometrici posso calcolare quanti grammi di sostanza reagiscono. 1) Quanto acido solforico reagisce con 100g
ESERCITAZIONE 6 RAPPORTI PONDERALI E VOLUMETRICI NELLE REAZIONI In base ai coefficienti stechiometrici posso calcolare quanti grammi di sostanza reagiscono. 1) Quanto acido solforico reagisce con 100g
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
Gas. Chimica generale ed Inorganica: Chimica Generale. I palloni ad aria calda
 Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Stati di aggregazione della materia. GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti
 9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
UNITA DI MISURA. Le unità di misura sono molto importanti
 Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Gas Ideale: Legge di Charles. V t =V 0 (1+αT)
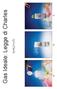 Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
LE LEGGI DEI GAS. Prof. Michele Barcellona
 LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
L equilibrio dei gas
 L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
. Proprietà degli stati della materia Aeriforme Liquido Solido
 . Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
. Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
LEGGI PONDERALI DELLA CHIMICA
 LEGGI PONDERALI DELLA CHIMICA LEGGE DI LAVOISIER (1743-1794) In ogni reazione la massa totale dei reagenti è uguale alla massa totale dei prodotti. Massa Totale R = Massa Totale P Esempio rame + zolfo
LEGGI PONDERALI DELLA CHIMICA LEGGE DI LAVOISIER (1743-1794) In ogni reazione la massa totale dei reagenti è uguale alla massa totale dei prodotti. Massa Totale R = Massa Totale P Esempio rame + zolfo
Quando si è raggiunto lo stato di equilibrio della reazione: Data una qualunque reazione in fase gassosa: reagenti e dei prodotti di reazione:
 EQUILIBRIO CHIMICO IN FASE GASSOSA Data una qualunque reazione in fase : aa + bb = cc + dd si trova sperimentalmente che quando essa ha raggiunto il suo stato di equilibrio esiste la seguente relazione
EQUILIBRIO CHIMICO IN FASE GASSOSA Data una qualunque reazione in fase : aa + bb = cc + dd si trova sperimentalmente che quando essa ha raggiunto il suo stato di equilibrio esiste la seguente relazione
Corso: Chimica Fisica
 Docente: Gianni ROMEO Corso: Chimica Fisica pagina 1 di 6 TEST N. 3 (IL CORRETTORE DEL TEST È A PAGINA 2 ) DATA: 07.01.2010 Argomenti (Moduli 1 e 2): Materia ed Energia; le Unità di Misura e l Analisi
Docente: Gianni ROMEO Corso: Chimica Fisica pagina 1 di 6 TEST N. 3 (IL CORRETTORE DEL TEST È A PAGINA 2 ) DATA: 07.01.2010 Argomenti (Moduli 1 e 2): Materia ed Energia; le Unità di Misura e l Analisi
Chimica generale. Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3
 Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Stati d aggregazione della materia
 Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
FISICA. Termodinamica GAS PERFETTI. Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica
 FISICA Termodinamica GAS PERFETTI Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica SISTEMI, STATI E VARIABILI TERMODINAMICHE Tutto ciò che circonda un sistema, che può influenzare e modificare
FISICA Termodinamica GAS PERFETTI Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica SISTEMI, STATI E VARIABILI TERMODINAMICHE Tutto ciò che circonda un sistema, che può influenzare e modificare
ESERCIZIO 1 Per combustione completa in eccesso di ossigeno di un composto costituito da calcio, carbonio e azoto, si formano CaO, CO 2 e NO 2 in
 ESERCIZIO 1 Per combustione completa in eccesso di ossigeno di un composto costituito da calcio, carbonio e azoto, si formano CaO, CO 2 e NO 2 in quantità rispettivamente pari a 3,500, 2,747 e 5,743 g.
ESERCIZIO 1 Per combustione completa in eccesso di ossigeno di un composto costituito da calcio, carbonio e azoto, si formano CaO, CO 2 e NO 2 in quantità rispettivamente pari a 3,500, 2,747 e 5,743 g.
PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI)
 1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
- Equilibri omogenei: tutte le sostanze che partecipano alla reazione fanno parte della stessa fase:
 ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
LA TEORIA CINETICA DEI GAS.
 LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
Temperatura. Il legame con le grandezze microscopiche è di tipo statistico. Pressione Volume Temperatura
 Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Composti chimici. Formula minima: CH 3 molecolare: C 2 H 6 di struttura: H H H C C H H H
 Stechiometria Composti chimici Formula minima: CH 3 molecolare: C H 6 di struttura: H H H C C H H H Formula di struttura Formula minima molecolare: C H 6 O Formula di struttura H O H H H H Reazioni
Stechiometria Composti chimici Formula minima: CH 3 molecolare: C H 6 di struttura: H H H C C H H H Formula di struttura Formula minima molecolare: C H 6 O Formula di struttura H O H H H H Reazioni
Lezione 5. Equazioni Chimiche e Stechiometria
 2018 Lezione 5. Equazioni Chimiche e Stechiometria n. moli = g sostanza M (g/mol) g sostanza = n. moli x M (g/mol) 1 Stechiometria Affronta gli aspeb quanctacvi delle reazioni chimiche, si basa sul principio
2018 Lezione 5. Equazioni Chimiche e Stechiometria n. moli = g sostanza M (g/mol) g sostanza = n. moli x M (g/mol) 1 Stechiometria Affronta gli aspeb quanctacvi delle reazioni chimiche, si basa sul principio
Esercizi Concentrazioni e diluizioni
 Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Teoria Cinetica Molecolare dei Gas Ideali
 Teoria Cinetica Molecolare dei Gas Ideali Un gas è composto da molecole molto lontane tra di loro in confronto alle loro dimensioni e possono essere considerate puntiformi, quindi prive di volume. Le molecole
Teoria Cinetica Molecolare dei Gas Ideali Un gas è composto da molecole molto lontane tra di loro in confronto alle loro dimensioni e possono essere considerate puntiformi, quindi prive di volume. Le molecole
Capitolo 5 La quantità chimica: la mole
 Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
CORSO DI CHIMICA. Esercitazione del 7 Giugno 2016
 CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
Miscela di gas 1, 2 e 3. P 1 = n1 R T P 2 = n2 R T P 3 = n3 R T V V V. Pressioni parziali dei gas P 1 P 2 P 3
 Miscele di gas Pressione parziale di un gas in una miscela gassosa: pressione esercitata da un componente della miscela se occupasse da solo l intero volume a disposizione della miscela.(legge di DALTON)
Miscele di gas Pressione parziale di un gas in una miscela gassosa: pressione esercitata da un componente della miscela se occupasse da solo l intero volume a disposizione della miscela.(legge di DALTON)
Gas. Vapore. Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente. microscopico MACROSCOPICO
 Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Generica equazione chimica:
 REAZIONI CHIMICHE Trasformazione di una o più sostanze (reagenti) in una o più sostanze (prodotti) EQUAZIONE CHIMICA Una equazione chimica è la rappresentazione simbolica di una reazione chimica in termini
REAZIONI CHIMICHE Trasformazione di una o più sostanze (reagenti) in una o più sostanze (prodotti) EQUAZIONE CHIMICA Una equazione chimica è la rappresentazione simbolica di una reazione chimica in termini
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
CdL Professioni Sanitarie A.A. 2012/2013. Unità 9: Gas e processi di diffusione
 L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
Scritto chimica generale
 Scritto chimica generale 23.01.2012 TESTO A 1. L idrogeno solfuro di ammonio solido si decompone ad ammoniaca gassosa e acido solfidrico gassoso a 25 C. Sapendo che a 25 C la costante per questo equilibrio
Scritto chimica generale 23.01.2012 TESTO A 1. L idrogeno solfuro di ammonio solido si decompone ad ammoniaca gassosa e acido solfidrico gassoso a 25 C. Sapendo che a 25 C la costante per questo equilibrio
Reazioni lente e reazioni veloci
 CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
COMPITO B DI CHIMICA DEL
 COMPITO B DI CHIMICA DEL 220713 1B) Un campione di aria (mm = 29.0 g/mol) del volume di 6.12 L, misurati a c.s., è inquinato da ossido di azoto. Il campione viene fatto passare attraverso 340 ml di una
COMPITO B DI CHIMICA DEL 220713 1B) Un campione di aria (mm = 29.0 g/mol) del volume di 6.12 L, misurati a c.s., è inquinato da ossido di azoto. Il campione viene fatto passare attraverso 340 ml di una
Stati di aggregazione della materia
 SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Le soluzioni La diluizione è il procedimento per preparare una soluzione meno concentrata da una soluzione più concentrata. Diluizione Aggiungi Solvente
La Vita è una Reazione Chimica Acqua Oro Zucchero Le soluzioni La diluizione è il procedimento per preparare una soluzione meno concentrata da una soluzione più concentrata. Diluizione Aggiungi Solvente
Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire.
 Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire. Molte reazioni procedono in modo incompleto; è importante quindi determinare
Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire. Molte reazioni procedono in modo incompleto; è importante quindi determinare
VIII ESERCITAZIONE. Soluzione
 VIII ESERCITAZIONE 1. Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 d di acqua a 80 C. Quale sarà, all equilibrio,
VIII ESERCITAZIONE 1. Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 d di acqua a 80 C. Quale sarà, all equilibrio,
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Esame di Chimica Generale 19 Febbraio 2013
 Esame di Chimica Generale 19 Febbraio 2013 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 19 Febbraio 2013 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Fondamenti di Chimica T-A T A (A-K) Calcolo n moli e rendimento reazione
 Università degli Studi di Bologna Anno Accademico 009/010 Facoltà di Ingegneria Corso di Laurea in Ingegneria Gestionale Fondamenti di Chimica T-A T A (A-K) Calcolo n moli e rendimento reazione Dott. Enzo
Università degli Studi di Bologna Anno Accademico 009/010 Facoltà di Ingegneria Corso di Laurea in Ingegneria Gestionale Fondamenti di Chimica T-A T A (A-K) Calcolo n moli e rendimento reazione Dott. Enzo
GAS IDEALI E REALI. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche:
 GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
