Lezioni LINCEI per la Scuola Storia Fisica Atomica - Introduzione
|
|
|
- Giovanni Valle
- 5 anni fa
- Visualizzazioni
Transcript
1 Lezioni LINCEI per la Scuola Storia Fisica Atomica - Introduzione Roberto Casalbuoni Dipartimento di Fisica e Astronomia, Sezione INFN, Istituto G. Galilei per la Fisica Teorica (GGI), Terza Cultura Firenze - casalbuoni@fi.infn.it 1
2 Sommario 1 - Idee sull atomo Ricerche sui gas e teoria cinetica La scoperta dell atomo di elettricita : l elettrone 2
3 2 - Spettroscopia Lo studio dell atomo Modelli atomici. L atomo di Rutherford Le difficolta dei modelli atomici 3 Planck e il corpo nero Einstein e i fotoni L atomo di Bohr e Sommerfeld Lo spin dell elettrone 3
4 La ricerca della causa naturale delle cose AC Talete, Anassimene, Anassimandro, Eraclito, Empedocle e Aristotele formularono l ipotesi che i quattro elementi aria, acqua, terra e fuoco fossero l origine di tuttele cose tramite processi di rarefazione e condensazione Ma gia nel 400 AC Democrito formulava l ipotesi atomica 4
5 Evoluzione storica dell atomismo Particelle semplici indivisibili (Greci) Ατομος = indivisibile Posizione filosofica: Cosa succede continuando a dividere la materia? Atomismo fisico (Dalton fine 1700) Posizione empirica tesa all uso di una particolare concezione della materia in quanto utile per spiegare i fenomeni osservati 5
6 Come e spiegato il cambiamento dall atomismo? Democrito (~ 460 AC- ~370 AC): Tutti gli atomi sono uguali eccetto per forma, grandezza e moto I cambiamenti sono dovuti a riposizionamenti relativi degli atomi. Tra gli atomi il vuoto!! 6
7 Empedocle (~350 AC), Epicuro ( AC), Lucrezio (98-55 AC) Atomismo di Democrito Sopravvento di Platone ( AC) e di Aristotele ( AC) che aborrivano l idea del vuoto sino al XVII secolo Filosofia Cartesiana ( ): corpuscolare sebbene contraria al vuoto 7
8 Democrito (~ 460 ~ 370 AC) Cartesio ( ) 8
9 Contributi alle idee corpuscolari Ricerche sui gas Dinamica di Newton ( ) (forze a distanza) Nel XVII secolo inizia lo sviluppo della chimica Boyle ( ): elementi come costituenti di tutte le sostanze Dalton ( ): gli atomi di uno stesso elemento sono identici, diversi quelli di differenti elementi (specie in peso) 9
10 Newton ( ) Boyle ( ) Dalton ( ) 10
11 Le ricerche sui gas Gli studi sui gas mostrarono che in condizioni di rarefazione tutti i gas obbediscono alle stesse leggi. Questo appariva molto chiaro se si assumeva che un gas, in prima approssimazione, fosse costituito da un insieme di molecole in moto continuo e con nessuna interazione tra loro eccetto quella derivante dagli urti 11
12 v Le molecole incidendo sulle pareti del recipiente danno luogo ad una forza contro la parete che genera una pressione (forza per unita di superficie). Piu frequenti sono gli urti (cioe maggiore e la velocita delle molecole) e piu grande e la pressione. v Diminuendo il volume la frequenza degli urti aumenta e quindi la pressione diventa maggiore v Aumentando la temperatura (espressa in gradi Kelvin T = t ) la velocita delle molecole aumenta e quindi aumenta la pressione 12
13 L ipotesi dei moti molecolari puo essere verificata nel moto Browniano. Il botanico Brown nel 1827 osservo il movimento delle particelle di polline di grano al microscopio (v. pulviscolo nell aria). Le particelle effettuano un moto irregolare che si puo attribuire come dovuto all urto con le molecole del mezzo. 13
14 Brown ( ) 14
15 Dal fatto che tutti i gas si comportano in ugual modo segue facilmente l ipotesi fondamentale di Avogadro (1811): Volumi uguali di gas alla stessa temperatura e pressione contengono lo stesso numero di molecole Pesando volumi uguali di gas diversi si puo risalire ai rapporti dei pesi molecolari P volume gas = Np molecola gas 15
16 Avogadro ( ) 16
17 Definendo i pesi molecolari relativamente all idrogeno atomico si ha che i pesi molecolari relativi dell idrogeno e dell ossigeno molecolare (H 2 e O 2 ) sono 2 e 32 Se si definisce grammomolecola la quantita in grammi pari al peso molecolare relativo, segue che in una grammomolecola di qualunque gas c e lo stesso numero di molecole. Questo numero e stato determinato in vari esperimenti ed e detto il numero di Avogadro, N A : N A = Il peso di una molecola di idrogeno e dunque 2gr = gr Il peso di una molecola di ossigeno e 16 volte piu grande, ecc. 17
18 Le osservazioni che portarono alla formulazione dell ipotesi di Avogadro erano basate su studi chimici effettuati all inizio del 1800: Lavoisier (1775): Se un elemento A si combina con B per formare il composto C: p C = p A + p B, conservazione della massa Proust (1800): I pesi relativi degli elementi che si combinano sono costanti 1(2)gr H (70.4)gr Cl = 36.2(72.4)gr HCl Dalton( ): Se A e B si combinano per dare C e A si combina con una quantita diversa di B per dare D, allora il rapporto tra le due quantita di B deve essere un numero razionale 16gr O + 14gr N = 30g NO(ossido nitrico) 16gr O + 28gr N = 44g N 2 O (ossido nitroso) 32gr O + 14gr N = 46g NO 2 (biossido di azoto) 18
19 La legge precedente (legge delle proporzioni multiple) fu spiegata da Dalton: Ad ogni elemento si associa un numero, numero atomico, che da solo o moltiplicato per un intero (piccolo) da il peso con cui l elemento entra in combinazione Prout (1815): I pesi atomici sono multipli interi del peso dell atomo di idrogeno e l atomo di idrogeno e la particella primaria con cui sono costituite tutte le altre. Dalton osservo anche che volumi uguali di gas si combinavano in modo semplice 1` N +1` O =2` NO 19
20 Proust ( ) Prout ( ) 20
21 Gay-Lussac continuo gli esperimenti con volumi di gas, per esempio: 2` H +1` O =2` H 2 O La spiegazione e quella di Avogadro, volume uguali di gas contengono lo stesso numero di molecole: 1` N +1` O =2` NO N 2 + O 2 =2NO + = 2` H +1` O =2` H 2 O 2H 2 + O 2 =2H 2 O + = 21
22 Gay-Lussac ( ) 22
23 La chimica adotto l indivisibilita atomica come comoda ipotesi di lavoro (atomismo fisico) La domanda successiva che si poneva era: Gli atomi hanno una struttura? 1800: L idea atomica era accettata quasi universalmente come ipotesi di lavoro. L idea che fossero una realta fisica fu accettata solo ai primi del
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
Gas perfetti e sue variabili
 Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
MASSE ATOMICHE. 1,000 g di idrogeno reagiscono con 7,9367 g di ossigeno massa atomica ossigeno=2 x 7,9367=15,873 g (relativa all'idrogeno)
 MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE LA MOLE 2.A PRE-REQUISITI 2.3 FORMULE E COMPOSIZIONE 2.B PRE-TEST
 LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
Unità di misura. Perché servono le unità di misura nella pratica di laboratorio e in corsia? Le unità di misura sono molto importanti
 Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
La Teoria dei Quanti e la Struttura Elettronica degli Atomi. Capitolo 7
 La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
Progettazione disciplinare:
 PIANO DI LAVORO ANNUALE-PROGETTAZIONE INDIVIDUALE PER SINGOLA DISCIPLINA E PER CLASSE Classe 1A A.S. 2015/2016 Disciplina: CHIMICA Docente: Rosselli Antonino Ore settimanali: 3 (1 di laboratorio) Libro
PIANO DI LAVORO ANNUALE-PROGETTAZIONE INDIVIDUALE PER SINGOLA DISCIPLINA E PER CLASSE Classe 1A A.S. 2015/2016 Disciplina: CHIMICA Docente: Rosselli Antonino Ore settimanali: 3 (1 di laboratorio) Libro
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO
 ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO Programmazione 2013-2014 Quella che viene qui presentato è la programmazione per moduli disciplinari, nel quale vengono evidenziati: l idea stimolo; i
ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO Programmazione 2013-2014 Quella che viene qui presentato è la programmazione per moduli disciplinari, nel quale vengono evidenziati: l idea stimolo; i
Stati di aggregazione della materia
 SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI
 Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012
 Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
Gas. Vapore. Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente. microscopico MACROSCOPICO
 Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
LE LEGGI DEI GAS. Dalle prime teorie cinetiche dei gas simulazioni della dinamica molecolare. Lezioni d'autore
 LE LEGGI DEI GAS Dalle prime teorie cinetiche dei gas simulazioni della dinamica molecolare. Lezioni d'autore alle Un video : Clic Un altro video : Clic Un altro video (in inglese): Clic Richiami sulle
LE LEGGI DEI GAS Dalle prime teorie cinetiche dei gas simulazioni della dinamica molecolare. Lezioni d'autore alle Un video : Clic Un altro video : Clic Un altro video (in inglese): Clic Richiami sulle
1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3.
 Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
Gas e gas perfetti. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
Stati di aggregazione della materia unità 2, modulo A del libro
 Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
ISTITUTO DI ISTRUZIONE SUPERIORE J.C. MAXWELL Data: 09/09 /2013 Pag. _1_ di _5 PROGRAMMAZIONE ANNUALE A.S. 2013_ / 2014_
 ISTITUTO DI ISTRUZIONE SUPERIORE J.C. MAXWELL Data: 09/09 /2013 Pag. _1_ di _5 INDIRIZZO SCOLASTICO DISCIPLINA DOCENTE / I CLASSE / I X MECCANICA e MECCATRONICA X ELETTRONICA X LOGISTICA e TRASPORTI LICEO
ISTITUTO DI ISTRUZIONE SUPERIORE J.C. MAXWELL Data: 09/09 /2013 Pag. _1_ di _5 INDIRIZZO SCOLASTICO DISCIPLINA DOCENTE / I CLASSE / I X MECCANICA e MECCATRONICA X ELETTRONICA X LOGISTICA e TRASPORTI LICEO
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Programmazione di Scienze A.S. 2013-2014
 Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
L ATOMO. Risponde (o almeno ci prova)
 L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Corso di Laurea in FARMACIA
 Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
Dimensioni Unità di misura. Lezione di fisica
 Dimensioni Unità di misura Lezione di fisica Argomenti della lezione Grandezze fisiche Dimensioni Unità di misura Il sistema internazionale - SI Taratura Le misure La Fisica, dall antico greco φύσις, è
Dimensioni Unità di misura Lezione di fisica Argomenti della lezione Grandezze fisiche Dimensioni Unità di misura Il sistema internazionale - SI Taratura Le misure La Fisica, dall antico greco φύσις, è
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05
 I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
La fisica e la misura
 La fisica e la misura La fisica è una scienza fondamentale che ha per oggetto la comprensione dei fenomeni naturali che accadono nel nostro universo. È basata su osservazioni sperimentali e misure quantitative
La fisica e la misura La fisica è una scienza fondamentale che ha per oggetto la comprensione dei fenomeni naturali che accadono nel nostro universo. È basata su osservazioni sperimentali e misure quantitative
LICEO SCIENTIFICO F.LUSSANA PROGRAMMA DI SCIENZE EFFETTIVAMENTE SVOLTO CLASSE 1 N : Liceo Scientifico delle Scienze Applicate a.s.
 LICEO SCIENTIFICO F.LUSSANA PROGRAMMA DI SCIENZE EFFETTIVAMENTE SVOLTO CLASSE 1 N : Liceo Scientifico delle Scienze Applicate a.s. 2014-2015 Testi in adozione : Scienze della Terra LA TERRA, UN INTRODUZIONE
LICEO SCIENTIFICO F.LUSSANA PROGRAMMA DI SCIENZE EFFETTIVAMENTE SVOLTO CLASSE 1 N : Liceo Scientifico delle Scienze Applicate a.s. 2014-2015 Testi in adozione : Scienze della Terra LA TERRA, UN INTRODUZIONE
UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI
 UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI Esercizio 3.1 Calcolare il potere calorifico superiore e inferiore del gas metano che brucia secondo la reazione CH 4 + 2 O 2 CO 2 + 2 H 2 O sapendo che l
UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI Esercizio 3.1 Calcolare il potere calorifico superiore e inferiore del gas metano che brucia secondo la reazione CH 4 + 2 O 2 CO 2 + 2 H 2 O sapendo che l
Il metodo scientifico
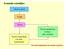 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Cenni di Teoria Cinetica dei Gas
 Cenni di Teoria Cinetica dei Gas Introduzione La termodinamica descrive i sistemi termodinamici tramite i parametri di stato (p, T,...) Sufficiente per le applicazioni: impostazione e progettazione di
Cenni di Teoria Cinetica dei Gas Introduzione La termodinamica descrive i sistemi termodinamici tramite i parametri di stato (p, T,...) Sufficiente per le applicazioni: impostazione e progettazione di
Il Metodo Scientifico
 Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013
 LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
Temperatura. V(t) = Vo (1+at) Strumento di misura: termometro
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
IL NUCLEO ATOMICO E LA MOLE
 IL NUCLEO ATOMICO E LA MOLE Gli atomi sono costituiti da un nucleo, formato da protoni (carica elettrica positiva, massa 1,6724 x 10-24 g) e neutroni (nessuna carica elettrica, massa 1,6745 x 10-24 g),
IL NUCLEO ATOMICO E LA MOLE Gli atomi sono costituiti da un nucleo, formato da protoni (carica elettrica positiva, massa 1,6724 x 10-24 g) e neutroni (nessuna carica elettrica, massa 1,6745 x 10-24 g),
ISTITUTO TECNICO INDUSTRIALE STATALE. B.Pascal Roma
 Ministero dell Istruzione, dell Università e della Ricerca ISTITUTO TECNICO INDUSTRIALE STATALE B.Pascal Roma Anno Scolastico 2012-201 PIANO DI LAVORO DELLE CLASSI PRIME MATERIA: Scienze Integrate CHIMICA
Ministero dell Istruzione, dell Università e della Ricerca ISTITUTO TECNICO INDUSTRIALE STATALE B.Pascal Roma Anno Scolastico 2012-201 PIANO DI LAVORO DELLE CLASSI PRIME MATERIA: Scienze Integrate CHIMICA
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
GAS. I gas si assomigliano tutti
 I gas si assomigliano tutti Aeriforme liquido solido GAS Descrizione macroscopica e microscopica degli stati di aggregazione della materia Fornendo energia al sistema, le forze di attrazione tra le particelle
I gas si assomigliano tutti Aeriforme liquido solido GAS Descrizione macroscopica e microscopica degli stati di aggregazione della materia Fornendo energia al sistema, le forze di attrazione tra le particelle
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
GIOCHI DELLA CHIMICA
 GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
SCUOLA PRIMARIA DI MAGGIATE Classe terza
 SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia
 Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
ISTITUTO ISTRUZIONE SUPERIORE POLO COMMERCIALE ARTISTICO GRAFICO MUSICALE
 a.s.2015/2016 CHIMICA, FISICA E SCIENZE ISTITUTO TECNICO GRAFICA E COMUNICAZIONE SCIENZE INTEGRATE (FISICA) A CURA DEL RESPONSABILE DELL'AMBITO TETI MERI L AMBITO DISCIPLINARE DI CHIMICA, FISICA E SCIENZE
a.s.2015/2016 CHIMICA, FISICA E SCIENZE ISTITUTO TECNICO GRAFICA E COMUNICAZIONE SCIENZE INTEGRATE (FISICA) A CURA DEL RESPONSABILE DELL'AMBITO TETI MERI L AMBITO DISCIPLINARE DI CHIMICA, FISICA E SCIENZE
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
cap 3 - LE ORIGINI DELLA TEORIA ATOMICA
 cap 3 - LE ORIGINI DELLA TEORIA ATOMICA 3.1 La teoria atomica di Democrito (400 a.c.) Proviamo ad immaginare di spezzare a metà un granello di sabbia: si ottiene ovviamente un granello più piccolo che,
cap 3 - LE ORIGINI DELLA TEORIA ATOMICA 3.1 La teoria atomica di Democrito (400 a.c.) Proviamo ad immaginare di spezzare a metà un granello di sabbia: si ottiene ovviamente un granello più piccolo che,
Quesiti e problemi. 10 Un gas viene compresso a temperatura costante. 11 Un cilindro con un pistone ha un volume di 250 ml. v f. v f.
 SUL LIBRO DA PAG 110 A PAG 114 Quesiti e problemi ESERCIZI 1 I gas ideali e la teoria cinetico-molecolare 1 Che cosa si intende per gas ideale? Rispondi in cinque righe. 2 Vero o falso? a) Le molecole
SUL LIBRO DA PAG 110 A PAG 114 Quesiti e problemi ESERCIZI 1 I gas ideali e la teoria cinetico-molecolare 1 Che cosa si intende per gas ideale? Rispondi in cinque righe. 2 Vero o falso? a) Le molecole
I GAS POSSONO ESSERE COMPRESSI.
 I GAS Tutti i gas sono accomunati dalle seguenti proprietà: I GAS POSSONO ESSERE COMPRESSI. L aria compressa occupa un volume minore rispetto a quello occupato dall aria non compressa (Es. gomme dell auto
I GAS Tutti i gas sono accomunati dalle seguenti proprietà: I GAS POSSONO ESSERE COMPRESSI. L aria compressa occupa un volume minore rispetto a quello occupato dall aria non compressa (Es. gomme dell auto
TEORIA QUANTISTICA E STRUTTURA ATOMICA
 TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
1.11.3 Distribuzione di carica piana ed uniforme... 32
 Indice 1 Campo elettrico nel vuoto 1 1.1 Forza elettromagnetica............ 2 1.2 Carica elettrica................ 3 1.3 Fenomeni elettrostatici............ 6 1.4 Legge di Coulomb.............. 9 1.5 Campo
Indice 1 Campo elettrico nel vuoto 1 1.1 Forza elettromagnetica............ 2 1.2 Carica elettrica................ 3 1.3 Fenomeni elettrostatici............ 6 1.4 Legge di Coulomb.............. 9 1.5 Campo
La chimica e il metodo scientifico. Lezioni d'autore di Giorgio Benedetti
 La chimica e il metodo scientifico Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) VIDEO INTRODUZIONE (III) Fino alla fine del settecento, la manipolazione dei metalli, degli
La chimica e il metodo scientifico Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) VIDEO INTRODUZIONE (III) Fino alla fine del settecento, la manipolazione dei metalli, degli
Indice generale. Prefazione
 26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
Istituto di Istruzione Superiore L. da Vinci Civitanova Marche. Anno scolastico 2014-2015. Programma svolto. Docente: Silvana Venditti
 Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Recenti Scoperte Scientifiche in Ottica
 Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
L'ENTROPIA. Lezioni d'autore
 L'ENTROPIA Lezioni d'autore Un video : Clic Un altro video : Clic La funzione di distribuzione delle velocità (I) Nel grafico accanto sono riportati i numeri delle molecole di un gas, suddivise a seconda
L'ENTROPIA Lezioni d'autore Un video : Clic Un altro video : Clic La funzione di distribuzione delle velocità (I) Nel grafico accanto sono riportati i numeri delle molecole di un gas, suddivise a seconda
Definiamo Entalpia la funzione: DH = DU + PDV. Variando lo stato del sistema possiamo misurare la variazione di entalpia: DU = Q - PDV.
 Problemi Una mole di molecole di gas ideale a 292 K e 3 atm si espandono da 8 a 20 L e a una pressione finale di 1,20 atm seguendo 2 percorsi differenti. Il percorso A è un espansione isotermica e reversibile;
Problemi Una mole di molecole di gas ideale a 292 K e 3 atm si espandono da 8 a 20 L e a una pressione finale di 1,20 atm seguendo 2 percorsi differenti. Il percorso A è un espansione isotermica e reversibile;
2) Successivamente, si aggiungono all acqua due piccoli cucchiai di sale, facendo si che quest ultimo si sciolga completamente.
 Camilla Castelanelli Classe 3^B Data esperienza: 7-05-15 In gruppo con Gabriele Silini, Gaia Ghidini e Federica Bettoni. CHIMICA RELAZIONE DI LABORATORIO Alla Ricerca Del DNA OBIETTIVO DELL ESPERIENZA:
Camilla Castelanelli Classe 3^B Data esperienza: 7-05-15 In gruppo con Gabriele Silini, Gaia Ghidini e Federica Bettoni. CHIMICA RELAZIONE DI LABORATORIO Alla Ricerca Del DNA OBIETTIVO DELL ESPERIENZA:
I GAS GAS IDEALI. PV=nRT. Pressione Volume numero di moli Temperatura Costante dei gas. P V n T R. n, T= cost Legge di Boyle
 I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
LE SOLUZIONI 1.molarità
 LE SOLUZIONI 1.molarità Per mole (n) si intende una quantità espressa in grammi di sostanza che contiene N particelle, N atomi di un elemento o N molecole di un composto dove N corrisponde al numero di
LE SOLUZIONI 1.molarità Per mole (n) si intende una quantità espressa in grammi di sostanza che contiene N particelle, N atomi di un elemento o N molecole di un composto dove N corrisponde al numero di
Programmazione individuale per competenze CLASSE 3^B LSA. Materia: CHIMICA
 Programmazione individuale per competenze CLASSE 3^B LSA Materia: CHIMICA Situazione della classe Accordi con la classe Accordi con le altre discipline Correlazione con i progetti proposti alla classe
Programmazione individuale per competenze CLASSE 3^B LSA Materia: CHIMICA Situazione della classe Accordi con la classe Accordi con le altre discipline Correlazione con i progetti proposti alla classe
INTRODUZIONE ALLO STUDIO DELLA CHIMICA
 INTRODUZIONE ALLO STUDIO DELLA CHIMICA La chimica si interessa dello studio della materia, delle sue proprietà, della sua struttura e delle trasformazioni che avvengono in essa. Materia è tutto ciò che
INTRODUZIONE ALLO STUDIO DELLA CHIMICA La chimica si interessa dello studio della materia, delle sue proprietà, della sua struttura e delle trasformazioni che avvengono in essa. Materia è tutto ciò che
Programma (piano di lavoro) preventivo
 I S T I T U T O T E C N I C O I N D U S T R I A L E S T A T A L E G u g l i e l m o M a r c o n i V e r o n a Programma (piano di lavoro) preventivo Anno Scolastico 2014/2015 Materia SCIENZE INTEGRATE:
I S T I T U T O T E C N I C O I N D U S T R I A L E S T A T A L E G u g l i e l m o M a r c o n i V e r o n a Programma (piano di lavoro) preventivo Anno Scolastico 2014/2015 Materia SCIENZE INTEGRATE:
Lezione del 24 Ottobre 2014
 MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Pagina 1 - Idee per scuole partecipanti al concorso
 Pagina 1 - Idee per scuole partecipanti al concorso SPERIMENTANDO edizione 2016 SCIENZA e SPORT: viaggio tra gli elementi e le discipline Idee e proposte per le scuole partecipanti al concorso "Sperimenta
Pagina 1 - Idee per scuole partecipanti al concorso SPERIMENTANDO edizione 2016 SCIENZA e SPORT: viaggio tra gli elementi e le discipline Idee e proposte per le scuole partecipanti al concorso "Sperimenta
Lo stato gassoso e le caratteristiche dei gas
 Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi
 È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
Programma Didattico Annuale
 LICEO SCIENTIFICO STATALE GALILEO GALILEI PdQ - 7.06 Ediz.: 1 Rev.: 0 Data 02/09/05 Alleg.: D01 PROG. M2 PROCEDURA della QUALITA' Programma Didattico Annuale Anno Scolastico 2011/2012 MATERIA : Scienze
LICEO SCIENTIFICO STATALE GALILEO GALILEI PdQ - 7.06 Ediz.: 1 Rev.: 0 Data 02/09/05 Alleg.: D01 PROG. M2 PROCEDURA della QUALITA' Programma Didattico Annuale Anno Scolastico 2011/2012 MATERIA : Scienze
La Misura del Mondo. 4 Le distanze nel sistema solare. Bruno Marano Dipartimento di Astronomia Università di Bologna
 La Misura del Mondo 4 Le distanze nel sistema solare Dipartimento di Astronomia Università di Bologna La triangolazione tra la Torre degli Asinelli, Porta S.Felice, il ponte sul Reno e il Colle della Guardia
La Misura del Mondo 4 Le distanze nel sistema solare Dipartimento di Astronomia Università di Bologna La triangolazione tra la Torre degli Asinelli, Porta S.Felice, il ponte sul Reno e il Colle della Guardia
IIS D ORIA - UFC. Laboratorio Relazioni di laboratorio Verifiche scritte di laboratorio (elaborazione dati, domande aperte, test a risposta multipla)
 INDICE DELLE UFC 0 OBIETTIVI MINIMI CLASSE PRIMA (v. programmazione anno precedente) 1 LA TEMPERATURA 2 IL CALORE 3 L EQUILIBRIO DEI SOLIDI 4 IL MOVIMENTO: LA VELOCITÀ 5 IL MOVIMENTO: L ACCELERAZIONE 6
INDICE DELLE UFC 0 OBIETTIVI MINIMI CLASSE PRIMA (v. programmazione anno precedente) 1 LA TEMPERATURA 2 IL CALORE 3 L EQUILIBRIO DEI SOLIDI 4 IL MOVIMENTO: LA VELOCITÀ 5 IL MOVIMENTO: L ACCELERAZIONE 6
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Cap. 1 - Stati di aggregazione della materia.
 Cap. 1 - Stati di aggregazione della materia. Lo stato di aggregazione di un sistema è determinato dalla energia cinetica delle particelle e dall energia potenziale dovuta alle forze di coesione fra le
Cap. 1 - Stati di aggregazione della materia. Lo stato di aggregazione di un sistema è determinato dalla energia cinetica delle particelle e dall energia potenziale dovuta alle forze di coesione fra le
Leggi dei gas. PV = n RT SISTEMI DI PARTICELLE NON INTERAGENTI. perché le forze tra le molecole sono differenti. Gas perfetti o gas ideali
 Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
La carica elettrica. Lezioni d'autore
 La carica elettrica Lezioni d'autore L'esperimento di Millikan (I) VIDEO L'esperimento di Millikan (II) Dai primi esperimenti realizzati con un numero elevato di goccioline di acqua (cloud) ionizzate in
La carica elettrica Lezioni d'autore L'esperimento di Millikan (I) VIDEO L'esperimento di Millikan (II) Dai primi esperimenti realizzati con un numero elevato di goccioline di acqua (cloud) ionizzate in
La struttura della materia
 Unità didattica 11 La struttura della materia Competenze 1 Descrivere il modello atomico di Dalton 2 Spiegare le caratteristiche macroscopiche e microscopiche delle principali trasformazioni fisiche 3
Unità didattica 11 La struttura della materia Competenze 1 Descrivere il modello atomico di Dalton 2 Spiegare le caratteristiche macroscopiche e microscopiche delle principali trasformazioni fisiche 3
GLI ELEMENTI CHIMICI. 1 Struttura dell atomo Lezione Treccani
 GLI ELEMENTI CHIMICI La teoria degli elementi rappresenta un aspetto fondamentale della chimica fin dalla sua costituzione come scienza, in quanto tratta il problema della definizione di numero, natura
GLI ELEMENTI CHIMICI La teoria degli elementi rappresenta un aspetto fondamentale della chimica fin dalla sua costituzione come scienza, in quanto tratta il problema della definizione di numero, natura
LE COMPETENZE ESSENZIALI DI FISICA
 LE COMPETENZE ESSENZIALI DI FISICA classe prima Liceo scientifico COMPETENZE raccogliere dati attraverso l osservazione diretta dei fenomeni naturali fisici e attraverso l attività di laboratorio OSA comprendere
LE COMPETENZE ESSENZIALI DI FISICA classe prima Liceo scientifico COMPETENZE raccogliere dati attraverso l osservazione diretta dei fenomeni naturali fisici e attraverso l attività di laboratorio OSA comprendere
I FENOMENI TERMICI. I fenomeni termici Fisica Medica Lauree triennali nelle Professioni Sanitarie. P.Montagna ott-07. pag.1
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano pag.1
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano pag.1
Le leggi dei gas. Capitolo 21. 21.1. Le leggi di Boyle e di Gay-Lussac. Massimo Banfi
 Cap. 1 - Le leggi dei gas Capitolo 1 Le leggi dei gas 1.1. Le leggi di Boyle e di Gay-Lussac Lo stato termodinamico di un gas è perfettamente noto quando si conoscano i valori delle tre variabili P, V,
Cap. 1 - Le leggi dei gas Capitolo 1 Le leggi dei gas 1.1. Le leggi di Boyle e di Gay-Lussac Lo stato termodinamico di un gas è perfettamente noto quando si conoscano i valori delle tre variabili P, V,
Università degli studi di Sassari. Corso di Chimica di Base. Mauro Rustici Dipartimento di Chimica e Farmacia, Via Vienna 2, 07100 SASSARI
 1 Università degli studi di Sassari Corso di Chimica di Base Mauro Rustici Dipartimento di Chimica e Farmacia, Via Vienna 2, 07100 SASSARI email rustici@uniss.it Anno Accademico 2013/2014 Indice 1 Materia
1 Università degli studi di Sassari Corso di Chimica di Base Mauro Rustici Dipartimento di Chimica e Farmacia, Via Vienna 2, 07100 SASSARI email rustici@uniss.it Anno Accademico 2013/2014 Indice 1 Materia
FISICA Biennio e Triennio Classico e Linguistico
 PROGRAMMAZIONE D ISTITUTO FISICA Biennio e Triennio Classico e Linguistico FISICA NEL LICEO LINGUISTICO (BIENNIO) FINALITA Lo studio della fisica al ginnasio deve fornire allo studente un bagaglio di conoscenze
PROGRAMMAZIONE D ISTITUTO FISICA Biennio e Triennio Classico e Linguistico FISICA NEL LICEO LINGUISTICO (BIENNIO) FINALITA Lo studio della fisica al ginnasio deve fornire allo studente un bagaglio di conoscenze
Indice PREFAZIONE. Capitolo 5 LE LEGGI DEL MOTO DI NEWTON 58 5.1 La terza legge di Newton 58
 Indice PREFAZIONE XV Capitolo 1 RICHIAMI DI MATEMATICA 1 1.1 Simboli, notazione scientifica e cifre significative 1 1.2 Algebra 3 1.3 Geometria e trigonometria 5 1.4 Vettori 7 1.5 Sviluppi in serie e approssimazioni
Indice PREFAZIONE XV Capitolo 1 RICHIAMI DI MATEMATICA 1 1.1 Simboli, notazione scientifica e cifre significative 1 1.2 Algebra 3 1.3 Geometria e trigonometria 5 1.4 Vettori 7 1.5 Sviluppi in serie e approssimazioni
Programmi relativi ai quesiti delle prove di ammissione ai corsi di. Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di
 Programmi relativi ai quesiti delle prove di ammissione ai corsi di Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di laurea delle professioni sanitarie Per l ammissione ai corsi è
Programmi relativi ai quesiti delle prove di ammissione ai corsi di Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di laurea delle professioni sanitarie Per l ammissione ai corsi è
 Misurazione di una grandezza fisica Definizione operativa: Grandezza fisica Proprietà misurabile Sensazione di caldo/freddo Temperatura NO (soggettiva, diversa per ciascuno) SI (oggettiva, uguale per tutti)
Misurazione di una grandezza fisica Definizione operativa: Grandezza fisica Proprietà misurabile Sensazione di caldo/freddo Temperatura NO (soggettiva, diversa per ciascuno) SI (oggettiva, uguale per tutti)
IL SISTEMA INTERNAZIONALE DI MISURA
 IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO
 LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO F I S I C A CLASSI NUOVO ORDINAMENTO A. S. 2014/2015 COMPETENZE PRIMO BIENNIO: SC1 SC2 Osservare descrivere ed
LICEO SCIENTIFICO STATALE G. BANZI BAZOLI LECCE P R O G R A M M A Z I O NE DI DIPARTIMENTO F I S I C A CLASSI NUOVO ORDINAMENTO A. S. 2014/2015 COMPETENZE PRIMO BIENNIO: SC1 SC2 Osservare descrivere ed
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Inquinamento da Campi Elettromagnetici
 Inquinamento da Campi Elettromagnetici Aspetti Tecnici, Sanitari, Normativi A cura di ECORICERCHE s.r.l. Lo Spettro Elettromagnetico ECORICERCHE s.r.l. 2 Elettrosmog: che cos è? E un termine entrato nell
Inquinamento da Campi Elettromagnetici Aspetti Tecnici, Sanitari, Normativi A cura di ECORICERCHE s.r.l. Lo Spettro Elettromagnetico ECORICERCHE s.r.l. 2 Elettrosmog: che cos è? E un termine entrato nell
