I Gas. Farmacia. Lezione
|
|
|
- Eva Valeri
- 5 anni fa
- Visualizzazioni
Transcript
1 I Gas Farmacia Lezione
2 GAS
3 Importanza dei gas L airbag si riempie di N2 gas in seguito ad un urto. Il gas viene generato dalla decomposizione della sodio azide NaN3. 2 NaN3 ---> 2 Na + 3 N2
4 Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti
5 Stato solido Nello stato solido l energia di interazione prevale sull energia cinetica. Le interazioni tra le particelle sono così intense da vincolare le particelle tra di loro. Se si prova a spostarne una, le altre la seguono e quindi si provoca uno spostamento fisico di tutto il solido. Il volume dipende dalla temperatura e dalla pressione. Al variare di pressione e temperatura si osservano piccole variazioni del volume di un solido.
6 Stato liquido Nello stato liquido l energia di interazione è comparabile con l energia cinetica delle particelle. Le interazioni tra le particelle sono capaci di vincolare parzialmente le particelle tra di loro. L energia cinetica delle particelle è capace comunque di provocarne un movimento continuo. Al variare della pressione si osservano piccole variazioni del volume.al variare della temperatura le dimensioni si modificano in maniera più marcata.
7 Stato gassoso Allo stato gassoso, la materia non ha né un proprio volume né una propria forma. Questo comportamento dipende dal fatto che l energia cinetica supera l energia di interazione tra le molecole
8 Passaggio di stato GAS Evaporazione/vaporizzazione EBOLLIZIONE LIQUIDO E IO N CA Z LI DI FI SO TO EN AM SOLIDO FU SI E IN N BR IO AZ ON E IM BL SU LIQUEFAZIONE
9 FASE Benzina H2O (g) H2O H2O (s) CCl4 H2O (l) Hg SISTEMA a 4 COMPONENTI in 4 FASI LIQUIDE porzione porzione Vapore Ghiaccio Acqua SISTEMA a 1 COMPONENTE a 3 FASI, ciascuna in uno stato differente del sistema fisicamente distinguibile ed omogenea di materia uniforme nella composizione e nelle proprietà intrinseche
10 I gas
11 I gas Van Helmont ( ): caos gas Torricelli ( ): l aria atmosferica esercita pressione; costruzione del primo barometro. Otto von Guericke: pompa per vuoto Per definire lo stato di un gas sono necessarie quattro grandezze: (a) La quantità del gas, n (in moli) b) La temperatura del gas, T (in Kelvin). (c) Il volume del gas, V (in litri). d) La pressione del gas, P (in atmosfere).
12 I gas I gas: Possono essere compressi. Occupano completamente ed in maniera uniforme il recipiente che li contiene. Bassa densità. Esercitano una pressione su tutte le pareti del recipiente che li contiene.
13 I gas e il loro volume Si definisce volume di un gas lo spazio messo a disposizione delle particelle del gas per il loro movimento. Una sostanza è allo stato gassoso, quando le sue particelle non sono legate da alcun legame chimico e non risentono di forze di attrazione. In un gas ogni particella si muove indipendentemente dalle altre.
14 Pressione Si definisce pressione di un gas la pressione che le particelle gassose determinano urtando contro le pareti del recipiente in cui il gas è contenuto. Dispositivi per la misura della pressione
15 Gas ideale e Gas reale ogni particella è un punto matematico, cioè ha un volume insignificante, assolutamente trascurabile rispetto al volume totale occupato dal gas; ogni particella è in continuo movimento caotico, senza nessuna direzione preferenziale; ogni particella è mediamente molto distante dalle altre e non è soggetta a forze di attrazione o repulsione da parte delle altre; se due particelle si scontrano, l urto è elastico e non si ha perdita di energia totale.
16 Pressione, volume e numero di molecole La pressione esercitata da un gas in un certo volume è direttamente proporzionale al numero delle molecole, e quindi al numero delle moli, di gas. Il volume occupato da un gas a una certa pressione è direttamente proporzionale al numero delle molecole, e quindi al numero delle moli, di gas.
17 Trasformazioni a T costante Per ogni quantità di gas a temperatura costante, il prodotto dei valori della pressione e del volume è costante. Questa legge, conosciuta anche come legge di Boyle, può essere espressa dalle relazioni: p1 V1 = p2 V2 = p3 V3 = cioè p V = k
18 Legge di Boyle Per una data quantità di gas, ad una data temperatura, il prodotto della pressione per il volume è costante P 1/V P = K (1/V) PV = K P 1V 1 = P 2V 2
19
20 Trasformazione di un gas a V costante (A), un gas alla temperatura t0 = 0 C occupa un volume V alla pressione p0. (B), mantenendo il volume costante, aumentiamo la temperatura fino al valore t. L energia delle particelle più elevata provoca un aumento del numero e della forza degli urti contro le pareti. Alla temperatura t il gas esercita una pressione pt maggiore di quella iniziale (legge di Gay-Lussac). Il riscaldamento o il raffreddamento di un gas a volume costante provoca, per ogni grado di differenza di temperatura, rispettivamente un aumento o una diminuzione di 1/273 della pressione esercitata dal gas a 0 C.
21 Legge di Gay Lussac Se una certa quantità di gas viene mantenuta a volume costante, la sua pressione è direttamente proporzionale alla temperatura assoluta K = P/T P1/T1 = P2/T2 P = Po(1 + αt)
22 Trasformazione di un gas a P costante (A), un gas alla temperatura t0 = 0 C occupa un volume V0 alla pressione p. (B), mantenendo la pressione costante, aumentiamo la temperatura fino al valore t. La maggiore energia delle particelle determina una spinta sullo stantuffo, che viene sollevato. Alla temperatura t il gas occupa un volume Vt maggiore di quello Iniziale (legge di CHARLES) Il riscaldamento o il raffreddamento di un gas a pressione costante provoca, per ogni grado di differenza di temperatura, rispettivamente un aumento o una diminuzione di 1/273 del volume occupato dal gas a 0 C.
23 Legge di Charles K = V/T V1/T1 = V2/T2 V = Vo(1 + αt) Se una certa quantità di gas viene mantenuta a pressione costante, il Legge Isobara suo volume è direttamente proporzionale alla temperatura assoluta
24
25
26 Legge dei gas e T La temperatura di 273 C rappresenta il valore limite della temperatura, perché non può esistere materia priva di energia e priva di volume. Dato che la temperatura in gradi centigradi si indica con t e quella in kelvin con T, la temperatura assoluta si ricava con la relazione: T = t Il ghiaccio fondente (0 C), per esempio, ha la temperatura di 273 K, mentre l acqua bollente (100 C) ha la temperatura di 373 K.
27 Principio di Avogadro Ipotesi di Amedeo Avogadro (1811): Volumi uguali di gas mantenuti nelle stesse condizioni di pressione e temperatura contengono un eguale numero di molecole (il volume di un gas a date T e P è direttamente proporzionale alla quantità di gas).
28 Legge di Avogadro V n V = Ca n Ca = costante Ipotesi di Amedeo Avogadro (1811): Volumi uguali di gas mantenuti nelle stesse condizioni di pressione e temperatura contengono un eguale numero di molecole (il volume di un gas a date T e P è direttamente proporzionale alla quantità di gas).
29 Principio di Avogadro A 0 C e a 1,013 bar il volume di una mole di qualsiasi gas risulta essere di 22,4 L. Per convenzione si è stabilito di scegliere la temperatura di 0 C e la pressione di 1,013 bar, cioè 1 atm, come condizioni di riferimento, che sono state chiamate condizioni normali (c.n.).
30 La legge dei gas ideali
31 Combinando insieme le tre leggi seguenti Legge di Boyle V (1/P) (T,n costanti) V nt/p Legge di Charles V T (P,n costanti) Legge dei gas ideali PV = nrt Legge di Avogadro V n (T,P costanti) V = RnT/P
32 R, costante universale Il valore della costante R, chiamata costante universale dei gas, può essere ricavato sostituendo nell equazione di stato i valori relativi a una mole di gas a c.n.
33 Esempio: Data la reazione Δ 2 KClO3 (s) 2 KCl(s) + 3 O2(g) quanti litri di ossigeno è possibile ottenere a 298 K e 1,02 atm da 1,226 g di KClO3? In maniera analoga si risolvono problemi in cui è dato il volume di O 2 sviluppato e si vuole sapere il peso di KClO3 necessario a produrlo
34 DENSITA Densità relativa. La densità dei gas è proporzionale al peso molecolare: d1/d2 = M1/M2
35
36 Legge di Dalton La pressione di una miscela di gas è la somma delle pressioni dei vari componenti della miscela.
37 Legge di Dalton ntotali = na + nb + nc + PV = ntotalirt PV = (na + nb + nc + )RT PV = nart + nbrt +.. P = nart/v + nbrt/v + ncrt/v. Ptotale = PA + PB + PC +. PA, PB, PC = pressioni parziali PA/Ptotale = (nart/v)/(ntotalert/v) = = na/ntotale = XA = frazione molare di A
38 GAS REALI il volume proprio delle particelle non è trascurabile rispetto al volume del gas; fra le particelle si stabiliscono interazioni che, anche se di bassa intensità,non sono trascurabili.
39 Teoria cinetica Le molecole dei gas si muovono in tutte le direzioni, si urtano e si scambiano energia. A condizioni normali ogni molecola è interessata da circa 1010 urti al secondo. Ogni molecola ha la propria energia cinetica e quindi la propria velocità. Istante per istante, però, la velocità cambia a seconda di come avvengono gli urti e l energia varia in base agli urti attivi e a quelli passivi.
40 Teoria cinetica I gas sono costituiti da molecole il cui volume è trascurabile rispetto al volume occupato dal gas. Le molecole di un gas sono soggette a un moto continuo, casuale e rapido. L energia cinetica media delle molecole di un gas è determinata dalla T di un gas. Le molecole di un gas collidono le une contro le altre e contro pareti del recipiente che le contiene, senza perdere energia L energia cinetica media di un insieme di molecole di un gas dipende solo dalla T: <Ecin> T <Ecin> =1/2 mv2
41 Teoria cinetica dei gas I grafici rappresentano la relazione esistente a diverse temperature tra velocità delle particelle di un gas, e quindi loro energia cinetica, e numero delle particelle che hanno quella velocità. (A), a 0 C le particelle hanno velocità diverse, ma per poche di esse la velocità è inferiore a 1 km/s (area azzurra), così come poche hanno velocità superiore a 3 km/s (area rossa); la maggior parte delle particelle ha velocità intermedia, intorno a 2 km/s. (B), il numero delle particelle che superano i 3 km/s di velocità è più alto a C (area verde) che a 0 C (area rossa).
42 Temperatura critica Un gas è un aeriforme che si trova al di sopra della sua temperatura critica, un vapore è un aeriforme che si trova al di sotto della sua temperatura critica. Un aeriforme che può essere trasformato in liquido per sola compressione è chiamato vapore.
43 Valori della temperatura critica in C di alcuni elementi e composti.
44 Temperatura critica Temperatura critica: temperatura al di sopra della quale un gas non può essere liquefatto.
45 Deviazione dall idealità Incidenza delle forze intermolecolari. PV/RT = Fattore di compressibilità Incidenza della temperatura.
46 Legge di Graham Due gas A e B in una miscela hanno la stessa T e quindi la stessa Energia Cinetica: mava2/2 = mbvb2/2 da cui: ma/mb = vb2/va2 Thomas Graham ( ) studiò l effusione e trovò sperimentalmente che le velocità di effusione di due gas sono inversamente proporzionali alla radice quadrata delle loro masse molecolari nelle stesse condizioni di P e T.
47 Densità dei gas Se PV = nrt si ricava che P = (n/v) RT e poiché n = Massa in g/massa Molare, si ottiene che: P = (Massa in g/v) (RT/M. Molare) Per definizione Massa/V = d dove d è la densità, per cui: d = P Massa Molare/ R T La densità di un gas è direttamente proporzionale alla sua massa molare e quindi al suo peso molecolare
48 Problema: Quale è il peso molecolare di una sostanza che pesa 0,970 g il cui vapore occupa 200 ml a 99 C e 0,964 atm? T=99+273=372 K
Stati di aggregazione della materia. GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti
 9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso. L atmosfera terrestre è il sistema gassoso in cui siamo immersi
 Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Legge di stato dei gas ideali
 Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
LA MATERIA ED I SUOI STATI
 LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
Il Gas Ideale. Il gas ideale é un'astrazione
 Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Leggi dei gas Equazione di stato dei gas perfetti
 Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
GAS IDEALI (o gas perfetti )
 GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
. Proprietà degli stati della materia Aeriforme Liquido Solido
 . Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
. Proprietà degli stati della materia Aeriforme Liquido Solido Volume variabile in funzione del recipiente Volume definito Volume definito Forma del recipiente Forma del recipiente Forma propria Miscibili
Diagramma di stato di H 2 O
 Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
Stati di aggregazione della materia. dal microscopico al macroscopico: struttura. interazioni GASSOSO. proprietà SOLIDO LIQUIDO
 Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Termodinamica Chimica
 Universita degli Studi dell Insubria Termodinamica Chimica I Gas Ideali dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini Proprietà di un Gas Può essere compresso facilmente Esercita
Universita degli Studi dell Insubria Termodinamica Chimica I Gas Ideali dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini Proprietà di un Gas Può essere compresso facilmente Esercita
Stati d aggregazione della materia
 Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
-GAS IDEALI- Le particelle che costituiscono un gas ideale:
 -GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
-GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
LEGGI DEI GAS. Gas sono sostanze sprovviste di forma e volume proprio
 LEGGI DEI GAS Gas sono sostanze sprovviste di forma e volume proprio Una grandezza molto significativa per descrivere un gas è la pressione, conseguenza delle collisioni del gas sulla superficie del contenitore.
LEGGI DEI GAS Gas sono sostanze sprovviste di forma e volume proprio Una grandezza molto significativa per descrivere un gas è la pressione, conseguenza delle collisioni del gas sulla superficie del contenitore.
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
= cost a p costante V 1 /T 1 =V 2 /T 2 LEGGE DI GAY-LUSSAC: Un sistema allo stato gassoso è definito da 4. mmhg (torr), bar.
 GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
Leggi ricavate da osservazioni sperimentali : mantenendo costante due dei 4 parametri, come variano gli altri due?
 Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
I gas. ChimicaGenerale_lezione10
 I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
I gas e loro proprietà Cap , 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96
 2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
Queste proprietà derivano dalla grande distanza che separa le molecole che compongono un gas.
 Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Stati di aggregazione della materia
 Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
L equilibrio dei gas
 L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
ATOMI E MOLECOLE. ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche.
 1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
Chimica generale. Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3
 Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Chimica generale Corsi di laurea in - Tecnologie alimentari per la ristorazione - Viticoltura ed enologia - Tecnologia agroalimentare PARTE 3 1 GLI STATI DI AGGREGAZIONE DELLA MATERIA 2 I composti chimici
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
approfondimento Fasi e cambiamenti di fase
 approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
STATO GASSOSO. parte I a. - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio
 STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
Gas. Chimica generale ed Inorganica: Chimica Generale. I palloni ad aria calda
 Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Stati della materia. Esempio. Fusione e solidificazione. Esempio. Stati di aggregazione della materia
 Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
1.Pressione di un Gas
 1.Pressione di un Gas Un gas è formato da molecole che si muovono in modo disordinato, urtandosi fra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti, le molecole esercitano
1.Pressione di un Gas Un gas è formato da molecole che si muovono in modo disordinato, urtandosi fra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti, le molecole esercitano
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
Sistemi Gassosi. GAS = specie che occupa tutto lo spazio disponibile. VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 )
 Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
GAS IDEALI E REALI. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche:
 GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1
 I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
UNITA DI MISURA. Le unità di misura sono molto importanti
 Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C.
 http://www. I GAS : ESERCIZI 1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C. da quanto espresso si evince che il numero di moli è costante
http://www. I GAS : ESERCIZI 1-Sia un gas a t = -100 C ed alla pressione P= 10 atm.calcolare la pressione se la temperatura viene portata a 20 C. da quanto espresso si evince che il numero di moli è costante
SISTEMA TERMODINAMICO STATO TERMODINAMICO
 SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
Stati di aggregazione della materia
 SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
Lez 14 16/11/2016. Lezioni in didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617
 Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
LE LEGGI DEI GAS. Prof. Michele Barcellona
 LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
Termodinamica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Termodinamica Studia sistemi estesi caratterizzati da pressione, volume e temperatura Si basa sulla definizione della temperatura e su tre principi Il primo principio riguarda la conservazione dell energia
Termodinamica Studia sistemi estesi caratterizzati da pressione, volume e temperatura Si basa sulla definizione della temperatura e su tre principi Il primo principio riguarda la conservazione dell energia
ESERCIZI ESERCIZI. 1) L equazione di stato valida per i gas perfetti è: a. PV = costante b. PV = nrt c. PV = znrt d. RT = npv Soluzione
 ESERCIZI 1) L equazione di stato valida per i gas perfetti è: a. PV = costante b. PV = nrt c. PV = znrt d. RT = npv 2) In genere, un gas si comporta idealmente: a. ad elevate pressioni e temperature b.
ESERCIZI 1) L equazione di stato valida per i gas perfetti è: a. PV = costante b. PV = nrt c. PV = znrt d. RT = npv 2) In genere, un gas si comporta idealmente: a. ad elevate pressioni e temperature b.
LA TEORIA CINETICA DEI GAS.
 LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
LO STATO GASSOSO. S: Forma e volume propri L: Volume proprio forma del contenitore G: Volume e forma del contenitore
 LO STATO GASSOSO Le diverse proprietà di massa degli stati di aggregazione della materia sono dovute all arrangiamento delle molecole (o atomi o ioni). Tutti gli stati rispondono ad una perturbazione (ad
LO STATO GASSOSO Le diverse proprietà di massa degli stati di aggregazione della materia sono dovute all arrangiamento delle molecole (o atomi o ioni). Tutti gli stati rispondono ad una perturbazione (ad
Forze Intermolecolari. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Forze Intermolecolari Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Forze Intermolecolari Le Forze Intermolecolari sono forze attrattive fra molecole. Le
Forze Intermolecolari Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Forze Intermolecolari Le Forze Intermolecolari sono forze attrattive fra molecole. Le
Stati d aggregazione della materia
 Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Stati d aggregazione della materia SOLIDO: Forma e volume propri. GASSOSO: Forma e volume del recipiente in cui è contenuto. LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. Parametri
Gli stati di aggregazione della materia.
 Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
Stati della materia. Una sostanza pura è una sostanza la cui composizione chimica non varia. Ossigeno. Acqua. Aria
 1. Una sostanza pura non deve necessariamente essere composta da un unico elemento chimico. 2. Anche una miscela di più sostanze può essere considerata una sostanza pura purchè abbia una composizione chimica
1. Una sostanza pura non deve necessariamente essere composta da un unico elemento chimico. 2. Anche una miscela di più sostanze può essere considerata una sostanza pura purchè abbia una composizione chimica
LEGAMI INTERMOLECOLARI LEGAMI INTERMOLECOLARI
 I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
TEORIA CINETICA DEI GAS IDEALI
 TEORIA CINETICA DEI GAS IDEALI T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e La F i s i c a di A m a l d
TEORIA CINETICA DEI GAS IDEALI T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e La F i s i c a di A m a l d
La temperatura: La pressione: Il volume:
 I gas Un gas è formato da un gran numero di molecole che si muovono in modo disordinato, urtandosi tra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti le molecole esercitano
I gas Un gas è formato da un gran numero di molecole che si muovono in modo disordinato, urtandosi tra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti le molecole esercitano
GLI STATI DELLA MATERIA
 GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
Gradi di libertà negli sta/ di aggregazione della materia
 Gradi di libertà negli sta/ di aggregazione della materia I solidi cristallini sono cara-erizza0 da un ordine nelle posizioni e nelle orientazioni. Gradi di libertà negli sta/ di aggregazione della materia
Gradi di libertà negli sta/ di aggregazione della materia I solidi cristallini sono cara-erizza0 da un ordine nelle posizioni e nelle orientazioni. Gradi di libertà negli sta/ di aggregazione della materia
GAS TERMODINAMICA CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE
 CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE GAS TERMODINAMICA GAS PERFETTI E GAS REALI TRASFORMAZIONI TERMODINAMICHE TRASMISSIONE DEL CALORE A. A. 2015-2016 Fabrizio
CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE GAS TERMODINAMICA GAS PERFETTI E GAS REALI TRASFORMAZIONI TERMODINAMICHE TRASMISSIONE DEL CALORE A. A. 2015-2016 Fabrizio
MODULO C IMPARIAMO A RICONOSCERE I COMPONENTI DI UN IMPIANTO. Lezione 50 Cenni di fisica per la pneumatica
 MODULO C IMPARIAMO A RICONOSCERE I COMPONENTI DI UN IMPIANTO Lezione 50 Cenni di fisica per la pneumatica Gli impianti pneumatici (pneumatica dal greco pneumatikos, proveniente dal vento, è una branca
MODULO C IMPARIAMO A RICONOSCERE I COMPONENTI DI UN IMPIANTO Lezione 50 Cenni di fisica per la pneumatica Gli impianti pneumatici (pneumatica dal greco pneumatikos, proveniente dal vento, è una branca
Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più
 I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
SCALA TERMOMETRICA CELSIUS
 TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Proprietà dei gas (Cap. 13)
 Proprietà dei gas (Cap. 13) I gas Misura della pressione Leggi di Boyle, di Charles e di Gay-Lussac Ipotesi di Avogadro Legge del gas ideale Determinazione della massa molecolare dei gas Legge di Dalton
Proprietà dei gas (Cap. 13) I gas Misura della pressione Leggi di Boyle, di Charles e di Gay-Lussac Ipotesi di Avogadro Legge del gas ideale Determinazione della massa molecolare dei gas Legge di Dalton
Lo stato liquido. Un liquido non ha una forma propria, ma ha la forma del recipiente che lo contiene; ha però volume proprio e non è comprimibile.
 I liquidi Lo stato liquido Lo stato liquido rappresenta una condizione intermedia tra stato aeriforme e stato solido, tra lo stato di massimo disordine e quello di perfetto ordine Un liquido non ha una
I liquidi Lo stato liquido Lo stato liquido rappresenta una condizione intermedia tra stato aeriforme e stato solido, tra lo stato di massimo disordine e quello di perfetto ordine Un liquido non ha una
14. Transizioni di Fase_a.a. 2009/2010 TRANSIZIONI DI FASE
 TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
UNITÀ 1 La temperatura. Test
 Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Temperatura. Il legame con le grandezze microscopiche è di tipo statistico. Pressione Volume Temperatura
 Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Gas Ideale: Legge di Charles. V t =V 0 (1+αT)
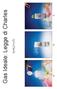 Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
Chimica. Gli stati di aggregazione della materia
 Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
TERMODINAMICA stato gassoso. TERMODINAMICA stato gassoso. Elio GIROLETTI - Università degli Studi di Pavia, Dip. Fisica nucleare e teorica
 UNIERSITÀ DEGLI STUDI DI PAIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 038298.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti TERMODINAMICA stato gassoso FISICA
UNIERSITÀ DEGLI STUDI DI PAIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 038298.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti TERMODINAMICA stato gassoso FISICA
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Capitolo 5 La quantità chimica: la mole
 Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Gas. Vapore. Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente. microscopico MACROSCOPICO
 Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Dipartimento di Scienze Chimiche. Ambiente. Sistema
 Descrizione macroscopica dei sistemi materiali Sistema: materia compresa entro una superficie chiusa (ad esempio la superficie interna di un contenitore, ma può essere anche una superficie matematica,
Descrizione macroscopica dei sistemi materiali Sistema: materia compresa entro una superficie chiusa (ad esempio la superficie interna di un contenitore, ma può essere anche una superficie matematica,
FISICA. Termodinamica GAS PERFETTI. Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica
 FISICA Termodinamica GAS PERFETTI Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica SISTEMI, STATI E VARIABILI TERMODINAMICHE Tutto ciò che circonda un sistema, che può influenzare e modificare
FISICA Termodinamica GAS PERFETTI Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica SISTEMI, STATI E VARIABILI TERMODINAMICHE Tutto ciò che circonda un sistema, che può influenzare e modificare
I Gas e Loro Proprietà (II)
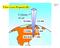 I Gas e Loro Proprietà (II) 2017 10 miles 0.2 atm 4 miles 0.5 atm Sea level 1 atm Dario Bressanini Gas e reazioni chimiche Determinare il volume di CO 2 prodotto a 37 0 C e 1.0 atm quando 5.6 g di glucosio
I Gas e Loro Proprietà (II) 2017 10 miles 0.2 atm 4 miles 0.5 atm Sea level 1 atm Dario Bressanini Gas e reazioni chimiche Determinare il volume di CO 2 prodotto a 37 0 C e 1.0 atm quando 5.6 g di glucosio
Esercizi sui Gas. Insegnamento di Chimica Generale CCS CHI e MAT
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 Un
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 Un
Densita. FLUIDI : liquidi o gas. macroscop.:
 6-SBAC Fisica 1/10 FLUIDI : liquidi o gas macroscop.: microscop.: sostanza che prende la forma del contenitore che la occupa insieme di molecole tenute insieme da deboli forze di coesione (primi vicini)
6-SBAC Fisica 1/10 FLUIDI : liquidi o gas macroscop.: microscop.: sostanza che prende la forma del contenitore che la occupa insieme di molecole tenute insieme da deboli forze di coesione (primi vicini)
Stato Gassoso (cap. 10)
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 08344 - CCS CHI e MAT Stato Gassoso (cap. 10) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 08344 - CCS CHI e MAT Stato Gassoso (cap. 10) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
