Biosensori Sensori Chimici.
|
|
|
- Federigo Palma
- 8 anni fa
- Visualizzazioni
Transcript
1 Biosensori Sensori Chimici
2 Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici per la misura della concentrazione ionica Elettrodi a vetro per la misura della concentrazione di idrogeno (ph) Elettrodi a vetro per la misura delle concentrazioni di sodio e potassio Elettrodi sensibili a anioni e cationi specifici di interesse clinico (Na, K) Misura di gas disciolti nel sangue Misura della pressione parziale di ossigeno (PO 2 ) e anidride carbonica (PCO 2 ) Variabili fondamentali ad uso diagnostico Page 2
3 Brevi Cenni La relazione tra una trasformazione chimica e un movimento di elettroni suggerisce la possibilità di utilizzare questo tipo di reazioni per produrre una corrente elettrica. Questa semplice intuizione, alla fine del 1700, permise allo scienziato italiano Alessandro Volta, che pur ignorava la struttura dell atomo, di costruire il primo apparecchio capace di produrre artificialmente una corrente elettrica, la pila elettrica. La pila di Volta è costituita da una colonna di elementi simili, detti elementi voltaici, impilati appunto uno sopra l altro. Ogni elemento è formato da un disco di rame e uno di zinco e i diversi elementi sono separati tra loro da un disco di cartone o feltro imbevuto di acqua salata o acidulata (in pratica una soluzione elettrolitica). Page 3
4 Principi Elettrochimici Le trasformazioni chimiche mettono in gioco sostanze ma anche energie che si convertono in altre forme nel corso delle reazioni. Le reazioni esotermiche, come le combustioni, trasformano energia chimica in energia termica mentre in quelle endotermiche l energia termica viene assorbita per essere trasformata in energia chimica. Reazioni come la combustione si realizzano con un trasferimento di elettroni da un reagente all altro e, con esso, un trasferimento di energia. Tutte le reazioni in cui si verifica il passaggio di elettroni da una specie (riducente) all altra (ossidante) sono dette di ossido-riduzione o, semplicemente, redox. Page 4
5 Semicella Elettrochimica Elettrodi metallici immersi in una soluzione che contiene ioni dello stesso metallo. Avvengono due tipi di reazione 1. Gli atomi del metallo abbandonano il reticolo cristallino e passano in soluzione sottoforma di ioni positivi, sulla superficie del metallo, in contatto con la soluzione, si forma un accumulo di cariche negative ossidazione + z M M + ze 2. I cationi della soluzione si depositano sulla fase metallica combinandosi con la carica negativa superficiale. Forma ossidata ox + z riduzione + Forma ridotta rx M ze M Si raggiunge (velocemente) una condizione di equilibrio dove la velocità con cui metallo perde cationi che passano in soluzione è uguale a quella con cui gli ioni del metallo in soluzione si depositano sul elettrodo (legandosi alle cariche elettriche negative accumulatesi sulla superficie del metallo). M M + z + ze Page 5
6 Semicella Elettrochimica Consideriamo un sistema semplice costituito da una lamina metallica M immersa in una soluzione molto diluita di un suo sale (M + ). Un sistema di questo tipo costituisce una semicella (o semielemento o più semplicemente elettrodo) All inizio sia il metallo che la soluzione sono elettricamente neutri, dopo il contatto si crea uno squilibrio elettrico: la soluzione assume carica positiva (perché alcuni ioni M+ sono passati in soluzione, mentre la lamina M, che ha trattenuto elettroni, assume carica negativa. Si forma così un doppio strato elettrico, cioè una separazione di carica all interfaccia metallo/soluzione e quindi una differenza di potenziale (d.d.p), fra la lamina e la soluzione, che viene definita potenziale di semicella (o di elettrodo). Page M + M Doppio strato Un sistema di questo genere è detto semicella o elettrodo e la d.d.p. (differenza di potenziale) all interfaccia metallo-soluzione viene detta semplicemente potenziale di elettrodo o potenziale di semicella.
7 Semicella Elettrochimica Equazione di Nernst In elettrochimica, l'equazione di Nernst esprime il potenziale di riduzione (E), relativamente al potenziale di riduzione standard (E 0 ), di un elettrodo o di un semielemento o di una coppia redox di una pila. In altre parole serve per calcolare il potenziale dell'elettrodo in condizioni diverse da quelle standard. riduzione Ox + ne Rx ossidazione RT E = E0 + nf ln v a ox i, ox v a red ired, R è la costante universale dei gas, uguale a J K -1 mol -1 T è la temperatura assoluta in K a i,red è l'attività chimica della specie i-esima in forma ridotta, ovvero a destra della freccia nella semi-reazione di riduzione a i,ox è l'attività chimica della specie i-esima in forma ossidata, ovvero a sinistra della freccia nella semi-reazione di riduzione ν red e ν ox sono i loro coefficienti stechiometrici n è il numero di elettroni trasferiti nella semireazione F è la costante di Faraday, uguale a 96485,309 C mol-1. Page 7 Ossidazione: descrive la perdita di elettroni da una molecola, atomo o ione e quindi aumenta il suo numero di ossidazione. Riduzione: descrive l'acquisizione di elettroni da una molecola, atomo o ione e quindi diminuisce il suo numero di ossidazione. Redox
8 Semicella Elettrochimica E 0 :Potenziale standard dell elettrodo (potenziale standard di riduzione) è una grandezza di fondamentale importanza in elettrochimica. Rappresenta il potenziale assunto da un elettrodo in esame, in condizioni di temperatura e pressione standard (25 C e 1 atm), con attività unitaria delle specie redox, riferito all'elettrodo standard a idrogeno. Dai potenziali standard di riduzione (tabulati), tramite l'equazione di Nernst è possibile risalire al potenziale di cella all'equilibrio, da cui si ottiene il valore del potenziale di cella. L equazione di Nernst permette di risalire al potenziale di elettrodo in condizioni non standard. Per misurare il potenziale di 1/2 cella si usa un elettrodo di riferimento (classicamente di idrogeno) con potenziale nullo per convenzione Potenziali standard sono tabulati relativamente all elettrodo di riferimento Page 8
9 Principi di elettrochimica L equazione di Nernst dipende dall attività (concentrazione) delle specie chimiche. La misura del potenziale può essere utilizzata per risalire a concentrazioni di interesse (metodi potenziometrici). Page 9
10 Metodi potenziometrici La tecnica potenziometrica si basa sulla misura della differenza di potenziale che si instaura tra due semicelle (elettrodi) al fine di determinare la concentrazione di un particolare elettrolita o di seguire l andamento di una titolazione. Gli elettrodi di riferimento hanno il potenziale elettrico perfettamente noto e costante, in questo modo ogni variazione di potenziale del sistema sarà imputabile esclusivamente all elettrodo di misura. Gli elettrodi di misura hanno la caratteristica che il loro potenziale, a temperatura costante, dipende dalla concentrazione di uno solo dei sistemi redox presenti in una soluzione. Page 10
11 Cella elettrochimica Una cella elettrochimica è formata da due semicelle formate da due elettrodi immersi in soluzioni che sono poste in contatto tra loro tramite un setto poroso o un ponte salino (garantisce la continuità elettrica ma non permette agli ioni di passare). Page 11
12 Cella elettrochimica Il potenziale dei due elettrodi è funzione dell attività degli ioni nelle rispettive soluzioni. Se la soluzione di una semicella viene mantenuta a concentrazione costante, il proprio potenziale di semicella resterà costante a una certa temperatura (semicella o elettrodo di riferimento) Il potenziale del secondo elettrodo è funzione dell attività di uno ione in cui è immerso e può essere misurato rispetto a quello della semicella di riferimento. Page 12
13 Esempio: cella di Daniel con e senza ponte salino Page 13
14 Cella di Daniell Una pila dove si verifica un processo in base al quale i cationi rameici si legano spontaneamente all elettrodo di destra, che in questo modo si polarizza positivamente, e gli ioni zinco si staccano spontaneamente dall elettrodo di sinistra che si polarizza negativamente, è possibile misurare (strumento di misura voltmetro) una differenza di potenziale che a circuito aperto, viene detta anche forza elettromotrice (f.e.m.). Quando si chiude il circuito si genera una corrente di elettroni che va dall elettrodo di sinistra a quello di destra e in soluzione una corrente di anioni che si muove dalla semicella di destra a quella di sinistra e una corrente di cationi che si muove in senso inverso. Con il procedere della reazione elettrochimica la concentrazione della soluzione rameica diminuisce, quella della soluzione di zinco aumenta mentre la differenza di potenziale diminuisce e tende a zero. La forza elettromotrice è data da: Page 14» E = Ec Ea dove Ec e Ea indicano i potenziali del catodo e dell anodo
15 Esempio: Cella di Daniel con e senza ponte salino Dai tabulati sulle tensioni di riduzione standard riduzione Zn e """"" " Zn ossidazione riduzione Cu e """"" " Cu ossidazione! E = # E " Page E Cu 2+ /Cu 0.34V Cu 2+ /Cu ( ) $! & # E % " RT ( a 2F ln Zn 2+ * * a ) Cu 2+ + RT 2F ln a Cu 2+ 0 E Zn 2+ /Zn V + RT 2F ln ( a ) $ Zn 2+ & = % + ( - RT a + = F ln Zn 2+ * - * a -, ) Cu 2+, Zn 2+ /Zn
16 La misurazione elettrochimica dell attività ionica fa uso principalmente di due elettrodi: indicatore e riferimento. Il primo risponde in maniera nota e riproducibile a variazioni dell attività ionica. Il secondo garantisce la continuità elettrica alla soluzione sotto esame (chiusura circuito). Le qualità che vengono richieste agli elettrodi di riferimento sono: 1.reversibilità 2.riproducibilità 3.stabilità Il grado di reversibilità peggiora all aumentare della densità di corrente che attraversa la superficie dell elettrodo (danneggiamento dell elettrodo per over-voltage). Riproducibilità: elettrodi con proprietà elettrochimiche simili, capacità di rispondere a variazioni di concentrazione e di temperatura senza isteresi (processo di fabbricazione). La stabilità: proprietà di un elettrodo invariate nel corso di una misurazione di lunga durata. In queste condizioni, la maggior parte degli elettrodi subisce un avvelenamento Possibile via d uscita : Accoppiare l elettrodo alla soluzione mediante un ponte salino che previene l inquinamento dell elettrodo. Page 16 Elettrodi di riferimento
17 Elettrodi di riferimento Gli elettrodi di riferimento devono essere il più possibile non polarizzabili: se fossero polarizzabili il loro potenziale di elettrodo dipenderebbe dalle condizioni esterne e non dalle sole proprietà dell interfaccia (attività ionica nota, temperatura) Condizione voluta: R->0 Elettrodi seconda specie : caratterizzati da bassa resistenza dovuta alla cinetica di trasferimento elettronico estremamente rapida. Elettrodo Ag/Cl Elettrodo metallo/ossido metallo Page 17
18 Possibili applicazioni della cella elettrochimica Misure di ph Elettrodi metallo/ossido metallo Elettrodi a vetro Misure di Ioni in Soluzione Misure di Sodio e Potassio Elettrodi a membrana Elettrodi ionoselettivi in Medicina Elettrodo per la misura del potassio nel sangue Elettrodi per la misurazione del calcio Page 18
19 Misure ph Misura del grado di acidità di una soluzione Fondamentale importanza in biochimica In acqua pura l attività degli ioni H + e OH - sono uguali, reazione di equilibrio (costante equilibrio K)! H + $ " H2O + H + OH "# %& OH % #$ &' K = Acqua poco dissociata (denominatore costante)!h " 2 O# $ 2! K w = H "# + $ " %& #$ OH % &' =10 14 M 2 Se è aggiunto un acido [H + ] cresce e [OH - ] diminuisce mantenendo costante K w ph = log( a ) H + Page 19! H "# + $ %& = " #$ OH % &' =10 7 ( ( ph = 7 Acqua pura ph <7 acido ph >7 base
20 Misure ph in fluidi biologici Molti dei processi naturali sono altamente dipendenti dal ph. Per gli organismi viventi è essenziale che il ph dei fluidi biologici sia mantenuto all interno di un range molto ristretto. Nei liquidi fisiologici umani, sangue e liquido extracellulare, il ph deve necessariamente essere compreso tra 7 e 8 (normalmente ph = 7.4), altrimenti si ha il decesso del soggetto. I meccanismi grazie ai quali l organismo riesce a bilanciare eventuali squilibri sono essenzialmente tre: Meccanismi Chimici : Sistemi Tampone (intervento in alcuni secondi); Meccanismo Respiratorio : variazione di frequenza e profondità di respirazione (intervento in qualche minuto); Meccanismo Renale : filtraggio ematico (intervento in ore o giorni); Page 20
21 Esempio: strumento per la misura del ph tramite elettrodo Sb/Sb 2 O 3! Concentrazione nota di Cl - Page 21
22 Elettrodo metallo/ossido metallo Elettrodi costituiti da un metallo ricoperto da un suo ossido. Sono da considerarsi un caso particolare di elettrodi di seconda specie (dove il sale poco solubile è l ossido stesso). La parte anionica del sale insolubile è presente nell equazione di dissociazione del solvente (H 2 O) Possono essere usati come sensori di ph Esempio Elettrodo Antimonio (Sb) / Ossido di Antimonio (Sb 2 O 3 ) Reazione: Sb 2 O 3 +6 H + +6e - -> 2Sb+3H 2 O E = E 0 (Sb 2 O 3 /Sb) + R T 6 F ln [H + ] 6 ( ) = E 0 (Sb 2 O 3 /Sb) R T 6 F log [H + ] 6 ( ) = = E R T (Sb 2 O 3 /Sb) F log ( [H + ]) = E R T (Sb 2 O 3 /Sb) F ph Page 22 E 0 (Sb 2 O 3 /Sb) = 0.152V ph = log" # H + $ % Questo potenziale di semicella va misurato Rispetto a un elettrodo di riferimento
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
Biosensori Sensori Chimici. Alessandro Tognetti
 Biosensori Sensori Chimici Alessandro Tognetti Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici per la misura
Biosensori Sensori Chimici Alessandro Tognetti Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici per la misura
ELETTROCHIMICA. Uso di reazioni chimiche per produrre corrente elettrica (Pile)
 ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
Elettrochimica. 1. Celle elettrolitiche. 2. Celle galvaniche o pile
 Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
CENNI DI ELETTROCHIMICA
 CENNI DI ELETTROCHIMICA Gli elettrodi a membrana sono elettrodi che permettono la determinazione rapida e selettiva, per potenziometria diretta, di numerosi cationi ed anioni. Il meccanismo di formazione
CENNI DI ELETTROCHIMICA Gli elettrodi a membrana sono elettrodi che permettono la determinazione rapida e selettiva, per potenziometria diretta, di numerosi cationi ed anioni. Il meccanismo di formazione
Celle a combustibile Fuel cells (FC)
 Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
ELETTROCHIMICA. Celle Galvaniche o Pile
 ELETTROCHIMICA Le reazioni di ossido-riduzione (redox) ci tengono in vita. Esse, ad esempio, si svolgono nei processi estremamente importanti che catturano l energia solare tramite la fotosintesi o in
ELETTROCHIMICA Le reazioni di ossido-riduzione (redox) ci tengono in vita. Esse, ad esempio, si svolgono nei processi estremamente importanti che catturano l energia solare tramite la fotosintesi o in
Storia dei generatori di tensione e della corrente elettrica
 Storia dei generatori di tensione e della corrente elettrica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia 1778 Alessandro Volta, in analogia al potenziale gravitazionale definito
Storia dei generatori di tensione e della corrente elettrica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia 1778 Alessandro Volta, in analogia al potenziale gravitazionale definito
Tesina di scienze. L Elettricità. Le forze elettriche
 Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
SISTEMI ELETTROCHIMICI
 Università degli studi di Palermo SISTEMI ELETTROCHIMICI Dott. Ing. Serena Randazzo Dipartimento di Ingegneria Chimica, Gestionale, Informatica e Meccanica OUTLINE 1) Introduzione sui sistemi elettrochimici
Università degli studi di Palermo SISTEMI ELETTROCHIMICI Dott. Ing. Serena Randazzo Dipartimento di Ingegneria Chimica, Gestionale, Informatica e Meccanica OUTLINE 1) Introduzione sui sistemi elettrochimici
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
OSSIDORIDUZIONI N H H. H ammoniaca. acido nitroso N = + 3. acido nitrico N = + 5
 OSSIDORIDUZIONI Le reazioni acido-base sono quelle in cui viene scambiato, fra due specie reagenti, un H. Come si è visto, esistono casi di reazioni acido-base in cui ciò non avviene (definizione di Lewis),
OSSIDORIDUZIONI Le reazioni acido-base sono quelle in cui viene scambiato, fra due specie reagenti, un H. Come si è visto, esistono casi di reazioni acido-base in cui ciò non avviene (definizione di Lewis),
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria
 Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
La serie elettrochimica dei potenziali standard di riduzione (25 C)
 MIGLIORI RIDUCENTI MIGLIORI OSSIDANTI La serie elettrochimica dei potenziali standard di riduzione (25 C) ELETTROLISI Una cella elettrolitica è una cella nella quale una corrente fa avvenire una reazione
MIGLIORI RIDUCENTI MIGLIORI OSSIDANTI La serie elettrochimica dei potenziali standard di riduzione (25 C) ELETTROLISI Una cella elettrolitica è una cella nella quale una corrente fa avvenire una reazione
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
Cu 2+ ) + Zn(s) potere ossidante. potere ossidante. Cu 2+ Cu. Zn 2+ Consideriamo le due reazioni di ossido-riduzione:
 Elettrochimica Consideriamo le due reazioni di ossido-riduzione: Cu(s) ) + Zn 2+ 2+ (aq aq) Cu Cu 2+ 2+ (aq) + ) + Zn(s) Cu 2+ 2+ (aq) + ) + Zn(s) Cu(s) ) + Zn 2+ 2+ (aq) Cu Zn Zn 2+ Cu 2+ Cu potere ossidante
Elettrochimica Consideriamo le due reazioni di ossido-riduzione: Cu(s) ) + Zn 2+ 2+ (aq aq) Cu Cu 2+ 2+ (aq) + ) + Zn(s) Cu 2+ 2+ (aq) + ) + Zn(s) Cu(s) ) + Zn 2+ 2+ (aq) Cu Zn Zn 2+ Cu 2+ Cu potere ossidante
IMMAGAZZINARE ENERGIA: GLI ACCUMULATORI ELETTROCHIMICI Prof. Nerino Penazzi
 IMMAGAZZINARE ENERGIA: GLI ACCUMULATORI ELETTROCHIMICI Prof. Nerino Penazzi Di cosa parleremo questa sera: Cos è un accumulatore di energia elettrica Pile e altro Comportamento di un buon accumulatore
IMMAGAZZINARE ENERGIA: GLI ACCUMULATORI ELETTROCHIMICI Prof. Nerino Penazzi Di cosa parleremo questa sera: Cos è un accumulatore di energia elettrica Pile e altro Comportamento di un buon accumulatore
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
DIPARTIMENTO DI SCIENZE INTEGRATE CHIMICA FISICA SCIENZE DELLA TERRA - BIOLOGIA
 IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
Chimica. Ingegneria Meccanica, Elettrica e Civile Simulazione d'esame
 Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Elettrolisi del solfato di rame
 Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
MPT Capitolo 12 Redox. Le ossidoriduzioni. Obiettivo. Definizioni di ossidazione e di riduzione
 1 Le ossidoriduzioni Obiettivo In questo capitolo svilupperemo i concetti fondamentali delle reazioni di ossido-riduzione. Si tratta di conoscenze fondamentali sia per la vita comune, sia, per molti di
1 Le ossidoriduzioni Obiettivo In questo capitolo svilupperemo i concetti fondamentali delle reazioni di ossido-riduzione. Si tratta di conoscenze fondamentali sia per la vita comune, sia, per molti di
Corrente elettrica. Esempio LA CORRENTE ELETTRICA CONTINUA. Cos è la corrente elettrica? Definizione di intensità di corrente elettrica
 Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Bioelettrodi. Elettrodi e pricipi di elettrochimica
 Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto:
 Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
SENSORI E TRASDUTTORI
 SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014. Prof.ssa Piacentini Veronica
 Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014 Prof.ssa Piacentini Veronica La corrente elettrica La corrente elettrica è un flusso di elettroni
Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014 Prof.ssa Piacentini Veronica La corrente elettrica La corrente elettrica è un flusso di elettroni
Le reazioni di ossidoriduzione (redox)
 Le reazioni di ossidoriduzione (redox) Reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida(funge da riducente) cede elettroni ed aumenta
Le reazioni di ossidoriduzione (redox) Reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida(funge da riducente) cede elettroni ed aumenta
Universita Degli Studi Di Roma La Sapienza Corso di Laurea Magistrale in Scienze e Tecnologie per la conservazione dei Beni Culturali A.A.
 Universita Degli Studi Di Roma La Sapienza Corso di Laurea Magistrale in Scienze e Tecnologie per la conservazione dei Beni Culturali A.A. 2011-2012 Esame di: Laboratorio di Chimica del Restauro PhD M.P.
Universita Degli Studi Di Roma La Sapienza Corso di Laurea Magistrale in Scienze e Tecnologie per la conservazione dei Beni Culturali A.A. 2011-2012 Esame di: Laboratorio di Chimica del Restauro PhD M.P.
Esercizi di Chimica (2 a prova in itinere)
 Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
Prova Parziale 1 Corso di Biosensori - Ing. Mazzei (22 Aprile 2013)
 Prova Parziale 1 Corso di Biosensori - Ing. Mazzei (22 Aprile 2013) Esercizio 1 Considerando la seguente tabella riportante i dati raccolti per la taratura di un sensore di temperatura. Si determini: -
Prova Parziale 1 Corso di Biosensori - Ing. Mazzei (22 Aprile 2013) Esercizio 1 Considerando la seguente tabella riportante i dati raccolti per la taratura di un sensore di temperatura. Si determini: -
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Dipendenza della Solubilità dalla temperatura
 SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
ENERGIA NELLE REAZIONI CHIMICHE
 ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
CORRENTE ELETTRICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V 2 isolati tra loro V 2 > V 1 V 2
 COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
Componenti elettronici. Condensatori
 Componenti elettronici Condensatori Condensatori DIELETTRICO La proprietà fondamentale del condensatore, di accogliere e di conservare cariche elettriche, prende il nome di capacità. d S C = Q V Q è la
Componenti elettronici Condensatori Condensatori DIELETTRICO La proprietà fondamentale del condensatore, di accogliere e di conservare cariche elettriche, prende il nome di capacità. d S C = Q V Q è la
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
LEZIONE 12. Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA. Scaricato da Sunhope.it
 LEZIONE 12 Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA Idrolisi salina Per IDROLISI SALINA si intende il fenomeno per il quale la dissoluzione in acqua di
LEZIONE 12 Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA Idrolisi salina Per IDROLISI SALINA si intende il fenomeno per il quale la dissoluzione in acqua di
L elettrochimica: le pile e l elettrolisi
 1 ESPANSIONE 7.2 L elettrochimica: le pile e l elettrolisi Ambra del Baltico contenente insetti. Fin dall antichità si conoscevano le particolari proprietà dell ambra, una resina fossile che se strofinata
1 ESPANSIONE 7.2 L elettrochimica: le pile e l elettrolisi Ambra del Baltico contenente insetti. Fin dall antichità si conoscevano le particolari proprietà dell ambra, una resina fossile che se strofinata
Corrente ele)rica. Cariche in movimento e legge di Ohm
 Corrente ele)rica Cariche in movimento e legge di Ohm Corrente ele)rica Nei metalli si possono avere elettroni che si muovono anche velocemente fra un estremo e l altro del metallo, ma la risultante istante
Corrente ele)rica Cariche in movimento e legge di Ohm Corrente ele)rica Nei metalli si possono avere elettroni che si muovono anche velocemente fra un estremo e l altro del metallo, ma la risultante istante
funzionamento degli accumulatori al piombo/acido.
 Il triangolo dell Incendio Possibili cause d incendio: I carrelli elevatori Particolare attenzione nella individuazione delle cause di un incendio va posta ai carrelli elevatori, normalmente presenti nelle
Il triangolo dell Incendio Possibili cause d incendio: I carrelli elevatori Particolare attenzione nella individuazione delle cause di un incendio va posta ai carrelli elevatori, normalmente presenti nelle
Inizia presentazione
 Inizia presentazione Che si misura in ampère può essere generata In simboli A da pile dal movimento di spire conduttrici all interno di campi magnetici come per esempio nelle dinamo e negli alternatori
Inizia presentazione Che si misura in ampère può essere generata In simboli A da pile dal movimento di spire conduttrici all interno di campi magnetici come per esempio nelle dinamo e negli alternatori
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI
 DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
AUTODIFFUSIONE Autodiffusione
 DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni
 Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni Una delle più importanti proprietà di una soluzione acquosa è la sua concentrazione di ioni idrogeno. Lo ione H + o
Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni Una delle più importanti proprietà di una soluzione acquosa è la sua concentrazione di ioni idrogeno. Lo ione H + o
Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s.
 Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s. 2015-2016 Mondovi 05/11/2015 Prof. Giancarlo Cardone PROGRAMMAZIONE DELL ATTIVITA
Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s. 2015-2016 Mondovi 05/11/2015 Prof. Giancarlo Cardone PROGRAMMAZIONE DELL ATTIVITA
La corrente elettrica
 PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
Prevenzione della Corrosione
 DL MK1 BANCO DI LAVORO PER LA PROTEZIONE CATODICA La Protezione Catodica è una tecnica di controllo della corrosione di una superficie metallica facendola funzionare come il catodo di una cella elettrochimica.
DL MK1 BANCO DI LAVORO PER LA PROTEZIONE CATODICA La Protezione Catodica è una tecnica di controllo della corrosione di una superficie metallica facendola funzionare come il catodo di una cella elettrochimica.
TERMODINAMICA DI UNA REAZIONE DI CELLA
 TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TRASDUTTORI di FORZA E PRESSIONE
 Fra i trasduttori di forza, gli estensimetri, o stain gage, si basano sull aumento di resistenza che si produce in un filo metallico sottoposto a trazione a causa dell aumento di lunghezza e della contemporanea
Fra i trasduttori di forza, gli estensimetri, o stain gage, si basano sull aumento di resistenza che si produce in un filo metallico sottoposto a trazione a causa dell aumento di lunghezza e della contemporanea
Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio,
 Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio, quasi mai) si può parlare di H 2 O molecolare; piuttosto
Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio, quasi mai) si può parlare di H 2 O molecolare; piuttosto
Le reazioni di ossidoriduzione
 I.S. G. TASSINARI PROGRAMMAZIONE di CHIMICA ANALITICA E STUMENTALE Classe 4L - A.S. 2015-16 Docenti: prof.ssa Stefania Comes- prof.ssa Anna Alfano ANALISI INIZIALE DELLA CLASSE: La classe risulta composta
I.S. G. TASSINARI PROGRAMMAZIONE di CHIMICA ANALITICA E STUMENTALE Classe 4L - A.S. 2015-16 Docenti: prof.ssa Stefania Comes- prof.ssa Anna Alfano ANALISI INIZIALE DELLA CLASSE: La classe risulta composta
1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore.
 ESERCIZI pag: 458 1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore. 2. Una dinamo produce 6 amp a 160 v. Calcolare
ESERCIZI pag: 458 1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore. 2. Una dinamo produce 6 amp a 160 v. Calcolare
CO 2 aq l anidride carbonica disciolta, reagendo con l'acqua, forma acido carbonico secondo la reazione:
 DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE
 REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE OSSIDORIDUTTIVA SECONDO IL METODO DELLO IONE-ELETTRIONE. 1) Si individuano le coppie di atomi il cui numero di ossidazione cambia
REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE OSSIDORIDUTTIVA SECONDO IL METODO DELLO IONE-ELETTRIONE. 1) Si individuano le coppie di atomi il cui numero di ossidazione cambia
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
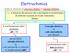 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Pile e accumulatori. Approfondimento. "" Pile e vita quotidiana. Capitolo. elettrolisi e le leggi di Faraday
 Capitolo Approfondimento elettrochimiche elettrolisi e le leggi di Faraday 14Le3. Ltrasformazioni Pile e accumulatori Pile e vita quotidiana Un applicazione importante delle celle elettrochimiche è il
Capitolo Approfondimento elettrochimiche elettrolisi e le leggi di Faraday 14Le3. Ltrasformazioni Pile e accumulatori Pile e vita quotidiana Un applicazione importante delle celle elettrochimiche è il
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di
 La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
Concetti fondamentali su acidità e basicità delle soluzioni acquose
 Concetti fondamentali su acidità e basicità delle soluzioni acquose Le molecole H 2 O dell acqua liquida pura possono andare incontro a dissociazione. Il processo può essere descritto come una reazione
Concetti fondamentali su acidità e basicità delle soluzioni acquose Le molecole H 2 O dell acqua liquida pura possono andare incontro a dissociazione. Il processo può essere descritto come una reazione
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
IMPIANTI DI TERRA Appunti a cura dell Ing. Emanuela Pazzola Tutore del corso di Elettrotecnica per meccanici, chimici e biomedici A.A.
 IMPIANTI DI TERRA Appunti a cura dell Ing. Emanuela Pazzola Tutore del corso di Elettrotecnica per meccanici, chimici e biomedici A.A. 2005/2006 Facoltà d Ingegneria dell Università degli Studi di Cagliari
IMPIANTI DI TERRA Appunti a cura dell Ing. Emanuela Pazzola Tutore del corso di Elettrotecnica per meccanici, chimici e biomedici A.A. 2005/2006 Facoltà d Ingegneria dell Università degli Studi di Cagliari
BILANCI DI ENERGIA. Capitolo 2 pag 70
 BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ
 Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
STATO LIQUIDO. Si definisce tensione superficiale (γ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Bioelettrodi. Elettrodi e pricipi di elettrochimica
 Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Elettricità e magnetismo
 E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
MISURE DI POTERE CALORIFICO E COMPOSIZIONE
 MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
Classificazione dei Sensori. (raccolta di lucidi)
 Classificazione dei Sensori (raccolta di lucidi) 1 Le grandezze fisiche da rilevare nei processi industriali possono essere di varia natura; generalmente queste quantità sono difficili da trasmettere e
Classificazione dei Sensori (raccolta di lucidi) 1 Le grandezze fisiche da rilevare nei processi industriali possono essere di varia natura; generalmente queste quantità sono difficili da trasmettere e
Bioelettrodi. Elettrodi e pricipi di elettrochimica
 Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Si classifica come una grandezza intensiva
 CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente
 Unità G16 - La corrente elettrica continua La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente 1 Lezione 1 - La corrente elettrica
Unità G16 - La corrente elettrica continua La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente 1 Lezione 1 - La corrente elettrica
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
Bioingegneria Elettronica I
 Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
Cenni sui trasduttori. Con particolare attenzione al settore marittimo
 Cenni sui trasduttori Con particolare attenzione al settore marittimo DEFINIZIONI Un Trasduttore è un dispositivo che converte una grandezza fisica in un segnale di natura elettrica Un Sensore è l elemento
Cenni sui trasduttori Con particolare attenzione al settore marittimo DEFINIZIONI Un Trasduttore è un dispositivo che converte una grandezza fisica in un segnale di natura elettrica Un Sensore è l elemento
CHIMICA GENERALE MODULO
 Corso di Scienze Naturali CHIMICA GENERALE MODULO 6 Termodinamica Entalpia Entropia Energia libera - Spontaneità Relatore: Prof. Finelli Mario Scienza che studia i flussi energetici tra un sistema e l
Corso di Scienze Naturali CHIMICA GENERALE MODULO 6 Termodinamica Entalpia Entropia Energia libera - Spontaneità Relatore: Prof. Finelli Mario Scienza che studia i flussi energetici tra un sistema e l
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Perché il logaritmo è così importante?
 Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
Selezione test GIOCHI DELLA CHIMICA
 Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
