DIGESTIONE delle PROTEINE
|
|
|
- Diana Lanza
- 4 anni fa
- Visualizzazioni
Transcript
1 DIGESTIONE delle PROTEINE ASSORBIMENTO DEGLI AMMINOACIDI Alessandra Bulbarelli
2 PROTEINE: componente importante dell alimentazione umana. dalle proteine otteniamo aminoacidi ( mattoni per la costruzione di nuove proteine). ingeriamo proteine per scomporle e formarne altre. gli aminoacidi sono anche associati alla formazione di glucosio, neurotrasmettitori o ormoni. MOLECOLE CHE DERIVANO DAGLI AA Porfirine eme glicina Nucleotidi purinici pirimidinici asp, gly, gln asp, gln AMMINE BIOGENE dopammina noradrenalina tirosina adrenalina GABA serotonina istamina glutammato triptofano istidina
3 Assumere proteine tramite gli alimenti permette di assumere aminoacidi ESSENZIALI.. Aminoacidi essenziali : Valina, Leucina, Isoleucina, Treonina, Metionina; Fenilalanina; Triptofano, Lisina, Istidina (*), Arginino (*) (*)= semiessenziali Aminoacidi non essenziali : Glicina, Alanina, Serina, Acido aspartico, Acido glutammico, Prolina, Idrossiprolina, Cisteina *semiessenziali: prodotti in quantità NON adeguata al fabbisogno un alimento non può contenere quantità sufficienti di tutti gli aminoacidi essenziali di cui necessitiamo un alimentazione varia, permette di combinare le diverse quantità di aminoacidi contenute nei vari alimenti.
4 VALORE BIOLOGICO: capacità di una proteina (o alimento) di fornire aminoacidi essenziali = una scala che va da 0 a 100, indica la quantità e la varietà di aminoacidi essenziali contenuti in una proteina. Valore vicino al 100 per uova o alcuni tipi di carne. Valori biologici bassi (0-20) per proteine vegetali (perché mancano di alcuni aminoacidi essenziali. Cereali e legumi, presi singolarmente hanno un valore biologico molto scarso (10-20) perché mancano rispettivamente di lisina e metionina Strategia: combinati insieme (nella pasta e fagioli, per esempio) compensano le rispettive mancanze arrivando ad un valore biologico molto alto). 2 porzioni di Pasta e fagioli (700 kcal),oppure una piccola fettina di carne magra da 70 gr (77 kcal circa). Seguendo una dieta a base di vegetali che soddisfi il fabbisogno amminoacidico giornaliero può contribuire ad assumere quantità elevate di calorie.
5 Digestione delle proteine 2 fasi: 1) Stomaco 2) Intestino Partecipano enzimi derivanti da organi diversi (stomaco, pancreas, intestino) attivi solo nel canale digerente per evitare l autodigestione. SINTETIZZATI SOTTO FORMA DI PRECURSORI INATTIVI ATTIVATI NEL TRATTO DIGERENTE.
6 GASTRINA Ormone polipeptidico secreto da cellule G (mucosecernenti della mucosa gastrica dell antro pilorico e del duodeno). La GASTRINA stimola le cellule parietali dello stomaco alla secrezione di acido cloridrico
7 DIGESTIONE PROTEICA (fase1) STOMACO PROTEASI GASTRICHE PEPSINOGENO (precursore pepsina) ph=2 (HCl) PEPSINA idrolizza i legami peptidici delle proteine, rompendoli. Trasforma le proteine in polipeptidi (Polipeptide < 40 aminoacidi, Proteina > 40 aminoacidi). PEPSINA forma attiva Il Ph del lume gastrico: Denatura le proteine ( distruzione ponti S-S e legami-h) è tossico nei confronti di batteri e microorganmismi
8 PEPSINA PEPSINA idrolizza anche pepsinogeno a dare nuova pepsina solo le prime molecole di pepsinogeno sono attivate dall HCl. Agisce su aa aromatici enzima non essenziale individui che ne sono carenti sono perfettamente in grado di fare digestione.
9 FASE 2 PIÙ IMPORTANTE Intestino enzimi idrolitici prodotti dal pancreas in forma di precursori inattivi: 1) TRIPSINOGENO si trasforma poi in tripsina grazie alla enteropeptidasi, (enzima prodotto dalle cellule intestinali). Enteropeptidasi legata alla membrana
10 ENZIMI DIGESTIVI PROTEASI PANCREATICHE prime molecole di tripsina idrolizzano esse stesse altro tripsinogeno in tripsina che agisce poi su: Procarbossipeptidasi A e B carbossipeptidasi A e B proelastasi elastasi ENZIMI ATTIVI chimotripsinogeno chimotripsina Questi enzimi digestivi trasformano i polipeptidi in peptidi, non in aa.
11 ENZIMI DIGESTIVI PROTEASI INTESTINALI AMMINOPEPTIDASI DIPEPTIDASI enzimi prodotti dalla mucosa intestinale Digeriscono i polipeptidi in AMINOACIDI LIBERI il nostro corpo non può assorbire proteine intere o polipeptidi Primi 2 giorni di vita: assorbimento intestinale di proteine intere arricchite di immunoglobuline materne sostegno del sistema immunitario ancora immaturo.
12 PATOLOGIE: CELIACHIA intolleranza permanente al glutine, proteina ricca di prolina e acido glutammico presente in avena, frumento, farro, orzo, ecc Assorbimeno di polipeptidi del glutine generati da pepsina e tripsina che inducono infiammazione e risposta anticorpale: reazione immunitaria dell'intestino tenue danno tissutale alla mucosa intestinale, atrofia villi intestinali, malassorbimento.
13 ENZIMI DIGESTIVI PROTEASI PANCREATICHE
14 LA DIGESTIONE DELLE PROTEINE
15 1 2 BIOSINTESI PROTEICA 4 vena porta 5 6 3
16 TRASPORTO degli aminoacidi Per entrare nei tessuti gli aminoacidi necessitano di trasportatori. Molecole proteiche integrali di membrana. Gli aa, grazie ai trasportatori entrano in cellula in favore di gradiente. 5 CLASSI PRINCIPALI: 1) Trasportatori di aminoacidi neutri piccoli 2) Trasportatori di aminoacidi neutri grandi 3) Trasportatori di aminoacidi acidi 4) Trasportatori di aminoacidi basici 5) Trasportatori di lisina e prolina
17 TRASPORTO AA Assorbiti dall intestino circolazione vena porta fegato SINTESI PROTEICA Le nuove proteine così formate rientrano nel circolo ed arrivano ai vari tessuti.
18
19 Gli aminoacidi, derivati dalla degradazione delle proteine della dieta o delle proteine intracellulari rappresentano l ultima classe di biomolecole la cui ossidazione contribuisce alla generazione di energia metabolica nella cellula
20 DEGRADAZIONE OSSIDATIVA DEGLI AA Gli aminoacidi sono degradati se: Non sono necessari per la sintesi di nuove proteine. La dieta è ricca di proteine e gli aminoacidi sono in eccesso rispetto alle richieste biosintetiche. Durante il digiuno o nel diabete mellito quando non sono disponibili i carboidrati.
21 POOL di AMMINOACIDI
22
23 POOL di AMMINOACIDI
24 TURN-OVER DI PROTEINE ENDOGENE Avviene ad opera di sistemi specializzati: A) MECCANISMO LISOSOMIALE (degradazione non selettiva. Proteine di membrana, extracellulari con emivita lunga) B) MECCANISMO CITOPLASMATICO ATP-DIPENDENTE (degradazione altamente selettiva, PROTEASOMA ) Tre funzioni importanti: -fornisce aminoacidi -rimuove proteine anomale -rimuove enzimi e fattori trascrizionali in eccesso (regolazione del metab.) Le proteine difettose sono degradate più rapidamente
25 Lys UBIQUITINAZIONE
26 Ubiquitina UBIQUITINAZIONE L ubiquitina è una piccola proteina di struttura globulare di 76 amminoacidi, 8.5 KDa E una proteina altamente termo-stabile E caratteristica di tutte le cellule eucariotiche, altamente conservata; l identità di sequenza tra l ubiquitina umana e quella di lievito è pari all 87%
27 Il PROTEASOMA è una proteasi ATP dipendente, molto abbondante (quasi l 1% delle proteine cellulari) CAPPUCCIO: subunità 19 s BARILE: subunità 20 s CAPPUCCIO: subunità 19 s I siti attivi del proteasoma si affacciano nella camera proteolitica interna (BARILE). I CAPPUCCI agiscono da cancelli regolati per l ingresso della proteina nella camera interna.
28 La proteina poliubiquitinata riconosciuta dal cappuccio del proteasoma, rimuove la poli-ubiquitina (verrà riciclata) e successivamente trasloca la proteina verso la camera interna dove sarà digerita Il processo di traslocazione è ATP dipendente. Una classe di proteine del cappuccio (unfoldase) promove lo svolgimento delle proteine
29
30 SISTEMA DI CONIUGAZIONE DELL UBIQUITINA L ubiquitina viene attivata mediante formazione di legame tio-estere tra il gruppo COOH dell ubiquitina ed una cisteina dell enzima E1 (enzima attivatore dell ubiquitina) in modo ATP-dipendente E1-Ubiquitina lega lega il complesso E2-E3 e trasferisce l ubiquitina ad E2 (enzima che coniuga l ubiquitina)
31 E3 (Ubiquitina ligasi) lega la poteina target (proteina che deve essere ubiquitinata) e catalizza l aggiunta dell ubiquitina al gruppo amminico epsilon (laterale) della lisina La proteina target può essere mono-ubiquitinata o poli-ubiquitinata. Nel caso di poli-ubiquitinazione, E2-E3 continuano a legare la proteina target e nuovi E1-Ubiquitina interverranno nel processo
32 LE PROTEINE POSSONO ESSERE MONO- O POLI- UBIQUITINATE La mono-ubiquitinazione è coinvolta in vari processi come trascrizione, funzione degli istoni, endocitosi, traffico vescicolare La poly-ubiquitinazione può essere al livello delle lisine 48, 11 o 29 (coinvolta nella degradazione delle proteine tramite proteasoma) La poly-ubiquitinazione può essere al livello delle lisine 63 (meccanismi di riparo del DNA, risposta a stress, trasduzione del segnale)
33 POLI- UBIQUITINAZIONE Degradazione nel proteasoma
34 POOL di AMMINOACIDI
35 catabolismo aminoacidico TRANSAMINAZIONE DEAMINAZIONEDE CARBOSSILAZIONE
36 TRANSAMINAZIONE Le transaminazioni, consentono l interconversione di quasi tutti gli aa (tranne lys e thr ), bilanciando il pool di aa in base alla richiesta. Nel loro insieme tendono a convogliare il gruppo aminico degli amino acidi sull a-chetoglutarato (accettore) per formare glutammato. Enzimi coinvolti: TRANSAMINASI. Altri α-chetoacidi sono piruvato e ossalacetato trasferimento del gruppo α-amminico dell aa sull α- chetoglutarato: si ottiene un α- chetoacido + glutammato PALP (piridossale fosfato) PALP (da VIT B6): permette lo spostamento del gruppo amminico dall aminoacido all αchetoacido.
37 Esempio: elevata concentrazione di alanina, bassa concentrazione di aspartato ALT alanina transaminasi AST aspartico transaminasi Queste reazioni sono reversibili: Keq prossime all unità, la loro direzione si sposta in funzione della concentrazione dei reagenti: REAZIONI a «PING-PONG» La presenza fissa della coppia alfa-chetoglutarato glutamato consente di spostare il gruppo aminico distribuendolo fra i vari aminoacidi, mantenendo equilibrato, per le necessità cellulari, il pool aminoacidico.
38 Transaminazione La maggior parte delle transaminasi utilizza come chetoacido Alfa-chetoglutarato Glutammato Biosintesi AA Via anabolica Deaminazione ossidativa NH 3 urea Via catabolica
39 ALT (alanina transaminasi) o GPT (transaminasi glutammico-piruvico) AST (aspartico transaminasi) o GOT (transaminasi glutammico-ossalacetico ENZIMI tra i più utilizzati nei test clinici per di danno cellulare. ALT localizzato principalmente nelle cellule epatiche rilasciato in caso di rottura parete cellulare indicatore abbastanza specifico di danno epatico AST particolarmente concentrato in mitocondri delle tessuto muscolare e cardiaco. cellule epatiche e del
40 DEAMINAZIONE RIMOZIONE DELL AZOTO AA (fegato e reni) formazione di ammoniaca + acido. Può essere OSSIDATIVA o NON OSSIDATIVA A) DEAMINAZIONE OSSIDATIVA Enzima:GLU-DEIDROGENASI: catalizza il passaggio da glutammato ad α-chetoglutarato. FLAVIN MONONUCLEOTIDE GLUTAMMATO GLUTAMMATO DEIDROGENASI Sintesi urea Per altri aa serve accoppiare la transaminazione
41 Glutammato deidrogenasi Costituisce il principale processo di formazione dell ammoniaca (nei mitocondri): P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 La glutammico deidrogenasi (PM ; 6 subunità uguali) è presente nella matrice mitocondriale Glutammico deidrogenasi -> enzima allosterico Attivato -> ADP GDP carica energetica bassa Inibito -> ATP GTP carica energetica alta
42
43 DEAMINAZIONE B) DEAMINAZIONE NON OSSIDATIVA solo per serina e treonina VIT B6 NH 3 CICLO DELL UREA
44
45 Deaminazione non ossidativa
46 DECARBOSSILAZIONE terza via del catabolismo aa consiste nella sottrazione del gruppo carbossilico formazione di ammine piridossale fosfato (PALP) Le ammine, che per azione di specifiche DECARBOSSILAI, derivano dalla decarbossilazione degli aa sono le AMMINE BIOGENE hanno una importante azione biologica: Glut GABA Phe adrenalina, noradrenalina Ser colina, acetilcolina Hist istamina (vasodilatatore)
47
Catabolismo di proteine
 Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine
 Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Digestione delle proteine e assorbimento degli aminoacidi
 Digestione delle proteine e assorbimento degli aminoacidi Temperatura La cottura degli alimenti aumenta la digeribilità perché i legami peptidici sono piu accessibili agli enzimi proteolitici Digestione
Digestione delle proteine e assorbimento degli aminoacidi Temperatura La cottura degli alimenti aumenta la digeribilità perché i legami peptidici sono piu accessibili agli enzimi proteolitici Digestione
Biochimica e Biologia per le professioni sanitarie, McGraw-Hill
 Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
Il metabolismo dei lipidi
 Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
Alle proteine è legato il concetto di principio elementare plastico per eccellenza Ruolo svolto dalle proteine:
 Alle proteine è legato il concetto di principio elementare plastico per eccellenza Ruolo svolto dalle proteine: 1. Componenti strutturali essenziali 2. Enzimi 3. Ormoni 4. Proteine plasmatiche 5. Trasporto
Alle proteine è legato il concetto di principio elementare plastico per eccellenza Ruolo svolto dalle proteine: 1. Componenti strutturali essenziali 2. Enzimi 3. Ormoni 4. Proteine plasmatiche 5. Trasporto
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Amminoacidi: l eliminazione dell azoto
 Amminoacidi: l eliminazione dell azoto P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Gli aa. Non sono conservati nell organismo, quelli che eccedono
Amminoacidi: l eliminazione dell azoto P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Gli aa. Non sono conservati nell organismo, quelli che eccedono
Secrezione dell HCl. Azione battericida Denaturazione delle proteine Ambiente ottimale per l azione della pepsina
 Secrezione dell HCl Gli inibitori della pompa protonica sono un gruppo di farmaci che inibiscono la H + /K + -ATPasi determinando un'inibizione efficace sulla secrezione acida. Succo gastrico (ph 1.5-2.5)
Secrezione dell HCl Gli inibitori della pompa protonica sono un gruppo di farmaci che inibiscono la H + /K + -ATPasi determinando un'inibizione efficace sulla secrezione acida. Succo gastrico (ph 1.5-2.5)
CATABOLISMO AMMINOACIDI
 CATABOLISMO AMMINOACIDI 1 Catabolismo aminoacidi Digestione di proteone dalla dieta Turnover delle proteine Digiuno prolungato 2 Digestione delle proteine dalla dieta L organismo ricava la maggior parte
CATABOLISMO AMMINOACIDI 1 Catabolismo aminoacidi Digestione di proteone dalla dieta Turnover delle proteine Digiuno prolungato 2 Digestione delle proteine dalla dieta L organismo ricava la maggior parte
METABOLISMO DEGLI AMMINOACIDI
 PRINCIPI NUTRITIVI METABOLISMO DEGLI AMMINOACIDI Nel corso della digestione le proteine vengono degradate in amminoacidi. Contrariamente ai carboidrati, gli amminoacidi non vengono immagazzinati, ma vengono
PRINCIPI NUTRITIVI METABOLISMO DEGLI AMMINOACIDI Nel corso della digestione le proteine vengono degradate in amminoacidi. Contrariamente ai carboidrati, gli amminoacidi non vengono immagazzinati, ma vengono
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi
 Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Ossidazione degli amminoacidi e produzione dell urea
 Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali:
 Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
Catabolismo degli aminoacidi
 Catabolismo degli aminoacidi Gli amminoacidi che non vengono utilizzati per la sintesi proteica sono catabolizzati in modo da ricavare l energia in essi contenuta. 10-15% dell energia necessaria all organismo
Catabolismo degli aminoacidi Gli amminoacidi che non vengono utilizzati per la sintesi proteica sono catabolizzati in modo da ricavare l energia in essi contenuta. 10-15% dell energia necessaria all organismo
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
I mammiferi sono privi dell enzima nitrogenasi, in grado di fissare l azoto atmosferico N2 NH3.
 Le proteine della dieta vengono scisse, nello stomaco e nell intestino, da diversi enzimi (pepsina, chimotripsina, carbossipeptidasi, elastasi) e i singoli amminoacidi sono assorbiti dalla parete intestinale.
Le proteine della dieta vengono scisse, nello stomaco e nell intestino, da diversi enzimi (pepsina, chimotripsina, carbossipeptidasi, elastasi) e i singoli amminoacidi sono assorbiti dalla parete intestinale.
PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a)
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Digestione e assorbimento delle proteine
 Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Scaricato da 21/01/2011
 1 2 Le due principali vie di rimozione del gruppo -NH 2 sono TRANSAMINAZIONE - transaminazione - deaminazione ossidativa La transaminazione è la prima tappa del catabolismo della maggior parte degli aa
1 2 Le due principali vie di rimozione del gruppo -NH 2 sono TRANSAMINAZIONE - transaminazione - deaminazione ossidativa La transaminazione è la prima tappa del catabolismo della maggior parte degli aa
 METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
Nella Biosfera viene mantenuto un un equilibrio tra l azoto totale inorganico e quello organico
 Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
La classificazione delle proteine
 protidi 1 La classificazione delle proteine In base al valore biologico (ovvero al contenuto di AAE) si distinguono: - p. ad alto valore biologico contengono tutti gli AAE (es. carne, pesce, uova, latte
protidi 1 La classificazione delle proteine In base al valore biologico (ovvero al contenuto di AAE) si distinguono: - p. ad alto valore biologico contengono tutti gli AAE (es. carne, pesce, uova, latte
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Scaricato da 21/01/2011
 Al contrario di quanto accade per glucidi e lipidi non esistono riserve di proteine. 1 2 Gli aa in eccesso non vengono messi in riserva ma utilizzati come combustibili metabolici. Non più del 10-15% dell
Al contrario di quanto accade per glucidi e lipidi non esistono riserve di proteine. 1 2 Gli aa in eccesso non vengono messi in riserva ma utilizzati come combustibili metabolici. Non più del 10-15% dell
TRANSAMINASI (AMINOTRANSFERASI) agiscono con un meccanismo ping-pong. sono presenti sia nel citosol che nei mitocondri
 TRANSAMINASI (AMINOTRANSFERASI) sono PLP-dipendenti agiscono con un meccanismo ping-pong catalizzano reazioni reversibili sono presenti sia nel citosol che nei mitocondri Seguiamo le fasi di una reazione
TRANSAMINASI (AMINOTRANSFERASI) sono PLP-dipendenti agiscono con un meccanismo ping-pong catalizzano reazioni reversibili sono presenti sia nel citosol che nei mitocondri Seguiamo le fasi di una reazione
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Fegato e metabolismo lipidico
 Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
FABBISOGNO CALORICO kcal kcal
 FABBISOGNO CALORICO DONNA UOMO 1500-2000 kcal 2000-2500 kcal Al contrario di quanto accade per i carboidrati e i lipidi non esistono riserve di proteine. Le proteine, come tutti i componenti cellulari,
FABBISOGNO CALORICO DONNA UOMO 1500-2000 kcal 2000-2500 kcal Al contrario di quanto accade per i carboidrati e i lipidi non esistono riserve di proteine. Le proteine, come tutti i componenti cellulari,
Esempi di quiz di biochimica. 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio
 Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Il metabolismo dell azoto
 Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
L integrazione proteica nelle diverse fisiopatologie
 Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Proteasi Serina proteasi Serina proteasi-coagulazione del sangue
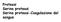 Proteasi Serina proteasi Serina proteasi-coagulazione del sangue PROTEASI Le proteasi catalizzano la scissione idrolitica di un legame peptidico Peptide bond -carboxyl group & -amino group La reazione
Proteasi Serina proteasi Serina proteasi-coagulazione del sangue PROTEASI Le proteasi catalizzano la scissione idrolitica di un legame peptidico Peptide bond -carboxyl group & -amino group La reazione
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
I PROTIDI. Aspetti generali
 I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
TCA cycle (ciclo di Krebs)
 TCA cycle (ciclo di Krebs) Come abbiamo detto la glicoli produce due molecole di ATP e due di NADH per ogni molecola di glucosio. La maggior parte dell energia potenziale contenuta nella molecola di glucosio
TCA cycle (ciclo di Krebs) Come abbiamo detto la glicoli produce due molecole di ATP e due di NADH per ogni molecola di glucosio. La maggior parte dell energia potenziale contenuta nella molecola di glucosio
Metabolismo. Metabolismo. Il complesso di tutte le reazioni organiche di trasformazioni tra energia e materia viene definito come metabolismo.
 Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
L NH 3 è prodotta da tutti i tessuti durante il metabolismo di diversi composti, ma solo il fegato èin grado di eliminarla sotto forma di urea
 L NH 3 è prodotta da tutti i tessuti durante il metabolismo di diversi composti, ma solo il fegato èin grado di eliminarla sotto forma di urea L NH 3 è estremamente tossica per il cervello: un aumento
L NH 3 è prodotta da tutti i tessuti durante il metabolismo di diversi composti, ma solo il fegato èin grado di eliminarla sotto forma di urea L NH 3 è estremamente tossica per il cervello: un aumento
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
TRANSAMINASI E CICLO DELL UREA
 TRANSAMINASI E CICLO DELL UREA L energia metabolica ottenuta dagli amminoacidi, sia derivati dalle proteine della dieta, sia dalle proteine dei tessuti, varia notevolmente a seconda del tipo di tessuto
TRANSAMINASI E CICLO DELL UREA L energia metabolica ottenuta dagli amminoacidi, sia derivati dalle proteine della dieta, sia dalle proteine dei tessuti, varia notevolmente a seconda del tipo di tessuto
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
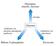 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH
 Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Una panoramica del ciclo dell acido ciclico
 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Protidi. Metabolismo
 Protidi Metabolismo CONTINUO RICAMBIO PROTEICO Serve energia sia per la sintesi che per la degradazione: 15-20 % del bilancio energetico La continua demolizione e sintesi è fondamentale per degradare e
Protidi Metabolismo CONTINUO RICAMBIO PROTEICO Serve energia sia per la sintesi che per la degradazione: 15-20 % del bilancio energetico La continua demolizione e sintesi è fondamentale per degradare e
Gluconeogenesi. Sintesi de-novo di glucosio
 Gluconeogenesi Sintesi de-novo di glucosio La gluconeogenesi garantisce il mantenimento dei livelli di glucosio nel sangue anche per molto tempo dopo l assorbimento e la completa ossidazione del glucosio
Gluconeogenesi Sintesi de-novo di glucosio La gluconeogenesi garantisce il mantenimento dei livelli di glucosio nel sangue anche per molto tempo dopo l assorbimento e la completa ossidazione del glucosio
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Fegato. Il fegato produce numerosi enzimi, come gli isoenzini del citocromo P450 che metabolizzano farmaci ed altre sostanze tossiche
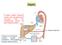 Fegato Il fegato produce numerosi enzimi, come gli isoenzini del citocromo P450 che metabolizzano farmaci ed altre sostanze tossiche Sangue ossigenato - Sangue ricco di nutrien0. Con0ene prodo4 del catabolismo
Fegato Il fegato produce numerosi enzimi, come gli isoenzini del citocromo P450 che metabolizzano farmaci ed altre sostanze tossiche Sangue ossigenato - Sangue ricco di nutrien0. Con0ene prodo4 del catabolismo
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Metabolismo dei composti azotati: aminoacidi e nucleotidi
 Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
AMMINO ACIDI. L equilibrio è regolato dal ph
 AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
IL METABOLISMO. Dal carbonio agli OGM Capitolo 2
 IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della nutrizione - Prof.ssa Luciana Avigliano A.A. 2009-2010 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE componente
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della nutrizione - Prof.ssa Luciana Avigliano A.A. 2009-2010 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE componente
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
scaricato da www.sunhope.it
 CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
Apparato endocrino. Controllo della glicemia. Il pancreas endocrino. Università degli Studi di Perugia
 Università degli Studi di Perugia Dipartimento di Medicina Sperimentale Sezione di Fisiologia e Biochimica Apparato endocrino Controllo della glicemia Il pancreas endocrino 1 Insulina: struttura e biosintesi
Università degli Studi di Perugia Dipartimento di Medicina Sperimentale Sezione di Fisiologia e Biochimica Apparato endocrino Controllo della glicemia Il pancreas endocrino 1 Insulina: struttura e biosintesi
GLUCOSIO. Vena porta DIGESTIONE DEI DISACCARIDI. Enzimi parete intestinale
 DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Son Formula supplementazione aminoacidica sicura
 Son Formula supplementazione aminoacidica sicura Dott. Giovanni Posabella Medico Chirurgo Specialista in Medicina dello Sport Docente Università degli Studi dell Aquila Esperto in omeopatia, omotossicologia
Son Formula supplementazione aminoacidica sicura Dott. Giovanni Posabella Medico Chirurgo Specialista in Medicina dello Sport Docente Università degli Studi dell Aquila Esperto in omeopatia, omotossicologia
1) Comunicazione diretta attraverso giunzioni comunicanti 2) Comunicazione tramite messaggeri chimici
 Una complessa rete di comunicazione tra cellule coordina la crescita, il differenziamento e il metabolismo in tutti gli organismi pluricellulari. Si riconoscono due tipologie di comunicazione intercellulare:
Una complessa rete di comunicazione tra cellule coordina la crescita, il differenziamento e il metabolismo in tutti gli organismi pluricellulari. Si riconoscono due tipologie di comunicazione intercellulare:
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
La scienza nell alimentazione
 La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
Il Fegato - ruolo centrale nel metabolismo
 Il Fegato - ruolo centrale nel metabolismo 1) È una ghiandola esocrina: produce bile cistifellea intestino tenue 2) È un organo a secrezione interna (endocrina): prodotti metabolici torrente circolatorio
Il Fegato - ruolo centrale nel metabolismo 1) È una ghiandola esocrina: produce bile cistifellea intestino tenue 2) È un organo a secrezione interna (endocrina): prodotti metabolici torrente circolatorio
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI
 GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
L INTESTINO TENUE (duodeno, digiuno, ileo)
 L INTESTINO TENUE (duodeno, digiuno, ileo) Lo sfintere pilorico, apertura distale dello stomaco, regola il passaggio del chimo acido dallo stomaco all intestino tenue. L intestino tenue è un sottile tubo
L INTESTINO TENUE (duodeno, digiuno, ileo) Lo sfintere pilorico, apertura distale dello stomaco, regola il passaggio del chimo acido dallo stomaco all intestino tenue. L intestino tenue è un sottile tubo
Destino dei principi nutritivi
 Destino dei principi nutritivi DIGESTIONE Demolizione nelle molecole costitutive ASSORBIMENTO TRASFORMAZIONE METABOLICA Produzione di energia glucosio, ac. grassi,aa Turnover proteico amminoacidi Metabolismo
Destino dei principi nutritivi DIGESTIONE Demolizione nelle molecole costitutive ASSORBIMENTO TRASFORMAZIONE METABOLICA Produzione di energia glucosio, ac. grassi,aa Turnover proteico amminoacidi Metabolismo
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
(o dotto di Santorini)
 Pancreas Il pancreas è una ghiandola a funzione mista. (o dotto di Santorini) Papilla di Vater Sfintere di Oddi Dotto di Wirshung (regola rilascio e impedisce reflusso) Il pancreas esocrino secerne tutti
Pancreas Il pancreas è una ghiandola a funzione mista. (o dotto di Santorini) Papilla di Vater Sfintere di Oddi Dotto di Wirshung (regola rilascio e impedisce reflusso) Il pancreas esocrino secerne tutti
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Metabolismo dei lipidi
 Metabolismo dei lipidi Digestione delle proteine Metabolismo di amminoacidi Ciclo dell urea scaricato da www.sunhope.it Generalità scaricato da www.sunhope.it I Lipidi sono composti organici formati da
Metabolismo dei lipidi Digestione delle proteine Metabolismo di amminoacidi Ciclo dell urea scaricato da www.sunhope.it Generalità scaricato da www.sunhope.it I Lipidi sono composti organici formati da
Corso di Formazione in Dietologia e Nutrizione
 Corso di Formazione in Dietologia e Nutrizione La dieta equilibrata: Alimentazione dell adulto 2 P Marina Mariani Che cosa sono i macronutrienti Proteine Lipidi Glucidi Cosa sono i macronutrienti Per vivere
Corso di Formazione in Dietologia e Nutrizione La dieta equilibrata: Alimentazione dell adulto 2 P Marina Mariani Che cosa sono i macronutrienti Proteine Lipidi Glucidi Cosa sono i macronutrienti Per vivere
