CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
|
|
|
- Adelaide Speranza
- 8 anni fa
- Visualizzazioni
Transcript
1 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico Lezione 7
2 Mioglobina Emoglobina
3 po 2 = 1 Torr po 2 = 26 Torr Curve di saturazione
4 Prologo L'ossigeno è richiesto per il metabolismo aerobico e per la produzione di energia nelle delle cellule. L'ossigeno è l accettore finale di elettroni ottenuti all ossidazione dei substrati introdotti dall'alimentazione con guadagno netto di energia.
5 L ossigeno è poco solubile in acqua La sua diffusione è inefficiente se le distanze superano pochi millimetri
6 DOBBIAMO TRASPORTARE OSSIGENO Nessuna catena laterale amminoacidica è in grado di legare ossigeno reversibilmente
7 Possiamo utilizzare metalli (per esempio il ferro). Però il ferro libero provoca la formazione di specie dell ossigeno altamente reattive (tossiche). Quindi si utilizza nei vertebrati un gruppo prostetico che lega con legami di coordinazione il Fe(II) (ha la possibilità di farne 6!)
8 Ricordiamoci che il gruppo potfirinico è presente anche in citocromi e in enzimi che eliminano l acqua ossigenata. In tali caso il ferro passa normalmente da stato ferroso a ferrico.
9 Quando l eme isolato reagisce con l ossigeno, il ferro passa irreversibilmente dallo stato ferroso allo stato ferrico. Inoltre, forma dei dimeri in presenza di ossigeno
10 Per evitarlo dobbiamo utilizzare un impalcatura per l eme che impedisca sia l ossidazione del Fe +2 a Fe +3 sia la dimerizzazione dei gruppi eme; una struttura proteica. Ciò lo allontana anche dall acqua
11 La % di similitudine si rispecchia nella struttura tridimensionale; si nota in proteine omologhe anche con basse % di similitudine
12
13 All inizio. proteina monomerica Alla fine. Mioglobina, nei muscoli Emoglobina, nel sangue
14 Pre e pro cordati Il tessuto ha pochi strati L ossigeno può diffondere attraverso i tessuti globina tipo mioglobina cioè monomerica
15 Vertebrati inferiori La dimensione dell organismo aumenta La complessità aumenta Una gobina monomerica non è più sufficiente La prima globina dimerica appare in Agnatha E un dimero, debolmente cooperativo Le prime catene alfa e beta appaiono nei pesci
16
17 Cosa accadeva oltre a ciò? Si aveva lo sviluppo di tutte le attrezzature che erano indispensabili per far in modo che il processo di ossigenazione avesse con le massime prestazioni. Evoluzione dell apparato circolatorio.
18 Mioglobina Cuore e muscoli Funziona come riserva di ossigeno nei muscoli Singola catena 1 eme 8 alfa eliche, 153 amminoacidi Emoglobina Eritrociti, globuli rossi Riserva e trasporto di ossigeno dai polmoni ai capillari 4 catene (2 alfa e 2 beta) 4 eme Ogni catena è simile in sequenza e struttura alla mioglobina Le catene sono tenute insieme da interazioni non covalenti Struttura Myo Struttura tura Emog
19 MIOGLOBINA Cuore e muscoli Funziona come riserva di ossigeno nei muscoli Singola catena 1 eme 8 alfa eliche, 153 amminoacidi Proteina monomerica, presente nei muscoli (mios = muscolo) e nel cuore.
20 75% α elica Elica n. residui A 16 B 16 C 7 D 7 E1+E2 20 F 10 G 19 H 26 Totale 121
21 La struttura proteica interagisce con la porfirina IX tramite legami ionici e ad idrogeno tramite i gruppi propionici, oltre ad interazioni idrofobiche.
22 Il Fe(II) presenta la possibilità di 6 legami di coordinazione: quattro sono con i gruppi amminici della porfirina, uno con un istidina (chiamata prossimale) e l ultimo con l ossigeno (in linea con tale legame di coordinazione vi una seconda istidina chiamata distale). L altra cosa da ricordare per il seguito è che l atomo di ferro rispetto al piano dell eme eme è sposto verso l istidina prossimale.
23
24 Ingrandimento di tale situazione che mette ben in evidenza le due istidine (ovviamente conservata in tutte le globine ). Prossimale Distale
25 LE INTERAZIONI CON I LIGANDI DIPENDONO DALLA STRUTTURA DELLA PROTEINA. L EME LEGA IL CO CIRCA VOLTE MEGLIO DELL OSSIGENO, NOI VOGLIAMO RIDURRE QUESTO RAPPORTO
26 Il fattore scende a circa 200 quando l eme è all interno della globina
27 Saturazione, siti con ligando sui siti totali Saturazione (θ) po 2 = 1 torr La cinetica di legame dell ossigeno alla mioglobina è una semplice curva di saturazione iperbolica. Tale curva è non cooperativa e non assomiglia alla curva della denaturazione delle proteine (curva sigmoide)
28 Come dovrebbe essere una proteina che trasporta ossigeno e lo cede alla mioglobina? A Proteina di trasporto efficiente nel legame ma inefficiente nel rilascio
29 B Proteina di trasporto efficiente nel rilascio ma inefficiente nel legame
30 C Proteina di trasporto efficiente sia nel legame che nel rilascio
31 Emoglobina La transizione tra gli stati di legame debole e forte spiega la curva sigmoide
32 Vi è cooperatività se vi è più di un unità unità Senza ossigeno, deossiemoglobina con ossigeno, ossiemoglobina
33 Interazioni dominanti tra le subunità di Hb Interazioni idrofobiche, 30 aa circa
34 po 2 = 1 Torr po 2 = 26 Torr Curva di saturazione dell emoglobina
35 Il significato della curva di legame sigmoidale dell'ossigeno Si può apprezzare il significato di questa curva riguardando il grafico. Mentre entrambe Hb e Mb sono saturate con O 2 alla pressione parziale di O 2 nei polmoni, solo l'emoglobina rilascerà significative quantità di O 2 nei tessuti. Infatti l'o 2 rilasciato da Hb può legarsi alla Mb nei i muscoli.
36 L emoglobina è una proteina molto più complessa del mioglobina; oltre a O 2, l emoglobina trasporta la CO 2 e H +. Inoltre 1. Il legame della prima molecola di O 2 all emoglobina favorisce il legame di altre molecole; 2. L affinità dell emoglobina per l ossigeno dipende dal ph e dalla CO 2. Sia la concentrazione di H + che la CO 2 promuovono il rilascio di O 2 3. L affinità dell emoglobina per l ossigeno è inoltre regolata da composti organici contenenti gruppi fosforici come il 2, 3-bisfosfoglicerato (BPG). Il risultato è che in presenza di tali composti l emoglobina presenta un affinità per l ossigeno più bassa.
37 L emoglobina è una proteina allosterica (dal greco allos, altro, e stereos, solido o forma). E una proteina in cui il legame di un ligando a un sito modifica le proprietà di un altro sito sulla stessa molecola proteica. In generale le proteine possono avere forme o conformazioni diverse indotte dal legame di ligandi chiamati anche modulatori. I modulatori di una proteina allosterica la convertono in una forma più o meno attive delle stessa proteina. I modulatori possono quindi avere effetti attivatori o inibitori
38 EFFETTO BOHR O 2 Hb + H + + CO 2 Negli alveoli polmonari Tessuti con attivo metabolismo Hb-H + -CO 2 + O 2 Effetto del ph sull affinità per l ossigeno. Abbassando il ph si provoca il rilascio di ossigeno dall ossiemoglobina.
39 Il rilascio di anidride carbonica da parte delle cellule abbassa l affinità dell emoglobina per l ossigeno in due modi: Una parte dell anidride carbonica si trasforma tramite l anidrasi carbonico in bicarbonato e rilascia H + CO 2 + H 2 O <> HCO 3- + H + Parte del bicarbonato è trasportato all esterno degli eritrociti, ma una parte reagisce direttamente con l emoglobina, legandosi agli amminogruppi N-terminali delle catene formando carbammati: -NH 2+ + HCO 3- <> -HNCOO - + H + + H 2 O Quindi di nuovo abbassiamo il ph e in più formiamo un legame salino tra catene α e β caratteristico dello stato deossi
40 L emoglobina lega composti con gruppi fosfato BPG ABBASSA L AFFINITÀ DI Hb PER L OSSIGENO Anfibi Tale composto si forma durante la glicolisi
41 Il BPG abbassa l affinità di Hb per l ossigeno
42
43 Il tutto può essere spiegato considerando che l emoglobina presenta due stadi conformazionali. Lo stato T (Teso) Lo stato R (Rilassato) I cambi sono dovuti a variazioni di legami deboli tra le subunità
44 Lo stato Teso è cosi chiamato perché presenta un numero superiore di legami non covalenti (ionici ed ad idrogeno), che mantengono la conformazione intrappolata nello stato TESO Nello stato Rilassato alcuni di questi legami vanno persi, dopo l interazione con l ossigeno molecolare
45 Struttura Tesa Struttura Rilassata
46 Legami che stabilizzano la forma T His146 in beta Asp94 in alfa
47 COSA SUCCEDE A LIVELLO MOLECOLARE PER DARE ALL EMOGLOBINE QUESTE PROPRIETÀ Allosteriche?
48 L istidina prossimale è legata al Fe quindi si muoverà anch'essa causando un contemporaneo spostamento dell'elica F in cui si trova
49
50 Residuo di Aspartico94 alfa (elica FG1) e Istidina146 beta (elica HC3)
51 Cominciano a saltare i legami deboli che stabilizzano la forma T (deossiemoglobina) Il ph c entra perché a ph più basso stabilizzo la His146 protonata (che può fare legame) Quindi un alta concentrazione di H + favorisce la forma deossi e quindi il rilascio dell ossigeno.
52 Questo movimento altera la struttura di ogni subunità che a loro volta cambiano le interazioni tra le subunità nell'interfaccia.
53 Il BPG stabilizza la forma deossi e quindi favorisce il rilascio di ossigeno
54
55 Transizione T R Legame del BPG alla deossiemoglobina. Il legame del BPG Stabilizza lo stato T (a). La tasca del legame con BPG scompare in seguito ad ossigenazione, in seguito alla transizione T R. In montagna stato di acclimatamento
56
57
58 (% di saturazione) Variazione della curva in presenza dei vari effettori
59 A causa del modo di impaccarsi delle subunità, una subunità non può passare da una conformazione ad un'altra senza far sì che anche l'altra cambi, anche se l'altra subunità non ha nessuna molecola di O 2 legata. Una volta avutosi il cambio di conformazione, l'affinità dei siti liberi per O 2 cresce poichè non ci sono blocchi sterici al legarsi dell'o 2.
60 Bassa affinità Alta affinità Modello MWC (concertato) Modello KNF (sequenziale)
61 Modello sequenziale Modello concertato Nessuno dei due modelli da una corretta interpretazione della curva dell emoglobina.
62 Nei polmoni Esempio dei 4 francobolli già libero per O 2
63 L anemia falciforme: la prima malattia molecolare
64
65
66
67 Ingram 1956 Elettroforesi a ph 8,6 HbA HbS è più positiva µ= kc/m HbA + HbS Condizione clinica 1- Adulto normale; 2- Portatore del carattere 3- Anemia falciforme Origine
68 - + - Elettroforesi su carta da filtro + Cromatografia
69
70
71
72 LE MUTAZIONI La sostituzione di un solo amminoacido (Glu Val) ha effetti 1- La sostituzione di un solo amminoacido ( ) ha effetti profondi sulla funzionalità della emoglobina; 2- Questa sostituzione a livello proteico è causata da una mutazione avvenuta a livello del DNA genomico: avvenuta a livello del DNA genomico: GAG GTG; 3- Le sostituzione possono anche migliorare una determinata funzione; 4- Il caso riportato è il risultato di un evento evolutivo naturale; 5- Oggi le mutazioni possono essere introdotte in maniera mirata. - Mutazione missense; - Mutazione nonsenso; - Mutazione della fase di lettura per delezione
73 Distribuzione del gene per Hb S e per il parassita della malaria. 73
74 Sono state ritrovate moltissime varianti di Hb A. Tali varianti riguardano sostituzioni di singoli residui che danno fenotipi normali. 74
75
76 Nell emoglobina emoglobina fetale la catena β è sostituita da una catena γ,, che non ha His 143 ma una serina La catena γ ha meno affinità per BPG e quindi l emoglobina fetale ha un affinità maggiore per l ossigeno!!
77 Curve a confronto tra Hb A e Hb F in cui l unica differenza è un istidina! (His 143).
78 Lo spettro di assorbimento può dare indicazioni sulla forma Deossi o Ossi dell emoglobina..
79 Saturazione (θ) (L) Per l ossigeno: θ= [O 2 ] / ([O 2 ] + K d ) = po 2 / (po 2 + po 50 po 50 è la pressione di O 2 quando la meta dei siti è occupata 50 )
80 P + L <-> L K a = [PL] / [P] [L] [PL] / [PL] = K a [L] Il rapporto tra proteina libera e legata è proporzionale alla concentrazione del ligando libero. θ = siti di legame occupati / siti di legame totali = [PL]/([PL] + [P]) [PL PL] [PL] + [P] K a [L] [P] K a [L] K a [L] [P] + [P] [ K a [L] + 1 [L] [L] + 1 / K a θ = [L] [L] + K d Questa è l equazione di un iperbole 1/K a = K d = costante di dissociazione
81 Il diagramma di Hill L'equazione di Hill descrive il legame di n molecole (emoglobina) di O 2 con un'equazione simile a quella precedente Una forma lineare è data da che può essere usata per stabilire la cooperatività del legame. n è il coefficiente di Hill
82 Il coefficiente di Hill è una misura della cooperatività del legame
83 (Per la Mb un simile grafico porta ad una linea retta con n=1,0) Per Hb si non ha una linea retta ma si distinguono invece tre parti: 1) a basse ed alte PO 2 il grafico ha una pendenza di 1. In queste condizioni si ha il legame o della prima molecola di O 2 (stato T) o dell'ultima (stato R). In queste condizioni Hb si comporta come se avesse un solo sito di legame; 2) per valori intermedi di PO 2 la pendenza è maggiore di 1. Questa è il campo della cinetica cooperativa. Il valore della pressione parziale di O 2 necessaria per saturare metà dell'emoglobina, P 50, ci dà il valore di n. Per Hb questo è circa 3,5. Il massimo valore possibile sarebbe 4, equivalente al numero delle subunità, ma il coefficiente di Hill è sempre inferiore al suo valore massimo.
84 Evoluzione Evoluzione molecolare
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
ossigeno e ne facilita la diffusione dai capillari all ambiente intracellulare.
 Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
La mutazione è una modificazione della sequenza delle basi del DNA
 La mutazione è una modificazione della sequenza delle basi del DNA Le mutazioni sono eventi rari e importanti in quanto sono alla base dell evoluzione biologica Le mutazioni possono essere spontanee (dovute
La mutazione è una modificazione della sequenza delle basi del DNA Le mutazioni sono eventi rari e importanti in quanto sono alla base dell evoluzione biologica Le mutazioni possono essere spontanee (dovute
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
Ripiegamento e stabilità delle proteine
 Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Le proteine che legano ossigeno:
 Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Rappresentazione dei Dati Biologici
 Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI
 Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Attivitá e cinetica enzimatica
 Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Funzioni dell apparato respiratorio
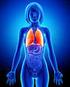 Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Istituto di Istruzione Superiore L. da Vinci Civitanova Marche. Anno scolastico 2014-2015. Programma svolto. Docente: Silvana Venditti
 Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Mioglobina Emoglobina
 Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica
 Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica Anno accademico 2009/2010 I anno, II semestre CdL Infermieristica e Fisioterapia PATOLOGIA GENETICA Oggetto di studio
Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica Anno accademico 2009/2010 I anno, II semestre CdL Infermieristica e Fisioterapia PATOLOGIA GENETICA Oggetto di studio
SDD - Seconde Equilibrio e ph. Equilibrio e ph. Obiettivo
 1 Obiettivo Capire che cosa è il ph, apprendere le leggi fondamentali che lo controllano e capire qualitativamente le applicazioni delle soluzioni tampone. Prerequisiti Il concetto di equilibrio (che comunque
1 Obiettivo Capire che cosa è il ph, apprendere le leggi fondamentali che lo controllano e capire qualitativamente le applicazioni delle soluzioni tampone. Prerequisiti Il concetto di equilibrio (che comunque
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
gruppo prostetico) Cromoproteine Legare l ossigeno Impedire che ossidi altre sostanze Cedere O 2 in particolari e ben definite condizioni
 Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno
 Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Verifica. Tutto il quaderno di lavoro. Riferimento. Gli studenti svolgono la verifica. Compito. Foglio di esercizio Soluzione.
 Livello 2 07 / Il sangue Informazione per gli insegnanti 1/6 Riferimento Tutto il quaderno di lavoro Compito Gli studenti svolgono la verifica. Materiale Soluzione Forma sociale Lavoro individuale Tempo
Livello 2 07 / Il sangue Informazione per gli insegnanti 1/6 Riferimento Tutto il quaderno di lavoro Compito Gli studenti svolgono la verifica. Materiale Soluzione Forma sociale Lavoro individuale Tempo
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma
 Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Modulo 4. Una proteina in azione
 Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG 27/4/2006 Cuore come dipolo elettrico Il cuore considerato come un generatore elettrico complesso, in cui sono presenti
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG 27/4/2006 Cuore come dipolo elettrico Il cuore considerato come un generatore elettrico complesso, in cui sono presenti
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Trasporto di CO 2. ed effetto Bohr. . La CO 2. nei tessuti produce CO 2. Il consumo di O 2. deve essere rimossa e portata ai polmoni (o alle branchie)
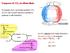 Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali
 Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
GLI ENZIMI ALLOSTERICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM)
 Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
COMPOSTI DI COORDINAZIONE (complessi)
 Gli ioni dei metalli di transizione nei sistemi biologici non si presentano come acquoioni [M(H 2 O) n ] x+ ma come. COMPOSTI DI COORDINAZIONE (complessi) derivano dall interazione (coordinazione) tra
Gli ioni dei metalli di transizione nei sistemi biologici non si presentano come acquoioni [M(H 2 O) n ] x+ ma come. COMPOSTI DI COORDINAZIONE (complessi) derivano dall interazione (coordinazione) tra
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
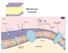 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
L adattamento dei batteri. Strategie di adattamento
 L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
θ = (siti occupati)/(siti disponibili totali) Al numeratore ritrovo solo la mioglobina che ha complessato l'ossigeno, solo l'ossigenata)
 LEZIONE DEL 03/04/2017 Emoglobina - complesso del metallo di transizione (ferro protoporfirina IX) complesso metallorganico. Derivazione della curva di legame iperbolica dell'ossigeno della mioglobina
LEZIONE DEL 03/04/2017 Emoglobina - complesso del metallo di transizione (ferro protoporfirina IX) complesso metallorganico. Derivazione della curva di legame iperbolica dell'ossigeno della mioglobina
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
MESSA IN SCALA DI ALGORITMI DIGITALI
 Ingegneria e Tecnologie dei Sistemi di Controllo Laurea Specialistica in Ingegneria Meccatronica MESSA IN SCALA DI ALGORITMI DIGITALI Cristian Secchi Tel. 0522 522235 e-mail: secchi.cristian@unimore.it
Ingegneria e Tecnologie dei Sistemi di Controllo Laurea Specialistica in Ingegneria Meccatronica MESSA IN SCALA DI ALGORITMI DIGITALI Cristian Secchi Tel. 0522 522235 e-mail: secchi.cristian@unimore.it
-malattie monogeniche o mendeliane:
 Martedì 16 Febbraio è venuta nella nostra classe la dr.ssa Petrelli Maria a spiegarci le malattie sessualmente trasmissibili e ereditarie, sessualità e affettività. Ci ha spiegato la divisione delle cellule
Martedì 16 Febbraio è venuta nella nostra classe la dr.ssa Petrelli Maria a spiegarci le malattie sessualmente trasmissibili e ereditarie, sessualità e affettività. Ci ha spiegato la divisione delle cellule
CO 2 aq l anidride carbonica disciolta, reagendo con l'acqua, forma acido carbonico secondo la reazione:
 DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
IDROGENO IN PRATICA. del gruppo degli allievi del Volta. Laboratorio di chimica I.T. I. Volta
 IDROGENO IN PRATICA Pratiche di laboratorio su iniziative del gruppo degli allievi del Volta Laboratorio di chimica I.T. I. Volta da: L Isola Misteriosa Giulio Verne 1874 Senza il carbone non ci sarebbero
IDROGENO IN PRATICA Pratiche di laboratorio su iniziative del gruppo degli allievi del Volta Laboratorio di chimica I.T. I. Volta da: L Isola Misteriosa Giulio Verne 1874 Senza il carbone non ci sarebbero
10) Se ad una soluzione aumentiamo la temperatura cosa succede? Dire quale delle seguenti affermazioni è corretta.
 Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
Transferasi che hanno come coenzima FOSFOPANTOTEINA E COENZIMA A (derivati dalla VITAMINA B3 )
 Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
LE MOLECOLE INFORMAZIONALI. Lezioni d'autore Treccani
 LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
C). Quindi, con la spettroscopia NMR, le informazioni sulla struttura molecolare vengono dedotte osservando il comportamento dei nuclei atomici.
 La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una tecnica analitica strumentale che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame. La spettroscopia
La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una tecnica analitica strumentale che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame. La spettroscopia
Applicazioni biotecnologiche in systems biology
 Applicazioni biotecnologiche in systems biology Lezione #6 Dr. Marco Galardini AA 2012/2013 Gene regulation analysis Lezione #6 Dr. Marco Galardini AA 2012/2013 Regolazione genica Elementi molecolari e
Applicazioni biotecnologiche in systems biology Lezione #6 Dr. Marco Galardini AA 2012/2013 Gene regulation analysis Lezione #6 Dr. Marco Galardini AA 2012/2013 Regolazione genica Elementi molecolari e
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Circuiti amplificatori
 Circuiti amplificatori G. Traversi Strumentazione e Misure Elettroniche Corso Integrato di Elettrotecnica e Strumentazione e Misure Elettroniche 1 Amplificatori 2 Amplificatori Se A V è negativo, l amplificatore
Circuiti amplificatori G. Traversi Strumentazione e Misure Elettroniche Corso Integrato di Elettrotecnica e Strumentazione e Misure Elettroniche 1 Amplificatori 2 Amplificatori Se A V è negativo, l amplificatore
Celle a combustibile Fuel cells (FC)
 Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Relazione struttura-funzione
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
FISICA. Le forze. Le forze. il testo: 2011/2012 La Semplificazione dei Testi Scolastici per gli Alunni Stranieri IPSIA A.
 01 In questa lezione parliamo delle forze. Parliamo di forza quando: spostiamo una cosa; solleviamo un oggetto; fermiamo una palla mentre giochiamo a calcio; stringiamo una molla. Quando usiamo (applichiamo)
01 In questa lezione parliamo delle forze. Parliamo di forza quando: spostiamo una cosa; solleviamo un oggetto; fermiamo una palla mentre giochiamo a calcio; stringiamo una molla. Quando usiamo (applichiamo)
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
