degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l l anidride carbonica tra i polmoni e i tessuti
|
|
|
- Tiziano Abbate
- 7 anni fa
- Visualizzazioni
Transcript
1
2 l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule del miocardio e del muscolo scheletrico, ha la funzione di trasferire l ossigeno l della emoglobina del sangue alla citocromo-ossidasi ossidasi mitocondriale. Ha infatti una affinità per l ossigeno l superiore a quella dell emoglobina). emoglobina).
3 Gli organismi superiori necessitano di un sistema di trasporto per l ossigeno,, in quanto tale molecola è scarsamente idrosolubile L emoglobina assolve ad una funzione estremamente importante, contribuisce a mantenere il valore di ph costante in condizioni fisio-patologiche, funzionando quindi anche da sistema tampone
4 L emoglobina dell adulto (HbA( HbA) è un tetramero costituito da 4 catene a due a due uguali (2α e 2β); 2 ogni subunità porta un gruppo eme (gruppo prostetico contenente un nucleo di Ferro bivalente)
5 Legame dell ossigeno all emoglobina Nel sangue intero l emoglobina l è per metà saturata ad una pressione di ossigeno di 26 torr. Le po 2 indicate sono considerate a livello del mare (la po 2 atmosferica a livello del mare è di torr): Per un confronto nella figura è riportata la curva di legame dell ossigeno alla mioglobina. La curva iperbolica tratteggiata si riferisce ad una ipotetica proteina con la stessa p 50 dell emoglobina. emoglobina.
6 Significato fisiologico dell interazione tra emoglobina e O 2 E possibile valutare quantitativamente il significato fisiologico della natura sigmoidale della curva di legame dell emoglobina, emoglobina, o, in altre parole l importanza l fisiologica del fenomeno di cooperatità. L equazione di Hill : y/(1-y) y) = (p0( 2 /p 50 ) n y = frazione dei siti occupati dall ossigeno per Y = 1, tutti i siti sono occupati per Y = 0, nessun sito è occupato n = indice di Hill (indica il grado di sigmoidicità della curva ed il grado di cooperatività a p 50 ). n = 1, per la mioglobina (iperbole, nessuna cooperatività) n = 2.8, per la emoglobina (sigmoide( sigmoide, cooperatività)
7 La saturazione Y è definita come la frazione di siti occupati dall ossigeno. Y = 0 tutti i siti sono vuoti Y = 1 tutti i siti sono occupati 50 = pressione parziale dell ossigeno a cui il 50% dei siti sono occupati. p 50 p 50 per la mioglobina circa 1 torr p 50 per l emoglobina l circa 26 torr La mioglobina ha una affinità per l ossigeno l maggiore di quella della emoglobina. La curva di dissociazione dell ossigeno presenta un andamento iperbolico per la mioglobina e sigmoide per la emoglobina N.B.: Dalle curve prima riportate si desume che se l emoglobina fosse anch essa monomerica,, cederebbe ai tessuti quantità irrilevanti di ossigeno.
8 La forma ad S italica è dovuta alla interdipendenza funzionale dei suoi 4 emi. Il primo eme si ricombina lentamente con l ossigeno il secondo per influenza del primo (già ossigenato) si combina più velocemente e così via (effetto cooperativo). Tale modalità è caratteristica della struttura quaternaria e costituisce un esempio di regolazione allosterica.
9 l ossigeno si lega agli atomi di ferro bivalenti normalmente lo stato di ossidazione del ferro non cambia, la metaemoglobina trivalente, formatasi per ossidazione del nucleo di ferro, non è in grado di trasportare O 2 l eme ha una struttura tetrapirrolica il ferro centrale crea 4 legami di coordinazione con gli atomi di azoto dell anello tetrapirrolico, uno con un residuo istidinico della globina e un sesto legame di coordinazione avviene con la molecola dell ossigeno (ossiemoglobina
10 struttura dell eme eme
11 l emoglobina è stata la prima proteina di cui sono stati osservati effetti allosterici (modificazioni strutturali) questa può infatti assumere 2 conformazioni, la forma R ( relaxed o rilassata) e la forma T ( tense o tesa); il passaggio dall una all altra forma è data da interazioni elettrostatiche che dipendono dalla presenza o l assenza di legami fra l eme e la molecola di ossigeno
12 aumentando la pressione parziale dell ossigeno, un numero sempre più crescente di molecole assume forma R, più affine all ossigeno; la cooperatività tra le subunità,, e quindi anche l affinitl affinità verso l ossigeno, l cresce all aumentare aumentare della pressione parziale dell ossigeno altri effettori allosterici possono influenzare l equilibrio fra le 2 forme
13 Movimenti dell eme eme e dell elica elica F durante la transizione T verso la R nell emoglobina. emoglobina. Nella forma T (in blu) il Fe è 0.6 Å al di fuori del piano dell eme, eme, che assume una forma a cupola, con il Fe al centro. Quando l emoglobina l assume la forma R (in rosso), il Fe si muove verso il piano dell eme eme e la porfirina diventa planare. In questa posizione il Fe lega saldamente una molecola di ossigeno. L HisL F8 e l elica l F sono costrette a seguire il movimento del Fe
14 l emoglobina partecipa al trasporto dell anidride carbonica dai tessuti ai polmoni; circa il 90% della CO 2 non viene trasportata come tale ma viene prima convertita in ione bicarbonato HCO 3-, molto più solubile nei polmoni lo ione HCO - 3 viene riconvertito in CO 2 viene eliminata con l espirazionel che i 2 processi sono rispettivamente accoppiati alla deossigenazione e all ossigenazione dell emoglobina emoglobina (HbH( HbH, HbO 2 ) a questi 2 processi interviene anche l anidrasil carbonica, presente negli eritrociti, che permette l interconversione l tra acido carbonico in CO 2 e viceversa
15 Effettori allosterici dell emoglobina (modificazioni strutturali) ossigeno: effettore positivo (omotropico) H + : effettore negativo (effetto Bohr) H-Hb Hb + O 2 HbO 2 + H + 2,3 2,3-bis bis-fosfoglicerato: effettore negativo Hb-2,3 2,3-BPG + 4 O 2 Hb(O 2 ) 4 + 2,3 - BPG CO 2 : effettore negativo CO H 3 N-globina - OOCHN-globina + 2H +
16 la CO 2 è un prodotto del metabolismo aerobico e deve essere trasportato ai polmoni per essere rilasciato dal nostro organismo la maggior parte della CO 2 viene convertita in bicarbonato, HCO 3-, mediante l azione l dell anidrasi carbonica e quindi rilasciato nel plasma CO 2 + H 2 O H 2 CO 3 HCO 3- + H + la restante CO 2 si lega reversibilmente all emoglobina attraverso la formazione di un legame carbamidico con gli α-amino gruppi della porzione N-terminale N dei polipeptidi della globina CO H 3 N-globina - OOCHN-globina + 2H +
17 L effetto Bohr non è altro che il rilascio di ossigeno da parte dell emoglobina emoglobina che si osserva quando la concentrazione di ioni H + aumenta (il ph diminuisce). L effetto Bohr è fisiologicamente importante, in quanto i tessuti che stanno ossidando grandi quantità di sostanze nutrienti, e che di conseguenza hanno bisogno di grandi quantità di ossigeno, generano ioni H +, rilasciando CO 2 nel sangue: CO 2 + H 2 O 2CO 3 H HCO 3- + H + Facilitando il rilascio di ossigeno, questi ioni H + consentono il deposito di O 2 extra in quei tessuti che stanno consumando molto attivamente
18 Emoglobina e trasporto di CO2 L'emoglobina partecipa anche al trasporto del biossido di carbonio (CO 2 ) dai tessuti ai polmoni. Circa il 90% della CO2 non viene trasportata come tale, ma viene trasformata in idrogenocarbonato (HCO3-) ) molto più solubile in acqua. Nei polmoni l'idrogenocarbonato viene ritrasformato in CO2 che viene eliminato con l'espirazione.
19 I I due processi - la formazione di HCO - 3 nei tessuti e la liberazione di CO 2 nei polmoni - sono rispettivamente accoppiati alla deossigenazione e all'ossigenazione dell'emoglobina. La deossiemoglobina è una base marcatamente più forte dell'ossiemoglobina e lega quindi protoni (circa 0,7 H+ per tetramero) favorendo così nei capillari dei tessuti la formazione di HCO3- da CO2.
20 Partecipa al processo anche l'anidrasi carbonica, presente in alte concentrazioni negli eritrociti. L'HCO3- formato viene rilasciato per la maggior parte nel plasma in cambio di Cl- e con il plasma va ai polmoni dove le reazioni descritte avvengono in direzione opposta : la deossiemoglobina viene ossigenata e cede protoni che spostano l'equilibrio HCO3-/H2CO3 e favoriscono così il rilascio di CO2.
21 Una piccola parte di CO 2 (circa il 5%) viene trasportata, legata covalentemente con l'emoglobina, come carbammino-hb. Si calcola che i meccanismi descritti siano responsabili per il 60% del trasporto di CO 2.
22 gli ioni H + producono uno spostamento verso destra della curva di saturazione dell ossigeno (effetto Bohr) 22
23 Nei capillari dei tessuti extrapolmonari,, gli eritrociti trasformano in HCO - 3 la CO 2 prodotta dal metabolismo dei tessuti; l HCOl 3- così prodotto esce dagli eritrociti per scambio con il Cl -. Nei capillari polmonari,, l l HCO3- penetra negli eritrociti per scambio con il Cl-.. Dentro gli eritrociti, l l HCO3- viene trasformato in CO2, che quindi diffonde fuori dagli eritrociti e viene espirata
24
25 Effetto tampone dell emoglobina emoglobina
26 Il 2,3-BPG deriva dall 1,3-BPG, un intermedio della glicolisi eritrocitaria ogni molecola di 2,3-BPG lega ciascuna molecola di emoglobina; la sua concentrazione nell eritrocita eritrocita è quasi identica a quella dell emoglobina emoglobina un incremento del 2,3-BPG stabilizza la forma T (deossihb)) e quindi favorisce il rilascio di O2 un incremento di 2,3-BPG interviene in risposta a ipossia tissutale (dovuta a: anemia, disfunzione polmonare, fumo di sigarette, elevate altitudini)
27
28 in assenza di effettori allosterici, nel caso di emoglobina purificata, la curva di saturazione di questa proteina tende ad assumere un andamento simile a quello della mioglobina. In definitiva, quindi, i, gli effettori negativi risultano di fondamentale importanza per il rilascio dell ossigeno.
29 La mioglobina, presente nelle fibre muscolari, ha un affinit affinità verso l ossigeno l maggiore rispetto all emoglobina, l andamento della curva non è sigmoidale in quanto l affinitl affinità non è influenzata da effettori allosterici come BPG e H +
30 Il paradosso fetale Il feto deve ottenere ossigeno dal sangue materno attraverso la placenta. Lo scambio può avvenire grazie al fatto che il sangue fetale presenta un affinit affinità maggiore rispetto al sangue della madre Come è possibile?
31 Il sangue fetale contiene un tipo di emoglobina differente rispetto a quella dell adulto (HbA), l HbF infatti è costituita da un tetramero di tipo α 2 γ 2 La subunità γ differisce rispetto alla b-globina in quanto presenta un residuo neutro di serina al posto del residuo carico His143. Questa differenza fa si che l HbF è estremamente meno affine al 2,3-BPG (effettore allosterico negativo) rispetto all HbA, di conseguenza l HbF lega l ossigeno con maggiore affinità
32
33
34 Le sindromi talassemiche Sono la conseguenza di anormalità o non- funzionamento dei geni per la codifica delle globine, l insufficiente l sintesi dei diversi tipi di globina porta ad un anemia emolitica. La severità del danno è funzione dei numeri di geni mutati.
35 Le sindromi talassemiche Si distinguono 2 tipi di talassemia: β-talassemia bassi livelli (β+) o completa assenza (β0) di β- globina. Si può verificare un overproduzione compensatoria di HbF (α2γ2) α-talassemia bassi livelli di α-globina. Questa forma risulta essere più complicata poiché vengono coinvolti 2 tipi di geni che codificano per l α-globina. Le vie compensatorie determinano la produzione di 2 tipi di emoglobina, l HbH (β4) e l Hb di Bart (γ4) che non esibiscono transizioni allosteriche, effetto Bohr, inoltre queste rimangono sempre nello stato R
36 Anemia falciforme L anemia falciforme è una patologia ereditabile; manifestazioni comuni: ricorrente anemia emolitica e dolore basi biochimiche: mutazione puntiforme del gene per la β-globina, il residuo di Glu 6 risulta essere sostituito da una Val (valina) Lo scambio di questo aminoacido riduce la solubilità, promuove la polimerizzazione di molecole di emoglobina di tipo S deossigenata (HbS( HbS)
37 Spettro dei genotipi: anemia falciforme (HbSS) quadro clinico severo anemia falciforme di tipo lieve (HbAS) minori problemi clinici anemia falciforme β + talassemia coesistenza delle 2 varianti di emoglobina con quadro clinico davvero complicato La severità della patologia dipende dalla quantità di HbA e di HbF presenti
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Fisiologia della Respirazione
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Trasporto dei gas. Pressioni Volumi
 Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
LA MIOGLOBINA e L EMOGLOBINA
 UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE
 VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
PORTA AGLI ORGANI E AI TESSUTI: RIMUOVE: OMEOTERMI INTERVIENE NELLA TERMOREGOLAZIONE FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO
 FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI
 Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari.
 I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Trasporto dell ossigeno
 Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie.
 Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
possiede una propria struttura, da cui dipende la specifica funzione
 LE PROTEINE SONO DEI POLIMERI LE CUI UNITA RIPETITIVE SONO GLI -AMMINO ACIDI: ogni proteina possiede una propria struttura, da cui dipende la specifica funzione AMMINOACIDI E PROTEINE Le proteine rappresentano
LE PROTEINE SONO DEI POLIMERI LE CUI UNITA RIPETITIVE SONO GLI -AMMINO ACIDI: ogni proteina possiede una propria struttura, da cui dipende la specifica funzione AMMINOACIDI E PROTEINE Le proteine rappresentano
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown)
 Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
trasporto di O 2 per la legge di Henry, ad una P O2 di 100 mmhg, l O 2 sciolto è ca. 3 ml/l di sangue
 trasporto di O 2 per la legge di Henry, ad una P O2 di 100 mmhg, l O 2 sciolto è ca. 3 ml/l di sangue con una gittata cardiaca normale di 5 L/min potremmo fornire all organismo solo 15 ml/min di O 2 ma
trasporto di O 2 per la legge di Henry, ad una P O2 di 100 mmhg, l O 2 sciolto è ca. 3 ml/l di sangue con una gittata cardiaca normale di 5 L/min potremmo fornire all organismo solo 15 ml/min di O 2 ma
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Le proteine che legano ossigeno: 2) emoglobina. identità di sequenza: 18%
 Le proteine che legano ossigeno: 2) emoglobina identità di sequenza: 18% Il legame dell ossigeno all emoglobina Fisiologicamente (2%) o per effetto di sostanze ossidanti, lo ione Fe2+ si trasforma in
Le proteine che legano ossigeno: 2) emoglobina identità di sequenza: 18% Il legame dell ossigeno all emoglobina Fisiologicamente (2%) o per effetto di sostanze ossidanti, lo ione Fe2+ si trasforma in
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Osmometria ed Emolisi
 Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE 1) Il collagene è una proteina (globulare / fibrosa). È formata da tre (catene alfa/alfa eliche) con andamento (destrorso/sinistrorso) che vanno
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE 1) Il collagene è una proteina (globulare / fibrosa). È formata da tre (catene alfa/alfa eliche) con andamento (destrorso/sinistrorso) che vanno
Effetti dell altitudine su cuore, polmone e circolazione
 Effetti dell altitudine su cuore, polmone e circolazione 2.035 metri Marina Tricoli, ASP 6 Palermo Sestriere 28 A livello del mare.. La pressione barometrica è 760 mmhg La pressione parziale di O2 dell
Effetti dell altitudine su cuore, polmone e circolazione 2.035 metri Marina Tricoli, ASP 6 Palermo Sestriere 28 A livello del mare.. La pressione barometrica è 760 mmhg La pressione parziale di O2 dell
Apparato Respiratorio
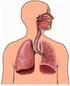 Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia e Biofisica A.A. 2016-2017 Apparato Respiratorio Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unina2.it
Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia e Biofisica A.A. 2016-2017 Apparato Respiratorio Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unina2.it
 Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Misure di gas disciolti
 Misure di gas disciolti Misura dell ossigeno Elettrodo di ossigeno L elettrodo Clark Misura di anidride carbonica Misurazione transcutanea dei gas nel sangue Monitoraggio transcutaneo di anidride carbonica
Misure di gas disciolti Misura dell ossigeno Elettrodo di ossigeno L elettrodo Clark Misura di anidride carbonica Misurazione transcutanea dei gas nel sangue Monitoraggio transcutaneo di anidride carbonica
po % O % N % CO 2 = 159 mmhg pn 2 = 597 mmhg pco 2 = 0.3 mmhg
 Scambi alveolari L aria che respiriamo è una miscela di gas, principalmente costituita da O 2, N 2 e CO 2. La velocità di diffusione di ciascuno di questi gas (quantità di gas che diffonde nell unità di
Scambi alveolari L aria che respiriamo è una miscela di gas, principalmente costituita da O 2, N 2 e CO 2. La velocità di diffusione di ciascuno di questi gas (quantità di gas che diffonde nell unità di
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Connessioni. Le cellule cardiache sono unite tra loro da parti più ispessite del sarcolemma dette: Gap - junction
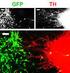 Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
matrice Sp. Interm. Il gambo (γε) cilindro C10 ruota con esso H + H+ H + H + H + H H + H H + H + H + H +
 I protoni si muovono secondo gradiente attraverso un canale d ingresso creato dalla subunità a e raggiungono il cilindro c 10. Quando una subunità c lega 1 un altro è rilasciato nella matrice lasciando
I protoni si muovono secondo gradiente attraverso un canale d ingresso creato dalla subunità a e raggiungono il cilindro c 10. Quando una subunità c lega 1 un altro è rilasciato nella matrice lasciando
Proprietà delle Soluzioni
 Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
Il sangue: il fluido della vita
 Il sangue: il fluido della vita Nutrirsi Respirare Eliminare i rifiuti Apparato circolatorio Le funzioni del sangue Trasporta i gas disciolti; Distribuisce le sostanze nutritive; Raccoglie le sostanze
Il sangue: il fluido della vita Nutrirsi Respirare Eliminare i rifiuti Apparato circolatorio Le funzioni del sangue Trasporta i gas disciolti; Distribuisce le sostanze nutritive; Raccoglie le sostanze
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Trasporto di ossigeno. Dr. Emilio D Avino Dip.to Cardioscienze AOSP SCAMILLO-FORLANINI ROMA
 Trasporto di ossigeno Dr. Emilio D Avino Dip.to Cardioscienze AOSP SCAMILLO-FORLANINI ROMA O 2 A B C OBIETTIVI DELLA LEZIONE 1. Comprendere le modalità di trasporto dei gas respiratori nel sangue 2. Comprendere
Trasporto di ossigeno Dr. Emilio D Avino Dip.to Cardioscienze AOSP SCAMILLO-FORLANINI ROMA O 2 A B C OBIETTIVI DELLA LEZIONE 1. Comprendere le modalità di trasporto dei gas respiratori nel sangue 2. Comprendere
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
gruppo prostetico) Cromoproteine Legare l ossigeno Impedire che ossidi altre sostanze Cedere O 2 in particolari e ben definite condizioni
 Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Utilizzazione dei dati di monitoraggio biologico
 Utilizzazione dei dati di monitoraggio biologico a livello individuale: valutazione del livello di di esposizione in in funzione dei valori di di riferimento e dei valori limite biologici health based
Utilizzazione dei dati di monitoraggio biologico a livello individuale: valutazione del livello di di esposizione in in funzione dei valori di di riferimento e dei valori limite biologici health based
FARMACODINAMICA. La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci.
 FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
Apparato respiratorio
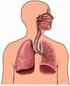 Apparato respiratorio Anatomia Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre muscolari
Apparato respiratorio Anatomia Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre muscolari
Apparato respiratorio. Anatomia
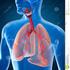 Apparato respiratorio Anatomia 1 Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre
Apparato respiratorio Anatomia 1 Le vie aeree: di conduzione e di scambio 3 L Trachea, bronchi principali, bronchioli (diametro 1 mm) sono dotati di struttura cartilaginea ad anello incompleto e fibre
Anatomia biochimica di un mitocondrio
 Anatomia biochimica di un mitocondrio Le involuzioni(creste)aumentano considerevolmente l area della superficie della membrana interna. La membrana interna di un singolo mitocondrio può avere anche più
Anatomia biochimica di un mitocondrio Le involuzioni(creste)aumentano considerevolmente l area della superficie della membrana interna. La membrana interna di un singolo mitocondrio può avere anche più
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI
 EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
COMPOSTI DI COORDINAZIONE
 CMPSTI DI CRDIAZIE Gli elementi di transizione hanno proprietà che variano relativamente poco andando da sinistra a destra lungo la tavola periodica; hanno inoltre la caratteristica di avere orbitali d
CMPSTI DI CRDIAZIE Gli elementi di transizione hanno proprietà che variano relativamente poco andando da sinistra a destra lungo la tavola periodica; hanno inoltre la caratteristica di avere orbitali d
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
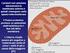 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi
 Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Fosforilazione ossidativa
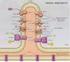 Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
ANEMIE : slidetube.it
 ANEMIE : Condizioni in cui il numero dei GR o il contenuto di Hb diminuiscono a causa di perdita ematica, eritropoiesi insufficiente, emolisi eccessiva o una combinazione di queste modificazioni. Una difettosa
ANEMIE : Condizioni in cui il numero dei GR o il contenuto di Hb diminuiscono a causa di perdita ematica, eritropoiesi insufficiente, emolisi eccessiva o una combinazione di queste modificazioni. Una difettosa
Gli equilibri di solubilità
 Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
TALASSEMIE (ANEMIA MEDITERRANEA)
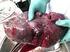 TALASSEMIE (ANEMIA MEDITERRANEA) Difetti genetici della sintesi di una o più catene globiniche normali Inadeguata produzione di emoglobina Anemia ipocromica-microcitica Sintesi bilanciata di catene globiniche,
TALASSEMIE (ANEMIA MEDITERRANEA) Difetti genetici della sintesi di una o più catene globiniche normali Inadeguata produzione di emoglobina Anemia ipocromica-microcitica Sintesi bilanciata di catene globiniche,
Apparato respiratorio
 Apparato respiratorio La respirazione Respirare è l attività che assolve l esigenza continua di fornire ossigeno alle nostre cellule affinché esse, attraverso la combustione delle sostanze nutritive, producano
Apparato respiratorio La respirazione Respirare è l attività che assolve l esigenza continua di fornire ossigeno alle nostre cellule affinché esse, attraverso la combustione delle sostanze nutritive, producano
FOSFORILAZIONE OSSIDATIVA
 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
