la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea
|
|
|
- Iolanda Cosentino
- 7 anni fa
- Visualizzazioni
Transcript
1 la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione in seguito al trattamento con
2 Le proprietà delle proteine che vengono sfruttate per ottenere lo scopo sono: La dimensione e forma il contenuto in aminoacidi acidi o basici: la carica di una proteina è la somma delle cariche (+) e (-) ad un determinato ph) il punto isoelettrico solubilità densità idrofobicità capacità a legare metalli o altre molecole specificità di sequenza o di struttura (anticorpi) presenza di modifiche post-traduzionali proprietà caratteristica (es. termolabilità)
3 OBIETTIVO: purificare una proteina I FASE: RICERCA BIBLIOGRAFICA DOMANDE: 1. Quali informazioni abbiamo? 2. Quali sono le caratteristiche della proteina? 3. Quali funzioni svolge nella cellula? 4. Dove è presente in elevate quantità? 5. Quali difficoltà ci aspettiamo di incontrare? II FASE: scelta della procedura DOMANDE: 1. Qualità o quantità? 2. Identificazione della fonte 3. Scelta dei passaggi FASE OPERATIVA Scelta del sistema biologico Tappe per il suo isolamento e purificazione Caratterizzazione GRADO DI PUREZZA Piccole quantità di contaminanti possono essere tollerate, dipende dalle indagini da effettuare Grado di purezza del 70% è sufficiente per la maggior parte delle analisi sperimentali Analisi cristallografica richiede campioni proteici puri
4 Fasi di una purificazione 1) sviluppo di un metodo di saggio adeguato 2) selezione del sistema biologico 3) Solubilizzazione della proteina 4) sviluppo dei passaggi di purificazione 5) concentrazione, conservazione
5 1) sviluppo di un metodo di saggio adeguato specifico sensibile poco costoso rapido saggio funzionale SDS-PAGE saggio immunologico marcatura (fluorescente o radioattiva)
6 2) selezione del migliore sistema biologico dove la proteina è maggiormente espressa Sistema dove la proteina può essere iperespressa
7 3) solubilizzazione della proteina e sviluppo dei passaggi di purificazione TEMPO, TEMPERATURA, ANTI-PROTEASI proteine proteine proteine intracellulari extracellulari di membrana disintegrazione separazione cellulare dalle cellule disintegrazione cellulare separazione da materiale insolubile (chiarificazione dell estratto)
8 Disintegrazione cellulare Metodi per rompere le cellule -metodi blandi lisi per osmosi digestione enzimatica solubilizzazione chimica omogenizzatori -metodi moderati omogenizzatori a lama mortaio -metodi vigorosi French press Sonicazione Macinazione con microsfere Na +, Ca 2+ K + Mg 2+ Coltura cellulare o tessuto Lisi per osmosi Shock osmotico
9 Digestione enzimatica Lisi della parete+ shock osmotico Solubilizzazione chimica O SO - 3 Na + Sodio dodecil solfato Omogeneizzazione con potter
10 Metodiche di omogenizzazione e lisi cellulare Potter, frullatori, French-press Metodiche per la separazione di organelli subcellulari (nuclei, mitocondri,ribosomi) Centrifugazione differenziale CONDIZIONI bassa temperatura uso di soluzioni tampone sterilità; uso di inibitori di proteasi
11
12 3) solubilizzazione della proteina e sviluppo dei passaggi di purificazione TEMPO, TEMPERATURA, ANTI-PROTEASI solubilita differenziale proteine proteine proteine intracellulari extracellulari di membrana disintegrazione separazione cellulare dalle cellule disintegrazione cellulare separazione da materiale insolubile (chiarificazione dell estratto)
13 Metodi di frazionamento - Le proteine vengono purificate tramite procedimenti di frazionamento. vengono sfruttate le proprietà chimico-fisiche della proteina di interesse a) la solubilità; b) la carica ionica; c) la massa molecolare d) l affinità di legame ad altre molecole e).
14 Perche in presenza di sali o metanolo le proteine precipitano? Le proteine differiscono nel numero di gruppi polari esposti al solvente La loro solubilita sara diversa in presenza di concentrazioni diverse di sali o solventi organici
15 Solubilità di una proteina dipende: Dalla concentrazione dei Sali disciolti Dalla polarità del solvente Dal ph Dalla temperatura SEPARAZIONE SELETTIVA DI PROTEINE CON I SALI SALTING IN a bassa concentrazione ionica l aggiunta l di un sale: Maschera i gruppi carichi della proteina Diminuisce le forze di attrazione tra le molecole LA SOLUBILITA DI UNA PROTEINA AUMENTA
16 + H + H O- Na + Cl - + H + H O- Na + Cl - + H + H O- I gruppi idrofobici sono rivolti verso l interno I gruppi idrofilici sono rivolti verso l esterno. + H Na + Cl - + H O- Na + Cl - al crescere della concentrazione salina i gruppi idrofobici delle proteine vengono scoperti
17 Questi frammenti idrofobici esposti causano l aggregazione delle proteine (interazioni idrofobiche) e la precipitazione salting out Precipitazione delle proteine meno solubili Precipitazione della proteina d interesse Precipitazione delle proteine più solubili 1.00 Frazione solubile [(NH 4 ) 2 SO 4 ] (M) Schema di precipitazione in presenza di Ammonio solfato Più la proteina contiene tratti idrofobici e piu risultera insolubile a basse concentrazioni saline (e viceversa)
18 Solubilita differenziale - salting out La solubilità di una proteina diminuisce quindi precipita (NH 4 ) 2 SO 4 influenza la sfera di idratazione delle proteine Favorisce le interazioni Idrofobiche tra le molecole e causa la loro precipitazione
19 PRECIPITAZIONE CON SOLVENTI ORGANICI In una soluzione acquosa contenente solventi organici (metanolo, etanolo, butanolo, acetone) le molecole di acqua si dispongono a idratare le molecole di solvente organico. L acqua di solvatazione viene quindi rimossa dai gruppi carichi e polari sulla superficie delle proteine. I gruppi carichi delle proteine vengono scoperti e le proteine si aggregano per la formazione di: interazioni ioniche precipitano in ordine decrescente a seconda del numero di gruppi carichi presenti sulla loro superficie e in misura maggiore man mano che aumenta la concentrazione del solvente
20 4) Sviluppo dei passaggi di purificazione TEMPO, TEMPERATURA, ANTI-PROTEASI solubilita differenziale proteine proteine proteine intracellulari extracellulari di membrana disintegrazione separazione cellulare dalle cellule disintegrazione cellulare separazione da materiale insolubile (chiarificazione dell estratto) isolamento della isolamento frazione cellulare della frazione di membrana, solubilizzazione
21 Centrifugazione differenziale Fc = mω 2 r
22 Frazione
23 La velocità di sedimentazione di una particella può essere espressa in termini di coefficiente di sedimentazione (s) che corrisponde alla velocità di sedimentazione per unità di campo centrifugo applicato Il coefficiente di sedimentazione ha le dimensioni di un tempo e si misura in Svedberg, S. 1 S = sec Esempio: s = 5 x sec corrisponde a 5S Specie sedimentate Enzimi, ormoni e proteine Acidi nucleici Ribosomi, polisomi Virus Lisosomi Membrane Mitocondri Coeff. di sedimentazione 2 25S 3 100S S S 4000S S S
24 Centrifugazione - coefficiente di sedimentazione e densita 150,000g /40min 10,000g /20min 1,000g /2min
25 Consente di separare una o più molecole disciolte in una soluzione sulla base delle loro dimensioni. membrana semipermeabile che permette il passaggio selettivo di molecole. Il movimento delle molecole si realizza a partire da una differenza di concentrazione (gradiente) di ciascuna di esse tra i soluti presenti nei due compartimenti, quello all interno del tubo e quello all esterno. La diffusione si arresta al raggiungimento dell equilibrio
26 4) Sviluppo dei passaggi di purificazione TEMPO, TEMPERATURA, ANTI-PROTEASI solubilita differenziale proteine proteine proteine intracellulari extracellulari di membrana disintegrazione separazione cellulare dalle cellule disintegrazione cellulare separazione da materiale insolubile (chiarificazione dell estratto) isolamento della isolamento frazione cellulare della frazione di membrana, solubilizzazione tecniche cromatografiche (logica nella sequenza)
27 Utilizzando tali metodiche si ottiene: UN ESTRATTO PROTEICO TOTALE PER ISOLARE LA PROTEINA di INTERESSE Metodiche sequenziali per il frazionamento (separazione) delle diverse proteine presenti nell estratto Cromatografia Scambio ionico Gel filtrazione Interazione idrofobica Di affinità
28 Cromatografia a scambio ionico
29 Gradiente salino: il tampone di eluizione è a concentrazione salina Crescente, elevate concentrazioni saline tendono a distruggere le interazioni elettrostatiche
30 Cromatografia per filtrazione su gel (gel-filtrazione)
31 Si determina il Kav di sostanze a peso molecolare noto
32 Cromatografia di affinità
33 Durante la procedura di purificazione occorrono inoltre metodiche per: identificare univocamente la proteina da purificare al fine di seguirne il processo di purificazione valutare la presenza delle proteine totali (metodi ottici) enzima attività enzimatica proteine proprietà ottiche antigene reazione con anticorpo SAGGIO DI ATTIVITA Dopo ogni stadio di purificazione il campione proteico si arricchisce della proteina di interesse in seguito all allontanamento delle altre proteine (Proteine totali) dette contaminanti
34 DETERMINAZIONE DELLA CONCENTRAZIONE TOTALE DELLE PROTEINE IN UN CAMPIONE Metodo diretto: assorbimento a 280 nm Metodi indiretti: Biureto: Formazione di complessi colorati tra Cu ++ ed i legami peptidici (550nm) Lowry: Biureto e riduzione con acidi fosfomolibdotungstici (750 nm) Bradford: Formazione di complessi tra proteine ed il coomassie si forma un prodotto colorato che assorbe a 595nm
35 Determinazione della concentrazione proteica mediante spettrofotometria Spettro di assorbimento UV-VIS VIS di una proteina Assorbimento Picco di assorbimento di Tirosina, Triptofano e Fenilalanina (nm)
36 Il legame del colorante Coomassie Brilliant Blue G-250 alle proteine determina massimo di assorbimento del colorante a 595 nm (blu) in soluzioni acide (Bradford, 1976) OCH 2 CH 3 Coomassie Brilliant Blu R Tale colorante forma forti complessi non covalenti con le proteine tramite interazioni elettrostatiche con gruppi amminici e carbossilici HN N SO 3 Na unico passaggio: il colorante è aggiunto ai campioni e si determina l assorbanza a 595 nm N+ SO 3 Na
37 La quantità di colorante che si lega è proporzionale alla quantità di proteina presente in soluzione. Curva standard per ogni saggio 1 mg/ml 2 mg/ml 4 mg/ml 8 mg/ml 16 mg/ml X mg/ml
38 LA LEGGE DI LAMBERT-BEER I t / I 0 =10 -εcl l = il cammino ottico (cm) c = concentrazione molare del soluto ε = coefficiente di estinsione molare, costante caratteristica di ogni soluto ma il log I 0 /I t = E = ε c l E = ε c l E= Densità ottica o ASSORBANZA è direttamente proporzionale alla concentrazione del soluto che sta assorbendo la luce
39 µg di proteina Intensità del colore blu Assorbanza a 595 nm
40 Ogni passaggio della procedura di purificazione viene determinata: la quantità di proteine totali e le unità di attività enzimatica della proteina di interesse. Una unità enzimatica (U) è definita come la quantità di enzima richiesta per convertire 1 µmol di substrato in prodotto in 1 min in condizioni definite (generalmente 25 o 30 C, ad un valore di ph ottimale). RESA mg o U di proteina di interesse nella frazione mg o U di proteina di interesse nella preparazione originale Il grado di purezza è espresso come: ATTIVITA SPECIFICA ATTIVITA SPECIFICA U di enzima di interesse nella frazione mg di proteine totali nella frazione
41 Nel corso di una purificazione ottimale la resa diminuisce e l attività specifica aumenta
42 Tabella di purificazione dell enzima NADH ossidasi da 120 g di cellule batteriche Stadio di purificazione Proteine totali (mg) Attività Totale (Unità) Attività Specifica (U/mg) Resa (%) Arricchimento (n. volte) omogenato , Centrifugazione , (fraz. Solubile) Precipitazione , Con (NH 4 ) 2 SO 4 DEAE-Sepharose 4,3 5,1 1, Cromatografia di affinità 1,1 4,7 4, Gel fitration 0,54 4,3 8,
43 Purificazione dell'inibitore della tripsina da endosperma di grano (Wheat Trypsin Inhibitor) passaggi Vol (ml) Proteina (mg) Attività specifica Resa % Unità totali estrazione salina frazionamento con (NH 4)2SO Sephadex G CM -sepharose CL 6B Mono S purificazione : 4802/25 = 192 volte
44 Fissaggio del gel in metanolo e acido acetico Colorazione con Blu di Coomassie Valutazione della PUREZZA DEI CAMPIONI DETERMINAZIONE DEL PESO MOLECOLARE delle proteine rispetto a STANDARD DI RIFERIMENTO Nell esempio la purificazione dell enzima RNA Polimerasi da E.Coli
45 X X
46
47 Esempio di purificazione di una proteina
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Passaggi preliminari di purificazione
 Passaggi preliminari di purificazione Estratto iniziale Omogenato contiene materiale insolubile che generalmente viene eliminato per centrifugazione. Talvolta la soluzione mostra torbidità (dovuta alla
Passaggi preliminari di purificazione Estratto iniziale Omogenato contiene materiale insolubile che generalmente viene eliminato per centrifugazione. Talvolta la soluzione mostra torbidità (dovuta alla
MATERIALE DIDATTICO. A supporto sono rese disponibili le slides delle lezioni
 MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
PURIFICAZIONE DELLE PROTEINE
 PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Acidi nucleici come materiale di studio. DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna
 Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
l'analisi dello spettro permette di individuare la natura della sostanza in esame
 L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi delle Proteine
 Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
DOSAGGIO ACIDI NUCLEICI
 DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
Determinazioni quantitative in farmacologia
 Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
A = εlc c = A/εl c = 0.2/38000 M -1 cm -1 1 cm c = M = 5 μm
 COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
Seminario di Cacciatore Rosalia
 Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Strategie di purificazione di proteine
 Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
5- Estrazione ed analisi di DNA
 5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
Estrazione di proteine - Scelta della fonte biologica
 Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Metodi di studio delle proteine (o altre macromolecole)
 Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA
 TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA TIPI DI CENTRIFUGHE CENTRIFUGHE PREPARATIVE Consentono la separazione, isolamento e purificazione
TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA TIPI DI CENTRIFUGHE CENTRIFUGHE PREPARATIVE Consentono la separazione, isolamento e purificazione
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
Dosaggio delle proteine
 Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
differente ripartizione delle sostanze tra due fasi immiscibili
 Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Strategia generale per la purificazione: metodi di frazionamento.
 Strategia generale per la purificazione: metodi di frazionamento. - Il fatto che le proteine fossero sostanze chimiche ben definite non venne accettato per intero finché James Sumner nel 1926 cristallizzò
Strategia generale per la purificazione: metodi di frazionamento. - Il fatto che le proteine fossero sostanze chimiche ben definite non venne accettato per intero finché James Sumner nel 1926 cristallizzò
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
I compartimenti intracellulari e gli organelli citoplasmatici
 I compartimenti intracellulari e gli organelli citoplasmatici Con lo sviluppo della microscopia elettronica (anni 40) si scoprì che nel citoplasma delle cellule eucariote è presente un complesso sistema
I compartimenti intracellulari e gli organelli citoplasmatici Con lo sviluppo della microscopia elettronica (anni 40) si scoprì che nel citoplasma delle cellule eucariote è presente un complesso sistema
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Preparazione del campione analitico
 Preparazione del campione analitico Workflow per l analisi farmaceutica Lotto Totalità del materiale Campionamento Il campione deve essere rappresentativo del lotto Conservazione Preparazione campione
Preparazione del campione analitico Workflow per l analisi farmaceutica Lotto Totalità del materiale Campionamento Il campione deve essere rappresentativo del lotto Conservazione Preparazione campione
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- Ricevimento: Martedì (Dipartimento di Biologia, dente L)
 Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- nadia.dambrosi@uniroma2.it Ricevimento: Martedì 14-16 (Dipartimento di Biologia, dente L) Organizzazione del corso: Lunedì h9-11 fino al 28/5 - didattica
Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- nadia.dambrosi@uniroma2.it Ricevimento: Martedì 14-16 (Dipartimento di Biologia, dente L) Organizzazione del corso: Lunedì h9-11 fino al 28/5 - didattica
Fondamenti di spettroscopia. Spettrofotometria UV/Vis (Tecnica analitica)
 Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Le soluzioni: Le soluzioni sono miscele omogenee di due o più componenti.
 Le soluzioni: Affinchè le molecole di specie diverse possano reagire fra di loro è necessario che si incontrino ed urtino le une con le altre. E chiaro che questa possibilità di urto è favorita quando
Le soluzioni: Affinchè le molecole di specie diverse possano reagire fra di loro è necessario che si incontrino ed urtino le une con le altre. E chiaro che questa possibilità di urto è favorita quando
OGRAMMA DI CHIMICA 2016
 ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE
 Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA
 Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
metodi poco sensibili, laboriosi, costosi, e indaginosi
 dosaggi ormonali L ANALISI CHIMICA fasi di isolamento, purificazione e concentrazione elaborate non sufficientemente sensibile per il dosaggio di tutti gli ormoni nel sangue metodi poco sensibili, laboriosi,
dosaggi ormonali L ANALISI CHIMICA fasi di isolamento, purificazione e concentrazione elaborate non sufficientemente sensibile per il dosaggio di tutti gli ormoni nel sangue metodi poco sensibili, laboriosi,
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Estrazione di DNA. Laboratorio di Biologia Applicata
 Estrazione di DNA Laboratorio di Biologia Applicata Tecniche di estrazione Qualità del campione di partenza Numero di campioni Costo Tempo Semplicità e affidabilità Automazione Sicurezza Materiale biologico
Estrazione di DNA Laboratorio di Biologia Applicata Tecniche di estrazione Qualità del campione di partenza Numero di campioni Costo Tempo Semplicità e affidabilità Automazione Sicurezza Materiale biologico
Docente di BIOCHIMICA APPLICATA per CTF: Prof.ssa Alessandra Olianas
 Tutor Farmacia: dott. Simone Serrao simone.serrao@unica.it Tutor CTF: dott. Gianluigi Cabiddu gianluigi-c@live.it Docente di BIOCHIMICA APPLICATA per CTF: Prof.ssa Alessandra Olianas olianas@unica.it Orari
Tutor Farmacia: dott. Simone Serrao simone.serrao@unica.it Tutor CTF: dott. Gianluigi Cabiddu gianluigi-c@live.it Docente di BIOCHIMICA APPLICATA per CTF: Prof.ssa Alessandra Olianas olianas@unica.it Orari
Fisiologia cellulare e Laboratorio di colture cellulari
 Corso di laurea in Biotecnologie UNIVERSITA DEGLI STUDI DI TERAMO Fisiologia cellulare e Laboratorio di colture cellulari Prof.ssa Luisa Gioia possibili sistemi di trasporto della cellula TRASPORTO TRANS-MEMBRANA
Corso di laurea in Biotecnologie UNIVERSITA DEGLI STUDI DI TERAMO Fisiologia cellulare e Laboratorio di colture cellulari Prof.ssa Luisa Gioia possibili sistemi di trasporto della cellula TRASPORTO TRANS-MEMBRANA
Chimica Analitica e Laboratorio 2. Modulo di Spettroscopia Analitica
 Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Caratteristiche delle membrane biologiche
 Membrane Biologiche Caratteristiche delle membrane biologiche 1. Le membrane sono strutture a foglio che formano setti di separazione tra compartimenti con composizione diversa tra loro. 2. Sono costituite
Membrane Biologiche Caratteristiche delle membrane biologiche 1. Le membrane sono strutture a foglio che formano setti di separazione tra compartimenti con composizione diversa tra loro. 2. Sono costituite
Laboratorio di Biologia Molecolare
 UNIVERSITÀ DEGLI STUDI DELL AQUILA DIPARTIMENTO DI MEDICINA CLINICA, SANITÀ PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE in collaborazione con Laboratorio di Biologia Molecolare Estrazione del DNA da tessuto
UNIVERSITÀ DEGLI STUDI DELL AQUILA DIPARTIMENTO DI MEDICINA CLINICA, SANITÀ PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE in collaborazione con Laboratorio di Biologia Molecolare Estrazione del DNA da tessuto
BIOFISICA DELLE MEMBRANE
 BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante scambio di sostanze ed informazioni attraverso membrane. Membrana = struttura che separa due mezzi diversi
BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante scambio di sostanze ed informazioni attraverso membrane. Membrana = struttura che separa due mezzi diversi
Estrazione con solventi. Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti
 Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
TECNOLOGIE BIOMOLECOLARI
 TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
- determinazione colorimetrica della concentrazione di una miscela proteica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2017/2018 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2017/2018 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Spettrofotometria. Foto di Clotilde B. Angelucci
 Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
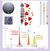 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Determinazione del contenuto di licopene
 Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE
 CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
Soluzioni RAGIONAMENTO LOGICO E CULTURA GENERALE. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta.
 Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Spettroscopia nell ultravioletto e nel visibile
 Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Soluzioni, elettroliti e non
 Soluzioni, elettroliti e non Il processo di solubilizzazione è un processo complesso, per interpretarlo occorre conoscere la natura ei legami chimici coinvolti COSA CONSIDERARE? 1) Interazioni soluto -
Soluzioni, elettroliti e non Il processo di solubilizzazione è un processo complesso, per interpretarlo occorre conoscere la natura ei legami chimici coinvolti COSA CONSIDERARE? 1) Interazioni soluto -
Di cosa è fatta una cellula?
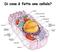 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA
 MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA ISTITUTO TECNICO COMMERCIALE LORGNA-PINDEMONTE VERONA INDIRIZZO AMMINISTRAZIONE, FINANZA E MARKETING/TURISMO PROGRAMMA ANALITICO
MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA ISTITUTO TECNICO COMMERCIALE LORGNA-PINDEMONTE VERONA INDIRIZZO AMMINISTRAZIONE, FINANZA E MARKETING/TURISMO PROGRAMMA ANALITICO
Test di ingresso LM Scienze Chimiche A. A
 Università degli Studi di Cagliari Test di ingresso LM Scienze Chimiche A. A. 2009-2010 Test di ingresso alla LM in Scienze Chimiche A.A. 2009 2010 1 Chimica Analitica 1) Indicare, tra quelle riportate
Università degli Studi di Cagliari Test di ingresso LM Scienze Chimiche A. A. 2009-2010 Test di ingresso alla LM in Scienze Chimiche A.A. 2009 2010 1 Chimica Analitica 1) Indicare, tra quelle riportate
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
LE PROPRIETÀ DELLE SOLUZIONI
 LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Elemento fondamentale
 Acqua Elemento fondamentale Usata x 90% Produzione Malteria Caldaie frigoriferi Lavaggio e sterilizzazione Ruoli dell acqua Permette il trasporto e la distribuzione nelle cellule delle sostanze Garantisce
Acqua Elemento fondamentale Usata x 90% Produzione Malteria Caldaie frigoriferi Lavaggio e sterilizzazione Ruoli dell acqua Permette il trasporto e la distribuzione nelle cellule delle sostanze Garantisce
Estrazione ed elettroforesi degli acidi nucleici
 Estrazione ed elettroforesi degli acidi nucleici Flavia Frabetti Estrazione acidi nucleici (DNA orna) Verifica tramite elettroforesi su gel di agarosio Amplificazione tramite PCR (da DNA) o RT-PCR (da
Estrazione ed elettroforesi degli acidi nucleici Flavia Frabetti Estrazione acidi nucleici (DNA orna) Verifica tramite elettroforesi su gel di agarosio Amplificazione tramite PCR (da DNA) o RT-PCR (da
Membrane Biologiche. Barriere per confinare sostanze o attività in ambienti specifici. Costituite da lipidi e proteine. Confini Cellulari Organelli
 Membrane Biologiche Membrane Biologiche Barriere per confinare sostanze o attività in ambienti specifici. Confini Cellulari Organelli Costituite da lipidi e proteine. Sistema di Endomembrane Delimitano
Membrane Biologiche Membrane Biologiche Barriere per confinare sostanze o attività in ambienti specifici. Confini Cellulari Organelli Costituite da lipidi e proteine. Sistema di Endomembrane Delimitano
Primo Levi Il sistema periodico
 Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Chimica e laboratorio
 ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
Membrana, trasporti, nutrizione, enzimi
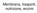 Membrana, trasporti, nutrizione, enzimi LA MEMBRANA PLASMATICA: - DETERMINA UNA COMPARTIMENTAZIONE; - FUNGE DA BARRIERA CON PERMEABILITA SELETTIVA; - TRASPORTA SOLUTI; - RISPONDE A SEGNALI ESTERNI; - PRESIEDE
Membrana, trasporti, nutrizione, enzimi LA MEMBRANA PLASMATICA: - DETERMINA UNA COMPARTIMENTAZIONE; - FUNGE DA BARRIERA CON PERMEABILITA SELETTIVA; - TRASPORTA SOLUTI; - RISPONDE A SEGNALI ESTERNI; - PRESIEDE
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
Tecniche Centrifugative
 Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
Solubilità dei sali Prodotto di solubilità
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
CARATTERIZZAZIONE DELLE INTERAZIONI
 CARATTERIZZAZIONE DELLE INTERAZIONI Costante di legame Concentrazione delle due specie Interazione Competizione con altre proteine Cofattori Compartimentazione cellulare Fattori che influenzano l interazione
CARATTERIZZAZIONE DELLE INTERAZIONI Costante di legame Concentrazione delle due specie Interazione Competizione con altre proteine Cofattori Compartimentazione cellulare Fattori che influenzano l interazione
