CHIMICA ORGANICA CHIMICA ORGANICA 14.A PRE-REQUISITI 14.B PRE-TEST 14.C OBIETTIVI 14.4 I POLIMERI 14.1 INTRODUZIONE: I COMPOSTI ORGANICI DEL CARBONIO
|
|
|
- Roberto Ruggiero
- 7 anni fa
- Visualizzazioni
Transcript
1 CIMICA RGANICA 14.A PRE-REQUISITI 14.B PRE-TEST 14.C BIETTIVI 14.1 INTRDUZINE: I CMPSTI RGANICI DEL CARBNI RAPPRESENTAZINE DELLE MLECLE ISMERIA 14.2 IDRCARBURI ETERI CMPSTI CARBNILICI: ALDEIDI E CETNI ACIDI CARBSSILICI E LR DERIVATI AMMINE 14.4 I PLIMERI PLIMERI DI CNDENSAZINE PLIMERI DI ADDIZINE 14.V VERIFICA SE AI CAPIT ESERCIZI ALCANI IDRCARBURI INSATURI: ALCENI E ALCINI IL BENZENE E GLI IDRCARBURI ARMATICI 14.3 CLASSI FUNZINALI ALCLI
2 14.A PRE-REQUISITI Prima di iniziare a lavorare su questa Unità, dovresti essere in grado di: comprendere il significato della reazione chimica, del simbolo che la rappresenta e del meccanismo di reazione; spiegare il significato generale dell ibridazione ed enunciare le caratteristiche fondamentali delle ibridazioni sp 3, sp 2 ed sp del C; sapere cosa si intende per reazioni endotermiche ed esotermiche, e tra reazioni spontanee e non spontanee; conoscere il significato generale delle reazioni di ossidoriduzione (redox) ed eseguire il loro bilanciamento; comprendere dal punto di vista elettrochimico i processi di ossidazione e di riduzione; conoscere i principali tipi di legame e le condizioni in cui si formano, con particolare riferimento alla teoria del legame di valenza; definire l elettronegatività, mettendola in relazione con le caratteristiche delle molecole polari. 14.B PRE-TEST 1. Individua le classi funzionali cui appartengono i composti seguenti ed attribuisci ad ogni composto un nome: - C = C - - C - - C - C 2. Individua i prodotti di reazione: C C - + Cl (ossidazione) - C + 2 Soluzione
3 14.C BIETTIVI Al termine di questa Unità dovrai essere in grado di: applicare le conoscenze relative all ibridazione del C ad alcune categorie di composti organici; definire in termini generali il concetto di isomeria; comprendere il significato della delocalizzazione elettronica nel benzene e descrivere alcune caratteristiche dell anello aromatico; riconoscere alcuni composti semplici appartenenti agli idrocarburi alifatici ed aromatici, ed attribuire loro un nome; riconoscere in alcuni composti semplici i gruppi funzionali caratteristici di alcune classi di composti ed attribuire ad ogni composto un nome; enunciare alcune proprietà chimiche e fisiche delle principali classi di composti organici; per ogni classe funzionale, elencare alcuni metodi di preparazione ed alcune reazioni caratteristiche; descrivere alcuni metodi di polimerizzazione e conoscere le caratteristiche e le proprietà pricipali dei polimeri INTRDUZINE: I CMPSTI RGANICI DEL CARBNI Il carbonio, oltre ai composti inorganici, forma molecole che contengono principalmente C ed, e, in certi casi, elementi elettronegativi (come, N, P, S e alogeni), studiate nel campo della CIMICA RGANICA. I CMPSTI RGANICI sono caratterizzati da catene stabili di atomi di C di varia lunghezza e, grazie alle proprietà del C, possono essere formati in numero elevatissimo. Nei composti organici il C (configurazione esterna s 2 p 2 ) forma quattro legami covalenti e una volta completato l ottetto non tende a formare ulteriori legami, per cui dà origine a catene o anelli molto stabili.
4 - C - C - C - C - C - C - I legami C-C, possono essere legami semplici, doppi o tripli, mentre i legami non impegnati nelle catene C-C vengono saturati da atomi di o da altri gruppi atomici (detti gruppi funzionali). Tutte le molecole che presentano lo stesso gruppo funzionale possono essere considerate come appartenenti ad una stessa famiglia, chiamata classe funzionale. E stato messo a punto un sistema di nomenclatura che consente di attribuire un nome ad ogni molecola sulla base della sua struttura, ed associa ad ogni classe funzionale un suffisso caratteristico. Trattando gli alcani, verrà descritto il metodo nel suo insieme, e per ogni classe funzionale verranno fatti ulteriori esempi. ESEMPI Molecole contenenti il gruppo - classe funzionale: alcoli Appartengono alla classe (cominciando dai composti a basso peso molecolare): - metanolo - etanolo - propanolo RAPPRESENTAZINE DELLE MLECLE I composti organici possono essere rappresentati attraverso vari tipi di formule: formula molecolare: compaiono gli atomi che costituiscono la molecola ed il loro numero relativo, ma non fornisce informazioni sulla struttura della molecola; formula di struttura: mette in evidenza la disposizione degli atomi nello spazio; spesso rendere la geometria tridimensionale sulla carta crea qualche problema, per cui si usano rappresentazioni alternative, come modello tridimensionale (forse, il più preciso) formula che mostra la catena, in forma estesa o abbreviata (quest ultima, molto usata).
5 ESEMPI Per alcuni composti appartenenti alla serie omologa degli alcani: METAN ETAN PRPAN F. molecolare C 4 C 2 6 C 3 8 Mod. tridimensionale Catena - C - - C - C - - C - C - C - - -
6 ISMERIA In molti casi, ad una stessa formula molecolare corrispondono varie formule di struttura; i composti di questo tipo vengono detti ISMERI. Consideriamo due tipi di isomeria: DI STRUTTURA, in cui gli isomeri presentano diversa disposizione nei legami che uniscono gli atomi e possono appartenere a due serie omologhe diverse, oppure alla stessa. GEMETRICA, caratteristica dei composti contenenti doppi legami, legata alla posizione relativa dei sostituenti da parti opposte del doppio legame. Si ha ISMERIA GEMETRICA e le due molecole vengono indicate con cis - (sostituenti uguali dalla stessa parte) e trans - (da parti opposte). C = C cis butene C = C trans butene ESEMPI isomeria geometrica (cis-trans) Nel 2 - butene la rotazione che normalmente può avvenire attorno ad un legame semplice (come nel 1,2 - dicloroetano) è impedita a causa della presenza del doppio legame. Non è quindi possibile convertire una forma nell altra ruotando una parte della molecola di 180. Cl - C - C - Cl 1,2 - dicloroetano
7 isomeria di struttura - etanolo (alcoli) C dimetiletere (eteri) - butano C C - metilpropano (o isobutano)
8 C pentano - C - isopentano (2 - metilbutano) - C - neopentano (2,2 - dimetilpropano)
9 14.2 IDRCARBURI Gli IDRCARBURI sono composti che contengono esclusivamente C ed ; come si può vedere dallo schema, esistono: idrocarburi alifatici (con struttura a catena) - saturi (contenenti solo legami C-C semplici) - insaturi (contenenti anche doppi e tripli legami) idrocarburi aromatici, derivati dal benzene ALCANI Gli ALCANI sono idrocarburi SATURI in cui il C presenta ibridazione sp 3 e forma esclusivamente legami semplici. Possono avere catena lineare o ramificata. Le tabelle seguenti riassumono schematicamente le informazioni essenziali e presentano alcuni esempi. alifatici idrocarburi alcani alcheni alchini - C-C - - C=C - - C C - aromatici (anello benzenico) Alcani Legami - C - C- semplici (σ) ibridazione del carbonio : sp 3 Formula generale : C n 2n+2 (n = 1, 2, 3...) Nome: suffisso -ano Nome sostituente: suffisso -ile
10 Alcani Nome Formula Radicale corrispondente Nome metano C 4 - metile etano - - etile propano - - propile butano - - butile pentano - - pentile esano - - esile A parte i primi quattro termini, che hanno nomi comuni, il nome comprende una radice che indica il numero di atomi di carbonio presenti seguito dal suffisso -ano. Il radicale o sostituente corrispondente si ottiene eliminando un atomo di e trasformando il suffisso -ano in -ile. I nomi delle molecole degli alcani costituiscono la base per costruire i nomi delle molecole più complesse.
11 REGLE GENERALI DI NMENCLATURA 1. Si sceglie la catena più lunga e si usa il nome dell alcano corrispondente a questa catena come base; si considerano le ramificazioni come sostituenti della catena principale. 2. Si numera la catena in modo da dare ai sostituenti (cioè alle ramificazioni) numeri di posizione più bassi possibile. ESEMPI - C - C - 2, 2, 4 - trimetilpentano 3. Si attribuisce ad ogni sostituente un nome ed un numero di posizione (separati da un trattino). C 2-4. Per più sostituenti uguali, si usano prefissi di-, tri-, tetra-, ecc. e si indicano tutti i numeri di posizione, separandoli con la virgola. 5. Si dispongono i sostituenti in ordine alfabetico (i prefissi non contano), seguiti dal nome della catena base. - C - C metil propileptano
12 PRPRIETA FISICE DEGLI ALCANI Le proprietà variano regolarmente all aumentare del numero di atomi della molecola (forze intermolecolari progressivamente maggiori). La temperatura di ebollizione e la densità crescono con il numero di atomi di C. lineari. REAZINI CARATTERISTICE DEGLI ALCANI 1. REAZINI DI CMBUSTINE (reazione fortemente esotermica, da cui dipende l uso degli alcani come combustibili). I primi quattro termini (C 1 - C 4 ) sono gassosi, i dodici successivi (C 5 - C 16 ) sono liquidi ed i rimanenti sono solidi. C C calore prodotto = 882 kj/mol Sono insolubili in solventi polari, come l acqua, e solubili in solventi poco polari. Allo stato puro sono incolori, la viscosità dei termini liquidi cresce con la massa molecolare. Gli alcani ramificati sono in generale più volatili e meno densi; la variazione delle proprietà con la massa molare è meno regolare rispetto ai composti C /2 2 4 C calore prodotto = 3000 kj/mol 2. REAZINI DI SSTITUZINE Gli alcani hanno scarsa reattività nei confronti di molti reagenti; in presenza di luce, possono reagire con gli alogeni e dare reazioni in cui un atomo di
13 viene sostituito. La reazione ha un meccanismo a catena che coinvolge i cosiddetti radicali (specie che hanno un elettrone spaiato, molto reattive). Ad esempio, per il metano: C 4 + Cl 2 Cl + Cl 2 C 2 Cl 2 + Cl C Cl + Cl C 2 Cl 2 + Cl CCl 3 + Cl di posizione minore tra quelli dei due atomi di C legati dal doppio legame); inoltre, la catena viene numerata in modo da attribuire al doppio legame il più basso numero di posizione possibile. Le tabelle riportano le caratteristiche fondamentali degli alcheni e presentano i primi termini della famiglia; il composto con due atomi di C (nome sistematico: etene) viene comunemente chiamato etilene ; la struttura dell etilene è stata rappresentata trattando l ibridazione sp 2. CCl 3 + Cl 2 CCl 4 + Cl IDRCARBURI INSATURI: ALCENI E ALCINI Gli ALCENI, in cui il C è ibridato sp 2, presentano un doppio legame C-C, e contengono due atomi di in meno dei corrispondenti alcani. Per dare il nome alle molecole, si seguono le regole già viste, con aggiunta del suffisso -ene e del numero di posizione del doppio legame (il numero Alcheni Legami - C = C - doppi (σ + π) ibridazione del carbonio : sp 2 Formula generale : C n 2n ( n 2) Nome : alcano con desinenza - ene Possono dare isomeria geometrica (cis-trans)
14 Nome Alcheni Formula - C = C - ESEMPI 2 - metil butene etene (etilene) propene C 2 = C 2 C 2 = C C 2 = C - C = C 2 1, 3 - butadiene (prefisso di- perché sono presenti due doppi legami) 1-butene C 2 = CC 2 2 butene C = C 1-pentene C 2 = C (C 2 ) 2 REAZINI CARATTERISTICE DEGLI ALCENI Le più importanti reazioni sono reazioni di ADDIZINE al doppio legame (che si trasforma in un legame semplice); le addizioni tra alcheni sono anche alla base delle reazioni di polimerizzazione.
15 Addizione di alogeni Addizione di acidi alogenidrici Cl - Cl + C = C etene C 2 = C + F CF propene 2- fluoro- propano Addizione di idrogeno C 2 = C C C 2 C 2 1-butene butano Addizione di acqua 1,2 - dicloroetano Cl - C - C - Cl C 2 = C 2 + C 3 C 2 etene etanolo Gli ALCINI sono idrocarburi contenenti tripli legami (C ibridato sp); la nomenclatura è simile a quella degli alcani, sostituendo il suffisso -ene con -ino. Il primo termine (nome sistematico: etino) viene comunemente chiamato acetilene ; la struttura dell acetilene è stata illustrata a proposito dell ibridazione sp. Anche gli alchini danno reazioni di addizione al triplo legame, che si trasforma in
16 legame doppio. Alchini Alchini Legami - C C - tripli (σ + 2π) ibridazione del carbonio : sp Formula generale : C n 2n-2 ( n = 2, 3..) Nome : alcano con desinenza - ino Reazioni caratteristiche: addizione al (analoghe a quelle degli alcheni) Nome etino (acetilene) propino 1-butino 1-pentino 1-ottino Formula C C C C C C C 2 C C (C 2 ) 2 C C (C 2 ) 5 1-decino C C (C 2 ) 7
17 IL BENZENE E GLI IDRCARBURI ARMATICI Il BENZENE (C 6 6 ) è formato da un anello esagonale (detto ANELL ARMATIC) in cui gli atomi di C (ibridati sp 2 ) sono legati alternativamente da legami singoli e legami doppi; la molecola reale del benzene può essere considerata come intermedia tra le due strutture possibili. C C C C C C BENZENE C 6 6 Legami alternati - C = C - doppi (σ, π) ibridazione del carbonio : sp 2 I sei legami C - C sono tutti equivalenti, in quanto i legami p non sono localizzati tra atomi di carbonio specifici, ma distribuiti attorno all anello a sei atomi. Per rappresentare questo legame delocalizzato, il benzene viene spesso rappresentato da un esagono con un cerchio al suo interno. L anello aromatico può dare REAZINI DI SSTITUZINE.
18 Reazioni di sostituzione sull anello aromatico alcuni esempi mezzo para- sostituenti in posizioni opposte dell anello. alogenazione cloro-benzene Cl Benzene con due sostituenti + Cl 2 Cl + toluene orto-xilene meta-xilene nitrazione (N 3, acido nitrico) N 2 + N nitro-benzene para-xilene Gli idrocarburi aromatici hanno strutture derivate da quelle del benzene; se sono presenti due sostituenti, la loro posizione reciproca può essere indicata con i prefissi: orto - sostituenti su atomi di C adiacenti meta- sostituenti con un atomo di C in
19 14.3 CLASSI FUNZINALI Consideriamo rapidamente le principali categorie di composti organici che vengono definite dalla presenza nella molecola di un determinato GRUPP FUNZINALE; esso conferisce alla molecola proprietà chimiche caratteristiche e permette di raggruppare un vasto numero di composti in un numero relativamente limitato di classi. Le reazioni caratteristiche ed i metodi di preparazione di alcune importanti classi di composti (alcoli, aldeidi, chetoni, acidi carbossilici) che comportano ossidazione/riduzione (reazioni redox) possono essere rappresentate con lo schema seguente, cui si farà riferimento in seguito: (ox) alcool primario aldeide alcool secondario chetone (rid) (ox) acido carbossilico (rid) mediante ossidazione si passa da alcool 1 ad aldeide ad acido carbossilico; mediante riduzione si passa da acido carbossilico ad aldeide ad alcool 1 ; ossidando un alcool 2 si ottiene un chetone, riducendo un chetone si ottiene un alcool ALCLI Consideriamo la classe funzionale degli ALCLI. Alcoli (R - ) gruppo funzionale - ( ossidrile) nome : idrocarburo con desinenza - olo (se necessario, indicando il numero di posizione dell sulla catena)
20 Alcoli Nome Formula p eb ( C) solubilità in 2 % metanolo 64,5 etanolo C 2 78,3 1-propanolo (C 2 ) butanolo (C 2 ) ,9 1-pentanolo (C 2 ) ,3 1-esanolo (C 2 ) ,6
21 ESEMPI C cloroetanolo (alcool PRIMARI, R - ) Cl - C propanolo (alcool SECNDARI, R 2 - C - ) R 1 R 1 - C metil - 2 butanolo (alcool TERZIARI, R 2 - C - ) R 3 R rappresenta un qualsiasi radicale (ad esempio, metile, etile, ecc.). Gli alcoli primari, secondari e terziari hanno reattività diversa, in particolare riguardo all ossidazione: ossidando un alcool primario si ottiene un aldeide ossidando un alcool secondario si ottiene un chetone gli alcoli terziari vengono ossidati con difficoltà
22 I composti in cui il gruppo - è direttamente legato ad un anello aromatico si chiamano FENLI; ad esempio: Proprietà degli alcoli T eb > di quelle degli alcani corrispondenti (molecole polari - legame idrogeno) l l - C - - C - l l Solubilità completa in solventi polari fino a C 4 I composti contenenti più gruppi - sulla stessa molecola sono detti GLICLI; nel loro nome, il suffisso - olo è preceduto da un prefisso moltiplicativo. 1,2 - etandiolo (glicole etilenico) 1,2,3 - propantriolo (glicerolo, glicerina) - C - C - - C - C - C - Il gruppo - rende la molecola polare e, grazie alla formazione di legame a idrogeno tra molecole adiacenti, le sostanze sono meno volatili e hanno temperature di ebollizione più elevate rispetto agli alcani corrispondenti. L effetto dell si indebolisce a mano a mano che la catena idrocarburica si allunga; ciò influenza anche la solubilità in solventi polari, come 2.
23 METDI DI PREPARAZINE Addizione di acqua agli alcheni - l l - C = C C - C - l l l l Riduzione di aldeidi, chetoni e acidi carbossilici Specificamente per l Alcol Etilico fermentazione degli zuccheri C C C 2 glucosio etanolo Per riduzione di un aldeide si ottiene un alcol primario; partendo da un acido carbossilico, questo viene prima ridotto ad aldeide, poi ad alcool. Riducendo un chetone si ottiene, invece, un alcool secondario ETERI Gli ETERI sono composti di formula generale R 1 R 2. Nel nome si indicano i radicali (R 1 ed R 2, che possono essere uguali o diversi) seguiti da etere. ESEMPI dimetiletere C 2 etilmetiletere Sono composti complessivamente poco reattivi, in quanto il legame etereo è stabile. Riguardo agli usi, alcuni eteri vengono usati come anestetici CMPSTI CARBNILICI: ALDEIDI E CETNI Entrambe le classi di composti sono caratterizzate
24 dal GRUPP CARBNILIC ( C = ), in cui il doppio legame è fortemente polare a causa della differenza di elettronegatività tra i due atomi, ma il cui effetto sulle proprietà fisiche è minore rispetto al gruppo -. Il gruppo funzionale occupa nei due casi posizioni diverse: gruppo carbonilico in posizione terminale della catena: ALDEIDI, formula generale R - C - (un radicale e un legati al ( C = ) Aldeidi Esempi C metanale (aldeide formica) - C - (C 2 ) 10 - C R - C = Gruppo funzionale - C (carbonilico aldeidico) Nome : idrocarburo con desinenza - ale (il C del gruppo carbonilico è generalmente in posizione 1) etanale (aldeide acetica) dodecanale gruppo carbonilico all interno della catena: CETNI, formula generale R - C - R (due radicali legati al C=) Preparazione : ossidazione di alcoli primari Cr C C = etanolo etanale
25 METDI DI PREPARAZINE: le aldeidi possono essere ottenute per ossidazione di un alcool primario. REAZINI CARATTERISTICE: per riduzione di un aldeide si ottiene un alcool primario (reazione inversa rispetto alla preparazione) per ossidazione di un aldeide si ottiene un acido carbossilico Chetoni R - C - R ll Gruppo funzionale - C (all interno della catena) Nome : idrocarburo con desinenza - one (indicando il numero di posizione del carbonile) Esempi - C - ll 2 - esanone - C - ll 2 - butanone - C - ll 3 - esanone Preparazione : ossidazione di alcoli secondari - C - - C - (2) - propanone (acetone)
26 METDI DI PREPARAZINE: i chetoni possono essere ottenuti per ossidazione di un alcool secondario ACIDI CARBSSILICI E LR DERIVATI (ESTERI E AMMIDI) REAZINI CARATTERISTICE: la riduzione di un chetone produce un alcool secondario (reazione inversa rispetto alla preparazione); i chetoni sono difficilmente ossidabili. Acidi carbossilici Gruppo funzionale - C (carbossilico) R - C - ll Nome : acido + idrocarburo con desinenza - oico (si usano anche nomi comuni; il C del gruppo carbossilico è generalmente in posizione 1) Preparazione : ossidazione delle aldeidi - C = etanale 2 Mn 2+ - C = acido etanoico (acido acetico)
27 Esempi - C acido metanoico (acido formico) - C acido etanoico (acido acetico) - C acido butanoico (acido butirrico) - C acido esanoico (acido capronico) acidi carbossilici danno in acqua reazioni di dissociazione acida comportandosi come acidi deboli. METDI DI PREPARAZINE: gli acidi carbossilici possono essere ottenuti per ossidazione di un aldeide. I gruppi C= ed -, presenti nel gruppo che caratterizza gli ACIDI CARBSSILICI, sono molto vicini e influenzano a vicenda le loro proprietà; per questo, le reazioni degli acidi carbossilici si differenziano da quelle degli alcoli e dei composti carbonilici. L elevato numero di legami a idrogeno che si forma tra le molecole conferisce loro punti di ebollizione relativamente elevati; per la stessa ragione, i primi termini della classe sono miscibili con acqua, e la miscibilità diminuisce a mano a mano che aumenta la dimensione delle molecole (catena idrocarburica apolare di lunghezza crescente). Il gruppo carbossilico è un gruppo acido, per cui gli REAZINI CARATTERISTICE: gli acidi carbossilici possono essere ridotti ad aldeidi (inverso della preparazione) per sostituzione dell - si ottengono i DERIVATI DEGLI ACIDI (dei quali consideriamo esteri ed ammidi).
28 ESTERI Esteri R - C - - R ll Derivati degli acidi carbossilici Gruppo funzionale - CR Il nome deriva da quello dell acido carbossilico corrispondente Esempi - C Butanoato di metile - CC 2 - Formiato di etile Preparazione: reazione tra acidi carbossilici e alcoli acido acetico metanolo C- + - reazione di esterificazione reazione di idrolisi (saponificazione) C acetato di metile Gli esteri si ottengono per reazione tra acidi carbossilici ed alcoli; inversamente, l idrolisi di un estere libera l acido carbossilico e l alcool da cui l estere è formato. Il loro nome deriva da quello degli acidi, dove la parola acido viene eliminata ed il suffisso oico sostituito con
29 il suffisso ato, seguito dal nome del radicale dell alcool. ESEMPI - C - acido propanoico AMMIDI La reazione tra un gruppo carbossilico C ed ammoniaca (N 3 ) porta alla formazione di un ammide. Anche in questo caso, il nome della molecola deriva da quello dell acido carbossilico di partenza (si elimina acido e si sostituisce oico con ammide). - C - propanoato di metile Gli esteri a basso peso molecolare, volatili hanno odori caratteristici di fiori e frutta. acido acetico Ammidi ammoniaca C- + N 3 R - C - N 2 ll Derivati degli acidi carbossilici Gruppo funzionale - CN 2 C--N 2 acetammide + 2 Esempi - C = formammide (derivata dall acido formico) N 2 - C = acetammide (derivata dall acido acetico) N 2
30 AMMINE Le AMMINE sono derivati organici dell ammoniaca, in cui uno o più atomi di sono sostituiti da radicali R. Nel nome vengono indicati i nomi dei radicali, seguiti da ammina. In certi casi si usano nomi comuni (ad esempio, la più semplice ammina aromatica si chiama anilina). I composti a basso peso molecolare sono gassosi e molto solubili in acqua, in cui danno soluzioni basiche. Formano anch esse legami a idrogeno, ma rispetto all acqua questi sono più deboli a causa della minore elettronegatività di N rispetto ad. Ammine Derivati dell ammoniaca - N - metilammina C N - anilina Basi deboli trimetilammina - N - - N - dimetilammina 14.4 I PLIMERI I PLIMERI sono molecole formate da lunghe catene di unità che si ripetono, derivate da molecole più piccole, dette monomeri. Le loro proprietà sono legate alla struttura della molecola e dipendono in particolare da alcuni fattori, tra cui: lunghezza della catena forze di interazione tra le catene
31 presenza di ramificazioni presenza di legami incrociati tra diverse catene Polimeri monomeri polimerizzazione polimeri gomme adesivi plastiche fibre vernici plastificanti additivi stabilizzanti cariche PLIMERI DI CNDENSAZINE Si ha polimerizzazione per condensazione quando le molecole di partenza hanno gruppi funzionali che reagiscono tra loro eliminando molecole d acqua e concatenando le unità monomeriche. Si ottengono importanti polimeri mediante reazione tra acidi carbossilici e alcoli (formazione di poliesteri) e tra acidi carbossilici ed ammine (formazione di poliammidi). Polimeri di condensazione poliammidi - C - Nll Reazione tra acido carbossilico ed ammina Le REAZINI DI PLIMERIZZAZINE sono principalmente due: condensazione e addizione. C- + N 2 - R poliesteri - C - - ll Reazione tra acido carbossilico ed alcool C--NR + 2 C- + - R C- - R + 2
32 ESEMPI l l -N-(C 2 ) 6 -N - esametilendiammina (1,6 - diammino esano) Poliammidi l l ll ll -N-(C 2 ) 6 -N - C - (C 2 ) 8 -C- + ll ll -C-(C 2 ) 8 -C- acido sebacico (acido 1,10 - decandioico) Poliesteri ll ll --(C 2 ) C-C 6 4 -C- glicole etilenico acido tereftalico ll ll --(C 2 ) C -C 6 4 -C PET - polietilentereftalato NYLN PLIMERI DI ADDIZINE Le molecole che presentano doppi legami polimerizzano con particolare facilità perché possono dare reazioni di addizione al doppio legame, sommandosi le une alle altre.
33 Polimerizzazione per addizione Polistirene (PS) monomeri contenenti doppi legami C = C - C = C C = C - l l l l catalizzatore - C = C - l l C 6 5 stirene (vinilbenzene) - C 2 - C - C 2 - C - l l C 6 5 C 6 5 PE - polietilene l l l l - C - C - C - C - l l l l La reazione vista per l etilene può essere schematizzata per molecole più complesse. PVC - polivinicloruro cloruro di vinile - C = C - l l l l l l - C - C - C - C - Cl l l l l Cl Cl Polimetilmetacrilato (PMMA) l l - C = C l =C- l l - C = C l =C-- metilmetacrilato (estere metilico) acido metacrilico l l - C - C - l l C-- C-- ll ll
34 La gomma è un polimero ottenuto per addizione, partendo da un monomero contenente due doppi legami; di questi, uno dei due dà una reazione di addizione, l altro viene mantenuto nel polimero. La gomma naturale e quella sintetica derivano da due monomeri leggermente diversi. Gomme 14.V VERIFICA SE AI CAPIT 14.V.1 Partendo dal significato dell isomeria, individua tra i composti seguenti quelli tra loro isomeri: a. - (C 3 8 ) b. - (C 3 8 ) l C 2 = C - C= C 2 2- metil 1,3- butadiene (isoprene) l C 2 = C - C= C 2 1,3- butadiene l - C = C - poli isoprene gomma naturale l - C = C - gomma sintetica c. - C - (C 4 10 ) d. - (C 5 12 ) e. - - (C 3 8 ) f. - (C 4 10 )
35 g. - C - (C 5 12 ) h. - (C 6 14 ) 14.V.2 Sulla base delle regole di nomenclatura, attribuisci un nome alle molecole seguenti: - C - Cl 14.V.3 Individua gli alcani prodotti per addizione di 2 sui seguenti idrocarburi insaturi: C 2 = C - C 2 = C - C = C C = C - - C - - C - - C C C C 14.V.4 Tenendo conto delle reazioni di ossidazione e di riduzione che interessano alcune classi di composti organici, individua quale tipo di composto si ottiene mediante: ossidazione di un alcool primario
36 riduzione di un chetone ossidazione di un aldeide riduzione di un acido carbossilico CIMICA RGANICA 14.V.5 Sulla base dei meccanismi di polimerizzazione, scrivi i prodotti ottenuti da: (polimerizzazione per condensazione, vedi esterificazione) C - C + - (polimerizzazione per addizione, vedi addizione al doppio legame) C 2 = C 2 + C 2 = C 2
37 Soluzione Pre-Test 1. alcheni, 2 - butene alcoli, (1) - propanolo acidi carbossilici, acido propanoico esteri, propanoato di metile C C C - + Cl 2 CCl = CCl (ossidazione) - C - C - C C + - CIMICA RGANICA
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
GRUPPI FUNZIONALI GLI ALCOLI
 GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
I composti del carbonio
 Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Capitolo A1 Chimica organica: un introduzione
 Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
CHIMICA delle MACROMOLECOLE BIOLOGICHE
 Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Gruppo carbonilico. Il gruppo carbonilico è caratterizzato dalla presenza C=O ed i composti che lo contengono vengono definiti composti carbonilici.
 Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
La chimica organica. La chimica organica è la chimica dei composti del carbonio.
 La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
2. Gli Idrocarburi IDROCARBURI. solo C e H. alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp 2 ) Alifatici
 2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Alcheni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Gli Alcheni. Ibridazione sp 2. I legami chimici degli alcheni
 Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Alchini. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA
 CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA INTRODUZIONE LA CHIMICA ORGANICA E LO STUDIO DELLA CHIMICA DEI COMPOSTI DEL CARBONIO. QUASI TUTTI GLI ELEMENTI DELLA TAVOLA PERIODICA
CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA INTRODUZIONE LA CHIMICA ORGANICA E LO STUDIO DELLA CHIMICA DEI COMPOSTI DEL CARBONIO. QUASI TUTTI GLI ELEMENTI DELLA TAVOLA PERIODICA
Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre
 Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre alla prof.savoia Che provvederà alla correzione con
Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre alla prof.savoia Che provvederà alla correzione con
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Gli idrocarburi e il petrolio
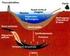 Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
GLI ALCANI. Michele Kodrič
 GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Alcheni e alchini. idrocarburi. Insaturi C-C doppi/tripli. alcani. Saturi C-C semplici cicloalcani. aromatici
 Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
R = GRUPPO FUNZIONALE Atomo o raggruppamento atomico
 GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 H 12 ; b. C 2 H 5 Cl; c. C 4 H 10 O.
 1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
CHIMICA ORGANICA. Gli idrocarburi aromatici
 1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
Soluzioni degli esercizi di fine capitolo
 SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
ELEMENTI DI CHIMICA ORGANICA
 ELEMENTI DI IMIA RGANIA La himica rganica è la chimica dei composti del carbonio, fatta eccezione per alcuni composti quali il monossido di carbonio (), il biossido di carbonio ( 2 ), i carbonati ( 3 -
ELEMENTI DI IMIA RGANIA La himica rganica è la chimica dei composti del carbonio, fatta eccezione per alcuni composti quali il monossido di carbonio (), il biossido di carbonio ( 2 ), i carbonati ( 3 -
La chimica organica. Approfondimenti di chimica. Introduzione. Gli idrocarburi C CH 2 CH CH 3 CH (CH 2 ) 3 CH CH CH 3. Nota. 2. La chimica organica
 2. La cimica organica Approfondimenti di cimica La cimica organica Introduzione La cimica organica studia i composti del arbonio (composti organici). Attualmente sono note milioni di sostanze organice
2. La cimica organica Approfondimenti di cimica La cimica organica Introduzione La cimica organica studia i composti del arbonio (composti organici). Attualmente sono note milioni di sostanze organice
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
CHIMICA ORGANICA. PON C1 di SCIENZE. Esperto prof. C. Formica
 CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
Contenuti della lezione:
 Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
IDROCARBURI ALIFATICI
 CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
Capitolo 23 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Capitolo A2 Dai gruppi funzionali ai polimeri
 Quesiti e problemi 1 Il radicale metile non è un gruppo funzionale perché, per definizione, il gruppo funzionale è un atomo o un gruppo di atomi che conferisce una reattività particolare al gruppo di cui
Quesiti e problemi 1 Il radicale metile non è un gruppo funzionale perché, per definizione, il gruppo funzionale è un atomo o un gruppo di atomi che conferisce una reattività particolare al gruppo di cui
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
