ARPAT Agenzia regionale per la protezione ambientale della Toscana
|
|
|
- Rossana Piccinini
- 6 anni fa
- Visualizzazioni
Transcript
1 ARPAT Agenzia regionale per la protezione ambientale della Toscana Dipartimento Provinciale di Livorno 114, Via Giovanni Marradi LIVORNO Tel. 0586/ Fax 0586/ f.righini@arpat.toscana.it
2 Proteine Sono etero polimeri lineari costituiti da 20 tipi di aminoacidi legati l uno all altro con legame peptidico. Un numero così elevato di monomeri diversi da luogo a numerosissime macromolecole proteiche dell ordine di Il PM varia da 5x10 3 a oltre 10 6 u.m.a. catene più corte sono denominate peptidi: oligopeptidi con n. a.a. 10 e polipeptidi con n. a.a. di Rappresentano oltre il 50% dei componenti organici e circa il 14-18% (a seconda dell'età) del peso corporeo totale. Esplicano numerosissime funzioni quali: modulano l espressione dei geni, regolano il metabolismo, sono trasportatori di molecole, intervengono nella coagulazione sanguigna, costituiscono gli anticorpi, danno luogo a strutture contrattili, intervengono nella trasmissione nervosa, danno origine a strutture di sostegno, sono costituenti delle forme di deposito di nutrienti per l embrione.
3 Proteine alimentari Le proteine alimentari fanno parte di tutte le categorie funzionali sopra descritte ma sono particolarmente importanti quelle del tessuto muscolare della carne e del pesce che sono costituite per circa il 40 % da actina e miosina e quelle di deposito come quelle dell uovo, del latte e dei cereali. Gli zuccheri, gli oli e, in genere, le bevande analcoliche ne sono privi. Alcune proteine costituiscono: fattori antinutrizionali: lecitine contenute nei legumi ed inattivate dalla cottura. Inibitori di enzimi quali l ovomucoide ( nell albume) e l amilasi nella cariosside del frumento. Allergeni: contenuti nel latte, nell uovo, nei crostacei e molluschi, nelle noci e nelle arachidi, ecc.. tossine: prodotte da microorganismi contaminati o contenute in piante ed animali ( micotossine, botulino, ricina ed altre)
4 Amminoacidi Nelle proteine sono presenti solamente L-amminoacidi
5 Struttura α - amminoacidi Trptofano
6 Formuule di struttura degli amminoacidi
7 α-amminoacidi Forma prevalente a ph acido Forma prevalente a ph neutro Forma prevalente a ph basico
8 Tavola degli amminoacidi (da
9 α- L-ammino acidi Essenziali P.M. non Essenziali P.M. ISOLEUCINA- Ile ARGININA Arg LEUCINA Leu CISTEINA Cys LISINA Lys ISTIDINA Hys METIONINA Met TIROSINA Tyr FENILALANINA Phe ALANINA Ala TREONINA Thr A. ASPARTICO Asp TRIPTOFANO Trp A. GLUTAMMico Glu VALINA Val GLICINA Gly PROLINA Pro SERINA IDROSSIPROLINA
10 Struttura delle Proteine Ogni proteina ha una specifica sequenza di a.a. legati fra loro con legame peptidico: questa è la carta d identità; questa è definita struttura primaria ed è determinata geneticamente. xray.bmc.uu.se virtuallaboratory.colorado.edu Ponti a disolfuro La struttura secondaria è data dalle conformazioni spaziali periodiche e regolari che la catena polipeptidica può assumere. Le principali sono l α elica, lamina β, oppure privi di struttura a gomitolo ( random coil). Le proteine di sostegno sono semplici e si fermano alla struttura secondaria un esempio è la cheratina dei capelli e delle unghie: è costituita da una triplice α -elica stabilizzata da ponti a disolfuro che si formano tra residui di cisteina della stessa catena ma lontani.
11 Struttura delle Proteine Strutture secondarie
12 Struttura delle proteine (ncbi.nlm.nih.gov)
13 Struttura delle proteine La struttura terziaria è un ulteriore struttura di organizzazione spaziale tridimensionale delle proteine. Riguarda le proteine globulari, le più importanti e specializzate: enzimi, ormoni, recettori ecc La struttura è stabilizzata da vari tipi di legami/interazioni: covalenti come i ponti a disolfuro, ionici fra gruppi con carica opposta, a idrogeno nella stessa catena e fra catene diverse, interazioni idrofobiche. www-3.unipv.it
14 Classificazione proteine: sulla base della/e.. Funzione: trasporto, deposito, struttura, enzimi, ormoni ecc.. Forma: fibrose con funzioni meccaniche: cheratina, collagene, elastina, miosina, actina, ecc. Origine animale. Globulari: più complesse, le rimanenti. Composizione chimica: semplici: per idrolisi originano solamente a.a.. Composizione elementare in %: C 50, O 23, N 16, H 7, S max 3. Coniugate: contengono catene polipeptidiche e gruppi prostetici non proteici come nell emoglobina Proprietà chimico-fisiche ( quelle di seguito sono tutte globulari): protammine o istoni: basiche perché contengono a.a. con basi amminiche, sono solubili in acqua, non coagulano con il calore, entrano nella composizione degli ac.nucleici e si ritrovano nei cromosoni. Albumine: coagulano per riscaldamento e sono solubili in acqua. Globuline coagulano per riscaldamento, solubili a ph neutro in soluzioni diluite di sali. Prolammine: sono solubili in al. etilico al 75%.( gliadina del frumento). Gluteline: sono solubili in acidi e basi ma non in alcool ( glutenina del frumento). Scleroproteine: fibrose, insolubili in acqua, alcali ed acidi e in soluzioni saline. Il collagene a freddo diventa gel (come la gelatina del brodo).
15 Nucleoproteine La parte proteica e costituita da protammine e istoni, la parte prostetica sono gli acidi nucleici. Questi sono costituiti da nucleotidi composti da: una base azotata, un pentoso ( ribosio o desossi ribosio), ac. Fosforico). Basi puriniche : adenina e guanina. Basi pirimidiniche: citosina, uracile, timina. Le xantine metilate: caffeina, teofillina, teobromina sono stimolanti contenuti nelle bevande nervine( tè, caffè, cioccolato)
16 Interesse nutrizionale delle nucleoproteine Queste basi azotate subiscono un metabolismo che trasforma le purine in ac. urico e le pirimidine in ammoniaca ed acqua. Infatti, adenina e guanina per deammininazione si trasformano in xantine e poi in acido urico. Gli alimenti ricchi di purine non devono entrare, quindi, nella dieta dell iperucemico
17 Indici nutrizionali proteici La qualità delle proteine alimentari dipende dalla loro composizione in amminoacidi e dall'efficienza con cui vengono digerite. Sono stati prodotti diversi indici che valutano queste grandezze: % P = contenuto proteico percentuale: indica il contenuto percentuale di proteine Valore biologico (VB): indica la quantità di azoto rattenuto dall'organismo per l'accrescimento e/o il mantenimento. I = N introdotto con la dieta F = N fecale F 0 = N fecale a dieta senza proteine U = N nelle urine U 0 = N nelle urine a dieta senza proteine VB = N trattenuto / N assorbito x 100 N trattenuto = I - (F - F 0 ) - (U - U 0 ) N assorbito = I - (F - F 0 )
18 Indici nutrizionali proteici Coefficiente di utilizzazione digestiva (C.U.D.) C.U.D. = (N assorbito / N introdotto con la dieta) x 100 Indica l'efficienza con la quale viene digerita la proteina in questione, il valore massimo è 100. Utilizzazione proteica netta (N.P.U.) N.P.U. = N trattenuto dall'organismo / N introdotto con la dieta Questo indice tiene conto sia dell'efficienza digestiva che del profilo in amminoacidi Indice chimico IC = mg di aa limitante per gr di proteina in esame / mg dello stesso aa di proteina standard La proteina standard è data da una combinazione tipo di amminoacidi stabilita dalla FAO, che rappresenta una proteina umana. a.a. limitanti considerati: lisina, metionina, trptofano, treonina.
19 Indici nutrizionali di alcuni alimenti (FAO /OMS) ALIMENTO % P VB CUD NPU IC Latte di mucca Uovo Carne di vitello Pesce Frumento Seme di soia
20 Fabbisogni proteici (FAO /OMS) L apporto proteico ottimale ( adulto sano) è intorno a 0,75 g/kg di p.c. (45 g per una femmina adulta sana di 60 kg di p.c. e 56 g per un maschio adulto sano di 75 kg di p.c.). I fabbisogni aumentano nella crescita, allattamento, stati patologici e convalescenza. In una persona sana circa il 13 % delle calorie deriva da proteine. In Italia considerate le abitudini alimentari, il valore consigliato si attesta intorno al 10% pari ad 1g/proteine/kg/die tenendo conto che l NPU della nostra dieta è pari a circa 70. L organismo non può immagazzinare le proteine per cui gli aminoacidi in eccesso sono trasformati in glucosio o sono avviate al catabolismo ossidativo. Se la dieta è invece in difetto di calorie gli a.a. sono utilizzati in tutto o in parte per produrre energia.
21 Amminoacidi essenziali (FAO /OMS) L organismo per poter sintetizzare tutte le proteine necessita di tutti i 20 amminoacidi. La carenza di un amminoacido ( a.a. limitante) non permette questa sintesi. In questo caso gli amminoacidi presenti non sono utilizzati e sono degradati. Gli a.a. essenziali sono valina, isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptofano e istidina. Il fabbisogno di a.a. essenziali è massimo durante i primi mesi di vita e diminuisce con l età perché gli organismi adulti sono più efficienti nel riciclare gli a.a. essenziali in presenza di una diminuzione dell apporto proteico. Il rapporto E /T si abbassa con l età. E = a.a. essenziali T = a.a. totali
22 Tabella bisogni in AAE per tutti i gruppi di età ( fonte SINU) Confronto dei pattern di riferimento in aminoacidi dei bambini e degli adulti con la composizione in aminoacidi di proteine di qualità diversa. Pattern di riferimento in (in mg di aminoacidi/g di proteine) Composizione di proteine alimentari (in mg di aminoacidi/g di proteine) Bambini pre-scolari Adulti Uovo Latte di mucca Carne Frumento Istidina Isoleucina Leucina Lisina Met. + Cist Fen.- ala.+tir Treonina Triptofano Valina
23 Valore proteico degli alimenti Le carni e i latticini forniscono proteine di alta qualità simili a quello del corpo umano, forniscono tutti gli aminoacidi essenziali nelle giuste proporzioni e per questo sono definite proteine ad alto valore biologico. I cereali e legumi forniscono notevoli quantità di proteine di discreto valore biologico ma sono meno disponibili di quelle precedenti. Contengono quantità troppo basse di a.a. essenziali quali lisina, triptofano, treonina ( cereali) e metionina (legumi) La frutta e gli ortaggi sono deficitari di proteine e di a.a. essenziali e non possono coprire il fabbisogno proteico nella dieta. I vegetali devono, quindi, essere abbinati tra loro o a latticini per fornire un apporto proteico di buona qualità. Il concetto della complementarità delle proteine al fine di un apporto ottimale in aminoacidi essenziali è antico quanto l uomo e si manifesta nella cucina di tutti i paesi. In Italia pasta e fagioli o pasta e ceci sono fra gli abbinamenti più antichi e più riusciti dal punto di vista nutrizionale
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
L integrazione proteica nelle diverse fisiopatologie
 Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
PROTEINE. DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico.
 LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
PROTEINE: funzioni e composizione chimica
 PROTEINE: funzioni e composizione chimica Funzioni strutturali componenti di diversi tessuti Funzioni di regolazione e di trasporto: enzimi, ormoni, carrier, proteine nucleari Contenuto (%) Carbonio 51
PROTEINE: funzioni e composizione chimica Funzioni strutturali componenti di diversi tessuti Funzioni di regolazione e di trasporto: enzimi, ormoni, carrier, proteine nucleari Contenuto (%) Carbonio 51
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
I PROTIDI. Aspetti generali
 I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
LE PROTEINE. Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O)
 LE PROTEINE Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O) Sono costituite dall'unione di tante unità di base dette amminoacidi Protidi negli alimenti Copyright
LE PROTEINE Sono composti quaternari composti da Carbonio (C), Idrogeno (H), Azoto (N) e Ossigeno (O) Sono costituite dall'unione di tante unità di base dette amminoacidi Protidi negli alimenti Copyright
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO
 LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
moli OH - /mole amminoacido
 ) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Sequenze nucleotidiche del DNA definite loci costituiscono i geni. Ogni gene codifica per una specifica proteina
 sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
20/12/ tipi di amino acidi: parecchie combinazioni
 20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
La scienza nell alimentazione
 La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
PROTEINA GREGGIA (P.G.)
 PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
Struttura degli Amminoacidi
 Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Corso di educazione alimentare
 Corso di educazione alimentare Appendice 2 Approfondimento alla lezione Gruppi di Alimenti Le Proteine Funzioni delle proteine Le proteine sono le molecole funzionali per eccellenza della cellula, grazie
Corso di educazione alimentare Appendice 2 Approfondimento alla lezione Gruppi di Alimenti Le Proteine Funzioni delle proteine Le proteine sono le molecole funzionali per eccellenza della cellula, grazie
NH 2 CHCOOH AMINOACIDI PRESENTI NELLE PROTEINE. Abbreviazione internazionale. Nome. acido aspartico acido glutammico. CXasparagina.
 Le proteine sono composti organici quaternari; esse sono costituite infatti da C,H,N e O. Pertanto rappresentano l'unica fonte di azoto del nostro organismo. Le proteine si formano per polimerizzazione
Le proteine sono composti organici quaternari; esse sono costituite infatti da C,H,N e O. Pertanto rappresentano l'unica fonte di azoto del nostro organismo. Le proteine si formano per polimerizzazione
VALUTAZIONE NUTRIZIONALE DEGLI ALIMENTI
 VALUTAZIONE NUTRIZIONALE DEGLI ALIMENTI COMPOSIZIONE CHIMICA DIGERIBILITA VALORE NUTRITIVO VALORE PROTEICO APPETIBLITA CONSERVABILITA FATTORI ANTINUTRIZIONALI VALUTAZIONE ECONOMICA VALORE PROTEICO GREZZA
VALUTAZIONE NUTRIZIONALE DEGLI ALIMENTI COMPOSIZIONE CHIMICA DIGERIBILITA VALORE NUTRITIVO VALORE PROTEICO APPETIBLITA CONSERVABILITA FATTORI ANTINUTRIZIONALI VALUTAZIONE ECONOMICA VALORE PROTEICO GREZZA
3.3.2. ALIMENTI DI ORIGINE VEGETALE. 3.3.2.1. Verdure
 3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Rappresentano il 14-18% dell organismo umano Ci sono miliardi di differenti tipi di proteine di cui oltre solo nell uomo 10% 15%
 Proteine Il loro nome significa che occupa il primo posto per indicare il ruolo che rivestono negli organismi Le macromolecole proteiche vanno da 50 a 500 amminoacidi. Catene più corte sono dette peptidi
Proteine Il loro nome significa che occupa il primo posto per indicare il ruolo che rivestono negli organismi Le macromolecole proteiche vanno da 50 a 500 amminoacidi. Catene più corte sono dette peptidi
PROTEINE (dal greco proteios, che occupa il primo posto)
 PRTEIE (dal greco proteios, che occupa il primo posto) costituite da una o più catene polipeptidiche; i peptidi sono eteropolimeri lineari formati da 0-50 amminoacidi (aa); si conoscono centinaia di aa
PRTEIE (dal greco proteios, che occupa il primo posto) costituite da una o più catene polipeptidiche; i peptidi sono eteropolimeri lineari formati da 0-50 amminoacidi (aa); si conoscono centinaia di aa
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Nome e cognome: [Totale: 80 punti]
![Nome e cognome: [Totale: 80 punti] Nome e cognome: [Totale: 80 punti]](/thumbs/74/70614081.jpg) Nome e cognome: ruppo / candidato No. SIENZE SPERIMENTLI: BIOLOI [Totale: 80 punti] Raccomandazioni: Rispondere direttamente sui fogli Non separare i fogli Rispondere in modo sintetico e chiaro, usando
Nome e cognome: ruppo / candidato No. SIENZE SPERIMENTLI: BIOLOI [Totale: 80 punti] Raccomandazioni: Rispondere direttamente sui fogli Non separare i fogli Rispondere in modo sintetico e chiaro, usando
Biochimica e Biologia per le professioni sanitarie, McGraw-Hill
 Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
lezione Prof. Spina miliardi di anni fa l universo comparve sotto forma di eruzioni
 Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a)
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Principi nutritivi calorici
 Principi nutritivi calorici funzione energetica costruttiva regolatrice principi nutritivi glucidi lipidi protidi 1 PROTEINE : cosa sono? Sono molecole organiche costituite da carbonio, ossigeno, idrogeno
Principi nutritivi calorici funzione energetica costruttiva regolatrice principi nutritivi glucidi lipidi protidi 1 PROTEINE : cosa sono? Sono molecole organiche costituite da carbonio, ossigeno, idrogeno
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
PRINCIPI NUTRITIVI O NUTRIENTI
 Corso per istruttori di Body Building PRINCIPI NUTRITIVI O NUTRIENTI Dott. Gianfranco Serino DIETISTA ISTRUTTORE DI BODY BUILDING PRINCIPI NUTRITIVI O NUTRIENTI Gli alimenti con il processo della digestione
Corso per istruttori di Body Building PRINCIPI NUTRITIVI O NUTRIENTI Dott. Gianfranco Serino DIETISTA ISTRUTTORE DI BODY BUILDING PRINCIPI NUTRITIVI O NUTRIENTI Gli alimenti con il processo della digestione
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
I principi nutritivi
 I principi nutritivi Quali sono? Qual è la loro funzione? In quali cibi si trovano? Perché sono importanti? Quante Kilocalorie sviluppano? Kilocalorie Unità di misura dell energia accumulata negli alimenti
I principi nutritivi Quali sono? Qual è la loro funzione? In quali cibi si trovano? Perché sono importanti? Quante Kilocalorie sviluppano? Kilocalorie Unità di misura dell energia accumulata negli alimenti
Amminoacidi e Proteine
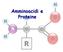 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
E. Giordano 16/09/2010
 GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
