Diabete e biosimilari dell insulina: evidenze cliniche
|
|
|
- Battista Spina
- 6 anni fa
- Visualizzazioni
Transcript
1 Diabete e biosimilari dell insulina: evidenze cliniche Francesco Rossi I progressi in farmacologia: le biotecnologie 1
2 La crescita dell industria biotech in Italia Anche in Italia, l industria biotecnologica ha conosciuto uno sviluppo straordinario riconducibile alle formidabili ricadute di queste tecnologie, alla riconosciuta eccellenza della nostra ricerca accademica e industriale, alla capacità delle imprese italiane di tradurre l innovazione in prodotti di valore. Centro Studi Assobiotec - Aprile 2016 Numero di prodotti in sviluppo per area terapeutica Centro Studi Assobiotec - Aprile
3 Definizione di Farmaco biologico/biotecnologico Farmaco il cui principio attivo è rappresentato da una sostanza (generalmente una proteina ad alto peso molecolare) prodotta naturalmente da un organismo vivente (microrganismi o cellule animali) (farmaco biologico propriamente detto) oppure farmaco derivante da una sorgente biologica attraverso l utilizzo delle tecniche del DNA ricombinante (farmaci biotecnologici). Farmaco biologico emoderivati, immunoglobuline, vaccini tradizionali. Farmaco biotecnologico anticorpi monoclonali, vaccini ricombinanti. Caratteristiche di un farmaco biologico/biotecnologico Molecola di dimensioni molto grandi e molto complessa L azione farmacologica è in funzione della composizione molecolare, della sua forma e struttura tridimensionale Lo sviluppo richiede l identificazione di una nuova proteina o altra entità chimica Le tecniche di produzione sono complesse e dipendono da: o Substrato biologico/organismo (cellula ospite utilizzata, plasmidi impiegati per trasfettare/infettare la cellula ospite) o Fattori ambientali o Materiale e condizioni di crescita/fermentazione o Possibile manipolazione genetica o Metodiche di estrazione e purificazione Per l autorizzazione all immissione in commercio si valutano gli studi relativi alla posologia, all efficacia clinica e alla sicurezza Gottleib S et al. Am J Health-Syst Pharm. 2008;65:S2-8. Johnson PE. Am J Health-Syst Pharm. 2008;65:S
4 Complessità dei farmaci biologici Farmaci di sintesi vs farmaci biologici principali differenze Farmaci di sintesi Farmaci biologici Prodotti attraverso sintesi chimica Prodotti da colture cellulari Basso peso molecolare Alto peso molecolare Struttura ben definita Struttura complessa e eterogenea Attività indipendente dal processo di produzione Attività fortemente dipendente dal processo di produzione Caratterizzato nella sua totalità Impossibile caratterizzarne completamente la composizione molecolare Stabile Non stabile Non immunogenico Immunogenico Effetti multipli Effetto specifico Generics and Biosimilars Initiative Journal
5 Il processo è il prodotto A differenza dei farmaci tradizionali ottenuti per sintesi chimica, la struttura molecolare dei farmaci biologici è strettamente dipendente dal processo di produzione che può durare mesi e che comprende tappe complesse Il processo produttivo di un farmaco biologico è complesso Differenze in diverse parti del processo Gene umano Vettore DNA Trasferimento in cellula ospite Clonaggio DNA in un vettore Sintesi proteine da cellule batteriche o di mammifero Fermentazione Tutti i farmaci Diverso biologici processo presentano = Diverso prodotto Formulazione 5
6 Farmaci Biologici/Biotecnologi disponibili in commercio Le principali classi di farmaci biologici/biotecnologici includono: Anticorpi monoclonali (adalimumab, rituximab, ranibizumab, trastuzumab, panitumumab, certolizumab, golimumab, infliximab, canakinumab, tocilizumab, cetuximab, bevacizumab, omalizumab, natalizumab, palivizumab, ustekinumab, brentuximab vedotin, pertuzumab, eculizumab, ramucirumab, blinatumomab, alirocumab, mepolizumab, necitumumab, pembrolizumab, nivolumab, dinutuximab, secukinumab, evolocumab) mab Inibitori delle tirosin-chinasi (sorafenib, sunitinib, imatinib, regorafenib, erlotinib) Citochine e loro antagonisti recettoriali (interferone-alfa, aldesleukin) Proteine di fusione (etanercept, aflibercept, abatacept) Ormoni (insulina, eritropoietina, somatotropina) Fattori di crescita (G-CSF) Pur essendo molecole di sintesi chimica, gli ITK rientrano tra i farmaci cosiddetti biologici perché farmaci a bersaglio (target) o ancora intelligenti, con una specificità d azione con conseguente minore tossicità. Fattori della coagulazione Vaccini (tradizionali e ricombinanti) (vaccino anti-epatite B, anti-hpv) Applicazioni terapeutiche dei farmaci biologici/biotecnologici Dislipidemie Oncologia Dermatologia Reumatologia Diabetologia Gastroenterologia 6
7 Farmaci con brevetto scaduto Farmaci tradizionali Farmaci biologici/biotecnologici Farmaci generici/equivalenti Farmaci biosimilari Farmaci biosimilari Si definiscono biosimilari quei farmaci biologici/biotecnologici il cui principio attivo è analogo, ma non identico per caratterizzazione e produzione, a quello del medicinale di riferimento. Con il termine biosimilare viene quindi indicato un farmaco simile (e non identico) ad un farmaco biologico/biotecnologico già autorizzato all immissione in commercio e per il quale sia scaduta la copertura brevettuale. 7
8 Correttezza del comparability exercise Il comparability exercise è una procedura sperimentale, richiesta a fini regolatori, per cui il prodotto biosimilare viene confrontato da un punto di vista fisico-chimico, pre-clinico e clinico (nella maggior parte dei casi con studi di Fase III sull indicazione principale usando hardendpoints o end-points surrogati). Un biosimilare è il farmaco che si sia dimostrato sovrapponibile a tutti i livelli. Opinioni contrastanti sono emerse in questi anni sul comparability exercise da parte della comunità scientifica, anche alla luce del fatto che lo scopo di questo esercizio non è dimostrare efficacia e sicurezza del farmaco biosimilare, ma la dimostrazione di comparabilità, in termini di qualità, efficacia e sicurezza, con il farmaco di riferimento. Insulina glargine: primo biosimilare di insulina glargine approvato il 9 settembre
9 STUDI DI SICUREZZA La principale preoccupazione riguarda l immunogenicità. A tal proposito, l EMA richiede studi clinici della durata di almeno 12 mesi, al fine di raccogliere informazioni relative alla sicurezza e all immunogenicità (valutata quest ultima attraverso la stima dell incidenza e la titolazione degli anticorpi con biosimilare e reference), con una fase comparativa di almeno 6 mesi. L outcome primario in questi studi è l incidenza di anticorpi alle due insuline. Utilizzare un ampia popolazione e garantire una lunga durata di studio consente di delineare al meglio il profilo di tollerabilità di tali farmaci. È opportuno per ciascun biosimilare approntare un appropriato piano di farmacovigilanza post-autorizzativo, così come fatto da EMA per le insuline umane e analoghi con il Risk Management Plan e il Pharmacovigilance Programme. Risultati di immunogenicità degli studi ABEB e ABEC Lo Studio ABEB (ELEMENT 1) ha dimostrato, per un periodo di 52 settimane, la comparabilità in termini di immunogenicità tra l insulina glargine biosimilare e l originator; tale comparabilità è stata espressa come incidenza dei livelli di anticorpi anti-insulina (sia totale che cross-reattivi all insulina umana). Lo studio ABEC (ELEMENT 2) ha dimostrato, invece, ugualmente una comparabilità in termini di immunogenicità tra le due insuline ma su un campione di pazienti più piccolo. Tale dato è spiegato dal fatto che i pazienti con diabete di tipo 2 tendono a sviluppare più raramente anticorpi anti-insulina se confrontati con i pazienti affetti da diabete mellito di tipo 1. 9
10 Conclusioni degli studi comparativi Gli studi comparativi di qualità condotti, quelli di farmacocinetica e farmacodinamica nonché quelli di efficacia e sicurezza (ABEB e ABEC) dimostrano che l insulina glargine biosimilare è comparabile in termini di qualità, efficacia e sicurezza all originator Lantus. I due farmaci hanno sovrapponibilità regolatoria. Insulina glargine: è possibile l interscambiabilità tra biosimilare e originator? Come per gli altri biosimilari, anche per l insulina glargine vi è un problema relativo alla interscambiabilità. Devono essere le evidenze cliniche in real life a supportare lo switch dal farmaco originatore al farmaco biosimilare. 10
11 In virtù delle differenze che si riscontrano nei processi produttivi, biosimilare non è sinonimo di bioequivalente Pertanto, la sostituzione automatica, che potrebbe essere applicata ai generici, non può essere estesa anche ai biosimilari. Come per la prescrizione, anche la sostituzione di un prodotto biologico/biotecnologico con un altro deve essere autorizzata dal medico. Su tale argomento l EMA ha espresso la seguente opinione: il biosimilare e il biologico di riferimento sono simili ma non identici, pertanto la decisione di trattare un paziente con l uno o l altro dovrebbe avvenire in seguito alla decisione di un operatore sanitario qualificato. 11
12 Nella prospettiva di arrivo di nuovi biosimilari di insulina sul mercato inglese, nell ottobre 2013 la UK Diabetes ha rilasciato un position statement; in tale documento, gli autori precisano che pazienti adeguatamente controllati con una specifica insulina non dovrebbero modificare la terapia o passare a un biosimilare. In caso di switch, il paziente deve monitorare la glicemia con maggiore attenzione. MARZO 2015 L Agenzia regolatoria olandese (Medicines Evaluation Board - MEB) aggiorna la sua posizione sui biosimilari Da evitare la sostituzione incontrollata tra farmaci biologici 12
13 L Agenzia regolatoria dei farmaci finlandese - Fimea annuncia l interscambiabilità dei biosimilari con i rispettivi originator. La Fimea ha dichiarato, attraverso un comunicato del 22 maggio 2015, l interscambiabilità dei biosimilari, tenuto conto del fatto che: la pratica dello switch tra farmaci di origine biologica/biotecnologica è comune e solitamente non problematica; vi sono scarse o nulle evidenze che correlino la comparsa di eventi avversi allo switch; Il rischio associato all uso di un biosimilare può essere definito sovrapponibile a quello associato all uso dell originator. In Italia, la posizione dell AIFA chiarisce che i medicinali biologici e biosimilari sono simili, ma non identici, pertanto vanno esclusi dalla sostituibilità terapeutica automatica. l AIFA, infatti, ha deciso di non includere i medicinali biosimilari nelle liste di trasparenza che consentono la sostituibilità automatica tra prodotti equivalenti. La scelta di trattare un paziente con un farmaco biologico originator o con un biosimilare rimane una decisione clinica affidata al medico specialista. In particolare, l AIFA considera i biosimilari un opzione terapeutica da preferire nei pazienti naive qualora costituiscano un vantaggio economico. Tale parere è stato confermato nel successivo Position Paper dell AIFA "Farmaci Biosimilari. Riapertura della consultazione pubblica" (06/03/2014), che sottolinea la possibilità e la procedura da seguire in caso si voglia chiedere parere alla Commissione Tecnico Consultiva dell AIFA sull equivalenza terapeutica tra biologici e corrispondenti biosimilari o tra biologici e biosimilari con principi attivi differenti. 13
14 Posizione della Commissione Regionale del Farmaco della Regione Emilia- Romagna sullo switch tra originator e biosimilare PAZIENTI DRUGS NAÏVE Data la qualità del percorso registrativo dei biosimilari, esiste un accordo nella comunità scientifica sull opportunità di utilizzarli nei pazienti di nuova diagnosi;. non esistono ragioni né di carattere regolatorio, né di carattere scientifico, per privilegiare l uso di un medicinale rispetto ad un altro.. Ne consegue che, per il fabbisogno proprio dei pazienti naïve nel capitolato tecnico delle gare di acquisto, debba essere inserito in un unico lotto il medicinale originator insieme ai rispettivi biosimilari, in modo da stimolare la concorrenza tra i produttori. PAZIENTI GIÀ IN TERAPIA Per i pazienti già in trattamento con un determinato prodotto biotecnologico, sia esso originator o biosimilare, la sostituzione del farmaco in uso non potrà essere automatica, ma dovrà essere valutata dal clinico caso per caso. Nello specifico per quanto riguarda l insulina biosimilare è l EMA stessa nelle conclusioni dell esercizio di comparabilità sottolinea il fatto che è stato effettuato uno switch da insulina glargine originator a biosimilare nei pazienti che erano già in terapia con il farmaco al momento dell arruolamento, senza che si evidenziassero nel periodo di trattamento criticità in termini di efficacia e di sicurezza. 14
I biosimilari dell insulina
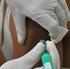 I biosimilari dell insulina Seconda Università degli Studi di Napoli Dipartimento di Medicina Sperimentale - Sezione di Farmacologia L. Donatelli Genova, 15 maggio 2015 Francesco Rossi Dichiarazione conflitto
I biosimilari dell insulina Seconda Università degli Studi di Napoli Dipartimento di Medicina Sperimentale - Sezione di Farmacologia L. Donatelli Genova, 15 maggio 2015 Francesco Rossi Dichiarazione conflitto
GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE
 XXXI CONGRESSO NAZIONALE SIFO CAGLIARI 6-8 OTTOBRE 2010 GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE DOTT.ssa ENRICA MARIA PROLI DOTT.ssa ELENA JACOBONI COSA SONO I FARMACI
XXXI CONGRESSO NAZIONALE SIFO CAGLIARI 6-8 OTTOBRE 2010 GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE DOTT.ssa ENRICA MARIA PROLI DOTT.ssa ELENA JACOBONI COSA SONO I FARMACI
BIOTECNOLOGICO Anticorpi monoclonali, vaccini ricombinanti BIOLOGICO. Farmaco il cui principio attivo è rappresentato da una proteina ad alto PM
 Farmaco il cui principio attivo è rappresentato da una proteina ad alto PM da una sorgente biologica tramite Rappresentano il 20% dei farmaci oggi in commercio procedimenti e il biotecnologici 50% di quelli
Farmaco il cui principio attivo è rappresentato da una proteina ad alto PM da una sorgente biologica tramite Rappresentano il 20% dei farmaci oggi in commercio procedimenti e il biotecnologici 50% di quelli
Farmaci Biosimilari. Un alleanza tra Farmacisti e Reumatologi Per la Sostenibilità del SSR. 13 gennaio 2017 Palazzo Pirelli
 Farmaci Biosimilari Un alleanza tra Farmacisti e Reumatologi Per la Sostenibilità del SSR 13 gennaio 2017 Palazzo Pirelli Cosa Chiedono il SSN e il SSR? Massimo Medaglia Direzione Generale Welfare Regione
Farmaci Biosimilari Un alleanza tra Farmacisti e Reumatologi Per la Sostenibilità del SSR 13 gennaio 2017 Palazzo Pirelli Cosa Chiedono il SSN e il SSR? Massimo Medaglia Direzione Generale Welfare Regione
MEDICINALI BIOEQUIVALENTI E BIOSIMILARI. Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara
 MEDICINALI BIOEQUIVALENTI E BIOSIMILARI Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara FARMACO GENERICO e EQUIVALENTE Con la Legge 28/12/1995 art. 130 comma 3, il
MEDICINALI BIOEQUIVALENTI E BIOSIMILARI Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara FARMACO GENERICO e EQUIVALENTE Con la Legge 28/12/1995 art. 130 comma 3, il
Uso di farmaci biosimilari Ylenia Ingrasciotta
 Uso di farmaci biosimilari Ylenia Ingrasciotta A.O.U. Policlinico «G. Martino», Messina Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia: tecnologia per la manipolazione
Uso di farmaci biosimilari Ylenia Ingrasciotta A.O.U. Policlinico «G. Martino», Messina Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia: tecnologia per la manipolazione
I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO
 I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO INTRODUZIONE I farmaci I farmaci generici Bioequivalenza I farmaci generici equivalenti I farmaci biologici Biosimilarità
I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO INTRODUZIONE I farmaci I farmaci generici Bioequivalenza I farmaci generici equivalenti I farmaci biologici Biosimilarità
ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
CLASSICHE GENETICA BIOTECNOLOGIE MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA
 CLASSICHE BIOTECNOLOGIE GENETICA MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA BIOLOGIA MOLECOLARE BIOCHIMICA CREAZIONE A FINI MEDICI DI MICRO-ORGANISMI GENETICAMENTE MODIFICATI
CLASSICHE BIOTECNOLOGIE GENETICA MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA BIOLOGIA MOLECOLARE BIOCHIMICA CREAZIONE A FINI MEDICI DI MICRO-ORGANISMI GENETICAMENTE MODIFICATI
I FARMACI BIOTECNOLOGICI E BIOSIMILARI
 I FARMACI BIOTECNOLOGICI E BIOSIMILARI Olga Addimanda, Riccardo Meliconi SSD Medicina e Reumatologia Istituto Ortopedico Rizzoli Università di Bologna Storia delle terapie immunosoppressive per le malattie
I FARMACI BIOTECNOLOGICI E BIOSIMILARI Olga Addimanda, Riccardo Meliconi SSD Medicina e Reumatologia Istituto Ortopedico Rizzoli Università di Bologna Storia delle terapie immunosoppressive per le malattie
Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore)
 1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
L Agenzia Italiana del Farmaco nel contesto europeo
 L Agenzia Italiana del Farmaco nel contesto europeo Luca Pani @Luca Pani - dg@aifa.gov.it Milano, 18 ottobre 2016 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono
L Agenzia Italiana del Farmaco nel contesto europeo Luca Pani @Luca Pani - dg@aifa.gov.it Milano, 18 ottobre 2016 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono
È opportuno introdurre una chiara indicazione sull etichettatura del farmaco per assicurare un informazione trasparente sul medicinale utilizzato.
 I biosimilari La posizione delle Aziende farmaceutiche Executive summary I farmaci biosimilari usati in modo appropriato possono essere uno strumento per liberare risorse da allocare per un rapido e universale
I biosimilari La posizione delle Aziende farmaceutiche Executive summary I farmaci biosimilari usati in modo appropriato possono essere uno strumento per liberare risorse da allocare per un rapido e universale
I biosimilari fra presente e futuro
 ANALISI DELLA PRESCRIZIONE FARMACEUTICA IN ITALIA presentazione del Rapporto Nazionale OsMed 2010 7 luglio 2011 aula Pocchiari I biosimilari fra presente e futuro Anna Maria Marata Lucia Magnano Che cos
ANALISI DELLA PRESCRIZIONE FARMACEUTICA IN ITALIA presentazione del Rapporto Nazionale OsMed 2010 7 luglio 2011 aula Pocchiari I biosimilari fra presente e futuro Anna Maria Marata Lucia Magnano Che cos
Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema. Dott.ssa Maria Susanna Rivetti
 Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema Dott.ssa Maria Susanna Rivetti 1 D.L.vo 219/2006 e s.m.i. Definizione Medicinali biologici Medicinali il cui principio attivo
Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema Dott.ssa Maria Susanna Rivetti 1 D.L.vo 219/2006 e s.m.i. Definizione Medicinali biologici Medicinali il cui principio attivo
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana.
 Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana. Le scadenze brevettuali sono aumentate dal 2000 ad 2008 ma dopo
Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana. Le scadenze brevettuali sono aumentate dal 2000 ad 2008 ma dopo
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici
 Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Il Ruolo del
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Il Ruolo del
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA 1 2 Il Ruolo
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA 1 2 Il Ruolo
Insuline biosimilari e antidiabetici generici
 POSITION STATEMENT Insuline biosimilari e antidiabetici generici Roberto Miccoli, Antonio Bossi, Daniela Bruttomesso, Angelo De Pascale, Gabriella Gruden, Davide Lauro, Frida Leonetti, Edoardo Mannucci,
POSITION STATEMENT Insuline biosimilari e antidiabetici generici Roberto Miccoli, Antonio Bossi, Daniela Bruttomesso, Angelo De Pascale, Gabriella Gruden, Davide Lauro, Frida Leonetti, Edoardo Mannucci,
Farmaci bioequivalenti o generici: ostacolo o opportunità per l innovazione terapeutica?
 Farmaci bioequivalenti o generici: ostacolo o opportunità per l innovazione terapeutica? Roberto Trevisan USC Malattie Endocrine - Diabetologia ASST Papa Giovanni XXIII (Bergamo) Background I farmaci costano.
Farmaci bioequivalenti o generici: ostacolo o opportunità per l innovazione terapeutica? Roberto Trevisan USC Malattie Endocrine - Diabetologia ASST Papa Giovanni XXIII (Bergamo) Background I farmaci costano.
I FARMACI BIOTECNOLOGICI E BIOSIMILARI
 I FARMACI BIOTECNOLOGICI E BIOSIMILARI Olga Addimanda, Riccardo Meliconi SSD Medicina e Reumatologia Istituto Ortopedico Rizzoli Università di Bologna Anno di approvazione FDA Storia delle terapie immunosoppressive
I FARMACI BIOTECNOLOGICI E BIOSIMILARI Olga Addimanda, Riccardo Meliconi SSD Medicina e Reumatologia Istituto Ortopedico Rizzoli Università di Bologna Anno di approvazione FDA Storia delle terapie immunosoppressive
DIFFERENTI MODALITA PER ANTAGONIZZARE IL TNF-α E DIVERSITA DEI BIOSIMILARI
 Milano, 18 ottobre 2011 DIFFERENTI MODALITA PER ANTAGONIZZARE IL TNF-α E DIVERSITA DEI BIOSIMILARI BACKGROUND L utilizzo dei nuovi farmaci definiti con il termine collettivo di biologici ha rivoluzionato
Milano, 18 ottobre 2011 DIFFERENTI MODALITA PER ANTAGONIZZARE IL TNF-α E DIVERSITA DEI BIOSIMILARI BACKGROUND L utilizzo dei nuovi farmaci definiti con il termine collettivo di biologici ha rivoluzionato
WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO
 WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE
WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE
Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva
 Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva Pierluigi Navarra Istituto di Farmacologia Facoltà di Medicina e Chirurgia Università Cattolica - Roma Analisi
Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva Pierluigi Navarra Istituto di Farmacologia Facoltà di Medicina e Chirurgia Università Cattolica - Roma Analisi
Malattie rare e farmaci orfani: la difficoltà di coniugare bisogno assistenziale e scarsità di risorse
 Malattie rare e farmaci orfani: la difficoltà di coniugare bisogno assistenziale e scarsità di risorse La ricerca farmaceutica ed i farmaci orfani Marina Del Bue Comitato di Presidenza ASSOBIOTEC CAMERA
Malattie rare e farmaci orfani: la difficoltà di coniugare bisogno assistenziale e scarsità di risorse La ricerca farmaceutica ed i farmaci orfani Marina Del Bue Comitato di Presidenza ASSOBIOTEC CAMERA
I biosimilari tra presente e futuro. L impatto nella pratica clinica. dei biosimilari in: Nefrologia. G. Brunori. Trento
 I biosimilari tra presente e futuro L impatto nella pratica clinica dei biosimilari in: Nefrologia G. Brunori Trento Corso di formazione manageriale per dirigenti sanitari 2 marzo 2010 Valutazione della
I biosimilari tra presente e futuro L impatto nella pratica clinica dei biosimilari in: Nefrologia G. Brunori Trento Corso di formazione manageriale per dirigenti sanitari 2 marzo 2010 Valutazione della
È un medicinale che contiene lo stesso principio attivo e nella stessa concentrazione di un farmaco di marca non più coperto da brevetto(definito
 CHE COS'È UN FARMACO EQUIVALENTE? È un medicinale che contiene lo stesso principio attivo e nella stessa concentrazione di un farmaco di marca non più coperto da brevetto(definito originator). I farmaci
CHE COS'È UN FARMACO EQUIVALENTE? È un medicinale che contiene lo stesso principio attivo e nella stessa concentrazione di un farmaco di marca non più coperto da brevetto(definito originator). I farmaci
Michela Franzin. Servizio di Farmacia. IRCCS Ospedale San Raffaele
 Michela Franzin Servizio di Farmacia IRCCS Ospedale San Raffaele La quota di mercato dei farmaci biologici con brevetto in scadenza tra il 2015 ed il 2020 è rilevante Potenziale risparmio derivante dalla
Michela Franzin Servizio di Farmacia IRCCS Ospedale San Raffaele La quota di mercato dei farmaci biologici con brevetto in scadenza tra il 2015 ed il 2020 è rilevante Potenziale risparmio derivante dalla
Sostenibilità dell innovazione e HTA delle terapie innovative
 Sostenibilità dell innovazione e HTA delle terapie innovative Marco Marchetti Responsabile dell'unità di Valutazione delle Tecnologie Policlinico Gemelli Università Cattolica del Sacro Cuore Roma, 14 Aprile
Sostenibilità dell innovazione e HTA delle terapie innovative Marco Marchetti Responsabile dell'unità di Valutazione delle Tecnologie Policlinico Gemelli Università Cattolica del Sacro Cuore Roma, 14 Aprile
INDICATORI DI APPROPRIATEZZA PRESCRITTIVA E FOCUS SU ALCUNE CATEGORIE TERAPEUTICHE AD ALTO COSTO
 INDICATORI DI APPROPRIATEZZA PRESCRITTIVA E FOCUS SU ALCUNE CATEGORIE TERAPEUTICHE AD ALTO COSTO gennaio-settembre 2014 COORDINAMENTO REGIONALE UNICO SUL FARMACO REGIONE VENETO INDICATORI DI APPROPRIATEZZA
INDICATORI DI APPROPRIATEZZA PRESCRITTIVA E FOCUS SU ALCUNE CATEGORIE TERAPEUTICHE AD ALTO COSTO gennaio-settembre 2014 COORDINAMENTO REGIONALE UNICO SUL FARMACO REGIONE VENETO INDICATORI DI APPROPRIATEZZA
DIPARTIMENTO DELL INNOVAZIONE DIREZIONE GENERALE DELLA RICERCA SCIENTIFICA E TECNOLOGICA UFFICIO IV DELL EX MINISTERO DELLA SALUTE ***
 DIPARTIMENTO DELL INNOVAZIONE DIREZIONE GENERALE DELLA RICERCA SCIENTIFICA E TECNOLOGICA UFFICIO IV DELL EX MINISTERO DELLA SALUTE *** LE BIOTECNOLOGIE CHE COSA SONO LE BIOTECNOLOGIE? Le biotecnologie
DIPARTIMENTO DELL INNOVAZIONE DIREZIONE GENERALE DELLA RICERCA SCIENTIFICA E TECNOLOGICA UFFICIO IV DELL EX MINISTERO DELLA SALUTE *** LE BIOTECNOLOGIE CHE COSA SONO LE BIOTECNOLOGIE? Le biotecnologie
Curriculum Farmaceutico Afferisce alla. Facoltà di Scienze del Farmaco
 Corso di Laurea in Biotecnologia Curriculum Farmaceutico Afferisce alla Facoltà di Scienze del Farmaco http://www.scienzedelfarmaco.unimi.it/ Dipartimenti: - Scienze Farmacologiche e Biomolecolari (DiSFeB)
Corso di Laurea in Biotecnologia Curriculum Farmaceutico Afferisce alla Facoltà di Scienze del Farmaco http://www.scienzedelfarmaco.unimi.it/ Dipartimenti: - Scienze Farmacologiche e Biomolecolari (DiSFeB)
Tecnologie del DNA ricombinante. Farmaci e tessuti BIOTECNOLOGICI
 Tecnologie del DNA ricombinante. Farmaci e tessuti BIOTECNOLOGICI INGEGNERIA CELLULARE definizioni: DNA ricombinante: Molecole di DNA prodotte artificialmente e contenenti sequenze provenienti da diversi
Tecnologie del DNA ricombinante. Farmaci e tessuti BIOTECNOLOGICI INGEGNERIA CELLULARE definizioni: DNA ricombinante: Molecole di DNA prodotte artificialmente e contenenti sequenze provenienti da diversi
L epidemiologia della psoriasi in Regione Veneto
 L epidemiologia della psoriasi in Regione Veneto Margherita Andretta Padova 9 novembre 2017 Dalla letteratura IN ITALIA si stima che: circa 1.500.000 soggetti sono affetti da psoriasi di cui: 10-20% soffre
L epidemiologia della psoriasi in Regione Veneto Margherita Andretta Padova 9 novembre 2017 Dalla letteratura IN ITALIA si stima che: circa 1.500.000 soggetti sono affetti da psoriasi di cui: 10-20% soffre
PRESCRIZIONE FARMACEUTICA ATTRAVERSO LE AZIENDE SANITARIE DELLA REGIONE VENETO. gennaio-marzo 2014
 PRESCRIZIONE FARMACEUTICA ATTRAVERSO LE AZIENDE SANITARIE DELLA REGIONE VENETO gennaio-marzo 2014 COORDINAMENTO REGIONALE UNICO SUL FARMACO REGIONE VENETO INDICATORI DI APPROPRIATEZZA PRESCRITTIVA 1. Protezione
PRESCRIZIONE FARMACEUTICA ATTRAVERSO LE AZIENDE SANITARIE DELLA REGIONE VENETO gennaio-marzo 2014 COORDINAMENTO REGIONALE UNICO SUL FARMACO REGIONE VENETO INDICATORI DI APPROPRIATEZZA PRESCRITTIVA 1. Protezione
Legislazione sui farmaci equivalenti, provvedimenti regionali, risparmi. farmaci genericati. Dott.ssa Maria Susanna Rivetti
 Legislazione sui farmaci equivalenti, provvedimenti regionali, risparmi realizzati e possibili con l uso dei farmaci genericati Dott.ssa Maria Susanna Rivetti NORMATIVA DI RIFERIMENTO LA LEGGE 425/1996
Legislazione sui farmaci equivalenti, provvedimenti regionali, risparmi realizzati e possibili con l uso dei farmaci genericati Dott.ssa Maria Susanna Rivetti NORMATIVA DI RIFERIMENTO LA LEGGE 425/1996
Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica
 Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Siamo partiti da questo La Repubblica 24
Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Siamo partiti da questo La Repubblica 24
Presentazione: L uso dei biosimilari e la tutela del paziente
 Presentazione: L uso dei biosimilari e la tutela del paziente Relatore: Avv. Francesca Mastroianni 30 maggio 2017 Public Declaration of transparency/interests* Interests in pharmaceutical industry NO Current
Presentazione: L uso dei biosimilari e la tutela del paziente Relatore: Avv. Francesca Mastroianni 30 maggio 2017 Public Declaration of transparency/interests* Interests in pharmaceutical industry NO Current
SVILUPPO DI UN FARMACO
 SVILUPPO DI UN FARMACO Storicamente l identificazione e lo sviluppo di nuovi farmaci di è evoluta da Approccio EURISTCO (empirico) Approccio MECCANICISTICO Approccio ORIENTATO AL BERSAGLIO Approccio EURISTICO
SVILUPPO DI UN FARMACO Storicamente l identificazione e lo sviluppo di nuovi farmaci di è evoluta da Approccio EURISTCO (empirico) Approccio MECCANICISTICO Approccio ORIENTATO AL BERSAGLIO Approccio EURISTICO
Il Farmaco Veterinario: l utilizzo off-label e i generici
 Audizione Commissione Senato Roma, 14 marzo 2017 Il Farmaco Veterinario: l utilizzo off-label e i generici M. Fornasier Medico Veterinario - SIVAL Disegno di legge n. 540 e 499: che cosa deve fare il veterinario?
Audizione Commissione Senato Roma, 14 marzo 2017 Il Farmaco Veterinario: l utilizzo off-label e i generici M. Fornasier Medico Veterinario - SIVAL Disegno di legge n. 540 e 499: che cosa deve fare il veterinario?
BIOSIMILARI LUCI E OMBRE
 BIOSIMILARI LUCI E OMBRE L avvento dei farmaci biotecnologici risale agli anni Ottanta del secolo scorso, con l immissione in commercio della prima insulina ricombinante. Attualmente sono disponibili numerosi
BIOSIMILARI LUCI E OMBRE L avvento dei farmaci biotecnologici risale agli anni Ottanta del secolo scorso, con l immissione in commercio della prima insulina ricombinante. Attualmente sono disponibili numerosi
Quaderni. della SIF. Anno XII n.41 Novembre Focus on Il Sistema Regolatorio in Italia tra certezze e contraddizioni
 ISSN 2039-9561 Anno XII n.41 Novembre 2016 Quaderni della SIF 3 Focus on Il Sistema Regolatorio in Italia tra certezze e contraddizioni 5 La posizione della SIF sui mab: le certezze e i punti ancora aperti
ISSN 2039-9561 Anno XII n.41 Novembre 2016 Quaderni della SIF 3 Focus on Il Sistema Regolatorio in Italia tra certezze e contraddizioni 5 La posizione della SIF sui mab: le certezze e i punti ancora aperti
AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI*
 1/5 Abatacept, Adalimumab, Anakinra, Certolizumab Pegol, Etanercept, Golimumab, Infliximab, Tocilizumab, Rituximab ARTRITE REUMATOIDE: i farmaci devono essere prescritti solamente dai centri specializzati
1/5 Abatacept, Adalimumab, Anakinra, Certolizumab Pegol, Etanercept, Golimumab, Infliximab, Tocilizumab, Rituximab ARTRITE REUMATOIDE: i farmaci devono essere prescritti solamente dai centri specializzati
FACOLTÀ DI MEDICINA E CHIRURGIA CORSO DI LAUREA IN BIOTECNOLOGIE MEDICHE E FARMACEUTICHE
 FACOLTÀ DI MEDICINA E CHIRURGIA CORSO DI LAUREA IN BIOTECNOLOGIE MEDICHE E FARMACEUTICHE PRESENTAZIONE Lo sviluppo scientifico in campo biomedico ha subito un accelerazione senza precedenti dalla scoperta
FACOLTÀ DI MEDICINA E CHIRURGIA CORSO DI LAUREA IN BIOTECNOLOGIE MEDICHE E FARMACEUTICHE PRESENTAZIONE Lo sviluppo scientifico in campo biomedico ha subito un accelerazione senza precedenti dalla scoperta
Corso di Laurea in Biotecnologie Mediche e Farmaceutiche
 Corso di Laurea in Biotecnologie Mediche e Farmaceutiche Corso di Laurea in Biotecnologie Mediche e Farmaceutiche Preside della Facoltà di Medicina e Chirurgia: Prof. Massimo Clementi Presidente del Corso
Corso di Laurea in Biotecnologie Mediche e Farmaceutiche Corso di Laurea in Biotecnologie Mediche e Farmaceutiche Preside della Facoltà di Medicina e Chirurgia: Prof. Massimo Clementi Presidente del Corso
Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica
 Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Principi generali del comparability exercise
Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Principi generali del comparability exercise
FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI
 FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI nelle Malattie Infiammatorie Croniche Intestinali Dr.ssa Valentina CASINI ASST Bergamo EST Bolognini Seriate (BG) FARMACO BIOLOGICO FARMACO BIOSIMILARE DI COSA
FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI nelle Malattie Infiammatorie Croniche Intestinali Dr.ssa Valentina CASINI ASST Bergamo EST Bolognini Seriate (BG) FARMACO BIOLOGICO FARMACO BIOSIMILARE DI COSA
Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO)
 Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO) SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi
Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO) SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi
Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali e nazionali. Francesca Mattioli
 FARMACO DI MARCA O EQUIVALENTE? Qualità, efficacia e responsabilità nell'attività prescrittiva Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali
FARMACO DI MARCA O EQUIVALENTE? Qualità, efficacia e responsabilità nell'attività prescrittiva Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali
Criteri AIFA per l equivalenza terapeutica tra farmaci
 Criteri AIFA per l equivalenza terapeutica tra farmaci a cura di Giorgio Cantelli Forti (Presidente, Società Italiana di Farmacologia) Francesco Rossi (Past President, Società Italiana di Farmacologia)
Criteri AIFA per l equivalenza terapeutica tra farmaci a cura di Giorgio Cantelli Forti (Presidente, Società Italiana di Farmacologia) Francesco Rossi (Past President, Società Italiana di Farmacologia)
Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie per l innovazione di processi e prodotti A.A. 2011/12
 Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie per l innovazione di processi e prodotti A.A. 2011/12 Titolo insegnamento: Biotecnologie delle fermentazioni (Prof. Luigi Palmieri) integrato
Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie per l innovazione di processi e prodotti A.A. 2011/12 Titolo insegnamento: Biotecnologie delle fermentazioni (Prof. Luigi Palmieri) integrato
Allegato A al Decreto n. 017 del 23 febbraio 2017 pag. 1/5
 giunta regionale Allegato A al Decreto n. 017 del 23 febbraio 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA,
giunta regionale Allegato A al Decreto n. 017 del 23 febbraio 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA,
n.4 LA SALUTE È UN DIRITTO DI TUTTI. I farmaci generici: UN ALTERNATIVA DI QUALITÀ E i farmaci generici danno il loro contributo
 n.4 I farmaci generici: UN ALTERNATIVA DI QUALITÀ IN EVIDENZA Quanto risparmia UNA FAMIGLIA? Una soluzione al problema dei FARMACI INTROVABILI LA SALUTE È UN DIRITTO DI TUTTI. E i farmaci generici danno
n.4 I farmaci generici: UN ALTERNATIVA DI QUALITÀ IN EVIDENZA Quanto risparmia UNA FAMIGLIA? Una soluzione al problema dei FARMACI INTROVABILI LA SALUTE È UN DIRITTO DI TUTTI. E i farmaci generici danno
Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5
 giunta regionale Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
giunta regionale Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
Liste di trasparenza- Precisazioni su alcuni farmaci. Topiramato-levetiracetam tacrolimus
 Liste di trasparenza- Precisazioni su alcuni farmaci Topiramato-levetiracetam tacrolimus Specialità medicinali contenenti Levetiracetam e Topiramato (17/09/2012) La prima prescrizione di un trattamento
Liste di trasparenza- Precisazioni su alcuni farmaci Topiramato-levetiracetam tacrolimus Specialità medicinali contenenti Levetiracetam e Topiramato (17/09/2012) La prima prescrizione di un trattamento
FACOLTA' DI FARMACIA Corso di Laurea in CHIMICA E TECNOLOGIA FARMACEUTICHE PIANO DEGLI STUDI ANNO ACCADEMICO 2004/2005
 FACOLTA' DI FARMACIA Corso di Laurea in CHIMICA E TECNOLOGIA FARMACEUTICHE PIANO DEGLI STUDI ANNO ACCADEMICO 00/005 L Ordinamento Didattico del Corso di Laurea in Chimica e Tecnologia Farmaceutiche per
FACOLTA' DI FARMACIA Corso di Laurea in CHIMICA E TECNOLOGIA FARMACEUTICHE PIANO DEGLI STUDI ANNO ACCADEMICO 00/005 L Ordinamento Didattico del Corso di Laurea in Chimica e Tecnologia Farmaceutiche per
La promozione della Sperimentazione Clinica in età pediatrica
 La promozione della Sperimentazione Clinica in età pediatrica Leonardo Felici Az. Ospedali Riuniti Marche Nord Pesaro-Fano Scenario generale Il numero delle sperimentazioni cliniche con farmaci in ambito
La promozione della Sperimentazione Clinica in età pediatrica Leonardo Felici Az. Ospedali Riuniti Marche Nord Pesaro-Fano Scenario generale Il numero delle sperimentazioni cliniche con farmaci in ambito
Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5
 giunta regionale Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
giunta regionale Allegato A al Decreto n. 77 del 22 giugno 2017 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
CONOSCENZE / COMPETENZE STRUMENTI E METODI LABORATORIO COLLEGAMENTI VERIFICHE ORE
 PROGRAMMAZIONE DIDATTICA DEL CORSO DI BIOLOGIA,MICROBIOLOGIA E TECNOLOGIE DI CONTROLLO SANITARIO CLASSE 5 D ANNO SCOLASTICO 2015-2016 Proff ELENA ZACCHIA, RAFFAELE FIORINI MODULI MODULO 1 Modulo di raccordo
PROGRAMMAZIONE DIDATTICA DEL CORSO DI BIOLOGIA,MICROBIOLOGIA E TECNOLOGIE DI CONTROLLO SANITARIO CLASSE 5 D ANNO SCOLASTICO 2015-2016 Proff ELENA ZACCHIA, RAFFAELE FIORINI MODULI MODULO 1 Modulo di raccordo
Open Speech: l AIFA incontra le Associazioni 8 febbraio 2013 Ad un anno dall incontro cosa è successo in termini di coinvolgimento delle associazioni?
 Open Speech: l AIFA incontra le Associazioni 8 febbraio 2013 Ad un anno dall incontro cosa è successo in termini di coinvolgimento delle associazioni? Le maggiori criticità nell accesso al farmaco dal
Open Speech: l AIFA incontra le Associazioni 8 febbraio 2013 Ad un anno dall incontro cosa è successo in termini di coinvolgimento delle associazioni? Le maggiori criticità nell accesso al farmaco dal
Milano, il 27 luglio del Al Ministro della Salute On.le Prof. Ferruccio Fazio Lungotevere Ripa, ROMA
 Milano, il 27 luglio del 2011 Al Ministro della Salute On.le Prof. Ferruccio Fazio Lungotevere Ripa, 1 00153 ROMA Al Sottosegretario alla Salute On.le Francesca Martini Lungotevere Ripa, 1 00153 ROMA Al
Milano, il 27 luglio del 2011 Al Ministro della Salute On.le Prof. Ferruccio Fazio Lungotevere Ripa, 1 00153 ROMA Al Sottosegretario alla Salute On.le Francesca Martini Lungotevere Ripa, 1 00153 ROMA Al
HTA e HS per la Farmaceutica al 2020 I Nuovi Scenari. Nello Martini Direttore Scientifico Accademia Nazionale di Medicina
 HTA e HS per la Farmaceutica al 2020 I Nuovi Scenari Nello Martini Direttore Scientifico Accademia Nazionale di Medicina LE 3 QUESTIONI DI FONDO Il nuovo modello di ricerca e sviluppo HS: il mercato farmaceutico
HTA e HS per la Farmaceutica al 2020 I Nuovi Scenari Nello Martini Direttore Scientifico Accademia Nazionale di Medicina LE 3 QUESTIONI DI FONDO Il nuovo modello di ricerca e sviluppo HS: il mercato farmaceutico
Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche Napoli 26 Maggio 2017, Hotel Holiday Inn
 Federico II University of Naples Founded in 1224 Divisione di Farmacologia Scuola di Medicina Università di Napoli Federico II Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche
Federico II University of Naples Founded in 1224 Divisione di Farmacologia Scuola di Medicina Università di Napoli Federico II Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche
FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF
 FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF Nell ambito della Terza edizione del progetto Il sistema regolatorio in Italia tra certezze
FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF Nell ambito della Terza edizione del progetto Il sistema regolatorio in Italia tra certezze
Farmainforma POSIZIONE SUI FARMACI BIOSIMILARI. MEDICINALE BIOLOGICO: medicinale che contiene. MEDICINALE BIOTECNOLOGICO: medicinale
 Farmainforma Informazione sui farmaci e la farmacovigilanza-numero Speciale Novembre 2016 Documento approvato dalla Commissione del PTOTA nella riunione del 30 novembre 2016 BIOSIMILARI - DEFINIZIONI MEDICINALE
Farmainforma Informazione sui farmaci e la farmacovigilanza-numero Speciale Novembre 2016 Documento approvato dalla Commissione del PTOTA nella riunione del 30 novembre 2016 BIOSIMILARI - DEFINIZIONI MEDICINALE
Biotecnologia: la salute nel portafoglio
 Biotecnologia: la salute nel portafoglio 2000 - Il genoma umano La decodificazione del DNA ha segnato l inizio dell era più importante nella storia della civiltà umana. Siamo passati dalla rivoluzione
Biotecnologia: la salute nel portafoglio 2000 - Il genoma umano La decodificazione del DNA ha segnato l inizio dell era più importante nella storia della civiltà umana. Siamo passati dalla rivoluzione
Stato dell assistenza alle persone con malattia rara in Italia: il contributo delle Regioni
 Stato dell assistenza alle persone con malattia rara in Italia: il contributo delle Regioni Le somministrazioni domiciliari dei farmaci orfani Giuseppe Secchi, Farmindustria Roma, 21 aprile 2015 Le imprese
Stato dell assistenza alle persone con malattia rara in Italia: il contributo delle Regioni Le somministrazioni domiciliari dei farmaci orfani Giuseppe Secchi, Farmindustria Roma, 21 aprile 2015 Le imprese
I Biosimilari: discussione. Alessandro Comandone SC Oncologia Ospedale Gradenigo Torino
 I Biosimilari: discussione Alessandro Comandone SC Oncologia Ospedale Gradenigo Torino Terminology Chemical drugs Biotech Medicines copy attempt to copy "Generics" Biosimilars Follow-on Biologics 2 INDICE
I Biosimilari: discussione Alessandro Comandone SC Oncologia Ospedale Gradenigo Torino Terminology Chemical drugs Biotech Medicines copy attempt to copy "Generics" Biosimilars Follow-on Biologics 2 INDICE
Premio Galeno Italia per l Innovazione del Farmaco 2017
 Premio Galeno Italia per l Innovazione del Farmaco 2017 Presentazione Springer Healthcare Italia annuncia l apertura dei bandi di concorso del Premio Galeno Italia 2017 per l Innovazione del Farmaco 1.
Premio Galeno Italia per l Innovazione del Farmaco 2017 Presentazione Springer Healthcare Italia annuncia l apertura dei bandi di concorso del Premio Galeno Italia 2017 per l Innovazione del Farmaco 1.
BIOTECNOLOGIE E SALUTE
 BIOTECNOLOGIE E SALUTE Le ragioni del successo del Biotech Leonardo Vingiani - Direttore Assobiotec Roma, 22 maggio 2007 Le biotecnologie rappresentano il futuro della Medicina Un settore che esiste da
BIOTECNOLOGIE E SALUTE Le ragioni del successo del Biotech Leonardo Vingiani - Direttore Assobiotec Roma, 22 maggio 2007 Le biotecnologie rappresentano il futuro della Medicina Un settore che esiste da
Dichiarazione di trasparenza/interessi*
 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA Interessi nell industria farmaceutica NO Attualmente Precedenti
Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA Interessi nell industria farmaceutica NO Attualmente Precedenti
Innovazione sostenibile in dermatologia e in reumatologia
 Innovazione sostenibile in dermatologia e in reumatologia Enrica Menditto CIRFF - Dipartimento di Farmacia Università degli Studi di Napoli Federico II Napoli, 26 maggio 2017 La sostenibilità del sistema
Innovazione sostenibile in dermatologia e in reumatologia Enrica Menditto CIRFF - Dipartimento di Farmacia Università degli Studi di Napoli Federico II Napoli, 26 maggio 2017 La sostenibilità del sistema
Allegato A al Decreto n. 46 del 11 Maggio 2016 pag. 1/5
 giunta regionale Allegato A al Decreto n. 46 del 11 Maggio 2016 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
giunta regionale Allegato A al Decreto n. 46 del 11 Maggio 2016 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
Milano, 13 gennaio 2017
 Milano, 13 gennaio 2017 L esperienza della ASST di Brescia U.O. Farmacia Spedali Civili di Brescia Daria Bettoni Responsabile del Settore Farmaci e Farmacovigilanza Progetto Spedali Civili, criticità e
Milano, 13 gennaio 2017 L esperienza della ASST di Brescia U.O. Farmacia Spedali Civili di Brescia Daria Bettoni Responsabile del Settore Farmaci e Farmacovigilanza Progetto Spedali Civili, criticità e
Le implicazioni per il farmacista ospedaliero
 IL NUOVO CODICE DEGLI APPALTI. INNOVAZIONI E CAMBIAMENTI NELLE PROCEDURE DI APPROVVIGIONAMENTO DI BENI E SERVIZI IN SANITÀ: POSSONO COESISTERE TRASPARENZA ED EFFICIENZA? Torino, 7 aprile 2017 Le implicazioni
IL NUOVO CODICE DEGLI APPALTI. INNOVAZIONI E CAMBIAMENTI NELLE PROCEDURE DI APPROVVIGIONAMENTO DI BENI E SERVIZI IN SANITÀ: POSSONO COESISTERE TRASPARENZA ED EFFICIENZA? Torino, 7 aprile 2017 Le implicazioni
Innovatività e appropriatezza : criteri di valutazione dei farmaci
 Innovatività e appropriatezza : criteri di valutazione dei farmaci Massimo Medaglia Dipartimento Farmaceutico Ospedale L. Sacco Azienda Ospedaliera Polo Universitario Milano L innovazione nella terapia
Innovatività e appropriatezza : criteri di valutazione dei farmaci Massimo Medaglia Dipartimento Farmaceutico Ospedale L. Sacco Azienda Ospedaliera Polo Universitario Milano L innovazione nella terapia
Insulina glargine biosimilare
 Scheda di valutazione del farmaco Insulina glargine biosimilare A cura della Commissione Regionale del Farmaco della Regione Emilia-Romagna Doc PTR n. 278 Recepito con determina n. 8419 del 26/05/2016
Scheda di valutazione del farmaco Insulina glargine biosimilare A cura della Commissione Regionale del Farmaco della Regione Emilia-Romagna Doc PTR n. 278 Recepito con determina n. 8419 del 26/05/2016
IL FARMACO GENERICO-EQUIVALENTE CRITICITA E PROSPETTIVE
 IL FARMACO GENERICO-EQUIVALENTE CRITICITA E PROSPETTIVE PROF. GUIDO RASI DIRETTORE GENERALE AGENZIA ITALIANA DEL FARMACO Congresso Assogenerici Roma, 25 settembre 1 2008 RIFERIMENTI NORMATIVI La legge
IL FARMACO GENERICO-EQUIVALENTE CRITICITA E PROSPETTIVE PROF. GUIDO RASI DIRETTORE GENERALE AGENZIA ITALIANA DEL FARMACO Congresso Assogenerici Roma, 25 settembre 1 2008 RIFERIMENTI NORMATIVI La legge
Iter prescrittivi e modelli organizzativi per accedere ai farmaci biologici: risultati del questionario
 UNIVERSITA DEGLI STUDI DI GENOVA S.C. FARMACEUTICA ASL CHIAVARESE Corso residenziale di aggiornamento a cura della sezione regionale SIFO Liguria I FARMACI BIOLOGICI NELLE PATOLOGIE AUTOIMMUNI Iter prescrittivi
UNIVERSITA DEGLI STUDI DI GENOVA S.C. FARMACEUTICA ASL CHIAVARESE Corso residenziale di aggiornamento a cura della sezione regionale SIFO Liguria I FARMACI BIOLOGICI NELLE PATOLOGIE AUTOIMMUNI Iter prescrittivi
Laurea in Biotecnologie Laurea in Scienze Biologiche. L M in Biotecnologie Industriali L M in Biotecnologie Mediche e Farmaceutiche L M in Biologia
 Laurea in Biotecnologie Laurea in Scienze Biologiche L M in Biotecnologie Industriali L M in Biotecnologie Mediche e Farmaceutiche L M in Biologia Corso di laurea in Corso di laurea in Parte pre-biologica
Laurea in Biotecnologie Laurea in Scienze Biologiche L M in Biotecnologie Industriali L M in Biotecnologie Mediche e Farmaceutiche L M in Biologia Corso di laurea in Corso di laurea in Parte pre-biologica
Biosimilari, per una nuova alleanza tra clinica e società Efficacia, sicurezza e corretta informazione. Consensus paper
 Biosimilari, per una nuova alleanza tra clinica e società Efficacia, sicurezza e corretta informazione Consensus paper Giugno 2016 Introduzione I farmaci biosimilari possiedono caratteristiche di efficacia
Biosimilari, per una nuova alleanza tra clinica e società Efficacia, sicurezza e corretta informazione Consensus paper Giugno 2016 Introduzione I farmaci biosimilari possiedono caratteristiche di efficacia
RESOCONTO ATTIVITÀ 2012
 RESOCONTO ATTIVITÀ 2012 La psoriasi e l importanza dei registri clinici La psoriasi è una malattia cronica che può avere un impatto rilevante sulla qualità di vita dei pazienti che ne sono affetti. Negli
RESOCONTO ATTIVITÀ 2012 La psoriasi e l importanza dei registri clinici La psoriasi è una malattia cronica che può avere un impatto rilevante sulla qualità di vita dei pazienti che ne sono affetti. Negli
Un opuscolo per il lettore interessato. Biosimilari. Opportunità nella terapia con la nuova generazione di farmaci. Quelli con l arcobaleno
 Un opuscolo per il lettore interessato Biosimilari Opportunità nella terapia con la nuova generazione di farmaci Quelli con l arcobaleno 1 Sommario Dalla fabbricazione del pane, del vino e della birra
Un opuscolo per il lettore interessato Biosimilari Opportunità nella terapia con la nuova generazione di farmaci Quelli con l arcobaleno 1 Sommario Dalla fabbricazione del pane, del vino e della birra
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
FARMACI BIOLOGICI ORIGINATOR E BIOSIMILARI NELL AMBITO DELLE GARE PUBBLICHE. Elisa Teti. 30 maggio 2017
 FARMACI BIOLOGICI ORIGINATOR E BIOSIMILARI NELL AMBITO DELLE GARE PUBBLICHE Elisa Teti 30 maggio 2017 1 BIOLOGICI E BIOSIMILARI I farmaci biologici e biosimilari rappresentano un importante risorsa terapeutica
FARMACI BIOLOGICI ORIGINATOR E BIOSIMILARI NELL AMBITO DELLE GARE PUBBLICHE Elisa Teti 30 maggio 2017 1 BIOLOGICI E BIOSIMILARI I farmaci biologici e biosimilari rappresentano un importante risorsa terapeutica
I farmaci potenzialmente innovativi nel monitoraggio AIFA: cosa sorvegliare
 SECONDO CORSO REGIONALE DI FARMACOVIGILANZA I farmaci potenzialmente innovativi nel monitoraggio AIFA: cosa sorvegliare Bologna, 4-5 dicembre 2008 Nicola Montanaro CReVIF, Dipartimento di Farmacologia
SECONDO CORSO REGIONALE DI FARMACOVIGILANZA I farmaci potenzialmente innovativi nel monitoraggio AIFA: cosa sorvegliare Bologna, 4-5 dicembre 2008 Nicola Montanaro CReVIF, Dipartimento di Farmacologia
 Cromosoma del batterio donatore Trasferimento della ORF nel vettore di espressione PRODUZIONE DELLA PROTEINA RICOMBINANTE Abbondante e facilmente purificabile Contiene una ORF continua!! 5 NT non tradotto
Cromosoma del batterio donatore Trasferimento della ORF nel vettore di espressione PRODUZIONE DELLA PROTEINA RICOMBINANTE Abbondante e facilmente purificabile Contiene una ORF continua!! 5 NT non tradotto
funzioni di indirizzo vigilanza personalità giuridica di diritto pubblico e di autonomia organizzativa, patrimoniale, finanziaria e gestionale.
 AIFA. Art. 48,comma 13, del decreto-legge 30 settembre 2003,n.269,convertito nella legge 24 novembre 2003,n.326 Decreto 20 settembre 2004, n.245 Regolamento recante norme sull organizzazione ed il funzionamento
AIFA. Art. 48,comma 13, del decreto-legge 30 settembre 2003,n.269,convertito nella legge 24 novembre 2003,n.326 Decreto 20 settembre 2004, n.245 Regolamento recante norme sull organizzazione ed il funzionamento
Analisi dei costi della terapia antidiabetica
 La Farmacoeconomia: Supporto delle scelte appropriate Analisi dei costi della terapia antidiabetica E. Torre - 2012 La spesa per il diabete in Europa London School of Economics - 2011 letture possibili:
La Farmacoeconomia: Supporto delle scelte appropriate Analisi dei costi della terapia antidiabetica E. Torre - 2012 La spesa per il diabete in Europa London School of Economics - 2011 letture possibili:
Biologici e Biosimilari
 Biologici e Biosimilari in oncologia, occhi aperti sulle differenze Associazione Italiana Malati di Cancro, parenti e amici Introduzione Nel 2010 l Associazione Italiana di Oncologia Medica (AIOM) insieme
Biologici e Biosimilari in oncologia, occhi aperti sulle differenze Associazione Italiana Malati di Cancro, parenti e amici Introduzione Nel 2010 l Associazione Italiana di Oncologia Medica (AIOM) insieme
Documento PTR n. 119 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Farmaci Cnn e le differenze di compensabilità dei farmaci ad alto costo. Servizio Assistenza Territoriale Area Farmaco e Dispositivi Medici
 Farmaci Cnn e le differenze di compensabilità dei farmaci ad alto costo Servizio Assistenza Territoriale Area Farmaco e Dispositivi Medici Nuovi farmaci e classificazione C(nn) Art. 12 comma 5 L.189/2012
Farmaci Cnn e le differenze di compensabilità dei farmaci ad alto costo Servizio Assistenza Territoriale Area Farmaco e Dispositivi Medici Nuovi farmaci e classificazione C(nn) Art. 12 comma 5 L.189/2012
ALTERNATIVA CHE FA LA DIFFERENZA
 n.1 Equivalenti e Uguali Zentiva Oltre i farmaci di marca: UN MONDO DI VANTAGGI IN EVIDENZA Efficacia terapeutica e risparmio: SI PUÒ! Non solo equivalenti. Ecco GLI UGUALI! Come scegliere un farmaco?
n.1 Equivalenti e Uguali Zentiva Oltre i farmaci di marca: UN MONDO DI VANTAGGI IN EVIDENZA Efficacia terapeutica e risparmio: SI PUÒ! Non solo equivalenti. Ecco GLI UGUALI! Come scegliere un farmaco?
Università degli Studi di Perugia Valutazione della Didattica A.A Facoltà di Farmacia
 FARMACIA (Classe LM 13) FARMACOLOGIA E FARMACOTERAPIA E CHEMIOTERAPIA 8,3 58 CHIMICA FARMACEUTICA E TOSSICOLOGICA 2 8,3 52 TERAPIE INNOVATIVE 8,2 11 ANALISI MEDICINALI 3 E 4 8,2 53 FARMACOLOGIA GENERALE
FARMACIA (Classe LM 13) FARMACOLOGIA E FARMACOTERAPIA E CHEMIOTERAPIA 8,3 58 CHIMICA FARMACEUTICA E TOSSICOLOGICA 2 8,3 52 TERAPIE INNOVATIVE 8,2 11 ANALISI MEDICINALI 3 E 4 8,2 53 FARMACOLOGIA GENERALE
PRESENTAZIONE AZIENDALE. Spin off dell Università di Ferrara RNA BASED THERAPEUTICS, A R&D CUTTING EDGE
 PRESENTAZIONE AZIENDALE Spin off dell Università di Ferrara RNA BASED THERAPEUTICS, A R&D CUTTING EDGE MISSIONE: ricercare, brevettare e sviluppare Farmaci Biotecnologici innovativi (Gene Therapy Medicinal
PRESENTAZIONE AZIENDALE Spin off dell Università di Ferrara RNA BASED THERAPEUTICS, A R&D CUTTING EDGE MISSIONE: ricercare, brevettare e sviluppare Farmaci Biotecnologici innovativi (Gene Therapy Medicinal
Sviluppo futuro della ricerca clinica Mario Scartozzi
 HER2Club in gastric cancer Sviluppo futuro della ricerca clinica Mario Scartozzi La ricerca clinica per lo sviluppo di nuove strategie terapeutiche nei pazienti affetti da carcinoma gastrico metastatico
HER2Club in gastric cancer Sviluppo futuro della ricerca clinica Mario Scartozzi La ricerca clinica per lo sviluppo di nuove strategie terapeutiche nei pazienti affetti da carcinoma gastrico metastatico
Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN
 Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN Dr. Eugenio Ciacco Servizio Aziendale del Farmaco ASL1 Avezzano Sulmona L Aquila PARTIAMO DALL i presupposti dell Abruzzo
Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN Dr. Eugenio Ciacco Servizio Aziendale del Farmaco ASL1 Avezzano Sulmona L Aquila PARTIAMO DALL i presupposti dell Abruzzo
