La crisi della fisica classica
|
|
|
- Fabiano Mancini
- 6 anni fa
- Visualizzazioni
Transcript
1 Il problema del corpo nero e l ipotesi di Planck La crisi della fisica classica All inizio del XX secolo ancora due problemi non trovavano spiegazione all interno delle teorie dell elettromagnetismo e della termodinamica: il corpo nero e l effetto fotoelettrico La risoluzione di queste anomalie arrivò con la fisica quantistica, branca della fisica che ha come oggetto di ricerca i più piccoli costituenti della materia: le molecole, gli atomi, gli elettroni e le particelle nucleari. Per questi enti non valgono le leggi classiche della meccanica, della termodinamica e dell elettromagnetismo.
2 Moltissime sono ormai oggi le applicazioni delle nuove conoscenze del mondo atomico e subatomico laser, cellule fotoelettriche, centrali nucleari, apparecchiature medicali per la diagnostica o per la cura e la prevenzione di malattie, memorie e microprocessori dei calcolatori elettronici Ogni corpo emette una radiazione elettromagnetica che dipende dalla sua temperatura. Per esempio il corpo umano emette prevalentemente raggi infrarossi. All aumentare della temperatura del corpo aumenta la frequenza di questa radiazione
3 Il problema del corpo nero e l ipotesi di Planck Il corpo nero Un corpo nero è un sistema fisico teorico formato da una cavità con un piccolissimo foro, tale che la radiazione che vi entra ha una bassissima probabilità di uscire quando la cavità viene riscaldata, il corpo nero si comporta come un perfetto radiatore emette la cosiddetta radiazione di corpo nero La radiazione di corpo nero dipende esclusivamente dalla temperatura delle pareti, ossia dalla temperatura assoluta del corpo. Riassumiamo i risultati che prevedeva la fisica classica per il corpo nero legge di Stefan-Boltzmann legge di Wien legge di Rayleigh-Jeans
4 Nel 1860 Gustav Kirchhoff dimostrò che una cavità si comporta come un corpo nero perfetto se: le pareti della cavità si trovano a temperatura T costante (temperatura del corpo nero) nella cavità è praticato un foro le cui dimensioni sono trascurabili rispetto a quelle del corpo stesso Questa cavità si comporta altrettanto bene come corpo nero se le pareti vengono riscaldate: esse rispondono emettendo radiazione, comportandosi da perfetto radiatore
5 Il problema del corpo nero e l ipotesi di Planck a) Una cavità con un piccolissimo foro può essere considerata un corpo nero assorbitore ideale. b) Riscaldando le pareti, la cavità emette radiazioni che difficilmente possono disperdersi, quindi è anche un buon radiatore.
6 Il problema del corpo nero e l ipotesi di Planck Legge di Stefan-Boltzmann La potenza termica emessa o assorbita da un corpo per irraggiamento è uguale a I = εσst 4 Dove: s = 5, W m 2 K 4 è la costante di Stefan e è il coefficiente di emissione (0 < e 1) nel caso del corpo nero e = 1 perché è un perfetto radiatore e assorbitore S è la superficie del corpo interessata alla radiazione T è la sua temperatura
7 Legge di Wien Studiando lo spettro della radiazione elettromagnetica emessa da un corpo nero o radiazione di corpo nero, si vede che l andamento dipende solo dalla temperatura assoluta del corpo, con un picco di emissione a una specifica lunghezza d onda data dalla legge di Wien Legge di Wien La lunghezza d onda che corrisponde al valore massimo dell intensità della radiazione emessa dal corpo nero è inversamente proporzionale alla sua temperatura λ max T = K dove T è la temperatura assoluta (in kelvin) del corpo e K una costante pari a 2, (m K)
8 ANDAMENTO DELLA POTENZA IRRADIATA PER UNITA DI SUPEFICIE DAL CORPO NERO Riscaldando sempre di più un corpo nero, il massimo della potenza si sposta in corrispondenza di lunghezze d onda della radiazione sempre minori, vale a dire ad alte frequenze Curve sperimentali della radiazione di corpo nero: si possono ottenere scaldando un forno da laboratorio, portandolo a differenti temperature, e misurando l intensità della luce emessa tramite uno spettroscopio. In corrispondenza di ogni temperatura esiste un massimo della lunghezza d onda. La lunghezza d onda corrispondente al massimo valore dell intensità della radiazione è inversamente proporzionale alla temperatura secondo la legge di Wien.
9 Legge di Rayleigh-Jeans Per una data temperatura T, l intensità della radiazione emessa in funzione della lunghezza d onda è uguale a Legge di Rayleigh-Jeans dove T è la temperatura assoluta (in kelvin) del corpo e k B = 1, J/K è la costante di Boltzmann Per piccolissimi valori della lunghezza d onda, fissando T, si ottiene una potenza molto grande (al limite infinita) questa previsione teorica prende il nome di catastrofe ultravioletta
10 Il problema del corpo nero e l ipotesi di Planck Mettendo in un grafico tutti i possibili modi di vibrazione previsti dal modello di Jeans, otteniamo uno spettro pressoché continuo per lunghezze d onda molto piccole (grandi frequenze). A destra di λ 0 sono presenti poche radiazioni, mentre a sinistra sono praticamente infinite. L energia a disposizione viene confinata nella zona a lunghezze d onda piccolissime.
11 L ipotesi di Planck: il quanto di azione Max Planck ( ) risolse definitivamente il problema del corpo nero mostrando che le onde elettromagnetiche non assorbono l energia in modo continuo, ma discreto. Lo scambio di energia fra radiazione e materia avviene per quanti di radiazione (fotoni) e non in modo continuo. Planck spezzettò la radiazione attribuendo a ogni oscillatore risonante a frequenza f un energia quantizzata pari a un multiplo intero di h ha le dimensioni fisiche di un azione (energia per tempo) e per questo motivo fu chiamata quanto di azione h = 6, J s
12 Il problema del corpo nero e l ipotesi di Planck Distribuzione dell intensità di radiazione emessa dal corpo nero: la trattazione classica della legge di Rayleigh-Jeans prevede una catastrofe ultravioletta per le piccole lunghezze d onda che sperimentalmente non è verificata. Le ipotesi di Planck su un energia quantizzata permettono invece di seguire correttamente il fit dei dati sperimentali.
13 L effetto fotoelettrico Alla fine del XIX secolo alcune scoperte casuali misero in crisi il modello ondulatorio della radiazione tali esperimenti mostrarono un effetto nuovo relativo all interazione della luce con la materia: l effetto fotoelettrico EFFETTO FOTOELETTICO: emissione di elettroni da parte di una lamina metallica su cui incide un fascio di radiazione con frequenza sufficientemente elevata. In particolare di osserva che esiste una soglia di frequenza sotto la quale il metallo non emette elettroni: l intensità della radiazione incidente ( cioè il numero di fotoni incidenti) determina il numero di elettroni emessi ma non la loro energia: l energia degli elettroni emessi dipende solo dalla frequenza della radiazione incidente.
14 L esperimento di Lenard Nel 1900 Philipp Lenard dimostrò sperimentalmente che, quando la luce incide su una superficie metallica, l energia dei fotoelettroni non dipende dall intensità della luce assorbita dalla lastra L intensità della luce (incidente) assorbita determina un aumento o una diminuzione del numero degli elettroni emessi, ma non una variazione della loro energia cinetica L energia degli elettroni emessi dipende solo dalla frequenza della radiazione incidente
15 L effetto fotoelettrico Nell apparecchiatura di Lenard la luce incide sul catodo C che emette elettroni questi migrano verso l anodo A e vengono rilevati dall amperometro tramite un potenziometro si può variare la differenza di potenziale V per un certo valore V 0, il potenziale d arresto, il passaggio degli elettroni è del tutto assente
16 L effetto fotoelettrico I risultati sperimentali contraddicono la teoria classica dell elettromagnetismo Riassumiamo i risultati sperimentali dell effetto fotoelettrico aumentando l intensità della luce monocromatica su una superficie metallica aumenta proporzionalmente il numero dei fotoelettroni emessi ma non la loro energia cinetica si ha emissione di fotoelettroni solo per frequenze superiori alla frequenza di soglia, che dipende esclusivamente dal materiale utilizzato l emissione è pressoché istantanea al crescere della frequenza della luce, aumenta linearmente l energia cinetica massima dei fotoelettroni Questi risultati contraddicono la teoria classica ondulatoria dell elettromagnetismo
17 2 L effetto fotoelettrico
18 L effetto fotoelettrico b) energia cinetica degli elettroni emessi in funzione della frequenza. Se la radiazione incidente ha una frequenza minore di quella di soglia, l effetto fotoelettrico non avviene. L inclinazione della retta è indipendente dal metallo utilizzato.
19 L effetto fotoelettrico La spiegazione di Einstein Einstein dimostrò che tutti i risultati sperimentali potevano essere spiegati ipotizzando che l energia fosse assorbita dagli atomi del materiale in pacchetti di energia chiamati fotoni Energia dei fotoni L energia della luce è quantizzata e ciascun fotone possiede un energia pari a
20 L effetto fotoelettrico La spiegazione di Einstein Un elettrone può essere emesso solo quando l urto di un singolo fotone riesce a cedere una quantità di energia almeno sufficiente a strappare l elettrone dalla superficie del metallo Questo valore di energia è chiamato lavoro di estrazione L e prende il nome di potenziale di estrazione
21 La teoria di Einstein sull effetto fotoelettrico spiega tutti i risultati sperimentali una maggiore intensità di luce comporta l emissione di un numero maggiore di fotoelettroni se un quanto di luce ha una frequenza inferiore a quella di soglia f0 l effetto fotoelettrico non avviene l emissione è istantanea perché ogni singolo elettrone riceve energia da un singolo fotone come in un urto tra particelle l ultimo risultato sperimentale deriva dall equazione di Einstein dell effetto fotoelettrico E = hf = E c + Le L energia E della radiazione luminosa incidente in parte è usata per estrarre l elettrone dal metallo (L e ), mentre la parte residua si trasforma in energia cinetica (E c ) dei fotoelettroni.
22 Dall equazione di Einstein si ottiene il valore dell energia cinetica residua E c dei fotoelettroni vale: E c = hf hf 0 = hdf L energia cinetica dei fotoelettroni è direttamente proporzionale alla differenza tra la frequenza della luce incidente e la frequenza di soglia e alla costante di Plank L equazione di Einstein può essere vista come un applicazione del principio di conservazione dell energia: Il fotone che arriva ha un energia pari ad hf; una parte di questa energia è utilizzata per estrarre l elettrone dell atomo e la restante parte viene ceduta all elettrone sotto forma di energia cinetica che genera la corrente fotoelettrica. Fu grazie a questa spiegazione dell Effetto Fotoelettrico, e non per la teoria sulla relatività, che Einstein ottenne nel 1921 il Premio Nobel
23 Raggi X e diffusione Compton I raggi X Nel 1895 il fisico tedesco Wilhelm Roentgen scoprì i raggi X radiazione elettromagnetica di lunghezza d onda dell ordine di 0,1 nm detta anche radiazione di Bremsstrahlung radiazione di frenamento Nel 1912 gli scienziati Friedrich e Knipping inviarono un fascio sottile e collimato di raggi X attraverso un cristallo raccolsero su una lastra fotografica una caratteristica figura di diffrazione chiamata spettro di Laue Quali conseguenze si potevano trarre da questi risultati?
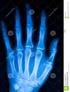
24 3 Raggi X e diffusione Compton Un immagine a raggi X di un serpente: la radiazione attraversa le parti molli, mettendo in luce la struttura scheletrica.
25 Raggi X e diffusione Compton Schema dell esperimento di Laue: I raggi X sono deviati dal cristallo e formano una caratteristica figura di diffrazione, raccolta e resa evidente dalla lastra fotografica.
26 Raggi X e diffusione Compton Dai risultati si dedusse che i raggi X sono onde elettromagnetiche ad alta frequenza i cristalli sono costituiti da strutture regolari (reticolo cristallino) che permettono la formazione della figura di diffrazione le onde diffuse sono in fase quando la loro differenza di cammino è un multiplo intero della lunghezza d onda» diffusione alla Bragg
27 La diffrazione dei raggi X a opera di un cristallo: Le due onde sono in fase quando la loro differenza di cammino δ = 2d senϑ è un multiplo intero della lunghezza d onda λ
28 La radiazione X è caratterizzata da uno spettro continuo da cui emergono due righe molto alte e sottili tipiche degli spettri discreti queste righe isolate dipendono dalle caratteristiche del materiale ciascuna di esse corrisponde all emissione di una radiazione con frequenza ben determinata e prevedibile attraverso formule empiriche Analizzando lo spettro dei raggi X notiamo che esiste una lunghezza d onda limite l min legata al potenziale V 0 del tubo che produce i raggi X tramite la relazione
29 Raggi X e diffusione Compton Lo spettro dei raggi X del molibdeno: sullo spettro continuo emergono due picchi a 0,06 nm e a circa 0,07 nm, che dipendono dalle caratteristiche del materiale; λ min ha un valore di circa 0,028 nm e corrisponde a un potenziale di V.
30 La diffusione Compton Agli inizi degli anni Venti, gli esperimenti di Compton dimostrarono che la luce poteva essere considerata una vera e propria particella, il fotone al fotone si potevano attribuire una quantità di moto e un energia, entrambe quantizzate Nella diffusione Compton un fotone ad alta energia urta un elettrone libero, dopodiché l elettrone viene diffuso con un angolo rispetto alla direzione del fotone incidente un secondo fotone viene diffuso con lunghezza d onda superiore a quella del fotone incidente Secondo la teoria quantistica questo avviene poiché parte dell energia del fotone incidente è ceduta all elettrone
31 Un fotone di lunghezza d onda λ 1 incide su un elettrone inizialmente fermo. Dopo l urto, l elettrone si muove con un angolo ϑ rispetto alla direzione del fotone incidente, mentre un secondo fotone è diffuso con lunghezza d onda λ 2 > λ 1, con un angolo α rispetto alla direzione del fotone incidente.
32 Quantità di moto del fotone La quantità di moto di un fotone è legata alla lunghezza d onda dalla relazione Variazione della lunghezza d onda nell effetto Compton Se a è l angolo di scattering di un fotone diffuso da un elettrone inizialmente fermo, allora la variazione della lunghezza d onda fra il fotone incidente e quello diffuso è uguale a Lunghezza d onda Compton
33 Dualismo onda-corpuscolo Il dualismo onda-corpuscolo esprime il concetto secondo il quale una radiazione elettromagnetica si può propagare come un onda, mostrando le tipiche figure d interferenza e di diffrazione, quando le dimensioni degli ostacoli sono confrontabili con la lunghezza dell onda, ma può scambiare con altri corpi dotati di massa la propria energia e la quantità di moto come un effettiva particella, benché priva di massa Dopo un lunghissimo tempo in cui l ipotesi ondulatoria della luce aveva preso il sopravvento, la natura corpuscolare della luce di Newton riprese vigore
34 Le origini del modello atomico L atomo indivisibile La parola atomo deriva dal greco àtomos, che significa indivisibile Quando gli atomi acquistarono evidenza scientifica ci si accorse che non erano affatto le particelle semplici e indivisibili che aveva supposto il filosofo greco Democrito
35 Le origini del modello atomico Gli spettri di emissione degli atomi Nel 1884, Johann Jakob Balmer scoprì che la lunghezza d onda delle prime righe dello spettro dell atomo di idrogeno poteva essere espressa tramite una formula empirica Serie di Balmer
36 Le righe dello spettro di emissione dell atomo di idrogeno per n = 3, 4, 5,...
37 Le origini del modello atomico Il modello di Thomson Nel modello atomico di Thomson gli elettroni erano sparsi all interno di una massa fluida dotata di carica positiva ciò rendeva l atomo elettricamente neutro Questo modello è chiamato familiarmente plum pudding ( budino di prugne ) Il modello di Thomson: gli elettroni caricati negativamente sono immersi in una massa fluida caricata positivamente, in modo da rendere l atomo elettricamente neutro.
38 L esperimento di Rutherford e il modello planetario Ernest Rutherford, allievo di Thomson, studiò a fondo la natura dell atomo facendo interagire particelle a (alfa) con lamine sottili di diverse sostanze I risultati del suo esperimento si spiegavano ipotizzando l esistenza di un piccolissimo nucleo centrale carico positivamente uno sciame elettronico che rimaneva nei pressi del nucleo ruotando per effetto dell attrazione coulombiana Il modello atomico che propose era dunque assimilabile a un modello planetario in cui gli elettroni ruotano intorno a un nucleo carico positivamente come i pianeti del sistema solare Le particelle α sono nuclei di elio di carica positiva pari al doppio della carica del protone, emessi da atomi di radio radioattivo: questo fenomeno era già noto con il nome di radioattività.
39 L esperimento di Rutherford: le particelle α emesse dalla sostanza radioattiva S α interagiscono con gli atomi della lamina L posta come bersaglio. Una piattaforma rotante permette di raccogliere le particelle diffuse a vari angoli.
40 Particelle α incidenti su un atomo secondo il modello di Rutherford: sono maggiormente deviate quelle che passano più vicine al nucleo positivo, giustificando così i diversi angoli di deflessione che si registrano sperimentalmente
41 In seguito, Geiger e Marsden scoprirono la relazione fra la quantità di carica positiva e la posizione nel Sistema Periodico degli elementi di Mendeleev Il numero di posizione di ciascun elemento fu chiamato numero atomico (Z)
42 Il modello di Bohr: la quantizzazione dell energia dell atomo Niels Bohr ipotizzò l esistenza nell atomo di livelli discreti di energia livelli quantizzati corrispondenti a stati stazionari dell intero atomo in questi stati il moto di rotazione degli elettroni non si modificava al passare del tempo Nel modello di Bohr la successione dei livelli energetici atomici inizia dallo stato fondamentale dell atomo gli altri livelli corrispondono agli stati eccitati dell atomo Passando da uno stato eccitato a quello fondamentale, gli elettroni cedono l energia in eccesso sotto forma di radiazione
43 Una particella classica carica che ruota perde energia sotto forma di radiazione, detta radiazione di sincrotrone: a ogni rotazione diminuisce il suo raggio, descrivendo così una traiettoria a spirale verso il centro.
44 Il modello di Bohr: la quantizzazione dell energia dell atomo I postulati di Bohr Primo postulato di Bohr Gli elettroni possono ruotare stabilmente e senza irradiare solo su determinate orbite chiamate stati stazionari. L irraggiamento dell atomo avviene quando uno o più elettroni passano da uno stato stazionario a un altro Secondo postulato di Bohr La frequenza f della radiazione emessa non coincide con la frequenza di rotazione dell elettrone in un orbita qualsiasi, bensì corrisponde a quella che si ottiene dalla relazione di Planck dove E f ed E i sono rispettivamente le energie relative allo stato finale e allo stato iniziale e h è la costante di Planck
45 Il modello di Bohr: la quantizzazione dell energia dell atomo In base al secondo postulato se un elettrone passa da uno stato energetico superiore a uno inferiore, l energia persa DE = hf è emessa sotto forma di un fotone di frequenza f l assorbimento, da parte dell atomo, di un fotone con energia hf pari alla differenza tra due stati stazionari causa la transizione dell elettrone da un livello energetico più basso a uno più elevato l energia nell atomo è quindi quantizzata
46 a) Transizione di un elettrone fra due stati energetici a energia iniziale E 2 e finale E 1, con E 2 > E 1. Il risultato è l emissione di un fotone a frequenza f; b) se l atomo assorbe un fotone a frequenza f, il quanto di energia hf causa l innalzamento del livello energetico dell elettrone da E 1 a E 2.
47 Il modello di Bohr: la quantizzazione dell energia dell atomo Energia totale dell elettrone su orbita di raggio r Per ricavare le regole di quantizzazione delle orbite elettroniche Bohr ipotizzò che il momento angolare dell elettrone L = mvr fosse quantizzato Ottenne quindi a 0 è il raggio della prima orbita di Bohr Raggi delle orbite stazionarie dell atomo di idrogeno
48 I livelli energetici dell atomo di idrogeno secondo Bohr. Solo alcune orbite, e quindi transizioni, sono permesse, e corrispondono a raggi uguali a r n = n 2 a 0. Tutto lo spazio compreso tra le orbite stabili quantizzate è proibito.
49 5 Il modello di Bohr: la quantizzazione dell energia dell atomo Il diagramma dei livelli energetici dell atomo di idrogeno Livelli energetici dell atomo di idrogeno Dove Definiamo energia di legame o di ionizzazione l energia necessaria per l estrazione di un elettrone dall atomo per l atomo di idrogeno nello stato fondamentale questo valore è E 1 = 13,6 ev
50 Le serie di righe spettrali note ai tempi della pubblicazione del modello di Bohr o negli anni immediatamente seguenti sono la serie di Lyman, n i = 2, 3, 4,... e n f = 1 la serie di Balmer n i = 3, 4, 5,... e n f = 2 la serie di Paschen n i = 4, 5, 6,... e n f = 3 la serie di Brackett n i = 5, 6, 7,... e n f = 4 la serie di Pfund n i = 6, 7, 8,... e n f = 5
51 I livelli energetici dell atomo di idrogeno secondo Bohr. I livelli energetici consentiti sono rappresentati da righe poste a distanza decrescente, rispetto alla prima che corrisponde al livello fondamentale (il disegno non è in scala). Sono indicate le transizioni che danno origine alle serie spettrali di Paschen, Balmer e Lyman.
52 L esperimento di Franck e Hertz Nel 1914 James Franck e Gustav L. Hertz eseguirono un esperimento cruciale che dimostrò che l energia degli atomi è quantizzata gli atomi assorbono energia solamente in corrispondenza di precisi valori discreti Il modello di Bohr ebbe così un importante conferma
53 Schema dell apparato sperimentale utilizzato da Franck e Hertz.
54 Schema dell esperimento gli elettroni emessi dal catodo vengono accelerati da una differenza di potenziale DV giunti su un rivelatore danno origine a una corrente nel loro cammino gli elettroni urtano gli atomi di mercurio e ciò ostacola il loro movimento aumentando la differenza di potenziale DV si nota un aumento della corrente ma anche delle cadute in corrispondenza di valori definiti di DV questi valori dipendono dalla natura del gas contenuto
55 L interpretazione dell esperimento Franck e Hertz interpretarono i risultati dell esperimento in termini di urti tra elettroni e atomi di mercurio finché la differenza di potenziale non supera il valore di 4,9 V gli urti sono sostanzialmente elastici gli elettroni non cedono energia agli atomi superato il valore di 4,9 V gli urti diventano anelastici gli elettroni cedono parte della loro energia agli atomi gli atomi emettono l energia assorbita sotto forma di radiazione gli elettroni non hanno più l energia cinetica sufficiente a raggiungere la piastra P e la corrente cade Aumentando la differenza di potenziale il processo continua per valori del potenziale che siano multipli interi di 4,9 V
56 Grafico dell intensità di corrente in funzione della differenza di potenziale.
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
La struttura della materia
 La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
La teoria del corpo nero
 La teoria del corpo nero Max Planck Primo Levi 2014 Roberto Bedogni INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
La teoria del corpo nero Max Planck Primo Levi 2014 Roberto Bedogni INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
Problemi con l'atomo. Significato delle righe spettrali. Modello dell'atomo
 Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
La radiazione elettromagnetica. aumento della frequenza n della radiazione aumento dell energia E della radiazione
 La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
P. Sapia Università della Calabria. a.a. 2009/10
 FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
Unità Didattica 3. L atomo di idrogeno
 Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Introduzione alla Meccanica Quantistica (MQ):
 Introduzione alla Meccanica Quantistica (MQ): 1 MECCANICA QUANTISTICA ELETTRONI MATERIA MOLECOLE ATOMI NUCLEI La nostra attuale comprensione della struttura atomica e molecolare si basa sui principi della
Introduzione alla Meccanica Quantistica (MQ): 1 MECCANICA QUANTISTICA ELETTRONI MATERIA MOLECOLE ATOMI NUCLEI La nostra attuale comprensione della struttura atomica e molecolare si basa sui principi della
Meccanica quantistica Mathesis 2016 Prof. S. Savarino
 Meccanica quantistica Mathesis 2016 Prof. S. Savarino Quanti Corpo nero: è un oggetto che assorbe tutta la radiazione senza rifletterla. Come una corda legata agli estremi può produrre onde stazionarie
Meccanica quantistica Mathesis 2016 Prof. S. Savarino Quanti Corpo nero: è un oggetto che assorbe tutta la radiazione senza rifletterla. Come una corda legata agli estremi può produrre onde stazionarie
1. La struttura atomica Le particelle subatomiche L atomo, per molti secoli ritenuto indivisibile, è formato da particelle più piccole.
 1. La struttura atomica Le particelle subatomiche L atomo, per molti secoli ritenuto indivisibile, è formato da particelle più piccole. Le particelle fondamentali che costituiscono l atomo sono: Il protone,
1. La struttura atomica Le particelle subatomiche L atomo, per molti secoli ritenuto indivisibile, è formato da particelle più piccole. Le particelle fondamentali che costituiscono l atomo sono: Il protone,
Estrazione di elettroni da un metallo illuminato. Prime osservazioni Hertz 1857 Esperimento di Lenard 1902 Spiegazione teorica di Einstein
 Estrazione di elettroni da un metallo illuminato Prime osservazioni Hertz 1857 Esperimento di Lenard 1902 Spiegazione teorica di Einstein - 1905 L elettrone di conduzione in un metallo è in una buca di
Estrazione di elettroni da un metallo illuminato Prime osservazioni Hertz 1857 Esperimento di Lenard 1902 Spiegazione teorica di Einstein - 1905 L elettrone di conduzione in un metallo è in una buca di
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9
 Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
La nascita della fisica moderna. (un racconto di inizio 900)
 La nascita della fisica moderna (un racconto di inizio 900) Sviluppo storico della fisica tra fine 800 e il 1927 Fisica sperimentale fine 800 Fisica teorica fine 800 1900 1905 1911 1913 1916 1924 1925-1927
La nascita della fisica moderna (un racconto di inizio 900) Sviluppo storico della fisica tra fine 800 e il 1927 Fisica sperimentale fine 800 Fisica teorica fine 800 1900 1905 1911 1913 1916 1924 1925-1927
Il corpo nero e l ipotesi di Planck
 Il corpo nero e l ipotesi di Planck La crisi della fisica classica Alla fine del XIX secolo ci sono ancora del fenomeni che la fisica classica non riesce a spiegare: lo spettro d irraggiamento del corpo
Il corpo nero e l ipotesi di Planck La crisi della fisica classica Alla fine del XIX secolo ci sono ancora del fenomeni che la fisica classica non riesce a spiegare: lo spettro d irraggiamento del corpo
FISICA QUANTISTICA LIMITI AL MODELLO ATOMICO DI RUTHERFORD. e - Per spiegare la disposizione degli elettroni nell atomo (STRUTTURA ELETTRONICA)
 LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI
 MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA
 LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
Unità 2. La teoria quantistica
 Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
I QUANTI DI PLANCK 1
 I QUANTI DI PLANCK 1 prerequisiti Concetto di onda v= f Energia f 2 Per le onde elettromagnetiche v= c Spettro di emissione 2 SPETTRO ELETTROMAGNETICO 3 Quando un flusso di energia raggiante cade sulla
I QUANTI DI PLANCK 1 prerequisiti Concetto di onda v= f Energia f 2 Per le onde elettromagnetiche v= c Spettro di emissione 2 SPETTRO ELETTROMAGNETICO 3 Quando un flusso di energia raggiante cade sulla
trico otoeletf to etf Ef Pina di Vito 1
 Pina di Vito 1 L elettrone di conduzione in un metallo è in una buca di potenziale metallo E i E cin U U e W U energia di legame degli elettroni nel reticolo metallico E cin energia cinetica dell elettrone
Pina di Vito 1 L elettrone di conduzione in un metallo è in una buca di potenziale metallo E i E cin U U e W U energia di legame degli elettroni nel reticolo metallico E cin energia cinetica dell elettrone
La fisica del XX secolo ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione
 ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
La Crisi della Fisica Classica
 La Crisi della Fisica Classica F. Borgonovi (Dipartimento di Matematica e Fisica) Interdisciplinary Laboratories for Advanced Materials Physics (i-lamp) Department of Mathematics and Physics, Catholic
La Crisi della Fisica Classica F. Borgonovi (Dipartimento di Matematica e Fisica) Interdisciplinary Laboratories for Advanced Materials Physics (i-lamp) Department of Mathematics and Physics, Catholic
Fisica delle Apparecchiature per Radioterapia, lez. III RADIOTERAPIA M. Ruspa 1
 RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Fisica atomica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
L'esperimento di Franck-Hertz
 L'esperimento di Franck-Hertz STAGES ESTIVI (11 15 Giugno 2012) LNF MATTEO MASCOLO Università di Roma Tor Vergata (Breve) riepilogo delle puntate precedenti... 1884 - Johann Balmer studia le righe di assorbimento
L'esperimento di Franck-Hertz STAGES ESTIVI (11 15 Giugno 2012) LNF MATTEO MASCOLO Università di Roma Tor Vergata (Breve) riepilogo delle puntate precedenti... 1884 - Johann Balmer studia le righe di assorbimento
La Struttura degli Atomi
 La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Radiazione e Materia. Insegnamento di Chimica Generale CCS CHI e MAT. Scuola di Ingegneria Industriale e dell Informazione
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
FAM. T 1) α ν. (e α ν T 1) 2. (con l ipotesi ν > 0) si ottiene
 Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
Fisica quantistica. Liceo Malpighi, a.s. 2016/17
 Fisica quantistica Liceo Malpighi, a.s. 2016/17 DALLA FISICA CLASSICA ALLA FISICA MODERNA (lungo periodo di transizione a cavallo fra 800 e 900) MECCANICA E ASTRONOMIA NEL XIX SEC. Previsione di Nettuno
Fisica quantistica Liceo Malpighi, a.s. 2016/17 DALLA FISICA CLASSICA ALLA FISICA MODERNA (lungo periodo di transizione a cavallo fra 800 e 900) MECCANICA E ASTRONOMIA NEL XIX SEC. Previsione di Nettuno
Il modello atomico fino all Ottocento
 Il modello atomico fino all Ottocento Fino a quasi tutto l Ottocento gli atomi vennero considerati, secondo il modello atomico di Dalton, come porzioni di materia indivisibili Il modello, di diretta derivazione
Il modello atomico fino all Ottocento Fino a quasi tutto l Ottocento gli atomi vennero considerati, secondo il modello atomico di Dalton, come porzioni di materia indivisibili Il modello, di diretta derivazione
Storia della meccanica quantistica
 Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
La Meccanica Quantistica
 La Meccanica Quantistica Se quando pensiamo a un atomo ci immaginiamo qualcosa di questo tipo Dobbiamo rivedere le nostre idee LA CRISI DELLA FISICA CLASSICA La crisi della fisica classica Un secolo fa
La Meccanica Quantistica Se quando pensiamo a un atomo ci immaginiamo qualcosa di questo tipo Dobbiamo rivedere le nostre idee LA CRISI DELLA FISICA CLASSICA La crisi della fisica classica Un secolo fa
Fisica Moderna per Matematica (Meccanica Quantistica Elementare) Udine, A.A. 2000/2001
 Fisica Moderna per Matematica (Meccanica Quantistica Elementare) Udine, A.A. 2000/2001 Introduzione alla meccanica quantistica e alla relatività ristretta Orario: Lunedì 11-12:30 oppure Giovedi 9-10:30
Fisica Moderna per Matematica (Meccanica Quantistica Elementare) Udine, A.A. 2000/2001 Introduzione alla meccanica quantistica e alla relatività ristretta Orario: Lunedì 11-12:30 oppure Giovedi 9-10:30
L Effetto Fotoelettrico. Daniela Rebuzzi
 L Effetto Fotoelettrico Daniela Rebuzzi Anno Accademico 2008/2009 introduzione Seconda meta del XIX secolo: meccanica classica : Newton e successivi sviluppi elettromagnetismo: sostanzialmente compreso
L Effetto Fotoelettrico Daniela Rebuzzi Anno Accademico 2008/2009 introduzione Seconda meta del XIX secolo: meccanica classica : Newton e successivi sviluppi elettromagnetismo: sostanzialmente compreso
Interazione radiazione materia Dott.ssa Alessandra Bernardini
 Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
LEZIONE N 28. Corso di Fisica II Prof. Giuseppe Ciancio
 LEZIONE N 28 1 Cenni storici atomo dal greco "atomòs" "indivisibile" Democrito In verità esistono solo atomi e il vuoto«. L uomo pensava che ogni cosa nel mondo fosse un composto dei quattro elementi:
LEZIONE N 28 1 Cenni storici atomo dal greco "atomòs" "indivisibile" Democrito In verità esistono solo atomi e il vuoto«. L uomo pensava che ogni cosa nel mondo fosse un composto dei quattro elementi:
La complessa semplicità dell'atomo di idrogeno!
 La complessa semplicità dell'atomo di idrogeno Bergamo, venerdì 1 Febbraio 2013 Stefano Covino INAF - Osservatorio Astronomico di Brera Un po di terminologia Atomo (dal greco, indivisibile): atomismo (Leucippo,
La complessa semplicità dell'atomo di idrogeno Bergamo, venerdì 1 Febbraio 2013 Stefano Covino INAF - Osservatorio Astronomico di Brera Un po di terminologia Atomo (dal greco, indivisibile): atomismo (Leucippo,
RADIAZIONI ELETTROMAGNETICHE E PRODUZIONE DI RAGGI X
 UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia RADIAZIONI ELETTROMAGNETICHE E PRODUZIONE DI RAGGI X A.A.
UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia RADIAZIONI ELETTROMAGNETICHE E PRODUZIONE DI RAGGI X A.A.
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Spettroscopia. Spettroscopia
 Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Schema di un tubo a raggi X
 Raggi X 1 Schema di un tubo a raggi X I raggi X sono prodotti quando una sostanza è bombardata da elettroni ad alta velocità. I componenti fondamentali di un tubo a raggi X sono: a) ampolla di vetro a
Raggi X 1 Schema di un tubo a raggi X I raggi X sono prodotti quando una sostanza è bombardata da elettroni ad alta velocità. I componenti fondamentali di un tubo a raggi X sono: a) ampolla di vetro a
Raccolta di esercizi di fisica moderna
 Raccolta di esercizi di fisica moderna M. Quaglia IIS Avogadro Torino M. Quaglia (IIS Avogadro Torino) Raccolta di esercizi di fisica moderna Torino, 20/11/2014 1 / 30 Prova AIF e Sillabo http://www.aif.it/archivioa/aif_seconda_prova_di_fisica.pdf
Raccolta di esercizi di fisica moderna M. Quaglia IIS Avogadro Torino M. Quaglia (IIS Avogadro Torino) Raccolta di esercizi di fisica moderna Torino, 20/11/2014 1 / 30 Prova AIF e Sillabo http://www.aif.it/archivioa/aif_seconda_prova_di_fisica.pdf
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Produzione dei raggi X
 I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
5) Modello atomico di BOHR
 5) Modello atomico di BOHR (pag.92 par.3 - parziale- ) PREMESSA: LIMITI DEL MODELLO DI RUTHERFORD Il modello planetario dell atomo sostenuto da Rutherford si adattava bene a molti dati sperimentali ma
5) Modello atomico di BOHR (pag.92 par.3 - parziale- ) PREMESSA: LIMITI DEL MODELLO DI RUTHERFORD Il modello planetario dell atomo sostenuto da Rutherford si adattava bene a molti dati sperimentali ma
Modelli atomici. Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle.
 Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
L atomo di Bohr. Argomenti. Al tempo di Bohr. Spettri atomici 19/03/2010
 Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA
 pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
Spettro elettromagnetico
 Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Università Primo Levi
 Università Primo Levi Primo Levi 2013 Le forze fondamentali e la fisica dei quanta INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
Università Primo Levi Primo Levi 2013 Le forze fondamentali e la fisica dei quanta INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
Dispositivi a raggi X
 Dispositivi a raggi X Università degli Studi di Cagliari Servizio di Fisica Sanitaria e Radioprotezione TUBO A RAGGI X v FILAMENTO BERSAGLIO DI TUNGSTENO CIRCUITO DEL FILAMENTO CATODO CUFFIA APERTURA TUBO
Dispositivi a raggi X Università degli Studi di Cagliari Servizio di Fisica Sanitaria e Radioprotezione TUBO A RAGGI X v FILAMENTO BERSAGLIO DI TUNGSTENO CIRCUITO DEL FILAMENTO CATODO CUFFIA APERTURA TUBO
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Lezione n. 13. Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo. di idrogeno. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
ESPERIMENTO DI YOUNG DOPPIA FENDITURA
 ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Apparati per uso industriale e ricerca Dott.ssa Alessandra Bernardini
 Apparati per uso industriale e ricerca Dott.ssa Alessandra Bernardini 1 Apparecchiature radiologiche per analisi industriali e ricerca Le apparecchiature a raggi X utilizzate nell industria utilizzano
Apparati per uso industriale e ricerca Dott.ssa Alessandra Bernardini 1 Apparecchiature radiologiche per analisi industriali e ricerca Le apparecchiature a raggi X utilizzate nell industria utilizzano
Chimica e laboratorio
 Chimica e laboratorio L atomo: configurazione elettronica Classi Terze Lic. Sc. Tecnologico Anno Scolastico 2007/2008 Prerequisiti Conoscere l evoluzione delle conoscenze sulla costituzione dell atomo,
Chimica e laboratorio L atomo: configurazione elettronica Classi Terze Lic. Sc. Tecnologico Anno Scolastico 2007/2008 Prerequisiti Conoscere l evoluzione delle conoscenze sulla costituzione dell atomo,
3. (Da Veterinaria 2006) Perché esiste il fenomeno della dispersione della luce bianca quando questa attraversa un prisma di vetro?
 QUESITI 1 FENOMENI ONDULATORI 1. (Da Medicina 2008) Perché un raggio di luce proveniente dal Sole e fatto passare attraverso un prisma ne emerge mostrando tutti i colori dell'arcobaleno? a) Perché riceve
QUESITI 1 FENOMENI ONDULATORI 1. (Da Medicina 2008) Perché un raggio di luce proveniente dal Sole e fatto passare attraverso un prisma ne emerge mostrando tutti i colori dell'arcobaleno? a) Perché riceve
LA PRODUZIONE DEI RAGGI X
 UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
L irraggiamento termico
 L irraggiamento termico Trasmissione del Calore - 42 Il calore può essere fornito anche mediante energia elettromagnetica; ciò accade perché quando un fotone, associato ad una lunghezza d onda compresa
L irraggiamento termico Trasmissione del Calore - 42 Il calore può essere fornito anche mediante energia elettromagnetica; ciò accade perché quando un fotone, associato ad una lunghezza d onda compresa
LE RADIAZIONI IONIZZANTI
 LE RADIAZIONI IONIZZANTI Generalità Le radiazioni ionizzanti sono, per definizione, onde elettromagnetiche e particelle capaci di causare, direttamente o indirettamente, la ionizzazione degli atomi e delle
LE RADIAZIONI IONIZZANTI Generalità Le radiazioni ionizzanti sono, per definizione, onde elettromagnetiche e particelle capaci di causare, direttamente o indirettamente, la ionizzazione degli atomi e delle
LA CRISI DELLA FISICA CLASSICA
 LA CRISI DELLA FISICA CLASSICA I a Parte: - Comportamento corpuscolare della luce II a Parte: - Il modello atomico - Comportamento ondulatorio della materia III a Parte: - Dualità onda-particella: esperimento
LA CRISI DELLA FISICA CLASSICA I a Parte: - Comportamento corpuscolare della luce II a Parte: - Il modello atomico - Comportamento ondulatorio della materia III a Parte: - Dualità onda-particella: esperimento
Lo Spettro Elettromagnetico
 Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Atomo: modello microscopico
 Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
- + MODELLI ATOMICI + + Particelle subatomiche
 MODELLI ATOMICI Particelle subatomiche L atomo è costituito da due zone: il NUCLEO, formato al suo interno da due tipi di particelle subatomiche, ovvero particelle ancora più piccole dell atomo (i protoni
MODELLI ATOMICI Particelle subatomiche L atomo è costituito da due zone: il NUCLEO, formato al suo interno da due tipi di particelle subatomiche, ovvero particelle ancora più piccole dell atomo (i protoni
Problema n. 1: L effetto Mössbauer
 Problema n. 1: L effetto Mössbauer Hai sentito parlare dell effetto Mössbauer e incuriosito hai trovato su un sito la seguente descrizione del fenomeno: Un nucleo con Z protoni e N neutroni che si trova
Problema n. 1: L effetto Mössbauer Hai sentito parlare dell effetto Mössbauer e incuriosito hai trovato su un sito la seguente descrizione del fenomeno: Un nucleo con Z protoni e N neutroni che si trova
May 5, 2013. Fisica Quantistica. Monica Sambo. Sommario
 May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
Il metodo scientifico
 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].
![Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].](/thumbs/62/47096832.jpg) Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
FISICA MODERNA per allievi di Matematica, Fisica Computazionale e Informatica (De Angelis)
 Università di Udine Facoltà di Scienze Matematiche, Fisiche e Naturali FISICA MODERNA per allievi di Matematica, Fisica Computazionale e Informatica (De Angelis) Appunti per il corso dell A.A. 2002/2003
Università di Udine Facoltà di Scienze Matematiche, Fisiche e Naturali FISICA MODERNA per allievi di Matematica, Fisica Computazionale e Informatica (De Angelis) Appunti per il corso dell A.A. 2002/2003
fenomeno livelli interni atomici legami chimici vibrazioni nm Å
 Spettroscopia Misura e studio dell andamento dell intensità della radiazione elettromagnetica/corpuscolare in funzione della frequenza (energia/lunghezza d onda) della radiazione stessa Quale tipo di informazione
Spettroscopia Misura e studio dell andamento dell intensità della radiazione elettromagnetica/corpuscolare in funzione della frequenza (energia/lunghezza d onda) della radiazione stessa Quale tipo di informazione
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Trasmissione di calore per radiazione
 Trasmissione di calore per radiazione Sia la conduzione che la convezione, per poter avvenire, presuppongono l esistenza di un mezzo materiale. Esiste una terza modalità di trasmissione del calore: la
Trasmissione di calore per radiazione Sia la conduzione che la convezione, per poter avvenire, presuppongono l esistenza di un mezzo materiale. Esiste una terza modalità di trasmissione del calore: la
Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici
 Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici Il presente documento individua le conoscenze, abilità e competenze che lo studente dovrà aver acquisito al termine
Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici Il presente documento individua le conoscenze, abilità e competenze che lo studente dovrà aver acquisito al termine
Incontriamo la Fisica: la Meccanica Quantistica. Stefano Spagocci, GACB
 Incontriamo la Fisica: la Meccanica Quantistica Stefano Spagocci, GACB Newton e Laplace Secondo la concezione di Newton e Laplace, specificate le condizioni iniziali (posizioni e velocità), il moto di
Incontriamo la Fisica: la Meccanica Quantistica Stefano Spagocci, GACB Newton e Laplace Secondo la concezione di Newton e Laplace, specificate le condizioni iniziali (posizioni e velocità), il moto di
Quantum Theory. E la natura dell'atomo. M. Orlandelli, A. Peloni
 Quantum Theory E la natura dell'atomo M. Orlandelli, A. Peloni Quantum Mechanics: prime idee (inizio 1900) A. Einstein: Effetto fotoelettrico C. Maxwell Equazioni delle onde elettromagnetiche M. Planck:
Quantum Theory E la natura dell'atomo M. Orlandelli, A. Peloni Quantum Mechanics: prime idee (inizio 1900) A. Einstein: Effetto fotoelettrico C. Maxwell Equazioni delle onde elettromagnetiche M. Planck:
E noto che la luce, o radiazione elettromagnetica, si propaga sottoforma di onde. Un onda è caratterizzata da due parametri legati fra loro: la
 1 E noto che la luce, o radiazione elettromagnetica, si propaga sottoforma di onde. Un onda è caratterizzata da due parametri legati fra loro: la lunghezza d onda ( ), definita come la distanza fra due
1 E noto che la luce, o radiazione elettromagnetica, si propaga sottoforma di onde. Un onda è caratterizzata da due parametri legati fra loro: la lunghezza d onda ( ), definita come la distanza fra due
Elettronica dello Stato Solido Lezione 3: La radiazione di corpo nero. Daniele Ielmini DEI Politecnico di Milano
 Elettronica dello Stato Solido Lezione 3: La radiazione di corpo nero Daniele Ielmini DEI Politecnico di Milano ielmini@elet.polimi.it D. Ielmini Elettronica dello Stato Solido 03 Outline Crisi della fisica
Elettronica dello Stato Solido Lezione 3: La radiazione di corpo nero Daniele Ielmini DEI Politecnico di Milano ielmini@elet.polimi.it D. Ielmini Elettronica dello Stato Solido 03 Outline Crisi della fisica
La Natura della Luce: dalle Scoperte alle Applicazioni
 La Natura della Luce: dalle Scoperte alle Applicazioni Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 27 Maggio 2013 Sommario L ottica geometrica
La Natura della Luce: dalle Scoperte alle Applicazioni Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 27 Maggio 2013 Sommario L ottica geometrica
Dalla meccanica classica alla meccanica quantistica
 Dalla meccanica classica alla meccanica quantistica A metà del XIX secolo, con il consolidamento delle teorie sulla meccanica e con la teoria di Maxwell (1864) sull unificazione della teoria dei campi
Dalla meccanica classica alla meccanica quantistica A metà del XIX secolo, con il consolidamento delle teorie sulla meccanica e con la teoria di Maxwell (1864) sull unificazione della teoria dei campi
PROGETTO AMICI DI SCIASCIA. Fisica delle particelle
 PROGETTO AMICI DI SCIASCIA Fisica delle particelle TEMI TRATTATI NELLA PRESENTAZIONE 1. STORIA DELLA FISICA DELLE PARTICELLE 2. COME E FATTO L ATOMO? IPOTESI SULLA STRUTTURA DELL ATOMO 3. LA FISICA DELLE
PROGETTO AMICI DI SCIASCIA Fisica delle particelle TEMI TRATTATI NELLA PRESENTAZIONE 1. STORIA DELLA FISICA DELLE PARTICELLE 2. COME E FATTO L ATOMO? IPOTESI SULLA STRUTTURA DELL ATOMO 3. LA FISICA DELLE
I QUANTI E LA VITA. laboratorio di chimica
 I QUANTI E LA VITA laboratorio di chimica Tutto ciò che ci circonda è costituito dalla combinazione di soli 90 elementi! LA NATURA DEL PROBLEMA DI COSA SONO FATTI GLI ELEMENTI? CERTI DELL ATOMO?! 1789
I QUANTI E LA VITA laboratorio di chimica Tutto ciò che ci circonda è costituito dalla combinazione di soli 90 elementi! LA NATURA DEL PROBLEMA DI COSA SONO FATTI GLI ELEMENTI? CERTI DELL ATOMO?! 1789
Produzione di un fascio di raggi x
 Produzione di un fascio di raggi x WWW.SLIDETUBE.IT Un fascio di elettroni penetra nella materia, dando origine a: produzione di elettroni secondari (raggi delta) emissione X caratteristica bremsstrahlung
Produzione di un fascio di raggi x WWW.SLIDETUBE.IT Un fascio di elettroni penetra nella materia, dando origine a: produzione di elettroni secondari (raggi delta) emissione X caratteristica bremsstrahlung
Atomi a più elettroni
 Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
