Metodi spettroscopici per le Biotecnologie
|
|
|
- Caterina Filippi
- 6 anni fa
- Visualizzazioni
Transcript
1 AA Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS Dott. Alfonso Zoleo
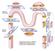
2 Spe$roscopia di Emissione Cosa succede ad una molecola portata in uno stato ele$ronico eccitato? Esistono diversi percorsi di diseccitazione: S 2 ISC A F Ph T 1 Processi radia8vi di emissione spontanea: Fluorescenza e Fosforescenza (emissione dell energia come fotone e ricaduta allo stato fondamentale) Processi non radia8vi di diseccitazione termica: trasferimento di energia ad altri gradi di libertà (vibrazioni, rotazioni, traslazioni) e/o ad altre molecole per collisione (solvente, quencher).
3 Spe$roscopia di Emissione Il «quenching» è il processo di trasferimento dell energia di eccitazione del cromoforo ad un altra molecola, il quencher, con cui il cromoforo collide : M* + Q M + Q* I processi cui è sogge$a la molecola in stato ele$ronico eccitato possono essere: - Fotofisici: cambia lo stato quan8co della molecola, cioè può cambiare la sua energia o il suo momento angolare, ma la molecola non cambia - Fotochimici: cambia la natura chimica della molecola Ad es.: M* M + hv Fotofisico: cambia solo l energia della molecola M* M a + M b Fotochimico: la molecola M si scinde per formare due specie M a e M b più piccole I processi di interesse spe$roscopico sono quelli fotofisici
4 Spe$roscopia di Emissione: Fluorescenza, Fosforescenza Consideriamo due soli sta8 ele$ronici: (stato fondamentale) ed (primo stato eccitato) Assorbimento: Emissione spontanea: coefficiente di assorbimento di Einstein coefficiente di emissione spontanea di Einstein Momento di dipolo di transizione tra gli sta8 ele$ronici I coefficien) di Einstein danno la probabilità per unità di tempo di una transizione, ovvero sono le costan) cine)che delle equazioni cine)che che regolano l assorbimento e l emissione spontanea
5 Equazione cine8ca dell assorbimento ne$o: 3 7 Esempio: In un secondo, due molecole passano da a per assorbimento di due fotoni. Nello stesso tempo, una molecola passa da a per emissione indo$a Bilancio ne,o: una molecola passa da a 4 6
6 Equazione cine8ca dell emissione spontanea: Emissione spontanea: il numero di molecole che nell unità di tempo passano da a per emissione spontanea di radiazione è proporzionale a N 1 (numero di molecole nello stato ). Il coefficiente di emissione spontanea è proporzionale al coefficiente di assorbimento indo$o: quindi, tanto più probabile è l assorbimento, tanto più probabile è l emissione spontanea. Inoltre, l emissione spontanea dipende fortemente dalla frequenza della radiazione emessa. Il processo è rilevante solo per frequenze del visibile o frequenze maggiori L emissione da uno stato di singole$o eccitato allo stato di singole$o fondamentale è de$a Fluorescenza
7 Regola di selezione sullo spin Due sta8 ele$ronici eccita8 possibili: di singole$o ( ) o di triple$o (T 1 ) π* n π π* π* n n π π S=0 S=0 S=1 T 1 Come nell assorbimento di radiazione, anche nell emissione spontanea la variazione di S deve essere zero: ΔS=0 Permessa T 1 «Proibita» Lo stato T 1 è ad energia più bassa di, perché nello stato di triple$o gli ele$roni stanno più lontani, quindi si respingono meno T 1
8 Fosforescenza Se un qualche processo popola lo stato T 1 a par8re da, le molecole nello stato T 1 possono eme$ere spontaneamente per tornare nello stato. Il processo è spin- proibito, quindi avviene lentamente per effe$o di deboli perturbazioni. L emissione spontanea dallo stato di triple$o T 1 è de$a fosforescenza T 1 fluorescenza fosforescenza
9 Des8no degli sta8 eccita8 Consideriamo adesso il processo di emissione includendo anche gli sta8 vibrazionali e le curve di energia potenziale 1) Il modo più semplice per portare le molecole nello stato è quello di fare assorbire radiazione alla lunghezza d onda di assorbimento. 2) Dopo l assorbimento, le molecole si trovano in vari livelli vibrazionali dello stato ele$ronico eccitato Assorbimento v =2 v =1 v =0
10 Des8no degli sta8 eccita8 3) Il processo successivo è il Rilassamento Vibrazionale (VR): è un processo molto veloce (10-12 s), nel quale le molecole che si trovano nei livelli vibrazionali eccita8 del singole$o ricadono al livello vibrazionale fondamentale (v =0) di. Non è un processo radia)vo: l energia è rilasciata come energia termica ad altri gradi di libertà o al solvente. Rilassamento vibrazionale
11 Fluorescenza 4) A questo punto possono avvenire vari fenomeni Fluorescenza: Emissione spontanea da v =0 di a vari livelli vibrazionali eccita8 di. Quindi ho un insieme di transizioni a varie energie, che determinano uno spe$ro con stru$ura vibrazionale nello spe$ro di fluorescenza
12 Fluorescenza Tu$e le transizioni in fluorescenza originano in v =0 di. Tu$avia, come nell assorbimento, esse terminano a vari livelli v dello stato, con una probabilità proporzionale aal quadrato del fa$ore di Franck- Condon (P=kS 2 ) con S: S = ψ dr ψ v ' = 0 Stavolta considero la funzione d onda vibrazionale fondamentale dello stato ele$ronico eccitato ( ) e le funzioni d onda vibrazionali eccitate dello stato ele$ronico fondamentale ( ) v
13 Fluorescenza E Spe$ro di Fluorescenza Come conseguenza, la stru$ura vibrazionale dello spe$ro di fluorescenza presenta la banda vibronica 0-0 ad energia più alta e le altre ad energia via via più bassa. La differenza tra due bande vibroniche successive mi dà la frequenza del modo di vibrazione dello stato eleironico fondamentale
14 Assorbimento- Fluorescenza Confrontiamo lo spettro di assorbimento e quello di fluorescenza di uno stesso cromoforo 1) Lo spettro di fluorescenza cade sempre a lunghezze d onda maggiori 2) La parte di spettro sovrapposta a quello di assorbimento è relativa alla transizione 0-0 3) Se lo spettro di assorbimento è dovuto unicamente alla -, è abbastanza simmetrico rispetto a quello di fluorescenza
15 Assorbimento- Fluorescenza Confrontiamo lo spettro di assorbimento e quello di fluorescenza di uno stesso cromoforo 4) Qualunque lunghezza d onda io scelga nello spettro di assorbimento per eccitare le molecole in, ottengo sempre lo stesso spettro di fluorescenza, perché VR porta sempre tutte le molecole in v =0 di! La fluorescenza parte sempre da v =0 di A 0-2 Mando fotoni alla lunghezza d onda per indurre la transizione vibronica 0-2 F VR
16 Assorbimen8 - S n Naturalmente, posso avere transizioni elettroniche in assorbimento anche verso stati elettronici eccitati ad energia maggiore di (purché usi fotoni di sufficiente energia). Anche in questo caso, in accordo con Franck-Condon, avrò una distribuzione di molecole nei vari stati vibrazionali eccitati di S 2 S 2 π* n π S 2 π* n π π* n π π* n π π* n π π* n π
17 Des8no degli sta8 S n Anche negli stati elettronici S n si ha rilassamento vibrazionale rapido allo stato vibrazionale fondamentale dello stato S n. Tuttavia, tutti gli stati elettronici S n hanno sempre il livello vibrazionale fondamentale che si sovrappone a livelli vibrazionali eccitati di S n-1. Nella figura, vediamo che il livello vibrazionale v=0 di S 2 si sovrappone ai livelli vibrazionali eccitati di S 2 S 2 S 2 VR CI Questa situazione rende molto probabile la conversione S 2, nella quale le molecole nello stato vibrazionale fondamentale dello stato elettronico S 2 passano a molecole vibrazionalmente eccitate dello stato elettronico (Conversione Interna, CI). Il processo CI avviene quasi senza variazione di energia, è solo una variazione di stato. Dallo stato vibrazionalmente eccitato di si ha poi rapido VR allo stato vibrazionale fondamentale di
18 Conversione interna La probabilità di conversione interna dipende, nuovamente, dalla sovrapposizione tra la funzione d onda vibrazionale fondamentale di S n e le funzioni vibrazionali eccitate di S n-1 S 2 S 2 CI molto probabile CI meno probabile Fra stati elettronici eccitati S n e S n-1, la conversione interna è sempre il processo favorito rispetto alla fluorescenza, poiché c è efficace sovrapposizione tra i loro livelli vibrazionali. Quindi la fluorescenza non può avere luogo da S n a (n>1), ma solo da a (REGOLA DI KASHA)
19 Conversione interna CI possibile CI impossibile, solo fluorescenza E possibile che anche lo stato abbia livelli vibrazionali sovrapposti con lo stato. In questo caso, è possibile la conversione interna. Se invece è separato da in modo da non avere livelli vibrazionali sovrapposti (cosa possibile solo fra e ), allora la fluorescenza è l unico processo possibile, in assenza di altri processi di diseccitazione diversi dalla conversione interna.
20 Assorbimento- emissione per spe$ri con transizioni - S n La forma dello spettro di fluorescenza è indipendente dalla λ ECC. Posso usare anche un assorbimento (eccitazione) da a S 2, la regola di Kasha dice che comunque la fluorescenza avverrà solo da Abs./ Em.!S 2! S 2 hν λ La fluorescenza, quindi, mi consente di identificare la transizione elettronica fondamentale ( - )!! S o
21 Esempio: la clorofilla a Spettro di fluorescenza: origina solo da Bande vibroniche 1 Spettro di assorbimento: varie transizioni elettroniche: quali bande sono vibroniche e quali transizioni elettroniche diverse? A Per confronto con la fluorescenza, ne deduco che: A è una transizione elettronica, e non una banda vibronica di 1. Ovviamente Bx e By sono a lunghezze d onda troppo corte per essere bande vibroniche di A o 1 Per vedere se una banda è vibronica, posso anche convertire le lunghezze d onda delle varie bande in numeri d onda: se due bande vicine distano non più di cm -1 appartengono probabilmente alla stessa struttura vibrazionale. Se sono >=10000 cm -1 appartengono a differenti bande elettroniche
22 Esempio: perilene e solfato di chinino Nel perilene in benzene, la simmetria tra fluorescenza e assorbimento suggerisce che tutte le bande che osservo nello spettro di assorbimento sono bande vibroniche della stessa transizione elettronica - Nel solfato di chinino in acqua acidulata, le differenze tra assorbimento e fluorescenza suggeriscono che la banda che osservo a lunghezze d onda minori è una transizione elettronica -S 2 e non una banda vibronica di -.
23 Conversione intersistema (ISC) π* n π π* n π T 1 S=0 S=1 T 1 Nello schema OM, uno stato elettronico eccitato presenta due elettroni su orbitali diversi: questi possono avere gli spin opposti (singoletto) o paralleli (tripletto) In generale, quindi, uno stato elettronico eccitato di singoletto ha sempre una controparte di tripletto. Usualmente, nello stato di tripletto gli elettroni sono più distanti (regola di Hund), il che causa una minore repulsione elettronica, e lo stato di tripletto è ad energia minore
24 Conversione intersistema (ISC) Subito dopo l assorbimento, le molecole si trovano nei livelli vibrazionali eccitati di. Se le curve di energia di T 1 e si incrociano, esisteranno dei livelli vibrazionali di T 1 accessibili da. La conversione da a T 1, però, comporta un cambiamento dello stato di spin da S=0 a S=1, cosa che è formalmente proibita. Tuttavia, l interazione tra il momento angolare di spin e il momento angolare orbitalico, chiamata interazione spin-orbita, è una perturbazione in grado di rendere debolmente permessa questa conversione singoletto-tripletto. T 1 T 1 Oltre all interazione spin-orbita, la probabilità di transizione dipende dalla sovrapposizione delle funzioni d onda vibrazionali di e T 1
25 Conversione intersistema (ISC) Quindi, la conversione intersistema (Inter System Crossing, ISC) è tanto più probabile quanto più: 1) È forte l interazione spin-orbita: questa cresce con la quarta potenza del numero atomico, per cui atomi più pesanti rendono la perturbazione più forte e il mutamento singoletto-tripletto probabile. 2) E lento il processo VR in : il processo VR è in competizione con l ISC; se è troppo veloce non ci sono abbastanza molecole che «saltino» in T 1 3) E elevata la sovrapposizione fra le funzioni d onda vibrazionali nel punto di incrocio T 1 - : come al solito, questo è legato al fattore di Franck-Condon. Maggiore è l overlap, maggiore è la probabilità di conversione
26 Fosforescenza Seguiamo adesso il destino delle molecole che hanno fatto ISC allo stato T 1 : VR T 1 T 1 Dopo rilassamento vibrazionale allo stato v =0 di T 1, le molecole possono cadere allo stato fondamentale per emissione. Si parla di fosforescenza. Il processo è formalmente proibito, perché comporta cambiamento dello spin, ma la stessa interazione spin-orbita che ha permesso il processo ISC rende possibile questa transizione radiativa. Di nuovo, da v =0 si cade in vari livelli vibrazionali eccitati di. Quindi lo spettro di fosforescenza presenta una struttura vibronica come lo spettro di fluorescenza.
27 Fosforescenza Benché l interazione spin-orbita renda possibile la fosforescenza, il processo è comunque poco probabile. Quindi, l emissione avviene in tempi molto più lunghi della fluorescenza. Tipicamente, intorno ai millisecondi (nella fluorescenza, nanosecondi). Comunque, alcune sostanze fosforescenti hanno tempi di emissione radiativa di ore! Luce emessa dal fosforo bianco in aria, dopo essere stato esposto alla luce I pigmenti fosforescenti che sono utilizzati nelle statuine e altri oggetti fosforescenti sono sali di metalli con elevato Z, per favorire l ISC. Il pigmento più comunemente usato è l alluminato di stronzio, che dà un emissione verde. La purezza di questi pigmenti è importante, perché le impurezze possono favorire processi competitivi di diseccitazione, con perdita di intensità di fosforescenza
28 Fosforescenza Interazione spin-orbita Momento angolare di spin Momento angolare orbitalico ξ Costante di accoppiamento spin-orbita: dipende da Z4 Esempio dell effetto «atomo pesante» Lo spettro del bromonaftonorbornene ha uno spettro di fosforescenza molto più intenso del naftonorbornene
29 DIAGRAMMA DI JABLONSKI Assorbimento Fluorescenza IC A F R ISC ISC Conversione interna Conversione intersistema ISC F T 1 In generale, i diversi percorsi di diseccitazione dallo stato S1 o superiore sono sempre presenti per tutte le molecole: ciò che cambia è la velocità (probabilità) di un processo rispetto ad un altro, in dipendenza dal tipo di molecola, dal solvente, dalla presenza di quencher, dalla temperatura Fosforescenza Rilassamento vibrazionale
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Maurizio D Auria. Fotochimica applicata alla sintesi organica
 A03 09 Maurizio D Auria Fotochimica applicata alla sintesi organica Copyright MMIV ARACNE editrice S.r.l. www.aracne editrice.it info@aracne editrice.it via Raffaele Garofalo, 133 A/B 00173 Roma redazione:
A03 09 Maurizio D Auria Fotochimica applicata alla sintesi organica Copyright MMIV ARACNE editrice S.r.l. www.aracne editrice.it info@aracne editrice.it via Raffaele Garofalo, 133 A/B 00173 Roma redazione:
Metodi spettroscopici
 Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Dipartimento di Scienze Chimiche. Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento
 Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento Emissione di Fluorescenza Intersystem Crossing e Fosforescenza Internal Conversion. 1 Diagramma
Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento Emissione di Fluorescenza Intersystem Crossing e Fosforescenza Internal Conversion. 1 Diagramma
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
Atomi a più elettroni
 Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Esercizio 1. Esercizio 2. Esercizio 5. Esercizio 3
 Esercizio Una ampolla contiene atomi di Be, eccitati in parte nello stato 3 3 S, in parte nello stato 3 S. ) Quali e quante transizioni si osservano nella diseccitazione allo stato fondamentale (2s) 2
Esercizio Una ampolla contiene atomi di Be, eccitati in parte nello stato 3 3 S, in parte nello stato 3 S. ) Quali e quante transizioni si osservano nella diseccitazione allo stato fondamentale (2s) 2
Metodi spettroscopici per le Biotecnologie
 AA 203-204 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS (2) Dott. Alfonso Zoleo I percorsi possibili dallo stato eccitato In ragione della maggiore o minore probabilità
AA 203-204 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS (2) Dott. Alfonso Zoleo I percorsi possibili dallo stato eccitato In ragione della maggiore o minore probabilità
LA FLUORESCENZA DELLA CLOROFILLA
 SPERIMENTA ANCHE TU ed. 2010 LICEO SCIENTIFICO L. DA VINCI TREVISO LA FLUORESCENZA DELLA CLOROFILLA Docente coordinatore: Sonia Mazzaro Assistente tecnico: Ornella Lorenzon Alunni classe 4C: Alessandro
SPERIMENTA ANCHE TU ed. 2010 LICEO SCIENTIFICO L. DA VINCI TREVISO LA FLUORESCENZA DELLA CLOROFILLA Docente coordinatore: Sonia Mazzaro Assistente tecnico: Ornella Lorenzon Alunni classe 4C: Alessandro
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
Interazione luce- atomo
 Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
ψ = Il carbonio (Z=6) - 2 elettroni equivalenti nello stato 2p - la funzione d onda globale deve essere antisimmetrica tripletto di spin, S=1
 s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
Principi di Spettroscopia in Chimica Inorganica
 1 Principi di Spettroscopia in Chimica Inorganica La spettroscopia misura la risposta di un sistema quantistico a perturbazioni esterne quali campi elettrici e magnetici. Si ottengono informazioni sulla
1 Principi di Spettroscopia in Chimica Inorganica La spettroscopia misura la risposta di un sistema quantistico a perturbazioni esterne quali campi elettrici e magnetici. Si ottengono informazioni sulla
Capitolo 10: Spettroscopia. Spettroscopia: interazione tra molecole e radiazione elettromagnetica
 Capitolo 10: Spettroscopia Spettroscopia: interazione tra molecole e radiazione elettromagnetica H O H 1 Dalla descrizione secondo Maxwell (1864) dei fenomeni elettromagnetici: radiazione elettromagnetica
Capitolo 10: Spettroscopia Spettroscopia: interazione tra molecole e radiazione elettromagnetica H O H 1 Dalla descrizione secondo Maxwell (1864) dei fenomeni elettromagnetici: radiazione elettromagnetica
Lezione n. 20. Visibile. La spettroscopia UV/Visibile. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
Corso di Laboratorio di Biofotonica
 SAPIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica Prof. Francesco Michelotti SAPIENZA Università di Roma Facoltà di Ingegneria
SAPIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica Prof. Francesco Michelotti SAPIENZA Università di Roma Facoltà di Ingegneria
Processi radiativi. Assorbimento Emissione spontanea Emissione stimolata. Gli stati eccitati sono instabili (il sistema non è in equilibrio)
 Processi radiativi conservazion e dell energia transizioni I I Assorbimento Emissione spontanea Emissione stimolata Lo stato ad energia più bassa è detto fondamentale, gli altri sono detti stati eccitati
Processi radiativi conservazion e dell energia transizioni I I Assorbimento Emissione spontanea Emissione stimolata Lo stato ad energia più bassa è detto fondamentale, gli altri sono detti stati eccitati
Capitolo 4 Le spettroscopie. 1. Lo spettro elettromagnetico
 Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Curve di taratura. Mostra la risposta di un metodo anali0co a quan0tà note di analita.
 Curve di taratura Mostra la risposta di un metodo anali0co a quan0tà note di analita. La re6a ideale ha un andamento lineare, e copre l intero intervallo di concentrazione nel quale prevediamo ricadano
Curve di taratura Mostra la risposta di un metodo anali0co a quan0tà note di analita. La re6a ideale ha un andamento lineare, e copre l intero intervallo di concentrazione nel quale prevediamo ricadano
Spettro elettromagnetico
 Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Energia degli orbitali
 Energia degli orbitali Il valore dell energia di un orbitale è, in modulo, il valore dell energia necessaria a portare l ele8rone a distanza infinita rispe8o al nucleo. Ha quindi valori sempre nega>vi.
Energia degli orbitali Il valore dell energia di un orbitale è, in modulo, il valore dell energia necessaria a portare l ele8rone a distanza infinita rispe8o al nucleo. Ha quindi valori sempre nega>vi.
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
16. Struttura elettronica delle molecole e legame chimico
 16. Struttura elettronica delle molecole e legame chimico Coordinate degli elettroni:,,, Coordinate dei nuclei,,, :,,, Funzione d onda esatta: Ψ(,,,,,,, ) Data la notevole differenza di masse, la dinamica
16. Struttura elettronica delle molecole e legame chimico Coordinate degli elettroni:,,, Coordinate dei nuclei,,, :,,, Funzione d onda esatta: Ψ(,,,,,,, ) Data la notevole differenza di masse, la dinamica
Spettroscopie di luminescenza
 Spettroscopie di luminescenza La luminescenza è il fenomeno per cui una specie eccitata ad un livello elettronico ad energia più elevata emette radiazione per tornare allo stato fondamentale: X eccitazione
Spettroscopie di luminescenza La luminescenza è il fenomeno per cui una specie eccitata ad un livello elettronico ad energia più elevata emette radiazione per tornare allo stato fondamentale: X eccitazione
Prof. R. Velotta Dr. R. Esposito
 Prof. R. Velotta Dr. R. Esposito La fluorescenza La spettroscopia di fluorescenza è un potente strumento per lo studio delle strutture e delle dinamiche molecolari, in fisica, chimica e biologia. Sebbene
Prof. R. Velotta Dr. R. Esposito La fluorescenza La spettroscopia di fluorescenza è un potente strumento per lo studio delle strutture e delle dinamiche molecolari, in fisica, chimica e biologia. Sebbene
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Sottodiscipline della Chimica Fisica Storicamente
 Sottodiscipline della Chimica Fisica Storicamente Termodinamica Chimica. Si occupa di tutti i processi (principalmente macroscopici) legati all energia e al suo scambio, nelle varie forme che esso può
Sottodiscipline della Chimica Fisica Storicamente Termodinamica Chimica. Si occupa di tutti i processi (principalmente macroscopici) legati all energia e al suo scambio, nelle varie forme che esso può
LA FOTOSINTESI: conversione di energia luminosa in energia chimica
 LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti).
 4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
fenomeno X nm Å UV - visibile legami chimici infrarosso
 Spettroscopia IR radiazione f (Hz) energia (ev) fenomeno λ / dim. tipica X 10 18 10 20 10 3 10 5 livelli interni atomici nm Å UV - visibile 10 14 10 16 0.1 10 legami chimici 300 800 nm infrarosso 10 11
Spettroscopia IR radiazione f (Hz) energia (ev) fenomeno λ / dim. tipica X 10 18 10 20 10 3 10 5 livelli interni atomici nm Å UV - visibile 10 14 10 16 0.1 10 legami chimici 300 800 nm infrarosso 10 11
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
Telerilevamento II. Spettroscopia in riflessione e trasmissione per materiali litoidi e Laboratorio
 Università degli Studi di Parma Programma dell corso integrativo al corso ufficiale dal titolo: Telerilevamento II rivolto agli studenti di Scienze Geologiche e Spettroscopia in riflessione e trasmissione
Università degli Studi di Parma Programma dell corso integrativo al corso ufficiale dal titolo: Telerilevamento II rivolto agli studenti di Scienze Geologiche e Spettroscopia in riflessione e trasmissione
Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI
 Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI Luce : Fonte di Energia Fotosintesi Sviluppo e mantenimento della vita sulla Terra 6CO 2 + 6H 2 O + 60 fotoni ----> C 6 H 12
Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI Luce : Fonte di Energia Fotosintesi Sviluppo e mantenimento della vita sulla Terra 6CO 2 + 6H 2 O + 60 fotoni ----> C 6 H 12
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II Analisi elementare: formula bruta (C x H y O z N x )? Analisi cromatografica: purezza, confronto con campioni noti Punto di fusione:
Identificazione di un composto organico: Laboratorio di Chimica Organica II Analisi elementare: formula bruta (C x H y O z N x )? Analisi cromatografica: purezza, confronto con campioni noti Punto di fusione:
Spettroscopia. Spettroscopia
 Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
fenomeno livelli interni atomici legami chimici vibrazioni nm Å
 Spettroscopia Misura e studio dell andamento dell intensità della radiazione elettromagnetica/corpuscolare in funzione della frequenza (energia/lunghezza d onda) della radiazione stessa Quale tipo di informazione
Spettroscopia Misura e studio dell andamento dell intensità della radiazione elettromagnetica/corpuscolare in funzione della frequenza (energia/lunghezza d onda) della radiazione stessa Quale tipo di informazione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
Lezione n. 13. Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo. di idrogeno. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
Il microscopio elettronico a scansione
 Il microscopio elettronico a scansione Nel SEM (ed in genere nella microscopia elettronica) viene sfruttata l interazione di un fascio di e - con il campione per ricavare informazioni sul campione stesso
Il microscopio elettronico a scansione Nel SEM (ed in genere nella microscopia elettronica) viene sfruttata l interazione di un fascio di e - con il campione per ricavare informazioni sul campione stesso
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Interazione luce-materia e Spettroscopia atomica e molecolare. Corso di Biofisica, Università di Cagliari 1
 Cenni su Interazione luce-materia e Spettroscopia atomica e molecolare 1 Riferimenti D. McQuarrie, Physical Chemistry: A molecular approach, chapters 13, 15. http://blogs.jccc.edu/astronomy/textbook/unit-two-conceptualand-observational-tools-of-astronomy/chapter-5-electromagneticradiation-and-matter/
Cenni su Interazione luce-materia e Spettroscopia atomica e molecolare 1 Riferimenti D. McQuarrie, Physical Chemistry: A molecular approach, chapters 13, 15. http://blogs.jccc.edu/astronomy/textbook/unit-two-conceptualand-observational-tools-of-astronomy/chapter-5-electromagneticradiation-and-matter/
Elettroni negli Atomi
 Elettroni negli Atomi Solo alcune orbite sono stabili In realtànon sonoorbitema FUNZIONI D ONDA Ψ Ψ 2 è la DENSITA di probabilità di trovare l elettrone in una certa posizione rispetto al nucleo Le varie
Elettroni negli Atomi Solo alcune orbite sono stabili In realtànon sonoorbitema FUNZIONI D ONDA Ψ Ψ 2 è la DENSITA di probabilità di trovare l elettrone in una certa posizione rispetto al nucleo Le varie
Prof. Mariano Casu (modulo II) (Prof. Navarra) (Prof. Casu)
 Università degli Studi di Cagliari Corso di Laurea triennale in Chimica Chimica fisica II e laboratorio CFU 6 + 6 Docenti Prof. Gabriele Navarra (modulo I) Prof. Mariano Casu (modulo II) SSD CHIM/02 Tel.
Università degli Studi di Cagliari Corso di Laurea triennale in Chimica Chimica fisica II e laboratorio CFU 6 + 6 Docenti Prof. Gabriele Navarra (modulo I) Prof. Mariano Casu (modulo II) SSD CHIM/02 Tel.
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
Cenni di Spettroscopia
 Cenni di Spettroscopia Gli elettroni di una molecola possono avere energie diverse, possono, cioè, essere più o meno legati ai nuclei degli atomi che costituiscono la molecola. l numero di energie possibili
Cenni di Spettroscopia Gli elettroni di una molecola possono avere energie diverse, possono, cioè, essere più o meno legati ai nuclei degli atomi che costituiscono la molecola. l numero di energie possibili
Light Amplification by Stimulated Emission of Radiation
 Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
Metodi spettroscopici per le Biotecnologie
 AA 2013-2014 Metodi spettroscopici per le Biotecnologie Spettroscopia UV-VIS 2 Dott. Alfonso Zoleo Principali aminoacidi cromoforici Phe Tyr Trp Max Assorb. Asorb. Molare (M -1 cm -1 ) Fenilalanina 257.4
AA 2013-2014 Metodi spettroscopici per le Biotecnologie Spettroscopia UV-VIS 2 Dott. Alfonso Zoleo Principali aminoacidi cromoforici Phe Tyr Trp Max Assorb. Asorb. Molare (M -1 cm -1 ) Fenilalanina 257.4
(2) cubico a facce centrate (3) esagonale compatto
 IL LEGAME METALLICO La maggior parte dei metalli cristallizza in strutture a massimo impacchettamento, ovvero in solidi in cui si può considerare che gli ioni metallici che occupano le posizioni reticolari,
IL LEGAME METALLICO La maggior parte dei metalli cristallizza in strutture a massimo impacchettamento, ovvero in solidi in cui si può considerare che gli ioni metallici che occupano le posizioni reticolari,
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
L ONDA ELETTROMAGNETICA UNITA DI MISURA E DEFINIZIONI. ν ν. λ =
 IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
Fisica atomica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
L atomo di Bohr. Argomenti. Al tempo di Bohr. Spettri atomici 19/03/2010
 Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
Teoria dell Orbitale Molecolare
 Teoria dell Orbitale Molecolare Un orbitale molecolare è il risultato della combinazione lineare degli orbitali atomici appartenenti agli atomi che costituiscono la molecola; questi orbitali molecolari
Teoria dell Orbitale Molecolare Un orbitale molecolare è il risultato della combinazione lineare degli orbitali atomici appartenenti agli atomi che costituiscono la molecola; questi orbitali molecolari
Struttura del sistema periodico Stato fondamentale degli elementi
 Struttura del sistema periodico Stato fondamentale degli elementi Singolo elettrone: 1)Numero quantico principale n 2)Numero quantico del momento angolare orbitale l = 0, 1,, n-1 3)Numero quantico magnetico
Struttura del sistema periodico Stato fondamentale degli elementi Singolo elettrone: 1)Numero quantico principale n 2)Numero quantico del momento angolare orbitale l = 0, 1,, n-1 3)Numero quantico magnetico
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
Lezione 3. Legame Chimico. Teoria degli Orbitali Molecolari
 Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
Il principio di indeterminazione di Heisenberg
 Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
numeri quantici orbitale spin
 La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
TECNICHE RADIOCHIMICHE
 TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
Sviluppo storico. Spettroscopia. Sviluppo storico della spettroscopia. Dal qualitativo al quantitativo. C. A. Mattia
 UNIVERSITÀ DEGLI STUDI DI SALERNO Sviluppo storico della spettroscopia L inizio: il problema del colore Il colore è contenuto nella luce o nei corpi? FACOLTÀ DI FARMACIA Spettroscopia C. A. Mattia Dal
UNIVERSITÀ DEGLI STUDI DI SALERNO Sviluppo storico della spettroscopia L inizio: il problema del colore Il colore è contenuto nella luce o nei corpi? FACOLTÀ DI FARMACIA Spettroscopia C. A. Mattia Dal
Corso di laboratorio di fisica della materia Prof. Mario Rocca AA Il progresso delle conoscenze in Fisica è indissolubilmente legato al
 Corso di laboratorio di fisica della materia Prof. Mario Rocca AA 2012-2013 Il progresso delle conoscenze in Fisica è indissolubilmente legato al progresso nei metodi di indagine sperimentale. Il corso
Corso di laboratorio di fisica della materia Prof. Mario Rocca AA 2012-2013 Il progresso delle conoscenze in Fisica è indissolubilmente legato al progresso nei metodi di indagine sperimentale. Il corso
Transizioni elettroniche per uno ione. Transizioni elettroniche per uno ione metallico in campo dei leganti
 Transizioni elettroniche per uno ione metallico in campo dei leganti d 2 ion Electron-electron repulsion Transizioni elettroniche per uno ione Applichiamo i concetti del modello del campo dei leganti ad
Transizioni elettroniche per uno ione metallico in campo dei leganti d 2 ion Electron-electron repulsion Transizioni elettroniche per uno ione Applichiamo i concetti del modello del campo dei leganti ad
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].
![Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].](/thumbs/62/47096832.jpg) Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Quarta unità didattica. Disposizione degli elettroni nell atomo
 Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
I 4 NUMERI QUANTICI. I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali.
 I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
Chimica-Fisica Biologica.
 Chimica-Fisica Biologica http://people.unica.it/flaminiacesaremarincola/ Il Il BIOLOGO MOLECOLARE studia negli organismi viventi i meccanismi molecolari fisiologici e patologici, concentrandosi in particolare
Chimica-Fisica Biologica http://people.unica.it/flaminiacesaremarincola/ Il Il BIOLOGO MOLECOLARE studia negli organismi viventi i meccanismi molecolari fisiologici e patologici, concentrandosi in particolare
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Unità Didattica 6. Spettroscopia delle nebulose
 Diapositiva 1 Unità Didattica 6 Spettroscopia delle nebulose Questa unità presenta i fondamenti della fisica del gas ionizzato che servono a comprendere gli spettri a righe d emissione osservati in alcune
Diapositiva 1 Unità Didattica 6 Spettroscopia delle nebulose Questa unità presenta i fondamenti della fisica del gas ionizzato che servono a comprendere gli spettri a righe d emissione osservati in alcune
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA
 LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
Schema di un tubo a raggi X
 Raggi X 1 Schema di un tubo a raggi X I raggi X sono prodotti quando una sostanza è bombardata da elettroni ad alta velocità. I componenti fondamentali di un tubo a raggi X sono: a) ampolla di vetro a
Raggi X 1 Schema di un tubo a raggi X I raggi X sono prodotti quando una sostanza è bombardata da elettroni ad alta velocità. I componenti fondamentali di un tubo a raggi X sono: a) ampolla di vetro a
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA. (Plank Einstein)
 L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
INTRODUZIONE AI METODI OTTICI
 INTRODUZIONE AI METODI OTTICI Con l espressione Metodi Ottici s intende l insieme delle tecniche analitiche nelle quali interviene una radiazione elettromagnetica. Per avere una sufficiente comprensione
INTRODUZIONE AI METODI OTTICI Con l espressione Metodi Ottici s intende l insieme delle tecniche analitiche nelle quali interviene una radiazione elettromagnetica. Per avere una sufficiente comprensione
Lezione n. 26. Principi generali della spettroscopia IR. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
ORBITA ORBIT LI ALI MOLECOLARI
 ORBITALI MOLECOLARI Una molecola è dotata di una serie di orbitali detti orbitali molecolari Gli elettroni risiedono negli orbitali molecolari che, in molti casi, sono distribuiti (delocalizzati) su tutta
ORBITALI MOLECOLARI Una molecola è dotata di una serie di orbitali detti orbitali molecolari Gli elettroni risiedono negli orbitali molecolari che, in molti casi, sono distribuiti (delocalizzati) su tutta
Lo Spettro Elettromagnetico
 Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009
 S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009 Conduzione elettrica nei metalli (conduttori e semiconduttori) Corso di Laboratorio di Didattica
S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009 Conduzione elettrica nei metalli (conduttori e semiconduttori) Corso di Laboratorio di Didattica
Spettroscopia di assorbimento nel visibile e nell ultravioletto. Carlo I.G. Tuberoso Appunti didattici uso laboratorio ver. 00
 Spettroscopia di assorbimento nel visibile e nell ultravioletto Carlo I.G. Tuberoso Appunti didattici uso laboratorio ver. 00 I metodi spettroscopici di analisi si basano sulla misura della radiazione
Spettroscopia di assorbimento nel visibile e nell ultravioletto Carlo I.G. Tuberoso Appunti didattici uso laboratorio ver. 00 I metodi spettroscopici di analisi si basano sulla misura della radiazione
Altro metodo di indagine che utilizza la spettroscopia. Spettrofluorimetria
 Altro metodo di indagine che utilizza la spettroscopia Spettrofluorimetria La luminescenza Luminescenza: emissione di luce da atomi, molecole o cristalli eccitati elettronicamente. Eccitazione luminosa:
Altro metodo di indagine che utilizza la spettroscopia Spettrofluorimetria La luminescenza Luminescenza: emissione di luce da atomi, molecole o cristalli eccitati elettronicamente. Eccitazione luminosa:
Produzione dei raggi X
 I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI
 LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI
 MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
