Il Livello Chimico di Organizzazione
|
|
|
- Eva Fantoni
- 6 anni fa
- Visualizzazioni
Transcript
1 Scuola di Ingegneria Industriale e dell Informazione Course (095857) Introduction to Green and Sustainable Chemistry Il Livello Chimico di Organizzazione Prof. (e Dr.ssa Ada Truscello) Dept. CMIC
2 Riassunto Atomi e Molecole Struttura dell atomo Elettroni Legami Notazione Chimica Reazioni Chimiche Concetti base sull energia Tipi di reazioni Acidi e basi ph Composti Inorganici Biossido di Carbonio e ossigeno Acqua Acidi e basi Sali Composti Organici ATP Carboidrati Lipidi Proteine Acidi Nucleici
3 Materia, Elementi e Atomi Materia: qualunque cosa che occupa spazio e possiede massa 3 stati di aggregazione Solido Liquido Gas Tutta la materia è composta da elementi Non si possono rompere (a bassa T) Il componente minimo di un elemento è l atomo Ogni elemento ha un unico simbolo chimico e n 0 n 0 p + p + 2p + Helium (He) e L Atomo è costituito da 3 particelle subatomiche Protoni Neutroni Elettroni
4 Struttura dell Atomo Protoni e neutroni si trovano nel nucleo (d = m) Gli elettroni occupano una nuvola elettronica (strato) esterno (d = m) Queste particelle caratterizzano le dimensioni dell atomo (Å) e la reattività chimica (cinetica e termodinamica). e p + (a) Nuvola elettronica o Modello «space filling» (b) Modello a strato elettronico
5 Struttura dell Atomo ed Elementi Numero Atomico = Z = # di protoni ed anche # di elettroni in un atomo neutro. Numero di Massa = A = # p + # n Gli atomi che differiscono per A ma hanno lo stesso Z sono chiamati isotopi ( ) C, C, C Gli Elementi rappresentano la distribuzione naturale degli isotopi. A (1) Cl = (0.758) 35 Cl + (0.242) 37 Cl Z
6 Elettroni e Strati Elettronici Solo gli elettroni dello strato più esterno interagiscono (formando legami)! Se lo strato esterno è pieno, l elemento è stabile a bassa T (He) Se lo strato esterno non è pieno, l elemento è instabile e si lega Il primo strato ospita 2 elettroni Il secondo strato ne ospita 8 Secondo strato elettronico Elettrone Primo strato elettronico (a) Atomo di Carbonio (6p +, 6n 0, 6e ) (b) Atomo di Neon (10p +, 10n 0, 10e )
7 Molecole e Composti Gli Atomi si stabilizzano mediante: Condivisione di elettroni Acquisto di elettroni Perdita di elettroni Ciò corrisponde ad una reazione chimica Molecole e composti ne sono il risultato Gli Elementi Molecolari sono strutture chimiche contenenti 2 o più atomi dello stesso elemento Per Es.: O 2, O 3, S 8 I Composti contengono 2 o più atomi di diversi elementi Per es.: H 2 O, CH 3 COOH, H 2 NCH 2 COOH
8 Importanti Concetti sui Legami Chimici Tutti gli atomi tendono a raggiungere uno stato stabile! Stabilità significa raggiungere la configurazione a 8 elettroni nello strato esterno per gli atomi dei primi periodi e 18 per i successivi A meno che non riempiano il primo strato (2 elettroni) (o gli orbitali d e f) Gli Opposti si attraggono! (per es. Ioni: Na + Cl ) Gli atomi sono elettricamente neutri! (N p + = N e ) 3 tipi di legami Ionico Covalente Polare Apolare Metallico Interazioni Legami a idrogeno, Van der Waals e altri
9 Legami Ionici Gli ioni sono atomi con una carica positiva o negativa Anioni Ioni con carica negativa L atomo guadagna un elettrone (accettore di elettroni) Più elettroni che protoni Stadio 1: Formazione Cationi di ioni Ioni con carica positiva L atomo perde un elettrone (datore di elettroni) più protoni che elettroni I legami ionici sono legami polimerici tra molti anioni e molti cationi Per es.: NaCl, KCl Atomo di Sodio Ione Sodio Na + Stadio 2: Attrazione tra cariche opposte Stadio 3: Formazione di un composto ionico Cloruro di Sodio (NaCl) (a) Atomo di Cloro Ione Cloruro Cl Ione Cloruro Cl (b) Cristallo di Cloruro di Sodio Ione Sodio Na +
10 Legami Covalenti Formano un legame scambiando elettroni Legame covalente Singolo Legame covalente Doppio (triplo) Scambiano una copia di elettroni Scambiano due (o tre) coppie di elettroni MODELLO A STRATO ELETTRONICO E FORMULA STRUTTURALE MODELLO A RIEMPIMENTO SPAZIALE Idrogeno Nitrogen Azoto (N 2 ) N N Biossido carbonio
11 Legami Covalenti Legami covalenti apolari Gli elettroni sono ugualmente condivisi Atomi di carbonio Creano strutture complesse di numerosi atomi negli organismi Tipicamente simmetrico (non polare) Legami covalenti polari Scambio diseguale di elettroni L acqua ne è un grande esempio Tipicamente contengono atomi elettronegativi, quali O, N, F
12 Interazioni: Legami ad Idrogeno Semplice interazione non un vero legame chimico. Debole (20-60 kj mol -1 ) Attrazione tra atomi di idrogeno di una molecola e atomi parzialmente carichi negativi di altre molecole (è essenzialmente elettrostatico) Non genera molecole Altera la forma di molecole L acqua è l esempio tipico Spiega l elevata tensione superficiale di H 2 O
13 Regole di Notazione Chimica L abbreviazione dell elemento rappresenta 1 atomo Il numero (#) prima dell abbreviazione dell elemento indica più di 1 atomo Una freccia suddivide a sinistra i Reagenti e a destra i Prodotti (reagenti e prodotti hanno formule chimiche diverse att. Isomeri!) Gli apici indicano uno ione + = perdita di 1 elettrone (Na + ione sodio) - = guadagno di 1 elettrone (Cl ione cloruro) ecc. Le reazioni chimiche devono essere bilanciate : La massa non cambia in una reazione chimica gli atomi in materie prime e in scarti sono gli stessi e sono quindi perfettamente riusabili!
14 Reazioni Chimiche Si hanno quando i legami tra atomi si spezzano e gli atomi si traspongono in nuove combinazioni Hanno un ruolo importante Consentono di ottenere prodotti non stabili inesistenti in natura Forniscono energia (combustione, glicolisi) Il metabolismo è l insieme delle reazioni chimiche che avvengono in un orgasmo vivente. Una reazione particolarmente importante è C 6 H 12 O 6 6CO 2 + 6H 2 O + ATP 3 tipi generali di reazioni importanti in biochimica: Reazioni di decomposizione Reazioni di sintesi Reazioni di scambio
15 Concetti di Base sull Energia Lavoro: movimento o variazione nella struttura fisica della materia Energia: capacità di compiere lavoro Energia cinetica Energia associata al movimento (rilasciata) E = ½(mv 2 ) Energia potenziale Energia accumulata (in un campo di forze, in legami, ecc.) Altre forme (gravitazionale, elettromagnetica, nucleare, calore) Si trasforma facilmente da una forma all altra Una forma importante di rilascio di energia è il calore L'Energia è anche associata a variazioni di configurazioni del sistema (entropia)
16 Reazioni di Decomposizione (C 6 H 10 O 5 ) n + n H 2 O n C 6 H 12 O 6 Catabolismo L energia è rilasciata nella reazione di depolimerizzazione idrolitica. Glicogeno Molecole di glucosio Esempio di reazione di decomposizione: rottura idrolitica del glicogeno con rilascio di unità di glucosio
17 Reazioni di Sintesi A + B AB + H 2 O Anabolismo Dell energia è immagazzinata nei legami della macromolecola. Amminoacidi Molecola di proteina Esempio di reazione di sintesi: degli amminoacidi sono legati in sequenza per formare una molecola di proteina
18 Reazioni di Scambio AB + CD AD + CB Reazioni di decomposizioni e sintesi. Scambio di atomi o gruppi. Reazione esotermica ( H < 0) Se i legami nei prodotti hanno E leg superiore a quella dei reagenti L energia è rilasciata sotto forma di calore Reazioni endotermiche ( H > 0) Se i legami nei prodotti hanno E leg inferiore a quella dei reagenti Si deve fornire e assorbire energia (calore) dal sistema Reazioni Spontanee : ( G < 0) : la reazione avviene spontaneamente da reagenti a prodotti (non si sa in quanto tempo!!); la reazione inversa avviene solo se si fornisce energia.
19 Acidi e Basi (secondo Brönsted) Acido: una sostanza che dissocia rilasciando ioni H + Acidi forti dissociano completamente HCl + H 2 O H 3 O + + Cl Acidi deboli dissociano solo parzialmente HCOOH + H 2 O a H 3 O + + HCOO Base: una sostanza che sottrae ioni idrogeno dalla soluzione o dissocia a dare ioni ossidrile (OH ) Basi forti dissociano completamente Basi deboli dissociano solo parzialmente NaOH + H 2 O Na + + OH NH 3 + H 2 O a NH OH
20 ph Misura la concentrazione di [H + ] in un mezzo acquoso (ph = -log[h + ]) Se elevata, altera le strutture e le funzioni di sistemi biologici Il ph varia tra 0-14; il mezzo è neutro se ph = 7 (acqua distillata) ph sotto 7 = acido; ph sopra 7 = basico Le cellule in sistemi biologici devono mantenere il ph in uno specifico intervallo attorno a 7 (per es. Il sangue è tamponato tra ) Tamponi: Combinazione di un acido e la sua base coniugata che stabilizzano il ph rimuovendo o fornendo ioni idrogeno. Per esempio, Acido Acetico (CH 3 COOH) e ione acetato (CH 3 COO ).
21 Biochimica Nutrienti: elementi e molecole essenziali Metaboliti: tutte le molecole sintetizzate o degradate in reazioni chimiche in un organismo vivente Si classificano in base al tipo di atomo e complessità dell aggregato: Composti Inorganici (tutte le combinazioni di elementi senza C); Composti di coordinazione (combinazioni di atomi organizzate attorno ad atomi centrali metallici); Composti Organici (tutte le combinazioni di scheletri di atomi C contenenti anche elementi importanti (H, O, N, P, S, Cl); Composti organometallici (tutte le combinazioni di scheletri di atomi C contenenti anche elementi metallici).
22 Composti Inorganici Elementi e Metalli Biossido di Carbonio (CO 2 ) Ossigeno (O 2 ) Acqua (H 2 O) e acqua ossigenata (H 2 O 2 ) Acidi inorganici (HCl, HNO 3, H 2 SO 4, H 3 PO 4 ) e basi (NaOH, NH 3, NH 2 NH 2 Sali (NaCl, Na 2 CO 3, NaH 2 PO 4, ecc.) Metalli e leghe metalliche Complessi Inorganici e clusters Polimeri inorganici (diamante, SiO 2, Silicati, Fosforo rosso, ecc.) Materiali inorganici Composti organometallici
23 Biossido di Carbonio e Ossigeno Biossido di Carbonio Prodotto dalle cellule tramite attività metabolica (fermentazione al.) C 6 H 12 O 6 2 CH 3 CH 2 OH + 2H 2 O + ATP (*) Si sposta nel sangue fino ai polmoni, dove viene rilasciato. Reagisce con acqua a dare acido carbonico e suoi ioni (il processo è lento! Catalisi dell enzima anidrasi carbonica) CO 2 + H 2 O a H 2 CO 3 a H + + HCO 3 a H + + CO 32 Ossigeno Prodotto dalle piante tramite la fotosintesi 6CO 2 + 6H 2 O + luce (E) C 6 H 12 O 6 + 6O 2 Usato per processi di combustione e nella respirazione: (*) C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + ATP
24 Acqua (H 2 O) e sue Proprietà Costituisce il 60-80% in volume delle cellule Tutti i sistemi biologici sono dipendenti dall acqua Proprietà importanti Eccellente solvente per composti ionici e molecole ad elevata polarità Capacità termica (calore specifico) molto elevata Reagente essenziale per molte reazioni metaboliche Soluzioni Solvente vs. soluto L acqua tramite il fenomeno della solvatazione rompe i legami ionici allontanando gli ioni di segno opposto (alta costante dielettrica)
25 Solvatazione di Ioni e Dissociazione di Composti Ionici Polo Negativo Sfere di solvatazione di molecole d acqua Polo Positivo Molecola d acqua Soluzione di cloruro di sodio (NaCl)
26 Acidi e Basi Inorganici Molti acidi inorganici si trovano nelle cellule di organismi viventi. I più importanti sono: Acido carbonico (H 2 CO 3 pk a1 = 6.35; pk a2 = 10.33)* Acido solforico (H 2 SO 4 pk a1 = strong; pk a2 = 1.92)* Acido fosforico (H 3 PO 4 pk a1 = 2.16; pk a2 = 7.21; pk a3 = 12.32)* Acido cloridrico (HCl; strong) Acido nitrico (HNO 3 pk a = strong) Acido silicico (H 4 SiO 4 e i suoi oligomeri, tutti deboli) Acido solfidrico (H 2 S pk a1 = 7.00; pk a2 = > 14)* Tra le basi rilevanti le più importanti sono: Ammoniaca (NH 3 pk b = 4.74)* Molti anioni (per es. HCO 3, H 2 PO 4, HPO 2 4 ) * a 20 C
27 Sali Un composto ionico formato da qualsiasi catione (eccetto H + ) e qualsiasi anione (eccetto OH - ) Per es. NaCl, CaCO 3, Ca 3 (PO 4 ) 3, CaSO 4, Mg 3 Si 4 O 10 (OH) 2 (Talco) Si dissociano in acqua (più o meno in funzione del loro K ps ) NaCl + n (H 2 O) Na + (id) + Cl (id) Nelle cellule tali composti si indicano come elettroliti Conducono la corrente elettrica in soluzione Devono essere mantenuti in intervalli di concentrazione adeguati In soluzione i cationi non sono legati agli anioni per cui l identità del sale non è evidente se non quando questi si separano per raggiunti limiti di solubilità.
28 Composti Organici Contengono H, C e altri elementi Sono caratterizzati da legami covalenti C-C e C-H forti. Carboidrati Monosaccaridi Disaccaridi Polisaccaridi Lipidi Acidi grassi Grassi Steroidi Fosfolipidi Proteine Funzione delle Proteine Struttura delle Proteine Enzimi Acidi Nucleici Struttura Funzioni ATP Metaboliti secondari
29 Principali Composti Organici in Sistemi Viventi COMPOSTI ORGANICI Carboidrati Lipidi Proteine includono includono composte da Acidi Nucleici includono Composti ad Alta Energia includono Polisaccaridi Trigliceridi Peptidi RNA DNA ATP contengono Disaccaridi Acidi grassi composti da composti da Ammino acidi composti da composto da Nucleotide Nucleotidi composti da due Monosaccaridi e e Glicerolo Gruppi Fosfato
30 Carboidrati Rapporto 1:2:1 di atomi di carbonio, idrogeno, ossigeno Principale fonte di energia per dismutazione o ossidazione con O 2 Costituiscono solo il 3% del peso totale del corpo umano! 3 principali tipi Monosaccaridi Disaccaridi Polisaccaridi Monosaccaridi: zuccheri semplici contenenti 3-7 C. Glucosio (il combustibile più importante nel corpo), fruttosio, ecc. H HO H H HC C C C C C H 2 O OH H OH OH OH H H OH HO H OH O OH (a) (b) (c) H OH H O
31 Disaccaridi Formati da 2 zuccheri semplici per reazione di condensazione con eliminazione di acqua Saccarosio, lattosio, maltosio Si possono idrolizzare con acqua a formare zuccheri semplici Sintesi per disidratazione Glucosio Fruttosio Saccarosio (a) Nel corso della condensazione si legano due molecole per rimozione di una molecola d acqua. Idrolisi Saccarosio Glucosio Fruttosio (b) L idrolisi inverte il processo; la molecola complessa viene spezzata per aggiunta di una molecola d acqua.
32 Polisaccaridi Nelle piante Amido Cellulosa Pectine Polisaccaridi complessi Molecole di glucosio Negli animali glicogeno Lunghe catene di glucosio Non si scioglie in acqua Immagazzinato in fegato e muscoli Idrolizzato in glucosio quando serve come combustibile Polisaccaridi complessi (c) Glicogeno, un polisaccaride ramificato di molecole di glucosio è immagazzinato nelle cellule dei muscoli e del fegato
33 Lipidi Contengono H, O, C, P, S, o N Grassi, oli, Cere Insolubili in acqua Costituiscono componenti strutturali essenziali delle cellule Servono come riserva energetica Forniscono il doppio di energia de carboidrati 12% del peso corporeo Si dividono in acidi grassi e grassi, steroidi, fosfolipidi terpeni
34 Acidi Grassi Lunghe catene idrocarburiche con in fondo un gruppo COOH FA Saturi Tutti i carboni sono saturi (singoli legami covalenti C-C) FA Insaturi Contengono C saturi ma anche doppi legami tra i Carboni Meno atomi di Idrogeno Hanno un ruolo essenziale come riserva di energia e come costituenti delle pareti cellulari. Saturo Insaturo (a) Acido laurico (C 12 H 24 O 2 ) (b)
35 Grassi Trigliceridi 1 molecola di glicerolo e 3 di acidi grassi Sono deputati allo stoccaggio dell energia Acido grasso 1 Saturo Acido grasso 2 Saturo condensazione Acido grasso 3 Insaturo Idrolisi Glicerolo
36 Steroidi Colesterolo Si trova in: H 3 C H 3 C H H Membrane cellulari H 3 C H Ormoni HO H H Estrogeni e testosterone H Deriva da: Dieta Fegato
37 Fosfolipidi Sono fatti da digliceridi e gruppi fosfato Hanno regioni polare e nonpolari Compongono le membrane cellulari Gruppi nonlipidici Gruppo fosfato Glicerolo Acidi grassi
38 Proteine Abbondanti e diverse 100,000 differenti tipi nel corpo 20% del peso corporeo Contengono C, H, O, N, e dello S Funzione Struttura Enzimi
39 Funzioni delle Proteine Supporto Movimento Trasporto Tamponamento Regolazioni Metaboliche Coordinazione, comunicazione e controllo Difesa
40 Struttura delle Proteine Composti di catene di amminoacidi Tipiche proteine contengono 1000 amminoacidi Le più grandi contengono 100,000 aa o più Il legame peptidico interconnette gli aa Dipeptide polipeptide Carbonio centrale Gruppo ammino Gruppo R Gruppo acido carbossilico (a) Struttura di un amminoacido Condensazione Idrolisi Glicina (gly) Alanina (ala) (b) Formazione del legame peptidico Legame peptidico
41 Struttura delle Proteine La forma di una proteina dipende dall interazione degli amminoacidi : Gruppo R Legami a idrogeno Solvatazione di molecole d acqua Forma = funzione!!!! Piccole variazioni nella struttura possono cambiare le funzioni! Modifiche: Sostituzione di un amminoacido Temperatura ph Denaturazione Se la temperatura è troppo alta, le proteine perdono la loro forma e non hanno più le loro funzioni Se il fenomeno continua, ne consegue la morte
42 Struttura delle Proteine: Proteine Globulari vs. Fibrose (a) Catena polipeptidica Subunità di proteina globulare (b) Mioglobina (c) Emoglobina (d) Fibre di cheratina
43 Enzimi e Reazioni Chimiche La maggior parte delle reazioni chimiche non avviene spontaneamente o così lentamente che saremmo già tutti morti! Gli enzimi aumentano la velocità delle reazioni Si rigenerano nel corso della reazione. Substrati of Sito attivo ENZIMA Stadio 1: I substrati si legano al sito attivo dell enzima Azione di un Enzima Complesso enzima-substrato
44 Acidi Nucleici Costituenti: C, H, O, N, P Immagazzinano ed elaborano le informazioni a livello molecolare Si trovano nelle cellule 2 tipi principali DNA (ac. deossiribonucleico) RNA (ac. ribonucleico) Composti da nucleotidi 3 componenti Zucchero Gruppo fosfato Base azotata Deossiribosio Gruppo fosfato Timina Adenina Legame a idrogeno Adenina Guanina Citosina Timina (DNA) Uracile (RNA) (a) molecola di RNA (b) molecola di DNA
45 Composti ad Alta Energia L energia è ottenuta dal catabolismo di composti organici (glucosio) I legami sono ad alta energia Covalenti; immagazzinano grandi quantità di energia ATP (adenosina trifosfato) Generato dall ADP (adenosina difosfato)
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
LIPIDI. I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi.
 LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
Costituzione dei viventi
 Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Idrogeno (H) Azoto (N) La materia è costituita da elementi chimici. In natura sono presenti 92 elementi
 Gli organismi sono fatti da MATERIA*. (*qualsiasi cosa che occupa uno spazio e ha una massa) Gli antichi filosofi greci dicevano che la materia deriva da 4 ingredienti di base o ELEMENTI (ARIA, ACQUA,
Gli organismi sono fatti da MATERIA*. (*qualsiasi cosa che occupa uno spazio e ha una massa) Gli antichi filosofi greci dicevano che la materia deriva da 4 ingredienti di base o ELEMENTI (ARIA, ACQUA,
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
LIPIDI. Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
I due studiosi tedeschi, Jacob Schleiden e Theodor Schwann, formularono la cosiddetta "teoria cellulare". Brevemente essa afferma che la cellula è:
 TEORIA CELLULARE Molti secoli sono trascorsi da quando gli studiosi dell'antica Grecia formularono la teoria della generazione spontanea della vita, secondo cui insetti ed altri piccoli animali avrebbero
TEORIA CELLULARE Molti secoli sono trascorsi da quando gli studiosi dell'antica Grecia formularono la teoria della generazione spontanea della vita, secondo cui insetti ed altri piccoli animali avrebbero
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
PROGRAMMA DISCIPLINARE SVOLTO a. s / N.B. il programma è pubblico ad uso degli studenti e delle famiglie.
 Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2. O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1
 NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
Legame Chimico. Legame Chimico
 Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
Le interazioni deboli:
 Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA
 FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti
FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti
Roberta Pierattelli. Metalli in Biologia. Qualche richiamo di chimica generale e inorganica
 Roberta Pierattelli Metalli in Biologia Qualche richiamo di chimica generale e inorganica Le proprietà periodiche n =1 n =2 n =3 n =4 n =5 n =6 n =7 Il numero del gruppo corrisponde alla somma degli elettroni
Roberta Pierattelli Metalli in Biologia Qualche richiamo di chimica generale e inorganica Le proprietà periodiche n =1 n =2 n =3 n =4 n =5 n =6 n =7 Il numero del gruppo corrisponde alla somma degli elettroni
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Teorie Acido-Base. valutazione degli acidi
 Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
MEMBRANE. struttura: fosfolipidi e proteine
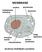 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
che è caratteristico degli alcoli (es CH 3 -CH 2 -OH etanolo) gruppo carbonilico che si trova in composti detti chetoni;
 LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Unità 1. Le molecole della vita
 Unità 1 Le molecole della vita In apertura: Lattosio, sì o no? Latte e latticini sono cibi nutrienti, ricchi di proteine e minerali Per milioni di persone, però, i benefici di questi alimenti sono accompagnati
Unità 1 Le molecole della vita In apertura: Lattosio, sì o no? Latte e latticini sono cibi nutrienti, ricchi di proteine e minerali Per milioni di persone, però, i benefici di questi alimenti sono accompagnati
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Stampa Preventivo. A.S Pagina 1 di 8
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Le molecole della vita
 Le molecole della vita Inorganici -Acqua -Ossigeno (O 2 ), Anidride carbonica (CO 2 ) -Elementi minerali quali Calcio (Ca), Fosforo (P), Magnesio (Mg), Sodio(Na), Potassio (K), Zolfo (S), Cloro (Cl), Ferro
Le molecole della vita Inorganici -Acqua -Ossigeno (O 2 ), Anidride carbonica (CO 2 ) -Elementi minerali quali Calcio (Ca), Fosforo (P), Magnesio (Mg), Sodio(Na), Potassio (K), Zolfo (S), Cloro (Cl), Ferro
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: H 2 O 2(aq) + MnO 4
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica -aminoacidi
 Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica α-aminoacidi (17.1) subunità che costituiscono le proteine formatei da un carbonio-α
Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica α-aminoacidi (17.1) subunità che costituiscono le proteine formatei da un carbonio-α
BIOCHIMICA. Studio delle caratteristiche e delle trasformazioni delle molecole biologiche che costituiscono tutti gli organismi viventi
 BIOCHIMICA Studio delle caratteristiche e delle trasformazioni delle molecole biologiche che costituiscono tutti gli organismi viventi Carbonio(C) 19,37% Ossigeno(O) 62,81% Idrogeno(H) 9,31% ELEMENTI CHIMICI
BIOCHIMICA Studio delle caratteristiche e delle trasformazioni delle molecole biologiche che costituiscono tutti gli organismi viventi Carbonio(C) 19,37% Ossigeno(O) 62,81% Idrogeno(H) 9,31% ELEMENTI CHIMICI
UNITÀ 1. Le molecole della vita
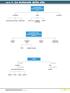 Le principali molecole biologiche sono i carboidrati i lipidi le proteine monosaccaridi disaccaridi polisaccaridi grassi e cere fosfolipidi e glicolipidi steroidi Le proteine sono caratterizzate da diverse
Le principali molecole biologiche sono i carboidrati i lipidi le proteine monosaccaridi disaccaridi polisaccaridi grassi e cere fosfolipidi e glicolipidi steroidi Le proteine sono caratterizzate da diverse
02/12/2014. Tutti gli esseri viventi sono composti da cellule LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI
 Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica. Lezione del 7 Marzo 2016
 C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
La chimica della vita
 La chimica della vita -Elementi : Carbonio (C), Ossigeno (O), Idrogeno (H), Calcio (Ca), Fosforo (P), Magnesio (Mg), Sodio(Na), Potassio (K), Zolfo (S), Cloro (Cl), Ferro (Fe), Zinco (Zn), Rame (Cu), Iodio
La chimica della vita -Elementi : Carbonio (C), Ossigeno (O), Idrogeno (H), Calcio (Ca), Fosforo (P), Magnesio (Mg), Sodio(Na), Potassio (K), Zolfo (S), Cloro (Cl), Ferro (Fe), Zinco (Zn), Rame (Cu), Iodio
INCLUSIONI MEMBRANA, CAPSULA, PARETE CELL. FLAGELLI PILI RIBOSOMI STRUTTURE CELLULARI INCLUSIONI MEMBRANA, CAPSULA, PARETE CELL.
 ANALISI ELEMENTARE Elemento % peso Funzione Origine secco Carbonio 50 Costituente principale del materiale cellulare Composti organici; CO2 Ossigeno 20 Costituente dei composti organici e dell'acqua cellulare
ANALISI ELEMENTARE Elemento % peso Funzione Origine secco Carbonio 50 Costituente principale del materiale cellulare Composti organici; CO2 Ossigeno 20 Costituente dei composti organici e dell'acqua cellulare
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
LA SINTESI PROTEICA LE MOLECOLE CHE INTERVENGONO IN TALE PROCESSO SONO:
 LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Nota dell editore Presentazione
 00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
Misure di ph e titolazione acidobase con metodo potenziometrico
 - Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
- Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
I LIPIDI (GRASSI) Cosa sono
 I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Anno scolastico 2015/16
 Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
Reazioni in Soluzioni Acquose. Capitolo 4
 Reazioni in Soluzioni Acquose Capitolo 4 Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza presente
Reazioni in Soluzioni Acquose Capitolo 4 Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza presente
GIOCHI DELLA CHIMICA
 GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
Biologia. Organismi: faa di materia, cosctuita di elemen%, che si combinano in compos%. La chimica della vita. I legami chimici. L acqua.
 Biologia Chimica Fisica Organismi: faa di materia, cosctuita di elemen%, che si combinano in compos%. ElemenC naturali nel corpo umano Simbolo Elemento % in peso Il 96% é fako di O Ossigeno 65.0 C Carbonio
Biologia Chimica Fisica Organismi: faa di materia, cosctuita di elemen%, che si combinano in compos%. ElemenC naturali nel corpo umano Simbolo Elemento % in peso Il 96% é fako di O Ossigeno 65.0 C Carbonio
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri).
 Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
PROGRAMMA EFFETTIVAMENTE SVOLTO DAL DOCENTE
 Ministero dell istruzione, dell università e della ricerca Istituto d Istruzione Superiore Severi-Correnti IIS Severi-Correnti 02-318112/1 via Alcuino 4-20149 Milano 02-33100578 codice fiscale 97504620150
Ministero dell istruzione, dell università e della ricerca Istituto d Istruzione Superiore Severi-Correnti IIS Severi-Correnti 02-318112/1 via Alcuino 4-20149 Milano 02-33100578 codice fiscale 97504620150
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
CAP. 3 Molecole organiche degli organismi: carboidrati, lipidi, amminoacidi, proteine, acidi nucleici.
 CAP. 3 Molecole organiche degli organismi: carboidrati, lipidi, amminoacidi, proteine, acidi nucleici. 3.1 Molecole organiche degli organismi 3.1.1 I carboidrati CARBOIDRATI: comprendono zuccheri semplici
CAP. 3 Molecole organiche degli organismi: carboidrati, lipidi, amminoacidi, proteine, acidi nucleici. 3.1 Molecole organiche degli organismi 3.1.1 I carboidrati CARBOIDRATI: comprendono zuccheri semplici
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Legame metallico + + + + + + + + Elettroni di valenza + + + + Ioni Na +, Be 2+, K + etc + + + +
 Legame metallico I metalli presentano elevata conducibilità termica ed elettrica e possono subire deformazioni permanenti più facilmente dei solidi ionici. Tali proprietà fisiche sono spiegate dalla natura
Legame metallico I metalli presentano elevata conducibilità termica ed elettrica e possono subire deformazioni permanenti più facilmente dei solidi ionici. Tali proprietà fisiche sono spiegate dalla natura
I lipidi. Semplici Complessi
 Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
Configurazione elettronica e Tavola periodica. Lezioni 13-16
 Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI)
 BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI) Sono i composti chimici dei viventi. Sono formate da Carbonio (C), Idrogeno (H), Ossigeno (O), Azoto (N), Fosforo (P) e Zolfo (S).
BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI) Sono i composti chimici dei viventi. Sono formate da Carbonio (C), Idrogeno (H), Ossigeno (O), Azoto (N), Fosforo (P) e Zolfo (S).
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi
 È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica. legami tra molecole più stabili
 I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di
 IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di energia, prontamente disponibile quando l organismo ne ha bisogno.
IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di energia, prontamente disponibile quando l organismo ne ha bisogno.
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Base. Acido. Acido. Base
 ACIDI E BASI Un acido è un donatore di protoni, una base è un accettore di protoni. La base coniugata di un acido è quella che si forma quando l acido si è privato del protone. L acido coniugato di una
ACIDI E BASI Un acido è un donatore di protoni, una base è un accettore di protoni. La base coniugata di un acido è quella che si forma quando l acido si è privato del protone. L acido coniugato di una
PROGRAMMA DI BIOLOGIA. CLASSE 2^ F a. s. 2014 2015. Prof.ssa RUBINO ALESSANDRA
 ISTITUTO TECNICO INDUSTRIALE DI STATO "ENRICO FERMI" Via Luosi n. 23-41124 Modena Tel. 059211092 059236398 - (Fax): 059226478 E-mail: info@fermi.mo.it Pagina web: www.fermi.mo.it PROGRAMMA DI BIOLOGIA
ISTITUTO TECNICO INDUSTRIALE DI STATO "ENRICO FERMI" Via Luosi n. 23-41124 Modena Tel. 059211092 059236398 - (Fax): 059226478 E-mail: info@fermi.mo.it Pagina web: www.fermi.mo.it PROGRAMMA DI BIOLOGIA
Programma svolto nell a.s
 ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
Elettrolita forte = specie chimica che in soluzione si dissocia completamente (l equilibrio di dissociazione è completamente spostato verso destra)
 A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
saccaridi glucidi (CH O) poli-idrossi chetoni aldeidi monosaccaridi oligo- e poli-saccaridi il glucosio amido cellulosa
 I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
ESERCIZI SUL ph 3 0,002 0,2 13. 2. Completa la seguente tabella relativa a acidi o basi deboli.
 ESERCIZI SUL ph Livello difficoltà 1 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2. Completa la seguente tabella relativa a acidi o basi
ESERCIZI SUL ph Livello difficoltà 1 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2. Completa la seguente tabella relativa a acidi o basi
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
LEZIONI Temi e competenze acquisite Argomenti Contenuti specifici Ore 1. INTRODUZIONE AL CORSO Informazioni per gli studenti. Strutture cicliche dei
 Insegnamento: CHIMICA DELLE SOSTANZE NATURALI (cod. 069; 6 CFU; 60 ore) A.A. 04-05 Corso di laurea: Tecnologie Alimentari (TA) Scuola di Agraria e Medicina Veterinaria - Campus di Cesena Dott.ssa ELENA
Insegnamento: CHIMICA DELLE SOSTANZE NATURALI (cod. 069; 6 CFU; 60 ore) A.A. 04-05 Corso di laurea: Tecnologie Alimentari (TA) Scuola di Agraria e Medicina Veterinaria - Campus di Cesena Dott.ssa ELENA
1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di
 Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Lezione del 24 Ottobre 2014
 MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
Stampa Preventivo. A.S Pagina 1 di 11
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 11 Insegnante BADALINI RENZO Classe 2BT Materia elementi di chimica e fisica preventivo consuntivo 99 84 titolo modulo 1. STRUTTURA E TRASFORM. DELL 2. L'ATOMO
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 11 Insegnante BADALINI RENZO Classe 2BT Materia elementi di chimica e fisica preventivo consuntivo 99 84 titolo modulo 1. STRUTTURA E TRASFORM. DELL 2. L'ATOMO
