GIOVEDI : :
|
|
|
- Leopoldo Guidi
- 6 anni fa
- Visualizzazioni
Transcript
1
2 MARTEDI E MEROLEDI : : GIOVEDI : :
3 LEZIONI TEORIE ESERITAZIONI
4 3 TEST DI VERIFIA IN ITINERE PROVA ORALE OPPURE FINE ORSO: PROVA SRITTA + PROVA ORALE
5 J.. Smith FONDAMENTI DI IMIA ORGANIA- Ed. McGraw-ill W.Brown-T. Poon INTRODUZIONE ALLA IMIA ORGANIA Ed. Edises
6
7 avoli Aglio O N Indolo-3-carbinolo S Diallil solfuro Uva Fragole O O O O O O Resveratrolo O O O O O Acido ellagico
8 Origine del termine IMIA ORGANIA omposti organici composti prodotti da organismi viventi Teoria del vitalismo (1780) F. Wöhler (1828) N 4 NO cianato d'ammonio calore O 2 N N 2 urea
9 Metano O Etanolo Metano O Etanolo Benzene Benzene
10 N O O S 3 O O O N N S O 2 2 O 3 O 2 O N + O O Nimesulide 2 2 O N 2 O efalosporina
11 avoli Aglio 2 N Indolo-3-carbinolo O O 2 S Diallil solfuro Uva O Resveratrolo O O O Fragole O O O O O O Acido ellagico O O
12 Tutte le molecole organiche contengono carbonio [A.Kekulé (1861)]
13 Metano O Etanolo Benzene O N S O O O 2 O 3 O N O N 2 O O efalosporina N S O O O 2 O 3 O N O N 2 O O O N + O O N S 3 O O Nimesulide O N + O O N S 3 O O
14 avoli Aglio O 2 O NN Indolo-3-carbinolo 2 S S Diallil solfuro Uva O Resveratrolo O O Fragole O O O O O O O Acido ellagico O O
15 La maggior parte dei composti organici sono costituiti, oltre che da carbonio, anche da idrogeno, ossigeno ed azoto [A.Lavoisier (1784)]
16 Metano O Benzene Benzene N N O O S 33 Etanolo O N O N S O 2 O 3 O O O N + + O O Nimesulide O N 2 O efalosporina
17 Nei composti organici gli atomi sono solitamente tenuti insieme tramite legami covalenti
18 Studio strutturale delle molecole organiche ( cioè come gli atomi si legano tra di loro) Studio della relazione Struttura Reattività (suddivisione dei composti in varie classi a seconda del gruppo funzionale presente) Studio della relazione Struttura Attività ( biologica e/o farmacologica)
19 Rappresentazione di un atomo ATOMO Nucleo (protoni + neutroni) Nuvola elettronica Numero protoni = Numero elettroni Numero protoni + Numero neutroni
20 Ancora sull atomo Media pesata della massa degli isotopi 6 IV Gruppo Numero atomico Peso atomico
21
22 Ancora sulla tavola periodica Riga = PERIODO Gli elementi di uno stesso gruppo hanno proprietà elettroniche e chimiche simili Elementi della stessa riga hanno dimensioni simili. olonna = GRUPPO N di elettroni nell orbitale più esterno Numero del gruppo VALENZA
23 on la formazione del legame, gli atomi completano il livello esterno degli elettroni di valenza (configurazione( stabile dei gas nobili) Il legame è l unione di due o più atomi per il raggiungimento di uno stato di maggiore stabilità Formazione di legami = liberazione di energia Rottura di legami = consumo di energia
24
25
26
27
28
29
30
31
32
33 1. Gli atomi degli elementi delle molecole organiche possono formare un numero definito di legami (VALENZA);
34
35 1. Gli atomi degli elementi delle molecole organiche possono formare un numero definito di legami (VALENZA);
36 2. l atomo di carbonio può formare legami mediante una o più valenze con altri atomi di carbonio
37
38
39 Stato fondamentale Stato eccitato Stato ibridato sp 3 2p 2s 2p 2s sp 3 1s 1s 1s Promozione dell'elettrone Ibridazione
40
41
42
43
44
45 Stato fondamentale Stato eccitato Stato ibridato sp 2 2p 2s 2p 2s 2p sp 2 1s 1s 1s Promozione dell'elettrone Ibridazione
46
47
48 Stato fondamentale Stato eccitato Stato ibridato sp 2p 2s 2p 2s 2p sp 1s 1s 1s Promozione dell'elettrone Ibridazione
49
50
51 INDIARE LO STATO DI IBRIDAZIONE DEL ARBONIO NEI SEGUENTI OMPOSTI 1) sp 2 2) 3) O O sp 3 sp 3 sp 2 2 sp 2 O O O O O BENZENE AETONE VITAMINA (A. ASORBIO) 4) sp 3 l l l LOROFORMIO 5) 3 sp 2 O N O N 3 3 N N 6) O sp 2 O AFFEINA IBUPROFENE
52 ome rappresentare le molecole? Formula Molecolare (o Bruta) fornisce informazioni su: (Es. 2 6 O) Tipi di atomi presenti Rapporto tra i vari atomi Peso molecolare Formula di Struttura permette di determinare: Es. l l l Il tipo di connessione tra gli atomi La disposizione spaziale degli atomi presenti (Isomeri costituzionali) (onformeri e Stereoisomeri)
53 Bidimensionali Tridimensionali F. di Lewis F. ad Asta e Sfera F. ondensate F. Space Filling F. a Tratti F. uneo e Tratteggio F. Schematiche F. a avalletto F. Proiettive di Fisher F. Proiettive di Newman
54
55
56
57
58 2 4 l 2 formula bruta l l formule a tratti l l 3 l 2 formule condensate l 2 2 l ed ovviamente.
59 2 6 O formula bruta O O formule a tratti 3 2 O 3 O 3 formule condensate O ed ovviamente. O O
60 3 5 N 3 8 O
61 2 6 O
62 I Gruppi Funzionali sono dei gruppi di atomi con proprietà chimiche tipiche che caratterizzano la molecola che li contiene. Sono la parte REATTIVA della molecola O
63 IDROARBURI Alcani Gruppo Funzionale -- Alcheni Legame doppio Alchini Legame triplo omposti aromatici Gruppo fenile
64 OMPOSTI ON LEGAME σ Gruppo Funzionale Alogenuri alchilici (X = l, Br, F, I) -X (gruppo Legame alogeno) triplo Alcoli -O(gruppo idrossi) Eteri -OR(gruppo alcossi) Ammine -N 2 (gruppo ammino)
65 OMPOSTI ON LEGAME =O Gruppo Funzionale Aldeidi hetoni -=O (gruppo carbonilico) -=O (gruppo carbonilico) Acidi carbossilici Esteri -OO (gruppo carbossilico) -OOR (gruppo estereo) Ammidi -ON 2 -ONR -ONR 2 (gruppo ammidico) loruri acilici -Ol (cloruro acilico)
66 Indica quali gruppi funzionali sono presenti nelle seguenti molecole. 2 l O 3 O 3 O O 3 O 3 3 Alanina Acetone N 2 3 2
67
68 Idrocarburi Solo carbonio ed idrogeno Alifatici Aromatici Alcani Alcheni Alchini icloalifatici
69
70 Formula generale n2n+2
71 LASSIFIAZIONE ATOMI DI ARBONIO carbonio PROPANO 3 carbonio 1 carbonio METIL PROPANO carbonio ,2-DIMETIL PENTANO
72
73 OMUNE Es. Acido formico, Vanillina, Acido acetico, ecc. SISTEMATIA IUPA
74 IUPA International Union of Pure and Applied hemistry
75 Prefisso - Radice - Desinenza Dove stanno i sostituenti? Quanti atomi di carbonio? Quale famiglia? (Gruppi funzionali)
76 Nomenclatura di alcani semplici Formula generale: n 2n+2 In accordo con la convenzione IUPA, il nome chimico di un alcano è basato sulla lunghezza della catena principale. Il nome consta di una radice (che indica il numero di atomi di carbonio della catena principale), seguito dal suffisso ano che sta ad indicare che il gruppo funzionale è un alcano. Radice met et prop but pent es ept ott.. non dec N arboni Formula
77 Regole IUPA per la nomenclatura sistematica degli alcani ramificati 1. Per alcani ramificati: : la catena continua più lunga di atomi di carbonio determina il nome base dell alcano Nome base: esano Nome base: eptano
78 Metano 4 Metile 3 Un Gruppo Alchilico si forma rimuovendo un idrogeno da un alcano Etano Etile
79 3 2 Nome base: esano Sostituente: metile Nome base: eptano Sostituenti: etile e metile
80 2. Numerare gli atomi della catena, iniziando dall estremit estremità più vicina al primo sostituente (o catena laterale),, la cui posizione verrà individuata dal numero del carbonio della catena normale da cui tale sostituente si diparte Metilesano e non 4 - Metilesano
81 3. Quando sono presenti due o più sostituenti, la loro posizione viene individuata dal numero del carbonio della catena principale a cui c sono legati. La numerazione della catena normale è scelta in modo da dare ai sostituenti il numero più basso possibile. iò vale anche quando si verifica il caso in cui la 1 1 ramificazione avviene alla stessa distanza dalle due estremità della catena normale Etil- 2- Metileptano O 2 - Metil- 4- Etileptano e non 4- Etil- 6- Metileptano
82 5. Quando si possono individuare nel composto due catene normali della stessa lunghezza,, quella che da luogo al maggior numero di sostituenti definisce il nome base dell alcano alcano ,5-dimetil-4-propil eptano
83 4. Quando sono presenti sullo stesso atomo di carbonio due sostituenti DIVERSI il numero corrispondente è riportato due volte Br Bromo metil esano
84 Se invece i sostituenti sono IDENTII si usa il prefisso di-, tri-,, tetra-, ecc. I numeri sono separati da virgole. 2,3- Dimetilbutano ,2,4,4- Tetrametilpentano
85 , 3, 5 - Trimetilesano e non 2, 4, 5 - Trimetilesano
86
87 ,6- Dimetil ottano Br 3 2-Bromo-4-metil butano
88 Etli-3-metil eptano 1 3 3
89 Gruppi alchilici con 3 atomi di carbonio Propano Propile 3 3 Isopropile
90 Gruppi alchilici con 4 atomi di carbonio Butano Butile sec-butile
91 Gruppi alchilici con 4 atomi di carbonio Isobutano (2-Metilpropano) 3 3 Isobutile terz-butile
92 terz-butil-3-metil nonano isopropil-3-metil nonano
93
94 Gruppi alchilici con 3 atomi di carbonio Propano Propile 3 3 Isopropile
95 Gruppi alchilici con 4 atomi di carbonio Butano Butile sec-butile
96 Gruppi alchilici con 4 atomi di carbonio Isobutano (2-Metilpropano) Isobutile terz-butile
97 2,3,5-trimetil-4-propil eptano
98 5- isopropil-3,3,7-trimetildecano
99 3-etil-5-isobutil nonano
100 Idrocarburi Solo carbonio ed idrogeno Alifatici Aromatici Alcani Alcheni Alchini icloalifatici
101
102 I ILOALANI vengono nominati premettendo il termine ILO alla radice del nome. Formula Generale n 2n icloesano iclopentano iclopropano icloeptano
103 Regole IUPA per la nomenclatura sistematica dei cicloalcani 1. Se sull anello è presente un solo sostituente non è necessario indicare la sua posizione. 3 3 l 3 Isopropilcicloesano lorociclopentano Metilciclopropano
104 2. Se sono presenti due sostituenti si numera a partire dal sostituente che è 1 in ordine alfabetico, assegnando al secondo sostituente il numero più basso l Isopropil-2-metilcicloesano loro-3-etilciclopentano
105 3. Quando sono presenti tre o più gruppi,, l anello l è numerato a partire da quel sostituente che permette di assegnare agli altri i numeri più bassi possibile F l l Etil-2-fluoro-1-isopropilcicloesano l l ,4-Dicloro-2-etilciclopentano oppure 2,4-Dicloro-1-etilciclopentano
106 4. Se un sistema ciclico singolo è legato ad una catena alchilica con un numero di atomi di carbonio maggiore di quelli dell anello anello,, oppure quando sono legati 2 o più cicli, è bene chiamare i composti con il termine cicloalchilalcani ciclobutilpentano 1,3-Dicicloesilpropano
107
108 etil-3-metilcicloesano 3 3 Br 1-bromo-1-isopropil ciclopentano 3 3 1,1-dimetil cicloesano
109 l Br Br bromo-4-cloro-2-etil ciclopentano 2-bromo-4-cloro-1-etil ciclopentano
110 3 F F terz-butil-2-fluoro-4-propil cicloesano
111 ciclopentil-4-metil esano
112
113 Preparazioni Alcani ALANI Fonti Industriali Laboratorio Petrolio Gas naturale Idrogenazione degli alcheni Riduzione di alogenuri alchilici a)idrolisi reattivi di Grignard b) Riduzione con metalli e acidi opulazione di alogenuri alchilici con composti organometallici a)sintesi di orey - ouse b) Sintesi di Wurtz
114 Idrogenazione degli alcheni + Pt o Ni solvente Esempi + Pt o Ni 2 5 O,25 iclopentene iclopentano Pt o Ni Br 3 + Br O, Bromo propene 1 - Bromo propano
115 Riduzione di alogenuri alchilici a) riduzione con metalli ed acidi 2 R X + Zn R + ZnX 2 Esempi R = gruppi alchilici Zn, Br 2 - bromo butano o Bromuro di sec-butile Butano l Zn, loro eptano Eptano
116 Riduzione di alogenuri alchilici b) idrolisi dei reattivi di Grignard etere 2 O R X + Mg R Mg X etilico (o N 3 o 3 O) R I reattivi di Grignard sono composti ORGANOMETALLII, in cui, cioè, un atomo di carbonio è legato ad un atomo di metallo.tutti questi composti hanno una proprietà in comune: sono capaci di cedere un carbonio con i suoi elettroni. R : Mg + X - δ δ + d- d + R Mg Meccanismo: Esempio: 3 Mg X 3 2 : Mg+ X - X+ R : + O - + Mg 2+ + X - 2 R :O: 2 Mg O O + Mg + X esempio etere dry 3 2 Br+ Mg 3 2 MgBr 2 O 3 3
117 I Reagenti Organometallici contengono un atomo di carbonio legato OVALENTEMENTE ad un metallo δ δ M R M Metalli più comuni: M= Li, Mg, u Legame polare R Li R Mg X R u Li regenti alchil litio regenti alchilmagnesio (reattivi di Grignard) R regenti litio dialchil rame
118 I Reagenti Organometallici contengono un atomo di carbonio legato OVALENTEMENTE ad un metallo δ δ M R M Metalli più comuni: M= Li, Mg, u Legame polare R Li R Mg X R u Li regenti alchil litio regenti alchilmagnesio (reattivi di Grignard) R regenti litio dialchil rame
119 Riduzione di alogenuri alchilici b) idrolisi dei reattivi di Grignard etere 2 O R X + Mg R Mg X etilico (o N 3 o 3 O) R I reattivi di Grignard sono composti ORGANOMETALLII, in cui, cioè, un atomo di carbonio è legato ad un atomo di metallo.tutti questi composti hanno una proprietà in comune: sono capaci di cedere un carbonio con i suoi elettroni. R : Mg + X - δ δ + d- d + R Mg Meccanismo: Esempio: 3 Mg X 3 2 : Mg+ X - X+ R : + O - + Mg 2+ + X - 2 R :O: 2 Mg O O + Mg + X esempio etere dry 3 2 Br+ Mg 3 2 MgBr 2 O 3 3
120 opulazione di alogenuri alchilici con composti organometallici a) sintesi di orey - ouse etere R X + Li R Li etilico Alchillitio ui R 2 uli Litio dialchilrame R' X R' R + R u + Li X R' X X X 3 3 Al. Alchilico 1 Al. Alchilico 2 E' una reazione che, tramite la formazione di un legame carbonio- carbonio, permette di ottenere alcani con un numero di atomi di carbonio superiore a quello degli alogenuri alchilici di partenza. Meccanismo: Sebbene non sia stato ancora chiarito completamente, pare che il gruppo R si distacchi dal rame portandosi via una coppia di elettroni, con i quali poi si attacca al gruppo R', espellendo contemporaneamente l'alogenione.(sostituzione NULEOFILA ALIFATIA BIMOLEOLARE) esempio 3 Br 3 R u RLi 2 : uli + R' X R : 3 R' u Li X R 1 X 3 R R R etere dry Li 3 Li ui ( 3 ) 2 uli 3 ( 2 ) 4 2 Br 3 3 ( 2 ) 5 3
121 b) sintesi di Wurtz 2 R X + 2 Na R R + 2 NaX reattività di R X 1 > 2 >3 I composti sodioorganici sono molto reattivi tanto che, appena formatisi, reagiscono con l'alogenuro alchilico di partenza : tale reazione porta, dunque, solo ad ALANI SIMMETRII. Meccanismo: 1) R X + 2 Na + Na + X - δ+ δ Na 2) R Na + R X R R + Na + X - R esempio 2 3 Br 2 Na 3 3 solvente
122
123 INDIARE TUTTI I MODI PER PREPARARE L OTTANOL a) Idrogenazione degli alcheni + Pt o Ni solvente oppure Ni o Pt solvente
124 b) Riduzione con metalli e acidi l + Zn c) Idrolisi reattivi di Grignard l + Mg etere Mg l 2 O
125 d) Sintesi di Wurtz l + Na Na WURTZ l
126 e) Sintesi di orey-ouse l + Li Li ui 1-cloro pentano R 2 uli 2 uli u Li Br 1-bromo propano SN
127 Eseguire la seguente reazione Br bromo propano butano a) Riduzione con metalli e acidi Br Zn / bromo propano propano b) Idrolisi reattivi di Grignard Br Mg Mg Br 2 O bromo propano propano
128 c) Idrolisi reattivi di Grignard Br Mg Mg Br 2 O bromo propano propano d) Sintesi di Wurtz Br 1-bromo propano Na Na Br WURTZ esano 3 2
129 e) Sintesi di orey-ouse Br 1-bromo propano Li Li ui orey- ouse uli 2 3 I butano
130 Ma cosa si intende per REAZIONE IMIA? IUPA Processo di interconversione di sostanze chimiche REAGENTI PRODOTTI
131
132 Le reazioni dei composti organici riguardano quasi esclusivamente la scissione e la formazione di legami OVALENTI. Tale scissione può avvenire in due distinte maniere: A : B A. + B. A : - + B + A + + B : - OMOLISI ETEROLISI Formazione di legami = liberazione di energia Rottura di legami = consumo di energia
133 In base a ciò, le più comuni reazioni organiche possono essere distinte in: REAZIONI IONIE REAZIONI RADIALIE Scissione eterolitica Scissione omolitica Le reazioni che decorrono in più stadi procedono attraverso la formazione di INTERMEDI,, specie estremamente reattive e talvolta non isolabili. Essi possono essere così rappresentati:
134 Reazioni radicaliche: alogenazione degli alcani + l l hν o l + l Lenta al buio Veloce in presenza di luce Veloce al buio ma con riscaldamento L ossigeno è un inibitore della reazione
135 Stadio d inizio: luce l l 2 l Stadi di propagazione: l + l Stadi di terminazione: l l l + l 2 l l l
136 Br 2 luce Radicale 2 Br (97%) Radicale Br (3%) Br 2 3 luce Radicale Br 3 (tracce) Br Radicale 3 3 (>99%)
137 R' R' R > R > R > R'' Terziario (3 ) Secondario (2 ) Primario (1 ) Metile Stabilità crescente Un Radicale è tanto più stabile quanto più può delocalizzare il suo elettrone.
138
139
140 Alogenuri alchilici di interesse
141 F F F F F F F F F F TEFLON
142 l l l 3 DDT
143 R X X= -l, -Br, -F, -I prodotti di sostituzione prodotti di eliminazione composti organometallici
144 oncetto di reazione chimica Reazioni ioniche e radicaliche Una reazione radicalica: l alogenazione degli alcani Stabilità dei radicali Alogenuri alchilici
145 R Primario (1 ) R' X R Secondario (2 ) R' X R R'' Terziario (3 ) X
146 Sistema IUPA Si seguono le stesse regole viste per gli alcani. L alogeno viene considerato come un qualunque sostituente presente sulla catena dell alcano l 2- loro butano l Br 4- Bromo- 1- loro esano
147 Nomi comuni Assai usati nel caso di alogenuri più semplici. Il nome viene determinato dal gruppo alchilico seguito dal termine cloruro, ioduro, bromuro o fluoruro, a seconda dell alogeno presente l sec- butil cloruro o cloruro di sec- butile 3 3 Br Isopropil bromuro o bromuro di isopropile
148 Alogenazione degli alcani R X 2 + hν R X + X Addizione di acidi alogenidrici agli alcheni X + X
149 Dagli alcooli X = Br, l PX 3 = PBr 3, Pl 3 R O X o PX 3 R X Alcooli 1 meglio usare PX 3 o Br concentrato Alcooli 2 o 3 Usare indifferentemente PX 3 o X
150 Esempi O Alcool propilico PBr 3 oppure Br conc Br Bromuro di propile 3 O PBr 3 3 Br Alcool 1- fenil etilico 1- Bromo- 1- fenil etano
151 Addizione di alogeni agli alcheni o agli alchini X X X 2 + X X + 2 X 2 X X
152 R X X= -l, -Br, -F, -I prodotti di sostituzione prodotti di eliminazione composti organometallici
153 Alogenuri alchilici: Reazioni di Sostituzione La Reattività degli alogenuri alchilici è determinata dalla Polarità del legame -X nucleo 3 2 δ δ Br δ δ R X Nucleofilo= specie chimica affine al nucleo
154 Alogenuri alchilici: Reazioni di Sostituzione La Reattività degli alogenuri alchilici è determinata dalla Polarità del legame -X omuni reazioni di Sostituzione Nucleofila δ δ R X R-X R' R'OO N S RO 2 O O R' -R ALINO R'OOR ESTERE R-N R-S R-OR ETERE R-O R-O ALOOL
155 Si tratta di reazioni in cui un gruppo (gruppo uscente o nucleofugo) viene SOSTITUITO da un altro gruppo (nucleofilo) ETEROLISI δ δ R X Nu + R X R Nu+ X nucleofilo gruppo uscente
156 Nu + R X R Nu+ X NULEOFILO: ione o molecola capace di donare una coppia elettronica ad un altro atomo o ione per formare un nuovo legame covalente. Esempi:
157 Nu + R X R Nu+ X ALOGENURO ALILIO: substrato ideale grazie alla intensa polarizzazione del suo legame -X.
158 Nu + R X R Nu+ X GRUPPO USENTE O NULEOFUGO: sostituente capace di staccarsi sotto forma di ione o di molecola relativamente stabile e debolmente basico. Esempi:
159 ETEROLISI Nu + R X R Nu+ X nucleofilo gruppo uscente
160 Le sostituzioni nucleofile alifatiche possono avvenire attraverso due meccanismi principali: S N 2 e S N 1. S N 2 δ δ Nu + R X Nu R X R Nu + A + B D X S N 1 1) R X R + X 2) Nu + R R Nu A + B D
161 S N 2 δ solvente δ Nu + 3 R l + O 3 O + X Nu l R X R Nu + X O l O δ δ l stato di transizione O + l Nu: attacca SEMPRE da parte opposta al gruppo uscente
162 S N 2 δ solvente δ Nu + 3 R l + O 3 O + X Nu l R X R Nu + X O l O δ δ l stato di transizione O + l INVERSIONE DI ONFIGURAZIONE Nu: attacca SEMPRE da parte opposta al gruppo uscente
163 velocità = k [ 3 l] [O ] reazione del 2 ordine O δ δ l stato di transizione
164 3 l + O solvente 3 O + l
165 3 3 3 l + O solvente
166
167 Struttura del substrato (R-X) S N 2 Il substrato più reattivo sarà quello con il minore ingombro sterico Reattività crescente Metile > 1 1 > 2 2
168 O O 3 I Nucleofili N 2 O 3 O 3 3
169 3 solvente 3 O + 3 l 3
170 O O 3 I Nucleofili N 2 O 3 O 3 3
171 oncentrazione e forza del nucleofilo (solo S N 2) Nucleofilo: Specie chimica ricca di elettroni sufficientemente piccola da arrivare velocemente al substrato O O 3 N
172 oncentrazione e forza del nucleofilo (solo S N 2) Nucleofilicità: proprietà INETIA che misura la velocità con la quale il nucleofilo attacca il substrato Basicità: proprietà TERMODINAMIA che risulta in relazione con la posizione dell equilibrio acido / base GENERIAMENTE: Un nucleofilo anionico è sempre più forte del suo acido coniugato O > 2 O ; N 2 > N 3 ; OR >RO
173
174 Nu + R X R Nu+ X è una reazione bimolecolare avviene in un unico stadio (reazione concertata) O δ δ l stato di transizione avviene con inversione di configurazione R-X R-Nu il nucleofilo deve essere forte R-X deve essere metilico, 1 o 2 X deve essere un buon gruppo uscente
175
176 Natura del solvente Il solvente gioca un ruolo fondamentale nelle reazioni SN, poiché è capace di influenzare sia l ordine di nucleofilicità che la velocità dell intero processo reattivo. Polari protici ( 2 O; R O) S. polari protici: possiedono idrogeni legati ad atomi fortemente elettronegativi Polari aprotici (DMF, DMSO, acetone) S. polari aprotici: non possiedono idrogeni legati ad atomi fortemente elettronegativi. Il loro potere solvatante è in relazione ai doppietti elettronici liberi. Non solvatano gli anioni
177 O Solvente: acqua
178 O 3 3 Solvente: acetone
179 Natura del solvente Il solvente gioca un ruolo fondamentale nelle reazioni SN, poiché è capace di influenzare sia l ordine di nucleofilicità che la velocità dell intero processo reattivo. Polari protici ( 2 O; R O) S. polari protici: possiedono idrogeni legati ad atomi fortemente elettronegativi Polari aprotici (DMF, DMSO, acetone) S. polari aprotici: non possiedono idrogeni legati ad atomi fortemente elettronegativi. Il loro potere solvatante è in relazione ai doppietti elettronici liberi. Non solvatano gli anioni
180
181 Natura del solvente Il solvente gioca un ruolo fondamentale nelle reazioni SN, poiché è capace di influenzare sia l ordine di nucleofilicità che la velocità dell intero processo reattivo. Polari protici ( 2 O; R O) S. polari protici: possiedono idrogeni legati ad atomi fortemente elettronegativi Polari aprotici (DMF, DMSO, acetone) S. polari aprotici: non possiedono idrogeni legati ad atomi fortemente elettronegativi. Il loro potere solvatante è in relazione ai doppietti elettronici liberi. SN2 Non solvatano gli anioni
182 Struttura del substrato (R-X) oncentrazione e forza del nucleofilo (solo S N 2) Natura del guppo uscente Natura del solvente
183 Nucleofilo FORTE
184
185 Antidepressivo Antitubercolosi
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
R-X ALOGENURI ALCHILICI. F Cl Br I. Nomenclatura. In genere si indicano con. + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo
 ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
Capitolo 7 Composti organici alogenati
 himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
S N. Reazioni di Sostituzione Nucleofila. Nucleofilo: Nu: + C X C + Nu + X - Sostituzione Nucleofila:
 Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Diagramma di flusso degli idrocarburi
 Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
3. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola:
 . Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1
 REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
REAZIONI E LORO MECCANISMI
 REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Prof.ssa Stacca Prof.ssa Stacca
 La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Alogenuri alchilici. Alogenuri alchilici: funzioni. Varietà di funzione dei composti alogenati. Figura
 Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: nomenclatura Alogenuri alchilici o aloalcani Bromo Alogenuri alchilici: struttura
Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: nomenclatura Alogenuri alchilici o aloalcani Bromo Alogenuri alchilici: struttura
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
CHIMICA ORGANICA. Fabrizio Mancin
 IMIA ORGANIA Fabrizio Mancin Dipartimento di Scienze himiche Edificio himica Organica, II Piano, Stanza 5 tel. 049 8275666, e-mail: fabrizio.mancin@unipd.it, http://www.chimica.unipd.it/fabrizio.mancin
IMIA ORGANIA Fabrizio Mancin Dipartimento di Scienze himiche Edificio himica Organica, II Piano, Stanza 5 tel. 049 8275666, e-mail: fabrizio.mancin@unipd.it, http://www.chimica.unipd.it/fabrizio.mancin
GLI ALCANI. Michele Kodrič
 GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Alchini. Suffisso: -ino. d. H 3 CCH 2 CC CH
 Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
La Chimica Organica idrogeno carbonio azoto ossigeno composti covalenti catene di atomi di carbonio strutture covalenti e debolmente polarizzate
 LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F
 Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab.
 I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
Gruppi funzionali. La maggior parte delle molecole organiche oltre ai legami C-C e C-H possiedono: - Eteroatomi (O, N, Alogeni);
 --- himica rganica - SG --- --- himica rganica - SG --- Gruppi funzionali Il carbonio forma sempre 4 legami, con l eccezione di intermedi di reazione, che possono avere 3 legami, e dei carbeni, che hanno
--- himica rganica - SG --- --- himica rganica - SG --- Gruppi funzionali Il carbonio forma sempre 4 legami, con l eccezione di intermedi di reazione, che possono avere 3 legami, e dei carbeni, che hanno
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Nomenclatura. Gli idrocarburi alifatici
 Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Alogenuri Alchilici R-Cl R-Br R-I R-F
 Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
Chimica organica: gli idrocarburi Capitolo C2
 himica organica: gli idrocarburi apitolo 2 VERIFIA LE TUE SEZE 1 2 3 D 4 5 B 6 A 7 A 8 9 10 A 11 A 12 A 13 B 14 15 A 16 17 D 18 19 B 20 A 21 B 22 A 23 B 24 D 25 A 26 A 27 D 28 B 29 A 30 31 A 32 B 33 B
himica organica: gli idrocarburi apitolo 2 VERIFIA LE TUE SEZE 1 2 3 D 4 5 B 6 A 7 A 8 9 10 A 11 A 12 A 13 B 14 15 A 16 17 D 18 19 B 20 A 21 B 22 A 23 B 24 D 25 A 26 A 27 D 28 B 29 A 30 31 A 32 B 33 B
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
Gli idrocarburi e il petrolio
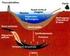 Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE
 CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Composti organici del silicio
 Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
Aldeidi e chetoni. Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni
 Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
1. COS È LA CHIMICA ORGANICA?
 Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
Proprietà fisiche di Alcani e Cicloalcani
 Proprietà fisiche di Alcani e Cicloalcani PUNTI DI EBOLLIZIONE DEGLI ALCANI sono regolati dalla entità delle forze di attrazione intermolecolari gli alcani sono composti non polari per cui non entrano
Proprietà fisiche di Alcani e Cicloalcani PUNTI DI EBOLLIZIONE DEGLI ALCANI sono regolati dalla entità delle forze di attrazione intermolecolari gli alcani sono composti non polari per cui non entrano
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Composti organici dello zolfo
 Complementi di Chimica rganica Composti organici dello zolfo He B C e i P Cl Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 Lo zolfo è un elemento della seconda riga della tavole periodica, è più grande, meno
Complementi di Chimica rganica Composti organici dello zolfo He B C e i P Cl Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 Lo zolfo è un elemento della seconda riga della tavole periodica, è più grande, meno
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
R OH. alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 )
 ALLI R Suffisso: -ol o olo R R R R R alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 ) Si sceglie la catena carboniosa più lunga contenente anche l ossidrile e si deduce il nome dell alcano
ALLI R Suffisso: -ol o olo R R R R R alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 ) Si sceglie la catena carboniosa più lunga contenente anche l ossidrile e si deduce il nome dell alcano
Alcheni: : struttura e reattività. Alcheni. Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n. H 2n. Alcheni in biologia
 Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
Sapienza, Università di Roma. Antonella Goggiamani
 Sapienza, Università di Roma CHIMICA ORGANICA Antonella Goggiamani antonella.goggiamani@uniroma1.it Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea in Scienze Naturali, canale M Z LEZIONI
Sapienza, Università di Roma CHIMICA ORGANICA Antonella Goggiamani antonella.goggiamani@uniroma1.it Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea in Scienze Naturali, canale M Z LEZIONI
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico
 Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
COMPOSTI AROMATICI. Formula C 6 H 6
 COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
Approccio alla CHIMICA ORGANICA. Chimica organica: gli idrocarburi I gruppi funzionali. Paolo Pistarà, Principi di chimica moderna - Tomo A ATLAS
 Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
Capitolo 8 Acidi Carbossilici e Derivati
 Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
 orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
L elemento carbonio e il suo più semplice composto con l idrogeno
 L elemento carbonio e il suo più semplice composto con l idrogeno L elemento carbonio è caratterizzato dal numero atomico Z=6, per cui la sua configurazione elettronica di base sarà: 6 C 1s 2 2s 2 2p 2
L elemento carbonio e il suo più semplice composto con l idrogeno L elemento carbonio è caratterizzato dal numero atomico Z=6, per cui la sua configurazione elettronica di base sarà: 6 C 1s 2 2s 2 2p 2
ETOILEPEDIA IL LEGAME CHIMICO
 IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
N H CH 3 H 3 C. Ammine. Struttura. Classificazione. Nomenclatura. Reattività
 Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Soluzioni degli esercizi di fine capitolo
 SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
