Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
|
|
|
- Biaggio Meli
- 8 anni fa
- Visualizzazioni
Transcript
1 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini che si formano nell interfaccia α 1 β 1 e α 2 β 2 e α 1 β 2 e α 2 β 1 2 catene globiniche α e 2 catene globiniche β Ogni globina α possiede 7 α-eliche Ogni globina β possiede 8 α-eliche Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
2 Graficamente la relazione esistente fra Y e po 2 è rappresentato da una CURVA DI OSSIGENAZIONE SIGMOIDALE, infatti il legame Hb/O 2 è di tipo COOPERATIVO. a) L AFFINITA DELL Hb PER L OSSIGENO AUMENTA MANO A MANO CHE LE MOLECOLE DI O 2 OCCUPANO I GRUPPI EME. Y 1, Hb semisatura, con minime variazioni di po 2 si deossigena e si ossigena quasi completamente Hb ad alta affinità, raggiunge la saturazione (STATO R) b) Esiste una cooperatività positiva fra i siti di legame dell ossigeno (fra i gruppi EME) c) Il legame di 1 molecola di O 2 ad un gruppo EME facilita il legame di altre molecole di O 2 agli altri gruppi EME Hb a bassa affinità, poco ossigenata STATO T p50 ~ 26 mm Hg, valore di po 2 che satura il 50% dei siti di legame dell Hb 20,0 40,0 60,0 80,0 po 2 (mmhg)
3 Qual è il vantaggio per un organismo vivente nel possedere una proteina respiratoria che lega l O 2 in modo cooperativo? 1,00 po 2 presente nei capillari tissutali po 2 presente nei capillari polmonari 0.75 Mb Hb Y 0.50 Hb rilascia e lega efficientemente l ossigeno ,0 40,0 60,0 80,0 100,0 po 2 (mmhg)
4 Il grado di ossigenazione della Hb dipende dalla po 2 e dalla K diss del complesso Hb(O 2 ) 4. Hb + 4[O 2 ] Hb[O 2 ] 4 Frazione di saturazione: Y = [Hb(O 2 ) 4 ] [Hb(O 2 ) 4 ] + [Hb] La Frazione di saturazione è legata alla po 2 e alla K diss secondo la seguente relazione: po 4 2 Y = K diss + po 4 2 n 4 po po 2 2 Y= Y = n 4 4 p50 + po 2 n K diss = p50 n Equazione di HILL
5 Le diverse emoproteine (per es. le diverse varianti di Hb prodotte a causa di mutazioni) possono avere un grado di cooperatività differente. Il termine n dà la misura della cooperatività In realtà in condizioni fisiologiche n H dell Hb è ~ 3 1< n H <n >> la proteina è Cooperativa e subisce una transizione fra stato a bassa affinità e stato ad alta affinità, per cui, nello stesso momento, avremmo una miscela di molecole di Hb completamente ossigenate, altre non ossigenate e altre parzialmente ossigenate. n H = 1 >> Non cooperativa (Mb) n H < 0 >> Cooperatività negativa po n 2 Y= n n p50 + po 2 La proteina è completamente cooperativa se il n dei siti di legame è uguale al coefficiente di Hill, cioè n = n H Se l Hb avesse n H = 4 vorrebbe dire che tutte le molecole di Hb sono o completamente legate o completamente dissociate e il legame con l O 2 è contemporaneo in tutti i siti.
6 STATO T Hb a bassa affinità α 1 β1 β2 α2 Transizione completa: quando sono occupati gli ultimi siti ormai tutte le molecole di Hb sono nella forma ad alta affinità STATO R ALTA AFFINITA + O 2 α 1 β1 α 1 β2 α2 β2 α 1 β1 β2 α2 β1 α2 α 1 β1 α 1 β1 β2 α2 β2 α2 α1 β1 α 1 β1 β2 α2 β2 α2 + O 2 α 1 β1 α 1 β1 β2 α2 β2 α2 + O 2 α 1 β1 + O 2 β2 α2 Legame con la molecola di O 2 >> cambia la struttura 3 aria della subunità legata CON LA PARZIALE OSSIGENAZIONE (almeno un sito occupato dall O 2 in ciascuno dei 2 dimeri αβ) L INTERA PROTEINA VA INCONTRO AD UNA MODIFICAZIONE DELLA SUA STRUTTURA 4 aria ASSUMENDO UNA STRUTTURA PIU DISPONIBILE AD ACCETTARE ALTRE MOLECOLE DI O 2.
7 La cooperatività di legame dell emoglobina è possibile perché lo stato di ossigenazione di un sito può essere comunicato agli altri siti attraverso un cambiamento della conformazione proteica dell Hb. L Hb passa da uno stato conformazionale a bassa affinità per l O 2 ad uno stato conformazionale ad alta affinità in funzione della concentrazione di O 2 (po 2 ). IL LEGAME CON L O 2 MODIFICA LA STRUTTURA DELLA PROTEINA DEOSSI-Hb >> stato T >> conformazione a bassa affinità OSSI-Hb >> stato R >> conformazione ad alta affinità PER PASSARE DALLO STATO A BASSA AFFINITÀ A QUELLO AD ALTA AFFINITÀ L HB SUBISCE UNA TRANSIZIONE ALLOSTERICA. L Hb è una proteina ALLOSTERICA.
8 L Hb è una proteina ALLOSTERICA. 1) Ha più siti di legame per il suo ligando 1) Il ligando è un effettore omoallosterico: occupando uno dei siti di legame della proteina influisce sull affinità degli altri siti liberi 2) Il legame proteina/ligando causa sempre una modificazione della struttura 3 aria e anche della struttura 4 aria della proteina che modifica la sua affinità nei confronti del ligando stesso. 3) Ha siti di legame per altri ligandi che agiscono come molecole regolatrici (effettori eteroallosterici) che influenzano l affinità della proteina verso il suo ligando 4) La modulazione e il legame proteina/effettori è sempre REVERSIBILE
9 Il legame fra l EME e l O 2 produce il cambiamento strutturale nella proteina. EME convesso EME appiattito His93 F8 His64, E7 Deossi-Hb: Il legame con l His prossimale trascina il Fe 2+ al di sopra del piano dell EME. Ossi-Hb: Il Fe 2+, è trascinato all interno dell EME per effetto del legame con l O 2, nel muoversi si tira dietro tutta l elica F e i segmenti adiacenti rompendo le interazioni che stabilizzavano lo stato T.
10 COSA SUCCEDE ALLA STRUTTURA DELLA EMOGLOBINA QUANDO AVVIENE LA TRANSIZIONE T R LA DEOSSI-HB (STATO T) È STABILIZZATA DA UNA RETE DI LEGAMI IDROGENO E INTERAZIONI IONICHE INTRA- E INTER- CATENA. Ponti salini molto importanti coinvolgono l His146 delle catene β che interagisce con l Asp94 e con la Lys40 delle catene α per mezzo del suo gruppo carbossi-terminale Lys C5 o 40 His HC3 o 146 Asp FG1 o 94 C-term.
11 Quando l Hb inizia a ossigenarsi, il legame EME/O 2 provoca un CAMBIAMENTO sia DELLA STRUTTURA TERZIARIA sia DELLA QUATERNARIA: un dimero α/β ruota e scivola rispetto all altro dimero α/β, questo movimento distorce e indebolisce la rete di legami H e ponti salini che stabilizza o stato T, le catene beta si avvicinano e si restringe la cavità centrale (146) (146) (146) Nello stato R l estremità C-terminale (His-146, HC3) delle catene β è ruotato verso la cavità centrale e non può più formare ponti salini
12 Effettori allosterici dell emoglobina O 2 H + (ph) CO 2 2,3-bisfosfoglicerato Regolano la transizione allosterica tra stato ad alta affinità e bassa affinità, aumentando l efficienza dell Hb nel rilasciare ossigeno ai tessuti. EFFETTO BOHR TESSUTI Hb 4O 2 + nh + Hb nh + + 4O 2 POLMONI La diminuzione di ph nei capillari abbassa l affinità dell Hb verso l O 2 rendendone più efficiente il rilascio. La p50 sale a ~ 40 mm Hg
13 COME SPIEGARE IL MECCANISMO DELL EFFETTO BOHR? La DEOSSI-Hb ha un pi più alto della OSSI-Hb, lega gli ioni H + con maggiore affinità. L Hb ha vari siti di legame per gli ioni H + come: 1) ammino-gruppi N-terminali delle catene alfa 2) His 146 (residuo C-terminale delle catene β). - + COO - terminale delle catene β + DEOSSI-Hb - (catene β) DEOSSI-Hb: His-146 (C-terminale delle catene β) ha un pka anormalmente elevato (> 7.2). Poiché nei capillari tissutali il ph scende a ~6.8: l His-146 si trova nella sua forma PROTONATA e forma un ponte salino intra-catena con l Asp 94, che stabilizza la forma T deossi.
14 OSSI-Hb: il pka dell His 146 scende a ~6.5 a causa della transizione dallo stato T a quello R Nel ph del sangue circolante (7.2) o dei capillari polmonari (7.6), l His sarà quasi del tutto DEPROTONATA e non formerà più il ponte salino. Questo contribuisce al cambiamento strutturale che favorisce l ossigenazione completa della Hb. H l94 C CH 2 l C=O l H l146 OOC C l CH 2 l H C N + CH C N H H l O -
15 ANIDRIDE CARBONICA (CO 2 ) La CO 2 viene liberata nel circolo sanguigno a livello periferico durante i processi metabolici cellulari. La CO 2 è trasportata nel sangue in tre forme: 1) disciolta: obbedisce alla Legge di Henry come l'o 2 ma è 20 volte più solubile di questo. In questa forma costituisce il 10% del gas liberato dal sangue venoso nel polmone. 2) Diffonde all interno degli eritrociti dove: CO 2 + H 2 O HCO H + (ANIDRASI CARBONICA) il bicarbonato quando aumenta di concentrazione diffonde dal globulo rosso al plasma scambiandosi con ioni Cl - Gli ioni H + si legano alla DEOSSI- Hb (che è meno acida della forma ossigenata ed è quindi un accettore di protoni migliore) Contribuisce all effetto BOHR e quindi al rilascio di O 2 e aumenta la capacità del sangue di trasportare H + e CO 2 (effetto HALDANE)
16
17 3) La CO 2 in parte si lega all Hb alle estremità N-terminali libere delle catene globiniche β formando CARBAMMATI = gruppi carichi negativamente che stabiliscono interazioni elettrostatiche con i residui di Arg-141 delle catene α stabilizzando la forma T
18 CONCENTRAZIONE CO 2 Effettore allosterico negativo per l Hb Y 1, Se la pco 2 diminuisce l affinità aumenta (p50 + bassa) Se la pco 2 aumenta l affinità diminuisce (p50 + alta) ,0 40,0 60,0 80,0 100,0 po 2 (mmhg)
19 2,3-bisfosfoglicerato È presente nel citoplasma degli eritrociti (ad una concentrazione ~ 5 mm), dove si forma a partire dall 1,3-bisfosfoglicerato (intermedio della glicolisi) È un effettore allosterico negativo, come gli ioni H + e la CO 2. Il 2,3-BPG si lega fortemente alla DEOSSI-Hb stabilizzando la forma T. Il 2,3-BPG si lega saldamente nella cavità centrale dell Hb fra le 4 catene globiniche nell Hb DEOSSIGENATA stabilizzandola e riducendo l affinità per l O 2
20 α 2 β β 2 α Il 2,3-BPG forma interazioni elettrostatiche con gruppi carichi positivamente che sporgono nella cavità centrale della DEOSSI-Hb: NH 3+ N-terminale ciò rafforza i ponti salini della forma T dell Hb. Lys-82 delle 2 catene β His-143 His-2 Quando l Hb lega la prima molecola di O 2 si innesca il cambiamento conformazionale che distrugge i ponti salini, la cavità centrale si restringe e il 2,3- BPG viene espulso.
21 Se negli eritrociti non ci fosse il 2,3-BPG la curva di ossigenazione dell Hb diventerebbe iperbolica, l Hb legherebbe l O 2 in modo non cooperativo Il 2,3-BPG modula l ossigenazione dell Hb in funzione delle condizioni ambientali in alta montagna >> basse po 2 adattamento alla carenza di ossigeno nei tessuti. Gli eritrociti aumentano la produzione di 2,3-BPG, >> diminuisce l affinità dell Hb per l O 2 (aumenta la p50) >> aumenta il rilascio di O 2 ai tessuti che altrimenti non sarebbero sufficientemente ossigenati
22 Emoglobina fetale: α 2 γ 2 Le catene γ hanno un residuo di Ser al posto dell His-143, manca una coppia di interazione ionica che stabilizza il complesso 2,3-BPG-deossiHb
23 Le mutazioni alterano la struttura e la funzione dell'emoglobina Sono state scoperte più di 1000 forme mutanti dell Hb, spesso con 1 unica sostituzione amminoacidica, non tutte le varianti emoglobiniche conducono a sintomi clinici. ca il 5% della popolazione mondiale possiede almeno una variante emoglobinica
24 Eritrociti umani normali Eritrociti umani falciformi Nell anemia falciforme viene prodotta Hb-S nella quale il residuo di Glu in posizione 6 delle catene β è sostituito da un residuo di Val. Nella Deossi-Hb-S questo residuo di Val costituisce un punto appiccicoso esposto sulla superficie del tetramero, infatti va ad inserirsi in una tasca idrofobica situata nelle subunità β di un altro tetramero: l Hb polimerizza, forma delle fibre insolubili
25 La deossiemoglobina S: la Val 6 mutante interagisce con la Phe 85
26 Struttura di una fibra di deossiemoglobina S
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Legano reversibilmente l OSSIGENO. La mioglobina (monomerica) è presente nelle cellule muscolari. L emoglobina (tetramerica) è presente negli
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Legano reversibilmente l OSSIGENO. La mioglobina (monomerica) è presente nelle cellule muscolari. L emoglobina (tetramerica) è presente negli
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto di CO 2. ed effetto Bohr. . La CO 2. nei tessuti produce CO 2. Il consumo di O 2. deve essere rimossa e portata ai polmoni (o alle branchie)
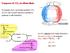 Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI
 Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Dipendenza della Solubilità dalla temperatura
 SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
FISIOLOGIA DELLA RESPIRAZIONE
 FISIOLOGIA DELLA RESPIRAZIONE SCAMBIO E TRASPORTO DEI GAS La composizione dell aria alveolare differisce rispetto all aria ambiente. A livello alveolare si verifica la continua diffusione della del sangue
FISIOLOGIA DELLA RESPIRAZIONE SCAMBIO E TRASPORTO DEI GAS La composizione dell aria alveolare differisce rispetto all aria ambiente. A livello alveolare si verifica la continua diffusione della del sangue
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine:
 La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
Mioglobina Emoglobina
 Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Modulo 4. Una proteina in azione
 Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
EME (Fe-PROTOPORFIRINA IX)
 EME (Fe-PROTOPORFIRINA IX) 1,3,5,8-tetrametil 2,4-divinil 6,7-dipropionil-porfirina 1 Il ferro può formare sei legami di coordinazione 4 con gli azoti dell anello tetrapirrolico 2 perpendicolari al piano
EME (Fe-PROTOPORFIRINA IX) 1,3,5,8-tetrametil 2,4-divinil 6,7-dipropionil-porfirina 1 Il ferro può formare sei legami di coordinazione 4 con gli azoti dell anello tetrapirrolico 2 perpendicolari al piano
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Eventi successivi alla comparsa dell O 2
 Eventi successivi alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione dell ossigeno: infatti,
Eventi successivi alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione dell ossigeno: infatti,
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
Funzioni dell apparato respiratorio
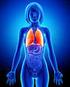 Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Mioglobina Emoglobina
 Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma
 Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
P aria (livello del mare) = 760 mmhg. Composizione: O 2 : 20.84% N 2 : 78.62% CO 2 : 0.04% po 2 = 159 mmhg. pn 2 = 597mmHg. pco 2 = 0.
 Scambi alveolari Aria atmosferica = miscela di gas (principalmente O 2, N 2, CO 2 ) La velocità di diffusione di un gas (quantità di gas che diffonde nell unità di tempo) è direttamente proporzionale alla
Scambi alveolari Aria atmosferica = miscela di gas (principalmente O 2, N 2, CO 2 ) La velocità di diffusione di un gas (quantità di gas che diffonde nell unità di tempo) è direttamente proporzionale alla
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Ripiegamento e stabilità delle proteine
 Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno
 Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
GLI ENZIMI ALLOSTERICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM)
 Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Relazione struttura-funzione
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica
 Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica Anno accademico 2009/2010 I anno, II semestre CdL Infermieristica e Fisioterapia PATOLOGIA GENETICA Oggetto di studio
Elementi di Patologia Generale Dott.ssa Samantha Messina Lezione: Patologia Genetica Anno accademico 2009/2010 I anno, II semestre CdL Infermieristica e Fisioterapia PATOLOGIA GENETICA Oggetto di studio
MACROECONOMIA DELLE ECONOMIE APERTE: CONCETTI E FONDAMENTI. Harcourt Brace & Company
 MACROECONOMIA DELLE ECONOMIE APERTE: CONCETTI E FONDAMENTI Economie aperte o chiuse Un economia chiusa è un economia che non interagisce con altre economie nel mondo. Non ci sono esportazioni, non ci sono
MACROECONOMIA DELLE ECONOMIE APERTE: CONCETTI E FONDAMENTI Economie aperte o chiuse Un economia chiusa è un economia che non interagisce con altre economie nel mondo. Non ci sono esportazioni, non ci sono
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Farmacocinetica dell escrezione dei farmaci nel latte. I neurotrasmettitori nella moderna diagnostica. Piperazina e suoi derivati
 Farmacocinetica dell escrezione dei farmaci nel latte I neurotrasmettitori nella moderna diagnostica Piperazina e suoi derivati dr. Angelo Marzìa FARMACOCINETICA DELL ESCREZIONE DEI FARMACI NEL LATTE
Farmacocinetica dell escrezione dei farmaci nel latte I neurotrasmettitori nella moderna diagnostica Piperazina e suoi derivati dr. Angelo Marzìa FARMACOCINETICA DELL ESCREZIONE DEI FARMACI NEL LATTE
Le proteine che legano ossigeno:
 Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO
 QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
STRUTTURA E FUNZIONE
 STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Relazioni statistiche: regressione e correlazione
 Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Emoglobina e mioglobina
 Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA)
 SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
SCIENZE. Il Sistema Circolatorio. Chi sono? il testo:
 01 Chi sono? Uno è piccolo come una mosca, l altro è grande come un giocatore di basket, ma in tutti gli esseri viventi il cibo che essi mangiano (assorbono) e l aria (ossigeno) che respirano devono andare
01 Chi sono? Uno è piccolo come una mosca, l altro è grande come un giocatore di basket, ma in tutti gli esseri viventi il cibo che essi mangiano (assorbono) e l aria (ossigeno) che respirano devono andare
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
Farmacodinamica II. Mariapia Vairetti. Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare
 Farmacodinamica II Mariapia Vairetti Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare Processo di riconoscimento fra farmaco e recettore TIPI DI
Farmacodinamica II Mariapia Vairetti Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare Processo di riconoscimento fra farmaco e recettore TIPI DI
gruppo prostetico) Cromoproteine Legare l ossigeno Impedire che ossidi altre sostanze Cedere O 2 in particolari e ben definite condizioni
 Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
INTEGRATORE E DERIVATORE REALI
 INTEGRATORE E DERIVATORE REALI -Schemi elettrici: Integratore reale : C1 R2 vi (t) R1 vu (t) Derivatore reale : R2 vi (t) R1 C1 vu (t) Elenco componenti utilizzati : - 1 resistenza da 3,3kΩ - 1 resistenza
INTEGRATORE E DERIVATORE REALI -Schemi elettrici: Integratore reale : C1 R2 vi (t) R1 vu (t) Derivatore reale : R2 vi (t) R1 C1 vu (t) Elenco componenti utilizzati : - 1 resistenza da 3,3kΩ - 1 resistenza
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria
 Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
IC Brescia Centro 3 Via dei Mille, 4b - Brescia Novembre 2012
 Ministero dell Istruzione, dell Università e della Ricerca Ufficio Scolastico Provinciale di Brescia GLIP di Brescia CTRH DI Brescia Incontri di formazione sul Piano Educativo Individualizzato IC Brescia
Ministero dell Istruzione, dell Università e della Ricerca Ufficio Scolastico Provinciale di Brescia GLIP di Brescia CTRH DI Brescia Incontri di formazione sul Piano Educativo Individualizzato IC Brescia
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare.
 Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ
 Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O 2 dagli alveoli al sangue e della
 Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O 2 dagli alveoli al sangue e della CO 2 in direzione opposta. L aria che respiriamo è una
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O 2 dagli alveoli al sangue e della CO 2 in direzione opposta. L aria che respiriamo è una
Trasporto gas nel sangue
 Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE
 FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
