Crisi della Fisica Classica & Fisica Quantistica
|
|
|
- Lamberto Lamberti
- 5 anni fa
- Visualizzazioni
Transcript
1 Crisi della Fisica Classica & Fisica Quantistica Guido Montagna Dipartimento di Fisica, Università di Pavia & INFN, Sezione di Pavia February 11, 2018 G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 1 / 14
2 Spettri e Modelli Atomici: Atomo di Bohr G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 2 / 14
3 Spettri atomici: emissione ed assorbimento Quando si analizza la radiazione emessa o assorbita dai vari stati della materia, si osservano ben precisi comportamenti che caratterizzano lo spettro della sostanza oggetto di studio. 1. Spettri continui: successione continua di lunghezze d onda. Emessi da solidi, liquidi o gas densi a temperatura sufficientemente elevata. 2. Spettri discreti: successione discreta di lunghezze d onda (righe spettrali). Emessi da gas rarefatti resi incandescenti o posti in un tubo a cui è applicata una d.d.p. (spettro di emissione) o da gas rarefatti freddi esposti a sorgente luminosa continua (spettro di assorbimento) G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 3 / 14
4 Spettri atomici: caratteristiche In un gas monoatomico, gli spettri a righe sono un fenomeno caratteristico del singolo atomo La lunghezza d onda delle righe di emissione coincide con la lunghezza d onda delle righe di assorbimento Gli spettri a righe sono quindi una caratteristica tipica di ogni elemento chimico G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 4 / 14
5 Esempi di spettri atomici L analisi spettroscopica è la base dell identificazione degli elementi G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 5 / 14
6 Atomo di idrogeno: formula di Balmer Formula di Balmer Rydberg ( 1 1 λ = R H m 2 1 ) n 2 n, m N, n > m R H costante di Rydberg = cm 1 m = 1 n = 2, 3, 4,... serie di Lyman m = 2 n = 3, 4, 5,... serie di Balmer m = 3 n = 4, 5, 6,... serie di Paschen G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 6 / 14
7 Modelli atomici: esperimento di Geiger e Marsden Modello di Thomson (a panettone): cariche positive e negative distribuite uniformemente entro sfera di raggio R m Geiger e Marsden ( ): particelle α contro bersaglio sottilissimo G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 7 / 14
8 Modello di Rutherford e sue difficoltà Modello di atomo nucleare o planetario: piccolo nucleo centrale pesante e carico positivamente attorno al quale ruotano elettroni legati da attrazione coulombiana gli elettroni, nel loro moto di rivoluzione, essendo carichi ed accelerati, emettono radiazione e.m., avvicinandosi con continuità al nucleo l atomo dovrebbe emettere uno spettro continuo di radiazioni gli elettroni, irraggiando, perdono energia e collassano sul nucleo atomico vita media dell atomo 10 9 s Le leggi della fisica classica, applicate a livello microscopico, contrastano con la stabilità della materia e non spiegano la natura a righe degli spettri atomici G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 8 / 14
9 Modello di Bohr: postulati generali Bohr ( ) Livelli energetici Per gli elettroni in un atomo esistono orbite privilegiate stabili (stati stazionari) sulle quali l elettrone non irraggia. Queste orbite sono discrete e discreti sono i corrispondenti valori (negativi) dell energia, detti livelli energetici. Emissione e assorbimento di radiazione L emissione (o assorbimento) di radiazione è dovuta alla transizione di un elettrone da un livello di energia superiore ad uno di energia inferiore (o viceversa), con emissione (o assorbimento) di un fotone di energia E i E f E = hν G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 9 / 14
10 Ipotesi di Bohr per atomo di idrogeno Restrizione a orbite circolari Per l elettrone, sono permesse solo orbite circolari m e a = m e v 2 r = e2 4πɛ 0 r 2 Regola di quantizzazione del momento angolare Il modulo del momento angolare L = r p è quantizzato m e v r = n h 2π n = 1, 2, 3,... Si ottiene allora che le orbite sono quantizzate e i livelli energetici E n dipendono da n secondo la legge di proporzionalità E n 1/n 2, spiegando così la legge di Balmer il valore della costante di Rydberg è dato da R H = 2π2 m e e 4 c h 3 (4πɛ 0) 2 in buon accordo con il valore sperimentale cm 1 G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 10 / 14
11 Spettro dell atomo di idrogeno Si ricava inoltre ɛ0 h2 r 1 = = Å Raggio di Bohr π m e e2 E 1 = R H h c = 13.6 ev Energia dello stato fondamentale G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 11 / 14
12 Esperimento di Franck e Hertz: dispositivo Franck e Hertz (1914) in un tubo contenente vapore di mercurio a bassa pressione sono posti tre elettrodi un catodo caldo che emette elettroni (filamento) una griglia forata a potenziale positivo variabile rispetto al filamento una placca (anodo) a potenziale leggermente negativo rispetto alla griglia un amperometro misura la corrente che raggiunge la placca, al variare della d.d.p. fra filamento e griglia G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 12 / 14
13 Franck e Hertz: risultato sperimentale Al variare della d.d.p. che accelera gli elettroni fra filamento e griglia la corrente di placca registrata aumenta, fino a raggiungere un picco per poi cadere bruscamente per un valore di d.d.p. pari a 4.9 V e quindi tornare a crescere, per calare di nuovo, regolarmente a multipli di 4.9 V G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 13 / 14
14 Franck e Hertz: interpretazione Evidenza non spettroscopica dell esistenza degli stati stazionari Se gli urti degli elettroni con gli atomi di mercurio sono elastici, allora gli elettroni non perdono energia raggiungono il massimo di energia nei pressi della griglia riescono a vincere il campo antagonista dovuto alla d.d.p. fra griglia e placca la corrente di placca cresce al crescere della d.d.p. fra filamento e griglia non appena la d.d.p. genera un energia per gli elettroni superiore all energia di eccitazione E 2 E 1 (E 2 = energia del primo livello eccitato dell atomo di mercurio, E 1 = energia dello stato fondamentale) gli urti vicino alla griglia diventano anelastici gli elettroni perdono quasi tutta la loro energia nell eccitazione dell atomo e non superano il campo antagonista la corrente cala vistosamente per E el. = e V E 2 E 1 quando la d.d.p. supera 2 (E 2 E 1) si hanno due urti anelastici la corrente cala di nuovo per E el. = e V 2 (E 2 E 1) I vistosi cali di corrente sono dovuti agli urti anelastici fra elettroni e atomi di mercurio e alla natura discreta dell energia associata agli stati stazionari dell atomo di mercurio G. Montagna, Università di Pavia & INFN (Dipartimento Crisi della di Fisica, Università Classica di Pavia & INFN, Sezione February di Pavia 11, 2018 ) 14 / 14
Problemi con l'atomo. Significato delle righe spettrali. Modello dell'atomo
 Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Il modello di Bohr. Lezioni d'autore di Giorgio Benedetti
 Il modello di Bohr Lezioni d'autore di Giorgio Benedetti VIDEO Gli spettri di emissione Nel 1859 il fisico G.R. Kirchoff scoprì che ogni elemento chimico presenta uno spettro di emissione caratteristico,
Il modello di Bohr Lezioni d'autore di Giorgio Benedetti VIDEO Gli spettri di emissione Nel 1859 il fisico G.R. Kirchoff scoprì che ogni elemento chimico presenta uno spettro di emissione caratteristico,
STRUTTURA ATOMICA. Per lo studio della struttura dell atomo ci si avvale della Spettroscopia.
 STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
1 3 STRUTTURA ATOMICA
 1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
Crisi della Fisica Classica & Fisica Quantistica
 Crisi della Fisica Classica & Fisica Quantistica Guido Montagna Dipartimento di Fisica, Università di Pavia & INFN, Sezione di Pavia February 8, 2018 G. Montagna, Università di Pavia & INFN (Dipartimento
Crisi della Fisica Classica & Fisica Quantistica Guido Montagna Dipartimento di Fisica, Università di Pavia & INFN, Sezione di Pavia February 8, 2018 G. Montagna, Università di Pavia & INFN (Dipartimento
La radiazione elettromagnetica. aumento della frequenza n della radiazione aumento dell energia E della radiazione
 La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
L atomo di Bohr e i raggi X
 L atomo di Bohr e i raggi X Corsi laboratorio per le scuole superiori gennaio 017 Prof. Federico Boscherini Dipartimento di Fisica e Astronomia Università di Bologna federico.boscherini@unibo.it www.unibo.it/docenti/federico.boscherini
L atomo di Bohr e i raggi X Corsi laboratorio per le scuole superiori gennaio 017 Prof. Federico Boscherini Dipartimento di Fisica e Astronomia Università di Bologna federico.boscherini@unibo.it www.unibo.it/docenti/federico.boscherini
L'esperimento di Franck-Hertz
 L'esperimento di Franck-Hertz STAGES ESTIVI (11 15 Giugno 2012) LNF MATTEO MASCOLO Università di Roma Tor Vergata (Breve) riepilogo delle puntate precedenti... 1884 - Johann Balmer studia le righe di assorbimento
L'esperimento di Franck-Hertz STAGES ESTIVI (11 15 Giugno 2012) LNF MATTEO MASCOLO Università di Roma Tor Vergata (Breve) riepilogo delle puntate precedenti... 1884 - Johann Balmer studia le righe di assorbimento
Struttura della materia
 Struttura della materia 1. L elettrone 2. Effetto Compton 3. Struttura dell atomo XIV - 0 Rapporto carica/massa dell elettrone Esperimento di Thomson: raggi catodici. Fascio non deflesso: Quando B=0: con
Struttura della materia 1. L elettrone 2. Effetto Compton 3. Struttura dell atomo XIV - 0 Rapporto carica/massa dell elettrone Esperimento di Thomson: raggi catodici. Fascio non deflesso: Quando B=0: con
Introduzione al corso. Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora...
 Introduzione al corso Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora... Legge di Boyle (1662)-> La pressione di un gas cresce quando decresce
Introduzione al corso Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora... Legge di Boyle (1662)-> La pressione di un gas cresce quando decresce
Il metodo scientifico
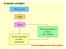 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Spettro elettromagnetico
 Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Unità Didattica 3. L atomo di idrogeno
 Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
ESPERIENZA DI FRANCK E HERTZ
 Scaltritti Matteo Caruggi Federico ESPERIENZA DI FRANCK E HERTZ SCOPO DELL ESPERIENZA: L obiettivo di questa esperienza è quello di osservare e misurare la quantizzazione dei livelli energetici nell atomo
Scaltritti Matteo Caruggi Federico ESPERIENZA DI FRANCK E HERTZ SCOPO DELL ESPERIENZA: L obiettivo di questa esperienza è quello di osservare e misurare la quantizzazione dei livelli energetici nell atomo
La teoria atomistica
 La teoria atomistica Joseph John Thomson Fisico britannico È noto per aver scoperto nel 1897 la particella di carica negativa: l'elettrone Ebbe come studente Rutherford Vinse il Nobel per la fisica nel
La teoria atomistica Joseph John Thomson Fisico britannico È noto per aver scoperto nel 1897 la particella di carica negativa: l'elettrone Ebbe come studente Rutherford Vinse il Nobel per la fisica nel
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Atomi a più elettroni
 Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
Produzione dei raggi X
 I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
L atomo di Bohr. Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913)
 L atomo di Bohr Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913) L atomo di Bohr L atomo di idrogeno presenta un solo elettrone 1. L elettrone
L atomo di Bohr Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913) L atomo di Bohr L atomo di idrogeno presenta un solo elettrone 1. L elettrone
FISICA QUANTISTICA LIMITI AL MODELLO ATOMICO DI RUTHERFORD. e - Per spiegare la disposizione degli elettroni nell atomo (STRUTTURA ELETTRONICA)
 LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA
 LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
MODELLO PLANETARIO ATTORNO AL NUCLEO ORBITANO GLI ELETTRONI COME PIANETI INTORNO AL SOLE TUTTAVIA
 MODELLO PLANETARIO ATTORNO AL NUCLEO ORBITANO GLI ELETTRONI COME PIANETI INTORNO AL SOLE TUTTAVIA LASCIAVA IRRISOLTI MOLTI PROBLEMI RIGUARDANTI IN PARTICOLARE LA DISPOSIZIONE DEGLI ELETTRONI INTORNO AL
MODELLO PLANETARIO ATTORNO AL NUCLEO ORBITANO GLI ELETTRONI COME PIANETI INTORNO AL SOLE TUTTAVIA LASCIAVA IRRISOLTI MOLTI PROBLEMI RIGUARDANTI IN PARTICOLARE LA DISPOSIZIONE DEGLI ELETTRONI INTORNO AL
Modelli atomici Modello atomico di Rutheford Per t s d u i diare la t s rutt ttura t a omica Ruth th f or (
 Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
TERMODINAMICA CLASSICA E LE ORIGINI DELLA TEORIA QUANTISTICA
 TERMODINAMICA CLASSICA E LE ORIGINI DELLA TEORIA QUANTISTICA (SISTEMI IN EQUILIBRIO TERMICO) LEZIONE N.2 Fisica moderna 1 SPETTRO CORPO NERO Legge di Stefan (1879)-Boltzmann Intensità di potenza totale
TERMODINAMICA CLASSICA E LE ORIGINI DELLA TEORIA QUANTISTICA (SISTEMI IN EQUILIBRIO TERMICO) LEZIONE N.2 Fisica moderna 1 SPETTRO CORPO NERO Legge di Stefan (1879)-Boltzmann Intensità di potenza totale
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
P. Sapia Università della Calabria. a.a. 2009/10
 FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9
 Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
La struttura della materia
 La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica
 ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
mvr = n h e 2 r = m v 2 e m r v = La configurazione elettronica r = e 2 m v 2 (1) Quantizzazione del momento angolare (2) 4 πε.
 La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
Crisi della Fisica Classica & Fisica Quantistica
 Crisi della Fisica Classica & Fisica Quantistica Guido Montagna Dipartimento di Fisica, Università di Pavia & INFN, Sezione di Pavia February 5, 2018 G. Montagna, Università di Pavia & INFN (Dipartimento
Crisi della Fisica Classica & Fisica Quantistica Guido Montagna Dipartimento di Fisica, Università di Pavia & INFN, Sezione di Pavia February 5, 2018 G. Montagna, Università di Pavia & INFN (Dipartimento
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
ATOMO. Avogadro (1811) Volumi uguali di gas diversi contengono un ugual numero di MOLECOLE (N A =6,022*10 23 )
 ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
Risultato: ELABORAZIONE della MECCANICA QUANTISTICA e sua applicazione sistematica ai nuovi fenomeni
 Tra la fine del XIX e inizio del XX secolo una serie di fenomeni non trovano interpretazione adeguata, basata su fisica classica (meccanica, elettromagnetismo, ottica e termodinamica) Essi risultarono
Tra la fine del XIX e inizio del XX secolo una serie di fenomeni non trovano interpretazione adeguata, basata su fisica classica (meccanica, elettromagnetismo, ottica e termodinamica) Essi risultarono
p e c = ev Å
 Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
La crisi della fisica classica
 Il problema del corpo nero e l ipotesi di Planck La crisi della fisica classica All inizio del XX secolo ancora due problemi non trovavano spiegazione all interno delle teorie dell elettromagnetismo e
Il problema del corpo nero e l ipotesi di Planck La crisi della fisica classica All inizio del XX secolo ancora due problemi non trovavano spiegazione all interno delle teorie dell elettromagnetismo e
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
La Struttura degli Atomi
 La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
Lezione n. 13. Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo. di idrogeno. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
Chimica Fisica Biotecnologie sanitarie Lezione n. 13 Radiazione elettromagnetica Il modello di Bohr Lo spettro dell atomo di idrogeno Antonino Polimeno 1 Radiazione elettromagnetica (1) - Rappresentazione
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
the power of ten Prof.ssa Patrizia Gallucci
 https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
Fisica atomica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
LUCE E ONDE ELETTROMAGNETICHE
 LUCE E ONDE ELETTROMAGNETICHE QUASI TUTTO QUELLO CHE SAPPIAMO SULLA STRUTTURA DELL ATOMO DERIVA DALL ANALISI DELLA LUCE EMESSA O ASSORBITA DALLE SOSTANZE CHI FU IL PRIMO AD ACCORGERSI CHE I SINGOLI ELEMENTI
LUCE E ONDE ELETTROMAGNETICHE QUASI TUTTO QUELLO CHE SAPPIAMO SULLA STRUTTURA DELL ATOMO DERIVA DALL ANALISI DELLA LUCE EMESSA O ASSORBITA DALLE SOSTANZE CHI FU IL PRIMO AD ACCORGERSI CHE I SINGOLI ELEMENTI
Radiazioni ionizzanti
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Radiazioni ionizzanti 11/3/2005 Struttura atomica Atomo Nucleo Protone 10 10 m 10 14 m 10 15 m ev MeV GeV 3 3,0 0,3 0 0 0 Atomo Dimensioni lineari
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Radiazioni ionizzanti 11/3/2005 Struttura atomica Atomo Nucleo Protone 10 10 m 10 14 m 10 15 m ev MeV GeV 3 3,0 0,3 0 0 0 Atomo Dimensioni lineari
crisi della fisica classica Esercizi
 Esercizi Crisi della fisica classica Se un elettrone viene colpito da un fotone, può assorbirlo senza emetterne un altro? Nell urto, l elettrone cambia velocità, quindi ha un accelerazione. Le equazioni
Esercizi Crisi della fisica classica Se un elettrone viene colpito da un fotone, può assorbirlo senza emetterne un altro? Nell urto, l elettrone cambia velocità, quindi ha un accelerazione. Le equazioni
Storia della meccanica quantistica
 Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
La struttura dell atomo
 La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
(c) laura Condorelli 2009
 Legge di Wien Emissione del corpo nero Il numero massimo di radiazione emmesse è chiamato lambda max. Quando la temperatura è minore, lambda max è maggiore. Quando la temperatura è maggiore, lambda max
Legge di Wien Emissione del corpo nero Il numero massimo di radiazione emmesse è chiamato lambda max. Quando la temperatura è minore, lambda max è maggiore. Quando la temperatura è maggiore, lambda max
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI
 MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
MODELLO ATOMICO DI BOHR - ULTERIORI APPROFONDIMENTI Se riscaldiamo un qualsiasi elemento chimico ponendolo ad esempio su una fiamma, notiamo che esso emette un colore caratteristico. Ad esempio riscaldando
Sommario della lezione 2. Materia e definizioni. Struttura dell atomo
 Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
1. L'esperienza di Rutherford Dal Seicento all'ottocento si sviluppò lo studio delle strutture microscopiche, grazie ai microscopi ottici.
 Il modello atomico 1. L'esperienza di Rutherford Dal Seicento all'ottocento si sviluppò lo studio delle strutture microscopiche, grazie ai microscopi ottici. I microscopi ottici, tuttavia, non vedono attraverso
Il modello atomico 1. L'esperienza di Rutherford Dal Seicento all'ottocento si sviluppò lo studio delle strutture microscopiche, grazie ai microscopi ottici. I microscopi ottici, tuttavia, non vedono attraverso
Modelli atomici. Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle.
 Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
dualismo onda corpuscolo
 dualismo onda corpuscolo Gli effetti che abbiamo visto finora sono manifestazioni della natura corpuscolare della radiazione elettromagnetica (e quindi della luce) Naturalmente la natura corpuscolare non
dualismo onda corpuscolo Gli effetti che abbiamo visto finora sono manifestazioni della natura corpuscolare della radiazione elettromagnetica (e quindi della luce) Naturalmente la natura corpuscolare non
STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA
 pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
Fisica Moderna e contemporanea
 Fisica Moderna e contemporanea SSIS Puglia Prof. Luigi Schiavulli luigi.schiavulli@ba.infn.it Dipartimento Interateneo di Fisica Michelangelo Merlin 02/02/2006 1 Sommario Quadro riassuntivo sulla Fisica
Fisica Moderna e contemporanea SSIS Puglia Prof. Luigi Schiavulli luigi.schiavulli@ba.infn.it Dipartimento Interateneo di Fisica Michelangelo Merlin 02/02/2006 1 Sommario Quadro riassuntivo sulla Fisica
A Z. L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone. +1e e.
 L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
Un introduzione alla meccanica quantistica per le secondarie
 1 / 252 Un introduzione alla meccanica quantistica per le secondarie Camillo Imbimbo Genova, Gen-Feb, 2016 Progetto Lauree Scientifiche Dipartimento di Fisica dell Università di Genova https://www.ge.infn.it/
1 / 252 Un introduzione alla meccanica quantistica per le secondarie Camillo Imbimbo Genova, Gen-Feb, 2016 Progetto Lauree Scientifiche Dipartimento di Fisica dell Università di Genova https://www.ge.infn.it/
Enrico Silva - diritti riservati - Non è permessa, fra l altro, l inclusione anche parziale in altre opere senza il consenso scritto dell autore
 Atomo Raggio atomico (Å) Atomi: diversi e uguali Raggi atomici: sostanzialmente simili per tutti gli atomi. perché? Non è permessa, in particolare, la riproduzione anche perché parziale proprio quella
Atomo Raggio atomico (Å) Atomi: diversi e uguali Raggi atomici: sostanzialmente simili per tutti gli atomi. perché? Non è permessa, in particolare, la riproduzione anche perché parziale proprio quella
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA. (Plank Einstein)
 L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
Introduzione alla meccanica quantistica. Vincenzo Barone
 Accademia delle Scienze di Torino 9 novembre 2017 Introduzione alla meccanica quantistica Vincenzo Barone barone@to.infn.it Parte I: Le basi della meccanica quantistica (questioni didattiche) Parte II:
Accademia delle Scienze di Torino 9 novembre 2017 Introduzione alla meccanica quantistica Vincenzo Barone barone@to.infn.it Parte I: Le basi della meccanica quantistica (questioni didattiche) Parte II:
FAM. T 1) α ν. (e α ν T 1) 2. (con l ipotesi ν > 0) si ottiene
 Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
La Crisi della Fisica Classica
 La Crisi della Fisica Classica F. Borgonovi (Dipartimento di Matematica e Fisica) Interdisciplinary Laboratories for Advanced Materials Physics (i-lamp) Department of Mathematics and Physics, Catholic
La Crisi della Fisica Classica F. Borgonovi (Dipartimento di Matematica e Fisica) Interdisciplinary Laboratories for Advanced Materials Physics (i-lamp) Department of Mathematics and Physics, Catholic
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
3. Struttura dell atomo
 Di cosa parleremo L organizzazione interna delle particelle che costituiscono gli atomi è stata oggetto di studio per lungo tempo e le ipotesi sulla struttura atomica si sono evolute nel tempo in base
Di cosa parleremo L organizzazione interna delle particelle che costituiscono gli atomi è stata oggetto di studio per lungo tempo e le ipotesi sulla struttura atomica si sono evolute nel tempo in base
CRISI DELLA FISICA CLASSICA e FISICA DEI QUANTI Esercitazione
 ! ISTITUTO LOMBARDO ACCADEMIA DI SCIENZE E LETTERE Ciclo formativo per Insegnanti di Scuola Superiore - anno scolastico 2017-2018 Prima lezione - Milano, 10 ottobre 2017 CRISI DELLA FISICA CLASSICA e FISICA
! ISTITUTO LOMBARDO ACCADEMIA DI SCIENZE E LETTERE Ciclo formativo per Insegnanti di Scuola Superiore - anno scolastico 2017-2018 Prima lezione - Milano, 10 ottobre 2017 CRISI DELLA FISICA CLASSICA e FISICA
LA CRISI DELLA FISICA CLASSICA
 CAPITOLO 44 LA CRISI DELLA FISICA CLASSICA IL CORPO NERO E L IPOTESI DI PLANCK All aumentare della temperatura aumenta la quantità di energia presente nella radiazione del corpo nero ed è quindi plausibile
CAPITOLO 44 LA CRISI DELLA FISICA CLASSICA IL CORPO NERO E L IPOTESI DI PLANCK All aumentare della temperatura aumenta la quantità di energia presente nella radiazione del corpo nero ed è quindi plausibile
La teoria del corpo nero
 La teoria del corpo nero Max Planck Primo Levi 2014 Roberto Bedogni INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
La teoria del corpo nero Max Planck Primo Levi 2014 Roberto Bedogni INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
La nascita della fisica moderna. (un racconto di inizio 900)
 La nascita della fisica moderna (un racconto di inizio 900) Sviluppo storico della fisica tra fine 800 e il 1927 Fisica sperimentale fine 800 Fisica teorica fine 800 1900 1905 1911 1913 1916 1924 1925-1927
La nascita della fisica moderna (un racconto di inizio 900) Sviluppo storico della fisica tra fine 800 e il 1927 Fisica sperimentale fine 800 Fisica teorica fine 800 1900 1905 1911 1913 1916 1924 1925-1927
Il corpo nero e l ipotesi di Planck
 Il corpo nero e l ipotesi di Planck La crisi della fisica classica Alla fine del XIX secolo ci sono ancora del fenomeni che la fisica classica non riesce a spiegare: lo spettro d irraggiamento del corpo
Il corpo nero e l ipotesi di Planck La crisi della fisica classica Alla fine del XIX secolo ci sono ancora del fenomeni che la fisica classica non riesce a spiegare: lo spettro d irraggiamento del corpo
Fisica atomica CAPITOLO. Contenuti
 CAPITOLO 3 Fisica atomica In alcune meduse, ad esempio nella Aequorea victoria mostrata nella fotografia, è presente una particolare proteina, la GFP, dall inglese Green Fluorescent Protein, che consente
CAPITOLO 3 Fisica atomica In alcune meduse, ad esempio nella Aequorea victoria mostrata nella fotografia, è presente una particolare proteina, la GFP, dall inglese Green Fluorescent Protein, che consente
Elettricità e Fisica Moderna
 Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
La complessa semplicità dell'atomo di idrogeno!
 La complessa semplicità dell'atomo di idrogeno Bergamo, venerdì 1 Febbraio 2013 Stefano Covino INAF - Osservatorio Astronomico di Brera Un po di terminologia Atomo (dal greco, indivisibile): atomismo (Leucippo,
La complessa semplicità dell'atomo di idrogeno Bergamo, venerdì 1 Febbraio 2013 Stefano Covino INAF - Osservatorio Astronomico di Brera Un po di terminologia Atomo (dal greco, indivisibile): atomismo (Leucippo,
Struttura dell Atomo
 LM85-bis Scienze della formazione primaria Struttura dell Atomo Prof. Federico Teloni Elementi di Chimica A. A. 2018-2019 e-mail: federico.teloni@istruzione.it Materia e Particelle Definiamo materia tutto
LM85-bis Scienze della formazione primaria Struttura dell Atomo Prof. Federico Teloni Elementi di Chimica A. A. 2018-2019 e-mail: federico.teloni@istruzione.it Materia e Particelle Definiamo materia tutto
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
Meccanica quantistica Giovanni Organtini
 Meccanica quantistica Giovanni Organtini Il corpo nero 2 Un corpo caldo Giovanni Organtini - Sapienza Università di Roma Tutti i corpi caldi emettono luce non è vero il viceversa Perché? 3 Un corpo nero
Meccanica quantistica Giovanni Organtini Il corpo nero 2 Un corpo caldo Giovanni Organtini - Sapienza Università di Roma Tutti i corpi caldi emettono luce non è vero il viceversa Perché? 3 Un corpo nero
Materia e radiazione. Lezione 6
 Materia e radiazione Lezione 6 Sommario Luce e radiazione: come estrarre l informazione fisica dalla luce delle stelle. La radiazione di corpo nero: leggi di Wien e di Stefan. Struttura Atomica: nucleo
Materia e radiazione Lezione 6 Sommario Luce e radiazione: come estrarre l informazione fisica dalla luce delle stelle. La radiazione di corpo nero: leggi di Wien e di Stefan. Struttura Atomica: nucleo
Fisica quantistica. Liceo Malpighi, a.s. 2016/17
 Fisica quantistica Liceo Malpighi, a.s. 2016/17 DALLA FISICA CLASSICA ALLA FISICA MODERNA (lungo periodo di transizione a cavallo fra 800 e 900) MECCANICA E ASTRONOMIA NEL XIX SEC. Previsione di Nettuno
Fisica quantistica Liceo Malpighi, a.s. 2016/17 DALLA FISICA CLASSICA ALLA FISICA MODERNA (lungo periodo di transizione a cavallo fra 800 e 900) MECCANICA E ASTRONOMIA NEL XIX SEC. Previsione di Nettuno
Radiazione e Materia. Insegnamento di Chimica Generale CCS CHI e MAT. Scuola di Ingegneria Industriale e dell Informazione
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
catastrofe ultravioletta
 Fisica moderna Radiazione termica La radiazione termica è l insieme di onde elettromagnetiche che ogni corpo emette per effetto della sua temperatura Un corpo nero è un corpo che assorbe completamente
Fisica moderna Radiazione termica La radiazione termica è l insieme di onde elettromagnetiche che ogni corpo emette per effetto della sua temperatura Un corpo nero è un corpo che assorbe completamente
Radiazione elettromagnetica
 Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
Materia e radiazione. Lezione 6
 Materia e radiazione Lezione 6 Sommario Luce e radiazione: come estrarre l informazione fisica dalla luce delle stelle. La radiazione di corpo nero: leggi di Wien e di Stefan. Struttura Atomica: nucleo
Materia e radiazione Lezione 6 Sommario Luce e radiazione: come estrarre l informazione fisica dalla luce delle stelle. La radiazione di corpo nero: leggi di Wien e di Stefan. Struttura Atomica: nucleo
Formazione di orbitali π. La differenza di energia tra due orbitali π è minore di quella tra due orbitali. Orbitali di non legame, n
 Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
ATOMI E PARTICELLE SUBATOMICHE
 ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
Capitolo 2. Cenni alla Composizione e Struttura dell atomo
 Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
L atomo di Bohr. Argomenti. Al tempo di Bohr. Spettri atomici 19/03/2010
 Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Rappresentazione dell atomo. Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano.
 Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
