La struttura dell atomo
|
|
|
- Albino Cipriani
- 5 anni fa
- Visualizzazioni
Transcript
1 La struttura dell atomo Il modello di Thomson Il modello di Rutherford Il modello di Bohr Teoria di Sommerfeld ed effetto Zeeman Il modello ondulatorio
2 Il modello ondulatorio Difetto fondamentale del modello di Bohr Postula che l elettrone dell atomo non ubbidisce alle leggi della fisica classica, ma poi usa queste leggi per definire l orbita dell elettrone intorno al nucleo e per ottenere l energia del sistema
3 Il modello ondulatorio Presupposti Ipotesi di de Broglie Principio di indeterminazione di Heisenberg Studi onde stazionarie
4 Ipotesi di De Broglie Dualismo onda-corpuscolo per la luce (Einstein, 1913) Ad una radiazione di frequenza ν è associato un fotone di massa m Energia di un fotone (Planck) E=h ν Teoria di Einstein E= m c 2 h ν = m c 2 ν = c/λ h (c/λ) = m c 2 λ= h/(m c) h: costante di Planck c: velocità della luce m: massa del fotone L ASPETTO CORPUSCOLARE si manifesta più frequentemente per le radiazioni di più alta frequenza (effetto Compton, fotoelettrico) L ASPETTO ONDULATORIO è più evidente nelle radiazioni di più bassa frequenza (interferenza)
5 Ipotesi di de Broglie Dualismo onda-corpuscolo per la materia (de Broglie) Ad ogni particella in movimento possiamo associare un onda con una lunghezza d onda data da: λ= h/(m v) h: costante di Planck v: velocità della particella m: massa della particella La natura ondulatoria degli elettroni è messa in evidenza sperimentalmente dalla diffrazione di un fascio di elettroni da un cristallo (es. MgO). Il fascio accelerato in modo che λ e fosse dell ordine di m, produce diffrazione come si osserva per i raggi X di pari λ. L ASPETTO CORPUSCOLARE E ONDULATORIO DEL FENOMENO NON POSSONO ESSERE EVIDENZIATI CONTEMPORANEAMENTE (Per corpi macroscopici λ non è misurabile poiché troppo piccola. Per corpi molto piccoli può prevalere l aspetto ondulatorio)
6 Il modello ondulatorio Lo studio della meccanica di un corpo macroscopico (es. pianeta o satellite) è possibile in quanto è relativamente semplice valutarne la posizione e quindi descrivere con estrema precisione l orbita percorsa (successione di punti certi in cui trovare il corpo in qualunque istante), e la velocità (energia) SISTEMA MACROSCOPICO SISTEMA MICRO/NANOSCOPICO Incertezza trascurabile nella posizione Incertezza non trascurabile nella posizione
7 Il modello ondulatorio Principio di indeterminazione di Heisenberg Non è possibile determinare contemporaneamente e con la stessa precisione la posizione e la quantità di moto (o velocità) di una particella Δp Δx h/2π mδv Δx h/2π Quanto più accurata risulta la determinazione della posizione della particella (Δx piccolo), tanto maggiore sarà l incertezza sulla quantità di moto (Δp) e viceversa. I MODELLI BOHR-SOMMERFELD IN CUI L ELETTRONE SI MUOVE LUNGO ORBITE DEFINITE A VELOCITA NOTA SONO INAFFIDABILI
8 Funzione d onda per l elettrone Per un elettrone la funzione d onda deve essere STAZIONARIA (il valore dell ampiezza dipende solo dalla posizione e non dal tempo) Ψ (x, y, z) L = n(λ/2 ) L= ½ λ L= 2 (½ λ)= λ L= 3 (½ λ) Nodi In un onda stazionaria la posizione dei nodi (punti ad ampiezza zero) non varia nel tempo e sono possibili solo certe vibrazioni: le vibrazioni sono quantizzate.
9 Funzione d onda per l elettrone L onda associata all elettrone deve essere stazionaria perché, in assenza di fenomeni perturbativi, la sua energia deve restare costante nel tempo
10 Equazione di Schrödinger Schrödinger postulò che la funzione d onda Ψ (x, y, z) fosse soluzione della seguente equazione 2 8π ψ + h dove 2 2 = x m ( E V) 2 + y 2 ψ(x,y,z) = z La funzione d onda Ψ non ha alcun significato fisico ma Ψ 2 rappresenta la densità di probabilità di trovare l elettrone in un punto (x, y, z) nell istante considerato. Ψ 2 (x, y, z) dv: probabilità di trovare l elettrone in un volume dv centrato su (x, y, z) 2 E: Energia totale V: Energia potenziale OPERATORE LAPLACIANO Hanno significato fisico solo quelle soluzioni Ψ che corrispondono a stati di energia costante (stazionari)
11 Equazione di Schrödinger L equazione di Schrödinger ammette infinite soluzioni matematiche ma solo alcune di queste sono fisicamente accettabili Le funzioni d onda fisicamente accettabili sono dette funzioni orbitaliche o semplicemente orbitali e si ottengono imponendo delle condizioni al contorno 1. La particella si trova necessariamente da qualche parte per cui la Ψ all infinito deve tendere a zero (Ψ è normalizzata) 2 ψ dv = 1 2. La Ψ deve essere ad un sol valore, altrimenti esisterebbero diverse probabilità di trovare l elettrone in un punto 3. La Ψ deve essere finita in ogni punto, altrimenti avremmo probabilità infinita di trovare la particella in un punto, che corrisponderebbe alla localizzazione della stessa
12 Numeri quantici Imponendo le condizioni al contorno si ottengono i quattro numeri quantici già visti che sono dei coefficienti della Ψ n, l, m (x, y, z) SIGNIFICATO FISICO DEI NUMERI QUANTICI n: individua lo strato (o livello) intorno al nucleo e da esso dipende la sua energia. n definisce anche la dimensione dell orbitale n= 1,., (7) l: definisce la forma dell orbitale e il numero di sottolivelli di energia di cui è costituito ciascun livello. Orbitali con l diversi hanno energie leggermente diverse. N SOTTOLIVELLI =n l= 0,, (n-1) m: definisce l orientazione nello spazio degli orbitali, ma non ha influenza sull energia. Orbitali dello stesso livello con m diverso hanno la stessa energia (sono degeneri). Definisce la molteplicità del sottolivello energetico. (2l+1) valori possibili m= -l,., 0,.., +l
13 Orbitali atomici Gli orbitali atomici possono anche essere indicati per semplicità con delle lettere Numero quantico secondario Numero quantico magnetico Simbolo orbitale l=0 m=0 s 1 l=1 m= -1, 0, +1 p x, p y, p z 3 l=2 m= -2, -1, 0, +1, +2 d xy, d yz, d xz, d z2, d( x2-y2 ) 5 Numero orbitali l=3 m= -3, -2, -1, 0, +1, +2, +3 f z3, f xz2, f yz2, f xyz, f z(x2-y2), 7 f x(x2-3y2), f y(3x2-y2)
14 Descrizione orbitali atomici Ψ 1,0,0 = N e -r/a 0 N: costante di normalizzazione a 0 = Å Ψ 1,0,0 (orbitale 1s) dipende solo da r, distanza dal nucleo. Ψ ha lo stesso valore in tutti i punti equidistanti dal nucleo Le zone di uguale probabilità di trovare l elettrone sono superfici sferiche concentriche Allontanandosi dal nucleo diminuisce la densità elettronica che si annulla solo all infinito Le superfici sferiche non terminano improvvisamente ma si estendono fino all infinito. Solo una sfera di raggio infinito racchiude tutta la carica elettronica Poiché la probabilità si abbatte ad una distanza molto piccola dal nucleo, è possibile definire delle superfici limite in cui è racchiuso il 90% di densità elettronica
15 Descrizione orbitali atomici Un altro modo di affrontare il problema è calcolare la densità di probabilità di trovare l elettrone su tutta la superficie sferica di raggio r: Ψ 2 4πr 2 Ψ 2 4πr 2 dr Densità di probabilità radiale Probabilità di trovare l elettrone in un guscio sferico di spessore infinitamente piccolo (compreso tra r e r + dr)
16 Forme degli orbitali atomici Orbitali s 1s 2s 3s La sfera entro cui esiste il 90% di probabilità di trovare l elettrone
17 Forme degli orbitali atomici Orbitali p p y p x p z z x Orbitali direzionali y
18 Forme degli orbitali atomici Orbitali p 2p x 3p x n 4p x
19 Forme degli orbitali atomici Orbitali d y x dz 2 y dx 2 -y 2 z y x x z dxy dxz dyz
20 Numero quantico di spin m s = ±1/2 Ψ(n, l, m, m s )
21 Ricapitolazione orbitali atomici Numero quantico principale Numero quantico secondario Numero quantico magnetico Orbitali n=1 l= 0 m=0 1s n=2 l= 0 l= 1 n=3 l= 0 l= 1 l=2 m=0 m= -1, 0, +1 m=0 m= -1, 0, +1 m= -2, -1, 0, +1, +2 2s 2p x, 2p y, 2p z 3s 3p x, 3p y, 3p z 3d xy, 3d yz, 3d xz, 3d z2, 3d( x2-y2 ) n=4 l= 0 l= 1 l=2 l=3 m=0 m= -1, 0, +1 m= -2, -1, 0, +1, +2 m=-3, -2, -1, 0, +1, +2, +3 4s 4p x, 4p y, 4p z 4d xy, 4d yz, 4d xz, 4d z2, 4d( x2-y2 ) 4f z3, 4f xz2, 4f yz2, 4f xyz, 4f z(x2-y2), 4f x(x2-3y2), 4f y(3x2-y2)
22 Energie orbitali 3d xy 3d yz 3d xz 3d x2-y2 3d z2 3 3px 3py 3pz 2 1 n, Energia 3s 2px 2py 2pz 2s 1s
23 Energie orbitali 4f 4d 4 3 n, Energia 3s 4s 4p 3p 3d 4s < 3d Mescolamento livelli energetici Le complicazioni aumentano con n
24 Regola della diagonale Fornisce un modo semplice per ordinare gli orbitali in ordine crescente di energia REGOLA DELLA SOMMA n+l L E di un orbitale è tanto minore quanto minore è n+l. A parità di somma ha E minore l orbitale con n minore 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p
25 Regola della diagonale
26 Configurazioni elettroniche Regole dell Aufbau o regole di riempimento degli orbitali atomici 1. Gli elettroni nello stato fondamentale (non eccitato) tendono ad occupare lo stato a più bassa energia disponibile 2. PRINCIPIO DI ESCLUSIONE DI PAULI In un atomo gli elettroni non possono avere i quattro numeri quantici uguali ma devono differenziarsi almeno per lo spin. Pertanto, un orbitale può contenere al massimo 2 elettroni 3. REGOLA DI HUND o REGOLA DELLA MASSIMA MOLTEPLICITA DI SPIN Nel riempimento di orbitali degeneri, gli elettroni devono occuparne il maggior numero possibile disponendosi in essi a spin parallelo
27 Configurazioni elettroniche Rappresentazione configurazione elettronica 2s 2 Livello E (n) Numero elettroni Orbitale (l) Numero massimo di elettroni per sottolivello Orbitali Molteplicità N max elettroni s 1 2 p 3 6 d 5 10 f 7 14
28 Configurazioni elettroniche H Z=1 E E 1s 1s He Z=2 E 1s 1 1s 1s 2
29 Configurazioni elettroniche Li Z=3 E 2s 1s Be Z=4 E 2s 1s E 1s 2 2s 1 1s 2 2s 2 B Z=5 2s 1s 1s 2 2s 2 2p 1 2p
30 Configurazioni elettroniche E C Z=6 2s 2p 1s E 1s 2 2s 2 2p 2 N Z=7 2s 2p 1s 2 2s 2 2p 3 1s
31 Configurazioni elettroniche O E Z=8 1s 2 2s 2 2p 4 E 2s 1s 2p F Z=9 2s 2p 1s 2 2s 2 2p 5 1s
32 Configurazioni elettroniche E Ne Z=10 2s 2p 1s 2 2s 2 2p 6 1s
33 Tavola periodica E una organizzazione di elementi secondo un criterio tale che elementi con proprietà simili vengono a trovarsi in un certo raggruppamento Può essere ottenuta attraverso la costruzione ideale degli atomi di tutti gli elementi partendo dall H e procedendo in ordine di Z crescente, aggiungendo progressivamente un elettrone ed un protone nel nucleo Scrivere sulla stessa riga i simboli degli elementi costruiti progressivamente fino a quando la freccia della diagonale non rimanda all orbitale s del livello successivo, e passare ad una nuova riga quando inizia il riempimento di questo orbitale, anche se il livello precedente non è stato completato Riportare per ciascun elemento di una riga solo gli elettroni dell ultimo livello, più esterni, detti elettroni di valenza, rinviando, per quella dei livelli sottostanti alla configurazione del gas nobile della riga precedente
34 Tavola periodica Gli elementi di un gruppo presentano stessa configurazione elettronica esterna Gruppo Periodo Gli elementi di un periodo si distinguono dal precedente e successivo per un e sul livello più esterno
35 Tavola periodica Schematizzazione a blocchi Blocco d Blocco s Blocco p Blocco f Il nome blocco deriva dall ultimo orbitale riempito
36 Tavola periodica Le proprietà chimiche e fisiche di un elemento dipendono dalla sua configurazione elettronica esterna Gruppo: stesse proprietà Periodo: le proprietà variano gradatamente
37 Esempi di configurazione Configurazione elettronica esterna Z=16 1s 2 2s 2 2p 6 3s 2 3p 4 2+4= 6 elettroni 6 gruppo n=3 3 periodo
38 Atomi e reattività Gli atomi in natura hanno una forte tendenza a combinarsi attraverso lo scambio o la condivisione di elettroni Per capire la reattività di un atomo occorre conoscere la sua tendenza a cedere o ad acquistare elettroni Questa tendenza viene quantificata con i seguenti parametri: POTENZIALE DI IONIZZAZIONE (Misura della tendenza di un atomo a cedere e) AFFINITA ELETTRONICA (Misura la tendenza di un atomo isolato ad acquistare e) ELETTRONEGATIVITA (Misura della tendenza di un atomo ad attirare a sé gli e di legame)
39 Energia di ionizzazione (E p ) E l energia che occorre somministrare ad un atomo per allontanare un elettrone del livello più esterno (elettone di valenza) Energia di prima ionizzazione A (g) E 1 A + (g) + e Ione positivo: catione Energia di seconda ionizzazione A + (g) E 2 A 2+ (g) + e Le energie di seconda ionizzazione sono maggiori di quelle di prima ionizzazione (e più attratti dal nucleo) 39
40 Affinità elettronica (E a ) L affinità elettronica è l energia sviluppata quando ad un atomo neutro si aggiunge un elettrone B (g) + 1e B - (g) Ione negativo: anione 40
41 E p ed E a Aumenta Lungo il periodo l e più esterno risulta più legato a causa dell aumento della carica nucleare Diminuisce Scendendo lungo il gruppo, l E dell orbitale da cui strappiamo l e è sempre più alta, e quindi minore è l E per portare l e a distanza infinita dal nucleo 41
42 Elettronegatività La capacità di un atomo legato ad attrarre a se il doppietto elettronico di legame A A A B δ A A A + δ B - 42
43 Elettronegatività E una grandezza relativa. All H è stato attribuito valore 2.1 nella scala Pauling. Il Fr è l elemento meno elettronegativo (0.7) e il F è l elemento più elettronegativo (4.1) Aumenta Diminuisce 43
44 Carica nucleare effettiva (Z eff ) Energia di un orbitale E= f (Z eff, n) Importante per comprendere le variazioni periodiche di E p, E a, elettronegatività (aumentano lungo il periodo e diminuiscono lungo il gruppo) Ze: carica nucleare S: costante di schermo Z eff = Ze - S Zeff COSTANTE n AUMENTA E p, E a DIMINUISCE S COSTANTE: modesta la schermatura degli e messi nello stesso n Ze, Zeff E p, E a 44
45 Carica nucleare effettiva (Z eff ) Elemento Z e - schermanti (S) Z eff Li Na K Rb n 45
46 Raggi atomici Impossibilità di misurare raggi di atomi isolati Determinati sulla base di distanze di legame in molecole omeopolari (r~d/2) Diminuisce n costante Z eff aumenta n aumenta Z eff costante Aumenta 46
47 Carattere metallico 47
48 Carattere metallico Cedono elettroni e si trasformano in ioni positivi. Hanno carattere riducente. Reagiscono con l ossigeno e formano ossidi basici 1 Gruppo Li Na K Rb Cs Fr Li + Na + K + Rb + Cs + Fr + 2 Gruppo Be Mg Ca Sr Ba Ra Be 2+ Mg 2+ Ca 2+ Sr 2+ Ba 2+ Ra 2+ 3 Gruppo Al Ga In Tl 1e 2e 3e Al 3+ Ga 3+ In 3+ Tl 3+ Cationi monovalenti Cationi bivalenti Cationi trivalenti 48 48
49 Carattere nonmetallico Acquistano elettroni e si trasformano in ioni negativi. Hanno carattere ossidante. Reagiscono con l ossigeno e formano ossidi acidi o anidridi 49 49
50 Semimetalli Reagiscono con l ossigeno e formano ossidi anfoteri Tali elementi possono comportarsi sia da metalli che da non metalli: SEMIMETALLI (anfoteri) B Al Si Ge As Sb Te Po At 50 50
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica
 ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
mvr = n h e 2 r = m v 2 e m r v = La configurazione elettronica r = e 2 m v 2 (1) Quantizzazione del momento angolare (2) 4 πε.
 La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
ATOMO. Avogadro (1811) Volumi uguali di gas diversi contengono un ugual numero di MOLECOLE (N A =6,022*10 23 )
 ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
- Dati sperimentali: interazione luce / materia spettri caratteristici
 - Thomson: evidenza sperimentale per elettrone misura e/m e - Millikan: misura la carica dell elettrone e ne ricava la massa e = 1,60 x 10-19 C - Rutherford: stima le dimensioni atomiche struttura vuota
- Thomson: evidenza sperimentale per elettrone misura e/m e - Millikan: misura la carica dell elettrone e ne ricava la massa e = 1,60 x 10-19 C - Rutherford: stima le dimensioni atomiche struttura vuota
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Struttura Elettronica degli Atomi Meccanica quantistica
 Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA. (Plank Einstein)
 L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
A Z. L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone. +1e e.
 L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno:
 La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Modelli atomici Modello atomico di Rutheford Per t s d u i diare la t s rutt ttura t a omica Ruth th f or (
 Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
La struttura dell atomo
 La struttura dell atomo raggi catodici (elettroni) raggi canale (ioni positivi) Modello di Thomson Atomo come una piccola sfera omogenea carica di elettricità positiva, nella quale sono dispersi gli elettroni,
La struttura dell atomo raggi catodici (elettroni) raggi canale (ioni positivi) Modello di Thomson Atomo come una piccola sfera omogenea carica di elettricità positiva, nella quale sono dispersi gli elettroni,
Unbowed, Unbent, Unbroken
 Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
COMPORTAMENTO DUALISTICO della MATERIA
 COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
ATOMI E PARTICELLE SUBATOMICHE
 ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
Il principio di indeterminazione di Heisenberg
 Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
Comune ordine di riempimento degli orbitali di un atomo
 Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
Come sono disposti gli elettroni intorno al nucleo in un atomo?
 Come sono disposti gli elettroni intorno al nucleo in un atomo? La natura ondulatoria della radiazione elettromagnetica e della luce La luce è una radiazione elettromagnetica che si muove nello spazio
Come sono disposti gli elettroni intorno al nucleo in un atomo? La natura ondulatoria della radiazione elettromagnetica e della luce La luce è una radiazione elettromagnetica che si muove nello spazio
the power of ten Prof.ssa Patrizia Gallucci
 https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
Comunicazioni Docente - Studenti
 Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Corso di CHIMICA LEZIONE 2
 Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
Forma e proprietà dell orbitale 1s
 Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
L atomo di Bohr. Argomenti. Al tempo di Bohr. Spettri atomici 19/03/2010
 Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Modello atomico ad orbitali e numeri quantici
 Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
La struttura degli atomi
 1 La struttura degli atomi pg. 298 27-28 31-37 43 47 51-53 55-57 61-62 67(a/h) 68(a/i) La struttura degli atomi e gli andamenti periodici pg.332 1-7 11-15 17-18 27-30 37 40-42 51 Solvay conference, 1927
1 La struttura degli atomi pg. 298 27-28 31-37 43 47 51-53 55-57 61-62 67(a/h) 68(a/i) La struttura degli atomi e gli andamenti periodici pg.332 1-7 11-15 17-18 27-30 37 40-42 51 Solvay conference, 1927
CHIMICA: studio della struttura e delle trasformazioni della materia
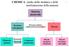 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Struttura atomica, configurazione elettronica e periodicità chimica
 Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
I numeri quantici. Numero quantico principale, n: numero intero Caratterizza l energia dell elettrone
 I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
Quarta unità didattica. Disposizione degli elettroni nell atomo
 Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
Principi della chimica
 6 Novembre 016 Principi della chimica L atomo La materia è formata da atomi, particelle subatomiche costituite da cariche negative (elettroni, e-) che sono situati intorno ad un nucleo dove risiedono le
6 Novembre 016 Principi della chimica L atomo La materia è formata da atomi, particelle subatomiche costituite da cariche negative (elettroni, e-) che sono situati intorno ad un nucleo dove risiedono le
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
STRUTTURA ATOMICA. tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica
 STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
Configurazione elettronica e Tavola periodica. Lezioni 13-16
 Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
1 3 STRUTTURA ATOMICA
 1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
raggio atomico: raggio del nucleo: cm cm
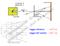 raggio atomico: raggio del nucleo: 10 10 8 1 cm cm Modello di Rutherford: contrasto con la fisica classica perché prima o poi l elettrone avrebbe dovuto cadere sul nucleo irradiando Energia. Le leggi valide
raggio atomico: raggio del nucleo: 10 10 8 1 cm cm Modello di Rutherford: contrasto con la fisica classica perché prima o poi l elettrone avrebbe dovuto cadere sul nucleo irradiando Energia. Le leggi valide
ORBITALE ATOMICO. Forma
 L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
Gli orbitali atomici. Il modo più semplice di visualizzare un atomo. TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e -
 Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
proprietà periodiche!!! tutti X -
 Molte delle proprietà degli elementi variano periodicamente lungo la tavola periodica(che si chiamerà periodica per qualche motivo!) L origine delle proprietà periodicheva ricercata nella struttura (o
Molte delle proprietà degli elementi variano periodicamente lungo la tavola periodica(che si chiamerà periodica per qualche motivo!) L origine delle proprietà periodicheva ricercata nella struttura (o
Configurazioni elettroniche e periodicità
 Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
J.J. Thomson (1897): dimostra l esistenza dell elettrone E. Ruthenford (1911): dimostra l esistenza del nucleo
 STRUTTURA dell ATOMO J.J. Thomson (1897): dimostra l esistenza dell elettrone E. Ruthenford (1911): dimostra l esistenza del nucleo J. Chadwich (193): dimostra l esistenza del neutrone J.J. Thomson (1897):
STRUTTURA dell ATOMO J.J. Thomson (1897): dimostra l esistenza dell elettrone E. Ruthenford (1911): dimostra l esistenza del nucleo J. Chadwich (193): dimostra l esistenza del neutrone J.J. Thomson (1897):
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica Teoria atomica della materia Teoria atomica di Dalton 1.Ciascun elemento è composto da particelle estremamente piccole chiamate atomi. 2.Tutti gli atomi di un dato
Struttura elettronica e tavola periodica Teoria atomica della materia Teoria atomica di Dalton 1.Ciascun elemento è composto da particelle estremamente piccole chiamate atomi. 2.Tutti gli atomi di un dato
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Bohr 1913 Gli elettroni viaggiano su orbite fisse
 Democrito ( 400 a.c.) [ ] quando due elementi si combinano in modi diversi per formare diversi composti, posta fissa la quantità di uno dei due elementi, la quantità dell'altro elemento necessaria a reagire
Democrito ( 400 a.c.) [ ] quando due elementi si combinano in modi diversi per formare diversi composti, posta fissa la quantità di uno dei due elementi, la quantità dell'altro elemento necessaria a reagire
Bohr 1913 Gli elettroni viaggiano su orbite fisse
 Democrito ( 400 a.c.) [ ] quando due elementi si combinano in modi diversi per formare diversi composti, posta fissa la quantità di uno dei due elementi, la quantità dell'altro elemento necessaria a reagire
Democrito ( 400 a.c.) [ ] quando due elementi si combinano in modi diversi per formare diversi composti, posta fissa la quantità di uno dei due elementi, la quantità dell'altro elemento necessaria a reagire
Unità 2. La teoria quantistica
 Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
Come si dispongono gli elettroni negli atomi
 Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
La tavola periodica. 1- Introduzione
 La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
Orbitali nei primi tre livelli
 Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
6) Modello atomico a ORBITALI
 6) Modello atomico a ORBITALI PREMESSA: LIMITI DEL MODELLO DI BOHR (pag. 94 par.3) Applicando il concetto di quantizzazione dell E all atomo, Bohr ipotizzò che un atomo potesse esistere solo in determinati
6) Modello atomico a ORBITALI PREMESSA: LIMITI DEL MODELLO DI BOHR (pag. 94 par.3) Applicando il concetto di quantizzazione dell E all atomo, Bohr ipotizzò che un atomo potesse esistere solo in determinati
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
LA RADIAZIONE ELETTROMAGNETICA. c = λ ν. c = 2, m s-1 (nel vuoto)
 LA RADIAZIONE ELETTROMAGNETICA c = λ ν c = 2,9979 108 m s-1 (nel vuoto) THE ELECTROMAGNETIC SPECTRUM E (erg) Alta energia Alta frequenza Piccola λ 10-6 VISIBLE X RAYS 2 10-12 ULTRAVIOLET 2 10-10 2 10-14
LA RADIAZIONE ELETTROMAGNETICA c = λ ν c = 2,9979 108 m s-1 (nel vuoto) THE ELECTROMAGNETIC SPECTRUM E (erg) Alta energia Alta frequenza Piccola λ 10-6 VISIBLE X RAYS 2 10-12 ULTRAVIOLET 2 10-10 2 10-14
Teoria Quantistica e Struttura Elettronica degli Atomi
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Teoria Quantistica e Struttura Elettronica degli Atomi Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Teoria Quantistica e Struttura Elettronica degli Atomi Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Tavola periodica. Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi.
 Tavola periodica Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi. Tavola periodica Serve a classificare in modo sistematico le proprietà
Tavola periodica Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi. Tavola periodica Serve a classificare in modo sistematico le proprietà
numeri quantici orbitale spin
 La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica Esperimento di Thomson elettrone Si ottenne il rapporto carica/massa. Con l esperimento di Millikan venne determinato il valore della carica. Esperimento di Rutherford
Struttura elettronica e tavola periodica Esperimento di Thomson elettrone Si ottenne il rapporto carica/massa. Con l esperimento di Millikan venne determinato il valore della carica. Esperimento di Rutherford
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
PROPRIETA PERIODICHE
 PROPRIETA PERIODICHE Sono tutte quelle proprietà il cui andamento lungo un periodo o lungo un gruppo presenta un andamento periodico. Le più rilevanti sono: 1) Raggi atomici (o ionici) 2) Potenziale di
PROPRIETA PERIODICHE Sono tutte quelle proprietà il cui andamento lungo un periodo o lungo un gruppo presenta un andamento periodico. Le più rilevanti sono: 1) Raggi atomici (o ionici) 2) Potenziale di
TAVOLA PERIODICA. 118 elementi, di cui 92 presenti in natura
 TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
Teoria atomica. Dr. Lucia Tonucci Ingegneria delle Costruzioni
 Teoria atomica Dr. Lucia Tonucci l.tonucci@unich.it Ingegneria delle Costruzioni Cenni storici V Sec. a.c. Democrito: la materia è costituita da corpuscoli indivisibili, gli atomi (atomo = indivisibile)
Teoria atomica Dr. Lucia Tonucci l.tonucci@unich.it Ingegneria delle Costruzioni Cenni storici V Sec. a.c. Democrito: la materia è costituita da corpuscoli indivisibili, gli atomi (atomo = indivisibile)
LA TAVOLA PERIODICA. Ingegneria delle costruzioni
 LA TAVOLA PERIODICA Chimica Applicata Dr. Lucia Tonucci Ingegneria delle costruzioni Evidenza sperimentale: alcune proprietà degli elementi chimici hanno andamento periodico Elencando gli elementi secondo
LA TAVOLA PERIODICA Chimica Applicata Dr. Lucia Tonucci Ingegneria delle costruzioni Evidenza sperimentale: alcune proprietà degli elementi chimici hanno andamento periodico Elencando gli elementi secondo
Sommario delle lezione 3. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
La struttura dell atomo
 La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
Tavola Periodica degli Elementi: Gruppi e Periodi
 La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
Riassunto modelli atomici.
 Lezione 6 1. La teoria atomica moderna 2. Il modello quantomeccanico dell atomo 3. Gli orbitali 4. Carica nucleare efficace 5. Principi di Pauli e Hund 6. Configurazioni elettroniche 7. AUFBAU Riassunto
Lezione 6 1. La teoria atomica moderna 2. Il modello quantomeccanico dell atomo 3. Gli orbitali 4. Carica nucleare efficace 5. Principi di Pauli e Hund 6. Configurazioni elettroniche 7. AUFBAU Riassunto
1. Principi della chimica
 3 Novembre 017 1. Principi della chimica L atomo La materia è formata da atomi, particelle subatomiche costituite da cariche negative (elettroni, e-) che sono situati intorno ad un nucleo dove risiedono
3 Novembre 017 1. Principi della chimica L atomo La materia è formata da atomi, particelle subatomiche costituite da cariche negative (elettroni, e-) che sono situati intorno ad un nucleo dove risiedono
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
GLI ELEMENTI CHIMICI
 I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
