Macromolecole biologiche
|
|
|
- Bianca Alfieri
- 6 anni fa
- Visualizzazioni
Transcript
1 MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole biologiche (1) MACROMOLECOLE Di grandi dimensioni & molto organizzate. Contengono da decine a milioni di atomi di Carbono. Possono svolgere compiti complessi con grande precisione ed efficienza. 1. PROTEINE 2. ACIDI NUCLEICI 3. POLISACCARIDI 4. Certi LIPIDI Molecole biologiche (2) Proteine, acidi nucleici e polisaccaridi sono polimeri costitutiti da un gran numero di unità a basso peso molecolare (monomeri). 1
2 Molecole biologiche (3) Unità costitutive delle macromolecole (pool di precursori): Amminoacidi, precursori delle proteine Zuccheri, precursori dei polisaccari Nucleotidi, precursori degli acidi nucleici Acidi grassi, precursori dei lipidi Molecole biologiche (4) Composti intermediari del metabolismo (metaboliti intermedi) Molecole biologiche (5) Molecole con funzione varie: Vitamine (cofattori dei enzimi) Ormonei steroidei o aminoacidici Molecole di reserva energetica (ATP, fosfocreatina) Molecole regolatrici (es. AMP ciclico) Prodotti di scarto del metabolismo (es. Urea) Ecc. Macromolecole biologiche 2. PROTEINE protean.com/protein structure.html 2
3 Le proteine giocano ruoli chiave negli organismi viventi Tre esampi di funzioni delle proteine Catalisi: Quasi tutte le reazioni chimiche in una cellula vivente sono catalizzate da enzimi proteici. Trasporto: Alcune proteine trasportano diverse sostanze, come ossigeno, ferro, ecc. Trasferimento di informazione: Ad esempio ormoni. L emoglobina trasporta l ossigeno La alcool deidrogenasi ossida gli alcooli ad aldeidi o chetoni L insulina controlla la quantità di zucchero nel sangue FUNZIONI BIOLOGICHE DELLE PROTEINE (1) Catalisi enzimatica. La maggior parte delle reazioni chimiche è catalizzata da enzimi che sono proteine. Gli enzimi possiedono un enorme potere catalitico aumentando la velocità delle reazioni almeno di un milione di volte. Si conoscono diverse migliaia di enzimi, e molti sono stati cristallizzati. FUNZIONI BIOLOGICHE DELLE PROTEINE (2) FUNZIONI BIOLOGICHE DELLE PROTEINE (2.1) _Esempi di trasportatori nelle membrane Trasporto e immagazzinamento. La maggior parte delle piccole molecole e degli ioni vengono trasportati da proteine specifiche. Ad es. l emoglobina e la mioglobina trasportano l ossigeno nel sangue e nel tessuto muscolare, rispettivamente. Il ferro è trasportato nel plasma sanguigno dalla transferrina ed è immagazzinato nel fegato come complesso con la ferritina. Trasportatori («carrier») di zuccheri o di aminoacidi Canali ionici Hemoglobin/MetalComplexinBlood.html lobin/metalcomplexinblood.html eport=objectonly 93/?report=objectonly 3
4 FUNZIONI BIOLOGICHE DELLE PROTEINE (2.2)_Trasportatori nelle membrane, segue FUNZIONI BIOLOGICHE DELLE PROTEINE (2.3)_Recettori per endocitosi di grandi complessi molecolari Pompe scambiatrici di ioni contro gradiente LDL science/metabolomics/enzyme explorer/learningcenter/plasma blood protein/lipoprotein function.html FUNZIONI BIOLOGICHE DELLE PROTEINE (3) Movimenti coordinati. Le proteine sono il principale componente del muscolo. Per es. la contrazione muscolare é realizzata mediante un movimento di scivolamento reciproco di due tipi di filamenti proteici (actina e miosina). Il movimento dei cromosomi durante la mitosi, la propulsione degli spermatozoi mediante flagelli o il movimento di vescicole all interno delle cellule sono anche essi prodotti da insiemi contrattili proteici. FUNZIONI BIOLOGICHE DELLE PROTEINE (4) Sostegno meccanico. Ad es. l elevata resistenza alla tensione della pelle e dell osso è dovuta alla presenza di collagene, una proteina fibrosa extracellulare. La resistenza agli stress meccanici delle cellule della pelle è dovuta alla presenza di cheratina, una proteina fibrosa del citoscheletro. fig_tab/ncb _F1.html 4
5 FUNZIONI BIOLOGICHE DELLE PROTEINE (5) Protezione immunologica. Gli anticorpi sono proteine altamente specifiche che riconoscono e si combinano con sostanze estranee tipo virus, batteri e cellule di altri organismi. FUNZIONI BIOLOGICHE DELLE PROTEINE (6) Generazione e propagazione di impulsi nervosi. La risposta delle cellule nervose a stimoli specifici é mediata da proteine recettrici. Ad es. la rodopsina é il fotorecettore delle cellule dei bastoncelli della retina. Proteine recettrici che vengono stimolate da piccole molecole specifiche, come l acetilcolina, sono responsabili della trasmissione degli impulsi nervosi nelle sinapsi. Le sinapsi sono giunzioni tra le cellule nervose. iki/antibody Health Fe Mu/Medications.html FUNZIONI BIOLOGICHE DELLE PROTEINE (7) Crescita e differenziamento. L espressione controllata e sequenziale dell espressione genica é essenziale per la crescita e il differenziamento ordinato delle cellule. Soltanto una piccola frazione del genoma di una cellula viene espresso in ogni momento. Nei batteri, proteine ad azione repressiva sono importanti elementi di controllo che silenziano segmenti specifici del DNA di una cellula. Negli organismi superiori la crescita e il differenziamento sono coordinati da proteine dette fattori di crescita o fattori di trasformazione. Ad es. il nerve growth factor (NGF) (fattore di crescita delle cellule nervose) guida la formazione delle cellule neurali. Le attività delle diverse cellule negli organismi multicellulari sono coordinate dagli ormoni. Dogma Centrale della Biologia (parere classico) (Francis Crick, 1958) in biologia molecolare il flusso dell informazione genetica è monodirezionale L informazione scorrerebbe dal DNA al RNA e dal RNA alle proteine, ma non in senso contrario (Francis Crick) ossia I geni (genotipo) codificano per messaggeri che vengono tradotti in proteine, gli effettori, che costituiscono il fenotipo 5
6 I geni vengono espressi mediante un processo di trascrizione seguito da traduzione Trascrizione ( transcription ): sintesi del RNA sotto la direzione del DNA Traduzione ( translation ): sintesi delle proteine sotto la direzione del RNA Un gene nel filamento stampo ( template ) viene usato per la trascrizione, dando origine ad un trascritto complementare al filamento stampo del DNA
7 Nuove scoperte ed eccezioni alla regola (risultato da recenti studi genomici) Molto del DNA che non codifica per proteine codifica per diversi tipi di RNA funzionali. I retrovirus non ubidiscono al dogma centrale in quanto il loro RNA codifica per il DNA trascrizione inversa («reverse transcription»). I prioni sono proteine capaci di replicarsi influenzando la struttura di altre proteine dello stesso tipo, senza prendere in considerazione alcun tipo di informazione genetica. Usando il suo enzima trascriptasi inversa e i materiali dell ospite (nucleotidi, zuccheri, ecc.) il virione dell HIV trascrive il suo RNA in DNA. SINTESI PROTEICA content/uploads/2013/02/process of protein synthesis.jpg 7
8 SINTESI PROTEICA: 1 a fase: TRASCRIZIONE («Transcription») SINTESI PROTEICA: 1 a fase: TRASCRIZIONE, segue Prima che la sintesi della proteina inizi, la corrispondente molecola di RNA é prodotta mediante il processo di trascrizione del RNA. Uno dei filamenti della doppia elica del DNA viene utilizzato come stampo ( template ) dall enzima RNA polimerasi per sintetizzare un RNA messaggero (mrna). Questo mrna migra dal nucleo nel citoplasma. Durante questo passo, il mrna subisce diversi tipi di passi di maturazione, incluso uno detto di splicing in cui le sequenze non codificanti vengono eliminate. La sequenza di mrna codificante può essere descritta come una unità di tre nucleotidi chiamata un codone. rna.net/2011/08/24/rna transcription/ dna rna/ SINTESI PROTEICA: 2 a fase: TRADUZIONE («Translation») Il ribosoma si lega al mrna nel codone iniziale (AUG) che viene riconosciuto dal trna iniziatore. Il ribosoma procede allora alla fase di alungamento della sintesi proteica. In questo stadio, i complessi, composti da un aminoacido legato al trna, si legano in modo sequenziale al codone appropriato del mrna, formando coppie di basi complementari con l anticodone del trna. Il ribosoma si muove da codone a codone lungo il mrna. Gli amino acidi vengono aggiunti uno ad uno, tradotti in sequenze polpeptidiche dettate dal DNA e rappresentate dal mrna. Alla fine, un fattore di rilasciosi lega al codone finale, terminando la traduzione e rilasciando il polipeptide completo dal ribosoma. rna.net/2011/08/28/translation of rna/ La sequenza di basi del DNA determina la sequenza di aminoacidi delle proteine. (H. Kreuzer & A. Massey: Biology and Biotechnology: Science, Applications and Issues ASM Press, Washington, D.C., 2005) 8
9 La sequenza di Amminoacidi è codificata dalla sequenza di basi del DNA in un gene Catena/residuo, laterale DNA molecule = G C G C TT A A G C G C C G C G A A TT C G C G DNA base sequence Le unità fondamentali delle Proteine AMMINOACIDI Amminoacidi: Unità basilari delle proteine Stereoisomeria degli amminoacidi I diversi gruppi (residui) laterali, R, determinano le proprietà dei 20 amminoacidi Poichè il carbonio α di tutti gli amminoacidi (ad eccezione della glicina) è legato a 4 gruppi diversi, per ogni AA possono esistere due stereoisomeri. (qui illustrate le forme D e L per l alanina) 9
10 Stereoisomeri degli amminoacidi Parete cellulare nei procarioti (1) («Cell wall») Gli AA usati per la sintesi delle proteine sono sempre L amminoacidi. I microorganismi (procarioti) usano D aminoacidi nella sintesi di alcuni piccoli peptidi, incluso quelli della parete cellulare e di parecchi antibiotici (es. Gramicidina A) ages/antibiotics_viruses/antibi13.jpg hamburg.de/bonline/library/micro229/ terry/229sp00/lectures/ cells2.html Gramicidina Polipeptide con L &D aminoacidi alternati, composti con la formula generale: formil L X Gly L Ala D Leu L Ala D Val L Val D Val L Trp D Leu L Y D Leu L Trp D Leu L Trpetanolamina. E attiva contro batteri Gram positivi, tranne che per bacilli Gram positivi, e contro organismi selezionati Gram negativi, quali i batteri Neisseria. Amminoacidi CATEGORIE 10
11 Ionizzazione degli AA polari previsti di carica Ac. glutammico A ph fisiologico (ph ~ 7.0) praticamente tutti i residui di ac. glutammico sono carichi negativamente A ph fisiologico praticamente tutti i residui di lisina sono carichi positivamente Lisina Polari carichi (1) Aminoacidi polari carichi basici (al ph tipico dei liquido biologici, ~ 7) 11
12 Aminoacidi polari carichi acidi (al ph tipico dei liquido biologici, ~ 7) Polari ma privi di carica Non Polari (Idrofobici) (1) Catene laterali con proprietà particolari Quanto maggiori sono le dimensioni dei gruppi laterali tanto più idrofobico sarà l aminoacido CISTEINA: Sebbene la catena laterale abbia un carattere polare non carico, ha la particolarità di costitutire un legame covalente con un altra cisteina, per formare ponti disolfuro (S S), che irrigidiscono la catena. GLICINA: la catena laterale è formata solo da un atomo di H e può adattarsi sia ad un ambiente idrofilo che idrofobico. Spesso si trova in siti dove due polipeptidi sono a stretto contatto PROLINA. Sebbene la catena laterale abbia carattere polare non carico, ha la particolarità di creare snodi nelle catene polipeptidiche ed interrompere la struttura secondaria ordinata 12
13 Ponti disulfuro (S-S) tra residui di cisteina FORMAZIONE DI PONTI S-S NELLE PROTEINE Questi legami incrociati possono collegare sia due parti della stessa catena polipeptidica che due catene polipeptidiche diverse. Poiché l energia necessaria per rompere un legame covalente è molto superiore all energia necessaria per rompere persino un intero insieme di legami non covalenti, un legame disulfuro può avere un effetto stabilizzante notevole in una proteina. Tipica proteina con diversi legami S S (1) Tipica proteina transmembrana a passaggio singolo single-pass. Si noti che la catena lipidica attraversa il doppio strato lipidico come α-elica destrogira e che le catene oligosaccaridiche e i legami disolfuro sono tutti sulla superficie non citosolica della membrana. I legami disolfuro non si formano fra i gruppi sulfidrilici nel dominio citoplasmatico della proteina, perchè l ambiente riducente del citosol mantiene questi gruppi nella loro forma ridotta (-SH). Tipica proteina con diversi legami S S (2) /?report=objectonly Una molecola di anticorpo. (A) Una tipica molecola di anticorpo ha la forma a Y e ha due siti di legame identici per il suo antigene, uno in ciascuna delle braccia della Y. La proteina è composta da quattro catene polipeptidiche (due catene pesanti identiche e due catene leggere identiche e più piccole) tenute insieme da legami disulfuro. Ogni catena è fatta da diversi domini di tipo immunoglobulina, qui ombreggiati sia in azzurro che in grigio. Il sito di legame con l antigene si forma laddove un dominio variabile della catena pesante (V H ) e un dominio variabile della catena leggera (V L ) vengono a contatto. Questi sono i domini che differiscono di più in sequenza e struttura nei diversi anticorpi. 13
14 Formazione del legame peptidico (1) Amminoacidi LEGAME PEPTIDICO Formazione del legame peptidico (2) Gli amminoacidi hanno un impalcatura idrofilica che può formare catene e uno fra i 20 diversi tipi di catene laterali, che possono essere idrofiliche o idrofobiche. (A)I legami peptidici si formano fra il gruppo NH 2 di un aminoacido e il gruppo COOH di un altro, con la formazione e perdita di una molecola di acqua. R n, catena laterale dell aminoacido. (B) Una proteina ha un impalcatura polipeptidica con diversi gruppi laterali degli aminoacidi H. Kreuzer & A. Massey: Biology and Biotechnology: Science, Applications and Issues ASM Press, Washington, D.C., Una proteina è una catena di aminoacidi che si piega in una conformazione tridimensionale specifica. H. Kreuzer & A. Massey: Biology and Biotechnology: Science, Applications and Issues ASM Press, Washington, D.C.,
15 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE STRUTTURA PROTEINE (1) Cooper: the Cell, a Molecular Approach, 2 nd ed. Natura ierarchica della struttura delle proteine Struttura Primaria (Sequenza di AA) Struttura Secondaria (α-elica, β-foglietto) StrutturaTerziaria (struttura 3D formata dall assemblaggio di strutture secondarie) Struttura Quaternaria (Struttura formata da più di una catena polipeptidica) 15
16 STRUTTURA PRIMARIA DELLE PROTEINE (1) STRUTTURA PROTEINE (3) E la sequenza lineare specifica degli AA che compongono la catena. Determina da sola il ripiegamento della proteina. Con 20 diversi AA il n di differenti polipeptidi che si possono formare è di 20 n dove n è il n di AA della catena. /SBI3U/Class_Summary/class_summary_spring_2009_sbi3u. html Questa grave malattia ereditaria deriva da un unico cambiamento nella sequenza amminoacidica della molecola di emoglobina: nella proteina mutata una VALINA (AA non polare) si trova al posto di un ACIDO GLUTAMICO (AA polare carico). Anemia falciforme (1) («Sickle cell anemia») VALINA Ac. GLUTAMICO Anemia falciforme (2) Le persone con anemia falciforme ( sickle cell anemia ) producono una forma di emoglobina A diversa, detta emoglobina S (S sta per sickle ). Gli eritrociti che contengono sopratutto l emoglobina S non hanno un tempo di vita lungo quanto i globuli rossi normali (che di solito è di 16 giorni). Inoltre diventano più rigide, distorte in forma e hanno difficoltà a passare attraverso i vasi sanguigni più sottili (capillari). Quando un eritrocito falciforme blocca un vaso sanguigno sottile, la quantità di sangue che raggiunge quella parte del corpo è inferiore. Il tessuto che non riceve un normale flusso sanguigno finisce per diventare danneggiato. Ci sono diverse forme di anemia falciforme. Le più comuni sono: Sickle Cell Anemia (SS), Sickle Hemoglobin C Disease (SC), la Sickle Beta Plus Thalassemia e la Sickle Beta Zero Thalassemia. 16
17 Struttura secondaria α elica & foglietto β La struttura secondaria rappresenta la conformazione ordinata che alcuni tratti di proteina possono assumere, sulla base della struttura primaria, cioè della sequenza aminoacidica. La struttura secondaria è caratterizzata dalla presenza di ponti idrogeno fra i gruppi del legame peptidico di residui non adiacenti, mentre non sono direttamente coinvolte le catene laterali degli aminoacidi. All'interno della stessa proteina, diversi tratti possono assumere la medesima struttura secondaria o strutture secondarie differenti. Le principali forme di strutture secondarie presenti nelle proteine sono l'α elica e le strutture β foglietto. IMPORTANZA DEI PONTI DI IDROGENO PER LA FORMAZIONE DI UN ELICA E DI ALTRE STRUTTURE ORDINATE Una elica si forma quando una serie di subunità si legano una all altra in modo regolare α elica (1) α elica (2) A529/ 17
18 β foglietto (1) β foglietto (2) Note sul ripiegamento delle proteine (1) Note sul ripiegamento delle proteine (2) L acqua contiene due legami polari ossigeno idrogeno ed è una molecola estremamente polare. Perciò si associa confortevolmente con altre molecole polari o cariche elettricamente. Per questa ragione, le molecole che sono elettrostaticamente cariche o polari sono IDROFILICHE. Poichè le molecole non polari non si associano confortevolmente con l acqua, esse sono IDROFOBICHE. Le catene laterali idrofobiche (non polari) degli amminoacidi non si associano stabilmente con il fluido intracellulare (o extracellulare). Viceversa, le catene laterali idrofiliche degli amminoacidi (cariche o polari) si possono associare stabilmente con il fluido perchè le loro cariche, o cariche parziali possono essere neutralizzate dalle cariche parziali complementari delle molecole polari dell acqua. Una regola basilare che determina la struttura delle proteine in ambiente acquoso è, per quanto possibile, il ripiegamento dei gruppi laterali idrofobici concentrandoli all interno della proteina, così creando un ambiente idrofobico privo di acqua. Le catene laterali idrofiliche sono invece stabili quando esposte al citoplasma sulla superficie della proteina. 18
19 Note sul ripiegamento delle proteine (3) Si dice perciò che una proteina in un ambiente acquoso contiene una zona centrale ( core ; nocciolo) idrofobica e stabile. La struttura tridimensionale di ogni singola proteina (STRUTTURA TERZIARIA) può essere vista come la migliore soluzione al problema di creare la zona centrale idrofobica per ogni struttura primaria. Questo presenta un ulteriore problema: l impalcatura/asse comune (sequenza di legami peptidici) contiene un gran numero di legami NH e CO, che sono altamente polari. Note sul ripiegamento delle proteine (4) Alla superficie della proteina questi legami parzialmente carichi possono essere prontamente neutralizzati mediante legami di idrogeno con l acqua. Tuttavia, perchè una struttura proteica sia stabile le cariche parziali dell impalcatura polipeptidica debbono essere neutralizzate anche all interno della proteina, dove l acqua non è presente. Note sul ripiegamento delle proteine (5) La soluzione di questo problema è un fattore di importanza fondamentale che determina la struttura della proteina: L asse della proteina deve neutralizzare le sue stesse cariche parziali. I gruppi NH possono formare legami d idrogeno con i gruppi CO, neutralizzandosi a vicenda. Per costrizioni geometriche, i gruppi CO e NH dello stesso amminoacido non sono in posizione tale da poter formare ponti d idrogeno l uno con l altro. Viceversa, l asse polipeptidico deve essere disposto accuratamente in posizione tale che gruppi NH e CO lungo l asse siano in posizione da potere formare ponti d idrogeno con gruppi complementari in altre posizioni lungo l asse. L elica e il foglietto (STRUTTURE SECONDARIE) sono le due disposizioni più comunemente riscontrate nelle proteine che permettono la formazione dei legami d idrogeno. 19
20 Three-dimensional structure of proteins Struttura terziaria Tertiary structure Quaternary structure Struttura terziaria Fosfoglicerato chinasi Gli elementi strutturali (spirali e tornanti, eliche, filamenti e stratti) si combinano a formare «motivi». I motivi a loro volta si combinano a formare «domini». Le proteine di piccole dimensioni possono formare un solo dominio. Le proteine di maggiori dimensioni sono combinazione di domini. La struttura prodotta dall organizzazione di elementi strutturali in domini nella struttura globale viene chiamata struttura terziaria della proteina. In genere i domini si comportano come se potessero avere esistenza e stabilità indipendenti. Struttura terziaria 20
21 Struttura quaternaria Struttura quaternaria (1) Molte proteine contengono più di una catena polipeptidica. L interazione tra queste catene sta alla base della struttura quaternaria. Le interazioni sono esattamente le stesse che determinano la struttura terziaria (ponti S S, ponti di idrogeno, interazioni ioniche e interazioni idrofobiche) solo con l eccezione che hanno luogo fra una o più catene polipeptidiche, dette «subunità». D. Whitford: «Proteins: Structure and Function». Wiley, Struttura quaternaria (2) Può essere basata su subunità identiche o subunità diverse: Omodimeri: es. triosifosfato isomerasi (enzima coinvolto nella glicolisi), HIV proteasi, molti fattori di trascrizione. Trimero: es. proteina MS2 del capside virale Tetramero: es. emoglobina, con due diverse subunità: 2 subunità α e 2 subunità β. Struttura quaternaria (3) La corretta attività funzionale della proteine richiede la formazione della struttura quaternaria e la specifica associazione della subunità. Nonostante singolarmente le forze siano deboli, esse sono numerose e portano all assemblaggio delle subunità ed ad aumentata stabilità. La struttura quaternaria permette la formazione di siti di catalisi o di legame nell interfaccia fra le unità; tali siti sono impossibili da trovare nelle proteine monomeriche. D. Whitford: «Proteins: Structure and Function». Wiley, D. Whitford: «Proteins: Structure and Function». Wiley,
22 Struttura quaternaria (4) HIV proteasi Ulteriori vantaggi derivano dal fatto che il legame con il substrato della reazione catalitica o con il ligando provoca alterazioni conformazionali all interno di tutto il complesso e offre la possibilità di regolazione dell attività biologica BASE PER LA REGOLAZIONE ALLOSTERICA DELLE PROTEINE. Permette quindi una grande versatilità di funzioni. ase_1eby.png Complesso fra fattore di trascrizione T box /DNA D. Whitford: «Proteins: Structure and Function». Wiley, grenoble.fr/groups/dna/t.gif Altre proteine con struttura quaternaria (1) Dimero della Triosifosfato isomerasi Triosifosfato isomerasi Integrina 22
23 Mioglobina e emoglobina Mioglobina (Non ha struttura quaternaria) e/a271/ html Hematology Allosteria nel legame con l ossigeno delle subunità dell emoglobina La cooperatività aumenta la quantità di ossigeno rilasciata dall emoglobina. Poichè la cooperatività fra i siti di legame con l O2, l emoglobina rilascia più O2 ai tessuti di quanto non faccia una proteina non cooperativa (po2, pressione parziale di ossigeno). 23
Macromolecole biologiche
 MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
Proteine 26/10/2015. Continuazione. Vantaggio di avere un intermediario tra il DNA e le proteine che codifica
 Dogma Centrale della Biologia (parere classico) (Francis Crick, 1958) in biologia molecolare il flusso dell informazione genetica è monodirezionale Proteine Continuazione L informazione scorrerebbe dal
Dogma Centrale della Biologia (parere classico) (Francis Crick, 1958) in biologia molecolare il flusso dell informazione genetica è monodirezionale Proteine Continuazione L informazione scorrerebbe dal
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
Macromolecole biologiche
 MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE NUCLEOTIDI ACIDI NUCLEICI Molecole
Macromolecole biologiche
 MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE Biologia della Cellula Animale
MACROMOLECOLE BIOLOGICHE & COSTITUENTI DI BASE Macromolecole biologiche 1. Introduzione ZUCCHERI POLISACCARIDI ACIDI GRASSI GRASSI, LIPIDI, MEMBRANE AMMINOACIDI PROTEINE Biologia della Cellula Animale
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
02/03/2016. Importanza dei legami non covalenti in Biologia. Legami covalenti (1) Legami covalenti
 Legami covalenti Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di atomi. La formazione del legame covalente si basa
Legami covalenti Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di atomi. La formazione del legame covalente si basa
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
IPOTESI UN GENE-UN ENZIMA
 IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
LA SINTESI PROTEICA LE MOLECOLE CHE INTERVENGONO IN TALE PROCESSO SONO:
 LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
DOGMA CENTRALE DELLA BIOLOGIA. Secondo il dogma centrale della biologia, il DNA dirige la. sintesi del RNA che a sua volta guida la sintesi delle
 DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Introduzione al Citoscheletro
 http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
COME È FATTO? Ogni filamento corrisponde ad una catena di nucleotidi
 Il DNA Il DNA è una sostanza che si trova in ogni cellula e contiene tutte le informazioni sulla forma e sulle funzioni di ogni essere vivente: eppure è una molecola incredibilmente semplice. COME È FATTO?
Il DNA Il DNA è una sostanza che si trova in ogni cellula e contiene tutte le informazioni sulla forma e sulle funzioni di ogni essere vivente: eppure è una molecola incredibilmente semplice. COME È FATTO?
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
IL DOGMA CENTRALE DELLA BIOLOGIA RNA
 La traduzione IL DOGMA CENTRALE DELLA BIOLOGIA Trascrizione DNA Passaggio dell informazione contenuta nel DNA mediante la sintesi di RNA RNA Proteine Duplicazione DNA Traduzione Costruzione della catena
La traduzione IL DOGMA CENTRALE DELLA BIOLOGIA Trascrizione DNA Passaggio dell informazione contenuta nel DNA mediante la sintesi di RNA RNA Proteine Duplicazione DNA Traduzione Costruzione della catena
TRASCRIZIONE DEL DNA. Formazione mrna
 TRASCRIZIONE DEL DNA Formazione mrna Trascrizione Processo mediante il quale l informazione contenuta in una sequenza di DNA (gene) viene copiata in una sequenza complementare di RNA dall enzima RNA polimerasi
TRASCRIZIONE DEL DNA Formazione mrna Trascrizione Processo mediante il quale l informazione contenuta in una sequenza di DNA (gene) viene copiata in una sequenza complementare di RNA dall enzima RNA polimerasi
Di cosa è fatta una cellula?
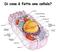 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
TRASCRIZIONE e TRADUZIONE
 TRASCRIZIONE e TRADUZIONE Trascrizione e traduzione Dogma centrale della biologia molecolare: processo con cui l informazione contenuta nel DNA dirige la sintesi delle proteine. Trascrizione Maturazione
TRASCRIZIONE e TRADUZIONE Trascrizione e traduzione Dogma centrale della biologia molecolare: processo con cui l informazione contenuta nel DNA dirige la sintesi delle proteine. Trascrizione Maturazione
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Sequenze nucleotidiche del DNA definite loci costituiscono i geni. Ogni gene codifica per una specifica proteina
 sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
02/12/2014. Tutti gli esseri viventi sono composti da cellule LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI
 Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Di cosa è fatta una cellula?
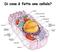 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
LA TRASCRIZIONE. Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene
 LA TRASCRIZIONE Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene GLI ACIDI RIBONUCLEICI Nelle cellule nucleate la sintesi proteica avviene nel citoplasma, mentre il DNA si
LA TRASCRIZIONE Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene GLI ACIDI RIBONUCLEICI Nelle cellule nucleate la sintesi proteica avviene nel citoplasma, mentre il DNA si
Le Biomolecole II parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione
 Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione CdL Tecnici di Lab Biomedico AA. 2011-12 - Prof.ssa Frabetti Come si esprime l informazione? Per i geni classici vedremo:
Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione CdL Tecnici di Lab Biomedico AA. 2011-12 - Prof.ssa Frabetti Come si esprime l informazione? Per i geni classici vedremo:
Amminoacidi/peptidi/proteine. Chimica Organica II
 Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI
 Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
Dal Genotipo al Fenotipo
 Dal Genotipo al Fenotipo Dal Fenotipo normale al Fenotipo patologico Regolazione dell espressione genica Figure 7-1 Molecular Biology of the Cell ( Garland Science 2008) Una cellula differenziata contiene
Dal Genotipo al Fenotipo Dal Fenotipo normale al Fenotipo patologico Regolazione dell espressione genica Figure 7-1 Molecular Biology of the Cell ( Garland Science 2008) Una cellula differenziata contiene
La chimica della vita
 La chimica della vita Ogni organismo vivente è una macchina sofisticata, risultato di un complesso insieme di reazioni chimiche. La costruzione e il funzionamento di questa macchina si devono all'esistenza
La chimica della vita Ogni organismo vivente è una macchina sofisticata, risultato di un complesso insieme di reazioni chimiche. La costruzione e il funzionamento di questa macchina si devono all'esistenza
Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei.
 DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Regolazione dell espressione genica
 Regolazione dell espressione genica definizioni Gene attivato quando viene trascritto in RNA e il suo messaggio tradotto in molecole proteiche specifiche Espressione genica processo complessivo con cui
Regolazione dell espressione genica definizioni Gene attivato quando viene trascritto in RNA e il suo messaggio tradotto in molecole proteiche specifiche Espressione genica processo complessivo con cui
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Codice Genetico (segue) 04/11/2015. «Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO
 «Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO http://www.atdbio.com/img/articles/rna wobble base pairs large.png CODICE GENETICO Codice mediante il quale la sequenza nucleotidica
«Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO http://www.atdbio.com/img/articles/rna wobble base pairs large.png CODICE GENETICO Codice mediante il quale la sequenza nucleotidica
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
10/30/16. non modificato CAP al 5 e poly-a al 3. RNA messaggero: soggetto a splicing
 procarioti eucarioti poli-cistronico mono-cistronico non modificato CAP al 5 e poly-a al 3 RNA messaggero: procarioti eucarioti policistronico monocistronico non modificato CAP al 5 e poly-a al 3 continuo
procarioti eucarioti poli-cistronico mono-cistronico non modificato CAP al 5 e poly-a al 3 RNA messaggero: procarioti eucarioti policistronico monocistronico non modificato CAP al 5 e poly-a al 3 continuo
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
07/01/2015. Come si ferma una macchina in corsa? Il terminatore. Terminazione intrinseca (rho-indipendente)
 Come si ferma una macchina in corsa? Il terminatore Terminazione intrinseca (rho-indipendente) Terminazione dipendente dal fattore Rho (r) 1 Operoni: gruppi di geni parte di una unica unità trascrizionale
Come si ferma una macchina in corsa? Il terminatore Terminazione intrinseca (rho-indipendente) Terminazione dipendente dal fattore Rho (r) 1 Operoni: gruppi di geni parte di una unica unità trascrizionale
INDICE PARTE I CHIMICA. Autori Introduzione
 INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Tutta la vita cellulare ha le seguenti caratteristiche in comune. tutte le cellule hanno una membrana cellulare che separa il liquido extracellulare
 Tutta la vita cellulare ha le seguenti caratteristiche in comune. tutte le cellule hanno una membrana cellulare che separa il liquido extracellulare dal citoplasma cellulare che ha un alto grado di organizzazione.
Tutta la vita cellulare ha le seguenti caratteristiche in comune. tutte le cellule hanno una membrana cellulare che separa il liquido extracellulare dal citoplasma cellulare che ha un alto grado di organizzazione.
E. Giordano 16/09/2010
 GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Codice Genetico (segue)
 CODICE GENETICO Nucleotidi, acidi nucleici CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. Consiste
CODICE GENETICO Nucleotidi, acidi nucleici CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. Consiste
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
Le proprietà elettive della cellula: Espressione della informazione genetica e differenziamento II Trascrizione- Codice genetico- Traduzione
 Le proprietà elettive della cellula: Espressione della informazione genetica e differenziamento II Trascrizione- odice genetico- Traduzione dl Infermieristica aa. 2011/12 Prof.ssa Frabetti ESPRESSIONE
Le proprietà elettive della cellula: Espressione della informazione genetica e differenziamento II Trascrizione- odice genetico- Traduzione dl Infermieristica aa. 2011/12 Prof.ssa Frabetti ESPRESSIONE
