La superconduttività. Sergio Caprara
|
|
|
- Nicolo Bartolini
- 5 anni fa
- Visualizzazioni
Transcript
1 La superconduttività Sergio Caprara
2 Prologo tra atomi e molecole La materia è fatta di atomi Gli atomi sono costituiti da un nucleo, contenente protoni (+) e neutroni, e da una nube di elettroni (-) Le proprietà chimiche di ciascun elemento sono determinate dal numero atomico Z (numero di protoni = numero di elettroni)
3 Prologo tra atomi e molecole Secondo il modello di Bohr li elettroni negli atomi si dispongono in orbitali a cui corrisponde una determinata energia, di modo che ogni atomo è caratterizzato da una serie di livelli energetici e può assorbire o cedere energia soltanto in quantità determinate ( spettri di righe). Il riempimento dei livelli obbedisce al principio di Pauli
4 Prologo tra atomi e molecole Gli elettroni negli orbitali più vicini al nucleo sono più fortemente legati, mentre gli elettroni più periferici (elettroni di valenza) determinano le proprietà chimiche dell elemento ( sistema periodico) Gli atomi tendono a condividere gli elettroni di valenza con altri atomi, formando molecole Gli orbitali atomici, combinandosi, formano gli orbitali molecolari (Heitler e London)
5
6 La materia Le molecole si attraggono Alle alte temperature (o basse densità) l attrazione non è sufficiente a tenere insieme le molecole e la materia si presenta allo stato gassoso Riducendo la temperatura (o aumentando la densità) l attrazione ha la meglio e la materia condensa nello stato liquido
7 La materia A temperature ancora più basse (o densità più elevate), la materia si presenta allo stato solido Un solido cristallino è realizzato da una disposizione regolare di atomi, è come un enorme molecola Gli elettroni in un solido occupano orbitali a ciascuno dei quali corrisponde un energia ben definita
8 Isolanti e conduttori Gli elettroni in un solido riempiono i livelli energetici obbedendo al principio di Pauli Se l ultimo livello occupato (livello di Fermi) è separato dal primo livello vuoto (gap) si ha un isolante (o dielettrico) Se l ultimo livello riempito è adiacente ad un livello vuoto si ha un conduttore
9 nodo Bande di valenza Larghezza di banda orbitali molecolari antileganti vuota piena gap Numero di orbitali atomici orbitali molecolari leganti gap Bande di core gap
10 Correnti elettriche: le leggi di Ohm Un conduttore in equilibrio elettrostatico espelle il campo elettrico e si mantiene a potenziale costante Applicando una differenza di potenziale ai capi di un conduttore si realizza uno stato di non equilibrio caratterizzato da una corrente elettrica (moto ordinato degli elettroni di conduzione)
11 Correnti elettriche: le leggi di Ohm 1. L intensità della corrente I e la differenza di potenziale V sono proporzionali: V = RI (resistenza elettrica) 2. La resistenza è direttamente proporzionale alla lunghezza L e inversamente proporzionale alla sezione S del conduttore: R = ρl/s (resistività)
12 V (V) I (A)
13 Materiali Rame Grafite Acqua di mare Conducibilità elettrica (S/m) Resistività (Ω m) Silicio Salgemma 21 ordini di grandezza! Acqua distillata Marmo Mica Paraffina Quarzo fuso
14 Correnti elettriche: le leggi di Ohm 3. La resistività di un conduttore cresce con la temperatura T : ρ = ρ 0 [ 1 + α (T T 0 ) ] Ad alta temperatura la resistività è dovuta alle oscillazioni del reticolo cristallino A bassa temperatura la resistività è dovuta ai difetti del reticolo cristallino (resistenza residua)
15 Metallo ρ (Ω m) T (K)
16 Heike Kamerlingh Onnes a Leida Liquefazione dell elio (T liq =4,2 K, 1908) Superconduttività del Mercurio (T c =4,2 K, 1911) Premio Nobel per la Fisica (1913) resistenza (Ω) temperatura (K)
17 ρ superconduttore metallo normale T c T
18 Effetto Meissner-Ochsenfeld Diamagnetismo perfetto: un superconduttore espelle il campo magnetico (1933) Levitazione Lo stato superconduttore è uno stato di equilibrio termodinamico
19 Effetto Meissner-Ochsenfeld
20 Fenomenologia dei superconduttori La superconduttività esiste solo per T<T c, B<B c0 (e I<I c0 ) Il calore specifico è discontinuo per T=T c (condensazione) ed è soppresso a basse temperature (gap) Campo magnetico Stato superconduttore Temperatura Stato metallico normale Calore specifico Superconduttore Temperatura Metallo Niobio Tantalio Stagno Teoria BCS
21 Elementi superconduttori Elementi superconduttori sotto pressione Elementi superconduttori in film sottili Elementi superconduttori dopo irradiazione
22 Teorie fenomenologiche della superconduttività Fritz & Heinz London sviluppano l elettrodinamica dei superconduttori e spiegano l effetto Meissner- Ochsenfeld (1935) Vitalij L. Ginzburg & Lev D. Landau spiegano le proprietà termodinamiche dei superconduttori (1950)
23 La teoria BCS Bardeen, Cooper & Shrieffer nel 1957 formulano la teoria microscopica della superconduttività (Nobel nel 1972): la deformazione del reticolo cristallino rende possibile la formazione di coppie di elettroni con un energia di legame Δ (gap). Le coppie non possono perdere energia negli urti con i difetti del reticolo spin Elettrone 1 Elettrone 2 velocità
24 Niobio Tantalio Stagno Teoria BCS Gap Δ (T c - T) (K) Effetto isotopico T c ω reticolo (K/M) M
25 Flash Mob in occasione del centenario (2011)
26 L album di famiglia della superconduttività Muller & Bednorz (Nobel 1987) Temperatura critica (K) Azoto liquido a base di rame a base di ferro Anno
27 La superconduttività nella vita di tutti i giorni
28 Grazie per l attenzione
CENNI SULLA TEORIA DEGLI ORBITALI MOLECOLARI
 CENNI SULLA TEORIA DEGLI ORBITALI MOLECOLARI Gli orbitali molecolari si ottengono dalla combinazione lineare degli orbitali atomici. Il numero di orbitali molecolari è pari al numero degli orbitali atomici
CENNI SULLA TEORIA DEGLI ORBITALI MOLECOLARI Gli orbitali molecolari si ottengono dalla combinazione lineare degli orbitali atomici. Il numero di orbitali molecolari è pari al numero degli orbitali atomici
Legame Covalente Polare e MOT. Polarità del legame aumenta con differenza di elettronegatività.
 Legame Covalente Polare e MOT Polarità del legame aumenta con differenza di elettronegatività. Legame Ionico Se differenza di elettronegatività è molto grande si ottiene un legame ionico. Legame Ionico
Legame Covalente Polare e MOT Polarità del legame aumenta con differenza di elettronegatività. Legame Ionico Se differenza di elettronegatività è molto grande si ottiene un legame ionico. Legame Ionico
ELETTRICITÀ CORRENTE CONTINUA LEZIONE N. 29
 LEZIONE N. 29 (LA CONDUZIONE ELETTRICA NEI METALLI) Nei metalli gli atomi sono talmente vicini che qualche elettrone esterno viene a trovarsi nel campo elettrico dell atomo più vicino. Per questo motivo
LEZIONE N. 29 (LA CONDUZIONE ELETTRICA NEI METALLI) Nei metalli gli atomi sono talmente vicini che qualche elettrone esterno viene a trovarsi nel campo elettrico dell atomo più vicino. Per questo motivo
Cenni sulla teoria dell orbitale molecolare
 Cenni sulla teoria dell orbitale molecolare Legame chimico: teoria dell orbitale molecolare (MO) La formazione della molecola genera ORBITALI MOLECOLARI che derivano dalla combinazione degli ORBITALI ATOMICI.
Cenni sulla teoria dell orbitale molecolare Legame chimico: teoria dell orbitale molecolare (MO) La formazione della molecola genera ORBITALI MOLECOLARI che derivano dalla combinazione degli ORBITALI ATOMICI.
S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009
 S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009 Conduzione elettrica nei metalli (conduttori e semiconduttori) Corso di Laboratorio di Didattica
S.I.C.S.I. Scuola Interuniversitaria Campana di Specializzazione all Insegnamento VIII ciclo - a.a. 2008/2009 Conduzione elettrica nei metalli (conduttori e semiconduttori) Corso di Laboratorio di Didattica
Elettroni negli Atomi
 Elettroni negli Atomi Solo alcune orbite sono stabili In realtànon sonoorbitema FUNZIONI D ONDA Ψ Ψ 2 è la DENSITA di probabilità di trovare l elettrone in una certa posizione rispetto al nucleo Le varie
Elettroni negli Atomi Solo alcune orbite sono stabili In realtànon sonoorbitema FUNZIONI D ONDA Ψ Ψ 2 è la DENSITA di probabilità di trovare l elettrone in una certa posizione rispetto al nucleo Le varie
Legame metallico. Metalli
 LEGAME METALLICO Un metallo può essere descritto come un reticolo di ioni positivi (nucleo più elettroni di core) immersi in una nube di elettroni di valenza mobili (delocalizzati) attorno ai cationi.
LEGAME METALLICO Un metallo può essere descritto come un reticolo di ioni positivi (nucleo più elettroni di core) immersi in una nube di elettroni di valenza mobili (delocalizzati) attorno ai cationi.
Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) A cura del Prof S. Giannitto
 Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) APPUNTI DI TDP- TEORIA 3 ANNO A cura del Prof S. Giannitto La molecola è la più piccola parte che si può ottenere da un corpo conservandone
Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) APPUNTI DI TDP- TEORIA 3 ANNO A cura del Prof S. Giannitto La molecola è la più piccola parte che si può ottenere da un corpo conservandone
CONDUTTORI E SUPERCONDUTTORI
 CONDUTTORI E SUPERCONDUTTORI Vera Montalbano Dipartimento di Fisica Università di Siena Riserva Naturale del Pigelleto 5-8 settembre 2011 Mille e una energia: dal sole a Fukushima CARICHE ELETTRICHE E
CONDUTTORI E SUPERCONDUTTORI Vera Montalbano Dipartimento di Fisica Università di Siena Riserva Naturale del Pigelleto 5-8 settembre 2011 Mille e una energia: dal sole a Fukushima CARICHE ELETTRICHE E
I FENOMENI ELETTRICI CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE
 CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE I FENOMENI ELETTRICI CARICA ELETTRICA FORZA DI COULOMB CAMPO ELETTRICO E POTENZIALE ELETTRICO CORRENTE E LEGGI DI OHM RESISTENZA
CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE I FENOMENI ELETTRICI CARICA ELETTRICA FORZA DI COULOMB CAMPO ELETTRICO E POTENZIALE ELETTRICO CORRENTE E LEGGI DI OHM RESISTENZA
FASE. Diversi stati fisici della materia e forme alternative di un medesimo stato fisico.
 FASE Diversi stati fisici della materia e forme alternative di un medesimo stato fisico. Esempi di fase sono il ghiaccio e l acqua liquida. Il diamante e la grafite sono due fasi del carbonio allo stato
FASE Diversi stati fisici della materia e forme alternative di un medesimo stato fisico. Esempi di fase sono il ghiaccio e l acqua liquida. Il diamante e la grafite sono due fasi del carbonio allo stato
Cenni sulla struttura della materia
 Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
IL LEGAME METALLICO 1
 IL LEGAME METALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli Elevata conducibilità elettrica; Elevata conducibilità termica; Effetto fotoelettrico; Elevata duttilità e malleabilità; Lucentezza;
IL LEGAME METALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli Elevata conducibilità elettrica; Elevata conducibilità termica; Effetto fotoelettrico; Elevata duttilità e malleabilità; Lucentezza;
Gas ultrafreddi di atomi fermonici e la bosonizzazione dei fermioni
 Gas ultrafreddi di atomi fermonici e la bosonizzazione dei fermioni Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova Congresso Nazionale SIF Tavola rotonda Enrico
Gas ultrafreddi di atomi fermonici e la bosonizzazione dei fermioni Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova Congresso Nazionale SIF Tavola rotonda Enrico
STRUTTURA ATOMICA. tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica
 STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
Molti ceramici sono sempre più utilizzati nel settore dell elettrotecnica e dell elettronica. La conducibilità di tipo elettronica o ionica può
 Molti ceramici sono sempre più utilizzati nel settore dell elettrotecnica e dell elettronica. La conducibilità di tipo elettronica o ionica può essere molto variabile a seconda della composizione: si passa
Molti ceramici sono sempre più utilizzati nel settore dell elettrotecnica e dell elettronica. La conducibilità di tipo elettronica o ionica può essere molto variabile a seconda della composizione: si passa
Esame di stato 2014_2 2 M.Vincoli
 Esame di stato 0_ M.Vincoli . Per semplificare i calcoli, evitando altresì di introdurre immediatamente grandezze numeriche, è utile adottare una notazione semplificatrice, per cui poniamo:, 0 0,,0 0,60
Esame di stato 0_ M.Vincoli . Per semplificare i calcoli, evitando altresì di introdurre immediatamente grandezze numeriche, è utile adottare una notazione semplificatrice, per cui poniamo:, 0 0,,0 0,60
Carica elettrica. Costituzione dell atomo: nucleo con protoni (carica +e) e neutroni (carica 0) elettroni (carica -e) orbitanti attorno al nucleo
 I FENOMENI ELETTRICI Carica elettrica Forza di Coulomb Potenziale elettrico Intensità di corrente Leggi di Ohm Resistenza e resistività Effetto termico della corrente Carica elettrica Proprietà elettriche
I FENOMENI ELETTRICI Carica elettrica Forza di Coulomb Potenziale elettrico Intensità di corrente Leggi di Ohm Resistenza e resistività Effetto termico della corrente Carica elettrica Proprietà elettriche
IL LEGAME METALLICO 1
 IL LEGAME METALLICO 1 Modello semplificato di un reticolo metallico Mare di elettroni di valenza, molto mobili e delocalizzati Cationi disposti secondo un reticolo ordinato 2 Non metalli Metalli Metalloidi
IL LEGAME METALLICO 1 Modello semplificato di un reticolo metallico Mare di elettroni di valenza, molto mobili e delocalizzati Cationi disposti secondo un reticolo ordinato 2 Non metalli Metalli Metalloidi
11 aprile Annalisa Tirella.
 Scienze dei Materiali A.A. 2010/2011 11 aprile 2011 Annalisa Tirella a.tirella@centropiaggio.unipi.it Metalli I metalli sono elementi chimici che possono essere utilizzati sia puri che in forma di leghe
Scienze dei Materiali A.A. 2010/2011 11 aprile 2011 Annalisa Tirella a.tirella@centropiaggio.unipi.it Metalli I metalli sono elementi chimici che possono essere utilizzati sia puri che in forma di leghe
(2) cubico a facce centrate (3) esagonale compatto
 IL LEGAME METALLICO La maggior parte dei metalli cristallizza in strutture a massimo impacchettamento, ovvero in solidi in cui si può considerare che gli ioni metallici che occupano le posizioni reticolari,
IL LEGAME METALLICO La maggior parte dei metalli cristallizza in strutture a massimo impacchettamento, ovvero in solidi in cui si può considerare che gli ioni metallici che occupano le posizioni reticolari,
Corso di Elettronica Industriale (CdL in Ingegneria Meccatronica, sede di Mantova) Semiconduttori intrinseci e drogati
 Corso di Elettronica Industriale (CdL in Ingegneria Meccatronica, sede di Mantova) Isolanti, conduttori e semiconduttori In un solido si può avere conduzione di carica elettrica (quindi passaggio di corrente)
Corso di Elettronica Industriale (CdL in Ingegneria Meccatronica, sede di Mantova) Isolanti, conduttori e semiconduttori In un solido si può avere conduzione di carica elettrica (quindi passaggio di corrente)
Ministero dell Istruzione, dell Università e della Ricerca
 Pag. / Sessione ordinaria 014 Seconda prova scritta Ministero dell Istruzione, dell Università e della icerca BST ESAME DI STATO DI LICEO SCIENTIFICO COSI SPEIMENTALI Tema di: FISICA Secondo tema Nel circuito
Pag. / Sessione ordinaria 014 Seconda prova scritta Ministero dell Istruzione, dell Università e della icerca BST ESAME DI STATO DI LICEO SCIENTIFICO COSI SPEIMENTALI Tema di: FISICA Secondo tema Nel circuito
Storia Il fenomeno della superconduttività fu scoperto nel mercurio nel 1911 dal fisico olandese Heike Kamerlingh Onnes,[1] che anche per questo motiv
![Storia Il fenomeno della superconduttività fu scoperto nel mercurio nel 1911 dal fisico olandese Heike Kamerlingh Onnes,[1] che anche per questo motiv Storia Il fenomeno della superconduttività fu scoperto nel mercurio nel 1911 dal fisico olandese Heike Kamerlingh Onnes,[1] che anche per questo motiv](/thumbs/91/105950244.jpg) Superconduttività La superconduttività o superconduzione, è un fenomeno fisico non descrivibile con la fisica classica, scoperto per la prima volta nel 1911 da Heike Kamerlingh Onnes,[1] il quale notò
Superconduttività La superconduttività o superconduzione, è un fenomeno fisico non descrivibile con la fisica classica, scoperto per la prima volta nel 1911 da Heike Kamerlingh Onnes,[1] il quale notò
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica. legami tra molecole più stabili
 I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
CENNI TEORIA ORBITALE MOLECOLARE
 CENNI TEORIA ORBITALE MOLECOLARE Teoria più avanzata: spiega anche perché O 2 è paramagnetico. Ne illustreremo la applicazione solo per molecole biatomiche E 2 del secondo periodo. Orbitali molecolari:
CENNI TEORIA ORBITALE MOLECOLARE Teoria più avanzata: spiega anche perché O 2 è paramagnetico. Ne illustreremo la applicazione solo per molecole biatomiche E 2 del secondo periodo. Orbitali molecolari:
1. L energia di legame. 2. I gas nobili e a regola dell ottetto. 3. Il legame covalente. 4. Il legame covalente dativo. 5. Il legame covalente polare
 Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
4πε. h m. Eq. di Schrödinger per un atomo di idrogeno:
 Eq. di Schrödinger per un atomo di idrogeno: h m e 1 ψ 4πε r 0 ( r) = Eψ ( r) Questa equazione è esattamente risolubile ed il risultato sono degli orbitali di energia definita E n = m e 1 α 1 1 e mc n
Eq. di Schrödinger per un atomo di idrogeno: h m e 1 ψ 4πε r 0 ( r) = Eψ ( r) Questa equazione è esattamente risolubile ed il risultato sono degli orbitali di energia definita E n = m e 1 α 1 1 e mc n
IL LEGAME METALLICO 1
 IL LEGAME METALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli Elevata conducibilità elettrica; Elevata conducibilità termica; Effetto fotoelettrico; Elevata duttilità e malleabilità; Lucentezza;
IL LEGAME METALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli Elevata conducibilità elettrica; Elevata conducibilità termica; Effetto fotoelettrico; Elevata duttilità e malleabilità; Lucentezza;
Carica elettrica. Costituzione dell atomo: nucleo con protoni (carica +e) e neutroni (carica 0) elettroni (carica -e) orbitanti attorno al nucleo
 I FENOMENI ELETTRICI Carica elettrica Forza di Coulomb Campo elettrico Potenziale elettrico Intensità di corrente Leggi di Ohm Resistenza e resistivita Effetto termico della corrente Elettrolisi Carica
I FENOMENI ELETTRICI Carica elettrica Forza di Coulomb Campo elettrico Potenziale elettrico Intensità di corrente Leggi di Ohm Resistenza e resistivita Effetto termico della corrente Elettrolisi Carica
Introduzione. Corso di Laurea in Informatica. c/o: Dipartimento di Fisica. Sito web:
 Introduzione Corso di Laurea in Informatica Corso di Fisica dei Dispositivi Elettronici Docente: c/o: Dipartimento di Fisica E-Mail: leonello.servoli@pg.infn.it Sito web: http://cms.pg.infn.it/servoli
Introduzione Corso di Laurea in Informatica Corso di Fisica dei Dispositivi Elettronici Docente: c/o: Dipartimento di Fisica E-Mail: leonello.servoli@pg.infn.it Sito web: http://cms.pg.infn.it/servoli
IL LEGAME METALLICO. Metalli
 IL LGAM MTALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli levata conducibilità elettrica; levata conducibilità termica; ffetto fotoelettrico; levata duttilità e malleabilità; Lucentezza;
IL LGAM MTALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli levata conducibilità elettrica; levata conducibilità termica; ffetto fotoelettrico; levata duttilità e malleabilità; Lucentezza;
Prof.ssa Silvia Martini. L.S. Francesco D Assisi
 Prof.ssa Silvia Martini L.S. Francesco D Assisi Modello atomico Bande di energia in un cristallo Le sostanze solide possono essere suddivise in tre categorie: isolanti, conduttori e semiconduttori. I livelli
Prof.ssa Silvia Martini L.S. Francesco D Assisi Modello atomico Bande di energia in un cristallo Le sostanze solide possono essere suddivise in tre categorie: isolanti, conduttori e semiconduttori. I livelli
Dispositivi elettronici
 Dispositivi elettronici Sommario Richiami sui semiconduttori conduttori, isolanti e semiconduttori bande di energia droganti nei semiconduttori corrente di deriva e diffusione Funzionamento della giunzione
Dispositivi elettronici Sommario Richiami sui semiconduttori conduttori, isolanti e semiconduttori bande di energia droganti nei semiconduttori corrente di deriva e diffusione Funzionamento della giunzione
T08: Dispositivi elettronici (3.3.1)
 T08: Dispositivi elettronici (3.3.1) Sommario Richiami sui semiconduttori conduttori, isolanti e semiconduttori bande di energia droganti nei semiconduttori corrente di deriva e diffusione Funzionamento
T08: Dispositivi elettronici (3.3.1) Sommario Richiami sui semiconduttori conduttori, isolanti e semiconduttori bande di energia droganti nei semiconduttori corrente di deriva e diffusione Funzionamento
Conduttori Semiconduttori Isolanti cm 3. Diamante = = 0.14
 30 48 IIB Zn IIIA IVA VA VIA 5 6 7 8 B C N O Boro Carbonio Azoto Ossigeno 13 14 15 16 Alluminio Silicio Fosforo Zolfo 31 32 33 34 Zinco Gallio Germanio Arsenico Selenio Cd Al Si P S Ga Ge As Se 49 50 51
30 48 IIB Zn IIIA IVA VA VIA 5 6 7 8 B C N O Boro Carbonio Azoto Ossigeno 13 14 15 16 Alluminio Silicio Fosforo Zolfo 31 32 33 34 Zinco Gallio Germanio Arsenico Selenio Cd Al Si P S Ga Ge As Se 49 50 51
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il
LA M A T E R I A. Ma, allora chiediamoci come è fatta la materia?
 LA M A T E R I A Nel mese di marzo 2007, alcuni scienziati tedeschi ed americani hanno dato l annuncio di avere creato il materiale più piccolo mai esistito al mondo e lo hanno chiamato grafene ( vedi
LA M A T E R I A Nel mese di marzo 2007, alcuni scienziati tedeschi ed americani hanno dato l annuncio di avere creato il materiale più piccolo mai esistito al mondo e lo hanno chiamato grafene ( vedi
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO L'atomo è costituito da un nucleo centrale costituito da protoni (carica positiva 1,62*10-19 coulomb) e neutroni (privi di carica), intorno al quale ruotano uno o più elettroni (carica
STRUTTURA DELL'ATOMO L'atomo è costituito da un nucleo centrale costituito da protoni (carica positiva 1,62*10-19 coulomb) e neutroni (privi di carica), intorno al quale ruotano uno o più elettroni (carica
I legami chimici. Perché si formano i legami? Perché si formano i legami? 16/01/2019. Come e perché gli atomi si legano tra loro
 I legami chimici Come e perché gli atomi si legano tra loro Perché si formano i legami? In natura, se non in casi eccezionali, non si trovano atomi liberi. Per separare due atomi legati è necessario fornire
I legami chimici Come e perché gli atomi si legano tra loro Perché si formano i legami? In natura, se non in casi eccezionali, non si trovano atomi liberi. Per separare due atomi legati è necessario fornire
ELETTRICITA. numero PROTONI = numero ELETTRONI
 STRUTTURA DELL ELETTRICITA MOLECOLA La materia è formata da molecole. Le molecole sono formate da atomi. In natura esistono 92 tipi di atomi. Molecola di acqua Ogni atomo è formato da un nucleo costituito
STRUTTURA DELL ELETTRICITA MOLECOLA La materia è formata da molecole. Le molecole sono formate da atomi. In natura esistono 92 tipi di atomi. Molecola di acqua Ogni atomo è formato da un nucleo costituito
1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno 5. Legami a confronto
 Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia
 Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
1. L energia di legame
 legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
Proprietà elettriche della materia
 Proprietà elettriche della materia Conduttori Materiali in cui le cariche elettriche scorrono con facilità. In un metallo gli elettroni più esterni di ciascun atomo formano una specie di gas all interno
Proprietà elettriche della materia Conduttori Materiali in cui le cariche elettriche scorrono con facilità. In un metallo gli elettroni più esterni di ciascun atomo formano una specie di gas all interno
Concetti fondamentali
 Indice CAPITOLO 1 CAPITOLO 2 Prefazione XI Concetti fondamentali 1.1 Chimica, chimica ovunque (con le dovute scuse a Samuel Taylor Coleridge) 2 1.2 Atomi come mattoni da costruzione: la teoria atomica
Indice CAPITOLO 1 CAPITOLO 2 Prefazione XI Concetti fondamentali 1.1 Chimica, chimica ovunque (con le dovute scuse a Samuel Taylor Coleridge) 2 1.2 Atomi come mattoni da costruzione: la teoria atomica
I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni.
 I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni. PLS 2016/17 Prof. Daniela Cavalcoli Dip di Fisica e Astronomia Università di Bologna Daniela.Cavalcoli@unibo.it outline I solidi
I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni. PLS 2016/17 Prof. Daniela Cavalcoli Dip di Fisica e Astronomia Università di Bologna Daniela.Cavalcoli@unibo.it outline I solidi
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
conduttori isolanti semiconduttori In un metallo la banda più esterna che contiene elettroni è detta banda di valenza
 Un solido sarà conduttore solo se la banda è parzialmente occupata. Se invece la banda è completamente occupata si possono avere due casi: se la banda successiva è molto alta in energia il solido è un
Un solido sarà conduttore solo se la banda è parzialmente occupata. Se invece la banda è completamente occupata si possono avere due casi: se la banda successiva è molto alta in energia il solido è un
Corso di fisica applicata con elementi di fisica tecnica A.A. 2016/2017
 Corso di fisica applicata con elementi di fisica tecnica A.A. 2016/2017 Programma svolto Lezione 1 Carica elettrica, legge di Coulomb, campo elettrico, potenziale elettrico Breve storia dell elettricità
Corso di fisica applicata con elementi di fisica tecnica A.A. 2016/2017 Programma svolto Lezione 1 Carica elettrica, legge di Coulomb, campo elettrico, potenziale elettrico Breve storia dell elettricità
Lezione 8. Cenni di struttura della materia
 Lezione 8 Cenni di struttura della materia Struttura della materia La meccanica, di cui ci siamo occupati finora, ha studiato il moto di corpi solidi sotto l azione di forze generiche e in particolare
Lezione 8 Cenni di struttura della materia Struttura della materia La meccanica, di cui ci siamo occupati finora, ha studiato il moto di corpi solidi sotto l azione di forze generiche e in particolare
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 15 Le forze intermolecolari e gli stati condensati della materia 3 Sommario 1. Le forze intermolecolari 2. Molecole polari e
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 15 Le forze intermolecolari e gli stati condensati della materia 3 Sommario 1. Le forze intermolecolari 2. Molecole polari e
Forma e proprietà dell orbitale 1s
 Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
l evoluzione dell elettronica
 1904 tubo a vuoto 1968 circuito integrato l evoluzione dell elettronica 1980 integrati VLSI 1947 transistor oggi integrati ULSI 1971 microprocessore diodi transistor tecnologie costruttive grafici, tabelle,
1904 tubo a vuoto 1968 circuito integrato l evoluzione dell elettronica 1980 integrati VLSI 1947 transistor oggi integrati ULSI 1971 microprocessore diodi transistor tecnologie costruttive grafici, tabelle,
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
il diodo a giunzione transistori ad effetto di campo (FETs) il transistore bipolare (BJT)
 Contenuti del corso Parte I: Introduzione e concetti fondamentali richiami di teoria dei circuiti la simulazione circuitale con SPICE elementi di Elettronica dello stato solido Parte II: Dispositivi Elettronici
Contenuti del corso Parte I: Introduzione e concetti fondamentali richiami di teoria dei circuiti la simulazione circuitale con SPICE elementi di Elettronica dello stato solido Parte II: Dispositivi Elettronici
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni.
 I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni. PLS 2018/19 Prof. Beatrice Fraboni Dip di Fisica e Astronomia Università di Bologna beatrice.fraboni@unibo.it outline I solidi cristallini
I metalli e i semiconduttori, le proprietà elettriche. Le applicazioni. PLS 2018/19 Prof. Beatrice Fraboni Dip di Fisica e Astronomia Università di Bologna beatrice.fraboni@unibo.it outline I solidi cristallini
Il Legame Ionico. Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B -
 Il Legame Ionico Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B - A + B - Le coppie di ioni si attraggono elettrostaticamente Il
Il Legame Ionico Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B - A + B - Le coppie di ioni si attraggono elettrostaticamente Il
ATOMO. Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas)
 http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI
 ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Corrente elettrica. In questo tratto di conduttore in cui si è stabilita una certa corrente, passa una carica dq nel tempo dt.
 Corrente elettrica La corrente elettrica è data da un flusso netto di cariche in moto. Gli elettroni di conduzione, all interno di un filo isolato di rame, si muovono in modo casuale a una velocità di
Corrente elettrica La corrente elettrica è data da un flusso netto di cariche in moto. Gli elettroni di conduzione, all interno di un filo isolato di rame, si muovono in modo casuale a una velocità di
XIV Indice ISBN
 Indice 1 Struttura della materia.................................... 1 1.1 Stati di aggregazione.................................... 1 1.2 Struttura atomistica.................................... 2 1.2.1
Indice 1 Struttura della materia.................................... 1 1.1 Stati di aggregazione.................................... 1 1.2 Struttura atomistica.................................... 2 1.2.1
Dispositivi Elettronici. Proprietà elettriche dei materiali
 Dispositivi Elettronici Proprietà elettriche dei materiali Proprietà elettriche I materiali vengono classificati in: isolanti o dielettrici (quarzo o SiO 2, ceramiche, materiali polimerici) conduttori
Dispositivi Elettronici Proprietà elettriche dei materiali Proprietà elettriche I materiali vengono classificati in: isolanti o dielettrici (quarzo o SiO 2, ceramiche, materiali polimerici) conduttori
I numeri quantici. Numero quantico principale, n: numero intero Caratterizza l energia dell elettrone
 I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
dq dt Università degli Studi di Bari Aldo Moro Dip. DiSAAT - Ing. Francesco Santoro Corso di Fisica
 Corrente elettrica Consideriamo il moto non accelerato e con velocità piccole rispetto a quella della luce nel vuoto di un insieme di particelle dotate di carica elettrica: possono ritenersi valide le
Corrente elettrica Consideriamo il moto non accelerato e con velocità piccole rispetto a quella della luce nel vuoto di un insieme di particelle dotate di carica elettrica: possono ritenersi valide le
Secondo tema. Risoluzione del problema Il testo stabilisce che il resistore con resistenza R 3 dissipa una potenza P 3 = 40,0 W. Dalla relazione (18)
 Secondo tema Nel circuito riportato in figura V = 3,60 10 2 V, R 1 = 1,20 10 2 Ω, R 2 = 2,40 10 2 Ω, R 3 = 3,60 10 2 Ω, R 4 è un resistore variabile di resistenza massima pari a 1,80 10 2 Ω. Considerando
Secondo tema Nel circuito riportato in figura V = 3,60 10 2 V, R 1 = 1,20 10 2 Ω, R 2 = 2,40 10 2 Ω, R 3 = 3,60 10 2 Ω, R 4 è un resistore variabile di resistenza massima pari a 1,80 10 2 Ω. Considerando
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
Definizioni. Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 1828
 CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
combinazione di atomi tenuti insieme da forze più o meno un insieme caratteristico di proprietà
 IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Stati della materia. Stati della materia
 Stati della materia La materia può esistere in 3 diversi STATI DI AGGREGAZIONE: SOLIDO LIQUIDO GASSOSO MACROSCOPICHE MICROSCOPICHE Stati della materia Lo stato di aggregazione di una sostanza dipende dal
Stati della materia La materia può esistere in 3 diversi STATI DI AGGREGAZIONE: SOLIDO LIQUIDO GASSOSO MACROSCOPICHE MICROSCOPICHE Stati della materia Lo stato di aggregazione di una sostanza dipende dal
satura SOLUZIONE concentrata diluita MISCUGLIO ETEROGENEO Sospensione (acqua e polvere di marmo) Miscuglio solido (es. sabbia)
 MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
Semiconduttori. Bande di energia. Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare
 Semiconduttori Bande di energia Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare Quando gli atomi formano un cristallo, il moto degli elettroni dello strato
Semiconduttori Bande di energia Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare Quando gli atomi formano un cristallo, il moto degli elettroni dello strato
Figura 3.1: Semiconduttori.
 Capitolo 3 Semiconduttori Con il termine semiconduttori si indicano alcuni elementi delle colonne III, IV e V della tavola periodica, caratterizzati da una resistività elettrica ρ intermedia tra quella
Capitolo 3 Semiconduttori Con il termine semiconduttori si indicano alcuni elementi delle colonne III, IV e V della tavola periodica, caratterizzati da una resistività elettrica ρ intermedia tra quella
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
COSTRUZIONE DI UN SUPERCONDUTTORE ED EFFETTO MEISSNER
 In collaborazione con Piano nazionale Lauree Scientifiche Dipartimento di Fisica dell Università di Roma Tor Vergata COSTRUZIONE DI UN SUPERCONDUTTORE ED EFFETTO MEISSNER Storia Il fenomeno della superconduttività
In collaborazione con Piano nazionale Lauree Scientifiche Dipartimento di Fisica dell Università di Roma Tor Vergata COSTRUZIONE DI UN SUPERCONDUTTORE ED EFFETTO MEISSNER Storia Il fenomeno della superconduttività
Principio dell Aufbau (riempimento)
 LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
I legami chimici. Programma: a che punto siamo? Funzioni di stato. Corso di Studi di Fisica Corso di Chimica. Luigi Cerruti
 Corso di Studi di Fisica Corso di Chimica Programma: a che punto siamo? Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica Programma: a che punto siamo? Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 Programma: a che punto siamo? I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 Programma: a che punto siamo? I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Testo di riferimento: Millman-Grabel MICROELECTRONICS McGraw Hill Cap. 1: 1,2,3,4 Cap. 2: 1,2,3,4,6,7,8,(9,10). Cap. 3: 1,2,4,5,6,8,9,10.
 Esperimentazioni di Fisica 3 AA 20122013 Semiconduttori Conduzione nei semiconduttori Semiconduttori intrinseci ed estrinseci (drogati) La giunzione pn Il diodo a semiconduttore Semplici circuiti con diodi
Esperimentazioni di Fisica 3 AA 20122013 Semiconduttori Conduzione nei semiconduttori Semiconduttori intrinseci ed estrinseci (drogati) La giunzione pn Il diodo a semiconduttore Semplici circuiti con diodi
La corrente elettrica
 1 La corrente elettrica All interno di ogni conduttore metallico vi sono degli elettroni che sono debolmente legati ai nuclei. Questi elettroni sono liberi di muoversi all interno del metallo e sono detti
1 La corrente elettrica All interno di ogni conduttore metallico vi sono degli elettroni che sono debolmente legati ai nuclei. Questi elettroni sono liberi di muoversi all interno del metallo e sono detti
OVERVIEW. Teoria atomica e tavola periodica. Legami e interazioni degli atomi
 OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
Materiale Energy Gap
 Semiconduttori Materiale diamante silicio germanio Energy Gap 5,3 ev 1,1 ev 0,7 ev 21 Semiconduttori Quando un elettrone, portatore di carica negativa, è promosso da banda di valenza a banda di conduzione,
Semiconduttori Materiale diamante silicio germanio Energy Gap 5,3 ev 1,1 ev 0,7 ev 21 Semiconduttori Quando un elettrone, portatore di carica negativa, è promosso da banda di valenza a banda di conduzione,
Il potenziale elettrico. Lezioni d'autore
 Il potenziale elettrico Lezioni d'autore Introduzione: i superconduttori VIDEO Introduzione: Gli elettroni nei superconduttori VIDEO Potenziale ed energia potenziale (I) In meccanica data una forza è possibile
Il potenziale elettrico Lezioni d'autore Introduzione: i superconduttori VIDEO Introduzione: Gli elettroni nei superconduttori VIDEO Potenziale ed energia potenziale (I) In meccanica data una forza è possibile
SCIENZA E TECNOLOGIA DEI MATERIALI
 Laurea Specialistica in Ingegneria Meccanica anno acc. 2007/08 25/09/2007 Scienza e Tecnologia dei Materiali Lez. 01 1 SCIENZA E TECNOLOGIA DEI MATERIALI Gianfranco Dell Agli Ufficio (piano 1) Laboratorio
Laurea Specialistica in Ingegneria Meccanica anno acc. 2007/08 25/09/2007 Scienza e Tecnologia dei Materiali Lez. 01 1 SCIENZA E TECNOLOGIA DEI MATERIALI Gianfranco Dell Agli Ufficio (piano 1) Laboratorio
I MATERIALI. Presentazione a cura di Prof. Ramona Sola
 I MATERIALI Presentazione a cura di Prof. Ramona Sola I materiali sono così radicati nella nostra cultura che quasi non ce rendiamo conto Ogni aspetto della nostra vita è influenzato dal materiale Casa/edifici
I MATERIALI Presentazione a cura di Prof. Ramona Sola I materiali sono così radicati nella nostra cultura che quasi non ce rendiamo conto Ogni aspetto della nostra vita è influenzato dal materiale Casa/edifici
VERIFICA Dalla tavola periodica al modello atomico
 VERIFICA Dalla tavola periodica al modello atomico Cognome Nome Classe Data I/1 Vero o Falso? Scegli per ciascuna risposta l'alternativa corretta V F Nella tavola periodica ogni elemento è contrassegnato
VERIFICA Dalla tavola periodica al modello atomico Cognome Nome Classe Data I/1 Vero o Falso? Scegli per ciascuna risposta l'alternativa corretta V F Nella tavola periodica ogni elemento è contrassegnato
Il legame chimico. Legame metallico
 Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
I legami chimici. (parte seconda) Lezioni d'autore
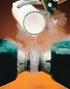 I legami chimici (parte seconda) Lezioni d'autore Introduzione (I) La teoria del legame di Lewis considera gli elettroni di valenza degli atomi che formano legami, ma prescinde totalmente dal fatto che
I legami chimici (parte seconda) Lezioni d'autore Introduzione (I) La teoria del legame di Lewis considera gli elettroni di valenza degli atomi che formano legami, ma prescinde totalmente dal fatto che
Fenomeni elettrici e magnetici
 Fenomeni elettrici e magnetici Le forze elettromagnetiche sono percepibili nella maggior parte dei fenomeni che avvengono in natura Caricamento elettrostatico di un corpo per strofinamento Fulmine Magnetismo
Fenomeni elettrici e magnetici Le forze elettromagnetiche sono percepibili nella maggior parte dei fenomeni che avvengono in natura Caricamento elettrostatico di un corpo per strofinamento Fulmine Magnetismo
