PRINCIPI FONDAMENTALI DELLA COMBUSTIONE
|
|
|
- Cecilia Mariotti
- 9 anni fa
- Просмотров:
Транскрипт
1 DEFINIZINE DELLA CMBUSTINE PRINCIPI FNDAMENTALI DELLA CMBUSTINE CAPITL 1 La combustione è la rapida ossidazione di un combustibile. La reazione è accompagnata da quel fenomeno fisico visibile che è denominato fiamma e dalla produzione di quella energia che è denominata calore. Il carbonio si combina con l ossigeno per formare anidride carbonica, un gas non tossico, e libera calore secondo la seguente formula: C 2 = C 2 Calore Analogamente l idrogeno si combina con l ossigeno per formare vapore d acqua, con conseguente produzione di calore, secondo la formula seguente: = 2 2 Calore È importante rilevare che il combustibile e l ossigeno si combinano in proporzioni ben definite e fisse. Le quantità di ossigeno e di combustibile nella miscela sono in proporzioni perfette o stechiometriche quando queste permettono una completa ossidazione del combustibile senza residui di ossigeno. Se avessimo eccesso di combustibile oppure insufficienza di ossigeno diremmo che la miscela è ricca e che la fiamma è riducente e tende ad essere lunga, gialla e fumosa. Tale tipo di combustione è anche definita combinazione incompleta perché, sebbene alcune delle particelle del combustibile vengano completamente ossidate dall ossigeno, altre invece non ne ricevono a sufficienza e ne consegue che la combustione di queste è parziale. Come indica la seguente formula di reazione, la combustione parziale o incompleta del carbonio è accompagnata dalla formazione di ossido di carbonio, un gas fortemente tossico: 2C 2 = 2C Calore La quantità di calore che qui si produce è inferiore a quella che accompagna la combustione completa. Una combustione incompleta o riducente è a volte richiesta in speciali trattamenti termici industriali, ma in qualsiasi altra circostanza tali condizioni debbono essere evitate. Se viceversa fornissimo alla miscela ossigeno in eccesso, diremmo che la miscela è povera e che la combustione è ossidante. Come risultato avremmo una fiamma molto corta di colore tendente al blu. Come meglio spiegheremo più avanti, il gas ossidante normalmente impiegato è l aria, cioè una miscela di ossigeno ed azoto. Quando si impiega aria in eccesso, cioè una quantità di ossigeno superiore a quella stechiometrica, avviene che tutto l azoto e la parte di ossigeno che non si combina con il combustibile non partecipano alla reazione di ossidazione. Naturalmente essi assorbono una certa quantità del calore prodotto durante la combustione di modo che l energia calorifica risultante rimane distribuita in un maggior volume di gas ed il livello termico è inferiore (minore temperatura di fiamma). CMBUSTIBILI GASSSI CMMERCIALI Questi gas hanno caratteristiche variabili che dipendono dalla quantità di ciascun elemento chimico. Diamo alcune caratteristiche fondamentali medie, dei gas più comunemente usati. PTERE CALRIFIC TIP DI GAS PRINCIPALI CSTITUENTI INFERIRE - kcal/m³ DENSITÀ VELCITÀ DI PRPAGAZINE DELLA FIAMMA - m/s Gas di città C ,56 3 Gas miscelato C 2 C 4 o altri ,60 1,5 Gas naturale C ,64 0,6 Miscela propano/aria C 3 8 aria ,20 0,7 Propano C ,52 0,7 Butano C ,00 0,7 Miscela propano/butano C 3 8 C ,75 0,7 eadquarters Esa S.r.l. Via E. Fermi 40 I Curno (BG) - Italy Tel Fax [email protected] - International Sales Pyronics International S.A./N.V. Zoning Ind., 4ème rue B-6040 Jumet - Belgium Tel Fax [email protected]
2 STECIMETRIA DELLA CMBUSTINE DEI GAS Per semplicità, nella seguente discussione, abbiamo assunto che il gas naturale contenga unicamente metano (C 4 ). Il metano brucia secondo la seguente reazione: C = C Calore cioè: Metano ssigeno = Anidride Carbonica Vapore d acqua Calore Dato che i reagenti ed i prodotti della reazione sono tutti allo stato gassoso, possiamo dire che un metro cubo di metano (gas naturale) richiede due metri cubi di ossigeno per la combustione completa e che produrrà nella combustione un metro cubo di anidride carbonica e due metri cubi di vapore d acqua. La reazione dell ossigeno puro e del metano è utilizzata soltanto in alcuni speciali impieghi industriali ed esattamente quando si voglia ottenere una elevata temperatura di fiamma: ad esempio nei cannelli per taglio. Tuttavia, la maggioranza delle applicazioni industriali di combustione utilizza l aria come sorgente comburente anziché l ossigeno puro. Per semplicità di calcolo possiamo considerare l aria come composta di 20% di ossigeno e di 80% di azoto. Pertanto dato che per ogni metro cubo di metano avremo bisogno di 10 m³ di aria, si avrà: 10 ARIA = 2 2 8N 2 La reazione di combustione del metano e dell aria può pertanto essere scritta così: C N 2 = C N 2 Calore Nella chimica della combustione, le molecole di azoto sono inerti e pertanto non hanno alcuna funzione. Purtroppo esse assorbono un po del calore prodotto. Concludendo si può dire che per bruciare completamente un metro cubo di gas naturale sono necessari 10 m³ di aria. La combustione del propano è viceversa regolata dalla seguente reazione: C N 2 = 3C N 2 Calore Ciò conferma che 1 m³ di propano richiede 25 m³ di aria per la sua completa combustione. Dalle reazioni del metano e del propano appena illustrate, possiamo facilmente dedurre che per liberare calore pari a kcal utilizzando 1 m³ di gas naturale (il cui potere calorifico inferiore è pari appunto a 8500 kcal/m³) occorrono 10 m³ di aria, mentre per liberare kcal, usando 1 m³ di propano occorrono 25 m³ di aria. Facendo i dovuti rapporti possiamo osservare che sia per il metano che per il propano è valida la legge secondo cui ogni 1000 kcal liberate sono necessari circa 1,18 Normal volumi di aria comburente. Entro certi limiti possiamo dire che ogni gas combustibile commerciale risponde a questa legge; anzi possiamo dire che in linea di massima essa è valida non soltanto per i combustibili gassosi ma anche per quelli solidi e liquidi. QUANTITÀ DI ARIA RICIESTA NELLA CMBUSTINE INDUSTRIALE Tutti i sistemi di combustione ed in particolar modo quelli industriali, sono limitati nella loro potenzialità termica dalla quantità di aria comburente che sono in grado di miscelare al gas. Pertanto la massima portata di gas di un sistema di combustione è determinata dalla massima quantità di aria che lo stesso sistema è in grado di trattare. Nei cataloghi dei costruttori di bruciatori è di solito riportata la capacità dei bruciatori in kcal/h (migliaia di Calorie/ora) erogate. Ciò nonostante agli effetti della progettazione di un sistema di combustione e della selezione dei bruciatori o dei miscelatori necessari a tale sistema, non ci si basa soltanto sulla potenzialità termica e quindi sulla portata di gas del sistema ma anche e soprattutto sulle quantità di aria primaria e secondaria necessaria alla combustione e sulla capacità del sistema di trattare tali quantità. Avendo stabilito che la quantità di aria necessaria alla combustione è di 1,18 Nm³ per ogni kcal prodotte, indipendentemente dal tipo di gas impiegato, si avrà che ogni sistema di combustione industriale su tale principio dimensionato, potrà essere considerato Universale se è in grado di operare con qualsiasi tipo di combustibile gassoso. In altre parole, stabilita la quantità di aria necessaria per ottenere in un sistema una buona combustione ad una determinata potenzialità termica, si potrà usare in quel sistema qualsiasi tipo di combustibile gassoso commerciale per produrre la stessa quantità di calore in perfette condizioni di combustione. L unica modifica richiesta nel passare da un tipo di combustibile ad un altro a parità di portata termica è quella relativa alla quantità di gas necessaria, tenuto conto del potere calorifico per metro cubo di ciascun gas. Ad un sistema di combustione avente una potenzialità termica di kcal/h si debbono fornire 118 Nm³/h di aria per ottenere una combustione perfetta. 2/5
3 Una minore quantità di aria metterebbe il sistema in condizioni di combustione riducente: se si aumentasse la portata del combustibile in modo da erogare kcal/h, e ciò può essere facilmente realizzato aumentando il diametro dell ugello iniettore del bruciatore, si otterrebbero delle condizioni di combustione imperfette se contemporaneamente non si aumentasse in proporzione anche la quantità di aria nella miscela. L unico modo per ottenere sempre perfette condizioni di combustione, volendo aumentare la capacità termica di un sistema di combustione, è di aumentare contemporaneamente la portata di gas e la portata di aria. ARIA PRIMARIA La maggior parte dei sistemi di combustione sono in grado di miscelare al gas combustibile una quantità di aria inferiore a quella teorica richiesta per la combustione prima che la combustione stessa avvenga. La rimanenza dell aria richiesta per bruciare totalmente il combustibile è miscelata dopo il punto di accensione. La quantità di aria miscelata con il gas prima del momento dell accensione è chiamata aria primaria. L aria miscelata dopo il punto di accensione è chiamata aria secondaria. La quantità di aria primaria nella miscela è normalmente espressa in percentuale dell aria totale teorica richiesta per la combustione; ciò comunemente si chiama aerazione. Per esempio un sistema di combustione operante con un gas naturale all 80% di aria primaria vuol dire che tale sistema è in grado di miscelare 8 m³ di aria per ogni metro cubo di gas naturale prima che avvenga la combustione. La rimanente quantità di aria necessaria alla combustione, e cioè gli altri 2 m³ per ogni metro cubo di gas naturale, saranno introdotti dopo l accensione come aria secondaria. Molte delle caratteristiche della fiamma sono determinate dalla quantità di aria primaria che un sistema di combustione è capace di trattare. Quanto minore è la percentuale di aria primaria fornita e tanto più soffice sarà la fiamma. Così dicasi della lunghezza della fiamma che è tanto maggiore quanto minore è la quantità di aria primaria fornita. MECCANICA DELLA CMBUSTINE Le equazioni chimiche indicate precedentemente, relative alla combustione del gas naturale, stabiliscono le quantità di aria e di gas naturale necessarie per ottenere la combustione teorica, nonché la quantità di prodotti della combustione che ne derivano, ma non indicano tuttavia come la reazione procede chimicamente e fisicamente. Le molecole gassose sono in uno stato di costante movimento. La velocità di movimento delle singole molecole è direttamente proporzionale alla loro temperatura: aumentando la temperatura aumenterà anche il movimento delle molecole e viceversa diminuendo la temperatura diminuirà il loro movimento. In una miscela perfetta di ossigeno e gas naturale o metano ci saranno sempre due molecole di ossigeno per ogni molecola di metano. Il metano contiene quattro atomi di idrogeno legati da una valenza chimica all atomo di carbonio; le molecole di ossigeno contengono due atomi di ossigeno legati tra loro da due valenze. C C FM001I01 Perché la combustione avvenga, è naturalmente necessario che gli atomi d idrogeno si separino da quelli di carbonio e che gli atomi di ossigeno si sgancino dai legami che li tengono tra loro uniti di modo che essi siano liberi di combinarsi con il carbonio e l idrogeno. Lo sganciamento degli atomi dell idrogeno, del carbonio e dell ossigeno è il risultato della collisione delle molecole tra loro. Alla normale temperatura ambientale tale collisione è talmente debole che gli atomi non riescono a sganciarsi. Aumentando la temperatura di una miscela di metano e di ossigeno avviene che il calore fornito ai componenti della miscela agisce sulle molecole, aumentandone la velocità di movimento. Raggiunta la temperatura di circa 650 C le molecole hanno ricevuto una quantità di energia sufficiente perché l urto tra loro provochi lo sganciamento degli atomi. Al di sotto di questa temperatura l ossidazione delle molecole del metano è impossibile mentre oltre la barriera dei 650 C gli atomi di carbonio e di idrogeno che si trovano liberi diventano avidi di ossigeno; la combustione ha allora inizio. La reazione chimica di ossidazione degli atomi di idrogeno e carbonio ha come effetto fisico la produzione di fiamma e di calore. Quest ultimo può essere utilizzato per processi termici. Quando si sia innescata la reazione di combustione, cioè quando una certa quantità di molecole di ossigeno e di metano abbiano raggiunto la temperatura di 650 C, avviene che il calore prodotto da questa reazione si irradia uniformemente in tutte le direzioni. Tale calore è sufficiente ad innalzare la temperatura delle molecole circostanti di 3/5
4 metano e di ossigeno oltre la temperatura di scissione degli atomi, di modo che questi a loro volta cominciano a reagire ed a produrre altro calore. La combustione è una reazione a catena che da un gruppo di molecole viene trasmessa a quello prossimo. La velocità con cui questa reazione si trasmette da una molecola all altra determina la velocità di propagazione della fiamma di una miscela. La quantità di calore liberata dalla combustione di una miscela di ossigeno puro e gas naturale è sufficiente per fare raggiungere alla fiamma una temperatura di circa 2850 C. Come abbiamo detto, nei processi industriali di combustione, salvo alcuni casi molto particolari, l ossigeno viene fornito dall aria dell atmosfera. Durante la reazione di combustione l azoto contenuto nell aria assorbe una certa quantità del calore prodotto dalla combustione stessa. Questo fenomeno evidentemente ha come conseguenza l effetto di rallentare il processo di passaggio a catena del calore da una molecola all altra e pertanto di diminuire la velocità di propagazione della fiamma. L azoto è un diluente della reazione di combustione. La massima temperatura teorica ottenibile nella fiamma prodotta dalla combustione di metano e aria è di circa 1930 C; in realtà la massima temperatura ottenibile in un forno industriale alimentato con metano ed aria è di circa 1800 C. Il calore irraggiato dalla fiamma ed altre perdite impediscono di raggiungere la massima temperatura teorica di combustione. Temperature di combustione più alte possono essere raggiunte arricchendo l aria comburente con ossigeno. Ciò ha come effetto di ridurre in proporzione la quantità di azoto presente nella reazione e di conseguenza l effetto diluente. Temperature di fiamma più elevate possono essere inoltre ottenute preriscaldando l aria comburente oppure l aria ed il gas combustibile contemporaneamente in modo da risparmiare una certa quantità di energia calorifica necessaria per innalzare la temperatura delle molecole al valore di accensione. Per esempio, preriscaldando una miscela di aria e gas naturale alla temperatura di 260 C, si può ottenere un incremento della temperatura della fiamma di circa 100 C. CMBUSTINE INCMPLETA - SPEGNIMENT DELLA FIAMMA Ricerche scientifiche della meccanica della combustione hanno dimostrato che il processo chimico della combustione passa attraverso prodotti intermedi prima di arrivare a quelli finali di massima ossidazione consistenti in anidride carbonica e vapore d acqua. I principali prodotti intermedi della combustione sono l ossido di carbonio e le aldeidi. Durante la reazione a catena, dovuta alla collisione delle molecole, che permette l ossidazione degli atomi con la conseguente produzione di calore, si formano questi prodotti intermedi della combustione; rapidamente essi vengono poi a loro volta trasformati da una ulteriore ossidazione via via che giungono in contatto con l ossigeno, in molecole di anidride carbonica e vapore d acqua. Una volta innescata, la reazione di combustione deve essere mantenuta ad una temperatura superiore a quella minima di accensione. Se in un momento qualsiasi, nella massa della fiamma, la miscela in fase di combustione viene raffreddata ad un valore di temperatura inferiore a quello di accensione, il processo di combustione viene arrestato e la fiamma si spegne. Immergendo nella massa di una miscela in fase di combustione un qualsiasi mezzo raffreddante o refrigerante accade che quest ultimo sottrae al processo di combustione una certa quantità di calore di reazione. Se il mezzo raffreddante assorbe calore in misura sufficientemente grande da impedire alle molecole dei componenti della reazione a contatto tra loro di raggiungere la temperatura di accensione, la combustione si arresta del tutto o comunque nei punti di contatto con il mezzo raffreddante. Ciò accadrebbe anche se il combustibile ed il comburente fossero tra loro in rapporto stechiometrico. In pratica i pericoli della combustione incompleta o dello spegnimento della fiamma sono presenti soltanto in applicazioni industriali a basse temperature: ad esempio in impianti di combustione con aria di ricircolo; quest ultima può agire sulla fiamma come mezzo refrigerante. Lunghe fiamme non protette che siano lambite da una forte corrente di aria fredda, possono essere disturbate da quest ultima soprattutto sulla superficie esterna. Anche se nella parte centrale della fiamma la combustione procede ad una temperatura di C, può accadere che la miscela lambente l aria fredda all esterno, sfugga completamente incombusta. L incompleta combustione provocata da un mezzo refrigerante può arrestare la reazione tra combustibile e comburente alle fasi intermedie. In queste condizioni è facile, per chi ha un certo naso, rilevare il caratteristico odore pungente delle aldeidi. Quando si verificano queste anormali condizioni di combustione è bene intervenire, ricercarne le cause ed eliminarle immediatamente. 4/5
5 VELCITA DI PRPAGAZINE DELLA FIAMMA Le miscele aerate al 100% e cioè aventi in sé tutto l ossigeno necessario per completare la combustione, già prima di arrivare al punto in cui inizia la reazione di combustione, hanno la massima velocità di propagazione della fiamma e pertanto realizzano le fiamme più corte a parità di portata di gas. Miscele ricche, che cioè necessitano di una certa quantità di aria secondaria per potere completare la combustione, daranno viceversa luogo a fiamme più lunghe in quanto l aria secondaria richiede un certo tempo per potersi miscelare con il gas combustibile. La velocità di propagazione della fiamma è proporzionale alla quantità di aria premiscelata. In determinate condizioni la velocità di propagazione della fiamma aumenta con l aumentare della rapidità con cui si effettua la miscelazione tra aria e gas. NTA: In base alla propria politica di continuo miglioramento della qualità del prodotto, la ESA-PYRNICS si riserva il diritto di modificare le caratteristiche tecniche del medesimo in qualsiasi momento e senza preavviso. Al nostro sito internet è disponibile il catalogo aggiornato all ultima versione, dal quale è possibile scaricare i documenti modificati. ATTENZINE: Il funzionamento dell'impianto di combustione può risultare pericoloso e causare ferimenti a persone o danni alle attrezzature. gni bruciatore deve essere provvisto di dispositivo di protezione e controllo della combustione. Le operazioni di installazione, regolazione e manutenzione dell'impianto devono essere eseguite solo da personale qualificato. 5/5
MISCELATORI PROPORZIONALI AD EFFETTO VENTURI
 Bollettino E23 rev04 15/05/07 MISCELATORI PROPORZIONALI AD EFFETTO VENTURI SERIE MIDGET-MIXER MM & EMM CARATTERISTICHE Corpo miscelatore: Funzionamento con vari tipi di gas: Funzionamento con: Ingressi
Bollettino E23 rev04 15/05/07 MISCELATORI PROPORZIONALI AD EFFETTO VENTURI SERIE MIDGET-MIXER MM & EMM CARATTERISTICHE Corpo miscelatore: Funzionamento con vari tipi di gas: Funzionamento con: Ingressi
BRUCIATORI AUTORECUPERANTI PER TUBI RADIANTI
 BRUCIATORI AUTORECUPERANTI PER TUBI RADIANTI SERIE SER CARATTERISTICHE Corpo miscelatore: ghisa G25 Tubo parafiamma: AISI310 Testa di combustione: AISI310 Tubo radiante esterno: 25/20 Tubo interno: inconel
BRUCIATORI AUTORECUPERANTI PER TUBI RADIANTI SERIE SER CARATTERISTICHE Corpo miscelatore: ghisa G25 Tubo parafiamma: AISI310 Testa di combustione: AISI310 Tubo radiante esterno: 25/20 Tubo interno: inconel
VALVOLE A FARFALLA FLANGIATE MANUALI E MOTORIZZATE
 VALVOLE A FARFALLA FLANGIATE MANUALI E MOTORIZZATE SERIE WBV E WBV-CMAP CARATTERISTICHE Caratteristiche della valvola a farfalla: Corpo valvola: ghisa Sede valvola: ghisa Disco di chiusura: AISI304 Alberino
VALVOLE A FARFALLA FLANGIATE MANUALI E MOTORIZZATE SERIE WBV E WBV-CMAP CARATTERISTICHE Caratteristiche della valvola a farfalla: Corpo valvola: ghisa Sede valvola: ghisa Disco di chiusura: AISI304 Alberino
BRUCIATORI ALTA VELOCITA`
 CARATTERISTICHE BRUCIATORI ALTA VELOCITA` SERIE HS Bollettino E3505 rev05 31/01/00 Corpo miscelatore: ghisa G25 Piastrone: ghisa G25 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 450 C
CARATTERISTICHE BRUCIATORI ALTA VELOCITA` SERIE HS Bollettino E3505 rev05 31/01/00 Corpo miscelatore: ghisa G25 Piastrone: ghisa G25 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 450 C
BRUCIATORI A RAGGI INFRAROSSI
 BRUCIATORI A RAGGI INFRAROSSI SERIE BR-70 CARATTERISTICHE Bollettino E3005 rev03 31/01/00 Corpo bruciatore: AISI304 Calotta radiante: inconel Miscelatore: ottone Bassa pressione d aria e gas al bruciatore:
BRUCIATORI A RAGGI INFRAROSSI SERIE BR-70 CARATTERISTICHE Bollettino E3005 rev03 31/01/00 Corpo bruciatore: AISI304 Calotta radiante: inconel Miscelatore: ottone Bassa pressione d aria e gas al bruciatore:
BRUCIATORI A FIAMMA PIATTA
 CARATTERISTICHE BRUCIATORI A FIAMMA PIATTA SERIE SW Bollettino E303 rev0 31/01/00 Corpo miscelatore: ghisa G2 Piastrone: ghisa G2 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 40 C Funzionamento
CARATTERISTICHE BRUCIATORI A FIAMMA PIATTA SERIE SW Bollettino E303 rev0 31/01/00 Corpo miscelatore: ghisa G2 Piastrone: ghisa G2 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 40 C Funzionamento
FUNZIONAMENTO DEL VENTURI E DEGLI ORIFICI
 Manuale M000 rev0 04/99 FUNZIONAMENTO DEL VENTURI E DEGLI ORIFICI CAPITOLO Tutti i sistemi di combustione industriale sono costituiti da tre parti principali: ) Il miscelatore, parte del sistema che provvede
Manuale M000 rev0 04/99 FUNZIONAMENTO DEL VENTURI E DEGLI ORIFICI CAPITOLO Tutti i sistemi di combustione industriale sono costituiti da tre parti principali: ) Il miscelatore, parte del sistema che provvede
BRUCIATORI ALTA VELOCITA CON CORPO IN ALLUMINIO
 BRUCIATORI ALTA VELOCITA CON CORPO IN ALLUMINIO SERIE EMB-1A/2A-SIK CARATTERISTICHE Corpo miscelatore Collettore Tubo guidafiamma Tubo gas Testa di combustione Flangia di fissaggio Funzionamento con aria
BRUCIATORI ALTA VELOCITA CON CORPO IN ALLUMINIO SERIE EMB-1A/2A-SIK CARATTERISTICHE Corpo miscelatore Collettore Tubo guidafiamma Tubo gas Testa di combustione Flangia di fissaggio Funzionamento con aria
CASSETTA PER TRASFORMATORI DI ACCENSIONE
 CASSETTA PER TRASFORMATORI DI ACCENSIONE SERIE ESA TRAFO CARATTERISTICHE GENERALI Materiale cassetta: vetro poliestere termoindurente BMC Materiale supporto ESA TRAFO per accoppiamento: acciaio FE37 Temperatura
CASSETTA PER TRASFORMATORI DI ACCENSIONE SERIE ESA TRAFO CARATTERISTICHE GENERALI Materiale cassetta: vetro poliestere termoindurente BMC Materiale supporto ESA TRAFO per accoppiamento: acciaio FE37 Temperatura
Inquinamento ARIA. Inquinamento ARIA. Inquinamento ARIA. Inquinamento ARIA
 COMBUSTIONE: principi Processo di ossidazione di sostanze contenenti C ed H condotto per ottenere energia termica (calore) C,H + O 2 calore + gas comb. COMBUSTIBILE + COMBURENTE CALORE + RESIDUI [ARIA]
COMBUSTIONE: principi Processo di ossidazione di sostanze contenenti C ed H condotto per ottenere energia termica (calore) C,H + O 2 calore + gas comb. COMBUSTIBILE + COMBURENTE CALORE + RESIDUI [ARIA]
CICLI TERMODINAMICI. Introduzione 1
 CICLI TERMODINAMICI Introduzione 1 CICLI TERMODINAMICI CICLO DI CARNOT CICLO RANKINE CICLO BRAYTON CICLO OTTO / CICLO DIESEL IL CICLO DI CARNOT RAPPRESENTA IL MODELLO DA PERSEGUIRE, PERCHE A PARITA DI
CICLI TERMODINAMICI Introduzione 1 CICLI TERMODINAMICI CICLO DI CARNOT CICLO RANKINE CICLO BRAYTON CICLO OTTO / CICLO DIESEL IL CICLO DI CARNOT RAPPRESENTA IL MODELLO DA PERSEGUIRE, PERCHE A PARITA DI
energia Cos è? è un lavoro.
 energia Cos è?! L energia NON si vede, NON si tocca, ma è qualcosa che è dentro, all interno della materia stessa e la rende capace di compiere un lavoro.! ENERGIA E LA CAPACITA' DI UN CORPO O DI UN SISTEMA
energia Cos è?! L energia NON si vede, NON si tocca, ma è qualcosa che è dentro, all interno della materia stessa e la rende capace di compiere un lavoro.! ENERGIA E LA CAPACITA' DI UN CORPO O DI UN SISTEMA
+ + Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria. CH 4 (g)+ 2 O 2 (g) CO 2 (g) + 2 H 2 O(l) 1
 Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria + + 1 molecola di metano (CH 4 ) 2 molecole di ossigeno (O 2 ) 1 molecola di biossido di carbonio (CO 2 ) 2 molecole
Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria + + 1 molecola di metano (CH 4 ) 2 molecole di ossigeno (O 2 ) 1 molecola di biossido di carbonio (CO 2 ) 2 molecole
BRUCIATORI CON FIAMMA A CONO RADIANTE
 BRUCIATORI CON IAMMA A CONO RADIANTE SERIE RAD-65, RAD-120 CARATTERISTICHE Corpo miscelatore: ghisa G25 Piastra di fissaggio WM: ferro Tubo gas: AISI310 unzionamento con aria preriscaldata fino a: 450
BRUCIATORI CON IAMMA A CONO RADIANTE SERIE RAD-65, RAD-120 CARATTERISTICHE Corpo miscelatore: ghisa G25 Piastra di fissaggio WM: ferro Tubo gas: AISI310 unzionamento con aria preriscaldata fino a: 450
BRUCIATORI AD ECCESSO D ARIA
 BRUCIATORI AD ECCESSO D ARIA SERIE XNM CARATTERISTICHE Bollettino E3502 rev06 3/0/00 Corpo miscelatore: ghisa G25 Piastrone: ghisa G25 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 450
BRUCIATORI AD ECCESSO D ARIA SERIE XNM CARATTERISTICHE Bollettino E3502 rev06 3/0/00 Corpo miscelatore: ghisa G25 Piastrone: ghisa G25 Tubo gas: AISI304 Funzionamento con aria preriscaldata fino a: 450
Combustione 2H 2 CO 2. Entalpie standard di combustione
 La combustione è una reazione di ossidoriduzione esotermica in cui si ha l'ossidazione di un combustibile da parte di un comburente (ossigeno presente nell aria), con sviluppo di calore e radiazioni luminose.
La combustione è una reazione di ossidoriduzione esotermica in cui si ha l'ossidazione di un combustibile da parte di un comburente (ossigeno presente nell aria), con sviluppo di calore e radiazioni luminose.
Comburente Solitamente l ossigeno contenuto nell aria o nelle molecole (esplosivi)
 termini Combustione Reazione chimica una sostanza combustibile con l ossigeno accompagnatada da sviluppo calore, fiamma, gas, fumo e luce. Inceno Combustione rapida e non controllata senza limitazioni
termini Combustione Reazione chimica una sostanza combustibile con l ossigeno accompagnatada da sviluppo calore, fiamma, gas, fumo e luce. Inceno Combustione rapida e non controllata senza limitazioni
Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 :
 2.3.1.3 Dinamica dell incendio Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 : Fase di agnizione; Fase di propagazione; Incendio generalizzato
2.3.1.3 Dinamica dell incendio Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 : Fase di agnizione; Fase di propagazione; Incendio generalizzato
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
Azoto. La molecola di azoto e formata da due atomi di azoto, legati insieme con un triplo legame:
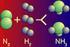 Aria ed atmosfera L aria Questo sottile strato, inodore ed incolore è una miscela di gas: 78 % di azoto; 21 % di ossigeno; 0,03 % di anidride carbonica; 0,97 % altri gas. Azoto La molecola di azoto e formata
Aria ed atmosfera L aria Questo sottile strato, inodore ed incolore è una miscela di gas: 78 % di azoto; 21 % di ossigeno; 0,03 % di anidride carbonica; 0,97 % altri gas. Azoto La molecola di azoto e formata
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
La formazione delle miscele ESPLOSIVE
 La formazione delle miscele ESPLOSIVE Caratterizzazione delle proprietà chimico-fisiche di GAS - VAPORI - POLVERI Atmosfere Esplosive. 8-9 Novembre 2005 Adolfo Buzzoni 1 Definizione: Atmosfera Esplosiva
La formazione delle miscele ESPLOSIVE Caratterizzazione delle proprietà chimico-fisiche di GAS - VAPORI - POLVERI Atmosfere Esplosive. 8-9 Novembre 2005 Adolfo Buzzoni 1 Definizione: Atmosfera Esplosiva
Aspetti formali e ponderali delle reazioni chimiche
 i g t c unità g1 obiettivo x + Aspetti formali e ponderali delle reazioni chimiche 1 L equazione chimica Saper rappresentare una trasformazione chimica mediante un equazione che utilizza simboli e formule
i g t c unità g1 obiettivo x + Aspetti formali e ponderali delle reazioni chimiche 1 L equazione chimica Saper rappresentare una trasformazione chimica mediante un equazione che utilizza simboli e formule
Misure Meccaniche e Termiche
 Misure Meccaniche e Termiche Ing. Daniele Bonomi a.s. 2010/2011 1 di 61 MISURA RENDIMENTO DI COMBUSTIONE SECONDO NORMA UNI 10389 DPR 26 agosto 1993, n. 412 (G. U. n.96 del 14/10/1993) (REGOLAMENTO RECANTE
Misure Meccaniche e Termiche Ing. Daniele Bonomi a.s. 2010/2011 1 di 61 MISURA RENDIMENTO DI COMBUSTIONE SECONDO NORMA UNI 10389 DPR 26 agosto 1993, n. 412 (G. U. n.96 del 14/10/1993) (REGOLAMENTO RECANTE
Combustione. Energia chimica. Energia termica Calore. Combustibili fossili
 Combustione La combustione è un processo di ossidazione rapido con produzione di luce e calore, con trasformazione di energia chimica in energia termica Energia chimica Combustibili fossili Energia termica
Combustione La combustione è un processo di ossidazione rapido con produzione di luce e calore, con trasformazione di energia chimica in energia termica Energia chimica Combustibili fossili Energia termica
COMBUSTIBILI Definizione: sostanze capaci di combinarsi con un comburente sviluppando calore.
 COMBUSTIBILI Definizione: sostanze capaci di combinarsi con un comburente sviluppando calore. La combustione è una reazione di ossidazione il combustibile è la sostanza che si ossida (riducente), il comburente
COMBUSTIBILI Definizione: sostanze capaci di combinarsi con un comburente sviluppando calore. La combustione è una reazione di ossidazione il combustibile è la sostanza che si ossida (riducente), il comburente
Le centrali a combustibile
 Le centrali a combustibile Sono soprattutto centrali termoelettriche che si basano su sistemi di conversione che trasformano l energia chimica dei combustibili fossili (es. carbone) in energia elettrica
Le centrali a combustibile Sono soprattutto centrali termoelettriche che si basano su sistemi di conversione che trasformano l energia chimica dei combustibili fossili (es. carbone) in energia elettrica
Saldatura alla Fiamma Ossiacetilenica
 Di seguito verranno trattati i principali processi di saldatura, in manuale e parzialmente meccanizzato. SALDATURA (PER FUSIONE A GAS) OSSIACETILENICA GENERALITA' E' un processo di saldatura autogena tramite
Di seguito verranno trattati i principali processi di saldatura, in manuale e parzialmente meccanizzato. SALDATURA (PER FUSIONE A GAS) OSSIACETILENICA GENERALITA' E' un processo di saldatura autogena tramite
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Il 'triangolo' del fuoco
 Il 'triangolo' del fuoco Schematizzazione del fenomeno della combustione In corrispondenza, dei vertici del triangolo del fuoco sono indicati tre parametri essenziali del fenomeno della combustione: -
Il 'triangolo' del fuoco Schematizzazione del fenomeno della combustione In corrispondenza, dei vertici del triangolo del fuoco sono indicati tre parametri essenziali del fenomeno della combustione: -
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 3. Le trasformazioni della materia SEGUI LA MAPPA Le leggi 1 Le leggi ANTOINE LAURENT
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 3. Le trasformazioni della materia SEGUI LA MAPPA Le leggi 1 Le leggi ANTOINE LAURENT
le reazioni chimiche
 le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
Appunti di Stechiometria per Chimica REAZIONI CHIMICHE
 Appunti di Stechiometria per Chimica REAZIONI CHIMICHE La reazione chimica è un processo in cui dei composti (reagenti) si trasformano in altri composti (prodotti) mediante una riorganizzazione degli atomi
Appunti di Stechiometria per Chimica REAZIONI CHIMICHE La reazione chimica è un processo in cui dei composti (reagenti) si trasformano in altri composti (prodotti) mediante una riorganizzazione degli atomi
Ing. Enrica Cattaneo
 Ing. Enrica Cattaneo Università di Genova- Facoltà di Architettura INPS- DIREZIONE REGIONALE LIGURIA- CATE IMPIANTI AD ALTA EFFICIENZA ENERGETICA CALDAIA A CONDENSAZIONE 1 Sistemi di generazione La teoria
Ing. Enrica Cattaneo Università di Genova- Facoltà di Architettura INPS- DIREZIONE REGIONALE LIGURIA- CATE IMPIANTI AD ALTA EFFICIENZA ENERGETICA CALDAIA A CONDENSAZIONE 1 Sistemi di generazione La teoria
MISCELATORI PROPORZIONALI AD EFFETTO VENTURI
 MISCELATORI PROPORZIONALI AD EFFETTO VENTURI SERIE FLOMIXER CARATTERISTICHE Struttura: Pressione massima aria: Pressione massima miscela: Ampio range di modulazione. compatta in alluminio 145 mbar 56 mbar
MISCELATORI PROPORZIONALI AD EFFETTO VENTURI SERIE FLOMIXER CARATTERISTICHE Struttura: Pressione massima aria: Pressione massima miscela: Ampio range di modulazione. compatta in alluminio 145 mbar 56 mbar
Principali Caratteristiche di un Combustore GT
 Principali Caratteristiche di un Combustore GT Diversamente dei sistemi di combustione tradizionali i combustori per Turbine a Gas hanno la particolarità di operare con: elevate temperature in ingresso;
Principali Caratteristiche di un Combustore GT Diversamente dei sistemi di combustione tradizionali i combustori per Turbine a Gas hanno la particolarità di operare con: elevate temperature in ingresso;
UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI
 UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI Esercizio 3.1 Calcolare il potere calorifico superiore e inferiore del gas metano che brucia secondo la reazione CH 4 + 2 O 2 CO 2 + 2 H 2 O sapendo che l
UNITA 3 COMBUSTIONE, CARBURANTI, LUBRIFICANTI Esercizio 3.1 Calcolare il potere calorifico superiore e inferiore del gas metano che brucia secondo la reazione CH 4 + 2 O 2 CO 2 + 2 H 2 O sapendo che l
Lezione 20: Atomi e molecole
 Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Capitolo 4 Le teorie della materia
 Atomo: Prime Teorie Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria atomica spiega le leggi ponderali 4. La teoria atomica e le
Atomo: Prime Teorie Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria atomica spiega le leggi ponderali 4. La teoria atomica e le
Corso di Chimica Generale e Inorganica
 Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
Guida pratica. Formatura. Cordone di saldatura senza protezione della radice. Cordone di saldatura con protezione della radice
 Guida pratica. Formatura. Indice: 1. Perché formatura? 2. Forming gas materiali 3. Dispositivi per la formatura 4. Note applicative 5. Sicurezza del lavoro Cordone di saldatura senza protezione della radice
Guida pratica. Formatura. Indice: 1. Perché formatura? 2. Forming gas materiali 3. Dispositivi per la formatura 4. Note applicative 5. Sicurezza del lavoro Cordone di saldatura senza protezione della radice
Appunti di storia della fisica: l atomo
 Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Come funziona un camino? Come funziona un camino?
 AGENDA Come funziona un camino Dimensionamento di un camino Esempi di calcolo Sistemi per stabilizzare il tiraggio Calcolo trasmittanza e resistenza al fuoco dei camini 2 Come funziona un camino? Come
AGENDA Come funziona un camino Dimensionamento di un camino Esempi di calcolo Sistemi per stabilizzare il tiraggio Calcolo trasmittanza e resistenza al fuoco dei camini 2 Come funziona un camino? Come
IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2. Bilanci di energia
 1 IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2 Bilanci di energia 1. Calcolare la quantità di calore ceduta da 1 m 3 di aria a TPS nel raffreddamento da 500 C a 0 C, alla pressione costante di
1 IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2 Bilanci di energia 1. Calcolare la quantità di calore ceduta da 1 m 3 di aria a TPS nel raffreddamento da 500 C a 0 C, alla pressione costante di
Valvole. Valvole a farfalla filettate manuali TBV-M (E1311 rev /03/2017)
 Valvole Valvole a farfalla filettate manuali TBV-M (E1311 rev. 04-09/03/2017) AVVERTENZE GENERALI: SMALTIMENTO: ¾ Tutte le operazioni di installazione, manutenzione, accensione e taratura devono essere
Valvole Valvole a farfalla filettate manuali TBV-M (E1311 rev. 04-09/03/2017) AVVERTENZE GENERALI: SMALTIMENTO: ¾ Tutte le operazioni di installazione, manutenzione, accensione e taratura devono essere
Reazione chimica In una reazione chimica le sostanze di partenza sono dette reagenti; le sostanze che si ottengono sono dette prodotti della reazione.
 Reazioni chimiche Reazione chimica Tutte le volte che una o più sostanze si trasformano in altre si verifica una reazione chimica. Una reazione chimica è il processo che porta alla rottura di alcuni legami
Reazioni chimiche Reazione chimica Tutte le volte che una o più sostanze si trasformano in altre si verifica una reazione chimica. Una reazione chimica è il processo che porta alla rottura di alcuni legami
COME RISOLVERE ESERCIZI SULLE LEGGI PONDERALI
 COME RISOLVERE ESERCIZI SULLE LEGGI PONDERALI LA LEGGE DI LAVOISIER m m iniziale finale è proprio come fare una torta L uguaglianza vale anche nel caso la reazione non consumi tutti i reagenti: in tal
COME RISOLVERE ESERCIZI SULLE LEGGI PONDERALI LA LEGGE DI LAVOISIER m m iniziale finale è proprio come fare una torta L uguaglianza vale anche nel caso la reazione non consumi tutti i reagenti: in tal
1) È una sostanza che a temperatura ambiente (20 C) ed alla pressione atmosferica si trova allo stato gassoso (aeriforme) V
 1601 Il gas... 1) È una sostanza che a temperatura ambiente (20 C) ed alla pressione atmosferica si trova allo stato gassoso (aeriforme) V 2) È una sostanza che si trova allo stato aeriforme alla temperatura
1601 Il gas... 1) È una sostanza che a temperatura ambiente (20 C) ed alla pressione atmosferica si trova allo stato gassoso (aeriforme) V 2) È una sostanza che si trova allo stato aeriforme alla temperatura
Dinamica delle reazioni chimiche (attenzione: mancano i disegni)
 Dinamica delle reazioni chimiche (attenzione: mancano i disegni) Primo principio della termodinamica L energia non si può creare o distruggere, ma solo convertire da una forma all altra. Questo significa
Dinamica delle reazioni chimiche (attenzione: mancano i disegni) Primo principio della termodinamica L energia non si può creare o distruggere, ma solo convertire da una forma all altra. Questo significa
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD
![7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD](/thumbs/59/43238545.jpg) 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Corso di Termofluidodinamica
 Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
4) 8 g di idrogeno reagiscono esattamente con 64 g di ossigeno secondo la seguente reazione:
 Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Cartelli antincendio forma quadrata o rettangolare e pittogramma bianco su fondo rosso
 Cartelli antincendio I cartelli antincendio devono avere forma quadrata o rettangolare e pittogramma bianco su fondo rosso (il rosso deve coprire almeno il 50% della superficie del cartello). I cartelli
Cartelli antincendio I cartelli antincendio devono avere forma quadrata o rettangolare e pittogramma bianco su fondo rosso (il rosso deve coprire almeno il 50% della superficie del cartello). I cartelli
1. CALCOLO DELLA QUANTITÀ D'ARIA NECESSARIA ALLA COMBUSTIONE DI UN DATO COMBUSTIBILE
 1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido.
 UNITÀ 8 LA MECCANICA DEI FLUIDI 1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido. 3. La pressione atmosferica. 4. La legge di Stevino. 5. La legge di Pascal. 6. La forza di Archimede.
UNITÀ 8 LA MECCANICA DEI FLUIDI 1. I fluidi e le loro caratteristiche. 2. La pressione in un fluido. 3. La pressione atmosferica. 4. La legge di Stevino. 5. La legge di Pascal. 6. La forza di Archimede.
LE REAZIONI CHIMICHE
 LE REAZIONI CHIMICHE Una reazione chimica è una trasformazione che comporta una nuova distribuzione degli atomi in una o più determinate sostanze Una reazione chimica è un processo dinamico in cui alcune
LE REAZIONI CHIMICHE Una reazione chimica è una trasformazione che comporta una nuova distribuzione degli atomi in una o più determinate sostanze Una reazione chimica è un processo dinamico in cui alcune
La classificazione delle miscele ai sensi del Regolamento (UE) 1272/2008 (CLP) Pericoli Fisici. Ing. Antonio Natale.
 La classificazione delle miscele ai sensi del Regolamento (UE) 1272/2008 (CLP) Pericoli Fisici Ing. Antonio Natale 28 novembre 2017 Come si determina il Pericolo Fisico? Per determinare se una sostanza
La classificazione delle miscele ai sensi del Regolamento (UE) 1272/2008 (CLP) Pericoli Fisici Ing. Antonio Natale 28 novembre 2017 Come si determina il Pericolo Fisico? Per determinare se una sostanza
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO
 2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
VALORIZZAZIONE ENERGETICA DEI RIFIUTI: NUOVE SOLUZIONI
 VALORIZZAZIONE ENERGETICA DEI RIFIUTI: NUOVE SOLUZIONI GIANCARLO BALDI, MILENA BERNARDI Dip.. Scienza dei materiali e Ingegneria Chimica POLITECNICO di TORINO Incontro AEIT 22 maggio 2008 RIFIUTI Problema
VALORIZZAZIONE ENERGETICA DEI RIFIUTI: NUOVE SOLUZIONI GIANCARLO BALDI, MILENA BERNARDI Dip.. Scienza dei materiali e Ingegneria Chimica POLITECNICO di TORINO Incontro AEIT 22 maggio 2008 RIFIUTI Problema
ASPETTI AMBIENTALI DELLA COMBUSTIONE
 ASPETTI AMBIENTALI DELLA COMBUSTIONE INTRODUZIONE Sino ad oggi non è stato possibile realizzare un impianto di combustione che non produca composti inquinanti. La combustione di fuel ed aria ad alta temperatura
ASPETTI AMBIENTALI DELLA COMBUSTIONE INTRODUZIONE Sino ad oggi non è stato possibile realizzare un impianto di combustione che non produca composti inquinanti. La combustione di fuel ed aria ad alta temperatura
I M P I A N TO D I R E C U P E R O ACIDI SOLFORICI Reflui pericolosi e non pericolosi
 I M P I A N TO D I R E C U P E R O ACIDI SOLFORICI Reflui pericolosi e non pericolosi So.Ri.S. spa Serravalle Scrivia (AL) Relazione impianto 2006 1 I M P I A N TO D I R E C U P E R O ACIDI SOLFORICI Reflui
I M P I A N TO D I R E C U P E R O ACIDI SOLFORICI Reflui pericolosi e non pericolosi So.Ri.S. spa Serravalle Scrivia (AL) Relazione impianto 2006 1 I M P I A N TO D I R E C U P E R O ACIDI SOLFORICI Reflui
SCUOLA PRIMARIA DI MAGGIATE Classe terza
 SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
OSSIDATORE TERMICO RIGENERATIVO
 OSSIDATORE TERMICO RIGENERATIVO PREMESSA I composti organici volatili (COV) rappresentano, per la loro presenza diffusa nelle emissioni dell industria di processo e per la loro riconosciuta tossicità,
OSSIDATORE TERMICO RIGENERATIVO PREMESSA I composti organici volatili (COV) rappresentano, per la loro presenza diffusa nelle emissioni dell industria di processo e per la loro riconosciuta tossicità,
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
Una reazioni chimica esprime il numero e il tipo di specie che si combinano ed il risultato della combinazione. Esempio:
 Reazioni chimiche Una reazioni chimica esprime il numero e il tipo di specie che si combinano ed il risultato della combinazione. Esempio: CH 4 + 2O 2 CO 2 + 2H 2 O La reazione chimica è formata da reagenti
Reazioni chimiche Una reazioni chimica esprime il numero e il tipo di specie che si combinano ed il risultato della combinazione. Esempio: CH 4 + 2O 2 CO 2 + 2H 2 O La reazione chimica è formata da reagenti
CARATTERISTICHE DELL IDROGENO
 Introduzione Perché la tecnologia dell idrogeno e delle celle a combustibile? L attuale sistema energetico e dei trasporti è basato principalmente sui combustibili di origine fossile e dunque non è sostenibile:
Introduzione Perché la tecnologia dell idrogeno e delle celle a combustibile? L attuale sistema energetico e dei trasporti è basato principalmente sui combustibili di origine fossile e dunque non è sostenibile:
Capitolo 3. LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino
 Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
Reazioni ed Equazioni Chimiche. Coefficienti stechiometrici :
 Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
4. LE REAZIONI CHIMICHE
 Pagina 1 di 7 Appunti di Chimica Generale e Inorganica per Scienze Biologiche 4. LE REAZINI CHIMICHE La reazione chimica è un processo in cui dei composti (reagenti) si trasformano in altri composti (prodotti)
Pagina 1 di 7 Appunti di Chimica Generale e Inorganica per Scienze Biologiche 4. LE REAZINI CHIMICHE La reazione chimica è un processo in cui dei composti (reagenti) si trasformano in altri composti (prodotti)
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
