RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Un flaconcino contiene 40 mg di pantoprazolo (in forma di pantoprazolo sodico sesquidrato)
|
|
|
- Chiara Tommasa Genovese
- 7 anni fa
- Visualizzazioni
Transcript
1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz GmbH 40 mg polvere per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene 40 mg di pantoprazolo (in forma di pantoprazolo sodico sesquidrato) 3. FORMA FARMACEUTICA Polvere per soluzione iniettabile. Polvere di colore da bianco a giallognolo. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Esofagite da reflusso. Ulcera gastrica e duodenale. Sindrome di Zollinger-Ellison e altri disturbi ipersecretivi patologici. 4.2 Posologia e modo di somministrazione Questo medicinale deve essere somministrato da un operatore sanitario e sotto adeguata supervisione medica. La somministrazione endovenosa di Pantoprazolo Sandoz GmbH è raccomandata solo quando quella per via orale non è appropriata. Sono disponibili dati sull uso per via endovenosa fino a 7 giorni. Pertanto, non appena è possibile passare alla terapia orale, il trattamento con Pantoprazolo Sandoz GmbH per via endovenosa deve essere interrotto e deve essere invece somministrato pantoprazolo 40 mg per via orale. Dose raccomandata Ulcera gastrica e duodenale, esofagite da reflusso La dose raccomandata per via endovenosa è un flaconcino di Pantoprazolo Sandoz GmbH (40 mg di pantoprazolo) al giorno. Sindrome di Zollinger-Ellison e altri disturbi ipersecretivi patologici Per la gestione a lungo termine della sindrome di Zollinger-Ellison e di altri disturbi ipersecretivi patologici i pazienti devono iniziare il trattamento con una dose giornaliera di 80 mg di Pantoprazolo Sandoz GmbH. Successivamente la dose può essere titolata verso l alto o verso il basso, a seconda delle necessità, sulla base della misurazione delle secrezioni di acido gastrico. Per dosi superiori a 80 mg al giorno, la dose deve essere divisa e somministrata due volte al giorno. È possibile aumentare temporaneamente la dose sopra i 160 mg, ma non oltre il tempo necessario a risolvere l acidità in modo adeguato. Nel caso si renda necessario un rapido controllo dell acidità, nella maggior parte dei pazienti una dose iniziale pari a 2 x 80 mg di Pantoprazolo Sandoz GmbH è sufficiente a ottenere una diminuzione della produzione di acido entro il range di valori desiderabili (<10 meq/h) nell arco di un ora. Popolazioni speciali Pazienti pediatrici L esperienza nei bambini è limitata, pertanto l uso di Pantoprazolo Sandoz GmbH 40 mg polvere per soluzione iniettabile non è raccomandato nei pazienti sotto i 18 anni di età fino a quando non saranno disponibili ulteriori dati. Compromissione della funzionalità epatica Nei pazienti con grave compromissione della funzionalità epatica non deve essere superata la dose giornaliera di 20 mg di pantoprazolo (mezzo flaconcino da 40 mg di pantoprazolo - vedere il paragrafo 4.4). 1
2 Compromissione della funzionalità renale Nei pazienti con compromissione della funzionalità renale non è necessario alcun aggiustamento della dose. Anziani Nei pazienti anziani non è necessario alcun aggiustamento della dose. Modo di somministrazione La soluzione pronta per l uso viene preparata con 10 ml di una soluzione iniettabile di cloruro di sodio 9 mg/ml (0,9%). Per le istruzioni per la preparazione vedere il paragrafo 6.6. La soluzione preparata può essere somministrata direttamente oppure dopo ulteriore miscelazione con 100 ml di una soluzione iniettabile di cloruro di sodio 9 mg/ml (0,9%) o di glucosio monoidrato 55 mg/ml (5%). Dopo la preparazione la soluzione deve essere utilizzata entro 12 ore. Il prodotto medicinale deve essere somministrato per via endovenosa nell arco di 2-15 minuti. 4.3 Controindicazioni Ipersensibilità al principio attivo, ai sostituti benzimidazolici o a uno qualsiasi degli eccipienti elencati al paragrafo Avvertenze speciali e precauzioni di impiego In presenza di sintomi allarmanti In presenza di qualsiasi sintomo allarmante (per esempio significativa perdita di peso non intenzionale, vomito ricorrente, disfagia, ematemesi, anemia o melena) e quando è presente o si sospetta ulcera gastrica, deve essere esclusa la malignità, poiché il trattamento con pantoprazolo può alleviarne i sintomi e ritardarne la diagnosi. Se i sintomi persistono nonostante un trattamento adeguato, deve essere considerata l opportunità di effettuare ulteriori analisi. Compromissione della funzionalità epatica Nei pazienti con grave compromissione della funzionalità epatica gli enzimi epatici devono essere monitorati durante la terapia. Nel caso di un aumento degli enzimi epatici il trattamento deve essere sospeso (vedere il paragrafo 4.2). Co-somministrazione con atazanavir La co-somministrazione di atazanavir con inibitori della pompa protonica non è raccomandata (vedere il paragrafo 4.5). Se la combinazione di atazanavir con un inibitore della pompa protonica è ritenuta inevitabile, si consiglia un attento monitoraggio clinico (per esempio della carica virale), in combinazione con un aumento della dose di atazanavir a 400 mg con 100 mg di ritonavir. Non deve essere superata la dose giornaliera di 20 mg di pantoprazolo. Infezioni gastrointestinali causate da batteri Come per tutti gli inibitori della pompa protonica (PPI), è lecito prevedere che anche pantoprazolo possa aumentare la conta dei batteri normalmente presenti nel tratto gastrointestinale superiore. Il trattamento con Pantoprazolo Sandoz GmbH può provocare un lieve aumento del rischio di infezioni gastrointestinali causate da batteri come Salmonella, Campylobacter e Clostridium difficile. Ipomagnesiemia È stato osservato che gli inibitori di pompa protonica (PPI) come pantoprazolo, in pazienti trattati per almeno tre mesi e in molti casi per un anno, possono causare grave ipomagnesiemia. Gravi sintomi di ipomagnesiemia includono stanchezza, tetania, delirio, convulsioni, capogiri e aritmia ventricolare. Essi, inizialmente, si possono manifestare in modo insidioso ed essere trascurati. L ipomagnesiemia, nella maggior parte dei pazienti, migliora dopo l assunzione di magnesio e la sospensione dell inibitore di pompa protonica. Gli operatori sanitari devono considerare l eventuale misurazione dei livelli di magnesio prima di iniziare il trattamento con PPI e periodicamente durante il trattamento nei pazienti in terapia per un periodo prolungato o in terapia con digossina o medicinali che possono causare ipomagnesiemia (ad esempio diuretici). 2
3 Fratture ossee Gli inibitori di pompa protonica, specialmente se utilizzati a dosaggi elevati e per periodi prolungati (> 1 anno), potrebbero causare un lieve aumento di rischio di fratture dell anca, del polso e della colonna vertebrale, sopratutto in pazienti anziani o in presenza di altri fattori di rischio conosciuti. Studi osservazionali suggeriscono che gli inibitori di pompa protonica potrebbero aumentare il rischio complessivo di frattura dal 10% al 40%. Tale aumento potrebbe essere in parte dovuto ad altri fattori di rischio. I pazienti a rischio di osteoporosi devono ricevere le cure in base alle attuali linee guida di pratica clinica e devono assumere un adeguata quantità di vitamina D e calcio. 4.5 Interazioni con altri medicinali ed altre forme di interazione Effetto di pantoprazolo sull assorbimento di altri medicinali A causa dell inibizione intensa e di lunga durata della secrezione di acido gastrico, pantoprazolo può ridurre l assorbimento di farmaci con una biodisponibilità dipendente dal ph gastrico, per esempio alcuni antifungini azolici come ketoconazolo, itraconazolo, posaconazolo e altri medicinali come erlotinib. Medicinali per il trattamento dell HIV (atazanavir) La co-somministrazione di atazanavir e di altri medicinali per il trattamento dell HIV il cui assorbimento è phdipendente con inibitori della pompa protonica può provocare una riduzione significativa della biodisponibilità di questi medicinali e comprometterne l efficacia. Pertanto la co-somministrazione di inibitori della pompa protonica con atazanavir non è raccomandata (vedere il paragrafo 4.4). Anticoagulanti cumarinici (fenprocumone o warfarin) Sebbene negli studi di farmacocinetica non sia stata osservata alcuna interazione durante la somministrazione concomitante di fenprocumone o warfarin, durante il trattamento concomitante nel periodo post-marketing sono stati riportati alcuni casi isolati di alterazioni dell International Normalized Ratio (INR). Pertanto nei pazienti trattati con anticoagulanti cumarinici (per esempio fenprocumone o warfarin) si consiglia il monitoraggio del tempo di protrombina/inr dopo l inizio o la sospensione o durante l uso irregolare di pantoprazolo. Metotrexato In alcuni pazienti è stato riportato un aumento dei livelli di metotrexato in seguito all utilizzo concomitante di metotrexato ad elevati dosaggi (per es. 300 mg) e inibitori di pompa protonica. Pertanto nelle situazioni in cui il metotrexato è utilizzato ad elevati dosaggi, come per es. cancro e psoriasi, è necessario considerare una sospensione temporanea del trattamento con pantoprazolo. Altri studi di interazione Pantoprazolo viene ampiamente metabolizzato nel fegato attraverso il sistema enzimatico del citocromo P450. La principale via metabolica è la demetilazione da parte del CYP2C19 e altre vie metaboliche comprendono l ossidazione da parte del CYP3A4. Studi di interazione con i farmaci egualmente metabolizzati tramite queste vie, come carbamazepina, diazepam, glibenclamide, nifedipina e un contraccettivo orale contenente levonorgestrel ed etinilestradiolo, non hanno evidenziato interazioni clinicamente significative. I risultati di una serie di studi di interazione dimostrano che pantoprazolo non influenza il metabolismo dei principi attivi metabolizzati dal CYP1A2 (come caffeina, teofillina), dal CYP2C9 (come piroxicam, diclofenac, naprossene), dal CYP2D6 (come metoprololo), dal CYP2E1 (come etanolo) né interferisce con l assorbimento di digossina correlato alla p-glicoproteina. Non si sono verificate interazioni con antiacidi somministrati in concomitanza. Sono stati effettuati studi di interazione anche somministrando pantoprazolo in concomitanza con i relativi antibiotici (claritromicina, metronidazolo, amoxicillina). Non è stata identificata alcuna interazione clinicamente rilevante. 4.6 Fertilità, gravidanza e allattamento Gravidanza Non sono disponibili dati adeguati sull uso di pantoprazolo nelle donne in gravidanza. Gli studi sugli animali hanno mostrato tossicità riproduttiva (vedere il paragrafo 5.3). Il rischio potenziale per l uomo non è noto. Pantoprazolo Sandoz GmbH non deve essere usato durante la gravidanza, a meno che non sia evidentemente necessario. 3
4 Allattamento Gli studi sugli animali hanno dimostrato secrezione di pantoprazolo nel latte materno. È stata riportata anche secrezione nel latte umano, pertanto la decisione se continuare o sospendere l allattamento al seno o continuare o sospendere la terapia con Pantoprazolo Sandoz GmbH deve essere presa dopo aver considerato i benefici dell allattamento per il bambino rispetto a quelli della terapia con Pantoprazolo Sandoz GmbH per la madre. 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Possono verificarsi reazioni avverse da farmaco, come capogiri e disturbi della vista (vedere il paragrafo 4.8). In questo caso i pazienti non devono guidare né usare macchinari. 4.8 Effetti indesiderati Si può prevedere che il 5% circa dei pazienti manifesti reazioni avverse da farmaco (ADR). Le reazioni avverse più comunemente riportate sono diarrea e cefalea, entrambe verificatesi nell 1% circa dei pazienti. La tabella seguente elenca le reazioni avverse riportate con pantoprazolo, suddivise in base alla seguente classificazione della frequenza: Molto comune ( 1/10); comune (da 1/100 a <1/10); non comune (da 1/1000 a <1/100), raro (da 1/ a <1/1000); molto raro (<1/10.000); non nota (non può essere definita sulla base dei dati disponibili). Per tutte le reazioni avverse segnalate dall esperienza post-marketing non è possibile stimare la frequenza, motivo per cui sono elencate con frequenza non nota. Nell ambito di ciascuna classe di frequenza gli effetti indesiderati sono riportati in ordine decrescente di gravità. Tabella 1. Reazioni avverse con pantoprazolo negli studi clinici e nell esperienza post-marketing Frequenza Comune Non comune Raro Molto raro Non nota Classificazione sistemica degli organi del sistema emolinfopoietico Disturbi del sistema immunitario Disturbi del metabolismo e della nutrizione Agranulocitosi Ipersensibilità (compresi reazioni anafilattiche e shock anafilattico) Iperlipidemia e aumenti dei lipidi (trigliceridi, colesterolo); alterazioni del peso Trombocitopeni a; leucopenia, pancitopenia Iponatremia, ipomagnesiemi a (vedere paragrafo 4.4) Ipocalcemia in associazione con ipomagnesemi a; Ipopotassiemia Disturbi psichiatrici Disturbi del sonno Depressione (e tutte le relative aggravanti) Disorientament o (e tutte le relative aggravanti) Allucinazioni; confusione (specialmente nei pazienti 4
5 Frequenza Comune Non comune Raro Molto raro Non nota Classificazione sistemica degli organi del sistema nervoso dell occhio gastrointestinali epatobiliari della cute e del tessuto sottocutaneo del sistema muscoloscheletri co e del tessuto connettivo renali e urinarie dell apparato riproduttivo e della mammella sistemiche e condizioni Tromboflebit e nel sito di iniezione Cefalea; capogiri Diarrea; nausea/vomito ; distensione e gonfiore addominale; costipazione; secchezza delle fauci; dolore e fastidio addominale Aumento degli enzimi epatici (transaminasi, γ-gt) Rash/esantem a/ eruzione; prurito Fratture dell anca, del polso e della colonna vertebrale (vedere paragrafo 4.4) Astenia, affaticamento e malessere Disturbi nel gusto Disturbi della vista/offuscamen to della vista Aumento della bilirubina Orticaria; angioedema Artralgia; mialgia Ginecomastia Aumento della temperatura corporea; predisposti, oltre a peggioramento di questi sintomi nel caso di preesistenza) Parestesia Danno epatocellulare; ittero; insufficienza epatocellulare Sindrome di Stevens- Johnson; sindrome di Lyell; eritema multiforme; fotosensibilità Spasmo muscolare come conseguenza di disturbi elettrolitici Nefrite interstiziale (con possibile progressione a insufficienza renale) 5
6 Frequenza Comune Non comune Raro Molto raro Non nota Classificazione sistemica degli organi relative alla sede di somministrazione edema periferico Segnalazione delle reazioni avverse sospette La segnalazione delle reazioni avverse sospette che si verificano dopo l autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all indirizzo Sovradosaggio Nell uomo non sono noti sintomi di sovradosaggio. Esposizioni sistemiche con dosi fino a 240 mg somministrate per via endovenosa nell arco di 2 minuti sono state ben tollerate. Poiché pantoprazolo si lega in modo esteso alle proteine, non è prontamente dializzabile. In caso di sovradosaggio con segni clinici di intossicazione, a parte il trattamento sintomatico e di supporto non è possibile formulare alcuna specifica raccomandazione terapeutica. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: inibitori della pompa protonica Codice ATC: A02BC02 Meccanismo d azione Pantoprazolo è un sostituto benzimidazolico che inibisce la secrezione di acido cloridrico nello stomaco mediante un azione specifica di blocco delle pompe protoniche delle cellule parietali. Pantoprazolo viene convertito nella sua forma attiva nell ambiente acido delle cellule parietali, dove inibisce l enzima H +, K + ATPasi, cioè lo stadio finale della produzione di acido cloridrico nello stomaco. Tale inibizione è dose-dipendente e interessa sia la secrezione acida sia quella basale stimolata. Nella maggior parte dei pazienti la remissione dei sintomi avviene entro 2 settimane. Come per altri inibitori della pompa protonica e inibitori del recettore H 2, il trattamento con pantoprazolo determina una riduzione dell acidità a livello gastrico e di conseguenza un aumento di gastrina proporzionale alla riduzione dell acidità. L incremento di gastrina è reversibile. Poiché si lega all enzima in posizione distale rispetto al recettore cellulare, pantoprazolo può influenzare la secrezione di acido cloridrico indipendentemente dalla stimolazione da parte di altre sostanze (acetilcolina, istamina, gastrina). Che la somministrazione del prodotto avvenga per via orale o per via endovenosa, l effetto è il medesimo. I valori di gastrina a digiuno aumentano durante il trattamento con pantoprazolo. Nell uso a breve termine, nella maggior parte dei casi non superano il limite superiore della norma. Durante il trattamento a lungo termine nella maggior parte dei casi i livelli di gastrina raddoppiano. Un aumento eccessivo si verifica tuttavia solo in casi isolati. Di conseguenza in una minoranza di casi durante il trattamento a lungo termine si osserva un aumento da lieve a moderato del numero di cellule endocrine specifiche (ECL) nello stomaco (iperplasia da semplice ad adenomatoide). Tuttavia, secondo gli studi condotti finora, la formazione di precursori carcinoidi (iperplasia atipica) o di carcinoidi gastrici come quelli identificati durante gli studi sugli animali (vedere il paragrafo 5.3) non è stata osservata negli esseri umani. Sulla base dei risultati degli studi condotti sugli animali, non può essere completamente escluso un effetto sui parametri endocrini della tiroide di un trattamento a lungo termine, superiore a un anno, con pantoprazolo. 5.2 Proprietà farmacocinetiche Farmacocinetica generale 6
7 Le caratteristiche farmacocinetiche non variano dopo una somministrazione singola o ripetuta. Con dosi comprese tra 10 e 80 mg le cinetiche plasmatiche di pantoprazolo sono lineari in seguito a somministrazione sia orale sia per via endovenosa. Distribuzione Il legame di pantoprazolo alle proteine seriche è di circa il 98%. Il volume di distribuzione è di circa 0,15 l/kg. Eliminazione La sostanza viene metabolizzata quasi esclusivamente a livello epatico. La principale via metabolica è la demetilazione da parte del CYP2C19 con conseguente coniugazione con solfato; l altra via metabolica comprende l ossidazione da parte del CYP3A4. L emivita terminale è di circa un ora e la clearance è intorno a 0,1 l/h/kg. Sono stati osservati alcuni casi di rallentata eliminazione del farmaco. A causa dello specifico legame di pantoprazolo alle pompe protoniche delle cellule parietali, l emivita di eliminazione non corrisponde alla durata dell azione (inibizione della secrezione acida), che è molto più lunga. L eliminazione renale rappresenta la principale via di escrezione (80% circa) dei metaboliti di pantoprazolo, il rimanente viene escreto con le feci. Il principale metabolita, sia nel siero sia nelle urine, è il demetilpantoprazolo, sotto forma di sulfoconiugato. L emivita del metabolita principale (circa 1,5 ore) non è molto più lunga di quella di pantoprazolo. Caratteristiche in pazienti/gruppi speciali Circa il 3% della popolazione europea manca di un enzima CYP2C19 funzionale e i soggetti vengono chiamati metabolizzatori scarsi. In questi individui il metabolismo di pantoprazolo è probabilmente catalizzata in prevalenza dal CYP3A4. Dopo la somministrazione di una singola dose di 40 mg di pantoprazolo, l AUC media è stata circa 6 volte superiore negli scarsi metabolizzatori rispetto ai soggetti che hanno un enzima CYP2C19 funzionale (metabolizzatori estesi). Le concentrazioni plasmatiche di picco sono state aumentate di circa il 60%. Queste osservazioni non hanno alcuna implicazione per quanto riguarda la posologia di pantoprazolo. Nessuna riduzione della dose è raccomandata quando pantoprazolo viene somministrato a pazienti con funzionalità renale compromessa (compresi i pazienti in dialisi). Come è stato osservato nei soggetti sani, l emivita di pantoprazolo è breve. Sebbene il principale metabolita abbia una emivita più lunga (2-3 h), l escrezione è tuttavia rapida e pertanto non si verifica accumulo. Sebbene nei pazienti con cirrosi epatica (classe A e B secondo Child-Pugh) i valori dell emivita siano aumentati tra 7 e 9 h e i valori di AUC siano aumentati di un fattore pari a 5-7, la C max è aumentata solo leggermente di un fattore pari a 1,5 rispetto ai soggetti sani. Inoltre, un leggero aumento dell AUC e della C max nei volontari anziani rispetto ai più giovani non è clinicamente rilevante. Bambini Dopo la somministrazione di singole dosi per via endovenosa di pantoprazolo 0,8 o 1,6 mg/kg a bambini dai 2 ai 16 anni non si è manifestata alcuna associazione significativa fra la clearance di pantoprazolo e l età o peso. L AUC e il volume di distribuzione sono stati coerenti con i dati osservati negli adulti. 5.3 Dati preclinici di sicurezza I dati preclinici non rivelano rischi particolari per l uomo sulla base di studi convenzionali di sicurezza farmacologica, tossicità a dosi ripetute e genotossicità. Negli studi di carcinogenesi a 2 anni nei ratti sono state rinvenute neoplasie neuroendocrine. Inoltre, in uno studio sono stati identificati papillomi a cellule squamose nella parte anteriore dello stomaco dei ratti. Il meccanismo che porta alla formazione di carcinoidi gastrici a opera dei sostituti benzimidazoli è stato accuratamente studiato e ha permesso di concludere che si tratta di una reazione secondaria al massiccio aumento dei livelli sierici di gastrina che si verifica nel ratto durante il trattamento cronico ad alto dosaggio. Negli studi a 2 anni nei roditori è stato osservato un aumento del numero di tumori epatici nei ratti e nei topi femmina, che è stato interpretato come dovuto all elevato tasso di metabolizzazione di pantoprazolo nel fegato. Nel gruppo di ratti trattati con la dose più alta (200 mg/kg) è stato osservato un leggero aumento di alterazioni neoplastiche della tiroide. L insorgenza di tali neoplasie è associata alle alterazioni indotte da pantoprazolo nella scomposizione di tiroxina nel fegato del ratto. Poiché la dose terapeutica per l uomo è bassa, non sono da prevedersi effetti indesiderati a carico delle ghiandole tiroidee. 7
8 Negli studi sugli animali sono stati osservati segni di leggera fetotossicità a dosi superiori a 5 mg/kg. Le indagini non hanno dimostrato alcuna compromissione della fertilità né effetti teratogeni. La penetrazione della placenta è stata studiata nel ratto e si è scoperta aumentare con il progredire della gestazione. Pertanto la concentrazione di pantoprazolo nel feto poco prima della nascita è risultata aumentata. 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Non pertinente 6.2 Incompatibilità Questo medicinale non deve essere preparato o miscelato con solventi diversi da quelli specificati ai paragrafi 4.2 e Periodo di validità Flaconcino non aperto: 18 mesi. Dopo la ricostituzione (o ricostituzione e diluizione) la stabilità chimica e fisica in uso è stata dimostrata per 12 ore a 25 C. Da un punto di vista microbiologico il medicinale deve essere usato immediatamente. In caso contrario i tempi e le modalità di conservazione in uso sono responsabilità dell utilizzatore. 6.4 Precauzioni particolari per la conservazione Non conservare a temperatura superiore a 25 C. Conservare il contenitore nella confezione esterna, per proteggere il medicinale dalla luce. Per le condizioni di conservazione dopo ricostituzione e diluizione del medicinale, vedere il paragrafo Natura e contenuto del contenitore Flaconcino di vetro trasparente di tipo I, chiusa con un tappo in gomma di colore rosso e sigillata con calotta in alluminio. Confezioni da 1, 5, 10 e 20 flaconcini. È possibile che non tutte le confezioni siano commercializzate. 6.6 Precauzioni particolari per lo smaltimento e la manipolazione Una soluzione pronta all uso si prepara iniettando 10 ml di soluzione fisiologica di cloruro di sodio 9 mg/ml (0,9%) in un flaconcino contenente la polvere. La soluzione ricostituita deve essere da incolore a un colore giallo chiaro. Questa soluzione può essere somministrata direttamente oppure dopo essere stata miscelata con 100 ml di soluzione fisiologica di cloruro di sodio 9 mg/ml (0,9%) o di glucosio monoidrato 55 mg/ml (5%). Per la diluizione devono essere utilizzati contenitori di vetro o di plastica. Dopo la ricostituzione (o ricostituzione e diluizione) la stabilità chimica e fisica in uso è stata dimostrata per 12 ore a 25 C. Da un punto di vista microbiologico il medicinale deve essere usato immediatamente. In caso contrario i tempi di conservazione in uso e le condizioni prima dell uso sono responsabilità dell utilizzatore e di norma non superano le 12 ore a una temperatura non superiore ai 25 C. Pantoprazolo polvere per soluzione iniettabile non deve essere preparato o miscelato con solventi diversi da quelli specificati. Il medicinale deve essere somministrato per via endovenosa nell arco di 2-15 minuti. 8
9 Il contenuto del flaconcino si intende per uso singolo. Ogni eventuale residuo di soluzione rimasto nel contenitore o il cui aspetto sia visivamente cambiato (per esempio se si osserva torbidità o precipitazione) deve essere eliminato nel rispetto delle normative locali. 7. TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO Sandoz GmbH Biochemiestrasse, Kundl (Austria) Rappresentante per l Italia: Sandoz Spa Largo U. Boccioni, Origgio (VA) 8. NUMERO(I) DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO 40 mg polvere per soluzione iniettabile 1 flaconcino in vetro AIC n mg polvere per soluzione iniettabile 5 flaconcini in vetro AIC n mg polvere per soluzione iniettabile 10 flaconcini in vetro AIC n mg polvere per soluzione iniettabile 20 flaconcini in vetro AIC n DATA DELLA PRIMA AUTORIZZAZIONE/ RINNOVO DELL AUTORIZZAZIONE 14 Luglio DATA DI REVISIONE DEL TESTO 9
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come pantoprazolo sodico sesquidrato).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVE E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVE E QUANTITATIVA Ogni compressa gastroresistente
20 mg. Riassunto delle caratteristiche del prodotto. 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti.
 20 mg Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio
20 mg Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio sesquidrato).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ZOLONIB 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ZOLONIB 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente contiene
Eccipienti con effetto noto: 38,425 mg maltitolo e lecitina di soia (vedere paragrafo 4.4).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Zentiva Italia 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Zentiva Italia 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC 20 mg compresse gastroresistenti RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC 20 mg compresse gastroresistenti RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia
 Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO
 ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO Nota: Questo RCP, etichettatura e foglio illustrativo è la versione valida al momento della Decisione della
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO Nota: Questo RCP, etichettatura e foglio illustrativo è la versione valida al momento della Decisione della
Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come pantoprazolo sodico sesquidrato 22,58 mg).
 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo GERMED 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come pantoprazolo
1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo GERMED 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come pantoprazolo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Germed 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Germed 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
Trattamento farmacologico dell ulcera gastro-duodenale L. 29
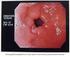 Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
Terapia del dolore in oncologia
 Terapia del dolore in oncologia Classi farmacologiche e interazioni con farmaci di uso comune Dr. Gianluigi Lunardi UC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar Interazioni tra farmaci
Terapia del dolore in oncologia Classi farmacologiche e interazioni con farmaci di uso comune Dr. Gianluigi Lunardi UC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar Interazioni tra farmaci
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo ratiopharm 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo ratiopharm 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
Acido ascorbico Medicinale equivalente
 Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX REFLUSSO 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX REFLUSSO 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Eugastrol reflusso 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Eugastrol reflusso 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO GENERALE DELLA VALUTAZIONE SCIENTIFICA DI PROTIUM E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
Foglio illustrativo: informazioni per l utilizzatore. Pantoprazolo
 Foglio illustrativo: informazioni per l utilizzatore Pantorc 40 mg polvere per soluzione iniettabile Pantoprazolo Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore Pantorc 40 mg polvere per soluzione iniettabile Pantoprazolo Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale Estratto glucosidico di rabarbaro e Acido salicilico Legga attentamente questo foglio prima di usare
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale Estratto glucosidico di rabarbaro e Acido salicilico Legga attentamente questo foglio prima di usare
1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA
 CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA Documento approvato nella seduta della Commissione PTR del 18.04.07 assorbimento L assorbimento di alcuni farmaci può La ridotta acidità intragastrica Alterazioni
CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA Documento approvato nella seduta della Commissione PTR del 18.04.07 assorbimento L assorbimento di alcuni farmaci può La ridotta acidità intragastrica Alterazioni
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini. Ketoprofene
 VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
4.3 Controindicazioni Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1.
 1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
FOGLIETTO ILLUSTRATIVO. Baytril flavour 25 mg/ml sospensione orale per gatti
 FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Foglio illustrativo: Informazioni per l utilizzatore. NOLPAZA 40 mg compresse gastroresistenti. Pantoprazolo Medicinale equivalente
 Foglio illustrativo: Informazioni per l utilizzatore NOLPAZA 40 mg compresse gastroresistenti Pantoprazolo Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: Informazioni per l utilizzatore NOLPAZA 40 mg compresse gastroresistenti Pantoprazolo Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE CONTROLOC Control 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE CONTROLOC Control 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
Ogni capsula rigida da 30 mg contiene 59,8 mg di saccarosio
 1. DENOMINAZIONE DEL MEDICINALE Lansox 15 mg capsule rigide Lansox 30 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 15 mg di lansoprazolo Ogni capsula rigida
1. DENOMINAZIONE DEL MEDICINALE Lansox 15 mg capsule rigide Lansox 30 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 15 mg di lansoprazolo Ogni capsula rigida
Compressa. La compressa è di forma rotonda, di colore giallo chiaro.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
Foglio illustrativo: informazioni per l utilizzatore. Connettivina Plus 2 mg/g + 10 mg/g crema Acido ialuronico sale sodico + sulfadiazina argentica
 Foglio illustrativo: informazioni per l utilizzatore Connettivina Plus 2 mg/g + 10 mg/g crema Acido ialuronico sale sodico + sulfadiazina argentica Legga attentamente questo foglio prima di usare questo
Foglio illustrativo: informazioni per l utilizzatore Connettivina Plus 2 mg/g + 10 mg/g crema Acido ialuronico sale sodico + sulfadiazina argentica Legga attentamente questo foglio prima di usare questo
Soluzione per infusione. La soluzione è limpida, leggermente giallognola e priva di particelle. ph 5,5. Volume per somministrazion e
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE Paracetamolo Actavis Italy 10 mg/ml soluzione per infusione 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE Paracetamolo Actavis Italy 10 mg/ml soluzione per infusione 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene
Foglio illustrativo: informazioni per il paziente. MAALOX 400 mg + 400 mg compresse masticabili. Magnesio idrossido + Alluminio ossido, idrato
 Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE CETIRIZINA ABC 10 mg compresse CETIRIZINA ABC 10 mg/ml gocce orali, soluzione 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA CETIRIZINA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE CETIRIZINA ABC 10 mg compresse CETIRIZINA ABC 10 mg/ml gocce orali, soluzione 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA CETIRIZINA
01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Influvac S sospensione iniettabile (vaccino influenzale inattivato preparato con l antigene di superficie). 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Influvac S sospensione iniettabile (vaccino influenzale inattivato preparato con l antigene di superficie). 2. COMPOSIZIONE
PER INFUSIONE CON SODIO CLORURO CARNITENE
 CARNITENE 1 g/10 ml SOLUZIONE ORALE CARNITENE 2 g/10 ml SOLUZIONE ORALE CARNITENE 1,5 g/5 ml SOLUZIONE ORALE CARNITENE 1 g COMPRESSE MASTICABILI CARNITENE 1 g/5 ml SOLUZIONE INIETTABILE PER USO ENDOVENOSO
CARNITENE 1 g/10 ml SOLUZIONE ORALE CARNITENE 2 g/10 ml SOLUZIONE ORALE CARNITENE 1,5 g/5 ml SOLUZIONE ORALE CARNITENE 1 g COMPRESSE MASTICABILI CARNITENE 1 g/5 ml SOLUZIONE INIETTABILE PER USO ENDOVENOSO
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film
 1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film 1. DENOMINAZIONE DEL MEDICINALE RANITIDINA ABC 150 mg
1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film 1. DENOMINAZIONE DEL MEDICINALE RANITIDINA ABC 150 mg
Foglio illustrativo: informazioni per l utilizzatore. NEOMERCUROCROMO soluzione cutanea. Eosina/ Cloroxilenolo/ Propilenglicole
 Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DESLORATADINA DOC 5 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa rivestita con
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DESLORATADINA DOC 5 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa rivestita con
INTERAZIONI FARMACOLOGICHE
 INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
Sollievo dai sintomi quali nausea, vomito, senso di ripienezza epigastrica, fastidio al tratto addominale superiore, rigurgito del contenuto gastrico.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DOMPERIDONE ABC 10 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene Principio attivo: domperidone
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DOMPERIDONE ABC 10 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene Principio attivo: domperidone
AIFA - Agenzia Italiana del Farmaco
 Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Foglio illustrativo. LOPERAMIDE ANGENERICO 2mg capsule rigide. Loperamide. Medicinale Equivalente
 Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
Foglio illustrativo: informazioni per l utilizzatore. Paracetamolo Sandoz 500 mg compresse. Medicinale equivalente
 Foglio illustrativo: informazioni per l utilizzatore Paracetamolo Sandoz 500 mg compresse Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore Paracetamolo Sandoz 500 mg compresse Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per il paziente. Lyseen 4 mg compresse Lyseen 2 mg/ml soluzione iniettabile pridinolo mesilato
 Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
Patologie del sistema emolinfopoietico Molto rari: Linfoadenopatia 1 Disturbi del metabolismo e della nutrizione Comuni: perdita di appetito 2 Disturb
 di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
FOGLIO ILLUSTRATIVO. KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10)
 1 FOGLIO ILLUSTRATIVO KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10) CATEGORIA FARMACOTERAPEUTICA Preparati per la tosse e le malattie
1 FOGLIO ILLUSTRATIVO KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10) CATEGORIA FARMACOTERAPEUTICA Preparati per la tosse e le malattie
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
Presentazione dei dati
 Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
batrevac sospensione iniettabile vaccino influenzale
 batrevac sospensione iniettabile vaccino influenzale RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Batrevac sospensione iniettabile (vaccino influenzale inattivato preparato
batrevac sospensione iniettabile vaccino influenzale RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Batrevac sospensione iniettabile (vaccino influenzale inattivato preparato
2. P RIMA DI U TILIZZARE ASQUAM
 Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. PARIET 20 mg compresse gastroresistenti 20 mg di rabeprazolo sodico, pari a 18,85 mg di rabeprazolo
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PARIET 10 mg compresse gastroresistenti PARIET 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PARIET
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PARIET 10 mg compresse gastroresistenti PARIET 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PARIET
INDICAZIONI TERAPEUTICHE
 FOGLIO ILLUSTRATIVO Potassio cloruro S.A.L.F. 2 meq/ml concentrato per soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Soluzioni elettrolitiche. INDICAZIONI TERAPEUTICHE Trattamento di deficienze
FOGLIO ILLUSTRATIVO Potassio cloruro S.A.L.F. 2 meq/ml concentrato per soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Soluzioni elettrolitiche. INDICAZIONI TERAPEUTICHE Trattamento di deficienze
FOGLIO ILLUSTRATIVO confezione 50 compresse. Sodio bicarbonato Sella 500 mg compresse. CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato
 FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
CEFODIE Cefonicid. Categoria farmacoterapeutica Antibiotico iniettabile.
 Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico
 1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
Foglio illustrativo: informazioni per il paziente. Calcium Sandoz 1000 mg granulato effervescente Calcio lattato gluconato e calcio carbonato
 Foglio illustrativo: informazioni per il paziente Calcium Sandoz 1000 mg granulato effervescente Calcio lattato gluconato e calcio carbonato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente Calcium Sandoz 1000 mg granulato effervescente Calcio lattato gluconato e calcio carbonato Legga attentamente questo foglio prima di prendere questo medicinale
SINTESI GENERALE DELLA VALUTAZIONE SCIENTIFICA DI LOSEC E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
Foglio illustrativo: informazioni per l utilizzatore. PANTOPAN 40 mg compresse gastroresistenti Pantoprazolo
 Foglio illustrativo: informazioni per l utilizzatore PANTOPAN 40 mg compresse gastroresistenti Pantoprazolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore PANTOPAN 40 mg compresse gastroresistenti Pantoprazolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore
 FOGLIO ILLUSTRATIVO 1 1 Foglio illustrativo: informazioni per l utilizzatore Neo Borocillina Antisettico Orofaringeo 6,4 mg + 52 mg compresse orosolubili alcool benzilico, sodio benzoato Legga attentamente
FOGLIO ILLUSTRATIVO 1 1 Foglio illustrativo: informazioni per l utilizzatore Neo Borocillina Antisettico Orofaringeo 6,4 mg + 52 mg compresse orosolubili alcool benzilico, sodio benzoato Legga attentamente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
NERIXIA RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NERIXIA 1. DENOMINAZIONE DEL MEDICINALE NERIXIA 25 mg soluzione iniettabile NERIXIA 100 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NERIXIA 1. DENOMINAZIONE DEL MEDICINALE NERIXIA 25 mg soluzione iniettabile NERIXIA 100 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA
Foglio illustrativo: informazioni per l utilizzatore. ACIDO CLODRONICO EG 100 mg/3,3 ml soluzione iniettabile. Medicinale equivalente
 Foglio illustrativo: informazioni per l utilizzatore ACIDO CLODRONICO EG 100 mg/3,3 ml soluzione iniettabile Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché
Foglio illustrativo: informazioni per l utilizzatore ACIDO CLODRONICO EG 100 mg/3,3 ml soluzione iniettabile Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Losipaco 2 mg/125 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide cloridrato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Losipaco 2 mg/125 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide cloridrato
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose
 GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente GOLAFAIR 1,5 mg pastiglie gusto Arancia - Limone GOLAFAIR 1,5 mg pastiglie gusto Menta GOLAFAIR 1,5 mg pastiglie gusto Miele Limone GOLAFAIR 1,5 mg pastiglie
Foglio illustrativo: informazioni per il paziente GOLAFAIR 1,5 mg pastiglie gusto Arancia - Limone GOLAFAIR 1,5 mg pastiglie gusto Menta GOLAFAIR 1,5 mg pastiglie gusto Miele Limone GOLAFAIR 1,5 mg pastiglie
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. HBVAXPRO 40 microgrammi/ml
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO HBVAXPRO 40 microgrammi/ml 1. DENOMINAZIONE DEL MEDICINALE HBVAXPRO 40 microgrammi/ml Sospensione iniettabile Vaccino dell epatite B (DNA ricombinante) 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO HBVAXPRO 40 microgrammi/ml 1. DENOMINAZIONE DEL MEDICINALE HBVAXPRO 40 microgrammi/ml Sospensione iniettabile Vaccino dell epatite B (DNA ricombinante) 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
gélules gastro-resistantes Lansoprazole BEXAL 30 mg gélules gastro-resistantes Lansoprazol HEXAL 15 mg Hartkapseln Lansoprazol HEXAL 30 mg Hartkapseln
 ALLEGATO I ELENCO DEI NOMI DEI MEDICINALI, DELLA FORMA FARMACEUTICA, DEI DOSAGGI, DELLA VIA DI SOMMINISTRAZIONE, DEL RICHIEDENTE, DEI TITOLARI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO NEGLI STATI
ALLEGATO I ELENCO DEI NOMI DEI MEDICINALI, DELLA FORMA FARMACEUTICA, DEI DOSAGGI, DELLA VIA DI SOMMINISTRAZIONE, DEL RICHIEDENTE, DEI TITOLARI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO NEGLI STATI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Una compressa di Torasemide GERMED 10 mg contiene 10 mg di torasemide.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Torasemide GERMED 10 mg Compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa di Torasemide GERMED 10 mg contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Torasemide GERMED 10 mg Compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa di Torasemide GERMED 10 mg contiene
Foglio illustrativo: informazioni per il paziente. CALCIO CARBONATO VITAMINA D3 EG 1000 mg U.I. Granulato effervescente. Medicinale equivalente
 Foglio illustrativo: informazioni per il paziente CALCIO CARBONATO VITAMINA D3 EG 1000 mg + 880 U.I. Granulato effervescente Medicinale equivalente Legga attentamente questo foglio prima di prendere questo
Foglio illustrativo: informazioni per il paziente CALCIO CARBONATO VITAMINA D3 EG 1000 mg + 880 U.I. Granulato effervescente Medicinale equivalente Legga attentamente questo foglio prima di prendere questo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Virus dell influenza* (inattivato con β-propiolattone, split) dei seguenti ceppi:
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE AFLURIA Sospensione iniettabile, in siringa preriempita. Vaccino influenzale (virus split (frammentato), inattivato) 2 COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE AFLURIA Sospensione iniettabile, in siringa preriempita. Vaccino influenzale (virus split (frammentato), inattivato) 2 COMPOSIZIONE
Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara
 Dipartimento Farmaceutico Interaziendale Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara Missere M.L.,
Dipartimento Farmaceutico Interaziendale Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara Missere M.L.,
Ogni capsula contiene 20 mg di esomeprazolo (come magnesio diidrato)
 1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Zentiva 20 mg capsule rigide gastroresistenti Esomeprazolo Zentiva 40 mg capsule rigide gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula
1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Zentiva 20 mg capsule rigide gastroresistenti Esomeprazolo Zentiva 40 mg capsule rigide gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula
