ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
|
|
|
- Raffaele Pala
- 6 anni fa
- Visualizzazioni
Transcript
1 ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NB: Questo SPC e` quello precedentemente annesso alla Decisione della Commissione riguardo questo 'Community Referral' (Articolo 31) per prodotti medicinali contenenti nimesulide. Il testo era quello valido all'epoca. Una volta ottenuta la Decisione della Commissione, le autorita` competenti degli Stati Membri aggiorneranno l'informazione rlativa al prodotto come stabilito. Questo SPC potrebbe percio` non rappresentare il testo attuale. CPMP/3086/03-REV.1 1 EMEA 2004
2 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NIMESULIDE COMPRESSE, COMPRESSE SOLUBILI, COMPRESSE EFFERVESCENTI, COMPRESSE RIVESTITE, CAPSULE, CAPSULE RIGIDE 100 MG NIMESULIDE GRANULATO O POLVERE 50/100 MG PER SOSPENSIONE ORALE NIMESULIDE 1%, 2% O 5% SOSPENSIONE ORALE CPMP/3086/03-REV.1 2 EMEA 2004
3 1. DENOMINAZIONE DEL MEDICINALE < DENOMINAZIONE COMMERCIALE DEL PRODOTTO > 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa, compressa solubile, compressa effervescente, compressa rivestita, capsula, capsula rigida contiene 100 mg di nimesulide. Ogni bustina contiene 50 o 100 mg di nimesulide. Sospensione orale contenente 10mg, 20mg o 50 mg per ml. Per gli eccipienti vedere paragrafo FORMA FARMACEUTICA Compresse, compresse solubili, compresse effervescenti, compresse rivestite: < Specifica per azienda>. Granulato o polvere per sospensione orale: < Specifica per azienda>. Capsule, capsule rigide: < Specifica per azienda>. Sospensione orale: < Specifica per azienda>. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Trattamento del dolore acuto. Trattamento sintomatico dell osteoartrite dolorosa. Dismenorrea primaria. 4.2 Posologia e modo di somministrazione <Specialità a base di nimesulide> deve essere usato per il minor tempo possibile in base alle esigenze cliniche. Adulti: Compresse, compresse solubili, compresse effervescenti, compresse rivestite, capsule, capsule rigide di nimesulide da 100 mg, granulato o polvere da 50 mg e 100 mg, 1%, 2% o 5% sospensione orale: 100 mg b.i.d. dopo i pasti. Anziani: nei pazienti anziani non occorre ridurre la dose giornaliera (vedere paragrafo 5.2). Bambini (<12 anni): <Specialità a base di nimesulide> è controindicato in questi pazienti (vedere anche paragrafo 4.3). Adolescenti (da 12 a 18 anni): sulla base del profilo cinetico negli adulti e delle caratteristiche farmacodinamiche di nimesulide, non è necessario modificare la dose in questi pazienti. Insufficienza renale: sulla base della farmacocinetica, non è necessario modificare la dose nei pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min), <specialità a base di nimesulide> è invece controindicato in caso di insufficienza renale grave (clearance della creatinina < 30ml/min) (vedere paragrafi 4.3 e 5.2). CPMP/3086/03-REV.1 3 EMEA 2004
4 Insufficienza epatica: l uso di <specialità a base di nimesulide> è controindicato in pazienti con insufficienza epatica (vedere paragrafo 5.2). 4.3 Controindicazioni Ipersensibilità nota a nimesulide o agli eccipienti del prodotto. Precedenti reazioni di ipersensibilità (per esempio, broncospasmo, rinite, orticaria) in risposta all acido acetilsalicilico o ad altri farmaci anti-infiammatori non steroidei. Precedenti reazioni epatotossiche alla nimesulide. Ulcera gastrica o duodenale attiva, precedenti ulcere o emorragie gastrointestinali ricorrenti, emorragie cerebrovascolari, altre emorragie o patologie emorragiche in corso. Disturbi gravi della coagulazione. Scompenso cardiaco grave. Insufficienza renale grave. Insufficienza epatica. Bambini al di sotto dei 12 anni. Terzo trimestre di gravidanza e allattamento (vedere paragrafi 4.6 e 5.3). 4.4 Avvertenze speciali e opportune precauzioni d impiego Il rischio di effetti indesiderati può essere ridotto usando <specialità a base di nimesulide> per il minor tempo possibile. Sospendere il trattamento se non si osservano benefici. In rari casi è stata riportata un associazione tra < specialità a base di nimesulide > e reazioni epatiche gravi, inclusi alcuni rarissimi casi di decesso (vedere anche paragrafo 4.8). I pazienti che accusano sintomi compatibili con lesioni epatiche durante il trattamento con <specialità a base di nimesulide> (per esempio, anoressia, nausea, vomito, dolori addominali, spossatezza, urine scure) o i pazienti che presentano nel corso del trattamento test anormali di funzionalità epatica devono sospendere il trattamento. Questi pazienti non dovrebbero più utilizzare nimesulide. Lesioni epatiche, reversibili nella maggior parte dei casi, sono state riportate dopo esposizione breve al farmaco. Durante il trattamento con <specialità a base di nimesulide> deve essere evitata la concomitante somministrazione di farmaci di cui è nota l epatotossicità e l abuso di alcolici in quanto possono aumentare il rischio di reazioni epatiche. Durante la terapia con <specialità a base di nimesulide>, occorre avvertire i pazienti di non assumere altri analgesici. Non è consigliato l uso concomitante di diversi FANS. In qualsiasi momento durante il trattamento si possono manifestare emorragie, ulcere o perforazioni gastrointestinali con o senza sintomi di preavviso o precedenti eventi gastrointestinali. Se si manifestano emorragie o ulcere gastrointestinali, sospendere il trattamento con nimesulide. Usare nimesulide con cautela nei pazienti con patologie gastrointestinali, inclusi precedenti ulcera peptica, emorragie gastrointestinali, colite ulcerosa o morbo di Crohn. Nei pazienti con insufficienza renale o cardiaca, occorre cautela perché l uso di <specialità a base di nimesulide> può danneggiare la funzionalità renale. In tal caso, sospendere il trattamento (vedere anche paragrafo 4.5 Interazioni con altri prodotti farmaceutici e altre forme di interazione ). I pazienti anziani sono particolarmente sensibili agli eventi avversi dei FANS, incluse emorragie e perforazioni gastrointestinali, insufficienza renale, cardiaca o epatica. E quindi consigliabile un costante monitoraggio clinico. Poiché nimesulide può interferire con la funzionalità piastrinica, va usata con cautela nei pazienti con diatesi emorragica (vedere anche paragrafo 4.3). <Specialità a base di nimesulide> non rappresenta tuttavia un sostituto dell acido acetilsalicilico nella profilassi cardiovascolare. I FANS possono mascherare la febbre dovuta a un infezione batterica sottostante. CPMP/3086/03-REV.1 4 EMEA 2004
5 L uso di <specialità a base di nimesulide> può ridurre la fertilità e non è consigliato in donne che cercano una gravidanza. Nelle donne che hanno difficoltà a concepire o che vengono sottoposte ad accertamenti per infertilità, si deve considerare la sospensione del trattamento con <specialità a base di nimesulide> (vedere paragrafo 4.6). Interazione con altri medicinali ed altre forme di interazione Interazioni farmacodinamiche I pazienti che ricevono warfarina, agenti anticoagulanti simili o acido acetilsalicilico presentano un maggior rischio di complicanze emorragiche se trattati con <specialità a base di nimesulide>. L associazione è pertanto sconsigliata (vedere anche paragrafo 4.4) ed è controindicata in pazienti con patologie gravi della coagulazione (vedere anche paragrafo 4.3). Se non si può evitare l associazione, monitorare costantemente l attività anticoagulante. Interazioni farmacodinamiche/farmacocinetiche con i diuretici Nei soggetti sani, nimesulide riduce transitoriamente l effetto di furosemide sull escrezione di sodio e, in misura minore, sull escrezione di potassio e riduce la risposta diuretica. La somministrazione concomitante di furosemide e nimesulide comporta una riduzione (di circa il 20%) dell AUC e dell escrezione totale di furosemide, senza comprometterne la clearance renale. L uso concomitante di furosemide e di <specialità a base di nimesulide> richiede cautela in pazienti con patologie renali o cardiache, come descritto al paragrafo 4.4. Interazioni farmacocinetiche con altri farmaci: E stato riportato che i farmaci anti-infiammatori non steroidei riducono la clearance del litio e questo comporta livelli plasmatici elevati e tossicità da litio. Se si prescrive <specialità a base di nimesulide> a un paziente in terapia con litio, occorre monitorare costantemente i livelli di litio. Sono anche state studiate in vivo potenziali interazioni farmacocinetiche con glibenclamide, teofillina, warfarina, digossina, cimetidina e un preparato antiacido (una combinazione di idrossido di alluminio e magnesio). Non sono state osservate interazioni clinicamente significative. Nimesulide inibisce il CYP2C9. Le concentrazioni plasmatiche dei farmaci che vengono metabolizzate da questo enzima possono aumentare se si somministrano in concomitanza con <specialità a base di nimesulide>. Occorre cautela se nimesulide viene assunta meno di 24 ore prima o dopo il trattamento con metotressato perché i livelli sierici di metotressato possono aumentare causando una maggiore tossicità del farmaco. Dato il loro effetto sulle prostaglandine renali, gli inibitori delle sintetasi delle prostaglandine come nimesulide possono aumentare la nefrotossicità delle ciclosporine. Effetti di altri farmaci su nimesulide: Studi in vitro hanno dimostrato che tolbutamide, acido salicilico e acido valproico spostano la nimesulide dai siti di legame con le proteine plasmatiche. Nonostante un possibile effetto sui livelli plasmatici di nimesulide, queste interazioni non sono risultate clinicamente significative. 4.6 Gravidanza ed allattamento L uso di <specialità a base di nimesulide> è controindicato nell ultimo trimestre di gravidanza (vedere paragrafo 4.3). Come per gli altri FANS, l uso di <specialità a base di nimesulide> non è consigliato nelle donne che cercano una gravidanza (vedere paragrafo 4.4). Come per gli altri FANS, di cui è nota l inibizione della sintesi delle prostaglandine, nimesulide può provocare chiusura prematura del dotto arterioso, ipertensione polmonare, oliguria, oligoamniosi, maggior rischio di emorragie, inerzia uterina ed edema periferico. Sono stati riportati casi isolati di CPMP/3086/03-REV.1 5 EMEA 2004
6 insufficienza renale in neonati di donne che avevano assunto nimesulide nell ultimo periodo di gravidanza. Inoltre, studi su conigli hanno dimostrato una tossicità riproduttiva atipica (vedere paragrafo 5.3) e non sono disponibili dati esaurienti sull uso di <specialità a base di nimesulide> nelle donne in gravidanza. Non è pertanto noto il rischio potenziale per l uomo e non è raccomandato prescrivere il farmaco durante i primi due trimestri di gravidanza. Allattamento: Non è noto se <specialità a base di nimesulide> viene secreto nel latte umano. <Specialità a base di nimesulide> è controindicato nelle donne che allattano (vedere paragrafi 4.3 e 5.3). 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Non sono stati effettuati studi sugli effetti di <specialità a base di nimesulide> sulla capacità di guidare o usare macchinari. Tuttavia, i pazienti che soffrono di capogiri, vertigini o sonnolenza dopo aver assunto <specialità a base di nimesulide> dovrebbero astenersi dal guidare o usare macchinari. 4.8 Effetti indesiderati Il seguente elenco di effetti indesiderati si basa sui risultati di sperimentazioni cliniche controllate* (su circa pazienti) e sui dati di farmacovigilanza. I con i casi riportati classificati come molto comuni (>1/10); comuni (>1/100, <1/10), non comuni (>1/1.000, <1/100); rari (>1/10.000, <1/1.000); molto rari (<1/10.000), inclusi i casi isolati. Sangue Anemia* Eosinofilia * Trombocitopenia Pancitopenia Porpora Sistema immunitario Ipersensibilità* Anafilassi Disordini del metabolismo e della nutrizione Iperkaliemia* Disturbi psichiatrici Ansia* Nervosismo* Incubi* Disordini del sistema nervoso Non comuni Vertigini* Mal di testa Sonnolenza Encefalopatia (sindrome di Reye) Disturbi oculari Visione sfuocata * Disturbi visivi Apparato uditivo e vestibolare Vertigini Disturbi cardiaci Tachicardia* Sistema vascolare Non comuni Ipertensione* Disturbi respiratori Non comuni Dispnea* Emorragia* Fluttuazioni della pressione arteriosa * Vampate di calore * Asma Broncospasmo CPMP/3086/03-REV.1 6 EMEA 2004
7 Apparato gastrointestinale Sistema epatobiliare (vedere paragrafo 4.4 Avvertenze e precauzioni d uso speciali ) Cute e annessi Sistema urinario Disordini generali Comuni Non comuni Non comuni Non comuni Diarrea* Nausea* Vomito* Stipsi* Flatulenza* Gastrite* Dolori addominali Dispepsia Stomatite Melena Emorragie gastrointestinali Ulcera e perforazione duodenale Ulcera e perforazione gastrica Epatite Epatite fulminante (inclusi casi letali) Ittero Colestasi Prurito* Eruzioni* Aumento della sudorazione* Eritema* Dermatite* Orticaria Edema angioneurotico Edema del viso Eritema multiforme Sindrome di Stevens Johnson Necrolisi epidermica tossica Disuria* Ematuria* Ritenzione urinaria* Insufficienza renale Oliguria Nefrite interstiziale Edema* Malessere* Astenia* Ipotermia Esami di laboratorio Comuni Aumento degli enzimi epatici* * dati di frequenza ricavati dalle sperimentazioni cliniche 4.9 Sovradosaggio I sintomi associati a sovradosaggio acuto di FANS si limitano di solito a sonnolenza, torpore, nausea, vomito e dolori epigastrici, generalmente reversibili con terapia di supporto. Si possono manifestare emorragie gastrointestinali. Si possono manifestare anche, sia pur raramente, ipertensione, insufficienza renale acuta, insufficienza respiratoria e coma. Dopo ingestione di FANS a dosi terapeutiche sono state riportate reazioni di anafilassi, che si potrebbero manifestare anche dopo sovradosaggio. In caso di sovradosaggio da FANS i pazienti vanno gestiti con terapie sintomatiche e di supporto. Non esistono antidoti specifici. Non sono disponibili informazioni sull eliminazione di nimesulide tramite emodialisi: dato il suo grado elevato di legame alle proteine plasmatiche (fino al 97,5%), è improbabile che la dialisi risulti utile in caso di sovradosaggio. L emesi e/o il carbone attivo (da 60 a 100 g negli adulti) e/o i catartici osmotici possono essere indicati, se somministrati entro 4 ore in pazienti con sintomi da sovradosaggio o che hanno assunto elevate dosi di nimesulide. La diuresi CPMP/3086/03-REV.1 7 EMEA 2004
8 forzata, l alcalinizzazione delle urine, l emodialisi o l emoperfusione possono non risultare utili a causa del legame elevato con le proteine. Occorre monitorare la funzionalità renale ed epatica. 5. PROPRIETA FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Gruppo farmacoterapico: ATC codice: M01AX17 La nimesulide è un farmaco anti-infiammatorio non steroideo con proprietà analgesiche e antipiretiche che agisce inibendo l enzima ciclo-ossigenasi che sintetizza le prostaglandine. 5.2 Proprietà farmacocinetiche Nimesulide viene ben assorbita dopo la somministrazione orale. Dopo una dose singola di 100 mg di nimesulide, negli adulti si raggiunge il livello massimo nel plasma di 3-4 mg/l dopo 2-3 ore. AUC = mg h/l. Non sono state riscontrate differenze statisticamente significative tra questi valori e quelli registrati dopo la somministrazione di 100 mg due volte al giorno per 7 giorni. Fino al 97,5% del farmaco si lega alle proteine plasmatiche. Nimesulide viene ampiamente metabolizzata nel fegato attraverso diverse vie, inclusi gli isoenzimi CYP2C9 del citocromo P450. Sussiste pertanto una potenziale interazione farmacologica con farmaci metabolizzati da CYP2C9 (vedere paragrafo 4.5). Il metabolita principale è il para-idrossi derivato che è anch esso attivo farmacologicamente. Il tempo alla comparsa del metabolita in circolo è breve (circa 0,8 ore), ma la sua costante di formazione non è elevata ed è notevolmente inferiore alla costante di assorbimento di nimesulide. L idrossinimesulide è il solo metabolita trovato nel plasma, ed è quasi completamente coniugato. Il suo T ½ varia da 3,2 a 6 ore. Nimesulide viene escreta principalmente nelle urine (circa il 50% della dose somministrata). Solo l 1-3% viene escreto come farmaco non modificato. L idrossinimesulide, il metabolita principale, si trova solo come glicuronato. Circa il 29% della dose viene escreta metabolizzata nelle feci. Il profilo cinetico di nimesulide non cambia negli anziani sia dopo dose singola e ripetute. In uno studio sperimentale con singola somministrazione svolto su pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min) vs. volontari sani, i picchi plasmatici di nimesulide e del suo metabolita principale non erano superiori a quelli dei volontari sani. AUC e t1/2 beta erano del 50% superiori, ma comunque sempre nell intervallo di variabilità dei valori cinetici osservati per nimesulide nei volontari sani. La somministrazione ripetuta non ha determinato accumulo. Nimesulide è controindicata in pazienti con insufficienza epatica (vedere paragrafo 4.3). 5.3 Dati preclinici di sicurezza I dati preclinici non evidenziano particolari rischi per l uomo sulla base degli studi convenzionali di farmacologia sulla sicurezza, tossicità di dosi ripetute, genotossicità e potenziale oncogeno. Negli studi di tossicità con dosi ripetute, nimesulide ha mostrato tossicità gastrointestinale, renale ed epatica. Negli studi di tossicità riproduttiva sono stati osservati segni di potenziale teratogeno o embriotossico (malformazioni scheletriche, dilatazione dei ventricoli cerebrali) nei conigli, ma non nei ratti, trattati fino a livelli di dose non tossici per le madri. Nei ratti, sono stati osservati un aumento della mortalità nella prole nel primo periodo postnatale ed effetti indesiderati sulla fertilità. CPMP/3086/03-REV.1 8 EMEA 2004
9 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti 6.2 Incompatibilità 6.3 Periodo di validità 6.4 Speciali precauzioni per la conservazione 6.5 Natura e contenuto del contenitore 6.6 Istruzioni per l impiego e la manipolazione 7. TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO 8. NUMERI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO 9. DATA DELLA PRIMA AUTORIZZAZIONE/RINNOVO DELL AUTORIZZAZIONE 10. DATA DI REVISIONE DEL TESTO CPMP/3086/03-REV.1 9 EMEA 2004
10 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NIMESULIDE-β-CICLODESTRINA 400 MG COMPRESSE NIMESULIDE-β-CICLODESTRINA 400 MG GRANULATO PER SOSPENSIONE ORALE CPMP/3086/03-REV.1 10 EMEA 2004
11 1. DENOMINAZIONE DEL MEDICINALE < DENOMINAZIONE COMMERCIALE DEL PRODOTTO > 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa e bustina contiene 400 mg di nimesulide-β-ciclodestrina, corrispondente a 100 mg di nimesulide. Per gli eccipienti vedere paragrafo FORMA FARMACEUTICA Compresse : < Specifica per azienda>. Granulato per sospensione orale: < Specifica per azienda>. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Trattamento del dolore acuto. Trattamento sintomatico dell osteoartrite dolorosa. Dismenorrea primaria. 4.2 Posologia e modo di somministrazione <Specialità a base di nimesulide> deve essere usato per il minor tempo possibile in base alle esigenze cliniche. Adulti: 400 mg nimesulide-β-ciclodestrina bustina e compressa: (=100 mg nimesulide) b.i.d. dopo i pasti. Anziani: nei pazienti anziani non occorre ridurre la dose giornaliera (vedere paragrafo 5.2). Bambini (<12 anni): <Specialità a base di nimesulide> è controindicato in questi pazienti (vedere anche paragrafo 4.3). Adolescenti (da 12 a 18 anni): sulla base del profilo cinetico negli adulti e delle caratteristiche farmacodinamiche di nimesulide, non è necessario modificare la dose in questi pazienti. Insufficienza renale: sulla base della farmacocinetica, non è necessario modificare la dose nei pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min), <specialità a base di nimesulide> è invece controindicato in caso di insufficienza renale grave (clearance della creatinina < 30ml/min) (vedere paragrafi 4.3 e 5.2). Insufficienza epatica: l uso di <specialità a base di nimesulide> è controindicato in pazienti con insufficienza epatica (vedere paragrafo 5.2). CPMP/3086/03-REV.1 11 EMEA 2004
12 4.3 Controindicazioni Ipersensibilità nota a nimesulide o agli eccipienti del prodotto. Precedenti reazioni di ipersensibilità (per esempio, broncospasmo, rinite, orticaria) in risposta all acido acetilsalicilico o ad altri farmaci anti-infiammatori non steroidei. Precedenti reazioni epatotossiche alla nimesulide. Ulcera gastrica o duodenale attiva, precedenti ulcere o emorragie gastrointestinali ricorrenti, emorragie cerebrovascolari, altre emorragie o patologie emorragiche in corso. Disturbi gravi della coagulazione. Scompenso cardiaco grave. Insufficienza renale grave. Insufficienza epatica. Bambini al di sotto dei 12 anni. Terzo trimestre di gravidanza e allattamento (vedere paragrafi 4.6 e 5.3). 4.4 Avvertenze speciali e opportune precauzioni d impiego Il rischio di effetti indesiderati può essere ridotto usando <specialità a base di nimesulide> per il minor tempo possibile. Sospendere il trattamento se non si osservano benefici. In rari casi è stata riportata un associazione tra < specialità a base di nimesulide > e reazioni epatiche gravi, inclusi alcuni rarissimi casi di decesso (vedere anche paragrafo 4.8). I pazienti che accusano sintomi compatibili con lesioni epatiche durante il trattamento con <specialità a base di nimesulide> (per esempio, anoressia, nausea, vomito, dolori addominali, spossatezza, urine scure) o i pazienti che presentano nel corso del trattamento test anormali di funzionalità epatica devono sospendere il trattamento. Questi pazienti non dovrebbero più utilizzare nimesulide. Lesioni epatiche, reversibili nella maggior parte dei casi, sono state riportate dopo esposizione breve al farmaco. Durante il trattamento con <specialità a base di nimesulide> deve essere evitata la concomitante somministrazione di farmaci di cui è nota l epatotossicità e l abuso di alcolici in quanto possono aumentare il rischio di reazioni epatiche. Durante la terapia con <specialità a base di nimesulide>, occorre avvertire i pazienti di non assumere altri analgesici. Non è consigliato l uso concomitante di diversi FANS. In qualsiasi momento durante il trattamento si possono manifestare emorragie, ulcere o perforazioni gastrointestinali con o senza sintomi di preavviso o precedenti eventi gastrointestinali. Se si manifestano emorragie o ulcere gastrointestinali, sospendere il trattamento con nimesulide. Usare nimesulide con cautela nei pazienti con patologie gastrointestinali, inclusi precedenti ulcera peptica, emorragie gastrointestinali, colite ulcerosa o morbo di Crohn. Nei pazienti con insufficienza renale o cardiaca, occorre cautela perché l uso di <specialità a base di nimesulide> può danneggiare la funzionalità renale. In tal caso, sospendere il trattamento (vedere anche paragrafo 4.5 Interazioni con altri prodotti farmaceutici e altre forme di interazione ). I pazienti anziani sono particolarmente sensibili agli eventi avversi dei FANS, incluse emorragie e perforazioni gastrointestinali, insufficienza renale, cardiaca o epatica. E quindi consigliabile un costante monitoraggio clinico. Poiché nimesulide può interferire con la funzionalità piastrinica, va usata con cautela nei pazienti con diatesi emorragica (vedere anche paragrafo 4.3). <Specialità a base di nimesulide> non rappresenta tuttavia un sostituto dell acido acetilsalicilico nella profilassi cardiovascolare. I FANS possono mascherare la febbre dovuta a un infezione batterica sottostante. CPMP/3086/03-REV.1 12 EMEA 2004
13 L uso di <specialità a base di nimesulide> può ridurre la fertilità e non è consigliato in donne che cercano una gravidanza. Nelle donne che hanno difficoltà a concepire o che vengono sottoposte ad accertamenti per infertilità, si deve considerare la sospensione del trattamento con <specialità a base di nimesulide> (vedere paragrafo 4.6). 4.5 Interazione con altri medicinali ed altre forme di interazione Interazioni farmacodinamiche I pazienti che ricevono warfarina, agenti anticoagulanti simili o acido acetilsalicilico presentano un maggior rischio di complicanze emorragiche se trattati con <specialità a base di nimesulide>. L associazione è pertanto sconsigliata (vedere anche paragrafo 4.4) ed è controindicata in pazienti con patologie gravi della coagulazione (vedere anche paragrafo 4.3). Se non si può evitare l associazione, monitorare costantemente l attività anticoagulante. Interazioni farmacodinamiche/farmacocinetiche con i diuretici Nei soggetti sani, nimesulide riduce transitoriamente l effetto di furosemide sull escrezione di sodio e, in misura minore, sull escrezione di potassio e riduce la risposta diuretica. La somministrazione concomitante di furosemide e nimesulide comporta una riduzione (di circa il 20%) dell AUC e dell escrezione totale di furosemide, senza comprometterne la clearance renale. L uso concomitante di furosemide e di <specialità a base di nimesulide> richiede cautela in pazienti con patologie renali o cardiache, come descritto al paragrafo 4.4. Interazioni farmacocinetiche con altri farmaci: E stato riportato che i farmaci anti-infiammatori non steroidei riducono la clearance del litio e questo comporta livelli plasmatici elevati e tossicità da litio. Se si prescrive <specialità a base di nimesulide> a un paziente in terapia con litio, occorre monitorare costantemente i livelli di litio. Sono anche state studiate in vivo potenziali interazioni farmacocinetiche con glibenclamide, teofillina, warfarina, digossina, cimetidina e un preparato antiacido (una combinazione di idrossido di alluminio e magnesio). Non sono state osservate interazioni clinicamente significative. Nimesulide inibisce il CYP2C9. Le concentrazioni plasmatiche dei farmaci che vengono metabolizzate da questo enzima possono aumentare se si somministrano in concomitanza con <specialità a base di nimesulide>. Occorre cautela se nimesulide viene assunta meno di 24 ore prima o dopo il trattamento con metotressato perché i livelli sierici di metotressato possono aumentare causando una maggiore tossicità del farmaco. Dato il loro effetto sulle prostaglandine renali, gli inibitori delle sintetasi delle prostaglandine come nimesulide possono aumentare la nefrotossicità delle ciclosporine. Effetti di altri farmaci su nimesulide: Studi in vitro hanno dimostrato che tolbutamide, acido salicilico e acido valproico spostano la nimesulide dai siti di legame con le proteine plasmatiche. Nonostante un possibile effetto sui livelli plasmatici di nimesulide, queste interazioni non sono risultate clinicamente significative. 4.6 Gravidanza ed allattamento L uso di <specialità a base di nimesulide> è controindicato nell ultimo trimestre di gravidanza (vedere paragrafo 4.3). Come per gli altri FANS, l uso di <specialità a base di nimesulide> non è consigliato nelle donne che cercano una gravidanza (vedere paragrafo 4.4). Come per gli altri FANS, di cui è nota l inibizione della sintesi delle prostaglandine, nimesulide può provocare chiusura prematura del dotto arterioso, ipertensione polmonare, oliguria, oligoamniosi, maggior rischio di emorragie, inerzia uterina ed edema periferico. Sono stati riportati casi isolati di insufficienza renale in neonati di donne che avevano assunto nimesulide nell ultimo periodo di gravidanza. CPMP/3086/03-REV.1 13 EMEA 2004
14 Inoltre, studi su conigli hanno dimostrato una tossicità riproduttiva atipica (vedere paragrafo 5.3) e non sono disponibili dati esaurienti sull uso di <specialità a base di nimesulide> nelle donne in gravidanza. Non è pertanto noto il rischio potenziale per l uomo e non è raccomandato prescrivere il farmaco durante i primi due trimestri di gravidanza. Allattamento: Non è noto se <specialità a base di nimesulide> viene secreto nel latte umano. <Specialità a base di nimesulide> è controindicato nelle donne che allattano (vedere paragrafi 4.3 e 5.3). 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Non sono stati effettuati studi sugli effetti di <specialità a base di nimesulide> sulla capacità di guidare o usare macchinari. Tuttavia, i pazienti che soffrono di capogiri, vertigini o sonnolenza dopo aver assunto <specialità a base di nimesulide> dovrebbero astenersi dal guidare o usare macchinari. 4.8 Effetti indesiderati Il seguente elenco di effetti indesiderati si basa sui risultati di sperimentazioni cliniche controllate* (su circa pazienti) e sui dati di farmacovigilanza. I con i casi riportati classificati come molto comuni (>1/10); comuni (>1/100, <1/10), non comuni (>1/1.000, <1/100); rari (>1/10.000, <1/1.000); molto rari (<1/10.000), inclusi i casi isolati. Sangue Anemia* Eosinofilia * Trombocitopenia Pancitopenia Porpora Sistema immunitario Ipersensibilità* Anafilassi Disordini del metabolismo e della nutrizione Iperkaliemia* Disturbi psichiatrici Ansia* Nervosismo* Incubi* Disordini del sistema nervoso Non comuni Vertigini* Mal di testa Sonnolenza Encefalopatia (sindrome di Reye) Disturbi oculari Visione sfuocata * Disturbi visivi Apparato uditivo e vestibolare Vertigini Disturbi cardiaci Tachicardia* Sistema vascolare Non comuni Ipertensione* Disturbi respiratori Non comuni Dispnea* Emorragia* Fluttuazioni della pressione arteriosa* Vampate di calore * Asma Broncospasmo CPMP/3086/03-REV.1 14 EMEA 2004
15 Apparato gastrointestinale Sistema epatobiliare (vedere paragrafo 4.4 Avvertenze e precauzioni d uso speciali ) Cute e annessi Sistema urinario Disordini generali Comuni Non comuni Non comuni Non comuni Diarrea* Nausea* Vomito* Stipsi* Flatulenza* Gastrite* Dolori addominali Dispepsia Stomatite Melena Emorragie gastrointestinali Ulcera e perforazione duodenale Ulcera e perforazione gastrica Epatite Epatite fulminante (inclusi casi letali) Ittero Colestasi Prurito* Eruzioni* Aumento della sudorazione* Eritema* Dermatite* Orticaria Edema angioneurotico Edema del viso Eritema multiforme Sindrome di Stevens Johnson Necrolisi epidermica tossica Disuria* Ematuria* Ritenzione urinaria* Insufficienza renale Oliguria Nefrite interstiziale Edema* Malessere* Astenia* Ipotermia Esami di laboratorio Comuni Aumento degli enzimi epatici* * dati di frequenza ricavati dalle sperimentazioni cliniche 4.9 Sovradosaggio I sintomi associati a sovradosaggio acuto di FANS si limitano di solito a sonnolenza, torpore, nausea, vomito e dolori epigastrici, generalmente reversibili con terapia di supporto. Si possono manifestare emorragie gastrointestinali. Si possono manifestare anche, sia pur raramente, ipertensione, insufficienza renale acuta, insufficienza respiratoria e coma. Dopo ingestione di FANS a dosi terapeutiche sono state riportate reazioni di anafilassi, che si potrebbero manifestare anche dopo sovradosaggio. In caso di sovradosaggio da FANS i pazienti vanno gestiti con terapie sintomatiche e di supporto. Non esistono antidoti specifici. Non sono disponibili informazioni sull eliminazione di nimesulide tramite emodialisi: dato il suo grado elevato di legame alle proteine plasmatiche (fino al 97,5%), è improbabile che la dialisi risulti utile in caso di sovradosaggio. L emesi e/o il carbone attivo (da 60 a 100 g negli adulti) e/o i catartici osmotici possono essere indicati, se somministrati entro 4 ore in pazienti con sintomi da sovradosaggio o che hanno assunto elevate dosi di nimesulide. La diuresi CPMP/3086/03-REV.1 15 EMEA 2004
16 forzata, l alcalinizzazione delle urine, l emodialisi o l emoperfusione possono non risultare utili a causa del legame elevato con le proteine. Occorre monitorare la funzionalità renale ed epatica. 5. PROPRIETA FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Gruppo farmacoterapico: ATC codice: M01AX17 La nimesulide è un farmaco anti-infiammatorio non steroideo con proprietà analgesiche e antipiretiche che agisce inibendo l enzima ciclo-ossigenasi che sintetizza le prostaglandine. 5.2 Proprietà farmacocinetiche Nimesulide viene ben assorbita dopo la somministrazione orale. Dopo una dose singola di 100 mg di nimesulide, negli adulti si raggiunge il livello massimo nel plasma di 3-4 mg/l dopo 2-3 ore. AUC = mg h/l. Non sono state riscontrate differenze statisticamente significative tra questi valori e quelli registrati dopo la somministrazione di 100 mg due volte al giorno per 7 giorni. Dopo singola somministrazione, nimesulide-β-ciclodestrina 400 mg bustine è risultata essere bioequivalente (in termini di AUC e Cmax) a 100 mg <specialità a base di nimesulide> bustine. Inoltre il t½ è risultato quasi identico per le due formulazioni, mentre il Tmax è stato di circa 1,5 e 2,5 ore rispettivamente per nimesulide-β-ciclodestrina bustine e <specialità a base di nimesulide> bustine, mostrando che nimesulide betaciclodestrina è più rapidamente assorbita. Fino al 97,5% del farmaco si lega alle proteine plasmatiche. Nimesulide viene ampiamente metabolizzata nel fegato attraverso diverse vie, inclusi gli isoenzimi CYP2C9 del citocromo P450. Sussiste pertanto una potenziale interazione farmacologica con farmaci metabolizzati da CYP2C9 (vedere paragrafo 4.5). Il metabolita principale è il para-idrossi derivato che è anch esso attivo farmacologicamente. Il tempo alla comparsa del metabolita in circolo è breve (circa 0,8 ore), ma la sua costante di formazione non è elevata ed è notevolmente inferiore alla costante di assorbimento di nimesulide. L idrossinimesulide è il solo metabolita trovato nel plasma, ed è quasi completamente coniugato. Il suo T ½ varia da 3,2 a 6 ore. Nimesulide viene escreta principalmente nelle urine (circa il 50% della dose somministrata). Solo l 1-3% viene escreto come farmaco non modificato. L idrossinimesulide, il metabolita principale, si trova solo come glicuronato. Circa il 29% della dose viene escreta metabolizzata nelle feci. Il profilo cinetico di nimesulide non cambia negli anziani sia dopo dose singola e ripetute. In uno studio sperimentale con singola somministrazione svolto su pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min) vs. volontari sani, i picchi plasmatici di nimesulide e del suo metabolita principale non erano superiori a quelli dei volontari sani. AUC e t1/2 beta erano del 50% superiori, ma comunque sempre nell intervallo di variabilità dei valori cinetici osservati per nimesulide nei volontari sani. La somministrazione ripetuta non ha determinato accumulo. Nimesulide è controindicata in pazienti con insufficienza epatica (vedere paragrafo 4.3). 5.3 Dati preclinici di sicurezza I dati preclinici non evidenziano particolari rischi per l uomo sulla base degli studi convenzionali di farmacologia sulla sicurezza, tossicità di dosi ripetute, genotossicità e potenziale oncogeno. Negli studi di tossicità con dosi ripetute, nimesulide ha mostrato tossicità gastrointestinale, renale ed epatica. CPMP/3086/03-REV.1 16 EMEA 2004
17 Negli studi di tossicità riproduttiva sono stati osservati segni di potenziale teratogeno o embriotossico (malformazioni scheletriche, dilatazione dei ventricoli cerebrali) nei conigli, ma non nei ratti, trattati fino a livelli di dose non tossici per le madri. Nei ratti, sono stati osservati un aumento della mortalità nella prole nel primo periodo postnatale ed effetti indesiderati sulla fertilità. 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti 6.2 Incompatibilità 6.3 Periodo di validità 6.4 Speciali precauzioni per la conservazione 6.5 Natura e contenuto del contenitore 6.6 Istruzioni per l impiego e la manipolazione 7. TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO 8. NUMERI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO 9. DATA DELLA PRIMA AUTORIZZAZIONE/RINNOVO DELL AUTORIZZAZIONE 10. DATA DI REVISIONE DEL TESTO CPMP/3086/03-REV.1 17 EMEA 2004
18 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO NIMESULIDE 100 MG O 200 MG SUPPOSTE CPMP/3086/03-REV.1 18 EMEA 2004
19 1. DENOMINAZIONE DEL MEDICINALE < DENOMINAZIONE COMMERCIALE DEL PRODOTTO > 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni supposta contiene 100 mg o 200 mg di nimesulide. Per gli eccipienti vedere paragrafo FORMA FARMACEUTICA Supposte: < Specifica per azienda>. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Trattamento del dolore acuto. Trattamento sintomatico dell osteoartrite dolorosa. Dismenorrea primaria. 4.2 Posologia e modo di somministrazione <Specialità a base di nimesulide> deve essere usato per il minor tempo possibile in base alle esigenze cliniche. Adulti: Supposte da 100 mg o 200 mg di nimesulide: 200 mg due volte al giorno. Anziani: nei pazienti anziani non occorre ridurre la dose giornaliera (vedere paragrafo 5.2). Bambini (<12 anni): <Specialità a base di nimesulide> è controindicato in questi pazienti (vedere anche paragrafo 4.3). Adolescenti (da 12 a 18 anni): sulla base del profilo cinetico negli adulti e delle caratteristiche farmacodinamiche di nimesulide, non è necessario modificare la dose in questi pazienti. Insufficienza renale: sulla base della farmacocinetica, non è necessario modificare la dose nei pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min), <specialità a base di nimesulide> è invece controindicato in caso di insufficienza renale grave (clearance della creatinina < 30ml/min) (vedere paragrafi 4.3 e 5.2). Insufficienza epatica: l uso di <specialità a base di nimesulide> è controindicato in pazienti con insufficienza epatica (vedere paragrafo 5.2). CPMP/3086/03-REV.1 19 EMEA 2004
20 4.3 Controindicazioni Ipersensibilità nota a nimesulide o agli eccipienti del prodotto. Precedenti reazioni di ipersensibilità (per esempio, broncospasmo, rinite, orticaria) in risposta all acido acetilsalicilico o ad altri farmaci anti-infiammatori non steroidei. Precedenti reazioni epatotossiche alla nimesulide. Ulcera gastrica o duodenale attiva, precedenti ulcere o emorragie gastrointestinali ricorrenti, emorragie cerebrovascolari, altre emorragie o patologie emorragiche in corso. Disturbi gravi della coagulazione. Scompenso cardiaco grave. Insufficienza renale grave. Insufficienza epatica. Bambini al di sotto dei 12 anni. Terzo trimestre di gravidanza e allattamento (vedere paragrafi 4.6 e 5.3). 4.4 Avvertenze speciali e opportune precauzioni d impiego Il rischio di effetti indesiderati può essere ridotto usando <specialità a base di nimesulide> per il minor tempo possibile. Sospendere il trattamento se non si osservano benefici. In rari casi è stata riportata un associazione tra < specialità a base di nimesulide > e reazioni epatiche gravi, inclusi alcuni rarissimi casi di decesso (vedere anche paragrafo 4.8). I pazienti che accusano sintomi compatibili con lesioni epatiche durante il trattamento con <specialità a base di nimesulide> (per esempio, anoressia, nausea, vomito, dolori addominali, spossatezza, urine scure) o i pazienti che presentano nel corso del trattamento test anormali di funzionalità epatica devono sospendere il trattamento. Questi pazienti non dovrebbero più utilizzare nimesulide. Lesioni epatiche, reversibili nella maggior parte dei casi, sono state riportate dopo esposizione breve al farmaco. Durante il trattamento con <specialità a base di nimesulide> deve essere evitata la concomitante somministrazione di farmaci di cui è nota l epatotossicità e l abuso di alcolici in quanto possono aumentare il rischio di reazioni epatiche. Durante la terapia con <specialità a base di nimesulide>, occorre avvertire i pazienti di non assumere altri analgesici. Non è consigliato l uso concomitante di diversi FANS. In qualsiasi momento durante il trattamento si possono manifestare emorragie, ulcere o perforazioni gastrointestinali con o senza sintomi di preavviso o precedenti eventi gastrointestinali. Se si manifestano emorragie o ulcere gastrointestinali, sospendere il trattamento con nimesulide. Usare nimesulide con cautela nei pazienti con patologie gastrointestinali, inclusi precedenti ulcera peptica, emorragie gastrointestinali, colite ulcerosa o morbo di Crohn. Nei pazienti con insufficienza renale o cardiaca, occorre cautela perché l uso di <specialità a base di nimesulide> può danneggiare la funzionalità renale. In tal caso, sospendere il trattamento (vedere anche paragrafo 4.5 Interazioni con altri prodotti farmaceutici e altre forme di interazione ). I pazienti anziani sono particolarmente sensibili agli eventi avversi dei FANS, incluse emorragie e perforazioni gastrointestinali, insufficienza renale, cardiaca o epatica. E quindi consigliabile un costante monitoraggio clinico. Poiché nimesulide può interferire con la funzionalità piastrinica, va usata con cautela nei pazienti con diatesi emorragica (vedere anche paragrafo 4.3). <Specialità a base di nimesulide> non rappresenta tuttavia un sostituto dell acido acetilsalicilico nella profilassi cardiovascolare. I FANS possono mascherare la febbre dovuta a un infezione batterica sottostante. CPMP/3086/03-REV.1 20 EMEA 2004
21 L uso di <specialità a base di nimesulide> può ridurre la fertilità e non è consigliato in donne che cercano una gravidanza. Nelle donne che hanno difficoltà a concepire o che vengono sottoposte ad accertamenti per infertilità, si deve considerare la sospensione del trattamento con <specialità a base di nimesulide> (vedere paragrafo 4.6). 4.5 Interazione con altri medicinali ed altre forme di interazione Interazioni farmacodinamiche I pazienti che ricevono warfarina, agenti anticoagulanti simili o acido acetilsalicilico presentano un maggior rischio di complicanze emorragiche se trattati con <specialità a base di nimesulide>. L associazione è pertanto sconsigliata (vedere anche paragrafo 4.4) ed è controindicata in pazienti con patologie gravi della coagulazione (vedere anche paragrafo 4.3). Se non si può evitare l associazione, monitorare costantemente l attività anticoagulante. Interazioni farmacodinamiche/farmacocinetiche con i diuretici Nei soggetti sani, nimesulide riduce transitoriamente l effetto di furosemide sull escrezione di sodio e, in misura minore, sull escrezione di potassio e riduce la risposta diuretica. La somministrazione concomitante di furosemide e nimesulide comporta una riduzione (di circa il 20%) dell AUC e dell escrezione totale di furosemide, senza comprometterne la clearance renale. L uso concomitante di furosemide e di <specialità a base di nimesulide> richiede cautela in pazienti con patologie renali o cardiache, come descritto al paragrafo 4.4. Interazioni farmacocinetiche con altri farmaci: E stato riportato che i farmaci anti-infiammatori non steroidei riducono la clearance del litio e questo comporta livelli plasmatici elevati e tossicità da litio. Se si prescrive <specialità a base di nimesulide> a un paziente in terapia con litio, occorre monitorare costantemente i livelli di litio. Sono anche state studiate in vivo potenziali interazioni farmacocinetiche con glibenclamide, teofillina, warfarina, digossina, cimetidina e un preparato antiacido (una combinazione di idrossido di alluminio e magnesio). Non sono state osservate interazioni clinicamente significative. Nimesulide inibisce il CYP2C9. Le concentrazioni plasmatiche dei farmaci che vengono metabolizzate da questo enzima possono aumentare se si somministrano in concomitanza con <specialità a base di nimesulide>. Occorre cautela se nimesulide viene assunta meno di 24 ore prima o dopo il trattamento con metotressato perché i livelli sierici di metotressato possono aumentare causando una maggiore tossicità del farmaco. Dato il loro effetto sulle prostaglandine renali, gli inibitori delle sintetasi delle prostaglandine come nimesulide possono aumentare la nefrotossicità delle ciclosporine. Effetti di altri farmaci su nimesulide: Studi in vitro hanno dimostrato che tolbutamide, acido salicilico e acido valproico spostano la nimesulide dai siti di legame con le proteine plasmatiche. Nonostante un possibile effetto sui livelli plasmatici di nimesulide, queste interazioni non sono risultate clinicamente significative. 4.6 Gravidanza ed allattamento L uso di <specialità a base di nimesulide> è controindicato nell ultimo trimestre di gravidanza (vedere paragrafo 4.3). Come per gli altri FANS, l uso di <specialità a base di nimesulide> non è consigliato nelle donne che cercano una gravidanza (vedere paragrafo 4.4). Come per gli altri FANS, di cui è nota l inibizione della sintesi delle prostaglandine, nimesulide può provocare chiusura prematura del dotto arterioso, ipertensione polmonare, oliguria, oligoamniosi, maggior rischio di emorragie, inerzia uterina ed edema periferico. Sono stati riportati casi isolati di insufficienza renale in neonati di donne che avevano assunto nimesulide nell ultimo periodo di gravidanza. CPMP/3086/03-REV.1 21 EMEA 2004
22 Inoltre, studi su conigli hanno dimostrato una tossicità riproduttiva atipica (vedere paragrafo 5.3) e non sono disponibili dati esaurienti sull uso di <specialità a base di nimesulide> nelle donne in gravidanza. Non è pertanto noto il rischio potenziale per l uomo e non è raccomandato prescrivere il farmaco durante i primi due trimestri di gravidanza. Allattamento: Non è noto se <specialità a base di nimesulide> viene secreto nel latte umano. <Specialità a base di nimesulide> è controindicato nelle donne che allattano (vedere paragrafi 4.3 e 5.3). 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Non sono stati effettuati studi sugli effetti di <specialità a base di nimesulide> sulla capacità di guidare o usare macchinari. Tuttavia, i pazienti che soffrono di capogiri, vertigini o sonnolenza dopo aver assunto <specialità a base di nimesulide> dovrebbero astenersi dal guidare o usare macchinari. 4.8 Effetti indesiderati Il seguente elenco di effetti indesiderati si basa sui risultati di sperimentazioni cliniche controllate* (su circa pazienti) e sui dati di farmacovigilanza. I con i casi riportati classificati come molto comuni (>1/10); comuni (>1/100, <1/10), non comuni (>1/1.000, <1/100); rari (>1/10.000, <1/1.000); molto rari (<1/10.000), inclusi i casi isolati. Sangue Anemia* Eosinofilia * Trombocitopenia Pancitopenia Porpora Sistema immunitario Ipersensibilità* Anafilassi Disordini del metabolismo e della nutrizione Iperkaliemia* Disturbi psichiatrici Ansia* Nervosismo* Incubi* Disordini del sistema nervoso Non comuni Vertigini* Mal di testa Sonnolenza Encefalopatia (sindrome di Reye) Disturbi oculari Visione sfuocata * Disturbi visivi Apparato uditivo e vestibolare Vertigini Disturbi cardiaci Tachicardia* Sistema vascolare Non comuni Ipertensione* Disturbi respiratori Non comuni Dispnea* Emorragia* Fluttuazioni della pressione arteriosa* Vampate di calore * Asma Broncospasmo CPMP/3086/03-REV.1 22 EMEA 2004
23 Apparato gastrointestinale Sistema epatobiliare (vedere paragrafo 4.4 Avvertenze e precauzioni d uso speciali ) Cute e annessi Sistema urinario Disordini generali Comuni Non comuni Non comuni Non comuni Diarrea* Nausea* Vomito* Stipsi* Flatulenza* Gastrite* Dolori addominali Dispepsia Stomatite Melena Emorragie gastrointestinali Ulcera e perforazione duodenale Ulcera e perforazione gastrica Epatite Epatite fulminante (inclusi casi letali) Ittero Colestasi Prurito* Eruzioni* Aumento della sudorazione* Eritema* Dermatite* Orticaria Edema angioneurotico Edema del viso Eritema multiforme Sindrome di Stevens Johnson Necrolisi epidermica tossica Disuria* Ematuria* Ritenzione urinaria* Insufficienza renale Oliguria Nefrite interstiziale Edema* Malessere* Astenia* Ipotermia Esami di laboratorio Comuni Aumento degli enzimi epatici* * dati di frequenza ricavati dalle sperimentazioni cliniche 4.9 Sovradosaggio I sintomi associati a sovradosaggio acuto di FANS si limitano di solito a sonnolenza, torpore, nausea, vomito e dolori epigastrici, generalmente reversibili con terapia di supporto. Si possono manifestare emorragie gastrointestinali. Si possono manifestare anche, sia pur raramente, ipertensione, insufficienza renale acuta, insufficienza respiratoria e coma. Dopo ingestione di FANS a dosi terapeutiche sono state riportate reazioni di anafilassi, che si potrebbero manifestare anche dopo sovradosaggio. In caso di sovradosaggio da FANS i pazienti vanno gestiti con terapie sintomatiche e di supporto. Non esistono antidoti specifici. Non sono disponibili informazioni sull eliminazione di nimesulide tramite emodialisi: dato il suo grado elevato di legame alle proteine plasmatiche (fino al 97,5%), è improbabile che la dialisi risulti utile in caso di sovradosaggio. L emesi e/o il carbone attivo (da 60 a 100 g negli adulti) e/o i catartici osmotici possono essere indicati, se somministrati entro 4 ore in pazienti con sintomi da sovradosaggio o che hanno assunto elevate dosi di nimesulide. La diuresi CPMP/3086/03-REV.1 23 EMEA 2004
24 forzata, l alcalinizzazione delle urine, l emodialisi o l emoperfusione possono non risultare utili a causa del legame elevato con le proteine. Occorre monitorare la funzionalità renale ed epatica. 5. PROPRIETA FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Gruppo farmacoterapico: ATC codice: M01AX17 La nimesulide è un farmaco anti-infiammatorio non steroideo con proprietà analgesiche e antipiretiche che agisce inibendo l enzima ciclo-ossigenasi che sintetizza le prostaglandine. 5.2 Proprietà farmacocinetiche Dopo singola somministrazione di una supposta da 200 mg di <specialità a base di nimesulide> viene raggiunto in 4 ore un picco plasmatico di circa 2 mg/l, con un AUC medio di 27 mg h/l. I corrispondenti valori allo steady state sono stati: Cmax circa 3 mg/l; Tmax= 4 ore e AUC di 25 mg h/l. Inoltre le supposte di <specialità a base di nimesulide> 200 mg si sono dimostrate bioequivalenti a <specialità a base di nimesulide> 100 mg compresse, malgrado un più lungo Tmax ed un ridotto Cmax. Fino al 97,5% del farmaco si lega alle proteine plasmatiche. Nimesulide viene ampiamente metabolizzata nel fegato attraverso diverse vie, inclusi gli isoenzimi CYP2C9 del citocromo P450. Sussiste pertanto una potenziale interazione farmacologica con farmaci metabolizzati da CYP2C9 (vedere paragrafo 4.5). Il metabolita principale è il para-idrossi derivato che è anch esso attivo farmacologicamente. Il tempo alla comparsa del metabolita in circolo è breve (circa 0,8 ore), ma la sua costante di formazione non è elevata ed è notevolmente inferiore alla costante di assorbimento di nimesulide. L idrossinimesulide è il solo metabolita trovato nel plasma, ed è quasi completamente coniugato. Il suo T ½ varia da 3,2 a 6 ore. Nimesulide viene escreta principalmente nelle urine (circa il 50% della dose somministrata). Solo l 1-3% viene escreto come farmaco non modificato. L idrossinimesulide, il metabolita principale, si trova solo come glicuronato. Circa il 29% della dose viene escreta metabolizzata nelle feci. Il profilo cinetico di nimesulide non cambia negli anziani sia dopo dose singola e ripetute. In uno studio sperimentale con singola somministrazione svolto su pazienti con insufficienza renale da lieve a moderata (clearance della creatinina ml/min) vs. volontari sani, i picchi plasmatici di nimesulide e del suo metabolita principale non erano superiori a quelli dei volontari sani. AUC e t1/2 beta erano del 50% superiori, ma comunque sempre nell intervallo di variabilità dei valori cinetici osservati per nimesulide nei volontari sani. La somministrazione ripetuta non ha determinato accumulo. Nimesulide è controindicata in pazienti con insufficienza epatica (vedere paragrafo 4.3). 5.3 Dati preclinici di sicurezza I dati preclinici non evidenziano particolari rischi per l uomo sulla base degli studi convenzionali di farmacologia sulla sicurezza, tossicità di dosi ripetute, genotossicità e potenziale oncogeno. Negli studi di tossicità con dosi ripetute, nimesulide ha mostrato tossicità gastrointestinale, renale ed epatica. Negli studi di tossicità riproduttiva sono stati osservati segni di potenziale teratogeno o embriotossico (malformazioni scheletriche, dilatazione dei ventricoli cerebrali) nei conigli, ma non nei ratti, trattati fino a livelli di dose non tossici per le madri. Nei ratti, sono stati osservati un aumento della mortalità nella prole nel primo periodo postnatale ed effetti indesiderati sulla fertilità. CPMP/3086/03-REV.1 24 EMEA 2004
Additions appear in italics and underlined deletions in italics and strikethrough
 ALLEGATO III 1 AMENDMENTS TO BE INCLUDED IN THE RELEVANT SECTIONS OF THE SUMMARY OF PRODUCT CHARACTERISTICS OF NIMESULIDE CONTAINING MEDICINAL PRODUCTS (SYSTEMIC FORMULATIONS) Additions appear in italics
ALLEGATO III 1 AMENDMENTS TO BE INCLUDED IN THE RELEVANT SECTIONS OF THE SUMMARY OF PRODUCT CHARACTERISTICS OF NIMESULIDE CONTAINING MEDICINAL PRODUCTS (SYSTEMIC FORMULATIONS) Additions appear in italics
Anziani: Nei pazienti anziani non occorre ridurre la dose giornaliera (vedere paragrafo 5.2).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ISODOL 100 mg compresse ISODOL 100 mg granulato per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ISODOL 100 mg compresse ISODOL 100 mg granulato per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa
FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE TRADEMARK. Nimesulide
 FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE ALLEGATO 2 TRADEMARK Nimesulide Legga attentamente questo foglio illustrativo prima di iniziare ad usare il medicinale. - Conservi questo foglio. Potrebbe
FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE ALLEGATO 2 TRADEMARK Nimesulide Legga attentamente questo foglio illustrativo prima di iniziare ad usare il medicinale. - Conservi questo foglio. Potrebbe
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ebastina Teva 10 mg compresse orodispersibili Ebastina Teva 20 mg compresse orodispersibili 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ebastina Teva 10 mg compresse orodispersibili Ebastina Teva 20 mg compresse orodispersibili 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
FRISIUM 10 MG CAPSULE RIGIDE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA FRISIUM 10 MG CAPSULE RIGIDE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/1598/2013 del 27 settembre
FARMACOVIGILANZA FRISIUM 10 MG CAPSULE RIGIDE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/1598/2013 del 27 settembre
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore Nimedex 400 mg compresse Nimedex 400 mg granulato per sospensione orale Nimesulide ß-ciclodestrina Legga attentamente questo foglio prima di prendere
Foglio illustrativo: informazioni per l utilizzatore Nimedex 400 mg compresse Nimedex 400 mg granulato per sospensione orale Nimesulide ß-ciclodestrina Legga attentamente questo foglio prima di prendere
Dialoghi in Farmacologia Medica
 Dialoghi in Farmacologia Medica Tempesta Nimesulide e non solo cosa sta succedendo ai FANS? Brescia 10 luglio 2007 Istituto Clinico Città di Brescia ASPIRINA Intolleranza gastrica Disturbi sul sistema
Dialoghi in Farmacologia Medica Tempesta Nimesulide e non solo cosa sta succedendo ai FANS? Brescia 10 luglio 2007 Istituto Clinico Città di Brescia ASPIRINA Intolleranza gastrica Disturbi sul sistema
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini. Ketoprofene
 VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
SULIDAMOR 100 mg polvere per sospensione orale SULIDAMOR 100 mg compresse
 FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE SULIDAMOR 100 mg polvere per sospensione orale SULIDAMOR 100 mg compresse Nimesulide Legga attentamente questo foglio illustrativo prima di iniziare ad usare
FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE SULIDAMOR 100 mg polvere per sospensione orale SULIDAMOR 100 mg compresse Nimesulide Legga attentamente questo foglio illustrativo prima di iniziare ad usare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Per l elenco completo degli eccipienti, vedere paragrafo 6.1
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE IBUSTRIN 200 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: principio attivo: Indobufene 200
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE IBUSTRIN 200 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: principio attivo: Indobufene 200
3. FORMA FARMACEUTICA Liofilizzato orale. Ogni dose di Kestine 10 mg liofilizzato orale è bianca, rotonda, liofilizzata.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE KESTINE 10 mg liofilizzato orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose di Kestine 10 mg liofilizzato orale contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE KESTINE 10 mg liofilizzato orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose di Kestine 10 mg liofilizzato orale contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE MAGNESIA S.PELLEGRINO 90% polvere per sospensione orale MAGNESIA S.PELLEGRINO 45% polvere effervescente 2 COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE MAGNESIA S.PELLEGRINO 90% polvere per sospensione orale MAGNESIA S.PELLEGRINO 45% polvere effervescente 2 COMPOSIZIONE QUALITATIVA
NEO BOROCILLINA GOLA DOLORE
 FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 - DENOMINAZIONE DEL MEDICINALE BRONCHENOLO GOLA 0,25% Collutorio BRONCHENOLO GOLA 0,25% Spray per mucosa orale 2 - COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 - DENOMINAZIONE DEL MEDICINALE BRONCHENOLO GOLA 0,25% Collutorio BRONCHENOLO GOLA 0,25% Spray per mucosa orale 2 - COMPOSIZIONE QUALITATIVA E QUANTITATIVA
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA' MEDICINALE OLBETAM 250 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula contiene: acipimox 250 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA' MEDICINALE OLBETAM 250 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula contiene: acipimox 250 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ESAPENT 1000 mg Capsule molli ESAPENT 500 mg Capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ESAPENT 1000 mg capsule
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ESAPENT 1000 mg Capsule molli ESAPENT 500 mg Capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ESAPENT 1000 mg capsule
TANTUM VERDE GOLA 0,25 % collutorio TANTUM VERDE GOLA 0,25% soluzione per mucosa orale Flurbiprofene
 PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE
 FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE DOMES 100 mg compresse orodispersibili DOMES 100 mg granulato per sospensione orale nimesulide Medicinale Equivalente Legga attentamente questo foglio illustrativo
FOGLIO ILLUSTRATIVO: INFORMAZIONE AL PAZIENTE DOMES 100 mg compresse orodispersibili DOMES 100 mg granulato per sospensione orale nimesulide Medicinale Equivalente Legga attentamente questo foglio illustrativo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Carbocisteina g 5 Eccipienti con effetti noti: metile
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Carbocisteina g 5 Eccipienti con effetti noti: metile
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia
 Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIDO-HYAL A 25 U.I. e LIDO-HYAL B 175 U.I. soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA IN PRINCIPI ATTIVI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIDO-HYAL A 25 U.I. e LIDO-HYAL B 175 U.I. soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA IN PRINCIPI ATTIVI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Riassunto delle caratteristiche del prodotto NIMESULIDE 100 mg compresse o 100 mg granulato per sospensione o 200 mg supposte
 Riassunto delle caratteristiche del prodotto NIMESULIDE 100 mg compresse o 100 mg granulato per sospensione o 200 mg supposte ALLEGATO 1 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Trattamento
Riassunto delle caratteristiche del prodotto NIMESULIDE 100 mg compresse o 100 mg granulato per sospensione o 200 mg supposte ALLEGATO 1 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Trattamento
FOGLIETTO ILLUSTRATIVO PER:
 FOGLIETTO ILLUSTRATIVO PER: TOLFEDINE, 40 mg/ml soluzione iniettabile per cani e gatti. TOLFEDINE, 60 mg compresse per cani. TOLFEDINE, 6 mg compresse per gatti e cani di piccola taglia. 1. NOME E INDIRIZZO
FOGLIETTO ILLUSTRATIVO PER: TOLFEDINE, 40 mg/ml soluzione iniettabile per cani e gatti. TOLFEDINE, 60 mg compresse per cani. TOLFEDINE, 6 mg compresse per gatti e cani di piccola taglia. 1. NOME E INDIRIZZO
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. IBUPAS 136 mg cerotto medicato Ibuprofene
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE IBUPAS 136 mg cerotto medicato Ibuprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE IBUPAS 136 mg cerotto medicato Ibuprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
Foglio illustrativo: informazioni per l utilizzatore VEGETALLUMINA Antidolore 10% gel Ibuprofene sale di lisina
 Pagina 1 di 4 Foglio illustrativo: informazioni per l utilizzatore VEGETALLUMINA Antidolore 10% gel Ibuprofene sale di lisina Legga attentamente questo foglio prima di prendere questo medicinale perchè
Pagina 1 di 4 Foglio illustrativo: informazioni per l utilizzatore VEGETALLUMINA Antidolore 10% gel Ibuprofene sale di lisina Legga attentamente questo foglio prima di prendere questo medicinale perchè
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Maggio 2013 Nuove importanti restrizioni all uso di Protelos/Osseor (ranelato di
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Maggio 2013 Nuove importanti restrizioni all uso di Protelos/Osseor (ranelato di
LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG
 IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG Marchio: Johnson e Johnson Codice Min.: 023673066 Link: clicca qui per acquistare IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG CATEGORIA FARMACOTERAPEUTICA: Antipropulsivi.
IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG Marchio: Johnson e Johnson Codice Min.: 023673066 Link: clicca qui per acquistare IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG CATEGORIA FARMACOTERAPEUTICA: Antipropulsivi.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 (Foglietto illustrativo) PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi
(Foglietto illustrativo) PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FOGLIO ILLUSTRATIVO. QUANDO NON DEVE ESSERE USATO Ipersensibilità al principio attivo o a uno qualsiasi degli eccipienti
 FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE, che potete usare per curare disturbi lievi e
FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE, che potete usare per curare disturbi lievi e
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Nimesulide. Medicinale equivalente
 Foglio illustrativo: informazione per l utilizzatore LEDOREN 100 mg Compresse LEDOREN 100 mg Granulato per sospensione orale Nimesulide Medicinale equivalente Legga attentamente questo foglio prima di
Foglio illustrativo: informazione per l utilizzatore LEDOREN 100 mg Compresse LEDOREN 100 mg Granulato per sospensione orale Nimesulide Medicinale equivalente Legga attentamente questo foglio prima di
FOGLIO ILLUSTRATIVO confezione 50 compresse. Sodio bicarbonato Sella 500 mg compresse. CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato
 FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE: INTRAFER 50 mg/ml gocce orali, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene: principio attivo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE: INTRAFER 50 mg/ml gocce orali, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene: principio attivo
Foglio illustrativo: informazioni per il paziente. ALGOFEN 200 mg compresse rivestite. Ibuprofene
 Foglio illustrativo: informazioni per il paziente ALGOFEN 200 mg compresse rivestite Ibuprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente ALGOFEN 200 mg compresse rivestite Ibuprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Trattamento farmacologico dell ulcera gastro-duodenale L. 29
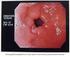 Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
Per l elenco completo degli eccipienti, vedere paragrafo 6.1.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Cetirizina Germed 10 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 10 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Cetirizina Germed 10 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 10 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ECOMESOL 1% crema vaginale ECOMESOL 50 mg ovuli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ECOMESOL 1% crema vaginale: 100 g
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ECOMESOL 1% crema vaginale ECOMESOL 50 mg ovuli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ECOMESOL 1% crema vaginale: 100 g
Foglio illustrativo: informazioni per l utilizzatore. Lasonil antidolore 10% gel Ibuprofene sale di lisina
 Foglio illustrativo: informazioni per l utilizzatore Lasonil antidolore 10% gel Ibuprofene sale di lisina Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per l utilizzatore Lasonil antidolore 10% gel Ibuprofene sale di lisina Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente. NEO BOROCILLINA GOLA DOLORE 0,25% collutorio flurbiprofene
 Foglio illustrativo: informazioni per il paziente NEO BOROCILLINA GOLA DOLORE 0,25% collutorio flurbiprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per il paziente NEO BOROCILLINA GOLA DOLORE 0,25% collutorio flurbiprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
Foglio illustrativo. LOPERAMIDE ANGENERICO 2mg capsule rigide. Loperamide. Medicinale Equivalente
 Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Itamifast 25 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 25 mg di diclofenac
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Itamifast 25 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 25 mg di diclofenac
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose
 GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE METFORMINA RATIOPHARM ITALIA 850 mg compresse rivestite con film METFORMINA RATIOPHARM ITALIA 1000 mg compresse rivestite con
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE METFORMINA RATIOPHARM ITALIA 850 mg compresse rivestite con film METFORMINA RATIOPHARM ITALIA 1000 mg compresse rivestite con
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
NOXON. 3) FORMA FARMACEUTICA: Polvere e solvente per soluzione iniettabile (uso intramuscolare ed endovenoso).
 NOXON RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1) DENOMINAZIONE DELLA SPECIALITA': ------------------------------ NOXON 8 mg Polvere e solvente per soluzione iniettabile. 2) COMPOSIZIONE QUALI-QUANTITATIVA:
NOXON RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1) DENOMINAZIONE DELLA SPECIALITA': ------------------------------ NOXON 8 mg Polvere e solvente per soluzione iniettabile. 2) COMPOSIZIONE QUALI-QUANTITATIVA:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fosfomicina ratiopharm Adulti 3 g granulato per soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una bustina di Fosfomicina
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fosfomicina ratiopharm Adulti 3 g granulato per soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una bustina di Fosfomicina
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FELDENE CREMADOL 1% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 grammi di crema contengono Principio attivo: Piroxicam
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FELDENE CREMADOL 1% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 grammi di crema contengono Principio attivo: Piroxicam
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE: Vitamina C Pfizer 500 mg/5 ml soluzione iniettabile Vitamina C Pfizer 1000 mg/5 ml soluzione iniettabile 2. COMPOSIZIONE
1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE: Vitamina C Pfizer 500 mg/5 ml soluzione iniettabile Vitamina C Pfizer 1000 mg/5 ml soluzione iniettabile 2. COMPOSIZIONE
Foglio illustrativo: informazioni per il paziente. Neo-Cibalgina compresse
 Foglio illustrativo: informazioni per il paziente Neo-Cibalgina compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei. Prenda questo
Foglio illustrativo: informazioni per il paziente Neo-Cibalgina compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei. Prenda questo
Foglio illustrativo: informazioni per il paziente. ACIDO ACETILSALICILICO ANGELINI 500 mg compresse
 Foglio illustrativo: informazioni per il paziente ACIDO ACETILSALICILICO ANGELINI 500 mg compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente ACIDO ACETILSALICILICO ANGELINI 500 mg compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
1.0 DENOMINAZIONE DEL MEDICINALE 2.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 3.0 FORMA FARMACEUTICA
 1.0 DENOMINAZIONE DEL MEDICINALE METBAY 500MG 2.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Metbay 500 mg compresse Ogni compressa contiene: Principio attivo: metformina cloridrato 500 mg, pari a 390 mg
1.0 DENOMINAZIONE DEL MEDICINALE METBAY 500MG 2.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Metbay 500 mg compresse Ogni compressa contiene: Principio attivo: metformina cloridrato 500 mg, pari a 390 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BENFER 50 mg/ml gocce orali, soluzione Soluzione orale da somministrarsi in gocce, contenente complesso di ferro polimaltosato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BENFER 50 mg/ml gocce orali, soluzione Soluzione orale da somministrarsi in gocce, contenente complesso di ferro polimaltosato
Eccipienti con effetti noti: saccarosio, sorbitolo, metile para-idrossibenzoato e propile
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LISOMUCIL TOSSE SEDATIVO 15 mg / 5 ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml contengono: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LISOMUCIL TOSSE SEDATIVO 15 mg / 5 ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml contengono: Principio attivo:
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
Foglio illustrativo: informazioni per il paziente. CEFIXIMA EUROGENERICI 400 mg compresse dispersibili. Medicinale equivalente
 Foglio illustrativo: informazioni per il paziente CEFIXIMA EUROGENERICI 400 mg compresse dispersibili Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente CEFIXIMA EUROGENERICI 400 mg compresse dispersibili Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
IBUPROFENE CARLO ERBA 200 mg compresse rivestite con film (Ibuprofene sale di lisina)
 Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e transitori, facilmente riconoscibili e risolvibili senza ricorrere all aiuto del medico. Può essere, quindi, acquistato
Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e transitori, facilmente riconoscibili e risolvibili senza ricorrere all aiuto del medico. Può essere, quindi, acquistato
Foglio Illustrativo. KETOROLAC ACTAVIS 30 mg/ml soluzione iniettabile Ketorolac trometamina
 Foglio Illustrativo KETOROLAC ACTAVIS 30 mg/ml soluzione iniettabile Ketorolac trometamina CATEGORIA FARMACO-TERAPEUTICA Farmaci antireumatici/antinfiammatori non steroidei. INDICAZIONI TERAPEUTICHE Ketorolac
Foglio Illustrativo KETOROLAC ACTAVIS 30 mg/ml soluzione iniettabile Ketorolac trometamina CATEGORIA FARMACO-TERAPEUTICA Farmaci antireumatici/antinfiammatori non steroidei. INDICAZIONI TERAPEUTICHE Ketorolac
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 .1. RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LEVIORINIL 10 mg Compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa rivestita con film
.1. RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LEVIORINIL 10 mg Compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa rivestita con film
4.3 Controindicazioni Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1.
 1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
Che cos è Flector EP granulare e quando si usa?
 Flector EP Granulare Che cos è Flector EP granulare e quando si usa? Flector EP granulare contiene il sale epolamina del diclofenac, un antiinfiammatorio non steroideo, che allevia efficacemente il dolore
Flector EP Granulare Che cos è Flector EP granulare e quando si usa? Flector EP granulare contiene il sale epolamina del diclofenac, un antiinfiammatorio non steroideo, che allevia efficacemente il dolore
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
La nimesulide è un farmaco antinfiammatorio
 112 Nimesulide ed epatotossicità Background La nimesulide è un farmaco antinfiammatorio non steroideo indicato per il trattamento del dolore acuto, della dismenorrea primaria e per il trattamento sintomatico
112 Nimesulide ed epatotossicità Background La nimesulide è un farmaco antinfiammatorio non steroideo indicato per il trattamento del dolore acuto, della dismenorrea primaria e per il trattamento sintomatico
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 .1. RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LEVIORINIL 10 mg/ml gocce orali, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene 10 mg di
.1. RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LEVIORINIL 10 mg/ml gocce orali, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di soluzione contiene 10 mg di
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente COLECALCIFEROLO EG 25.000 U.I./2,5 ml soluzione orale Colecalciferolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Foglio illustrativo: informazioni per il paziente COLECALCIFEROLO EG 25.000 U.I./2,5 ml soluzione orale Colecalciferolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
Allegato III. Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo
 Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
FOGLIO ILLUSTRATIVO. Voltaren Ofta 0,1% collirio, soluzione diclofenac sodico. Categoria farmacoterapeutica Oftalmologico, antiinfiammatorio.
 FOGLIO ILLUSTRATIVO Voltaren Ofta 0,1% collirio, soluzione diclofenac sodico Categoria farmacoterapeutica Oftalmologico, antiinfiammatorio. Indicazioni terapeutiche Stati infiammatori eventualmente dolorosi
FOGLIO ILLUSTRATIVO Voltaren Ofta 0,1% collirio, soluzione diclofenac sodico Categoria farmacoterapeutica Oftalmologico, antiinfiammatorio. Indicazioni terapeutiche Stati infiammatori eventualmente dolorosi
3. INDICAZIONE DEL(I) PRINCIPIO(I) ATTIVO(I) E DEGLI ALTRI INGREDIENTI
 FOGLIETTO ILLUSTRATIVO PER: Onsior 5 mg compresse per cani Onsior 10 mg compresse per cani Onsior 20 mg compresse per cani Onsior 40 mg compresse per cani 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO PER: Onsior 5 mg compresse per cani Onsior 10 mg compresse per cani Onsior 20 mg compresse per cani Onsior 40 mg compresse per cani 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BRONCHENOLO TOSSE 1,54 mg/ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BRONCHENOLO TOSSE 1,54 mg/ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA MEDICINALE NEPITUSS 1g/100ml gocce NEPITUSS 0,1g/100ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Gocce (flacone
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA MEDICINALE NEPITUSS 1g/100ml gocce NEPITUSS 0,1g/100ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Gocce (flacone
DENOMINAZIONE DEL MEDICINALE. Danka 30 mg/5 ml sciroppo Levodropropizina. CHE COSA E Sedativo della tosse.
 PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
Alfasigma S.p.A. DICLOREUM dolore granulato Pagina 1
 Alfasigma S.p.A. DICLOREUM dolore granulato Pagina 1 USO ORALE Ogni bustina contiene 32,5 mg di diclofenac idrossietilpirrolidina (pari a Diclofenac sodico 25 mg). Contiene aspartame, sorbitolo. Per ulteriori
Alfasigma S.p.A. DICLOREUM dolore granulato Pagina 1 USO ORALE Ogni bustina contiene 32,5 mg di diclofenac idrossietilpirrolidina (pari a Diclofenac sodico 25 mg). Contiene aspartame, sorbitolo. Per ulteriori
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Foglio illustrativo: informazioni per il paziente Ibuprofene E-Pharma Trento 400 mg granulato per soluzione orale ibuprofene
 Foglio illustrativo: informazioni per il paziente Ibuprofene E-Pharma Trento 400 mg granulato per soluzione orale ibuprofene Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente Ibuprofene E-Pharma Trento 400 mg granulato per soluzione orale ibuprofene Legga attentamente questo foglio prima di prendere questo medicinale perché
CHE COSA E FLUIBRON TOSSE SECCA 30 mg/5 ml sciroppo è un farmaco sedativo della tosse.
 PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
Aleve 220 mg compresse rivestite con film
 PRIMA DELL'USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e transitori facilmente
PRIMA DELL'USO LEGGETE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e transitori facilmente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DEI MEDICINALI CONTENENTI PIROXICAM
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DEI MEDICINALI CONTENENTI PIROXICAM 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 3. FORMA FARMACEUTICA 4. INFORMAZIONI CLINICHE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DEI MEDICINALI CONTENENTI PIROXICAM 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 3. FORMA FARMACEUTICA 4. INFORMAZIONI CLINICHE
RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIBRADIN 10 mg capsule a rilascio modificato LIBRADIN 20 mg capsule a rilascio modificato 2. COMPOSIZIONEQUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIBRADIN 10 mg capsule a rilascio modificato LIBRADIN 20 mg capsule a rilascio modificato 2. COMPOSIZIONEQUALITATIVA E QUANTITATIVA
Acido ascorbico Medicinale equivalente
 Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE IBUPROFENE DOC Generici 600 mg granulato effervescente. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni bustina contiene 600
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE IBUPROFENE DOC Generici 600 mg granulato effervescente. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni bustina contiene 600
Foglio illustrativo: informazioni per il paziente. CORYFIN GOLA DOLORE 2,5 mg/ml collutorio. Flurbiprofene
 Foglio illustrativo: informazioni per il paziente CORYFIN GOLA DOLORE 2,5 mg/ml collutorio Flurbiprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente CORYFIN GOLA DOLORE 2,5 mg/ml collutorio Flurbiprofene Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
