Riassunto delle caratteristiche del prodotto
|
|
|
- Gerardina Rocca
- 7 anni fa
- Visualizzazioni
Transcript
1 Pagina 1 di 9 Riassunto delle caratteristiche del prodotto 1. Denominazione del medicinale Rabeprazolo Zentiva 10 mg compresse gastroresistenti Rabeprazolo Zentiva 20 mg compresse gastroresistenti 2. Composizione qualitativa e quantitativa Ogni compressa gastroresistente contiene 10 mg di rabeprazolo sodico (come anidro o monoidrato) equivalente a 9,42 mg di rabeprazolo. Ogni compressa gastroresistente contiene 20 mg di rabeprazolo sodico (come anidro o monoidrato) equivalente a 18,85 mg di rabeprazolo. Per l elenco completo degli eccipienti vedere paragrafo Forma farmaceutica Compressa gastroresistente. Rabeprazolo Zentiva 10 mg compresse: compressa rivestita con film di colore rosa, rotonda, biconvessa con un diametro di circa 5,5 mm Rabeprazolo Zentiva 20 mg compresse: compressa rivestita con film di colore giallo, rotonda, biconvessa con un diametro di circa 7 mm 4. Informazioni cliniche 4.1 Indicazioni terapeutiche Rabeprazolo Zentiva compresse gastroresistenti è indicato per il trattamento di: - Ulcera duodenale attiva, - Ulcera gastrica benigna attiva, - Malattia da reflusso gastroesofageo (MRGE) sintomatica erosiva o ulcerativa, - Terapia a lungo termine della malattia da reflusso gastroesofageo (terapia di mantenimento della MRGE), - Trattamento sintomatico della malattia da reflusso gastroesofageo di grado da moderato a molto grave (MRGE sintomatica), - Sindrome di Zollinger-Ellison, - In associazione a un appropriato regime terapeutico antibatterico per l eradicazione dell Helicobacter pylori in pazienti con ulcera peptica. Vedere paragrafo Posologia e modo di somministrazione Posologia Adulti/pazienti anziani: Ulcera duodenale attiva e Ulcera gastrica benigna attiva: la dose orale raccomandata per entrambe, ulcera duodenale attiva e ulcera gastrica benigna attiva, è di 20 mg da prendere una volta al giorno al mattino. Nella maggioranza dei pazienti con ulcera duodenale attiva la cicatrizzazione avviene entro 4 settimane. Tuttavia alcuni pazienti possono richiedere una terapia addizionale di altre 4 settimane per ottenere la cicatrizzazione. Nella maggioranza dei pazienti con ulcera gastrica benigna attiva la cicatrizzazione avviene entro 6 settimane. Tuttavia, alcuni pazienti possono richiedere un trattamento addizionale di 6 settimane di terapia per ottenere la cicatrizzazione. Malattia da reflusso gastroesofageo di tipo erosivo o ulcerativo (MRGE): la dose orale raccomandata per questa condizione è di 20 mg da prendere una volta al giorno per quattro o otto settimane. Terapia a lungo termine della malattia da reflusso gastroesofageo (terapia di mantenimento della MRGE). Per la terapia a lungo termine, la dose di mantenimento di rabeprazolo sodico è di 20 mg o 10 mg una volta al giorno a seconda della risposta del paziente.
2 Pagina 2 di 9 Trattamento sintomatico della malattia da reflusso gastroesofageo di grado da moderato a molto grave (MRGE sintomatica): 10 mg una volta al giorno in pazienti senza esofagite. Se non si ottiene il controllo dei sintomi entro 4 settimane, il paziente deve essere sottoposto ad ulteriori accertamenti. Una volta risolta la sintomatologia, il successivo controllo dei sintomi può essere ottenuto adottando un regime di assunzione di 10 mg una volta al giorno al bisogno. Sindrome di Zollinger-Ellison: Negli adulti, la dose orale iniziale raccomandata è di 60 mg una volta al giorno. La dose può essere aumentata fino a raggiungere 120 mg/giorno in base al bisogno del singolo paziente. Possono essere somministrate dosi singole giornaliere fino a 100 mg/ giorno. La dose da 120 mg può essere suddivisa in 60 mg due volte al giorno. II trattamento deve proseguire sino a quando clinicamente indicato. Eradicazione dell Helicobacter pylori: pazienti con infezioni da Helicobacter pylori devono essere trattati con la terapia per l eradicazione. E raccomandata la seguente associazione per 7 giorni: Rabeprazolo sodico 20 mg due volte al giorno + claritromicina 500 mg due volte al giorno + amoxicillina 1 g due volte al giorno. Popolazioni speciali Pazienti con compromissione epatica e renale Non è necessario un aggiustamento del dosaggio per pazienti con compromissione della funzionalità renale o epatica. Vedere paragrafo 4.4 Avvertenze speciali e precauzioni di impiego di Rabeprazolo Zentiva nel trattamento di pazienti con grave compromissione della funzionalità epatica. Popolazione pediatrica: L uso di Rabeprazolo Zentiva non è raccomandato nei bambini, dato che non c è esperienza dell uso del medicinale in questo gruppo di pazienti. Modo di somministrazione Per le indicazioni che richiedono il trattamento una volta al giorno, le compresse di rabeprazolo sodico devono essere ingerite al mattino, prima di mangiare; sebbene non siano state evidenziate interferenze sull'attività del rabeprazolo sodico da parte del cibo o del momento della giornata in cui viene assunto il medicinale, questo schema facilita la compliance del paziente al trattamento. I pazienti devono essere avvisati di non masticare o frantumare le compresse gastroresistenti di Rabeprazolo Zentiva ma di inghiottirle intere. 4.3 Controindicazioni Ipersensibilità al principio attivo o a uno qualunque degli eccipienti elencati nel paragrafo 6.1. Rabeprazolo Zentiva è controindicato in gravidanza e durante l allattamento al seno. 4.4 Speciali avvertenze e precauzioni di impiego La risposta sintomatica alla terapia con Rabeprazolo Zentiva non esclude la presenza di patologie maligne a livello gastrico o esofageo; tale possibilità deve, quindi, essere esclusa prima di iniziare il trattamento con Rabeprazolo Zentiva. l pazienti in terapia a lungo termine (in particolare quelli trattati per più di un anno) devono essere tenuti sotto regolare osservazione. Gli inibitori di pompa protonica (PPI), specialmente se utilizzati a dosaggi elevati e per periodi prolungati (> 1 anno), potrebbero causare un lieve aumento di rischio di fratture dell'anca, del polso e della colonna vertebrale, soprattutto in pazienti anziani o in presenza di altri fattori di rischio conosciuti. Studi osservazionali suggeriscono che gli PPI potrebbero aumentare il rischio complessivo di frattura dal 10% al 40%. Tale aumento potrebbe essere in parte dovuto ad altri fattori di rischio. I pazienti a rischio di osteoporosi devono ricevere le cure in base alte attuali linee guida di pratica clinica e devono assumere un'adeguata quantità di vitamina D e calcio Il rischio di ipersensibilità crociata con altri PPI o benzoimidazolici sostituiti non può essere escluso.
3 Pagina 3 di 9 I pazienti devono essere avvertiti di non masticare o frantumare le compresse gastroresistenti di Rabeprazolo Zentiva, ma di inghiottirle intere. Rabeprazolo Zentiva non è raccomandato per l uso in bambini, dato che non c è esperienza nell uso del medicinale in questo gruppo di pazienti. Sono state riportate segnalazioni post-marketing di discrasia ematica (trombocitopenia e neutropenia). Nella maggior parte dei casi in cui non si è potuta identificare un'eziologia alternativa, gli eventi non hanno avuto complicazioni e si sono risolti con la sospensione del rabeprazolo. Anormalità degli enzimi epatici sono state osservate durante gli studi clinici e sono state riportate anche dopo l inizio della commercializzazione. Nella maggior parte dei casi in cui non si è potuta identificare un'eziologia alternativa, gli eventi non hanno avuto complicazioni e si sono risolti con la sospensione del rabeprazolo. Uno studio in pazienti con compromissione della funzionalità epatica da lieve a moderata non ha evidenziato significativi problemi di sicurezza correlabili all'uso del medicinale differenti da quelli osservati nei pazienti del gruppo di controllo, analogo per età e sesso. Comunque, dal momento che non vi sono dati clinici sull'uso di Rabeprazolo Zentiva nel trattamento di pazienti con gravi disfunzioni epatiche, il medico deve prestare particolare attenzione nel somministrare Rabeprazolo Zentiva per la prima volta a tali pazienti. La co-somministrazione di atazanavir con Rabeprazolo Zentiva non è raccomandata (vedere paragrafo 4.5). Il trattamento con PPI, incluso il rabeprazolo, può aumentare il rischio di infezioni gastrointestinali come da Salmonella, Campylobacter e Clostridium difficile (vedere paragrafo 5.1) Ipomagnesiemia E stato osservato che gli inibitori di pompa protonica come lansoprazolo, in pazienti trattati per almeno tre mesi e in molti casi per un anno, possono causare grave ipomagnesiemia. Gravi sintomi di ipomagnesiemia includono stanchezza, tetania, delirio, convulsioni, vertigini e aritmia ventricolare. Essi, inizialmente, si possono manifestare in modo insidioso ed essere trascurati. L ipomagnesiemia, nella maggiore parte dei pazienti, migliora dopo l assunzione di magnesio e la sospensione dell inibitore di pompa protonica. Gli operatori sanitari devono considerare l eventuale misurazione dei livelli di magnesio all inizio e periodicamente nei pazienti in trattamento con PPI per un periodo prolungato o in terapia con digossina o medicinali che possono causare ipomagnesiemia (ad esempio diuretici). 4.5 Interazioni con altri medicinali ed altre forme di interazione Rabeprazolo sodico produce un intensa e duratura inibizione della secrezione acida gastrica. E possibile che vi sia interazione con i composti il cui assorbimento è ph dipendente. La co-somministrazione di rabeprazolo sodico con ketoconazolo o itraconazolo può portare ad una significativa diminuzione dei livelli plasmatici dell antifungineo. Quindi per alcuni pazienti può essere necessario il monitoraggio al fine di determinare se è necessario un aggiustamento del dosaggio quando ketoconazolo o itraconazolo sono assunti in concomitanza con Rabeprazolo Zentiva. Negli studi clinici, gli antiacidi sono stati usati in concomitanza con la somministrazione di rabeprazolo sodico e, in specifici studi di interazione farmaco-farmaco, non sono state osservate interazioni con antiacidi liquidi. La co-somministrazione di atazanavir 300 mg/ritonavir 10 mg con omeprazolo (40 mg una volta al giorno) o atazanavir 400 mg con lansoprazolo (60 mg una volta al giorno) a volontari sani ha avuto come risultato una sostanziale riduzione dell esposizione ad atazanavir. L assorbimento di atazanavir è ph dipendente. Anche se non sono stati studiati, sono attesi risultati simili con altri PPI. Quindi gli IPP, incluso rabeprazolo, non devono essere co-somministrati con atazanavir (vedere paragrafo 4.4). 4.6 Gravidanza e allattamento Gravidanza: Non ci sono dati sulla sicurezza di rabeprazolo sodico nella gravidanza umana. Studi sulla riproduzione condotti su ratti e conigli non hanno evidenziato effetti dannosi sulla fertilità o danni ai feti causati da rabeprazolo sodico, sebbene in basse quantità attraversa la barriera feto-placentare nel ratto. Rabeprazolo Zentiva è controindicato durante la gravidanza. Allattamento: Non è noto se rabeprazolo sodico sia escreto nel latte materno. Non sono stati condotti studi su donne che allattano. Rabeprazolo sodico è tuttavia escreto nella secrezione mammaria nel ratto. Quindi Rabeprazolo Zentiva non deve essere usato durante l allattamento al seno.
4 Pagina 4 di Effetti sulla capacità di guidare veicoli e sull uso di macchinari Sulla base delle proprietà farmacodinamiche e il profilo degli eventi avversi è improbabile che rabeprazolo sodico possa causare alterazioni della capacità di guidare o compromettere la capacità di usare macchinari. Se, tuttavia, la vigilanza è compromessa a causa della sonnolenza, si raccomanda di evitare di guidare o operare macchinari complessi. 4.8 Effetti indesiderati Le più comuni reazioni avverse da farmaco riportate durante studi clinici controllati sono stati cefalea, diarrea, dolori addominali, astenia, flatulenza, eruzione e bocca secca. La maggior parte degli eventi avversi riscontrati durante gli studi clinici erano da lievi a moderati e di natura transitoria. I seguenti eventi avversi sono stati riportati da studi clinici e dall esperienza post commercializzazione. Le frequenze sono definite come: comune (>1/100, < 1/10), non comune (>1/1000, < 1/100), raro (> 1/10.000, <1/1000), molto raro (< 1/10.000), non nota (la frequenza non può essere definita sulla base dei dati disponibili). COMUNE NON COMUNE RARO MOLTO RARO NON NOTA Infezioni ed infestazioni Patologie del sistema emolinfopoietico Disturbi del sistema immunitario Disturbi del metabolismo e della nutrizione infezioni Neutropenia Leucopenia Trombocitopenia Leucocitosi Ipersensibilità 1,2 Anoressia Iponatriemia Ipomagnesiemia (vedere 4.4) Disturbi psichiatrici Insonnia Nervosismo Depressione Confusione Patologie del sistema Cefalea Sonnolenza nervoso Capogiri Patologie dell'occhio Disturbi visivi Patologie vascolari Edema periferico Patologie respiratorie, toraciche e mediastiniche Patologie gastrointestinali Patologie epatobiliari Tosse Faringiti Riniti Diarrea Vomito Nausea Dolori addominali Costipazione Flatulenza Bronchiti Sinusiti Dispnea Bocca secca Eruttazione Gastriti Stomatiti Alterazioni del gusto Epatiti Ittero Encefalopatia epatica 3 Patologie della cute e del tessuto sottocutaneo Patologie del sistema muscoloscheletrico e del tessuto connettivo Dolore non specifico, Dolore alla schiena Rush Eritema 2 Mialgia Crampi muscolari Artralgia frattura dell'anca, del polso o della Prurito Sudorazione Reazioni bollose 2 Eritema multiforme, Necrolisi epidermica tossica (NET), sindrome di Stevens- Johnson (SSJ)
5 Pagina 5 di 9 Patologie renali e urinarie Patologie dell'apparato riproduttivo e della mammella Patologie sistemiche e condizioni relative alla sede di somministrazione Astenia Sindrome simil influenzale colonna vertebrale (vedere paragrafo 4,4) Infezioni del tratto urinario Dolore al petto Brividi Piressia Esami diagnostici Aumento degli enzimi epatici 3 1 Inclusi gonfiore del viso, ipotensione e dispnea Nefriti interstiziali Aumento di peso Ginecomastia 2 Eritema, reazioni bollose e reazioni di ipersensibilità risolte di solito dopo la sospensione della terapia 3 Rari casi di encefalopatia epatica sono stati segnalati in pazienti con cirrosi in corso. Nel trattamento di pazienti con grave disfunzione epatica il medico è avvisato di prestare cautela quando il trattamento con rabeprazolo sodico viene iniziato per la prima volta in questi pazienti (vedere paragrafo 4.4). Segnalazione delle reazioni avverse sospette. La segnalazione delle reazioni avverse sospette che si verificano dopo l autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all indirizzo Sovradosaggio I dati sull esperienza di sovradosaggio intenzionale o accidentale sono limitati. La massima esposizione stabilita non è stata superiore a 60 mg due volte al giorno, o 160 mg una volta al giorno. Gli effetti sono solitamente minimi e rispecchiano il profilo degli eventi avversi noti, reversibili senza necessità di alcun intervento medico ulteriore. Non si conosce uno specifico antidoto. Rabeprazolo sodico si lega ampiamente alle proteine e quindi non è dializzabile. Come in qualunque caso di sovradosaggio, il trattamento deve essere sintomatico e devono essere intraprese misure di supporto. 5. Proprietà farmacologiche 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: apparato gastrointestinale e metabolismo, farmaci per l ulcera peptica e malattia da reflusso gastroesofageo (MRGE), inibitori di pompa protonica. Codice ATC: A02B C 04 Meccanismo d azione: Rabeprazolo sodico appartiene alla classe dei composti antisecretori, derivati benzoimidazolici che non presentano proprietà anticolinergiche o antagoniste dei recettori H 2 istaminergici, ma sopprimono la secrezione acida per inibizione dell enzima H+/K+ - ATPasi (pompa protonica o acida). L effetto è dose correlato e conduce all inibizione della secrezione acida sia basale che stimolata indipendentemente dagli stimoli. Studi sugli animali indicano che dopo somministrazione rabeprazolo sodico scompare rapidamente dal plasma e dalla mucosa gastrica. Essendo una base debole, il rabeprazolo viene rapidamente assorbito a tutti i dosaggi e si concentra nell ambiente acido delle cellule parietali. Rabeprazolo sodico è trasformato nella forma sulfenamide attiva attraverso la protonazione e reagisce di conseguenza con la cisteina presente sulla pompa protonica. Attività antisecretoria Dopo somministrazione orale di una dose di 20 mg di rabeprazolo sodico la comparsa dell'effetto antisecretorio si manifesta entro 1 ora, mentre l'effetto massimo è evidente entro 2-4 ore. L'inibizione della secrezione acida, sia basale che stimolata dal cibo, 23 ore dopo la somministrazione della prima dose di rabeprazolo sodico è pari a 69% ed 82%, rispettivamente, e l'inibizione si protrae fino a 48 ore, L'effetto inibitorio del rabeprazolo sodico sulla secrezione acida aumenta leggermente con somministrazioni giornaliere ripetute, raggiungendo lo steady-state dell'inibizione dopo 3 giorni. Quando le somministrazioni vengono interrotte, l'attività secretoria si normalizza entro 2-3 giorni.
6 Pagina 6 di 9 La diminuzione dell acidità gastrica dovuta a varie cause, inclusi PPI come rabeprazolo, aumenta la conta dei batteri normalmente presenti nel tratto gastrointestinale. Il trattamento con PPI può verosimilmente aumentare il rischio di infezioni gastrointestinali come Salmonella, Cambylobacter e Clostridium difficile. Effetti sulla gastrina serica: Negli studi clinici i pazienti sono stati trattati con rabeprazolo sodico 10 o 20 mg una volta al giomo sino a una durata di 43 mesi. I livelli di gastrina nel siero sono aumentati durante le prime 2-8 settimane, riflettendo gli effetti inibitori sulla secrezione acida e sono rimasti poi stabili per la durata della terapia. Alla sospensione della terapia i valori della gastrina sono poi tornati ai livelli pre-trattamento, normalmente entro 1-2 settimane. I campioni bioptici umani prelevati dall'antro e dal fundus dello stomaco di oltre 500 pazienti trattati con rabeprazolo sodico o farmaco di confronto fino a 8 settimane, non hanno messo in evidenza modifiche nell'istologia delle cellule ECL., nella gravità della gastrite, nell'incidenza della gastrite atrofica, della metaplasia intestinale o della distribuzione dell'infezione da H. pylori. In oltre 250 pazienti monitorati per 36 mesi di terapia continua, non sono state osservate variazioni significative nei parametri controllati prima e dopo il trattamento. Altri effetti: Finora non sono stati rilevati effetti sistemici del rabeprazolo sodico sul SNC e sui sistemi cardiovascolare e respiratorio. Il rabeprazolo sodico, somministrato alla dose orale di 20 mg per 2 settimane, non ha causato alcun effetto sulla funzionalità tiroidea, sul metabolismo dei carboidrati, sui livelli in circolo di ormone paratiroideo, cortisolo, estrogeni, testosterone, prolattina, colecistochinina, secretina, glucagone, ormone follicolo-stimolante (FSH), ormone luteinlzzante (LH), renina, aldosterone o di ormone somatotropo. Studi in soggetti sani hanno dimostrato che rabeprazolo sodico non ha interazioni clinicamente significative con amoxicillina. Rabeprazolo non influenza negativamente le concentrazioni plasmatiche di amoxicillina e claritromicina durante la somministrazione concomitante nell'eradicazione dell infezione da H. pylori dal tratto gastrointestinale superiore. 5.2 Proprietà farmacocinetiche Assorbimento: Le compresse sono formulate con un rivestimento enterico (gastroresistenti). Questa presentazione è necessaria in quanto il rabeprazolo è acido-labile. Quindi l assorbimento del rabeprazolo inizia dopo che le compresse hanno lasciato lo stomaco. L assorbimento è rapido con un picco plasmatico di concentrazione dopo 3,5 ore dopo una dose di 20 mg. Il picco di concentrazione plasmatica (Cmax) di rabeprazolo e l AUC hanno una cinetica lineare nell intervallo 10 mg - 40 mg. La biodisponibilità assoluta di una dose orale di 20 mg (confrontata con la somministrazione endovenosa) è di circa 52% dovuto nella gran parte dal metabolismo pre-sistemico. In aggiunta la biodisponibilità non aumenta con somministrazioni ripetute. Nei soggetti sani l emivita plasmatica è approssimativamente di 1 ora (intervallo 0,7-1,5 ore) e la clearance totale si stima essere di 283± 98 ml/min. Non vi è un interazione clinicamente rilevante con il cibo. Né il cibo, né l ora della somministrazione del trattamento hanno influenza sull assorbimento di rabeprazolo sodico. Distribuzione: Rrabeprazolo si lega alle proteine plasmatiche approssimativamente per il 97%. Biotrasformazione: Rabeprazolo sodico, come altri medicinali della classe degli PPI, è metabolizzato attraverso il sistema metabolizzante epatico del citocromo P450 (CYP450). Studi in vitro con microsomi epatici umani indicano che il rabeprazolo sodico è metabolizzato dagli isoenzimi del CYP450 (CYP2C19 e CYP3A4). In questi studi, alle concentrazioni plasmatiche previste nell uomo, il rabeprazolo non ha effetti inducenti o inibenti sul CYP3A4; sebbene gli studi in vitro possano non essere sempre predittivi della situazione in vivo, queste evidenze indicano che non è attesa un interazione tra rabeprazolo e ciclosporina. Nell'uomo il tioetere (M1) e l'acido carbossilico (M6) sono i maggiori metaboliti plasmatici. Il sulfone (M2), il desmetiltioetere (M4) e il coniugato con l' acido mercapturico (M5) sono metaboliti minori presenti a bassi livelli. Solo il metabolita desmetil (M3) ha una lieve attività antisecretoria, ma non è presente nel plasma. Eliminazione Dopo una dose orale singola da 20 mg di rabeprazolo sodico marcato con 14 C non è presente farmaco immodificato nelle urine. Circa il 90% della dose viene eliminata nelle urine, principalmente sotto forma di 2 metaboliti, un prodotto di coniugazione con l'acido mercapturico (M5) ed un acido carbossilico (M6), più due metaboliti non identificati. La parte rimanente della dose somministrata viene recuperata nelle feci. Caratteristiche in pazienti/gruppo speciale di soggetti
7 Pagina 7 di 9 Sesso: Non ci sono differenze imputabili al sesso nei parametri farmacocinetici, quando rapportati alla massa corporea ed all'altezza, dopo somministrazione di una dose singola di rabeprazolo 20 mg. Pazienti con danno renale: E stato osservato che nei pazienti con stabile insufficienza renale allo stadio finale in dialisi di mantenimento (clearance della creatinina < 5 ml/min/1,73 m 2 ) la disponibilità del rabeprazolo è molto simile a quella che si riscontra nei volontari sani. l valori di AUC e di C max in questi pazienti erano circa il 35% più bassi di quelli corrispondenti nei volontari sani. Il tempo di emivita medio di rabepralolo era di 0,82 ore nel volontario sano, 0,95 ore nei pazienti durante l'emodialisi e 3,6 ore dopo la dialisi. La clearance del farmaco nei pazienti con disfunzione renale richiedente emodialisi di mantenimento era circa 2 volte quella dei volontari sani. Pazienti con compromissione epatica: Dopo somministrazione di una dose singola di 20 mg di rabeprazolo, in pazienti con disfunzioni epatiche croniche, di entità da lieve a moderata, si è evidenziato, rispetto a quanto osservato nei volontari sani, un raddoppiamento della AUC e un incremento di 2 o 3 volte del tempo di emivita del rabeprazolo. Tuttavia, dopo una dose giornaliera di 20 mg ripetuta per 7 giorni, il valore di AUC è aumentato solo di 1,5 volte ed il valore di Cmax solo di 1,2 volte. II tempo di emivita del rabeprazolo nei pazienti con compromissione della funzionalità epatica era di 12,3 ore mentre nei volontari sani era di 2,1 ore. La risposta farmacodinamica (controllo del ph gastrico) nei due gruppi era clinicamente comparabile. Pazienti anziani: La velocità di eliminazione del rabeprazolo è lievemente ridotta nei pazienti anziani. Dopo 7 giorni di somministrazione quotidiana di rabeprazolo sodico 20 mg i valori di AUC erano quasi raddoppiati, i valori di Cmax erano superiori del 60% circa e il t½ era aumentato del 30% circa rispetto a quanto riscontrato in giovani volontari sani. Non vi sono tuttavia evidenze di accumulo di rabeprazolo. Polimorfismo del CYP2C19 Dopo somministrazione di una dose giornaliera di 20 mg di rabeprazolo per 7 giorni i rnetabolizzatori lenti dei CYP2C19 presentavano valori di AUC e di t½ pari a circa 1,9 ed 1,6 volte quelli riscontrati per i metabolizzatori rapidi, mentre la Cmax aumentava solo del 40%. 5.3 Dati preclinici di sicurezza Effetti non-clinici sono stati osservati solo con dosaggi così elevati rispetto alla dose massima prevista per l'uomo da rendere trascurabile, rispetto ai dati nell'animale, i timori per la sicurezza del prodotto nell'uomo. Gli studi di mutagenesi hanno dato risultati non univoci. l test su linee cellulari di linfoma di topo sono stati positivi ma il test del micronucleo in vivo ed i test di riparazione del DNA in vivo ed in vitro sono stati negativi. Gli studi di carcinogenesi non hanno evidenziato particolari rischi per l'uomo. 6. Informazioni farmaceutiche 6.1 Elenco degli eccipienti Nucleo della compressa: Mannitolo Crospovidone (tipo A) Ossido di magnesio leggero Povidone (K30) Sodio edetato Calcio stearato Rivestimento: Etilcellulosa Ipromellosa Trietil citrato Sodio carbonato anidro Rivestimento enterico: Copolimero dell acido metacrilico etilacrilato (Tipo A) (1:1) Rivestimento esterno compresse da 10 mg: Ipromellosa Titanio diossido (E171) Macrogol 400 Ferro ossido giallo (E172)
8 Pagina 8 di 9 Ferro ossido rosso (E172) Rivestimento esterno compresse da 20 mg: Ipromellosa Titanio diossido (E171) Macrogol 400 Ferro ossido giallo (E172) 6.2 Incompatibilità Non pertinente. 6.3 Periodo di validità 30 mesi. 6.4 Precauzioni particolari per la conservazione Questo medicinale non richiede nessuna particolare condizione di conservazione. 6.5 Natura e contenuto del contenitore Confezioni blister Al/Al contenente 5, 7, 14, 15, 25, 28, 30, 50, 56, 75, 98 o 120 compresse gastroresistenti. È possibile che non tutte le confezioni siano commercializzate. 6.6 Precauzioni particolari per lo smaltimento e la manipolazione Nessuna istruzione in particolare. Il medicinale non utilizzato e i rifiuti derivati da tale medicinale devono essere smaltiti in conformità alla normativa locale vigente 7. Titolare dell Autorizzazione all Immissione in Commercio Zentiva Italia S.r.l. Viale Bodio, 37/b Milano Italia 8. Numero (i) dell autorizzazione all immissione in commercio Rabeprazolo Zentiva 10 mg compresse gastroresistenti 5 compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n Rabeprazolo Zentiva 20 mg compresse gastroresistenti 5 compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n
9 Pagina 9 di 9 56 compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n compresse in blister OPA/AL/PVC/AL AIC n Data di prima autorizzazione/rinnovo dell autorizzazione Determinazione A.I.C. n.628/2012 del 19/10/2012. Gazzetta Ufficiale n.260 del 07/11/ Data di revisione del testo Marzo 2015
Riassunto delle caratteristiche del prodotto. 10 mg di rabeprazolo sodico (come anidro o monoidrato) equivalente a 9,42 mg di rabeprazolo.
 Pagina 1 di 8 Riassunto delle caratteristiche del prodotto 1. Denominazione del medicinale Rabeprazolo Zentiva 10 mg compresse gastroresistenti Rabeprazolo Zentiva 20 mg compresse gastroresistenti 2. Composizione
Pagina 1 di 8 Riassunto delle caratteristiche del prodotto 1. Denominazione del medicinale Rabeprazolo Zentiva 10 mg compresse gastroresistenti Rabeprazolo Zentiva 20 mg compresse gastroresistenti 2. Composizione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. PARIET 20 mg compresse gastroresistenti 20 mg di rabeprazolo sodico, pari a 18,85 mg di rabeprazolo
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PARIET 10 mg compresse gastroresistenti PARIET 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PARIET
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PARIET 10 mg compresse gastroresistenti PARIET 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PARIET
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia
 Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE RABEPRAZOLO DOC Generici 10 mg compresse gastroresistenti RABEPRAZOLO DOC Generici 20 mg compresse gastroresistenti 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE RABEPRAZOLO DOC Generici 10 mg compresse gastroresistenti RABEPRAZOLO DOC Generici 20 mg compresse gastroresistenti 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE COMBANTRIN 250 mg compresse masticabili COMBANTRIN 250 mg/5 ml sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
Trattamento farmacologico dell ulcera gastro-duodenale L. 29
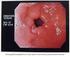 Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Rabeprazolo Teva 10 mg compresse gastroresistenti Rabeprazolo Teva 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Rabeprazolo Teva 10 mg compresse gastroresistenti Rabeprazolo Teva 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Compressa. La compressa è di forma rotonda, di colore giallo chiaro.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE MAALOX 400 mg + 400 mg compresse masticabili senza zucchero 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
REGIONE CALABRIA Dipartimento Tutela della Salute e Politiche Sanitarie
 REGIONE CALABRIA Dipartimento Tutela della Salute e Politiche Sanitarie OMEPRAZOLO Posologia negli adulti Trattamento dell'ulcera duodenale La dose raccomandata nei pazienti con ulcera duodenale attiva
REGIONE CALABRIA Dipartimento Tutela della Salute e Politiche Sanitarie OMEPRAZOLO Posologia negli adulti Trattamento dell'ulcera duodenale La dose raccomandata nei pazienti con ulcera duodenale attiva
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Zerinol Gola 20 mg pastiglie 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una pastiglia contiene 20 mg di ambroxolo cloridrato.
01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Foglio illustrativo. Informazioni per il paziente
 Foglio illustrativo. Informazioni per il paziente Rabeprazolo Zentiva 10 mg compresse gastroresistenti Rabeprazolo Zentiva 20 mg compresse gastroresistenti Medicinale equivalente Legga attentamente questo
Foglio illustrativo. Informazioni per il paziente Rabeprazolo Zentiva 10 mg compresse gastroresistenti Rabeprazolo Zentiva 20 mg compresse gastroresistenti Medicinale equivalente Legga attentamente questo
4.3 Controindicazioni Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1.
 1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
1. DENOMINAZIONE DEL MEDICINALE LOPERAMIDE DOC Generici 2 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide (come loperamide cloridrato). Eccipiente con
Foglio illustrativo. LOPERAMIDE ANGENERICO 2mg capsule rigide. Loperamide. Medicinale Equivalente
 Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini. Ketoprofene
 VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
VET-KETOFEN, 100 mg/ml Soluzione iniettabile per bovini, cavalli e suini (Ketoprofene) Il ketoprofene è un antinfiammatorio non steroideo, dotato di una forte attività antinfiammatoria, antalgica ed antipiretica.
FOGLIO ILLUSTRATIVO. KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10)
 1 FOGLIO ILLUSTRATIVO KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10) CATEGORIA FARMACOTERAPEUTICA Preparati per la tosse e le malattie
1 FOGLIO ILLUSTRATIVO KALOBA 20 mg compresse rivestite con film Estratto liquido essiccato delle radici di Pelargonium sidoides (1 : 8-10) CATEGORIA FARMACOTERAPEUTICA Preparati per la tosse e le malattie
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Documento reso disponibile da AIFA il 10/06/2016 1. DENOMINAZIONE DEL MEDICINALE OMKASA 1mg/ml collirio, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Confezione 20 mg compresse gastroresistenti 100 compresse in flacone HDPE AIC n /M (in base 10) 1513XC(in base 32)
 MEDICINALE PANTOPRAZOLO MYLAN GENERICS TITOLARE AIC: MYLAN S.P.A. Via Vittor Pisani, 20 20124 Milano Autorizzazione all immissione in commercio del medicinale per uso umano «Pantoprazolo Mylan Generics»
MEDICINALE PANTOPRAZOLO MYLAN GENERICS TITOLARE AIC: MYLAN S.P.A. Via Vittor Pisani, 20 20124 Milano Autorizzazione all immissione in commercio del medicinale per uso umano «Pantoprazolo Mylan Generics»
Ogni capsula rigida da 30 mg contiene 59,8 mg di saccarosio
 1. DENOMINAZIONE DEL MEDICINALE Lansox 15 mg capsule rigide Lansox 30 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 15 mg di lansoprazolo Ogni capsula rigida
1. DENOMINAZIONE DEL MEDICINALE Lansox 15 mg capsule rigide Lansox 30 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 15 mg di lansoprazolo Ogni capsula rigida
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
FOGLIO ILLUSTRATIVO confezione 50 compresse. Sodio bicarbonato Sella 500 mg compresse. CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato
 FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRENTAL 600 mg compresse a rilascio modificato. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa a rilascio modificato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Becozym dosaggio alto compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa gastroresistente contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Becozym dosaggio alto compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa gastroresistente contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Un flaconcino contiene 40 mg di pantoprazolo (in forma di pantoprazolo sodico sesquidrato)
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz GmbH 40 mg polvere per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz GmbH 40 mg polvere per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
Confezione 20 mg compresse gastro-resistenti 7 compresse in blister ALU/ALU AIC n /M (in base 10) 156NMC (in base 32)
 MEDICINALE PANTOPRAZOLO RANBAXY TITOLARE AIC: Ranbaxy Italia S.p.A. Piazza Filippo Meda, 3 20121 Milano Italia Autorizzazione all immissione in commercio del medicinale per uso umano «Pantoprazolo Ranbaxy»
MEDICINALE PANTOPRAZOLO RANBAXY TITOLARE AIC: Ranbaxy Italia S.p.A. Piazza Filippo Meda, 3 20121 Milano Italia Autorizzazione all immissione in commercio del medicinale per uso umano «Pantoprazolo Ranbaxy»
Farmacologia Antiulcera
 Farmacologia Antiulcera Goodman & Gilman s, 2001 La cellula parietale gastrica H + K + Cl - G = gastrina, A = ACh, H = istamina; la H + /K + -ATPasi si attiva quando, in seguito a stimoli secretagoghi,
Farmacologia Antiulcera Goodman & Gilman s, 2001 La cellula parietale gastrica H + K + Cl - G = gastrina, A = ACh, H = istamina; la H + /K + -ATPasi si attiva quando, in seguito a stimoli secretagoghi,
CETIRIZINA DOC Generici 10 mg, compresse rivestite con film Medicinale Equivalente
 CETIRIZINA DOC Generici 10 mg, compresse rivestite con film Medicinale Equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
CETIRIZINA DOC Generici 10 mg, compresse rivestite con film Medicinale Equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DESLORATADINA DOC 5 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa rivestita con
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DESLORATADINA DOC 5 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa rivestita con
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Losipaco 2 mg/125 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide cloridrato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Losipaco 2 mg/125 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 2 mg di loperamide cloridrato
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
Sollievo dai sintomi quali nausea, vomito, senso di ripienezza epigastrica, fastidio al tratto addominale superiore, rigurgito del contenuto gastrico.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DOMPERIDONE ABC 10 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene Principio attivo: domperidone
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DOMPERIDONE ABC 10 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene Principio attivo: domperidone
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO
 ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
SINTESI GENERALE DELLA VALUTAZIONE SCIENTIFICA DI LOSEC E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SIBELIUM 10 mg compresse SIBELIUM 5 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SIBELIUM 10 mg compresse SIBELIUM 5 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene:
Compressa rivestita con film di color rosso mattone, di forma rotonda, biconvessa, con impresso "20" da un lato e liscia sull'altro lato.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Germed 20 mg compresse gastroresistenti Esomeprazolo Germed 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Germed 20 mg compresse gastroresistenti Esomeprazolo Germed 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC Generici 40 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALMOTRIPTAN DOC Generici 12,5 mg compresse rivestite con film. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALMOTRIPTAN DOC Generici 12,5 mg compresse rivestite con film. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa
RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW. Dott. Domenico Pecora Brescia
 RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW Dott. Domenico Pecora Brescia Scelta del NAO Scheda tecnica Piani terapeutici AIFA Linee guida Position paper Rimborsabilità NAO
RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW Dott. Domenico Pecora Brescia Scelta del NAO Scheda tecnica Piani terapeutici AIFA Linee guida Position paper Rimborsabilità NAO
PRIMA DELL'USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 Foglio illustrativo PRIMA DELL'USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
Foglio illustrativo PRIMA DELL'USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA
 CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA Documento approvato nella seduta della Commissione PTR del 18.04.07 assorbimento L assorbimento di alcuni farmaci può La ridotta acidità intragastrica Alterazioni
CONFRONTO SCHEDE TECNICHE INIBITORI DI POMPA Documento approvato nella seduta della Commissione PTR del 18.04.07 assorbimento L assorbimento di alcuni farmaci può La ridotta acidità intragastrica Alterazioni
Eccipienti con effetto noto: 38,425 mg maltitolo e lecitina di soia (vedere paragrafo 4.4).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Zentiva Italia 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Zentiva Italia 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente
20 mg. Riassunto delle caratteristiche del prodotto. 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti.
 20 mg Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio
20 mg Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Zobuxa 15 mg compresse per cani di piccola taglia e gatti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Zobuxa 15 mg compresse per cani di piccola taglia e gatti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa
Foglio illustrativo: informazioni per il paziente. MAALOX 400 mg + 400 mg compresse masticabili. Magnesio idrossido + Alluminio ossido, idrato
 Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
FOGLIETTO ILLUSTRATIVO. Baytril flavour 25 mg/ml sospensione orale per gatti
 FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE XATRAL 2,5 mg compresse rivestite 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene 2,5 mg di alfuzosina cloridrato.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE XATRAL 2,5 mg compresse rivestite 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene 2,5 mg di alfuzosina cloridrato.
INTERAZIONI FARMACOLOGICHE
 INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
Foglio illustrativo: Informazioni per l utilizzatore. NOLPAZA 40 mg compresse gastroresistenti. Pantoprazolo Medicinale equivalente
 Foglio illustrativo: Informazioni per l utilizzatore NOLPAZA 40 mg compresse gastroresistenti Pantoprazolo Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: Informazioni per l utilizzatore NOLPAZA 40 mg compresse gastroresistenti Pantoprazolo Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
4. Informazioni cliniche 4.1 Indicazioni terapeutiche VECTAVIR LABIALE è indicato per il trattamento dell'herpes labialis.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale VECTAVIR LABIALE 1% crema 2. Composizione qualitativa e quantitativa Ogni grammo di crema contiene 10 mg di penciclovir Eccipienti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale VECTAVIR LABIALE 1% crema 2. Composizione qualitativa e quantitativa Ogni grammo di crema contiene 10 mg di penciclovir Eccipienti
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose
 GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
Foglio illustrativo: informazioni per il paziente. CALCIO CARBONATO VITAMINA D3 EG 1000 mg U.I. Granulato effervescente. Medicinale equivalente
 Foglio illustrativo: informazioni per il paziente CALCIO CARBONATO VITAMINA D3 EG 1000 mg + 880 U.I. Granulato effervescente Medicinale equivalente Legga attentamente questo foglio prima di prendere questo
Foglio illustrativo: informazioni per il paziente CALCIO CARBONATO VITAMINA D3 EG 1000 mg + 880 U.I. Granulato effervescente Medicinale equivalente Legga attentamente questo foglio prima di prendere questo
RIASSUNTO GENERALE DELLA VALUTAZIONE SCIENTIFICA DI PROTIUM E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come sodio sesquidrato).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantorc 20 mg compresse gastroresistenti. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa gastroresistente contiene
Ogni capsula contiene 20 mg di esomeprazolo (come magnesio diidrato)
 1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Zentiva 20 mg capsule rigide gastroresistenti Esomeprazolo Zentiva 40 mg capsule rigide gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula
1. DENOMINAZIONE DEL MEDICINALE Esomeprazolo Zentiva 20 mg capsule rigide gastroresistenti Esomeprazolo Zentiva 40 mg capsule rigide gastroresistenti 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula
gélules gastro-resistantes Lansoprazole BEXAL 30 mg gélules gastro-resistantes Lansoprazol HEXAL 15 mg Hartkapseln Lansoprazol HEXAL 30 mg Hartkapseln
 ALLEGATO I ELENCO DEI NOMI DEI MEDICINALI, DELLA FORMA FARMACEUTICA, DEI DOSAGGI, DELLA VIA DI SOMMINISTRAZIONE, DEL RICHIEDENTE, DEI TITOLARI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO NEGLI STATI
ALLEGATO I ELENCO DEI NOMI DEI MEDICINALI, DELLA FORMA FARMACEUTICA, DEI DOSAGGI, DELLA VIA DI SOMMINISTRAZIONE, DEL RICHIEDENTE, DEI TITOLARI DELLE AUTORIZZAZIONI ALL IMMISSIONE IN COMMERCIO NEGLI STATI
Foglio illustrativo. In caso di reazioni da ipersensibilità il trattamento deve essere interrotto immediatamente e non ripreso.
 Foglio illustrativo IMMUCYTAL Compresse IMMUCYTAL Granulato per soluzione orale Categoria Farmacoterapeutica Vaccini batterici. Indicazioni terapeutiche Profilassi delle infezioni batteriche ricorrenti
Foglio illustrativo IMMUCYTAL Compresse IMMUCYTAL Granulato per soluzione orale Categoria Farmacoterapeutica Vaccini batterici. Indicazioni terapeutiche Profilassi delle infezioni batteriche ricorrenti
Confezione 10 mg compresse rivestite con film 14 compresse in blister AL/AL AIC n /M (in base 10) 17858X (in base 32)
 Autorizzazione all immissione in commercio del medicinale «Atorvastatina Zentiva» MEDICINALE ATORVASTATINA ZENTIVA TITOLARE AIC: Zentiva Italia S.r.l. Viale L. Bodio, 37/b 20158 Milano Estratto determinazione
Autorizzazione all immissione in commercio del medicinale «Atorvastatina Zentiva» MEDICINALE ATORVASTATINA ZENTIVA TITOLARE AIC: Zentiva Italia S.r.l. Viale L. Bodio, 37/b 20158 Milano Estratto determinazione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come pantoprazolo sodico sesquidrato).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVE E QUANTITATIVA Ogni compressa gastroresistente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Pantoprazolo Sandoz 20 mg compresse gastroresistenti 2. COMPOSIZIONE QUALITATIVE E QUANTITATIVA Ogni compressa gastroresistente
Foglio illustrativo: informazioni per l utilizzatore. Ursilon 150 mg capsule rigide Ursilon 300 mg capsule rigide
 Foglio illustrativo: informazioni per l utilizzatore Ursilon 150 mg capsule rigide Ursilon 300 mg capsule rigide Ursilon 150 mg granuli per sospensione orale Ursilon 300 mg granuli per sospensione orale
Foglio illustrativo: informazioni per l utilizzatore Ursilon 150 mg capsule rigide Ursilon 300 mg capsule rigide Ursilon 150 mg granuli per sospensione orale Ursilon 300 mg granuli per sospensione orale
Allegato III. Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo
 Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico
 1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BRONCHENOLO TOSSE 1,54 mg/ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BRONCHENOLO TOSSE 1,54 mg/ml sciroppo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di sciroppo contengono: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
Foglio illustrativo: informazioni per l utilizzatore
 FOGLIO ILLUSTRATIVO 1 1 Foglio illustrativo: informazioni per l utilizzatore Neo Borocillina Antisettico Orofaringeo 6,4 mg + 52 mg compresse orosolubili alcool benzilico, sodio benzoato Legga attentamente
FOGLIO ILLUSTRATIVO 1 1 Foglio illustrativo: informazioni per l utilizzatore Neo Borocillina Antisettico Orofaringeo 6,4 mg + 52 mg compresse orosolubili alcool benzilico, sodio benzoato Legga attentamente
NEO BOROCILLINA GOLA DOLORE
 FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
Foglio illustrativo. LOPERAMIDE HEXAL 2 mg capsule rigide LOPERAMIDE HEXAL 2 mg compresse effervescenti LOPERAMIDE HEXAL 2 mg/ml soluzione orale
 Foglio illustrativo LOPERAMIDE HEXAL 2 mg capsule rigide LOPERAMIDE HEXAL 2 mg compresse effervescenti LOPERAMIDE HEXAL 2 mg/ml soluzione orale medicinale equivalente CATEGORIA FARMACOTERAPEUTICA Antidiarroico.
Foglio illustrativo LOPERAMIDE HEXAL 2 mg capsule rigide LOPERAMIDE HEXAL 2 mg compresse effervescenti LOPERAMIDE HEXAL 2 mg/ml soluzione orale medicinale equivalente CATEGORIA FARMACOTERAPEUTICA Antidiarroico.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC 20 mg compresse gastroresistenti RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
1. DENOMINAZIONE DEL MEDICINALE PANTOPRAZOLO DOC 20 mg compresse gastroresistenti RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa gastroresistente
RIVISTA: lnt Journal of lmpotence Research (2006) 18, MJ. Dresser, D. Desai, S. Gidwani, AD. Seftel, NB. Modi O B I E T T I V I
 I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
Foglio illustrativo: informazioni per l utilizzatore. Becozym compresse gastroresistenti
 Foglio illustrativo: informazioni per l utilizzatore Becozym compresse gastroresistenti Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per
Foglio illustrativo: informazioni per l utilizzatore Becozym compresse gastroresistenti Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale Estratto glucosidico di rabarbaro e Acido salicilico Legga attentamente questo foglio prima di usare
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE PYRALVEX 50 mg/ml + 10 mg/ml Soluzione gengivale Estratto glucosidico di rabarbaro e Acido salicilico Legga attentamente questo foglio prima di usare
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film
 1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film 1. DENOMINAZIONE DEL MEDICINALE RANITIDINA ABC 150 mg
1 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO RANITIDINA ABC 150 mg compresse rivestite con film RANITIDINA ABC 300 mg compresse rivestite con film 1. DENOMINAZIONE DEL MEDICINALE RANITIDINA ABC 150 mg
Patologie del sistema emolinfopoietico Molto rari: Linfoadenopatia 1 Disturbi del metabolismo e della nutrizione Comuni: perdita di appetito 2 Disturb
 di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
AIFA - Agenzia Italiana del Farmaco
 Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Acarphage 50 mg compresse Acarphage 100 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa di Acarphage
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Acarphage 50 mg compresse Acarphage 100 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa di Acarphage
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LANSOPRAZOLO DOC GENERICI 15 mg capsule rigide gastroresistenti LANSOPRAZOLO DOC GENERICI 30 mg capsule rigide gastroresistenti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LANSOPRAZOLO DOC GENERICI 15 mg capsule rigide gastroresistenti LANSOPRAZOLO DOC GENERICI 30 mg capsule rigide gastroresistenti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE METFORMINA RATIOPHARM ITALIA 850 mg compresse rivestite con film METFORMINA RATIOPHARM ITALIA 1000 mg compresse rivestite con
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE METFORMINA RATIOPHARM ITALIA 850 mg compresse rivestite con film METFORMINA RATIOPHARM ITALIA 1000 mg compresse rivestite con
