LA CHIMICA NUCLEARE. Figura 1 - La lastra fotografica trovata impressionata da Becquerel
|
|
|
- Olimpia Salvatori
- 8 anni fa
- Visualizzazioni
Transcript
1 LA CHIMICA NUCLEARE Lo studio delle trasformazione che avvengono nel nucleo atomico permette applicazioni che spaziano in numerosi campi della scienza, dallo studio della formazione degli elementi nell universo alla sintesi di molecole radioattive per la medicina La storia della scoperta e dell isolamento di questa sostanza [il radio] ha fornito la prova della mia ipotesi, secondo cui la radioattività è una proprietà atomica della materia e può fornire un metodo di ricerca per nuovi elementi. L ipotesi ha condotto alle attuali teorie sulla radioattività. (Marie Curie, Nobel Lecture, ). Le reazioni chimiche sono trasformazioni che comportano lo scambio o la condivisione degli elettroni tra gli atomi coinvolti nella formazione dei legami, mentre le reazioni nucleari provocano cambiamenti dell identità degli elementi stessi in quanto interessano il cuore dell atomo fatto di protoni e neutroni. Le reazioni nucleari sono spesso accompagnate dal rilascio di quantità di energia enormemente più grandi di quelle coinvolte nelle reazioni chimiche, ed inoltre, la velocità e la resa di queste reazioni generalmente non dipendono dalle variazioni di temperatura, pressione o dalla presenza di catalizzatori. La chimica nucleare ha avuto origine dalla scoperta del chimico francese Henri Becquerel che nel 1896, durante i suoi studi sulla fosforescenza, notò casualmente che un minerale ricco di uranio, la pechblenda, posto accanto a lastre Figura 1 - La lastra fotografica trovata impressionata da Becquerel fotografiche chiuse nei loro contenitori a prova di luce, ne provocava l'annerimento e ne dedusse che tali minerali dovevano emettere dei raggi molto più penetranti di quelli luminosi (fig.1). Questo significava che questi raggi dovevano trasportare energia, ma la pechblenda li emetteva in continuazione senza alcun apporto esterno di energia. Questa apparente violazione del principio di conservazione dell energia rese presto evidente che i raggi di Becquerel dovevano aver origine nei nuclei dell atomo. Infatti, dato che la radiazione dell uranio rimane invariata sia nella forma di elemento che di composto, ed essa non varia con la temperatura, pressione o stato di ionizzazione, la radiazione non può essere derivata dalle transizioni elettroniche. Becquerel chiamò queste emissioni raggi uranici. Nel 1898 i coniugi Curie scoprirono il radio, un nuovo elemento che emetteva dei raggi cinquecento più intensi di quelli dell'uranio. Questo elemento era in grado di emettere tre tipi di radiazioni: i raggi alfa, i raggi beta e i raggi gamma. I raggi gamma sono radiazioni elettromagnetiche come i raggi X; i raggi alfa e beta consistono invece in 1 curie lecture.html
2 particelle di materia. Il radio, emettendo energia e materia, si trasforma in elio e piombo, cioè in elementi più leggeri. Dato che la stessa cosa avviene per tutte le altre sostanze radioattive, si può dedurre che in natura si realizza spontaneamente la trasmutazione degli elementi. Dato che era chiaro che questi raggi non erano una caratteristica solo dell uranio fu cambiato il nome da raggi uranici a radioattività. Ai Curie e Bacquerel nel 1903 fu assegnato il premio Nobel per la Fisica per il loro lavoro sulla radioattività. Nel 1911 Marie Curie vinse il premio Nobel per la Chimica per aver scoperto due nuovi elementi e rimane l unica persona ad essere stata premiata con il Premio Nobel sia in fisica che in chimica. Ci sono essenzialmente tre sorgenti elementi radioattivi: i nuclidi primordiali sono gli elementi radioattivi presenti dalla formazione della Terra e hanno un età comparabile a quella del sistema solare; i nuclidi cosmogenici che sono atomi costantemente prodotti nell atmosfera dal bombardamento dei raggi cosmici; gli elementi radioattivi di origine antropogenica sono il risultato delle attività umane nella produzione dell energia nucleare e nella dispersione di fallout radioattivo durante le esplosioni nucleari. Il nucleo costituisce la parte centrale dell atomo, presenta dimensioni dell ordine di m ed è formato da protoni e da neutroni, che sono detti nucleoni (particelle formanti il nucleo). I primi presentano carica elettrica positiva, mentre i secondi sono privi di carica elettrica. Il numero di protoni è uguale al numero di elettroni, così che l'atomo è elettricamente neutro. La somma del numero dei protoni più il numero dei neutroni viene chiamato numero di massa e si indica con la lettera A, mentre il numero totale di protoni viene chiamato numero atomico e si indica con la lettera Z. Per un dato elemento, il numero di protoni è fisso ed è quello che lo caratterizza, mentre il numero di neutroni può essere variabile. Atomi che presentano lo stesso numero atomico ma diversa massa atomica sono detti isotopi. Nel 1903, Ernest Rutherford e Frederik Soddy proposero che la radioattività è il risultato del cambiamento naturale di un isotopo di un elemento in un isotopo di un altro elmento, e chiamarono questo processo reazione nucleare. A differenza delle equazioni chimiche in cui gli elementi mantengono la loro identità, nelle reazioni nucleari questi si trasformano in altri elementi con diverse caratteristiche. Comunque anche le reazioni nucleari vanno bilanciate, nel senso che la somma delle masse iniziali deve essere uguale a quella delle masse finali. L isotopo generico X viene rappresentato con la seguente notazione: Per esempio, i simboli e rapprentano rispettivamente l isotopo del Carbonio con 6 protoni e 6 neutroni e l isotopo con 6 protoni e 8 neutroni. Le principali particelle subatomiche (protoni, neutroni ed elettroni) hanno notazioni simili: Protone Neutrone Elettrone
3 Nel caso dell elettrone l esponente 0 sta ad indicare un numero di massa praticamente zero rispetto al nucleo. L indice inferiore -1 indica la carica negativa della particella. Esso non è un è un numero atomico ma scrivendo il simbolo in questo modo è utile per bilanciare le equazioni nucleari. Consideriamo il decadimento del radio-226 in radon-222. In questa reazione nucleare detta decadimento alfa, il nucleo instabile emette una particella alfa composta da due protoni e due neutroni (un nucleo di elio ), e si trasforma in un nucleo diverso, con numero atomico (Z-2) e numero di massa (A 4). Come si può vedere dalla tabella precedente, la somma dei numeri dei numeri di massa e dei numeri atomici rimane uguale nella reazione nucleare. Le radiazioni alfa sono poco penetranti e nell aria possono percorrere pochi cm perché vengono bloccate dagli urti con le molecole che costituiscono l aria stessa. Il passaggio di una particella alfa attraverso un mezzo provoca, a causa della carica elettrica +2 e della massa 7400 volte maggiore di quella dell'elettrone, la ionizzazione di un gran numero di atomi. Quando la radiazione ionizza molecole all interno di cellule di organismi viventi, queste possono modificare le normali reazioni biochimiche determinando la morte della cellula o la sua riproduzione anormale. La capacità di ionizzare molecole o atomi da parte della radiazione è detto potere ionizzante. Di tutti i tipi di radiazione, quella alfa presenta il potere ionizzante maggiore Nel decadimento beta, un neutrone può essere convertito in un protone, un elettrone e un altra particella chiamata antineutrino 2. Il nucleo si trasforma in un nucleo con numero atomico (Z + 1) ma stesso numero di massa A. Un esempio è il decadimento del Carbonio-14 in Azoto-14: La somma dei numeri di massa rimane uguale nella reazione ([14 = ], così come la somma della carica elettrica [6 = ]). Le radiazioni beta sono più penetranti di quelle alfa e sono in grado di attraversare sottili fogli metallici, ma sono molto meno massive delle particelle alfa e quindi hanno un potere ionizzante inferiore. Il decadimento gamma è di natura elettromagnetica ed accompagna solitamente una radiazione alfa o una radiazione beta. Infatti, dopo l'emissione alfa o beta, il nucleo è ancora eccitato perché i suoi protoni e neutroni non hanno ancora raggiunto il nuovo stato di equilibrio. Pertanto, il nucleo si libera rapidamente dell eccesso di energia attraverso l'emissione di una radiazione gamma. Il raggio gamma non ha massa né carica e pertanto quando viene emesso da un atomo radioattivo questo non cambia la 2 Il neutrino è una particella ad elevato contenuto di energia senza carica elettrica e di massa praticamente nulla, la cui esistenza fu prevista teoricamente da L.Pauli nel 1931 per rendere conto dell'energia e della quantità di moto mancanti nel decadimento beta e da E. Fermi nel Nel 1956 trovò evidenza sperimentale ad opera di F. Reines e C.L. Cowan Jr. L antineutrino è l antiparticella del neutrino.
4 sua massa atomica o il numero atomico. Per esempio, l emissione alfa dell U-238 è anche accompagnato dall emissione di un raggio gamma: Le radiazioni gamma sono molto penetranti, e bloccarle richiede materiali ad elevata densità come il piombo (Fig. 2). Altro tipo di radiazione è l emissione di positroni. Questa avviene quando in un nucleo instabile un protone è convertito in un neutrone ed è emesso un positrone ed un neutrino. Il positrone è Figura 2 - Diverso potere di penetrazione delle un antiparticella dell elettrone: ha la radiazioni nucleari stessa massa dell elettrone ma carica opposta. Se un positrone collide con un elettrone queste due particelle si annichilano l una con l altra rilasciando energia nella forma di raggi gamma. L emissione di positroni è a volte chiamata emissione β +. Il potere ionizzante e di penetrazione dei positroni è simile a quello dei raggi β. Quando un atomo emette un positrone, il suo numero atomico decresce di 1, mentre il numero di massa rimane invariato: ad esempio, l equazione nucleare per l emissione positronica del fosforo-30: ν Lo stesso risultato dell emissione positronica si ha con un altro tipo di decadimento, la cattura elettronica. In questo tipo di radiazione, un elettrone proveniente dallo strato più esterno dell atomo viene assorbito da un nucleo instabile, e unendosi ad un protone, si trasforma in un neutrone con l emissione di un neutrino. Un esempio di cattura elettronica è il decadimento del potassio-40 in argo-40: ν Il potassio-40 costituisce lo 0,01% della crosta terrestre ed è il responsabile della maggior parte della radiazione di origine naturale nelle specie viventi e nel suolo. Il rapporto tra protoni e neutroni all'interno di un nucleo ed il numero ed il tipo di interazioni che si stabiliscono tra essi determina se questo nucleo sia o non sia stabile (fig. 3). Ciascun nucleone è in grado di stabilire interazioni con altri nucleoni; una coppia protone-neutrone stabilisce una somma di interazioni stabili e bilanciate reciprocamente, mentre un eccesso o un difetto di neutroni nel nucleo sbilancia il numero ed il tipo delle interazioni e pertanto il nucleo risulta instabile. Solo quei nuclei che possiedono approssimativamente lo stesso numero di protoni e di neutroni risulta stabile nelle condizioni attuali presenti sulla terra.
5 Nel nucleo la repulsione elettrostatica tra i protoni è molto intensa, ma esso è mantenuto unito da una forza specifica, detta interazione (o forza) nucleare forte (fig.3). Questa forza è estremamente intensa, ma decresce molto rapidamente all'aumentare della distanza tra i nucleoni; perciò il nucleo, quando le sue dimensioni aumentano tanto da non permettere all interazione forte di superare quella elettrica repulsiva, tende a decomporsi formando, così, nuclei più stabili. Un importante numero per determinare la stabilità nucleare è il rapporto di neutroni e protoni (N/Z). La fig. 4 mostra un grafico in cui sono posti in ascisse il numero di protoni (Z) ed in ordinata il numero di neutroni (N) per tutti i nuclei conosciuti. Gli elementi che stanno sulla diagonale hanno tutti una stabilità nucleare elevata, (questa regione è conosciuta come banda di stabilità) mentre quelli che si trovano sopra la diagonale (eccesso di neutroni) e sotto (eccesso di protoni) sono instabili e soggetti a decadimento radioattivo. I nuclei degli elementi leggeri hanno un rapporto N/Z tendente ad uno, mentre i nuclei degli elementi pesanti mostrano tutti un eccesso di neutroni noto come eccesso di massa. Figura 3 - Le due opposte forze presenti in un nucleo sono la repulsione elettrostatica tra i protoni positivi e la forza nucleare forte che tiene insieme i protoni e neutroni Figura 4 - La banda di stabilità nucleare mostra diverse combinazioni di protoni/neutroni che danno luogo a isotopi con tempo di dimezzamento misurabile. L ingrandimento della banda nella regione da Z=66 a Z=79 mostra i diversi tipi di decadimento radioattivo Quando Z cresce, la stabilità del nucleo tende a diminuire a causa della repulsione coulombiana, le forze nucleari attrattive devono quindi aumentare ed è necessario un numero N di neutroni percentualmente maggiore. Pertanto all'aumentare del numero di protoni, la repulsione elettrostatica rende necessario un leggero eccesso di neutroni e per questo il rapporto N/Z si discosta dall'unità per molti nuclei stabili. Per esempio, a Z=40 i nuclei stabili hanno un rapporto N/Z di circa 1,25 e a Z=80 il rapporto raggiunge 1,5. Il limite di questa stabilità è dato dall'elemento bismuto con Z=83, dopodiché in natura non esistono nuclei stabili in condizioni normali. Per raggiungere la stabilità i nuclei con Z > 83 danno luogo a processi di decadimento che riducono il valore di Z. Nuclei con Z elevato (>83) come l americio emettono spontaneamente particelle alfa diminuendo il suo numero atomico Z due unità e il suo numero di massa A di quattro unità.
6 Il tipo di radioattività emessa dipende in parte dal rapporto N/Z. Se questo è molto alto, i nuclidi che si trovano sopra la valle di stabilità hanno troppi neutroni e tendono a dar luogo a decadimenti beta, convertendo neutroni in protoni e incrementando così il numero atomico. Se il rapporto N/Z è troppo basso, i nuclidi sotto la valle di stabilità tendono convertire protoni in neutroni attraverso una emissione di positroni. Oltre al rapporto N/Z, anche il numero reale di protoni e neutroni agisce sulla stabilità del nucleo. La tabella mostra diversi nuclidi che hanno combinazioni di nucleoni pari o dispari. È da notare che i nuclidi stabili hanno un numero pari sia di protoni che di neutroni. A partire dagli anni 50 è stato sviluppato un modello a gusci del nucleo, costituito da particelle che si muovono in un campo di forze nucleari. Analogamente ai gusci elettronici completi, il modello prevede che, in corrispondenza di gusci nucleari pieni, contenenti un prestabilito numero di nucleoni (N o Z = 2, 8, 20, 28, 50, 82 e N=126), il sistema sia particolarmente stabile. Questi numeri sono chiamati numeri magici. Dato che i numeri magici sono pari, questo spiega perché gli elementi con numeri di protoni e neutroni pari rappresentano il 90% degli elementi presenti nella crosta terrestre (tab. 1). Esempi sono:,,, e Il piombo-208, ha 82 protoni e 126 neutroni e il nucleo, doppiamente magico, appare essere virtualmente eterno. Diversi isotopi radioattivi decadono spontaneamente per formare un prodotto che a sua volta è radioattivo. La maggior parte degli elementi radioattivi non decade direttamente in un nucleo stabile, ma passa attraverso una serie di decadimenti successivi fino a raggiungere un isotopo stabile. Queste sequenze di reazioni nucleari sono dette catene di decadimento radioattivo. In ogni stadio della sequenza, il reagente è chiamato isotopo Figura 5 - Catena di decadimento dell U-238; i pallini celesti rappresentano emissione beta e quelli rosa emissione gamma genitore, e il prodotto isotopo figlio. Ad esempio l uranio, il più pesante elemento presente in natura (Z=92), ha l isotopo la cui catena di decadimento segue lo schema seguente riportato in fig.5. Nel primo stadio l uranio-238 emette una particella alfa e si trasforma in torio-234.
7 Il nuclide figlio,, che si forma in seguito al decadimento dell uranio, è esso stesso radioattivo, e decade a Proactinio-234. Anche il è radioattivo e pertanto decade a attraverso l emissione beta. Il decadimento radioattivo continua finché è raggiunto lo stato stabile del Pb-207. Le leggi del decadimento radioattivo sono stabilite in termini matematici. Il momento in cui un dato nucleo radioattivo decadrà non può essere previsto. La radioattività è un processo statisticamente casuale, e la probabilità che un nucleo decada in un dato momento è la stessa per tutti i nuclei di ogni nuclide radioattivo. Tutti i nuclei radioattivi decadono con una cinetica di primo ordine, e ciò significa che la velocità di decadimento di un particolare campione è direttamente proporzionale al numero di nuclei presenti. La velocità di decadimento sarà quindi espressa dalla relazione: Dove N è il numero di nuclei radioattivi e λ la costante di velocità detta costante di decadimento, che rappresenta la frazione dei nuclei radioattivi presenti che decadrà in una data unità di tempo (il segno meno sta ad indicare che N diminuisce). Integrando questa equazione si ottiene: (1) Dove N o e N t sono i numeri di atomi della specie radioattiva esistenti rispettivamente al tempo zero e al tempo t. Indicando con /, il tempo necessario affinché il 50% degli atomi considerati decadano, la (1) diventa: e quindi: 0,5 / /, / è chiamato tempo di dimezzamento ed è caratteristico per ogni nuclide. Il tempo di dimezzamento è Figura 6 - Decadimento del Radon-220 con tempo di indipendente dal numero di dimezzamento di 55,6 s nuclei ed è inversamente proporzionale alla costante di decadimento. In fig. 6 è riportato l andamento del
8 Tabella 2 Tipo di decadimento e tempo di dimezzamento di diversi isotopi radioattivi decadimento del Radon-220. In tabella 2 sono riportati i valori dei tempi di dimezzamento di alcuni isotopi radioattivi, e da essi risulta quanto sia ampio l intervallo di valori di /, anche per i diversi nuclidi di uno stesso elemento. Sulla base della velocità di decadimento di un isotopo radioattivo è possibile datare l età di un materiale. L esempio più conosciuto è la procedura usata per datare i manufatti archeologici basata sulla misura delle quantità di carbonio-14 e carbonio-12 in materiali di origine biologica. Confrontando il rapporto tra il contenuto di 238 U (t 1/2 = 4, anni) e quello del prodotto finale del suo decadimento, 206 Pb nei meteoriti, è stato possibile misurare l età del Sistema Solare, e quindi della Terra: 4,7 miliardi di anni 3. Figura 7 - Diagramma schematico di un ciclotrone. Al centro vengono introdotte le particelle cariche che subiscono un accelerazione mediante i due elettrodi cavi. Magneti presenti sopra e sotto questi elettrodi determinano una traiettoria a spirale che si espande all aumentare della velocità delle particelle. Quando queste hanno velocità sufficiente escono dall acceleratore e si dirigono verso i nuclei target In natura è possibile trovare isotopi instabili, o perché questi isotopi presentano tempi di dimezzamento molto lunghi come (ad esempio l uranio-235, l uranio-238 e il torio- 232) o perché, nonostante abbiano brevi tempi di dimezzamento sono continuamente formati da reazioni nucleari (ad esempio, il carbonio-14 formato in reazioni nucleari iniziate dai raggi cosmici o gli isotopi formati nelle catene di decadimento radioattivo). Tutti gli altri isotopi sono stati sintetizzati mediante reazioni nucleari artificiali, indicate come trasmutazioni. La prima trasmutazione è stata realizzata da Ernest Rutherford nel 1919, il quale bombardando con particelle alfa atomi di azoto osservò tra i prodotti la formazione di protoni. Egli correttamente concluse che era avvenuta la reazione nucleare seguente: 3 Le trasformazioni nucleari: "La datazione mediante radioisotopi" - Lezioni di Scienze Naturali Treccani.it
9 Le particelle alfa usate nei primi studi sulle reazioni nucleari venivano da materiali radioattivi naturali come l uranio e presentavano energie relativamente basse rispetto a quelle necessarie per superare la repulsione elettrostatica dei nuclei. La scoperta del neutrone e il suo uso come proiettile nel bombardamento dei nuclei e l utilizzo di particelle di alta energia ottenute mediante acceleratori, hanno esteso notevolmente la chimica delle reazioni nucleari aprendo la strada alle trasmutazioni artificiali degli elementi chimici. Le particelle, accelerate ad altissima velocità, sono in grado di superare la repulsione elettrostatica e penetrare i nuclei bersaglio, dando luogo a trasformazioni nucleari. In fig. 7 è riportato il diagramma schematico di un acceleratore di particelle, il ciclotrone. Grazie alle reazioni nucleari si sono ottenuti degli elementi artificiali con numero atomico Z superiore a 92 (uranio), i cosiddetti elementi transuranici. Lo sviluppo degli acceleratori di particelle ad alta energia ha permesso di far avvenire collisioni di nuclei più leggeri mediante fasci di ioni pesanti ed ottenere anche nuclidi con tempi di dimezzamento brevissimo ampliando così il sistema periodico con nuovi elementi con numero atomico fino a Gli elementi radioattivi sono usati in molte aree della scienza e della medicina. Ad esempio la diagnostica per immagini (nuclear imaging), che consiste nella creazione di immagini di specifiche parti del corpo, utilizzando un isotopo radioattivo somministrato come elemento o incorporato in un composto che si concentra nei tessuti che devono essere analizzati. Le emissioni radioattive vengono rilevate e utilizzate per ricostruire un immagine dei tessuti (fig.8). La tabella mostra una lista di radioisotopi normalmente utilizzati nei processi di nuclear imaging. Tutti Tabella 3 Isotopi radioattivi utilizzati nella diagnostica per immagini. Sono indicati i tempi di dimezzamento e i principali aree analizzate gli isotopi emettono radiazione gamma. Questo tipo di radiazione è preferita per la creazione di immagini perché, in piccole dosi, danneggia meno i tessuti delle radiazioni alfa o beta. La tomografia ad emissione di positroni (PET) è un metodo di diagnostica per immagini utilizzato per osservare la struttura e la funzione del cervello. Si inietta nel flusso sanguigno una sostanza marcata con un isotopo che emette positroni (decadimento beta) che viene trasportata fino al cervello. L isotopo radioattivo emette positroni che vengono annichiliti da elettroni con una simultanea emissione a 180 l uno dall altro di due fotoni gamma. Una serie di sensori rilevano le zone di emissione e mediante un computer viene costruita una mappa che mostra dove l emissione è localizzata nel corpo (fig.8). Due degli isotopi utilizzati sono l 15 O, iniettato come H 2 15 O per misurare il flusso del sangue e il 18 F legato a una molecola simile al glucosio per misurare l assunzione di glucosio, un indicatore del metabolismo. 4 I nuovi elementi superpesanti - Chimica moderna Treccani.it
10 Figura 8 - La PET permette di vedere come il cervello utilizza il glucosio. A destra immagine di persona normale. Il colore rosso mostra la più alta utilizzazione del glucosio. A sinistra, immagine di persona che abusa di cocaina. Il cervello mostra un utilizzazione minore del glucosio. Ci sono molte aree con ridotta attività metabolica una mole di deuterio in una mole di protoni e neutroni: Poiché, gli isotopi utilizzati hanno tempi di dimezzamento brevi, l apparecchiatura per la PET deve essere localizzata vicino ad un ciclotrone dove sono preparati i radionuclidi che vengono incorporati nel composto di trasporto. Si può determinare la stabilità termodinamica di un nucleo calcolando l energia nucleare di legame, E b cioè l energia richiesta per separare i nuclei di un atomo in protoni e neutroni. Per esempio l energia di legame nucleare per il deuterio è l energia richiesta per separare 2,15 10 L energie di legame nucleare è legata al fatto che quando i nucleoni si uniscono la massa del nucleo è sempre minore di quella delle masse dei suoi componenti e la differenza (difetto di massa) è quella che fornisce - con la famosa legge di Einstein - l'energia di legame del nucleo 5 : Figura 9 energia di legame per nucleone in funzione del numero di massa dell atomo (espressa in MeV) decomporre un nucleo) corrisponde al dove c = 2, m/s. Per confrontare i valori delle energie di legame che intercorrono tra i nucleoni di nuclidi diversi, si può calcolare l energia per nucleone, dividendo il valore dell energia di legame per il numero dei nucleoni che lo costituiscono (fig. 9). Da notare che il valore più stabile (cioè il valore maggiore di energia per con energia di legame di 8,79 MeV. 5 Ad esempio considerando la formazione di una mole deuterio da mole di protoni e neutroni, tendendo presente le masse relative si calcola, per il difetto di massa, il valore: Δm =[ g/mol g/mol] g/mol = g/mol
11 L andamento del grafico mostra che i nuclei con numeri di massa più bassi del ferro dovrebbero tendere ad unirsi, mentre quelli con numeri più alti a dividersi per ottenere nuclei con valori attorno a 60. Le energie di attivazione richieste per queste trasformazioni nucleari sono tali che nelle condizioni normali avvengono spontaneamente solo per rari elementi radioattivi naturali. Le reazioni nucleari possono essere provocate attraverso il processo di fissione nucleare (nuclei grandi che si rompono per dare nuclei più piccoli) e di fusione nucleare (nuclei leggeri che si uniscono per dare nuclei più pesanti). La fissione nucleare fu scoperta alla fine degli anni 30 a seguito del bombardamento con neutroni dell isotopo dell uranio-235. Questo, inizialmente cattura il neutrone per formare uranio-236 che è però instabile e successivamente si spezza dando due nuovi nuclei che possono essere uguali (fissione simmetrica) o diversi (fissione asimmetrica). Durante il processo si liberano nuovi neutroni che provocano a loro volta altre fissioni determinando un processo a catena. Ad esempio: 3 L energia liberata è di 2, J per mole di. Il processo di fissione produce un energia 26 milioni di volte maggiore di Figura 10 - Rappresentazione del processo di quella prodotta dalla combustione del fissione in cui ogni evento produce tre neutroni che possono provocare altre fissioni metano (8, J). La reazione a catena, determinando un processo a catena fatta avvenire lentamente, può essere sfruttata per produrre energia elettrica nei reattori nucleari. In una reazione di fusione nucleare piccoli nuclei reagiscono per formare nuclei più pesanti. Un esempio di fusione è quello tra i nuclei di idrogeno-2 (deuterio) e idrogeno-3 (trizio): 1,7 10 Questa reazione richiede un enorme energia di attivazione per superare la forza di repulsione elettrostatica tra i nuclei di idrogeno e pertanto per realizzarla sono necessarie temperature dell ordine da 10 6 a 10 7 K, come quelle presenti all interno del sole. A queste temperature la materia non esiste come atomi o molecole ma nella forma di plasma costituito da nuclei non legati ed elettroni. Anche se c è la speranza che in futuro le reazioni di fusione possano essere sfruttate come fonte di energia per scopi civili, esistono ancora molti problemi tecnici che devono essere risolti, soprattutto per quanto riguarda le temperature estremamente alte richieste dalle reazioni e come confinare il plasma abbastanza a lungo da permettere il rilascio di una quantità netta di energia. Poiché il plasma è un conduttore
12 elettrico, esso è soggetto alle forze magnetiche. Così, un approccio è confinare il plasma caldo mediante un campo magnetico. Un altro metodo, detto a confinamento inerziale, consiste nel riscaldare con fasci di raggi laser o fasci di particelle accelerate la materia così rapidamente che le reazioni di fusione hanno luogo prima che questa abbia il tempo di espandersi. Ciononostante le enormi difficoltà, molte caratteristiche della fusione nucleare incoraggiano a proseguire la ricerca in questo campo. Primo, l idrogeno è un propellente poco costoso e disponibile in quantità praticamente illimitata. Secondo, molti isotopi radioattivi che si generano durante la fusione nucleare hanno tempi di dimezzamento brevi e pertanto essi rimangono un pericolo per un tempo molto limitato.
La radioattività e la datazione al radio-carbonio
 1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
Il nucleo degli atomi
 Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
RADIAZIONI RADIAZIONI IONIZZANTI RADIAZIONI IONIZZANTI
 RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
Capitolo 7 Le particelle dell atomo
 Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER:
 ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
LE RADIAZIONI. E = h. in cui è la frequenza ed h una costante, detta costante di Plank.
 LE RADIAZIONI Nel campo specifico di nostro interesse la radiazione è un flusso di energia elettromagnetica o di particelle, generato da processi fisici che si producono nell atomo o nel nucleo atomico.
LE RADIAZIONI Nel campo specifico di nostro interesse la radiazione è un flusso di energia elettromagnetica o di particelle, generato da processi fisici che si producono nell atomo o nel nucleo atomico.
Stabilita' dei nuclei
 Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t1/2 circa 900 s), i protoni sono stabili.
Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t1/2 circa 900 s), i protoni sono stabili.
April 11, 2011. Fisica Nucleare. Monica Sambo. Sommario. Introduzione. Radioattivitá. Fisica del nucleo. Bibliografia. Esempio. Raggi emessi Esempio
 April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
Paleontologia. Archeologia. Radioisotopi. Industria. Biologia. Medicina
 Paleontologia Industria Radioisotopi Archeologia Medicina Biologia I radioisotopi I radioisotopi (o radionuclidi), sono dei nuclidi instabili che decadono emettendo energia sottoforma di radiazioni, da
Paleontologia Industria Radioisotopi Archeologia Medicina Biologia I radioisotopi I radioisotopi (o radionuclidi), sono dei nuclidi instabili che decadono emettendo energia sottoforma di radiazioni, da
La propagazione delle onde luminose può essere studiata per mezzo delle equazioni di Maxwell. Tuttavia, nella maggior parte dei casi è possibile
 Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone
 Unità n 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Unità n 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Nascita e morte delle stelle
 Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
LEZIONE 12 Esposizioni da Radioattività Naturale
 LEZIONE 12 Esposizioni da Radioattività Naturale Radioattività naturale Sorgenti esterne e sorgenti interne L uomo è sottoposto ad irradiazione naturale dovuta a sorgenti sia esterne che interne. L irradiazione
LEZIONE 12 Esposizioni da Radioattività Naturale Radioattività naturale Sorgenti esterne e sorgenti interne L uomo è sottoposto ad irradiazione naturale dovuta a sorgenti sia esterne che interne. L irradiazione
IL FOTOVOLTAICO E L ARCHITETTURA
 IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi)
 Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi) Il presente documento schematizza le principali particelle sub atomiche. Lo scopo di questa dispensa è fornire una schematizzazione sintetica
Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi) Il presente documento schematizza le principali particelle sub atomiche. Lo scopo di questa dispensa è fornire una schematizzazione sintetica
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Spettrometria di massa
 Tecniche di monitoraggio ambientale di tipo fisico Spettrometria di massa (J. B. Fenn, K. Tanaka, K. Wüthrich, premio nobel per la chimica nel 2002) Analisi chimica dell aerosol Riconoscimento di inquinanti
Tecniche di monitoraggio ambientale di tipo fisico Spettrometria di massa (J. B. Fenn, K. Tanaka, K. Wüthrich, premio nobel per la chimica nel 2002) Analisi chimica dell aerosol Riconoscimento di inquinanti
L ATOMO. Risponde (o almeno ci prova)
 L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
19 Il campo elettrico - 3. Le linee del campo elettrico
 Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Metodi di datazione di interesse archeologico
 Metodi di datazione di interesse archeologico Radioattività La radioattività, o decadimento radioattivo, è un insieme di processi fisico-nucleari attraverso i quali alcuni nuclei atomici instabili o radioattivi
Metodi di datazione di interesse archeologico Radioattività La radioattività, o decadimento radioattivo, è un insieme di processi fisico-nucleari attraverso i quali alcuni nuclei atomici instabili o radioattivi
Appunti sulla Macchina di Turing. Macchina di Turing
 Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
LA RADIOATTIVITA. Nel caso degli isotopi dell idrogeno: Nel caso degli isotopi del Carbonio:
 LA RADIOATTIVITA Gli atomi di un elemento non sono in realtà tutti uguali, una piccola percentuale di essi ha un numero di neutroni differente, questi atomi si chiamano isotopi di quell elemento. Il 99,9%
LA RADIOATTIVITA Gli atomi di un elemento non sono in realtà tutti uguali, una piccola percentuale di essi ha un numero di neutroni differente, questi atomi si chiamano isotopi di quell elemento. Il 99,9%
Un altro importante parametro di questo processo è la risoluzione che rappresenta la distanza minima che la litografia può apprezzare.
 TECNICHE LITOGRAFICHE La litografia è un processo basilare nella realizzazione di circuiti integrati,esso consiste nel depositare un materiale detto resist sul wafer da processare che una volta esposto
TECNICHE LITOGRAFICHE La litografia è un processo basilare nella realizzazione di circuiti integrati,esso consiste nel depositare un materiale detto resist sul wafer da processare che una volta esposto
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
Tesina di scienze. L Elettricità. Le forze elettriche
 Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
L energia nucleare La radioattività
 L energia nucleare La radioattività La radioattività fu scoperta nel 1896 da Henri Bequerel, un fisico francese che per primo osservò l emissione spontanea di radiazioni da un pezzo di un minerale di uranio,
L energia nucleare La radioattività La radioattività fu scoperta nel 1896 da Henri Bequerel, un fisico francese che per primo osservò l emissione spontanea di radiazioni da un pezzo di un minerale di uranio,
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Elettricità e magnetismo
 E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
MOTO DI UNA CARICA IN UN CAMPO ELETTRICO UNIFORME
 6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
Più processori uguale più velocità?
 Più processori uguale più velocità? e un processore impiega per eseguire un programma un tempo T, un sistema formato da P processori dello stesso tipo esegue lo stesso programma in un tempo TP T / P? In
Più processori uguale più velocità? e un processore impiega per eseguire un programma un tempo T, un sistema formato da P processori dello stesso tipo esegue lo stesso programma in un tempo TP T / P? In
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
Campione sciolto in un solvente (deuterato) e. posto in un tubo. di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm
 posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
Si classifica come una grandezza intensiva
 CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
Corso acceleratori per la produzione di radioisotopi: Progetto impianto produzione radioisotopi
 Corso acceleratori per la produzione di radioisotopi: Progetto impianto produzione radioisotopi Gabriele Chiodini Istituto Nazionale di Fisica Nucleare di Lecce! Progetto di ricerca e formazione Rif. PON01_03054
Corso acceleratori per la produzione di radioisotopi: Progetto impianto produzione radioisotopi Gabriele Chiodini Istituto Nazionale di Fisica Nucleare di Lecce! Progetto di ricerca e formazione Rif. PON01_03054
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Grandezze fisiche e loro misura
 Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e caratterizzati da entità o grandezze misurabili.
Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e caratterizzati da entità o grandezze misurabili.
Radon. un problema per la salute negli ambienti confinati. Centro Regionale per le Radiazioni Ionizzanti e non Ionizzanti
 Radon un problema per la salute negli ambienti confinati Centro Regionale per le Radiazioni Ionizzanti e non Ionizzanti 1 ARPA PIEMONTE Agenzia Regionale per la Protezione Ambientale del Piemonte Realizzazione
Radon un problema per la salute negli ambienti confinati Centro Regionale per le Radiazioni Ionizzanti e non Ionizzanti 1 ARPA PIEMONTE Agenzia Regionale per la Protezione Ambientale del Piemonte Realizzazione
RIVELAZIONE DELLE RADIAZIONI IONIZZANTI. Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse:
 RIVELAZIONE DELLE RADIAZIONI IONIZZANTI Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse: -Fluenza di particelle -Fluenza di energia -Informazioni
RIVELAZIONE DELLE RADIAZIONI IONIZZANTI Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse: -Fluenza di particelle -Fluenza di energia -Informazioni
Il concetto di valore medio in generale
 Il concetto di valore medio in generale Nella statistica descrittiva si distinguono solitamente due tipi di medie: - le medie analitiche, che soddisfano ad una condizione di invarianza e si calcolano tenendo
Il concetto di valore medio in generale Nella statistica descrittiva si distinguono solitamente due tipi di medie: - le medie analitiche, che soddisfano ad una condizione di invarianza e si calcolano tenendo
Economia Applicata ai sistemi produttivi. 06.05.05 Lezione II Maria Luisa Venuta 1
 Economia Applicata ai sistemi produttivi 06.05.05 Lezione II Maria Luisa Venuta 1 Schema della lezione di oggi Argomento della lezione: il comportamento del consumatore. Gli economisti assumono che il
Economia Applicata ai sistemi produttivi 06.05.05 Lezione II Maria Luisa Venuta 1 Schema della lezione di oggi Argomento della lezione: il comportamento del consumatore. Gli economisti assumono che il
LE FUNZIONI A DUE VARIABILI
 Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
1. Distribuzioni campionarie
 Università degli Studi di Basilicata Facoltà di Economia Corso di Laurea in Economia Aziendale - a.a. 2012/2013 lezioni di statistica del 3 e 6 giugno 2013 - di Massimo Cristallo - 1. Distribuzioni campionarie
Università degli Studi di Basilicata Facoltà di Economia Corso di Laurea in Economia Aziendale - a.a. 2012/2013 lezioni di statistica del 3 e 6 giugno 2013 - di Massimo Cristallo - 1. Distribuzioni campionarie
SISTEMA BINARIO DI DUE LIQUIDI VOLATILI TOTALMENTE MISCIBILI che seguono Raoult
 SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
La corrente elettrica
 PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
PROGRAMMA OPERATIVO NAZIONALE Fondo Sociale Europeo "Competenze per lo Sviluppo" Obiettivo C-Azione C1: Dall esperienza alla legge: la Fisica in Laboratorio La corrente elettrica Sommario 1) Corrente elettrica
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
V= R*I. LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro.
 LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
COMPONENTI TERMODINAMICI APERTI
 CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
Lunedì 20 dicembre 2010. Docente del corso: prof. V. Maiorino
 Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
IL NUCLEO ATOMICO E LA MOLE
 IL NUCLEO ATOMICO E LA MOLE Gli atomi sono costituiti da un nucleo, formato da protoni (carica elettrica positiva, massa 1,6724 x 10-24 g) e neutroni (nessuna carica elettrica, massa 1,6745 x 10-24 g),
IL NUCLEO ATOMICO E LA MOLE Gli atomi sono costituiti da un nucleo, formato da protoni (carica elettrica positiva, massa 1,6724 x 10-24 g) e neutroni (nessuna carica elettrica, massa 1,6745 x 10-24 g),
Radioattività e dosimetria
 Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose.
 Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
IL SOLE. Il Sole è una stella cioè un corpo che emette luce ed energia ed è formato da gas, principalmente idrogeno (74%) ed elio (24%)
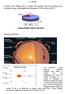 IL SOLE Il Sole è una stella cioè un corpo che emette luce ed energia ed è formato da gas, principalmente idrogeno (74%) ed elio (24%) Struttura del Sole 0 - nel NUCLEO viene prodotta l energia emessa
IL SOLE Il Sole è una stella cioè un corpo che emette luce ed energia ed è formato da gas, principalmente idrogeno (74%) ed elio (24%) Struttura del Sole 0 - nel NUCLEO viene prodotta l energia emessa
CONDUTTORI, CAPACITA' E DIELETTRICI
 CONDUTTORI, CAPACITA' E DIELETTRICI Capacità di un conduttore isolato Se trasferiamo una carica elettrica su di un conduttore isolato questa si distribuisce sulla superficie in modo che il conduttore sia
CONDUTTORI, CAPACITA' E DIELETTRICI Capacità di un conduttore isolato Se trasferiamo una carica elettrica su di un conduttore isolato questa si distribuisce sulla superficie in modo che il conduttore sia
Q 1 = +3 10-5 C carica numero 1 Q 2 = +4 10-5 C carica numero 2 forza esercitata tra le cariche distanza tra le cariche, incognita
 Problema n 1 A quale distanza, una dall'altra bisogna porre nel vuoto due cariche (Q 1 =3 10-5 C e Q 2 =4 10-5 C) perché esse esercitino una sull'altra la forza di 200 N? Q 1 = +3 10-5 C carica numero
Problema n 1 A quale distanza, una dall'altra bisogna porre nel vuoto due cariche (Q 1 =3 10-5 C e Q 2 =4 10-5 C) perché esse esercitino una sull'altra la forza di 200 N? Q 1 = +3 10-5 C carica numero
Elettrostatica dei mezzi materiali
 Elettrostatica dei mezzi materiali Nel caso dei conduttori si è visto che: Il campo elettrico farà muovere le cariche all interno del conduttore in modo tale che: Tutte le cariche sono sulla superficie
Elettrostatica dei mezzi materiali Nel caso dei conduttori si è visto che: Il campo elettrico farà muovere le cariche all interno del conduttore in modo tale che: Tutte le cariche sono sulla superficie
P.Volpe. Dip. Chim. Generale e Organica Applicata. Università di Torino
 P.Volpe. Dip. Chim. Generale e Organica Applicata. Università di Torino Dalla tabella si può vedere come la catena dell uranio è divisa in due dal Rn-222 e come nella parte che lo precede la radioattività
P.Volpe. Dip. Chim. Generale e Organica Applicata. Università di Torino Dalla tabella si può vedere come la catena dell uranio è divisa in due dal Rn-222 e come nella parte che lo precede la radioattività
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
Da Newton a Planck. La struttura dell atomo. Da Newton a Planck. Da Newton a Planck. Meccanica classica (Newton): insieme
 Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
RIASSUNTO DI FISICA 3 a LICEO
 RIASSUNTO DI FISICA 3 a LICEO ELETTROLOGIA 1) CONCETTI FONDAMENTALI Cariche elettriche: cariche elettriche dello stesso segno si respingono e cariche elettriche di segno opposto si attraggono. Conduttore:
RIASSUNTO DI FISICA 3 a LICEO ELETTROLOGIA 1) CONCETTI FONDAMENTALI Cariche elettriche: cariche elettriche dello stesso segno si respingono e cariche elettriche di segno opposto si attraggono. Conduttore:
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
Il fotone. Emanuele Pugliese, Lorenzo Santi URDF Udine
 Il fotone Emanuele Pugliese, Lorenzo Santi URDF Udine Interpretazione di Einstein dell effetto fotoelettrico Esistono «particelle»* di luce: i fotoni! La luce è composta da quantità indivisibili di energia
Il fotone Emanuele Pugliese, Lorenzo Santi URDF Udine Interpretazione di Einstein dell effetto fotoelettrico Esistono «particelle»* di luce: i fotoni! La luce è composta da quantità indivisibili di energia
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
ELETTROSTATICA + Carica Elettrica + Campi Elettrici + Legge di Gauss + Potenziale Elettrico + Capacita Elettrica
 ELETTROSTATICA + Carica Elettrica + Campi Elettrici + Legge di Gauss + Potenziale Elettrico + Capacita Elettrica ELETTRODINAMICA + Correnti + Campi Magnetici + Induzione e Induttanza + Equazioni di Maxwell
ELETTROSTATICA + Carica Elettrica + Campi Elettrici + Legge di Gauss + Potenziale Elettrico + Capacita Elettrica ELETTRODINAMICA + Correnti + Campi Magnetici + Induzione e Induttanza + Equazioni di Maxwell
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
LA MATERIA MATERIA. COMPOSIZIONE (struttura) Atomi che la compongono
 LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
ENERGIA NELLE REAZIONI CHIMICHE
 ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
Fondamenti e didattica delle scienze
 Fondamenti e didattica delle scienze Energia Daniela Allasia Andrea De Bortoli CORSI SPECIALI - Indirizzo Scuola Primaria 73 L energia e le sue proprietà L energia e le sue proprietà La parola energia
Fondamenti e didattica delle scienze Energia Daniela Allasia Andrea De Bortoli CORSI SPECIALI - Indirizzo Scuola Primaria 73 L energia e le sue proprietà L energia e le sue proprietà La parola energia
Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014. Prof.ssa Piacentini Veronica
 Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014 Prof.ssa Piacentini Veronica La corrente elettrica La corrente elettrica è un flusso di elettroni
Classe 3 D Bucci Arianna Evangelista Andrea Palombo Leonardo Ricci Alessia Progetto di Scienze a.s. 2013/2014 Prof.ssa Piacentini Veronica La corrente elettrica La corrente elettrica è un flusso di elettroni
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Indice. Bibliografia... 23
 Indice 1 Legge del decadimento radioattivo......................... 1 1.1 I fenomeni radioattivi.................................... 1 1.2 La legge esponenziale del decadimento radioattivo........... 4
Indice 1 Legge del decadimento radioattivo......................... 1 1.1 I fenomeni radioattivi.................................... 1 1.2 La legge esponenziale del decadimento radioattivo........... 4
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
SENSORI E TRASDUTTORI
 SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
Corrente elettrica. Esempio LA CORRENTE ELETTRICA CONTINUA. Cos è la corrente elettrica? Definizione di intensità di corrente elettrica
 Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
La distribuzione Normale. La distribuzione Normale
 La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
IL CAMPO MAGNETICO. V Scientifico Prof.ssa Delfino M. G.
 IL CAMPO MAGNETICO V Scientifico Prof.ssa Delfino M. G. UNITÀ - IL CAMPO MAGNETICO 1. Fenomeni magnetici 2. Calcolo del campo magnetico 3. Forze su conduttori percorsi da corrente 4. La forza di Lorentz
IL CAMPO MAGNETICO V Scientifico Prof.ssa Delfino M. G. UNITÀ - IL CAMPO MAGNETICO 1. Fenomeni magnetici 2. Calcolo del campo magnetico 3. Forze su conduttori percorsi da corrente 4. La forza di Lorentz
Complementi di Termologia. I parte
 Prof. Michele Giugliano (Dicembre 2) Complementi di Termologia. I parte N.. - Calorimetria. Il calore è una forma di energia, quindi la sua unità di misura, nel sistema SI, è il joule (J), tuttavia si
Prof. Michele Giugliano (Dicembre 2) Complementi di Termologia. I parte N.. - Calorimetria. Il calore è una forma di energia, quindi la sua unità di misura, nel sistema SI, è il joule (J), tuttavia si
Inizia presentazione
 Inizia presentazione Che si misura in ampère può essere generata In simboli A da pile dal movimento di spire conduttrici all interno di campi magnetici come per esempio nelle dinamo e negli alternatori
Inizia presentazione Che si misura in ampère può essere generata In simboli A da pile dal movimento di spire conduttrici all interno di campi magnetici come per esempio nelle dinamo e negli alternatori
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
Dai colori alle stelle: un excursus tra Fisica e Ottica
 Dai colori alle stelle: un excursus tra Fisica e Ottica Martina Giordani Facoltà di Scienze matematiche, fisiche e naturali Corso di Laurea in Ottica e Optometria Federica Ricci Facoltà di Scienze matematiche,
Dai colori alle stelle: un excursus tra Fisica e Ottica Martina Giordani Facoltà di Scienze matematiche, fisiche e naturali Corso di Laurea in Ottica e Optometria Federica Ricci Facoltà di Scienze matematiche,
MISURE DI POTERE CALORIFICO E COMPOSIZIONE
 MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
Na (T 1/2 =15 h), che a sua volta decade β - in 24 12
 Esercizio 1 Il 24 10 Ne (T 1/2 =3.38 min) decade β - in 24 11 Na (T 1/2 =15 h), che a sua volta decade β - in 24 12 Mg. Dire quali livelli sono raggiungibili dal decadimento beta e indicare lo schema di
Esercizio 1 Il 24 10 Ne (T 1/2 =3.38 min) decade β - in 24 11 Na (T 1/2 =15 h), che a sua volta decade β - in 24 12 Mg. Dire quali livelli sono raggiungibili dal decadimento beta e indicare lo schema di
