L ATOMO. Risponde (o almeno ci prova)
|
|
|
- Faustina Giuseppe
- 10 anni fa
- Просмотров:
Транскрипт
1 L ATOMO Di cosa sono fatte le cose? Come si è arrivati a capire gli atomi? Com è fatto un atomo? Quanto è grande un atomo? Che atomi esistono in natura? Perché esistono gli atomi? Risponde (o almeno ci prova) Paolo Montagna Ricercatore in Fisica Nucleare all Università di Pavia Docente di Fisica Medica e Radioattività nei corsi di laurea delle Professioni Sanitarie Tecniche pag.1
2 Di che cosa sono fatte le cose? Lo scienziato indaga osservando la realtà con una particolare lente di ingrandimento : dal complesso al semplice Ad es. tutti gli edifici sono fatti di mattoni, ferro, legno, cemento, sabbia, acqua Ma di cosa sono fatti i mattoni, il ferro, il legno, il cemento, la sabbia, l acqua? pag.2
3 L antica storia dell atomo I filosofi greci nel VI-V secolo a.c. fanno le prime ipotesi sulla struttura della materia. Secondo Empedocle, tutte le cose sono composte da 4 elementi: terra, acqua, aria e fuoco. Secondo Democrito, suddividendo la materia in pezzettini sempre più piccoli, prima o poi si deve arrivare ad una particella fondamentale e indivisibile (altrimenti, se si potesse dividere sempre più fino all infinito, le cose si dissolverebbero nel nulla). in greco: à-tomos Anche se questa ipotesi (2300 anni dopo!) si è rivelata sbagliata, contiene un idea esatta fondamentale: per tutte le cose, la struttura più interna della materia è IDENTICA!!! pag.3
4 Diversi atomi per diverse sostanze Lo studio della struttura della materia riprende solo agli inizi del XIX secolo. Si è ormai affermato il metodo sperimentale di Galileo: sono gli esperimenti a condurre alle teorie, non viceversa! Teoria atomica di Dalton-Avogadro La materia è formata da atomi indivisibili e indistruttibili I diversi elementi hanno atomi diversi tra loro e con masse diverse I composti sono sostanze pure formate da due o più atomi diversi che si combinano in molecole secondo un rapporto definito Le reazioni chimiche avvengono tra molecole e non tra atomi pag.4
5 Le proprietà chimiche si ripetono periodicamente! Mendeleev 1869: tutte le sostanze possono essere descritte in termini di diverse composizioni di solo poco più di 100 atomi (lui ne conosceva 63, ma ne prevedeva altri poi scoperti), suddivisi in modo che a intervalli regolari (periodici) si presentano elementi con uguali proprietà chimiche! pag.5
6 Le cariche elettriche e la divisione dell atomo Thomson 1897: i raggi catodici sono costituiti da una particella di carica negativa e massa 2000 volte minore della massa dell atomo di idrogeno: l elettrone. Tubo catodico La materia è elettricamente neutra. Da dove viene l elettrone? L elettrone deve essere contenuto all interno dell atomo. Ma allora nell atomo devono esistere anche delle cariche positive in modo che l atomo nel suo complesso sia neutro! L atomo non è indivisibile: è stato diviso! Modello atomico di Thomson: Un panettone di carica positiva che contiene gli elettroni come uvetta e canditi!. Ma è giusto? Bisogna verificare sperimentalmente pag.6
7 Il nucleo atomico e gli elettroni orbitali Esperimento di Rutherford (1911): bombardando con particelle alfa (massa dell elio, 4 volte l idrogeno) una lamina d oro, si osserva che in alcuni casi (1 su 20000) le particelle vengono deflesse all indietro, come se rimbalzassero, mentre quasi sempre proseguono in avanti. L atomo di Thomson è sbagliato! Modello planetario di Rutherford: L atomo non è omogeneo: ha un nucleo centrale a carica positiva attorno al quale orbitano gli elettroni attirati dalla forza elettromagnetica pag.7
8 Il protone e il neutrone Rutherford 1919: scoperta del protone particella a carica positiva e massa 1836 volte superiore all elettrone Modello finale dell atomo di Rutherford: Gli atomi hanno tanti protoni nel nucleo quanti elettroni nelle orbite, in modo che le cariche elettriche positive e negative si compensano. Atomi di elementi diversi hanno diverso numero di protoni e elettroni. Capito tutto? Ancora no! L analisi sperimentale dice che: gli atomi hanno masse doppie o anche più di quel che dovrebbero in base al numero dei protoni i protoni dovrebbero respingersi fortemente per la forza elettromagnetica Ipotesi: nel nucleo c è anche un altra particella, neutra e pesante come il protone, e un altra forza attrattiva, più forte della repulsione elettrica! Chadwick 1932: scoperta del neutrone pag.8
9 Entriamo nell atomo L atomo quindi è un piccolissimo sistema planetario. Ma quanto è piccolo? Ci serve - ahimé la matematica! Per raggiungere l infinitamente grande e l infinitamente piccolo bisogna saper utilizzare bene le potenze di 10 Per capirlo meglio, facciamo un viaggio prima verso l infinitamente grande e poi verso l infinitamente piccolo grazie alla mia assistente Mah, il mio papà sarà anche un fisico ma non sa nemmeno scaricare un filmato da YouTube!! pag.9
10 Com è fatto un atomo: masse e dimensioni Z protoni m p = kg carica positiva N neutroni m n = kg carica nulla Z elettroni m e = kg carica negativa R nucleo cm R atomo 10-8 cm il nucleo è volte più piccolo dell atomo! Se l atomo fosse uno stadio di calcio, il nucleo sarebbe il pallone!!! l elettrone è 2000 volte più leggero del protone e del neutrone, che invece sono quasi uguali tra loro! pag.10
11 Atomi, nuclei, particelle: le loro dimensioni pag.11
12 Numero atomico e peso atomico atomi 92 elementi naturali, da idrogeno a uranio nucleo (protoni, neutroni) + elettroni dimensioni : raggio 10 8 cm = cm Z = numero atomico A = numero di massa N = numero di neutroni Peso atomico : Numero di massa: A = Z + N Notazione: A Z X 1 unità di massa atomica (u.m.a.) = 1 dalton = g = g (circa uguale al peso dell atomo di idrogeno: Z=1) pag.12
13 Elementi chimici Elementi chimici: atomi con diverso Z naturali: da idrogeno (Z=1) a uranio (Z=92) artificiali: tecnezio (Z=43) e transuranici (Z>92) pag.13
14 Gli isotopi e la valle dei nuclei Isotopi: stesso n.protoni Z diverso n.neutroni N (stessa specie chimica, diversa massa) N stabili radioattivi (naturali e artificiali) Stabilità dei nuclei: Nuclei leggeri (Z 20) N = Z Nuclei pesanti (Z > 20) N > Z come si spiega? Z pag.14
15 Abbondanza isotopica isotopi = elementi con stesso Z e diverso N elemento isotopi Z A N=A Z abbondanza relativa (%) carbonio ossigeno potassio piombo 12 C 13 C 14 C 16 O 17 O 18 O 39 K 40 K 41 K 204 Pb 206 Pb 207 Pb 208 Pb tracce peso atomico pag.15
16 Ma i protoni non si respingono? Nel nucleo ci sono Z protoni molto vicini tra loro (d m). Essi risentono delle forze di: attrazione gravitazionale - 0, N repulsione elettrostatica N (un miliardo di miliardi di miliardi di miliardi di volte più forte!)?!? F E F G F G P P F E In base alle forze che conosciamo (gravitazionale ed elettromagnetica) i protoni dovrebbero respingersi violentemente e quindi distruggere o impedire la formazione dei nuclei atomici. A MENO CHE pag.16
17 La colla nucleare A MENO CHE All interno dei nuclei atomici si manifesti una ulteriore nuova forza di attrazione, capace di incollare tra loro i protoni vincendo la loro repulsione coulombiana. Per tenere uniti i protoni sono necessari anche i neutroni! FORZA NUCLEARE FORTE: E sempre attrattiva Si manifesta solo a distanze d m Vale tra protoni, tra neutroni, tra protoni e neutroni... ma ancora non basta a spiegare come sono fatti i nuclei... pag.17
18 Guardando i nuclei leggeri... si vede che quando ci sono troppi o pochi neutroni il nucleo non è stabile Idrogeno: Z=1 Elio: Z=2 1 1 H 2 1 H 3 1 H Deuterio Trizio instabile! 2 2 He 3 2 He 4 2 He non esiste! He 5 2 instabile! La forza nucleare non basta ancora: ci deve essere un altra forza responsabile dei decadimenti nucleari FORZA NUCLEARE DEBOLE pag.18
19 Ma quanti neutroni ci vogliono nel nucleo? Né troppi, né troppo pochi! N Z La forza nucleare p-p, p-n, n-n è uguale. Quindi aggiungendo neutroni, il nucleo dovrebbe essere sempre più stabile perché la forza forte vince sempre di più la repulsione elettrica. Invece si verifica che gli isotopi naturali hanno un numero di neutroni al massimo pari a una volta e mezza quello dei protoni. Altri nuclei non esistono, o se prodotti decadono spontaneamente dopo un certo tempo, emettendo particelle, o trasformandosi in altre specie, o spezzandosi in nuclei più piccoli. RADIOATTIVITA pag.19
20 Le 4 forze fondamentali della natura In natura esistono 4 forze fondamentali: Le prime 2 governano il mondo macroscopico (dall atomo in su) perché agiscono anche a grandissime distanze 1) Gravitazionale Intensità = ) Elettromagnetica Intensità 10-2 =0.01 Le altre 2 governano il mondo microscopico (subatomico) perché agiscono solo a distanze di m = m 3) Nucleare forte Intensità 1 4) Nucleare debole Intensità = ne parliamo magari l anno prossimo.. Grazie a tutti! Ciao!!! pag.20
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
Capitolo 7 Le particelle dell atomo
 Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone
 Unità n 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Unità n 7 Le particelle dell atomo 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le particelle fondamentali dell atomo 4. La scoperta dell elettrone 5. L esperimento
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
MODELLI ATOMICI. Dai primi modelli alla teoria moderna
 MODELLI ATOMICI Dai primi modelli alla teoria moderna Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole,
MODELLI ATOMICI Dai primi modelli alla teoria moderna Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole,
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI
 Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail [email protected] [email protected]
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail [email protected] [email protected]
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER:
 ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
Lunedì 20 dicembre 2010. Docente del corso: prof. V. Maiorino
 Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
La radioattività e la datazione al radio-carbonio
 1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi)
 Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi) Il presente documento schematizza le principali particelle sub atomiche. Lo scopo di questa dispensa è fornire una schematizzazione sintetica
Atomo: Particelle sub atomiche (appunti prof. Paolo Marchesi) Il presente documento schematizza le principali particelle sub atomiche. Lo scopo di questa dispensa è fornire una schematizzazione sintetica
RIASSUNTO DI FISICA 3 a LICEO
 RIASSUNTO DI FISICA 3 a LICEO ELETTROLOGIA 1) CONCETTI FONDAMENTALI Cariche elettriche: cariche elettriche dello stesso segno si respingono e cariche elettriche di segno opposto si attraggono. Conduttore:
RIASSUNTO DI FISICA 3 a LICEO ELETTROLOGIA 1) CONCETTI FONDAMENTALI Cariche elettriche: cariche elettriche dello stesso segno si respingono e cariche elettriche di segno opposto si attraggono. Conduttore:
Tesina di scienze. L Elettricità. Le forze elettriche
 Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
10) Se ad una soluzione aumentiamo la temperatura cosa succede? Dire quale delle seguenti affermazioni è corretta.
 Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: [email protected] - www.agora.lesina.org
Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: [email protected] - www.agora.lesina.org
RADIAZIONI RADIAZIONI IONIZZANTI RADIAZIONI IONIZZANTI
 RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
4 3 4 = 4 x 10 2 + 3 x 10 1 + 4 x 10 0 aaa 10 2 10 1 10 0
 Rappresentazione dei numeri I numeri che siamo abituati ad utilizzare sono espressi utilizzando il sistema di numerazione decimale, che si chiama così perché utilizza 0 cifre (0,,2,3,4,5,6,7,8,9). Si dice
Rappresentazione dei numeri I numeri che siamo abituati ad utilizzare sono espressi utilizzando il sistema di numerazione decimale, che si chiama così perché utilizza 0 cifre (0,,2,3,4,5,6,7,8,9). Si dice
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
PARTICELLE SUBATOMICHE
 MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
MODELLI ATOMICI Il cammino per arrivare alla moderna teoria atomica è stato lungo e complesso: ogni nuova scoperta faceva venire alla luce anche nuovi problemi, che dovevano essere affrontati e risolti;
April 11, 2011. Fisica Nucleare. Monica Sambo. Sommario. Introduzione. Radioattivitá. Fisica del nucleo. Bibliografia. Esempio. Raggi emessi Esempio
 April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
I NUMERI DECIMALI. che cosa sono, come si rappresentano
 I NUMERI DECIMALI che cosa sono, come si rappresentano NUMERI NATURALI per contare bastano i numeri naturali N i numeri naturali cominciano con il numero uno e vanno avanti con la regola del +1 fino all
I NUMERI DECIMALI che cosa sono, come si rappresentano NUMERI NATURALI per contare bastano i numeri naturali N i numeri naturali cominciano con il numero uno e vanno avanti con la regola del +1 fino all
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
Elettrostatica dei mezzi materiali
 Elettrostatica dei mezzi materiali Nel caso dei conduttori si è visto che: Il campo elettrico farà muovere le cariche all interno del conduttore in modo tale che: Tutte le cariche sono sulla superficie
Elettrostatica dei mezzi materiali Nel caso dei conduttori si è visto che: Il campo elettrico farà muovere le cariche all interno del conduttore in modo tale che: Tutte le cariche sono sulla superficie
LA LEGGE DI GRAVITAZIONE UNIVERSALE
 GRAVIMETRIA LA LEGGE DI GRAVITAZIONE UNIVERSALE r La legge di gravitazione universale, formulata da Isaac Newton nel 1666 e pubblicata nel 1684, afferma che l'attrazione gravitazionale tra due corpi è
GRAVIMETRIA LA LEGGE DI GRAVITAZIONE UNIVERSALE r La legge di gravitazione universale, formulata da Isaac Newton nel 1666 e pubblicata nel 1684, afferma che l'attrazione gravitazionale tra due corpi è
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Il nucleo degli atomi
 Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
DETERMINAZIONE DELL ALTEZZA DI UN ALBERO NEL CORTILE DELLA SCUOLA
 DETERMINAZIONE DELL ALTEZZA DI UN ALERO NEL CORTILE DELLA SCUOLA Attività 1 Si propone alla classe, divisa in gruppi, un problema e si chiede agli studenti di riflettere e di confrontarsi sulle possibili
DETERMINAZIONE DELL ALTEZZA DI UN ALERO NEL CORTILE DELLA SCUOLA Attività 1 Si propone alla classe, divisa in gruppi, un problema e si chiede agli studenti di riflettere e di confrontarsi sulle possibili
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
Energia potenziale elettrica
 Energia potenziale elettrica La dipendenza dalle coordinate spaziali della forza elettrica è analoga a quella gravitazionale Il lavoro per andare da un punto all'altro è indipendente dal percorso fatto
Energia potenziale elettrica La dipendenza dalle coordinate spaziali della forza elettrica è analoga a quella gravitazionale Il lavoro per andare da un punto all'altro è indipendente dal percorso fatto
IL NUCLEO ATOMICO E L ENERGIA NUCLEARE
 IL NUCLEO ATOMICO E L ENERGIA NUCLEARE Il nucleo atomico Struttura atomica Elementi e isotopi Forze nucleari Decadimento radioattivo Fissione e fusione L energia nucleare Reattori nucleari Centrali nucleari
IL NUCLEO ATOMICO E L ENERGIA NUCLEARE Il nucleo atomico Struttura atomica Elementi e isotopi Forze nucleari Decadimento radioattivo Fissione e fusione L energia nucleare Reattori nucleari Centrali nucleari
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Nascita e morte delle stelle
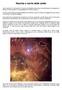 Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Due applicazioni dei logaritmi
 Due applicazioni dei logaritmi 22 febbraio 203 I logaritmi vengono usati per trattare grandezze che presentano ampie variazioni su un intervallo di diversi ordini di grandezze; il ph ne è un esempio. Il
Due applicazioni dei logaritmi 22 febbraio 203 I logaritmi vengono usati per trattare grandezze che presentano ampie variazioni su un intervallo di diversi ordini di grandezze; il ph ne è un esempio. Il
Siamo così arrivati all aritmetica modulare, ma anche a individuare alcuni aspetti di come funziona l aritmetica del calcolatore come vedremo.
 DALLE PESATE ALL ARITMETICA FINITA IN BASE 2 Si è trovato, partendo da un problema concreto, che con la base 2, utilizzando alcune potenze della base, operando con solo addizioni, posso ottenere tutti
DALLE PESATE ALL ARITMETICA FINITA IN BASE 2 Si è trovato, partendo da un problema concreto, che con la base 2, utilizzando alcune potenze della base, operando con solo addizioni, posso ottenere tutti
FISICA. Le forze. Le forze. il testo: 2011/2012 La Semplificazione dei Testi Scolastici per gli Alunni Stranieri IPSIA A.
 01 In questa lezione parliamo delle forze. Parliamo di forza quando: spostiamo una cosa; solleviamo un oggetto; fermiamo una palla mentre giochiamo a calcio; stringiamo una molla. Quando usiamo (applichiamo)
01 In questa lezione parliamo delle forze. Parliamo di forza quando: spostiamo una cosa; solleviamo un oggetto; fermiamo una palla mentre giochiamo a calcio; stringiamo una molla. Quando usiamo (applichiamo)
UNA LEZIONE SUI NUMERI PRIMI: NASCE LA RITABELLA
 UNA LEZIONE SUI NUMERI PRIMI: NASCE LA RITABELLA Tutti gli anni, affrontando l argomento della divisibilità, trovavo utile far lavorare gli alunni sul Crivello di Eratostene. Presentavo ai ragazzi una
UNA LEZIONE SUI NUMERI PRIMI: NASCE LA RITABELLA Tutti gli anni, affrontando l argomento della divisibilità, trovavo utile far lavorare gli alunni sul Crivello di Eratostene. Presentavo ai ragazzi una
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Gli orbitali: modello atomico probabilistico
 1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
1 Approfondimento 2.1 Gli orbitali: modello atomico probabilistico Modello atomico planetario (o a gusci): gli elettroni ruotano intorno al nucleo percorrendo orbite prefissate. Il modello atomico planetario
Esercizio 1 Dato il gioco ({1, 2, 3}, v) con v funzione caratteristica tale che:
 Teoria dei Giochi, Trento, 2004/05 c Fioravante Patrone 1 Teoria dei Giochi Corso di laurea specialistica: Decisioni economiche, impresa e responsabilità sociale, A.A. 2004/05 Soluzioni degli esercizi
Teoria dei Giochi, Trento, 2004/05 c Fioravante Patrone 1 Teoria dei Giochi Corso di laurea specialistica: Decisioni economiche, impresa e responsabilità sociale, A.A. 2004/05 Soluzioni degli esercizi
G3. Asintoti e continuità
 G3 Asintoti e continuità Un asintoto è una retta a cui la funzione si avvicina sempre di più senza mai toccarla Non è la definizione formale, ma sicuramente serve per capire il concetto di asintoto Nei
G3 Asintoti e continuità Un asintoto è una retta a cui la funzione si avvicina sempre di più senza mai toccarla Non è la definizione formale, ma sicuramente serve per capire il concetto di asintoto Nei
1 Gli effetti della forza di Coriolis
 LA FORZA DI CORIOLIS di Giulio Mazzolini 2012 1 Gli effetti della forza di Coriolis È un effetto noto che i venti nell emisfero nord deviano sempre verso destra, invece nell emisfero sud deviano sempre
LA FORZA DI CORIOLIS di Giulio Mazzolini 2012 1 Gli effetti della forza di Coriolis È un effetto noto che i venti nell emisfero nord deviano sempre verso destra, invece nell emisfero sud deviano sempre
Gas perfetti e sue variabili
 Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Corso di fisica generale con elementi di fisica tecnica
 Corso di fisica generale con elementi di fisica tecnica Aniello (Daniele) Mennella Dipartimento di Fisica Secondo modulo Parte prima (fondamenti di elettromagnetismo) Lezione 1 Carica elettrica, legge
Corso di fisica generale con elementi di fisica tecnica Aniello (Daniele) Mennella Dipartimento di Fisica Secondo modulo Parte prima (fondamenti di elettromagnetismo) Lezione 1 Carica elettrica, legge
LA RIVOLUZIONE INDUSTRIALE
 LA RIVOLUZIONE INDUSTRIALE Alla fine del 1700 in Inghilterra c è un grande sviluppo dell industria. Gli inventori costruiscono delle macchine per lavorare il cotone. Le macchine fanno in poco tempo e in
LA RIVOLUZIONE INDUSTRIALE Alla fine del 1700 in Inghilterra c è un grande sviluppo dell industria. Gli inventori costruiscono delle macchine per lavorare il cotone. Le macchine fanno in poco tempo e in
Lezione 14: L energia
 Lezione 4 - pag. Lezione 4: L energia 4.. L apologo di Feynman In questa lezione cominceremo a descrivere la grandezza energia. Per iniziare questo lungo percorso vogliamo citare, quasi parola per parola,
Lezione 4 - pag. Lezione 4: L energia 4.. L apologo di Feynman In questa lezione cominceremo a descrivere la grandezza energia. Per iniziare questo lungo percorso vogliamo citare, quasi parola per parola,
L elettromagnetismo nella ricerca per l energia da fusione nucleare di plasma d idrogeno. R Cesario
 L elettromagnetismo nella ricerca per l energia da fusione nucleare di plasma d idrogeno R Cesario R Cesario I primi tesisti di Roma Tre a Frascati (2005-2006) Sommario del corso integrativo di Progetto
L elettromagnetismo nella ricerca per l energia da fusione nucleare di plasma d idrogeno R Cesario R Cesario I primi tesisti di Roma Tre a Frascati (2005-2006) Sommario del corso integrativo di Progetto
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione
 Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
Esercizi su elettrostatica, magnetismo, circuiti elettrici, interferenza e diffrazione 1. L elettrone ha una massa di 9.1 10-31 kg ed una carica elettrica di -1.6 10-19 C. Ricordando che la forza gravitazionale
Dai primi modelli atomici alla teoria moderna
 Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
f(x) = 1 x. Il dominio di questa funzione è il sottoinsieme proprio di R dato da
 Data una funzione reale f di variabile reale x, definita su un sottoinsieme proprio D f di R (con questo voglio dire che il dominio di f è un sottoinsieme di R che non coincide con tutto R), ci si chiede
Data una funzione reale f di variabile reale x, definita su un sottoinsieme proprio D f di R (con questo voglio dire che il dominio di f è un sottoinsieme di R che non coincide con tutto R), ci si chiede
I modelli atomici da Dalton a Bohr
 1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
Fisica Medica x OPD. Angelo Scribano (ottobre 2006) Le scienze e il metodo scientifico Fisica Medica. A. Scribano 10-06. pag.1
 x OPD Le trasparenze qui presentate sono in gran parte originariamente state create e utilizzate dal prof. Domenico Scannicchio nella sua lunga esperienza didattica in presso l'università di Pavia. Sono
x OPD Le trasparenze qui presentate sono in gran parte originariamente state create e utilizzate dal prof. Domenico Scannicchio nella sua lunga esperienza didattica in presso l'università di Pavia. Sono
INIZIO E FINE DI UNA STELLA. Osservatorio Astronomico di Pedaso
 INIZIO E FINE DI UNA STELLA Osservatorio Astronomico di Pedaso Le stelle nascono dentro al grembo celeste che è la NEBULOSA. La nebulosa è un insieme di gas composto per la maggior parte di IDROGENO, ELIO,
INIZIO E FINE DI UNA STELLA Osservatorio Astronomico di Pedaso Le stelle nascono dentro al grembo celeste che è la NEBULOSA. La nebulosa è un insieme di gas composto per la maggior parte di IDROGENO, ELIO,
1. Limite finito di una funzione in un punto
 . Limite finito di una funzione in un punto Consideriamo la funzione: f ( ) = il cui dominio risulta essere R {}, e quindi il valore di f ( ) non è calcolabile in =. Quest affermazione tuttavia non esaurisce
. Limite finito di una funzione in un punto Consideriamo la funzione: f ( ) = il cui dominio risulta essere R {}, e quindi il valore di f ( ) non è calcolabile in =. Quest affermazione tuttavia non esaurisce
Elettrolisi del solfato di rame
 Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012
 Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
19 Il campo elettrico - 3. Le linee del campo elettrico
 Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Moto di una carica in un campo elettrico uniforme Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice se il campo elettrico è uniforme,
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Elettronica I Grandezze elettriche e unità di misura
 Elettronica I Grandezze elettriche e unità di misura Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: [email protected] http://www.dti.unimi.it/
Elettronica I Grandezze elettriche e unità di misura Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: [email protected] http://www.dti.unimi.it/
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B. Evento prodotto: Evento in cui si verifica sia A che B ; p(a&b) = p(a) x p(b/a)
 Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B Eventi indipendenti: un evento non influenza l altro Eventi disgiunti: il verificarsi di un evento esclude l altro Evento prodotto:
Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B Eventi indipendenti: un evento non influenza l altro Eventi disgiunti: il verificarsi di un evento esclude l altro Evento prodotto:
LEZIONE 23. Esempio 23.1.3. Si consideri la matrice (si veda l Esempio 22.2.5) A = 1 2 2 3 3 0
 LEZIONE 23 231 Diagonalizzazione di matrici Abbiamo visto nella precedente lezione che, in generale, non è immediato che, data una matrice A k n,n con k = R, C, esista sempre una base costituita da suoi
LEZIONE 23 231 Diagonalizzazione di matrici Abbiamo visto nella precedente lezione che, in generale, non è immediato che, data una matrice A k n,n con k = R, C, esista sempre una base costituita da suoi
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.6 ENERGIE DI IONIZZAZIONE E DISTRIBUZIONE DEGLI ELETTRONI 4.C OBIETTIVI
 LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
IL FOTOVOLTAICO E L ARCHITETTURA
 IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2
 INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
I poli magnetici isolati non esistono
 Il campo magnetico Le prime osservazioni dei fenomeni magnetici risalgono all antichità Agli antichi greci era nota la proprietà della magnetite di attirare la limatura di ferro Un ago magnetico libero
Il campo magnetico Le prime osservazioni dei fenomeni magnetici risalgono all antichità Agli antichi greci era nota la proprietà della magnetite di attirare la limatura di ferro Un ago magnetico libero
4. Operazioni aritmetiche con i numeri binari
 I Numeri Binari 4. Operazioni aritmetiche con i numeri binari Contare con i numeri binari Prima di vedere quali operazioni possiamo effettuare con i numeri binari, iniziamo ad imparare a contare in binario:
I Numeri Binari 4. Operazioni aritmetiche con i numeri binari Contare con i numeri binari Prima di vedere quali operazioni possiamo effettuare con i numeri binari, iniziamo ad imparare a contare in binario:
Alessandro Pellegrini
 Esercitazione sulle Rappresentazioni Numeriche Esistono 1 tipi di persone al mondo: quelli che conoscono il codice binario e quelli che non lo conoscono Alessandro Pellegrini Cosa studiare prima Conversione
Esercitazione sulle Rappresentazioni Numeriche Esistono 1 tipi di persone al mondo: quelli che conoscono il codice binario e quelli che non lo conoscono Alessandro Pellegrini Cosa studiare prima Conversione
LA RADIOATTIVITA. Nel caso degli isotopi dell idrogeno: Nel caso degli isotopi del Carbonio:
 LA RADIOATTIVITA Gli atomi di un elemento non sono in realtà tutti uguali, una piccola percentuale di essi ha un numero di neutroni differente, questi atomi si chiamano isotopi di quell elemento. Il 99,9%
LA RADIOATTIVITA Gli atomi di un elemento non sono in realtà tutti uguali, una piccola percentuale di essi ha un numero di neutroni differente, questi atomi si chiamano isotopi di quell elemento. Il 99,9%
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
ENERGIA SOLARE: Centrali fotovoltaiche e termosolari. Istituto Paritario Scuole Pie Napoletane - Anno Scolastico 2012-13 -
 ENERGIA SOLARE: Centrali fotovoltaiche e termosolari L A V E R A N A T U R A D E L L A L U C E La luce, sia naturale sia artificiale, è una forma di energia fondamentale per la nostra esistenza e per quella
ENERGIA SOLARE: Centrali fotovoltaiche e termosolari L A V E R A N A T U R A D E L L A L U C E La luce, sia naturale sia artificiale, è una forma di energia fondamentale per la nostra esistenza e per quella
Energia potenziale elettrica
 Energia potenziale elettrica Simone Alghisi Liceo Scientifico Luzzago Novembre 2013 Simone Alghisi (Liceo Scientifico Luzzago) Energia potenziale elettrica Novembre 2013 1 / 14 Ripasso Quando spingiamo
Energia potenziale elettrica Simone Alghisi Liceo Scientifico Luzzago Novembre 2013 Simone Alghisi (Liceo Scientifico Luzzago) Energia potenziale elettrica Novembre 2013 1 / 14 Ripasso Quando spingiamo
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
Capitolo 25: Lo scambio nel mercato delle assicurazioni
 Capitolo 25: Lo scambio nel mercato delle assicurazioni 25.1: Introduzione In questo capitolo la teoria economica discussa nei capitoli 23 e 24 viene applicata all analisi dello scambio del rischio nel
Capitolo 25: Lo scambio nel mercato delle assicurazioni 25.1: Introduzione In questo capitolo la teoria economica discussa nei capitoli 23 e 24 viene applicata all analisi dello scambio del rischio nel
1. LE GRANDEZZE FISICHE
 1. LE GRANDEZZE FISICHE La fisica (dal greco physis, natura ) è una scienza che ha come scopo guardare, descrivere e tentare di comprendere il mondo che ci circonda. La fisica si propone di descrivere
1. LE GRANDEZZE FISICHE La fisica (dal greco physis, natura ) è una scienza che ha come scopo guardare, descrivere e tentare di comprendere il mondo che ci circonda. La fisica si propone di descrivere
Relazione sull incontro con. Massimo Volante. Esperto del Gruppo Astrofili Di Alessandria
 Relazione sull incontro con Massimo Volante Esperto del Gruppo Astrofili Di Alessandria Il ciclo della vita di una stella (1) Protostella (2b) Nana bruna (2a) Stella (3) Gigante rossa Sono esaurite le
Relazione sull incontro con Massimo Volante Esperto del Gruppo Astrofili Di Alessandria Il ciclo della vita di una stella (1) Protostella (2b) Nana bruna (2a) Stella (3) Gigante rossa Sono esaurite le
LA FORZA. Il movimento: dal come al perché
 LA FORZA Concetto di forza Principi della Dinamica: 1) Principio d inerzia 2) F=ma 3) Principio di azione e reazione Forza gravitazionale e forza peso Accelerazione di gravità Massa, peso, densità pag.1
LA FORZA Concetto di forza Principi della Dinamica: 1) Principio d inerzia 2) F=ma 3) Principio di azione e reazione Forza gravitazionale e forza peso Accelerazione di gravità Massa, peso, densità pag.1
MOTO DI UNA CARICA IN UN CAMPO ELETTRICO UNIFORME
 6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
6. IL CONDNSATOR FNOMNI DI LTTROSTATICA MOTO DI UNA CARICA IN UN CAMPO LTTRICO UNIFORM Il moto di una particella carica in un campo elettrico è in generale molto complesso; il problema risulta più semplice
Moto circolare uniforme
 Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
Successioni ESEMPI: Matematica con Elementi di Statistica, Anna Torre a.a. 2013-2014
 Successioni Vi sono fenomeni naturali e situazioni concrete che presentano sviluppi significativi in tempi discreti. Vale a dire è naturale che i controlli per quei dati fenomeni o per quelle date situazioni
Successioni Vi sono fenomeni naturali e situazioni concrete che presentano sviluppi significativi in tempi discreti. Vale a dire è naturale che i controlli per quei dati fenomeni o per quelle date situazioni
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
A Ferrara, 14 miliardi di anni fa
 A Ferrara, 14 miliardi di anni fa 1 L eredità di Copernico Quale è la relazione fra l uomo e l universo per ciò che riguarda: x : lo spazio t : il tempo m: la materia m t C X 2 Un viaggio nel tempo t di
A Ferrara, 14 miliardi di anni fa 1 L eredità di Copernico Quale è la relazione fra l uomo e l universo per ciò che riguarda: x : lo spazio t : il tempo m: la materia m t C X 2 Un viaggio nel tempo t di
Il principio di induzione e i numeri naturali.
 Il principio di induzione e i numeri naturali. Il principio di induzione è un potente strumento di dimostrazione, al quale si ricorre ogni volta che si debba dimostrare una proprietà in un numero infinito
Il principio di induzione e i numeri naturali. Il principio di induzione è un potente strumento di dimostrazione, al quale si ricorre ogni volta che si debba dimostrare una proprietà in un numero infinito
Ciao! Come fa il Sole a tenere legati i pianeti, gli asteroidi... che pure sono
 Ciao! La volta scorsa abbiamo detto che il Sistema Solare è una sfera. Abbiamo parlato di tutti gli strati che formano questa sfera, li abbiamo descritti all incirca. Adesso parliamo del Sole! Dicono gli
Ciao! La volta scorsa abbiamo detto che il Sistema Solare è una sfera. Abbiamo parlato di tutti gli strati che formano questa sfera, li abbiamo descritti all incirca. Adesso parliamo del Sole! Dicono gli
Il potenziale a distanza r da una carica puntiforme è dato da V = kq/r, quindi è sufficiente calcolare V sx dovuto alla carica a sinistra:
 1. Esercizio Calcolare il potenziale elettrico nel punto A sull asse di simmetria della distribuzione di cariche in figura. Quanto lavoro bisogna spendere per portare una carica da 2 µc dall infinito al
1. Esercizio Calcolare il potenziale elettrico nel punto A sull asse di simmetria della distribuzione di cariche in figura. Quanto lavoro bisogna spendere per portare una carica da 2 µc dall infinito al
Dimensioni Unità di misura. Lezione di fisica
 Dimensioni Unità di misura Lezione di fisica Argomenti della lezione Grandezze fisiche Dimensioni Unità di misura Il sistema internazionale - SI Taratura Le misure La Fisica, dall antico greco φύσις, è
Dimensioni Unità di misura Lezione di fisica Argomenti della lezione Grandezze fisiche Dimensioni Unità di misura Il sistema internazionale - SI Taratura Le misure La Fisica, dall antico greco φύσις, è
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
