SAPERI ESSENZIALI PROGETTO ISOMERI TEST FACOLTA AGRARIA BIOLOGIA
|
|
|
- Romano Di Lorenzo
- 7 anni fa
- Visualizzazioni
Transcript
1 SAPERI ESSENZIALI PROGETTO ISOMERI TEST FACOLTA AGRARIA BIOLOGIA 1) Lo zucchero, componente di un nucleotide, è il: A) maltosio B) ribosio C) glucosio D) fruttosio E) saccarosio 2) In una cellula priva di mitocondri non può svolgersi la: A) sintesi della cellulosa B) respirazione cellulare C) sintesi dell amido D) sintesi della cellulosa E) fotosintesi clorofilliana 3) L ATP è usato dalla cellula come: A) riserva di energia B) trasportatore di elettroni C) riserva di acido fosforico D) pigmento fotosintetico E) proteina di riserva 4) La parete cellulare è: A) interna alla membrana cellulare B) presente solo nelle cellule vegetali C) costituita da un doppio strato di proteine D) costituita da un doppio strato di lipidi E) presente in tutte le cellule eucariotiche 5) Attraverso la riproduzione asessuale si generano organismi geneticamente: A) uguali per il 100% B) uguali per il 75% C) uguali per il 50% D) diversi per il 100% E) diversi per il 75% 6) Le membrane cellulari sono costituite da: A) sostanze pectiche e cellulosa B) proteine e cellulosa C) lipidi ed amido D) amido e cellulosa E) lipidi e proteine 7) La corretta scala di livelli di organizzazione è: A) cellula-tessuto-organo-organulo B) cellula-organulo-tessuto-organo C) organulo-cellula-tessuto-organo D) organo-cellula-tessuto-organulo E) organulo-tessuto-cellula-organo 8) E un polisaccaride vegetale: A) il fruttosio B) il saccarosio C) il glicogeno D) il glucosio E) la cellulosa 9) Il crossing over è lo scambio di: A) informazioni tra due cellule B) soluti attraverso una membrana C) alleli tra cromosomi omologhi
2 D) proteine tra due organuli cellulari E) informazioni tra nucleo e citoplasma 10)In una cellula procariotica sono presenti: A) i mitocondri B) i ribosomi C) il vacuolo D) il nucleo E) i plastidi 11) Il corretto abbinamento (organulo-funzione) è: A) nucleo trasmissione caratteri ereditari B) cloroplasto - sintesi delle proteine C) mitocondrio - sintesi degli zuccheri D) parete cellulare - sintesi della cellulosa E) ribosomi - sintesi dei lipidi 12) In una cellula, le informazioni genetiche sono contenute: A) negli acidi nucleici B) nelle proteine C) nei lipidi D) nei polisaccaridi E) negli amminoacidi 13) Se una cellula con 12 cromosomi si divide per meiosi si ottengono: A) 4 cellule con 6 cromosomi B) 2 cellule con 12 cromosomi C) 2 cellule con 6 cromosomi D) 4 cellule con 12 cromosomi E) 4 cellule con 24 cromosomi 14) Gli organismi appartenenti al regno vegetale sono: A) eucariotici autotrofi B) procariotici autotrofi C) procariotici unicellulari D) procariotici eterotrofi E) eucarioti eterotrofi 15) La reazione 6CO H 2 O = C 6 H 12 O 6 + 6O 2 si svolge: A) nel nucleo B) nei mitocondri C) nei ribosomi D) nella parete cellulare E) nei cloroplasti CHIMICA 16) Il legame covalente si instaura tra: A) atomi di differente elettronegatività B) ioni di carica opposta C) protoni ed elettroni degli atomi nei composti D) atomi che condividono un doppietto di elettroni E) atomi che condividono un doppietto di protoni 17) Il soluto in una soluzione è: A) il componente presente in quantità maggiore B) il componente presente in quantità minore C) un liquido D) un solido E) una miscela di gas 18) La formula H 2 SO 3 corrisponde a: A) acido solforico B) Acido solfidrico C) Acido solforoso
3 D) Acido cloridrico E) Acido nitrico 19) Un aumento di temperatura ha l'effetto di: A) aumentare la velocità di una reazione B) spostare l'equilibrio di reazione verso i prodotti C) diminuire il rendimento di una reazione D) far avvenire reazioni non spontanee E) far avvenire reazioni spontanee 20) Quale dei seguenti composti è un acido?: A) BaCl 2 B) HCl C) NaCl D) Ca(NO 3 ) 2 E) Ca(OH) 2 21) P è il simbolo chimico del: A) potassio B) fluoro C) fosforo D) zolfo E) azoto 22) Un sale si può ottenere da una reazione tra: A) un gas e un acido B) un acido e un liquido C) un metallo ed un ossido D) un acido e una base E) un ossido e una base 23) Quale dei seguenti composti è una base?: A) H 2 SO 4 B) NaCl C) KOH D) CaBr 2 E) HBr 24) Il propano è: A) uno zucchero B) un acido organico C) un idrocarburo D) un alogenuro organico E) un acido 25) Il numero atomico di un atomo è: A) Il numero di neutroni B) Il numero di elettroni C) La somma di protoni e neutroni D) Il diametro E) La carica 26) Il benzene è una molecola: A) aromatica B) acida C) basica D) neutra E) solida
4 27) La formula dell ossido di calcio è: A) CaO B) CO 2 C) NO 2 D) SO 3 E) CaCO 3 28) Una soluzione di NaOH ha un ph: A) Maggiore di 7 B) Minore di 7 C) 7 D) 0 E) 25 29) La molarità di una soluzione rappresenta: A) Numero di moli di soluto sul volume della soluzione in litri B) Numero di equivalenti di soluto sul volume della soluzione in litri C) Peso in grammi di soluto sul volume della soluzione in litri D) Peso in grammi di soluto su 100 grammi di soluzione E) Volume in millilitri su 100 millilitri di soluzione 30) Una soluzione a ph 0.5 è: A) neutra B) acida C) basica D) acquosa E) alcalina FISICA 31) La somma di due vettori può essere effettuata usando la regola: A) del parallelogramma B) del triangolo C) della mano destra D) della mano sinistra E) la regola del cavatappi 32) Come si misura l accelerazione nel sistema di misura SI?: A) m/sec B) m/sec 2 C) km/h D) km/sec E) km/sec 2 33) Se una lampadina da 60W rimane accesa per 180 minuti l energia richiesta è?: A) Wh B) 180 kwh C) J D) 180 J E) 180 kj 34) Per misurare la velocità di un corpo, quale unità di misura si può usare?: A) Km/h B) m/sec 2 C) sec D) m/sec E) g 35) Un vettore è univocamente identificato da: A) una lettera maiuscola B) una freccia C) inclinazione rispetto all orizzontale
5 D) inclinazione rispetto alla verticale E) modulo, direzione e verso 36) Una leva di quarto genere: A) non esiste B) è sempre vantaggiosa C) è vantaggiosa solo se il fulcro si trova tra potenza e resistenza D) è sempre svantaggiosa E) è vantaggiosa solo se il fulcro si trova tra resistenza e potenza 37) Il valore 10-6 equivale a: A) -6x10 B) 0, C) 0, D) 0, E) 6x-10 38) Il risultato del prodotto vettoriale tra due vettori è: A) un numero sempre negativo B) un numero sempre positivo C) un vettore ortogonale ai due vettori D) uno scalare E) un vettore parallelo ai due vettori 39) Il prodotto scalare di due vettori è sempre: A) un vettore parallelo al primo vettore del prodotto B) un vettore ortogonale ai due vettori C) un numero diverso da zero D) un numero E) un numero complesso 40) Un corpo di massa 80g e volume 100 cm 3 immerso in acqua: A) affonda B) galleggia se è piatto C) affonda se è appuntito D) galleggia se è sferico E) galleggia 41) Il coefficiente di attrito statico: A) dipende dalla natura delle superfici a contatto e dalla temperatura B) dipende dall accelerazione di gravità C) dipende dalla massa del corpo D) dipende solo dalla temperatura E) dipende dalla forma del corpo 42) 5x x10 2 è uguale a?: A) 5.5x10 5 B) 5110 C) 55 D) 55x10 3 E) 5,11x ) La sublimazione rappresenta il passaggio di stato da: A) liquido a solido B) liquido a gas C) solido a gas D) gas a liquido E) gas a solido 44) L induzione è un passaggio di stato: A) solo a basse temperature B) solo ad elevate pressioni C) si D) no E) solo nel vuoto
6 45) Se una macchina compie un lavoro di 7200 J in 1 minuto, essa ha una potenza di: A) 7200 W B) 72 W C) 60 kw D) 60 W E) 120 W MATEMATICA 46) L area di un trapezio con base maggiore 6 m, base minore 1 m, altezza 2 m risulta: A) 3 m 2 B) 5 m 2 C) 6 m 2 D) 4 m 2 E) 7 m 2 47) L area di una circonferenza avente diametro 2 m, misura: A) 6.28 m 2 B) 3.14 m 2 C) 1 m 2 D) 2 m 2 E) 0 m 2 48) In un triangolo rettangolo, l ipotenusa misura 5 m e un cateto 4 m. L altro cateto misura: A) 8 m B) 4 m C) 2 m D) 1 m E) 3 m 49) In una circonferenza trigonometrica, l unità di misura dei segmenti è: A) 0 B) il diametro della circonferenza C) il raggio della circonferenza D) 1 cm E) 1 m 50) Un angolo di p/6 radianti corrisponde in gradi a: A) 30 B) 20 C) 40 D) 60 E) 45 51) Il seno di un angolo di 0 risulta: A) -1 B) 0,5 C) +1 D) 0 E) +0,25 52) Il coseno di un angolo di 0 risulta: A) +1 B) 0,5 C) -1 D) 0 E) +0,25 53) La seguente somma è uguale a: A) 5 B) 14 C) 4 D) 6
7 E) 1 54) La potenza (2 3 ) 2 è uguale a: A) 2 5 B) 2 6 C) 2 7 D) 2 12 E) ) Se il log 10 (a) = 1 il valore di a è: A) 0 B) 1 C) 10 D) 100 E) ) Il grado del polinomio 2x 6-5x 2 y 7 + 9x 2 y 6 + 3y 7 risulta: A) 4 B) 2 C) 8 D) 9 E) 7 57) Il prodotto (y + 2x) (y - 2x) è uguale a: A) y 2-4x 2 B) y 2 +4x 2 C) y 2 +8xy+4x 2 D) y 2 -x 2 E) x 2-8xy+4x 2 58) L equazione 2x - 4= 0 è soddisfatta da: A) x=0 B) x=+4 C) x=-4 D) x=+2 E) x=-2 59) L equazione x 2 - x - 6 = 0 è soddisfatta per: A) x 1 = -1 x 2 = +6 B) x 1 = -2 x 2 = -3 C) x 1 = +2 x 2 = -3 D) x 1 = -2 x 2 = +3 E) x 1 = +1 x 2 = -6 60) L equazione ax 2 + bx + c = 0 ammette soluzioni reali distinte quando: A) il discriminante è >0 B) il discriminante è <0 C) il discriminante è =0 D) il discriminante è =1 E) il discriminante non esiste
FAC-SIMILE FACOLTÀ DI AGRARIA TEST DI VALUTAZIONE
 FAC-SIMILE FACOLTÀ DI AGRARIA TEST DI VALUTAZIONE Matematica 1 - Il luogo geometrico dei punti del piano per cui risulta costante la differenza delle distanze da due punti fissi detti fuochi è: a) una
FAC-SIMILE FACOLTÀ DI AGRARIA TEST DI VALUTAZIONE Matematica 1 - Il luogo geometrico dei punti del piano per cui risulta costante la differenza delle distanze da due punti fissi detti fuochi è: a) una
SIMULAZIONE ( ) BIOTECNOLOGIE
 SIMULAZIONE (25.02.2016) BIOTECNOLOGIE 1. La corrispondenza tra le triplette di basi del DNA e gli amminoacidi delle proteine è codificata A) dal codice genetico B) dai geni C) dai ribosomi D) dal genoma
SIMULAZIONE (25.02.2016) BIOTECNOLOGIE 1. La corrispondenza tra le triplette di basi del DNA e gli amminoacidi delle proteine è codificata A) dal codice genetico B) dai geni C) dai ribosomi D) dal genoma
UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali. Biotecnologie. Fascicolo delle Domande
 UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali Prova di Selezione per il Corso di Laurea in Biotecnologie Fascicolo delle Domande Applicare qui il CODICE TEST ATTENZIONE
UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali Prova di Selezione per il Corso di Laurea in Biotecnologie Fascicolo delle Domande Applicare qui il CODICE TEST ATTENZIONE
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali. Biotecnologie. Fascicolo delle Domande
 UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali Prova di Selezione per il Corso di Laurea in Biotecnologie Fascicolo delle Domande Applicare qui il CODICE TEST ATTENZIONE
UNIVERSITÀ DEGLI STUDI DI VERONA Facoltà di Scienze Matematiche Fisiche e Naturali Prova di Selezione per il Corso di Laurea in Biotecnologie Fascicolo delle Domande Applicare qui il CODICE TEST ATTENZIONE
Test di Matematica di base e Logica
 Università degli Studi di Perugia. Facoltà di Scienze MM.FF.NN. Test di Autovalutazione per l accesso al corso di laurea triennale in chimica 1 ottobre 2010 Test di Matematica di base e Logica 1) Un triangolo
Università degli Studi di Perugia. Facoltà di Scienze MM.FF.NN. Test di Autovalutazione per l accesso al corso di laurea triennale in chimica 1 ottobre 2010 Test di Matematica di base e Logica 1) Un triangolo
Olimpiadi di Chimica
 Olimpiadi di Chimica Acqua Oro Zucchero Relazioni di massa nelle reazioni chimiche Massa atomica è la massa di un atomo espressa in unità di massa atomica (uma) Per definizione: 1 atomo 12 C pesa 12 uma
Olimpiadi di Chimica Acqua Oro Zucchero Relazioni di massa nelle reazioni chimiche Massa atomica è la massa di un atomo espressa in unità di massa atomica (uma) Per definizione: 1 atomo 12 C pesa 12 uma
8. Un numero di Avogrado di atomi di carbonio corrisponde a quanti grammi? a) 6 b) 12 c) 24
 1. Un atomo ha numero atomico 12 ed una massa di 24. L atomo consiste di: a) 24 protoni, 24 elettroni, e 12 neutroni. b) 12 protoni, 12 elettroni, e 24 neutroni. c) 12 protoni, 12 elettroni, e 12 neutroni.
1. Un atomo ha numero atomico 12 ed una massa di 24. L atomo consiste di: a) 24 protoni, 24 elettroni, e 12 neutroni. b) 12 protoni, 12 elettroni, e 24 neutroni. c) 12 protoni, 12 elettroni, e 12 neutroni.
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica -
 Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena
 LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena Docente: Francesco Parigi Classe: 2 D Materia: Scienze naturali Origine e storia della biologia. Il metodo scientifico. Caratteristiche degli esseri viventi.
LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena Docente: Francesco Parigi Classe: 2 D Materia: Scienze naturali Origine e storia della biologia. Il metodo scientifico. Caratteristiche degli esseri viventi.
Percorso formativo disciplinare. Disciplina: SCIENZE NATURALI. Anno scolastico 2015/2016 MODULO 1 LA BIOLOGIA E LA SCIENZA DELLA VITA:
 Percorso formativo disciplinare Disciplina: SCIENZE NATURALI CLASSE 2 Cm LICEO CLASSICO Anno scolastico 2015/2016 MODULO 1 LA BIOLOGIA E LA SCIENZA DELLA VITA: U.D. n 1: la Biologia studia gli esseri viventi:
Percorso formativo disciplinare Disciplina: SCIENZE NATURALI CLASSE 2 Cm LICEO CLASSICO Anno scolastico 2015/2016 MODULO 1 LA BIOLOGIA E LA SCIENZA DELLA VITA: U.D. n 1: la Biologia studia gli esseri viventi:
Test di verifica delle conoscenze
 Test di verifica delle conoscenze Stabilire il risultato dell'operazione Stabilire quale delle seguenti relazioni traduce l'affermazione "La differenza tra l'area di un quadrato di lato e l'area di un
Test di verifica delle conoscenze Stabilire il risultato dell'operazione Stabilire quale delle seguenti relazioni traduce l'affermazione "La differenza tra l'area di un quadrato di lato e l'area di un
INDICE DEL BOOK DI BIOLOGIA
 INDICE DEL BOOK DI BIOLOGIA SEZIONE A - STRUTTURA E FUNZIONE DEGLI ECOSISTEMI 1 A.1 - FLUSSO DI ENERGIA 1 A.2 - GLI ORGANISMI AUTOTROFI 5 A.3 - GLI ORGANISMI ETEROTROFI 7 A.4 - LA COMPONENTE BIOTICA E
INDICE DEL BOOK DI BIOLOGIA SEZIONE A - STRUTTURA E FUNZIONE DEGLI ECOSISTEMI 1 A.1 - FLUSSO DI ENERGIA 1 A.2 - GLI ORGANISMI AUTOTROFI 5 A.3 - GLI ORGANISMI ETEROTROFI 7 A.4 - LA COMPONENTE BIOTICA E
LICEO CLASSICO V.POLLIONE FORMIA A.S. 2014/2015 PROGRAMMA DI BIOLOGIA CLASSE V GINNASIO SEZIONE B C E DOCENTE: ORLANDO GIOVANNA
 LICEO CLASSICO V.POLLIONE FORMIA A.S. 2014/2015 PROGRAMMA DI BIOLOGIA CLASSE V GINNASIO SEZIONE B C E DOCENTE: ORLANDO GIOVANNA UNITA 1 LE MOLECOLE DELLA VITA Elementi composti e legami - Tutti gli organismi
LICEO CLASSICO V.POLLIONE FORMIA A.S. 2014/2015 PROGRAMMA DI BIOLOGIA CLASSE V GINNASIO SEZIONE B C E DOCENTE: ORLANDO GIOVANNA UNITA 1 LE MOLECOLE DELLA VITA Elementi composti e legami - Tutti gli organismi
CHIMICA. 1. Tra gli isotopi 39 K, 40 K e 41 K quale ha il numero atomico più alto? A. B. Hanno lo stesso numero atomico C. 40 K D.
 CHIMICA 1. Tra gli isotopi 39 K, 40 K e 41 K quale ha il numero atomico più alto? A. 39 K B. Hanno lo stesso numero atomico C. 40 K D. 41 K 2. Quali particelle compongono il nucleo di un atomo? A. Neutroni
CHIMICA 1. Tra gli isotopi 39 K, 40 K e 41 K quale ha il numero atomico più alto? A. 39 K B. Hanno lo stesso numero atomico C. 40 K D. 41 K 2. Quali particelle compongono il nucleo di un atomo? A. Neutroni
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Phelan- Pignocchino Le scienze naturali Vol.2. Osservare i viventi SOLUZIONI DEGLI ESERCIZI DEL LIBRO. Capitolo B 2. C 3. B 14.
 Phelan, Pignocchino Le scienze naturali Osservare i viventi SOLUZIONI DEGLI ESERCIZI DEL LIBRO Capitolo 1 1. B 3. B 4. D 5. B 6. D 8. asessuata, unicellulari, dominio, sessuata, pluricellulari, regno.
Phelan, Pignocchino Le scienze naturali Osservare i viventi SOLUZIONI DEGLI ESERCIZI DEL LIBRO Capitolo 1 1. B 3. B 4. D 5. B 6. D 8. asessuata, unicellulari, dominio, sessuata, pluricellulari, regno.
I composti organici e i loro polimeri
 I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson
 La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson ORGANISMI FOTOSINTETICI Osservando piante o alghe al microscopio si possono vedere organuli colorati, all'interno dei
La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson ORGANISMI FOTOSINTETICI Osservando piante o alghe al microscopio si possono vedere organuli colorati, all'interno dei
ESERCIZI sulle SOLUZIONI
 ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
PROGRAMMA DI BIOLOGIA. CLASSE 2^ F a. s. 2014 2015. Prof.ssa RUBINO ALESSANDRA
 ISTITUTO TECNICO INDUSTRIALE DI STATO "ENRICO FERMI" Via Luosi n. 23-41124 Modena Tel. 059211092 059236398 - (Fax): 059226478 E-mail: info@fermi.mo.it Pagina web: www.fermi.mo.it PROGRAMMA DI BIOLOGIA
ISTITUTO TECNICO INDUSTRIALE DI STATO "ENRICO FERMI" Via Luosi n. 23-41124 Modena Tel. 059211092 059236398 - (Fax): 059226478 E-mail: info@fermi.mo.it Pagina web: www.fermi.mo.it PROGRAMMA DI BIOLOGIA
Unità fondamentale di tutti gli organismi viventi.
 La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
PERCORSI ABILITANTI SPECIALI CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA
 PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
UNIVERSITA DEGLI STUDI DI PERUGIA Dipartimento di Scienze Farmaceutiche
 UNIVERSITA DEGLI STUDI DI PERUGIA Dipartimento di Scienze Farmaceutiche Corso di Laurea Magistrale a ciclo unico in F A R M A C I A Corso di Laurea Magistrale a ciclo unico in CHIMICA E TECNOLOGIA FARMACEUTICHE
UNIVERSITA DEGLI STUDI DI PERUGIA Dipartimento di Scienze Farmaceutiche Corso di Laurea Magistrale a ciclo unico in F A R M A C I A Corso di Laurea Magistrale a ciclo unico in CHIMICA E TECNOLOGIA FARMACEUTICHE
MURST - PROVA AMMISSIONE 1999 CL IN MEDICINA E CHIRURGIA PROVA DI AMMISSIONE AL CORSO DI LAUREA IN MEDICINA E CHIRURGIA Selezione 1999
 MURST - PROVA AMMISSIONE 1999 CL IN MEDICINA E CHIRURGIA PROVA DI AMMISSIONE AL CORSO DI LAUREA IN MEDICINA E CHIRURGIA Selezione 1999 Test di Chimica 1)Una soluzione acquosa non satura di glucosio rappresenta
MURST - PROVA AMMISSIONE 1999 CL IN MEDICINA E CHIRURGIA PROVA DI AMMISSIONE AL CORSO DI LAUREA IN MEDICINA E CHIRURGIA Selezione 1999 Test di Chimica 1)Una soluzione acquosa non satura di glucosio rappresenta
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Le Reazioni Chimiche
 I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
UNIVERSITÀ DEGLI STUDI DI CATANIA. Test di Verifica
 UNIVERSITÀ DEGLI STUDI DI CATANIA Dipartimento di Agricoltura, Alimentazione e Ambiente (Di3A) A.A. Test di Verifica LOGICO MATEMATICA 1 Quanto vale + 0,08 + 0,12 a. 0,22 b. 0,4 c. Nessuno dei precedenti
UNIVERSITÀ DEGLI STUDI DI CATANIA Dipartimento di Agricoltura, Alimentazione e Ambiente (Di3A) A.A. Test di Verifica LOGICO MATEMATICA 1 Quanto vale + 0,08 + 0,12 a. 0,22 b. 0,4 c. Nessuno dei precedenti
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
LA VITA DIPENDE DALLE PROPRIETA DELL ACQUA I COMPOSTI DEL CARBONIO E LE BIOMOLECOLE I CARBOIDRATI E I LIPIDI:I COMBUSTIBILI DELLE CELLULE
 PROGRAMMA DI BIOLOGIA E CHIMICA ANNO SCOLASTICO 2014/2015 CLASSE 2^E DOCENTE:ASSUNTA ALVITI BIOLOGIA CAPITOLO 3: LA CHIMICA DELLA VITA LA VITA DIPENDE DALLE PROPRIETA DELL ACQUA - La molecola dell acqua
PROGRAMMA DI BIOLOGIA E CHIMICA ANNO SCOLASTICO 2014/2015 CLASSE 2^E DOCENTE:ASSUNTA ALVITI BIOLOGIA CAPITOLO 3: LA CHIMICA DELLA VITA LA VITA DIPENDE DALLE PROPRIETA DELL ACQUA - La molecola dell acqua
Per gli studenti che intendono iscriversi per l anno accademico 2008/09 al Corso di Laurea in Biotecnologie
 Luglio 2008 Per gli studenti che intendono iscriversi per l anno accademico 2008/09 al Corso di Laurea in Biotecnologie Elenco dei quesiti proposti dalla Commissione per la prova di ammissione relativa
Luglio 2008 Per gli studenti che intendono iscriversi per l anno accademico 2008/09 al Corso di Laurea in Biotecnologie Elenco dei quesiti proposti dalla Commissione per la prova di ammissione relativa
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Anno scolastico 2014/2015
 LICEO SCIENTIFICO STATALE GALILEO GALILEI PROGRAMMA SVOLTO Classi: 1 E/1 F Materia: Scienze naturali MODULO I: Geografia astronomica UD 1: il sistema solare: il sole, i pianeti, asteroidi, comete, meteore,
LICEO SCIENTIFICO STATALE GALILEO GALILEI PROGRAMMA SVOLTO Classi: 1 E/1 F Materia: Scienze naturali MODULO I: Geografia astronomica UD 1: il sistema solare: il sole, i pianeti, asteroidi, comete, meteore,
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Test di ingresso per il corso di laurea triennale in Scienze della Natura Conoscenze di base di matematica 22 settembre 2011
 Test di ingresso per il corso di laurea triennale in Scienze della Natura Conoscenze di base di matematica 22 settembre 2011 1. Il massimo comun divisore e il minimo comune multiplo dei numeri 288 e 1350
Test di ingresso per il corso di laurea triennale in Scienze della Natura Conoscenze di base di matematica 22 settembre 2011 1. Il massimo comun divisore e il minimo comune multiplo dei numeri 288 e 1350
DOMANDE A RISPOSTA APERTA 1. Gli organismi interagiscono con il loro ambiente scambiando materia e energia: descrivere come gli organismi vegetali
 DOMANDE A RISPOSTA APERTA 1. Gli organismi interagiscono con il loro ambiente scambiando materia e energia: descrivere come gli organismi vegetali sono in grado di convertire l energia luminosa in energia
DOMANDE A RISPOSTA APERTA 1. Gli organismi interagiscono con il loro ambiente scambiando materia e energia: descrivere come gli organismi vegetali sono in grado di convertire l energia luminosa in energia
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SIMULAZIONE TEST DI CHIMICA
 SIMULAZIONE TEST DI CHIMICA C1) Il numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma del numero di protoni e neutroni d) la differenza tra il numero
SIMULAZIONE TEST DI CHIMICA C1) Il numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma del numero di protoni e neutroni d) la differenza tra il numero
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione. Composti: specie chimiche definite formate da due o più elementi
 Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro
 Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro Trovare una bilancia che possa pesare un atomo è un sogno irrealizzabile. Non potendo determinare
Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro Trovare una bilancia che possa pesare un atomo è un sogno irrealizzabile. Non potendo determinare
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Chimica e laboratorio
 ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
LA CLASSIFICAZIONE DEI COMPOSTI CHIMICI
 LA LASSIFIAZIONE DEI OMPOSTI IMII Inorganici Acqua Sali minerali omposti chimici Idrocarburi arboidrati Organici Alcoli, aldeidi Molecole biologiche o biomolecole Lipidi Proteine Acidi nucleici Vitamine
LA LASSIFIAZIONE DEI OMPOSTI IMII Inorganici Acqua Sali minerali omposti chimici Idrocarburi arboidrati Organici Alcoli, aldeidi Molecole biologiche o biomolecole Lipidi Proteine Acidi nucleici Vitamine
LE MOLECOLE DELLA VITA
 LE MOLECOLE DELLA VITA LE CELLULE SONO COSTITUITE DA ACQUA E BIOMOLECOLE Una biomolecola è un composto chimico che riveste un ruolo importante negli esseri viventi. Le molecole biologiche possono essere
LE MOLECOLE DELLA VITA LE CELLULE SONO COSTITUITE DA ACQUA E BIOMOLECOLE Una biomolecola è un composto chimico che riveste un ruolo importante negli esseri viventi. Le molecole biologiche possono essere
TAVOLA PERIODICA. Lo strumento principe della chimica
 TAVOLA PRIODICA Lo strumento principe della chimica Classificazione degli elementi Problema: ordinare gli elementi secondo un criterio logico e memorizzabile metalli non-metalli solidi (escluso mercurio)
TAVOLA PRIODICA Lo strumento principe della chimica Classificazione degli elementi Problema: ordinare gli elementi secondo un criterio logico e memorizzabile metalli non-metalli solidi (escluso mercurio)
Dopo l invenzione del microscopio è stato possibile scoprire l esistenza delle cellule.
 CELLULA Dopo l invenzione del microscopio è stato possibile scoprire l esistenza delle cellule. 1. La cellula Definizione di cellula 1. È la più piccola parte di un organismo (pluricellulare). 2. Può costituire
CELLULA Dopo l invenzione del microscopio è stato possibile scoprire l esistenza delle cellule. 1. La cellula Definizione di cellula 1. È la più piccola parte di un organismo (pluricellulare). 2. Può costituire
02/12/2014. Tutti gli esseri viventi sono composti da cellule LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI
 Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Anno scolastico 2015/16
 Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
le reazioni chimiche
 le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
Teoria di Lewis. Un acido di Lewis è una specie chimica che può formare un legame covalente accettando una coppia di elettroni da un altra specie.
 Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
Determinare il ph di una soluzione costituita da 100 ml di HCl 0.01 M.
 Come prima cosa bisogna chiarire che cosa succeda in soluzione e quali siano le specie presenti all equilibrio. È inoltre necessario considerare sempre il risultato ottenuto in maniera critica e non accettarlo
Come prima cosa bisogna chiarire che cosa succeda in soluzione e quali siano le specie presenti all equilibrio. È inoltre necessario considerare sempre il risultato ottenuto in maniera critica e non accettarlo
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING
 Largo Zecca, 4-16124 GENOVA Tel. 010/247.07.78 - Fax 010/251.29.60- E-mail geis00600r@istruzione.it C.F. 95062410105 CLASSI PRIME: CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING Grandezze
Largo Zecca, 4-16124 GENOVA Tel. 010/247.07.78 - Fax 010/251.29.60- E-mail geis00600r@istruzione.it C.F. 95062410105 CLASSI PRIME: CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING Grandezze
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Le Reazioni Chimiche
 Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Reazioni chimiche e stechiometria
 Reazioni chimiche e stechiometria REAZIONI CHIMICHE Trasformazione di una o più sostanze (reagenti) in una o più sostanze (prodotti) EQUAZIONE CHIMICA Una equazione chimica è la rappresentazione simbolica
Reazioni chimiche e stechiometria REAZIONI CHIMICHE Trasformazione di una o più sostanze (reagenti) in una o più sostanze (prodotti) EQUAZIONE CHIMICA Una equazione chimica è la rappresentazione simbolica
PRINCIPI NUTRITIVI. I principi nutritivi sono sostanze che si trovano negli alimenti e che hanno particolari funzioni per il nostro organismo.
 PRINCIPI NUTRITIVI I principi nutritivi sono sostanze che si trovano negli alimenti e che hanno particolari funzioni per il nostro organismo. I principi nutritivi sono : 1. I glucidi detti anche carboidrati
PRINCIPI NUTRITIVI I principi nutritivi sono sostanze che si trovano negli alimenti e che hanno particolari funzioni per il nostro organismo. I principi nutritivi sono : 1. I glucidi detti anche carboidrati
La vita e le sue molecole. Il mondo della cellula. Sommario. Nelle risorse digitali. Nelle risorse digitali
 1 La vita e le sue molecole 1. La biologia studia le caratteristiche della vita 2 2. L acqua e le sue proprietà 6 3. I composti del carbonio 11 Competenze in azione 14 4. I carboidrati e i lipidi 15 Competenze
1 La vita e le sue molecole 1. La biologia studia le caratteristiche della vita 2 2. L acqua e le sue proprietà 6 3. I composti del carbonio 11 Competenze in azione 14 4. I carboidrati e i lipidi 15 Competenze
LICEO SCIENTIFICO "FRANCESCO SEVERI" BIOLOGIA
 LICEO SCIENTIFICO "FRANCESCO SEVERI" Programma consuntivo A. S. 2009/2010 Testo utilizzato,volume unico:"invito alla biologia" H.Curtis & N.Sue Barnes Classi 3 A - 3 H - 3 D BIOLOGIA U.D. N 1 COME NACQUE
LICEO SCIENTIFICO "FRANCESCO SEVERI" Programma consuntivo A. S. 2009/2010 Testo utilizzato,volume unico:"invito alla biologia" H.Curtis & N.Sue Barnes Classi 3 A - 3 H - 3 D BIOLOGIA U.D. N 1 COME NACQUE
Esercizi di stechiometria
 Esercizi di stechiometria La reazione globale da bilanciare) per ottenere il carbonato di sodio secondo il processo di Solvay è la seguente: Calcolare quanto cloruro di sodio NaCl) occorre per ottenere
Esercizi di stechiometria La reazione globale da bilanciare) per ottenere il carbonato di sodio secondo il processo di Solvay è la seguente: Calcolare quanto cloruro di sodio NaCl) occorre per ottenere
1) Bilanciare la seguente reazione redox con il metodo ionico-elettronico Ag (s) + H + (aq) + NO 3
 A ) Soluzioni Esercizi I esonero del 29/11/2005 1) Bilanciare la seguente reazione redox con il metodo ionicoelettronico Ag (s) + + (aq) + N 3 (aq) Ag + (aq) + N 2 (g) + 2 (l) Calcolare quanti grammi di
A ) Soluzioni Esercizi I esonero del 29/11/2005 1) Bilanciare la seguente reazione redox con il metodo ionicoelettronico Ag (s) + + (aq) + N 3 (aq) Ag + (aq) + N 2 (g) + 2 (l) Calcolare quanti grammi di
Al Dirigente Scolastico dell I.I.S.. F. Algarotti Venezia PROGRAMMA
 MATERIA: SCIENZE INTEGRATE -SCIENZE DELLA TERRA CLASSE: I E -La Terra come sistema integrato: litosfera, atmosfera, idrosfera, biosfera; esempi di relazioni ed interazioni che tra queste intercorrono -
MATERIA: SCIENZE INTEGRATE -SCIENZE DELLA TERRA CLASSE: I E -La Terra come sistema integrato: litosfera, atmosfera, idrosfera, biosfera; esempi di relazioni ed interazioni che tra queste intercorrono -
ISTITUTO SALESIANO DON BOSCO Villa Ranchibile. LICEO SCIENTIFICO Anno scolastico 2015/2016 PROGRAMMA DI SCIENZE Svolto nella classe II a sez.
 ISTITUTO SALESIANO DON BOSCO Villa Ranchibile Via Libertà, 199 90143 PALERMO LICEO SCIENTIFICO Anno scolastico 2015/2016 PROGRAMMA DI SCIENZE Svolto nella classe II a sez. A Docente: Prof. Rosario Papa
ISTITUTO SALESIANO DON BOSCO Villa Ranchibile Via Libertà, 199 90143 PALERMO LICEO SCIENTIFICO Anno scolastico 2015/2016 PROGRAMMA DI SCIENZE Svolto nella classe II a sez. A Docente: Prof. Rosario Papa
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Angoli e loro misure
 Angoli e loro misure R s Unità di misura: gradi, minuti, secondi 1 o =60' 1'=60'' Es: 35 o 41'1'' radianti α(rad) s R Angolo giro = 360 o = R/R = rad R=1 arco rad Es.: angolo retto R Arco 4 : se R=1 π
Angoli e loro misure R s Unità di misura: gradi, minuti, secondi 1 o =60' 1'=60'' Es: 35 o 41'1'' radianti α(rad) s R Angolo giro = 360 o = R/R = rad R=1 arco rad Es.: angolo retto R Arco 4 : se R=1 π
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
B.U.S.-T.C.S. B. Pascal Reggio Emilia
 Anno Scolastico 2006/2007 Classi 1 e Compiti per le vacanze Materia: Scienze B.U.S.-T.C.S. B. Pascal Reggio Emilia Agli allievi che hanno ottenuto la promozione alla classe seconda senza il debito in Scienze,
Anno Scolastico 2006/2007 Classi 1 e Compiti per le vacanze Materia: Scienze B.U.S.-T.C.S. B. Pascal Reggio Emilia Agli allievi che hanno ottenuto la promozione alla classe seconda senza il debito in Scienze,
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
4 Il 3% di una certa somma ammonta a 6000 euro; allora l ammontare dell intera somma è di euro a) b) c) d) 18000
 1 In un triangolo equilatero a) le bisettrici sono fra loro ortogonali b) le altezze sono anche mediane e bisettrici c) le altezze sono fra loro ortogonali d) uno dei suoi angoli è retto 2 Due triangoli
1 In un triangolo equilatero a) le bisettrici sono fra loro ortogonali b) le altezze sono anche mediane e bisettrici c) le altezze sono fra loro ortogonali d) uno dei suoi angoli è retto 2 Due triangoli
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
A_Test di valutazione di Biologia Generale:
 COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi Iscritti 2011-2012 A_Test di valutazione di Biologia Generale: Il ciclo
COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi Iscritti 2011-2012 A_Test di valutazione di Biologia Generale: Il ciclo
caratteristiche dei viventi
 caratteristiche dei viventi teoria cellulare Teoria cellulare La Teoria Cellulare formulata da Schleiden e Schwann tra il 1838 e il 1839 afferma che Tutti gli organismi viventi sono formati da cellule.
caratteristiche dei viventi teoria cellulare Teoria cellulare La Teoria Cellulare formulata da Schleiden e Schwann tra il 1838 e il 1839 afferma che Tutti gli organismi viventi sono formati da cellule.
8. L insieme delle soluzioni della disequazione x 2 0 è:
 1. Due grandezze sono direttamente proporzionali se a) il loro rapporto è costante b) la loro somma è costante c) il loro prodotto è costante d) la loro differenza è costante 2. Due triangoli sono simili
1. Due grandezze sono direttamente proporzionali se a) il loro rapporto è costante b) la loro somma è costante c) il loro prodotto è costante d) la loro differenza è costante 2. Due triangoli sono simili
Acidi e Basi. Capitolo 15
 Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
2. La chimica della vita Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA
 Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Di cosa è fatta una cellula?
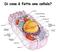 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: I - (aq) + NO 3
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: I (aq) + 3 (aq) + + (aq) I 2(s) + (g) + 2 (l). Calcolare i grammi di I 2 (s) che si ottengono se si formano
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: I (aq) + 3 (aq) + + (aq) I 2(s) + (g) + 2 (l). Calcolare i grammi di I 2 (s) che si ottengono se si formano
La cellula. La cellula.
 La cellula La cellula è l unità biologica elementare che costituisce tutti gli esseri viventi: essa è la più piccola porzione di materia vivente in grado di vivere autonomamente. Ogni cellula, infatti,
La cellula La cellula è l unità biologica elementare che costituisce tutti gli esseri viventi: essa è la più piccola porzione di materia vivente in grado di vivere autonomamente. Ogni cellula, infatti,
CELLULA. La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule.
 LA CELLULA CELLULA La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. CELLULA La teoria cellulare Le cellule furono
LA CELLULA CELLULA La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. CELLULA La teoria cellulare Le cellule furono
- FASE OSCURA (Ciclo di Calvin)
 CAP. 6 Conversione dell Energia: Concetti relativi a fotosintesi, glicolisi, respirazione aerobica, fermentazione, trasportatori di energia, riserve di energia a breve e lungo termine. 6.1 La fotosintesi
CAP. 6 Conversione dell Energia: Concetti relativi a fotosintesi, glicolisi, respirazione aerobica, fermentazione, trasportatori di energia, riserve di energia a breve e lungo termine. 6.1 La fotosintesi
ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE. Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO. a.s.
 ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO a.s. 2O13-2014 Materia : Chimica e Biologia Classe : II sez. E Rimini,05/06/2014
ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO a.s. 2O13-2014 Materia : Chimica e Biologia Classe : II sez. E Rimini,05/06/2014
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena
 LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena Docente: Francesco Parigi Classi: 1 D Materia: Scienze naturali e laboratorio Anno scolastico 2015/2016 PROGRAMMA PREVENTIVO I QUADRIMESTRE MODULO I: Chimica
LICEO SCIENTIFICO STATALE GALILEO GALILEI Siena Docente: Francesco Parigi Classi: 1 D Materia: Scienze naturali e laboratorio Anno scolastico 2015/2016 PROGRAMMA PREVENTIVO I QUADRIMESTRE MODULO I: Chimica
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
