2015 /2016. scaricato da
|
|
|
- Miranda Fabiani
- 6 anni fa
- Visualizzazioni
Transcript
1 Enzimi Prof Spina Riabilitativa 2015 /2016
2
3 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il sito attivo, tutti gli enzimi sono proteine, con l eccezione di molecole di RNA cataliticamente attive, legano con specificità diversa molte molecole di cui promuovono la catalisi fornendo loro il giusto orientamento e stabilizzando lo stato di transizione.
4 Gli enzimi sono catalizzatori molto efficaci. Possono accellerare una reazione di migliaia di volte: L anidrasi carbonica ad esempio porta la velocità di reazione da 1,3 x10-1 sec a 1 x 10 6 sec, con un potenziamento di 7,7 x10 6. Ogni molecola l di E può òid idratare 10 5 CO 2 al secondo
5 La specificità ità di un E è dovuta alla interazione con il substrato; ciò è reso possibile grazie all intricata struttura tridimensionale della p. enzimatica, che garantisce la corretta funzione dell E. Si consideri i che la DNA polimerasi i I introduce un nucleotide sbagliato nella catena meno di 1 volta su
6
7
8
9 Molti E hanno bisogno di cofattori per svolgere la loro attività. Apoenzima + Cofattore = Oloenzima
10 Cofattore Tiamina pirofosfato (B1)... Flavin adenin dinucleotide (B2).. Enzima Piruvato Deidrogenasi Monoamina Ossidasi Nicotinamide id adenin dinucleotide (niacina i NAD)... Lattico Deidrogenasi i Piridossal Fosfato (B6).. Transaminasi Coenzima A (Ac. Pantotenico). Acetil CoA Carbossilasi Biotina Piruvato Carbossilasi Zn2+ Anidrasi Carbonica Mg2+... Esochinasi Mg2+... Ureasi
11 Gli Enzimi convertono l energia da una forma all altra L energia contenuta nei reagenti viene riconvertita con elevata efficienza; ad es. - Nella fotosintesi t i l energia radiante della luce è convertita in energia di un legame attraverso un gradiente ionico; - nei mitocondri l energia libera contenuta nelle molecole dei nutrienti è convertita prima nell energia libera di un gradiente ionico poi in energia libera del legame del Pi nell ATP. - L energia dell ATP può essere usata in molti modi:in lavoro meccanico (contrazione della miosina), movimento (trasporto di ioni o piccole molecole da un comparto all altro -pompe-ioniche)
12 Gli E vengono classificati in base al tipo di reazione che catalizzano Ossidoreduttasi Ossidoriduzione es. LDH. Transferasi transf.di 1gruppo es. NMPchinasi. Idrolasi Reaz. di idrolisi es. Carbossilasi. Liasi Agg. o Rim. di un gruppo es. Fumarasi. Isomerasi Trasferimento intramolecolare es. Ti Trioso PI. Ligasi Unione di 2 substrati a spese di ATP es.aminoacil- transferasi.
13 La specificità ità di un E è dovuta all interazione con il substrato; ciò è reso possibile dall intricata struttura tridimensionale della proteina enzimatica, ciò garantisce il corretto funzionamento dell E, si consideri che la DNA polimerasi i I introduce un nucleotide sbagliato nella catena meno di 1 volta su
14
15
16 L energia libera è la funzione termodinamica + utile per capire gli E. Ricordiamo brevemente che l energia dell universo è costante, (sistema + ambiente= K). L entropia è il grado di ordine, entropia ordine; la variazione di entropia dell ambiente sarà collegato alla quantità di calore trasferita dal sistema. L entalpia è il calore contenuto in un sistema. L energia libera di Gibbs è in relazione alla differenza di entalpia e di entropia del sistema tenendo conto della T.: G = Hsist - T ssistini altre parole una reazione può avvenire spontaneamente solo se la variazione di energia libera è negativa
17 Due proprietà termodinamiche di una reazione sono utili per comprendere il funzionamento degli E. La differenza di energia libera G tra i prodotti P e i reagenti S e L energia richiesta per la conversione dei reagenti nei corrispondenti stati di transizione. La prima determina se una reazione può avvenire spontaneamente, la seconda la velocità con cui avviene.
18 E+S ES EP E+P Equilibrio Chimico e Velocità della Reazione
19 G ++ : energia di attivazione non
20
21
22 Quanto prodotto per unità di tempo è la velocità della reazione
23 LE MIGLIAIA DI REAZIONI CHE AVVENGONO NEGLI ORGANISMI VIVENTI SI VERIFICANO IN CONDIZIONI ESTREMAMENTE BLANDE E AD UNA VELOCITÁ UTILE ALL'ECONOMIA CELLULARE GRAZIE ALL'ATTIVITÁ CATALITICA DI PROTEINE SPECIFICHE: GLI ENZIMI
24 UNA REAZIONE CHIMICA AVVIENE PERCHÈ UNA CERTA FRAZIONE DI MOLECOLE DI REAGENTE(I) POSSIEDE, IN UN DATO ISTANTE, ABBASTANZA ENERGIA PER RAGGIUNGERE UNA CONDIZIONE ATTIVATA, A PIÚ ALTO CONTENUTO ENERGETICO, DETTA STATO DI TRANSIZIONE NE
25
26 IL CATALIZZATORE SI LEGA TRANSITORIAMENTE AL REAGENTE FORMANDO UN COMPLESSO IL CUI STATO DI TRANSIZIONE HA MINOR ENERGIA DI QUELLO DELLA REAZIONE NON CATALIZZATA.
27 IN ANALOGIA CON GLI ALTRI CATALIZZATORI, GLI ENZIMI: 1. ACCELERANO LE REAZIONI 2. ABBASSANO L'ENERGIA DI ATTIVAZIONE 3. NON ALTERANO L'EQUILIBRIO DELLE REAZIONI
28 A DIFFERENZA DEGLI ALTRI CATALIZZATORI, GLI ENZIMI PRESENTANO: 1. UN ENORME POTERE CATALITICO 2. UN'ELEVATA SPECIFICITÁ 3. LA POSSIBILITÁ DI ESSERE REGOLATI
29 LA VELOCITÁ DELLE REAZIONI CATALIZZATE DAGLI ENZIMI È DA 10 3 A VOLTE MAGGIORE DI QUELLA DELLE STESSE REAZIONI IN ASSENZA DI ENZIMA.
30 H 2 O + CO 2 <-----> HCO 3- + H + VELOCITÁ = 1 H + <-----> O CO 2 HCO H ANIDRASI CARBONICA VELOCITÁ = 10 7
31 L'ANIDRASI CARBONICA È UNO DEGLI ENZIMI A PIÙ ELEVATO NUMERO DI TURNOVER : OGNI MOLECOLA PUÒ IDRATARE 6x10 5 MOLECOLE DI CO 2 PER SECONDO
32
33
34
35
36
37 MODELLO CHIAVE-SERRATURA IL SITO ATTIVO DELL'ENZIMA HA UNA FORMA COMPLEMENTARE A QUELLA DEL SUBSTRATO
38
39 MODELLO DI ADATTAMENTO INDOTTO IL SITO ATTIVO ASSUME UNA FORMA COMPLEMENTARE A QUELLA DEL SUBSTRATO SOLO DOPO CHE QUESTO SI È LEGATO
40
41
42 CINETICA ENZIMATICA STUDIA LA VELOCITÁ DELLE REAZIONI ENZIMATICHE.
43 VELOCITÁ E' DEFINITA DAL NUMERO DI MOLI DI PRODOTTO CHE SI FORMANO IN UN SECONDO.
44 VELOCITÁ INIZIALE (V 0 ) LA VELOCITÁ DEVE ESSERE MISURATA A TEMPI BREVI, QUANDO CIOÈ SI È CONSUMATA SOLO UNA PICCOLA PARTE DEL SUBSTRATO.
45
46
47
48 L' equazione di Michaelis-Menten può però essere manipolata per ottenere l' equazione di una retta in cui Vmax e Km siano delle intercette e non più degli asintoti. Uno dei metodi più usati e quello di Lineweaver-Burk che usa la forma reciproca dell' equazione di Michaelis-Menten: Menten: ove le variabili sono 1/v e 1/[S]. 1/Vmax è l' intercetta sull' asse y e -1/Km èl' intercetta sull' asse x.
49 1/Vmax è l' intercetta sull' asse y e -1/Km è l' intercetta sull' asse x.
50 Sia la trasformazione di Lineweaver-Burk che quella di Eadie-Hofstee rendono più semplice e più accurata la determinazione di Vmax e Km e permettono di scoprire se l' enzima stia lavorando secondo una cinetica classica (stato stazionario ed equilibrio rapido). L'uso di trasformazioni lineari dell' equazione di Michaelis- Menten sono inoltre particolarmente utili nello studio degli inibitori reversibili E E E+S ES E+P
51 E+S ES E +P E+S ES E + P
52 Significato pratico della Km. Il valore della Km è importante per varie ragioni: La Km rappresenta approssimativamente il valore della concentrazione intracellulare del substrato. Infatti per [S intracell ] << Km, l' enzima sarebbe estremamente sensibile a variazioni della concentrazione del substrato, ma gran parte del suo potenziale catalitico sarebbe inutilizzato in quanto in queste condizioni v<<vmax. a) Non avrebbe senso dal punto di vista fisiologico neppure che [S intracell ] fosse >> Km, in quanto l' enzima pur lavorando con una velocità vicino alla Vmax,,perderebbe la possibilità di essere regolato da variazioni della concentrazione del substrato.
53 Quindi LA Km PUO ESSERE DEFINITA COME QUEL VALORE DI CONCENTRAZIONE DEL SUBSTRATO A CUI: LA REAZIONE PROCEDE AD UNA VELOCITÁ PARI A METÁ DELLA Vmax
54 L'INIBIZIONE ENZIMATICA È CLASSIFICATA IN DUE TIPI: - IRREVERSIBILE - REVERSIBILE
55 ESEMPIO TIPICO DI INIBITORE IRREVERSIBILE È IL DIISOPROPILFLUOROFOSFATO CHE SI LEGA COVALENTEMENTE CON UN RESIDUO DI Ser DELLE PROTEASI SERINICHE
56
57 INIBIZIONE REVERSIBILE VIENE FONDAMENTALMENTE DISTINTA IN DUE TIPI: - COMPETITIVA - NON COMPETITIVA
58
59 INIBIZIONE COMPETITIVA L'INIBITORE PRESENTA ANALOGIA STRUTTURALE CON IL SUBSTRATO E QUINDI COMPETE CON QUESTO PER IL SITO ATTIVO
60
61
62 INIBIZIONE NON COMPETITIVA L'INIBITORE ED IL SUBSTRATO SI POSSONO LEGARE SIMULTANEAMENTE ALL'ENZIMA. CIÒ SIGNIFICA CHE I SITI DI LEGAME SONO DISTINTI.
63
64 INIBIZIONE SUICIDA UN ENZIMA CONVERTE UN SUBSTRATO IN UN INIBITORE REATTIVO CHE IMMEDIATAMENTE BLOCCA LA SUA ATTIVITÁ CATALITICA.
65 POICHE' LA VELOCITÁ DELLE E REAZIONI CELLULARI DIPENDE DAGLI ENZIMI, IL CONTROLLO DELLA LORO ATTIVITÁ RAPPRESENTA IL PIU IMPORTANTE FATTORE DI REGOLAZIONE DEL METABOLISMO.
66
67 LA VARIAZIONE DELLA CONCENTRAZIONE DELL'ENZIMA ENZIMA O DELLE SUE PROPRIETÁ CINETICHE RAPPRESENTA IL MEZZO PIÙ EFFICACE DI REGOLAZIONE.
68
69 E CHIAMATA TAPPA LIMITANTE LA REAZIONE PIÙ LENTA CHE CONDIZIONA LA VELOCITÁ COMPLESSIVA DI UNA VIA METABOLICA.
70 ALTRI IMPORTANTI FATTORI DI REGOLAZIONE POSSONO ESSERE: - ORGANIZZAZIONE DI SISTEMI MULTIENZIMATICI - COMPARTIMENTALIZZAZIONE - TRASPORTO SELETTIVO DI METABOLITI ATTRAVERSO LE MEMBRANE
71
72 QUATTRO SONO I MECCANISMI DI REGOLAZIONE DELL'ATTIVITÁ ENZIMATICA: - ATTIVAZIONE DI ZIMOGENI - INTERCONVERSIONE - ALLOSTERISMO - REGOLAZIONE ONE DA PARTE DI PROTEINE DI CONTROLLO
73
74
75
76
77 MODIFICHE POST-SINTETICHE PIU FREQUENTI DELLE PROTEINE - FOSFORILAZIONE - ACETILAZIONE - IDROSSILAZIONE - METILAZIONE - ADP-RIBOSILAZIONE - UBIQUITINAZIONE
78
79
80
81 Teoria Chiave-Serratura
82
83 Gli isoenzimi forniscono un mezzo di regolazione specifico di stadi di sviluppo e tessuti distinti Differiscono nella sequenza di aa., ma catalizzano la stessa reazione. Presentano di solito differenti parametri cinetici: Km e Vmax, o differenti tipologie di regolazione. Sono codificati da diversi loci genici: per duplicazione e divergenza. Possono essere distinti per la diversa mobilità elettroforetica.
84 GLI ENZIMI CHE CONSENTONO LA DIGESTIONE Indispensabile per l utilizzazione delle proteine, sono peptidasi o proteasi dette: endopeptidasi i (quando idrolizzano i legami peptidici all interno della molecola, generando spezzoni polipetidici) esopeptidasi (quando attaccano il legame peptidico p terminale della catena polipeptidica). p p I frammenti polipeptidici possono essere ulteriormente t demoliti rimuovendo l aminoacido id con l aminogruppo libero (aminopeptidasi) o quello con il gruppo carbossilico libero (carbossipeptidasi). Una dipeptidasi libera gli aminoacidi dai dipeptidi
85 LA DIGESTIONE PROTEICA AVVIENE IN TRE FASI: gastrica, pancreatica, intestinale. Nel duodeno termina l azione della pepsina gastrica ed inizia quella degli enzimi del succo pancreatico (tripsina, i chimotripsina, i i elastasi, carbossipeptidasi). Un sistema di enzimi secreti dall intestino (duodeno e digiuno) è l erepsina. ASSORBIMENTO aminoacidi: intestino>colon>stomaco vena porta fegato
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Destino dei principi nutritivi
 Destino dei principi nutritivi DIGESTIONE Demolizione nelle molecole costitutive ASSORBIMENTO TRASFORMAZIONE METABOLICA Produzione di energia glucosio, ac. grassi,aa Turnover proteico amminoacidi Metabolismo
Destino dei principi nutritivi DIGESTIONE Demolizione nelle molecole costitutive ASSORBIMENTO TRASFORMAZIONE METABOLICA Produzione di energia glucosio, ac. grassi,aa Turnover proteico amminoacidi Metabolismo
Chimica Biologica A.A. 2010-2011. Bioenergetica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni
 5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
scaricato da www.sunhope.it
 CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti:
 Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Connessioni. Le cellule cardiache sono unite tra loro da parti più ispessite del sarcolemma dette: Gap - junction
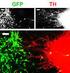 Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
Digestione e assorbimento delle proteine
 Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Gli enzimi. L azione degli enzimi è caratterizzata da alcune proprietà fondamentali:
 Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico 2014-15
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2014-15 Lezione 16 Degradazione dei lipidi
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2014-15 Lezione 16 Degradazione dei lipidi
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono
 Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Ossidazione del glucosio
 Ossidazione del glucosio Vie metaboliche all uso del glucosio Glicolisi e Fermentazioni 1 Reazione di ossidazione C 6 H 12 O 6 + 6 O 2 => 6 CO 2 + 6 H 2 O + 686 Kcal/mole Il glucosio reagisce direttamente
Ossidazione del glucosio Vie metaboliche all uso del glucosio Glicolisi e Fermentazioni 1 Reazione di ossidazione C 6 H 12 O 6 + 6 O 2 => 6 CO 2 + 6 H 2 O + 686 Kcal/mole Il glucosio reagisce direttamente
I MEDIATORI CHIMICI DELLA FLOGOSI
 I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
Relazione sequenza-struttura e funzione
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione sequenza-struttura e funzione Marco Nardini Dipartimento
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione sequenza-struttura e funzione Marco Nardini Dipartimento
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
3 SISTEMI ENERGETICI NEL MUSCOLO SCHELETRICO
 24-04-2013 3 SISTEMI ENERGETICI NEL MUSCOLO SCHELETRICO 1. METABOLISMO OSSIDATIVO (GLICOLISI AEROBICA) CONSUMO DI OSSIGENO 2. M. ANAEROBICO LATTACIDO (FERMENTAZIONE LATTICA) ACIDO LATTICO 3. M. ANAEROBICO
24-04-2013 3 SISTEMI ENERGETICI NEL MUSCOLO SCHELETRICO 1. METABOLISMO OSSIDATIVO (GLICOLISI AEROBICA) CONSUMO DI OSSIGENO 2. M. ANAEROBICO LATTACIDO (FERMENTAZIONE LATTICA) ACIDO LATTICO 3. M. ANAEROBICO
Enzimi. Nomenclatura:
 Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di
 IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di energia, prontamente disponibile quando l organismo ne ha bisogno.
IL TESSUTO ADIPOSO La funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all organismo animale una riserva di energia, prontamente disponibile quando l organismo ne ha bisogno.
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Il ciclo di Krebs e la fosforilazione ossidativa
 Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
PROGRAMMA DISCIPLINARE SVOLTO a. s / N.B. il programma è pubblico ad uso degli studenti e delle famiglie.
 Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Importanza degli enzimi in Medicina
 ENZIMI Importanza degli enzimi in Medicina 1. Chiave per capire errori del metabolismo 2. Importanti nelle reazioni di detossificazione 3. Targets di chemioterapia 4. Essenziali per formulare il razionale
ENZIMI Importanza degli enzimi in Medicina 1. Chiave per capire errori del metabolismo 2. Importanti nelle reazioni di detossificazione 3. Targets di chemioterapia 4. Essenziali per formulare il razionale
Biologia Molecolare. CDLM in CTF La trascrizione negli eucarioti
 Biologia Molecolare CDLM in CTF 2010-2011 La trascrizione negli eucarioti I meccanismi della trascrizione Organizzazione generale delle sequenze regolative Il macchinario generale della trascrizione Si
Biologia Molecolare CDLM in CTF 2010-2011 La trascrizione negli eucarioti I meccanismi della trascrizione Organizzazione generale delle sequenze regolative Il macchinario generale della trascrizione Si
energia di attivazione complesso attivato
 GLI ENZIMI: i catalizzatori delle reazioni nei sistemi biologici Diagrammi dello stato di L'energia di attivazione è l energia necessaria al sistema per iniziare un particolare processo L'energia di attivazione
GLI ENZIMI: i catalizzatori delle reazioni nei sistemi biologici Diagrammi dello stato di L'energia di attivazione è l energia necessaria al sistema per iniziare un particolare processo L'energia di attivazione
LA SINTESI PROTEICA LE MOLECOLE CHE INTERVENGONO IN TALE PROCESSO SONO:
 LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
Duplicazione del DNA. 6 Dicembre 2007
 Duplicazione del DNA 6 Dicembre 2007 Duplicazione - Trascrizione - Traduzione DNA Trascrizione DNA - La DUPLICAZIONE è il processo che porta alla formazione di copie delle molecole di DNA ed al trasferimento
Duplicazione del DNA 6 Dicembre 2007 Duplicazione - Trascrizione - Traduzione DNA Trascrizione DNA - La DUPLICAZIONE è il processo che porta alla formazione di copie delle molecole di DNA ed al trasferimento
ENZIMI. Gli enzimi sono dei catalizzatori biologici
 ENZIMI Gli enzimi sono dei catalizzatori biologici catalizzatore: una sostanza che senza subire variazioni produce come effetto macroscopicamente apprezzabile un incremento della velocità di reazione La
ENZIMI Gli enzimi sono dei catalizzatori biologici catalizzatore: una sostanza che senza subire variazioni produce come effetto macroscopicamente apprezzabile un incremento della velocità di reazione La
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
APPARATO DIGERENTE. Digestione e assorbimento. A.Megighian Farmacia 2011
 APPARATO DIGERENTE Digestione e assorbimento A.Megighian Farmacia 2011 Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700
APPARATO DIGERENTE Digestione e assorbimento A.Megighian Farmacia 2011 Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700
Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione
 Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione CdL Tecnici di Lab Biomedico AA. 2011-12 - Prof.ssa Frabetti Come si esprime l informazione? Per i geni classici vedremo:
Espressione ed utilizzo della informazione genetica II Trascrizione e Traduzione CdL Tecnici di Lab Biomedico AA. 2011-12 - Prof.ssa Frabetti Come si esprime l informazione? Per i geni classici vedremo:
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Apparato digerente. È formato dal un lungo tubo che inizia con la bocca e finisce con l'ano. Le parti principali in cui si suddivide sono:
 Apparato digerente È formato dal un lungo tubo che inizia con la bocca e finisce con l'ano. Le parti principali in cui si suddivide sono: bocca faringe esofago stomaco intestino tenue intestino crasso
Apparato digerente È formato dal un lungo tubo che inizia con la bocca e finisce con l'ano. Le parti principali in cui si suddivide sono: bocca faringe esofago stomaco intestino tenue intestino crasso
UNITÀ 3. L attività delle cellule
 Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico mediato da canali di membrana molecole piccole
Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico mediato da canali di membrana molecole piccole
L apparato digerente è composto dal. Tubo digerente. Che comprende. Bocca. Faringe. Esofago. Stomaco. Intestino
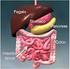 L apparato digerente è composto dal Tubo digerente Che comprende Bocca Faringe Esofago Stomaco Intestino Ghiandole Salivari Costituita da Lingua Cosparsa di Producono 32 Denti Papille Gustative Saliva
L apparato digerente è composto dal Tubo digerente Che comprende Bocca Faringe Esofago Stomaco Intestino Ghiandole Salivari Costituita da Lingua Cosparsa di Producono 32 Denti Papille Gustative Saliva
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Idratazione (introduciamo un gruppo OH sul Cβ) per mezzo della enoil-coa idratasi
 β-ossidazione di un Ac. Grasso Saturo con n PARI di atomi di carbonio Deidrogenazione FAD-dipendente del legame Cα- Cβ per mezzo della Acil-CoA deidrogenasi che è legata alla membrana mitocondriale interna)
β-ossidazione di un Ac. Grasso Saturo con n PARI di atomi di carbonio Deidrogenazione FAD-dipendente del legame Cα- Cβ per mezzo della Acil-CoA deidrogenasi che è legata alla membrana mitocondriale interna)
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Le trasformazioni energetiche
 BIOENERGETICA Le trasformazioni energetiche Tutti i processi vitali di un organismo dipendono dalla disponibilità di energia. La bioenergetica è la scienza che studia tali trasformazioni energetiche che
BIOENERGETICA Le trasformazioni energetiche Tutti i processi vitali di un organismo dipendono dalla disponibilità di energia. La bioenergetica è la scienza che studia tali trasformazioni energetiche che
LA FOTOSINTESI: conversione di energia luminosa in energia chimica
 LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
Le trasformazioni energetiche
 BIOENERGETICA Le trasformazioni energetiche Tutti i processi vitali di un organismo dipendono dalla disponibilità di energia. La bioenergetica è la scienza che studia tali trasformazioni energetiche che
BIOENERGETICA Le trasformazioni energetiche Tutti i processi vitali di un organismo dipendono dalla disponibilità di energia. La bioenergetica è la scienza che studia tali trasformazioni energetiche che
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
VALUTAZIONE DELL ATTIVITA ANTIPROLIFERATIVA DI CELLFOOD IN CELLULE TUMORALI IN COLTURA. (relazione preliminare)
 VALUTAZIONE DELL ATTIVITA ANTIPROLIFERATIVA DI CELLFOOD IN CELLULE TUMORALI IN COLTURA. (relazione preliminare) Serena Benedetti, Simona Catalani, Valentina Carbonaro, Francesco Palma, Franco Canestrari.
VALUTAZIONE DELL ATTIVITA ANTIPROLIFERATIVA DI CELLFOOD IN CELLULE TUMORALI IN COLTURA. (relazione preliminare) Serena Benedetti, Simona Catalani, Valentina Carbonaro, Francesco Palma, Franco Canestrari.
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi
 Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Trascrizione negli eucarioti
 Trascrizione negli eucarioti TRASCRIZIONE EUCARIOTI Fattori di trascrizione fattori basali, attivatori (costitutivi, non costitutivi), co-attivatori, repressori Enhancer Promotore 100bp 200bp Enhancer:
Trascrizione negli eucarioti TRASCRIZIONE EUCARIOTI Fattori di trascrizione fattori basali, attivatori (costitutivi, non costitutivi), co-attivatori, repressori Enhancer Promotore 100bp 200bp Enhancer:
PECULIARITA DELLA RESPIRAZIONE CELLULARE DELLE PIANTE
 La respirazione nelle piante è fondamentalmente simile a quella negli animali salvo alcune peculiarità: La succinil-coa sintasi produce ATP invece che GTP Il malato è decarbossilato a piruvato da un enzima
La respirazione nelle piante è fondamentalmente simile a quella negli animali salvo alcune peculiarità: La succinil-coa sintasi produce ATP invece che GTP Il malato è decarbossilato a piruvato da un enzima
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Stampa Preventivo. A.S Pagina 1 di 11
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 11 Insegnante BADALINI RENZO Classe 2BT Materia elementi di chimica e fisica preventivo consuntivo 99 84 titolo modulo 1. STRUTTURA E TRASFORM. DELL 2. L'ATOMO
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 11 Insegnante BADALINI RENZO Classe 2BT Materia elementi di chimica e fisica preventivo consuntivo 99 84 titolo modulo 1. STRUTTURA E TRASFORM. DELL 2. L'ATOMO
26 Aprile 1915, 81 compleanno
 Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
MODULO 2 ENZIMI CARATTERISTICHE GENERALI
 MODULO 2 ENZIMI CARATTERISTICHE GENERALI Introduzione L elevatissimo numero di reazioni chimiche, che in ogni istante avvengono all interno e all esterno delle cellule che costituiscono i nostri tessuti
MODULO 2 ENZIMI CARATTERISTICHE GENERALI Introduzione L elevatissimo numero di reazioni chimiche, che in ogni istante avvengono all interno e all esterno delle cellule che costituiscono i nostri tessuti
ενζυµον ( nel lievito ): un po di storia...
 ENZIMI CATALISI ENZIMATICA. Meccanismo d azione degli enzimi; Energia dl attivazione; Componenti strutturali e funzionali; Nomenclatura e classificazione; Specificità dl substrato ed azione; Modello Lock
ENZIMI CATALISI ENZIMATICA. Meccanismo d azione degli enzimi; Energia dl attivazione; Componenti strutturali e funzionali; Nomenclatura e classificazione; Specificità dl substrato ed azione; Modello Lock
LIPIDI. I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi.
 LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
Come calcolare i parametri farmacocinetici
 Come calcolare i parametri farmacocinetici La conoscenza dei parametri farmacocinetici fondamentali di un farmaco è essenziale per comprendere in che modo esso venga trattato dall organismo e come sia
Come calcolare i parametri farmacocinetici La conoscenza dei parametri farmacocinetici fondamentali di un farmaco è essenziale per comprendere in che modo esso venga trattato dall organismo e come sia
Anno scolastico 2015/16
 Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
Anno scolastico 2015/16 P R O G R A M M A S V O L T O Docente: David Fiacchini Materia: Scienze Naturali - Classe - - Indirizzo - 2^C Liceo Scientifico Primo quadrimestre UNITA DIDATTICA FORMATIVA n. 1
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Cinetica enzimatica Inibitori enzimatici
 Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Alimentazione ed efficienza dei sistemi alimentari
 Corso di laurea magistrale in Scienze e tecnologie animali Alimentazione ed efficienza dei sistemi alimentari Effetti delle tipologie dei consumi alimentari sui flussi della materia e dell energia, sulle
Corso di laurea magistrale in Scienze e tecnologie animali Alimentazione ed efficienza dei sistemi alimentari Effetti delle tipologie dei consumi alimentari sui flussi della materia e dell energia, sulle
Unità 6. La respirazione cellulare e la fermentazione
 Unità 6 La respirazione cellulare e la fermentazione Obiettivi Comprendere il rapporto tra respirazione polmonare e respirazione cellulare Capire la relazione tra ossidazione delle molecole organiche e
Unità 6 La respirazione cellulare e la fermentazione Obiettivi Comprendere il rapporto tra respirazione polmonare e respirazione cellulare Capire la relazione tra ossidazione delle molecole organiche e
Trasporto di membrana
 Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
2. Negli Anfibi la circolazione e doppia ma incompleta. Il cuore di una rana ha pertanto:
 Test n. 3 Dalle olimpiadi delle Scienze Naturali 2004 1. L uomo, come tutti i vertebrati, possiede un sistema circolatorio chiuso. Nei mammiferi la circolazione è doppia e completa, poiché il sangue ossigenato
Test n. 3 Dalle olimpiadi delle Scienze Naturali 2004 1. L uomo, come tutti i vertebrati, possiede un sistema circolatorio chiuso. Nei mammiferi la circolazione è doppia e completa, poiché il sangue ossigenato
INTRODUZIONE ALLA TERMODINAMICA. Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta
 INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
LA REAZIONE A CATENA DELLA POLIMERASI PCR
 LA REAZIONE A CATENA DELLA POLIMERASI PCR INTRODUZIONE Tecnica ideata da Mullis e collaboratori nel 1984 La possibilita' di disporre di quantità virtualmente illimitate di un determinato frammento di DNA,
LA REAZIONE A CATENA DELLA POLIMERASI PCR INTRODUZIONE Tecnica ideata da Mullis e collaboratori nel 1984 La possibilita' di disporre di quantità virtualmente illimitate di un determinato frammento di DNA,
Apparato Digerente. Digestione e assorbimento
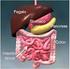 Apparato Digerente Digestione e assorbimento Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700 Cal/d=7300 kj/d 500-2500
Apparato Digerente Digestione e assorbimento Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700 Cal/d=7300 kj/d 500-2500
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
IL CODICE GENETICO E I CARATTERI EREDITARI
 IL CODICE GENETICO E I CARATTERI EREDITARI Il DNA porta le informazioni genetiche scritte nella sequenza di basi. Qualunque sequenza è possibile. Il DNA virus più semplici: 5000 basi appaiate; 46 cromosomi
IL CODICE GENETICO E I CARATTERI EREDITARI Il DNA porta le informazioni genetiche scritte nella sequenza di basi. Qualunque sequenza è possibile. Il DNA virus più semplici: 5000 basi appaiate; 46 cromosomi
LA FORZA E LA POTENZA CREATINA - FOSFOCREATINA
 LA FORZA E LA POTENZA CREATINA - FOSFOCREATINA Il corretto uso degli integratori nello sport agonistico FIDAL - FMSI BARI 19.9.2009 Marco Majorano ISTITUTO DI MEDICINA DELLO SPORT - BARI VITO ACCETTURA
LA FORZA E LA POTENZA CREATINA - FOSFOCREATINA Il corretto uso degli integratori nello sport agonistico FIDAL - FMSI BARI 19.9.2009 Marco Majorano ISTITUTO DI MEDICINA DELLO SPORT - BARI VITO ACCETTURA
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Il metabolismo dell azoto
 Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi
 È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
È stimato che oggi sulla terra sono presenti da 10*10 6 a 100*10 6 specie viventi Enorme diversità di forme Costanza di struttura interna La cellula è l unità fondamentale di tutti gli organismi viventi
L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA
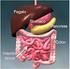 L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA FARINGE, L ESOFAGO, LO STOMACO, L INTESTINO TENUE, L
L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA FARINGE, L ESOFAGO, LO STOMACO, L INTESTINO TENUE, L
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Grandezze fisiche e loro misura
 Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e caratterizzati da grandezze misurabili.
Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e caratterizzati da grandezze misurabili.
Chimica: energia e velocità di reazione
 cbnd Antonio Guermani Scheda n 1 Nome Data Se forniamo al sistema 50 kj di calore e un Per trovare il catalizzatore più adatto per una La sintesi dell'acqua 2H2 + O2 2H2O è lavoro di 40 kj ΔU = 10 kj si
cbnd Antonio Guermani Scheda n 1 Nome Data Se forniamo al sistema 50 kj di calore e un Per trovare il catalizzatore più adatto per una La sintesi dell'acqua 2H2 + O2 2H2O è lavoro di 40 kj ΔU = 10 kj si
Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO
 Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali
Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Ciclo dell acido citrico
 Ciclo dell acido citrico Il metabolismo ossidativo dei carburanti metabolici I gruppi acetili derivati da carboidrati, amminoacidi e acidi grassi entrano nel ciclo dell acido citrico dove vengono ossidati
Ciclo dell acido citrico Il metabolismo ossidativo dei carburanti metabolici I gruppi acetili derivati da carboidrati, amminoacidi e acidi grassi entrano nel ciclo dell acido citrico dove vengono ossidati
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Prodotti avanzati dell ossidazione proteica (AOPP): proteine ossidate, marcatori di stress ossidativo specifico delle proteine.
 marcatori di stress ossidativo e di infiammazione Prodotti avanzati dell ossidazione proteica (AOPP): proteine ossidate, marcatori di stress ossidativo specifico delle proteine. Ossidanti totali: marcatori
marcatori di stress ossidativo e di infiammazione Prodotti avanzati dell ossidazione proteica (AOPP): proteine ossidate, marcatori di stress ossidativo specifico delle proteine. Ossidanti totali: marcatori
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Energia introdotta (cibo) = + Energia conservata
 EQUAZIONE DEL BILANCIO ENERGETICO Energia spesa (calore, lavoro, biosintesi ) Energia introdotta (cibo) = + Energia conservata UTILIZZAZIONE DELL ENERGIA INTRODOTTA L energia chimica assorbita (assimilata)
EQUAZIONE DEL BILANCIO ENERGETICO Energia spesa (calore, lavoro, biosintesi ) Energia introdotta (cibo) = + Energia conservata UTILIZZAZIONE DELL ENERGIA INTRODOTTA L energia chimica assorbita (assimilata)
