1/v
|
|
|
- Cristina Volpe
- 9 anni fa
- Просмотров:
Транскрипт
1 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare la retta che si riferisce all esperimento in assenza di inibitore. b) Individuare la retta che si riferisce all esperimento in presenza della minore concentrazione di inibitore. Che tipo di inibitore è stato usato? 1/v (min/mm ) /[S] (mm -1 ) 2. Una chinasi catalizza la fosforilazione del suo substrato con una Km di.5 mm e una Kcat di 3 s -1, sapendo che la concentrazione dell enzima è 5 μm determinare la Vmax della reazione. Disegnare la curva cinetica relativa a tale reazione sul seguente grafico di Micaelis-Menten. Disegnare sullo stesso grafico la curva che si ottiene dopo aver raddoppiato la concentrazione dell enzima V (mm/sec) [S] mm 3. In che modo può essere modulata l attività enzimatica? 4. Come agiscono gli inibitori irreversibili? Fare degli esempi. 5. I 2 enzimi Esochinasi e Glucochinasi catalizzano entrambi la reazione: Glucosio + ATP Glu-6-P + ADP. I valori di Km sono 1 μm per l esochinasi e 2 mm per la glucochinasi. Quale dei due enzimi fosforila il glucosio con una velocità vicina a Vmax in condizioni di digiuno? ([Glu] a digiuno 5 mm) 6. Se si considera la cinetica di una reazione catalizzata da un enzima allosterico in presenza di un attivatore allosterico, la Km per il substrato: a) aumenta b) diminuisce c) rimane invariata, rappresentare in un grafico la curva cinetica dell enzima allosterico in assenza e in presenza dell attivatore. 7. Calcolare la velocità iniziale della reazione di seguito riportata: Mannosio + ATP Man-6-P + ADP [Mannosio] =.2 mm Km =.1 mm Vmax = 1 mm/min - Quanto vale il numero di turnover quando la concentrazione dell esochinasi è 5 μm? - Disegnare la curva che descrive la dipendenza di V da [Mannosio] nelle condizioni sperimentali riportate nell esercizio.
2 - Disegnare la curva ottenuta in presenza di un inibitore incompetitivo, commentando brevemente le scelte fatte. - Tracciare il corrispondente grafico dei doppi reciproci. V (mm/min) [S] mm 1/V (min/mm) [1/S] mm Le due rette del seguente grafico descrivono i risultati di un esperimento condotto utilizzando due diverse concentrazioni dello stesso enzima. Il substrato utilizzato era lo stesso nei due esperimenti. - Dire in quale dei due esperimenti è stata utilizzata la minore concentrazione di enzima. - Disegnare le corrispondenti curve cinetiche sul grafico di Micaelis-Menten. 1.8 A 1/V (min/mm) B [1/S] mm V (mm/min)
3 9. Calcolare la v max della reazione di seguito riportata sapendo la concentrazione dell enzima Fumarasi corrisponde a 5x1-9 M e la k cat vale 8,x1 2 sec -1. Fumarato Malato Calcolare inoltre la velocità iniziale della reazione ad una concentrazione di fumarato pari a 1-5 M sapendo che la K M vale 5,x1-6 M. 1. Nel seguente grafico dei doppi reciproci sono riportati i dati cinetici di una reazione enzimatica condotta in presenza ed in assenza di un inibitore. Indicare quali variabili sono riportate sui due assi e disegnare il grafico di Michaelis-Menten corrispondente. Sul grafico di Michaelis-Menten individuare la curva che si riferisce all esperimento condotto in presenza dell inibitore e stabilire di quale tipo di inibizione si tratta. 4. (min/mm) (mm/min) mm 11. Quanti tipi di meccanismi di catalisi consentono agli enzimi di diminuire l energia di attivazione della reazione da loro catalizzata? Elencarli ed illustrarne brevemente uno. 12. Dal grafico di seguito riportato, che descrive la dipendenza della velocità di reazione enzimatica dalla concentrazione del substrato, ricavare i seguenti parametri, sapendo che la concentrazione dell enzima è pari a 1-3 M. a. Km b. Vmax c. kcat Disegnare sullo stesso grafico la curva che descrive i risultati ottenuti in presenza di un inibitore competitivo.
4 13. Quali sono i composti fosforici così detti a bassa energia e ad alta energia? Qual è il loro ruolo nel metabolismo? 14. La reazione: fosfoenolpiruvato + ADP + H + piruvato + ATP ha un ΔG di -31 KJ/mole. Calcolare il ΔG di idrolisi del fosfoenolpiruvato sapendo che la variazione di energia libera di idrolisi dell ATP corrisponde a KJ/mole. 15. Sapendo che la seguente idrolisi: creatina-p creatina + Pi ha un ΔG = -1 Kcal/mole, e che l idrolisi dell ATP ha un ΔG = -7.3 Kcal/mole. Calcolare il ΔG totale della reazione: ADP + creatina-p ATP + creatina. 16. Nella glicolisi la conversione del glucosio in fruttosio-1,6-bisfosfato è un processo che avviene in 3 tappe: glucosio + ATP glucosio-6-p + ADP ΔG = KJ/mole glucosio-6-p fruttosio-6-p ΔG = +1.7 KJ/mole fruttosio-6p fruttosio-1,6-bisfosfato ΔG = -14 KJ/mole considerando i ΔG riportati calcolare la variazione di energia libera in condizioni standard del processo globale. 17. Scegliere il o i composti la cui reazione di idrolisi può essere accoppiata alla reazione ADP + Pi ATP (ΔG = +3.5 KJ/mole) in modo tale da avere un processo globalmente esoergonico. FOSFOENOLPIRUVATO ΔG = KJ/mole PPi ΔG = KJ/mole GLUCOSIO 6-P ΔG = KJ/mole GLUCOSIO 1-P ΔG = -2.9 KJ/mole ACETIL-CoA ΔG = KJ/mole 18. Considerando la seguente reazione: Malato + NAD + Ossalacetato + NADH + H + E noti i potenziali di riduzione standard delle coppie redox: Ossalacetato + 2H + + 2e - Malato E = V NAD + + H e - NADH E = V Calcolare il ΔG e dire se la reazione è spontanea. (F = 96.5 KJ/V mole) 19. Date le seguenti coppie redox di cui sono riportati i valori di E ordinare le coppie in modo che gli elettroni fluiscano spontaneamente dalla prima coppia verso l ultima. Calcolare la variazione di energia libera standard per il processo relativo al trasferimento di 2 elettroni dalla prima all ultima coppia. UBICHINONE/ UBICHINOLO E = +.5 V FMN/FMNH 2 E = -.3 V NAD + /NADH E = -.32 V Centro Fe-S E = -.15 V 2. Data la reazione: Piruvato + NADH + H + Lattato + NAD + e noti i potenziali standard di riduzione delle 2 semireazioni: Piruvato + 2e - +2H + lattato (E = V) NAD + + 2e - +2H + NADH + H + (E = V) Dire se la reazione avverrà spontaneamente in condizioni standard. 21. Data la seguente reazione: ACETALDEIDE + NADH + H + ETANOLO + NAD + CONSIDERANDO I SEGUENTI POTENZIALI STANDARD DI RIDUZIONE: ACETALDEIDE / ETANOLO NAD + / NADH + H + LA REAZIONE E SPONTANEA IN CONDIZIONI STANDARD? E = -.2 V E = -.32 V 22. CALCOLARE IL ΔG PER LAREAZIONE: SUCCINATO + FAD FUMARATO + FADH 2 SAPENDO CHE: Fumarato/Succinato E =.3 V FAD/FADH 2 E =. V 23. Calcolare la variazione di energia libera della seguente reazione in condizioni standard: Glucosio-6P + ADP Glucosio + ATP sapendo che i G delle semireazioni nel senso dell idrolisi sono: kj/mole per ATP ADP + Pi; kj/mole per Glucosio-6P Glucosio + Pi. Dire se la reazione è spontanea.
5 24. Data la reazione: Ossalacetato + Succinato malato + fumarato in cui il succinato viene ossidato a fumarato, calcolare la variazione di energia libera in condizioni standard sapendo che ciascuna coppia scambia 2 elettroni e i potenziali di riduzione standard valgono: Ossalacetato/malato (E = V) Fumarato/succinato (E = +.31) (F = 96.5 kj/v mole) 25. Di seguito sono riportati i potenziali di riduzione standard di alcune coppie redox, ordinarle in maniera tale da ottenere un flusso spontaneo di 2 elettroni attraverso di essi e calcolare la ΔG del processo globale. Ossalacetato/malato FMN/FMNH2 α-chetoglutarato/isocitrato Acetaldeide/Etanolo citocromo a3(ox)/citocromo a3(rid) UBICHINONE/ UBICHINOLO E.166 V E.3 V E.38 V E.197 V E +.35 V E +.5 V 26. Il potenziale di riduzione standard del NADH a NAD + è.32 V e quello dell Ubichinone a ubichinolo è +.4 V. Noti questi due valori a) valutare se l ossidazione del NADH da parte dell ubichinone liberi energia sufficiente per la sintesi di una molecola di ATP, in condizioni standard. (ΔG idrolisi di ATP = -31kJ/mole) F (costante di Faraday) = 96,5 kj/v mole. b) indicare quanti elettroni sono scambiati nella reazione di ossidoriduzione specificando la struttura della porzione reattiva del NAD nella forma ossidata e ridotta. 27. Di seguito sono riportati i potenziali di riduzione standard di alcune coppie redox, ordinarle in maniera tale da ottenere un flusso spontaneo di elettroni attraverso di essi e calcolare la ΔG del processo globale. Fe +3 /Fe +2 (Centro Fe-S) E.15 V NADP + /NADPH E.32 V FAD/FADH 2 E.22 V α-chetoglutarato/isocitrato E -.38 V Acetaldeide/Etanolo E V citocromo b(ox)/citocromo b(rid) E +.7 V citocromo a 3(ox)/citocromo a 3(rid) E +.35 V 28. Scrivete la struttura dell 1,3-bisfosfoglicerato e illustrate i motivi termodinamici per i quali l energia libera standard di idrolisi del fosfato di questa molecola è molto elevato. 29. Quali sono i composti la cui energia libera standard di idrolisi viene accoppiata alla fosforilazione dell ADP nei processi metabolici a voi noti? Dopo averli elencati, sceglietene uno, scrivetene la struttura e spiegate brevemente perché la sua idrolisi è esoergonica. 3. Data la concentrazione dei metaboliti di seguito riportata: Fruttosio 6-P Fruttosio 1,6-bisfosfato ATP ADP 87 MicroM 22 MicroM 114 MicroM 132 MicroM e noti i valori di variazione di energia libera standard delle reazioni: Fruttosio 1,6-bisfosfato Fruttosio 6-P + Pi G = KJ/mole ATP ADP + Pi G = KJ/mole Calcolare il valore del G della reazione:
6 PFK1 Fruttosio 6-P Fruttosio 1,6-bisfosfato ATP ADP 31. Quale/i affermazione/i non sono vere? La variazione di energia libera ( G ) : a. Dipende dalla concentrazione dei reagenti e dei prodotti. b. È uguale a zero all equilibrio c. È uguale a RT ln Keq 32. Dati i valori di E delle seguenti semireazioni di riduzione: Ossalacetato+ 2e - + 2H + Malato V NAD + + 2e - + 2H + NADH -.32 V e la reazione Malato + NAD + Ossalacetato + NADH dire se la reazione procederà spontaneamente nel verso in cui è stata scritta in condizioni standard: e alle seguenti concentrazioni di reagenti e prodotti: [Ossalacetato] = 1 microm [Malato] = 1 mm [NAD+] =.1 mm [NADH] = 1 microm (F=96.5 kj/v*mole) 33. Data la reazione: piruvato + 2 [centro Fe-S(Fe 2+ )] lattato + 2 [centro Fe-S(Fe 3+ )] in cui il piruvato viene ridotto a lattato, calcolare la variazione di energia libera in condizioni standard e alle concentrazione di reagenti e prodotti di seguito riportate: [piruvato] =.2M [lattato] =.2M [centro Fe-S(Fe 3+ )] =.2M [centro Fe-S(Fe 2+ )] =.2M sapendo che i potenziali di riduzione standard valgono: piruvato/lattato E =.19 V centro Fe-S(Fe 2+ )/centro Fe-S(Fe 3+ ) E =.15 V (F = 96.5 kj/v mole) (R= 8.3 J/K mole)
7 34. Calcolare la variazione di energia libera della seguente reazione in condizioni standard: Glutammato + NH3 + ATP e alle seguenti concentrazioni: [Glutammina] = 1 mm [ATP] =.2 mm [ADP] = 5 mm [Glutammato] = 2 mm sapendo che: Glutammina + ADP + Pi ATP ADP + Pi ( G = kj/mole) Glutammato + NH3 Glutammina ( G = kj/mole) Dire se la reazione è spontanea nelle due condizioni. 35. L enolasi catalizza la seguente reazione: 2-FOSFOGLICERATO FOSFOENOLPIRUVATO + H2O il cui ΔG in condizioni standard è KJ/mol. Calcolare la variazione di energia libera nelle seguenti condizioni: ph 7., 25 C [2-FOSFOGLICERATO] = 8 mm [FOSFOENOLPIRUVATO] = 8 mm 36. Determinate in quale verso procede spontaneamente la reazione di seguito riportata: ADP + Fosfocreatina ATP + Creatina Nelle seguenti condizioni: 25 C, ph 7., [ATP] = 4 mm, [ADP] =.15 mm, [fosfocreatina] = 2.5 mm, [creatina] = 1 mm. ΔG di idrolisi della fosfocreatina = KJ/mol ΔG di idrolisi dell ATP = KJ/mol R = 8.3x 1-3 KJ/mol. 37. Calcolare il ΔG della reazione: FADH2 + AC. LIPOICO FAD + AC. DIIDROLIPOICO Sapendo che: FAD + 2H + + 2e - FADH2 E = -.22 V AC. LIPOICO + 2H + + 2e - AC. DIIDROLIPOICO E = -.29 V La reazione è spontanea in condizioni standard? La reazione è spontanea nelle seguenti condizioni? [FAD] = 1 mm [FADH2] = 1 4 mm [AC. LIPOICO] = 6x1 4 mm [AC. DIIDROLIPOICO] = 3 mm 25 C, ph 7.. (F = 96.5 KJ/V mole).
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
metano alcool metilico formaldeide acido formico CO 2
 -4-2 0 +2 +4 metano alcool metilico formaldeide acido formico CO 2 + ridotto + ossidato + ossidato Glicolisi 2 Glucosio Piruvato Glicolisi Glucosio + 2NAD + 2 piruvato + 2NADH + 2H + ΔG = -146 kj/mol 2ADP
-4-2 0 +2 +4 metano alcool metilico formaldeide acido formico CO 2 + ridotto + ossidato + ossidato Glicolisi 2 Glucosio Piruvato Glicolisi Glucosio + 2NAD + 2 piruvato + 2NADH + 2H + ΔG = -146 kj/mol 2ADP
Cap.16 GLICOLISI. Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP H 2 O 2 NAD + 2 NADH + 2H +
 Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Utilizzo del glucosio: la glicolisi
 Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la
 Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
GLICOLISI ADP ATP. Condizioni aerobiche. Condizioni anaerobiche ATP
 GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
Respirazione cellulare: processi molecolari medianti i quali le cellule consumano O 2 e producono CO 2
 AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono:
 Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
Catabolismo dei carboidrati Glicolisi
 Catabolismo dei carboidrati Glicolisi Principali vie di utilizzo del Glucosio L estrazione dell energia dai composti organici può essere divisa in tre stadi Metabolismo del glucosio C 6 H 12 O 6 + 6O 2
Catabolismo dei carboidrati Glicolisi Principali vie di utilizzo del Glucosio L estrazione dell energia dai composti organici può essere divisa in tre stadi Metabolismo del glucosio C 6 H 12 O 6 + 6O 2
Fosforilazione a livello del substrato
 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una:
 1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
Fosforilazione a livello del substrato
 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
Carboidrati! Oligosaccaridi Polisaccaridi. B) Carboidrati complessi
 Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
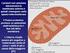 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Lezione 5. Il metabolismo dei carboidrati
 Lezione 5 Il metabolismo dei carboidrati 1 La produzione di energia: catabolismo dei nutrienti La degradazione enzimatica delle sostanze nutritive principali (carboidrati, lipidi e proteine) procede attraverso
Lezione 5 Il metabolismo dei carboidrati 1 La produzione di energia: catabolismo dei nutrienti La degradazione enzimatica delle sostanze nutritive principali (carboidrati, lipidi e proteine) procede attraverso
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Una panoramica del ciclo dell acido ciclico
 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
NADH FADH 2 (trasportatori ridotti di elettroni) Catena respiratoria (trasferimento degli
 NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
Chimica Biologica A.A. 2010-2011. Bioenergetica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico
 Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
6 H 2. con G=-686 kcal/mole di H 12 O 6 O + 6 CO O 2. glucosio La respirazione avviene in tre stadi principali; ognuno di questi
 La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
Introduzione al metabolismo
 Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
La quantità di glu presente nei liquidi extracellulari è di circa 20g, 80kcal.
 I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
AGISCONO NEL SISTEMA NAVETTA 2 ISOFORME DELL ENZIMA: UNA FORMA MITOCONDRIALE ( MEMBRANA MIT. INTERNA) FAD-dipendente
 METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Lattato. Glicolisi. Piruvato
 Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
FOSFORILAZIONE OSSIDATIVA
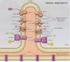 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti
 ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Regolazione della Glicolisi
 Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Modulo 16: La fosforilazione ossidativa
 1 Modulo 16: La fosforilazione ossidativa La fosforilazione ossidativa NADH e FADH 2 trasferiscono e - ad alto potenziale di trasferimento all O 2 liberando una quantità di energia sufficiente per generare
1 Modulo 16: La fosforilazione ossidativa La fosforilazione ossidativa NADH e FADH 2 trasferiscono e - ad alto potenziale di trasferimento all O 2 liberando una quantità di energia sufficiente per generare
Biosintesi dei carboidrati
 Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Metabolismo del Glucosio
 Metabolismo del Glucosio Schema generale del metabolismo del glucosio Una panoramica della glicolisi Conce2 chiave La glicolisi consiste nella degradazione del glucosio a piruvato e utilizza, al contempo,
Metabolismo del Glucosio Schema generale del metabolismo del glucosio Una panoramica della glicolisi Conce2 chiave La glicolisi consiste nella degradazione del glucosio a piruvato e utilizza, al contempo,
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
prodotto finale della glicolisi
 Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa
 IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa Glucagone = innalza il livello ematico di glucosio Adrenalina = scatena una
IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa Glucagone = innalza il livello ematico di glucosio Adrenalina = scatena una
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Catabolismo = degradazione di composti per recuperare i loro. Anabolismo = Le vie anaboliche e cataboliche sono in relazione fra loro
 Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Introduzione allo studio del metabolismo Parte I
 Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
GLUCOSIO. Vena porta DIGESTIONE DEI DISACCARIDI. Enzimi parete intestinale
 DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
Chimica Biologica A.A Glicolisi. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Glicolisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Glicolisi Glicolisi - via di degradazione del glucosio (1940) - glucosio
Chimica Biologica A.A. 2010-2011 Glicolisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Glicolisi Glicolisi - via di degradazione del glucosio (1940) - glucosio
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
Modulo 13 La glicolisi
 1 Modulo 13 La glicolisi La glicolisi: via metabolica centrale del catabolismo del glucosio Via metabolica antica avviene interamente nel citoplasma delle cellule. onverte il glucosio in piruvato, producendo
1 Modulo 13 La glicolisi La glicolisi: via metabolica centrale del catabolismo del glucosio Via metabolica antica avviene interamente nel citoplasma delle cellule. onverte il glucosio in piruvato, producendo
Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale
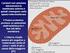 Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Gluconeogenesi. Glicemia. Digiuno prolungato. prolungato,, la glicemia. digiuno, anche. scarse. subisce. Nel. sangue ed il cervello. Digiuno.
 Gluconeogenesi Glicemia [Glu] blood Insulina Fed Fast early Glucagone 1-2 hrs Digiuno late fast Glycogen Glicogeno esaurito gone 6-12 hrs Digiuno prolungato (giorni) Meal Un pasto Nel digiuno, anche prolungato,,
Gluconeogenesi Glicemia [Glu] blood Insulina Fed Fast early Glucagone 1-2 hrs Digiuno late fast Glycogen Glicogeno esaurito gone 6-12 hrs Digiuno prolungato (giorni) Meal Un pasto Nel digiuno, anche prolungato,,
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe. Substrato
 Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato
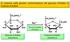 2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Catabolismo = degradazione di composti per recuperare i loro. Anabolismo = Le vie anaboliche e cataboliche sono in relazione fra loro
 Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
ADP + HPO 3, NAD +, NADP +, FAD ATP, NADH, NADPH, FADH 2 ENERGIA CHIMICA
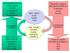 MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
Il ciclo di Krebs e la fosforilazione ossidativa
 Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
