Gli enzimi. L azione degli enzimi è caratterizzata da alcune proprietà fondamentali:
|
|
|
- Erico Pappalardo
- 9 anni fa
- Visualizzazioni
Transcript
1 Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso allo spazio alveolare avviene previa idratazione del diossido di carbonio. Questo processo è spontaneo ma avverrebbe in tempi lentissimi, non fisiologici. Questa semplice reazione è catalizzata, nel nostro organismo, da un enzima altamente specifico ed efficiente, l anidrasi carbonica. Una sola molecola può idratare 10 5 molecole di CO 2 al secondo e la reazione è 10 milioni di volte più veloce di quella senza enzima! Solo grazie alla presenza di enzimi le trasformazioni chimiche del nostro organismo possono avvenire nei tempi e nei modi compatibili con le necessità vitali. Gli enzimi sono proteine altamente specializzate con una funzione di catalisi estremamente specifica. Tutte le catene o i cicli metabolici sono costituiti da una serie di passaggi e di trasformazioni, anche minime, catalizzate da sistemi multienzimatici. Molti enzimi effettuano la loro azione solo con i residui aminoacidici di aminoacidi posti nel sito attivo e, in questo caso, sono proteine pure. Altri, invece, per la loro azione catalitica, necessitano della presenza di componenti chimici addizionali, cofattori, che possono essere ioni inorganici come il Fe 2+, il Mg 2+, il Mn 2+, o lo Zn 2+, oppure complesse molecole organiche chiamate coenzimi. Sia i cofattori che i coenzimi sono chiamati gruppi prostetici. L azione degli enzimi è caratterizzata da alcune proprietà fondamentali: 1) possono accelerare le reazioni anche più di un milione di volte 2) escono immodificati e di nuovo efficienti alla fine della catalisi. 3) sono efficaci in piccole quantità. 4) non influenzano l equilibrio chimico di una reazione reversibile. Essi rendono più veloce il processo in entrambe le direzioni. L equilibrio chimico viene semplicemente raggiunto prima. 5) sono, in genere, altamente specifici. Taluni hanno una specificità assoluta Importanza dei cofattori I cofattori sono i coenzimi, molecole organiche estremamente importanti per la funzione degli enzimi, in genere vitamine idrosolubili oppure gli ioni metallici che in genere operano sulla struttura enzimatica permettendole di combinarsi col substrato.
2 Se il coenzima è legato covalentemente alla proteina si parla di oloenzima, enzima biologicamente attivo.la proteina prende il nome di apoenzima. I coenzimi sono pochi e li ritroviamo, sempre gli stessi, in numerosi enzimi. Essi si consumano nelle reazioni enzimatiche e vengono rigenerati in altre reazioni che avvengono in compartimenti cellulari diversi Meccanismo d azione degli enzimi La reazione di catalisi enzimatica avviene all interno di una tasca della proteina chiamata sito attivo. La molecola che si lega all enzima e su cui l enzima opera si chiama substrato. Gli enzimi, fondamentalmente, stabilizzano lo stato di transizione (ES) che è la specie molecolare a maggior contenuto energetico. Si usa indicare con S il substrato su cui l enzima opera la trasformazione (catalisi) ed E l enzima. Tutto il meccanismo parte dalla formazione del complesso enzima-substrato ES ed avviene secondo lo schema: E + S ES EP E + P dove ES è il complesso enzima-substrato ed EP il complesso enzima-substrato modificato, ovvero il prodotto P. La reazione è reversibile. Come si vede l enzima esce immodificato dalla reazione e il substrato ha invece subito la trasformazione operata dall enzima ed è il prodotto della catalisi. Una reazione chimica spontanea avviene dopo che si è superata una barriera energetica, energia di attivazione, necessaria per favorire l allineamento degli orbitali di legame e gli urti tra i reagenti. Tali urti, proporzionali alla concentrazione dei reagenti sono definiti urti utili. La velocità con cui questa reazione avviene dipende dal movimento casuale delle molecole che è proporzionale alla temperatura. Gli enzimi catalizzano le reazioni abbassando l energia di attivazione Nelle reazioni spontanee il contenuto d energia libera dei reagenti (substrato in questo caso) è maggiore di quella del prodotto. Nella figura A si vede l'andamento di una reazione esoergonica (spontanea) non catalizzata. Il picco massimo è l'energia d'attivazione che occorre superare affinché la reazione proceda. La figura B mostra l andamento della reazione catalizzata in cui si può osservare come lo stato di transizione sia ad un livello di energia molto più bassa.
3 Abbassando l energia d attivazione, si avranno un numero superiore di molecole in grado di superarla senza ricorrere ad aumenti di temperatura. Nel grafico (B) si possono osservare le tappe descritte e gli stati di transizione che corrispondono ai punti di maggior impegno energetico, in cui è possibile il ritorno verso i reagenti. Per questo sono i momenti più critici della reazione. I complessi ES ed EP invece sono i momenti di maggiore stabilità energetica. Superato l ultimo stato di transizione la reazione libera il prodotto (substrato modificato) e l enzima esce immodificato pronto per una nuova catalisi. L azione dell enzima è quindi quella di abbassare l energia di attivazione in modo selettivo costringendo i reagenti ad avvicinarsi, orientarne gli atomi in modo che si possano formare o rompere i legami. Gli enzimi sono proteine globulari complesse nella cui struttura terziaria si può individuare una zona specifica, chiamata sito attivo, in cui avviene la reazione col substrato e la sua trasformazione nel prodotto specifico. Il meccanismo d azione dell enzima è spesso paragonato a quello della chiaveserratura per evidenziarne la specificità. In termini molecolari è chiaro che esistono delle zone in cui, in modo altamente specifico, si possono formare legami tra la residui aminoacidici della proteina enzimatica e il substrato. Non raramente il sito attivo dell enzima è la zona nella quale è presente il gruppo prostetico la cui funzione è sempre di primaria importanza nella catalisi. Il modello chiave-serratura per esemplificare l azione di un enzima è largamente intuitivo ma anche decisamente insufficiente per comprendere il delicato processo di legame di un enzima con il suo substrato, la catalisi e la liberazione del prodotto. Ci possiamo chiedere come è possibile questo enorme aumento della velocità indotto dagli enzimi. e da dove arriva l'energia necessaria ad abbassare l'energia d'attivazione di una reazione?
4 I gruppi funzionali nel sito attivo (residui aminoacidici, ioni metallici, coenzimi) reagiscono col substrato generando una via della reazione a bassa energia ricavata dalle numerose interazioni deboli non covalenti, le stesse che stabilizzano le proteine: legami idrogeno, forze di van Der Waals, interazioni idrofobiche ed ioniche. Queste interazioni, esoergoniche, sono fondamentali per la formazione del complesso ES e ne determinano la stabilità La somma di questo rilascio di piccole quantità di energia, chiamata energia di legame, è la fonte principale di energia libera necessaria per abbassare l'energia d'attivazione. In definitiva, le interazioni deboli che portano alla formazione del complesso ES sono le forze che contribuiscono alla catalisi. Per avere la massima efficacia l'enzima dovrà avere solo una parziale complementarietà al S ma dovrà essere totalmente complementare allo stato di transizione ES. Così anche la elevata specificità di un enzima, che è la proprietà di distinguere molecole simili, si può spiegare con la caratteristica disposizione dei gruppi funzionali nel sito attivo che se formano interazioni perfette con un determinato substrato nello stato di transizione, non potranno farlo con un substrato simile ma non identico. Da un punto di vista strettamente molecolare il sito attivo si orienta in modo tale da portare i gruppi specifici del sito attivo in condizioni di massima efficienza per la catalisi. Questo adattamento porta ad una modificazione conformazionale dell'enzima indotta da uno specifico substrato. Proprietà degli enzimi 1. Gli enzimi sono sensibili al calore, e possono essere danneggiati (il termine chimico corretto è denaturati) facilmente per eccesso di freddo o di caldo. Queste due cause possono modificare irreparabilmente il sito attivo : danneggiando il sito attivo non si forma il complesso enzima-substrato. 2. Gli enzimi sono creati nelle cellule ma sono capaci di funzionare anche fuori di essa.questo consente agli enzimi di essere immobilizzati senza distruggerli. 3. Gli enzimi sono sensibili al ph, il tasso al quale possono condurre una reazione è dipendente dal ph.un esempio è la pepsina che funziona in presenza di ph vicino a 2. Invece l'amilasi salivare raggiunge il massimo rendimento con un ph neutro, cioè vicino a Gli enzimi sono riutilizzabili ed alcuni enzimi sono capaci di catalizzare centinaia di migliaia di reazioni ogni secondo. 5. Ogni enzima è specifico cioè può catalizzare una sola reazione. 6. Gli enzimi lavorano anche in modo da raggiungere la quantità desiderata e mai in eccesso: quando si forma un eccesso di composto, smettono di produrlo finché il sistema non è tornato in equilibrio.
5 Classificazione degli enzimi Ossidoreduttasi: ossidazione, deidrogenazione e riduzione in presenza di coenzimi o accettori di idrogeno - Transferasi: trasferimento di radicali (aminici, carbossilici, ecc.) - Idrolasi: idrolisi di legami peptidici (proteasi), esterici (esterasi, fosfatasi, nucleotidasi) e glucosidici (glucosidasi, glucuronidasi) - Sintetasi: reazioni di sintesi di due o più molecole con l ausilio di energia fornita da nucleotidi trifosfati - Isomerasi: interconversione di isomeri - Liasi: rottura di un legame C -C, C -O, C -N, C -S con formazione di un doppio legame; saturazione di un doppio legame per introduzione di H 2 0, H 2 S, NH 3. Cinetica enzimatica Lo studio della velocità delle reazioni catalizzate da enzimi parte considerando gli effetti della [ S ], concentrazione del substrato che, naturalmente, varia nel corso della reazione essendo S trasformato in P. Allora ponendo in vitro una [ S ] molto superiore a quella dell'enzima si può calcolare la V 0, velocità iniziale, considerando la variazione di [ S ] trascurabile. Il grafico mostra l' effetto dell'aumento della concentrazione di substrato sulla velocità iniziale di una reazione catalizzata da un enzima. La velocità aumenta esponenzialmente fino a raggiungere un plateau che rappresenta la velocità massima che non varia anche con aggiunte successive di substrato. Questa velocità si raggiunge quando tutto l enzima è saturato dal substrato. La velocità della reazione è data dall equazione di Michaelis-Menten che lega la velocità ad una costante, la Km, caratteristica per ogni enzima e che è utile conoscere perché ci fornisce una misura dell affinità di un enzima per il suo suo substrato. V max [S] V 0 = Km +[S]
6 Poiché è difficile calcolare la velocità massima, ci conviene calcolare ½ Vmax, sostituendo questo valore a V 0. V max [S] [S] da cui sostituendo: Vmax = ; 1 = e Km = [S] 2 Km+ [S] 2 Km+ [S] V 0 = ½ Vmax Dalla relazione si evince che gli enzimi con una Km alta, hanno una minore affinità per il loro substrato e viceversa. L esochinasi, enzima presente nelle cellule del cervello, ha una Km di circa 400 volte più piccola della glucochinasi che catalizza la stessa reazione nel fegato: la fosforilazione del glucosio. Il motivo risiede nelle piccole concentrazioni di glucosio presenti nel circolo encefalico e dalla necessità che le cellule nervose hanno di utilizzarlo anche in basse concentrazioni. Gli inibitori enzimatici Gli enzimi, oltre a catalizzare le reazioni, intervengono nei processi di regolazione metabolica. Quindi saranno necessari meccanismi di attivazione o di inibizione enzimatica. Le sostanze che inibiscono gli enzimi sono potenti agenti farmacologici. Per esempio l'aspirina inibisce il primo enzima della sintesi delle prostaglandine che partecipano al processo della produzione del dolore. Gli enzimi catalizzano tutti i processi che avvengono all interno delle cellule. Sfruttando l inibizione enzimatica sono stati creati alcuni fra i più importanti agenti farmaceutici. La stessa aspirina inibisce l enzima catalizzatore della prima reazione della sintesi delle prostaglandine. Esistono due classi di inibitori enzimatici: quelli reversibili e quelli irreversibili. Uno dei comuni tipi di inibizione reversibile è definita competitiva. Un inibitore competitivo, compete con il substrato per il legame al sito attivo di un enzima, e la reazione viene impedita a causa dell inibitore (I) legato, poichè impedisce fisicamente al substrato di legarsi all enzima. Essendo l inibizione di natura reversibile è possibile spostare l azione enzimatica a favore del substrato semplicemente aggiungendone dell altro all ambiente. Questo diminuisce le probabilità che un enzima si leghi ed un inibitore, consentendo così la normale catalisi.
7 Nella categoria degli inibitori reversibili rientrano anche gli inibitori non competitivi e gli inibitori in competitivi. L inibizione non competitiva si lega ad un sito distinto da quello preposto a legare il substrato senza interferire quindi con il legame ES, tuttavia questo legame inattiva l enzima, tanto in presenza che in assenza di S. L inibitore non competitivo riduce la quantità di enzima attivo abbassando di fatto la V max. L inibizione incompetitiva funziona come l inibizione non competitiva ma, al contrario di questa il cui inibitore si lega all enzima, l inibitore incompetitivo si lega solo a complessi ES. Gli inibitori irreversibili modificano o distruggono un gruppo funzionale dell enzima, essenziale per la sua funzione. Una classe particolare di inibitori irreversibili è quella degli inibitori suicidi, relativamente poco reattivi se non quando raggiungono il sito attivo di un dato enzima. Questi inibitori portano avanti le prime tappe di una normale reazione, ma invece di essere trasformati nel prodotto previsto, vengono convertiti in prodotti molto reattivi che si combinano in maniera irreversibile con l enzima. La regolazione enzimatica È chiaro che in un organismo le vie metaboliche debbano funzionare con una coordinazione tale che siano attive solo quelle necessarie al momento e inibite quelle che non servono, in quel momento, alla vita di una cellula. Vi sono enzimi particolari che operano nella catena metabolica, attivandola o inibendola secondo la richiesta e la concentrazione ottimale del prodotto finale che concorrono a produrre. A sua volta questo importante enzima chiamato enzima regolatore, è controllato dall organismo attraverso vari sistemi come la stimolazione o l inibizione a produrre quel determinato enzima mediante ormoni o neurotrasmettitori. L enzima regolatore determina quindi la velocità complessiva di una catena metabolica. Nelle vie metaboliche vi sono due classi di enzimi regolatori: gli enzimi allosterici che agiscono mediante un legame reversibile di un metabolita regolatore chiamato modulatore o effettore e gli enzimi regolati mediante modificazioni covalenti reversibili.
8 Gli enzimi allosterici Gli enzimi allosterici hanno quasi sempre una struttura quaternaria (più subunità polipeptidiche) e possiedono, oltre al sito attivo in una subunità, anche un altro sito, sito regolatore in un'altra subunità, al quale si lega l effettore (o modulatore). L enzima esiste in due configurazioni tra loro convertibili. In una subunità troviamo il sito regolatore che può essere nella configurazione attivata oppure in quella inattivata. Se il modulatore induce una attivazione della catena metabolica allora esso si lega al sito regolatore dell enzima stimolando il sito attivo, situato generalmente in altra subunità, a legarsi col substrato. Al contrario, se il modulatore è un inibitore, si avrà la perdita di affinità sul sito attivo dell enzima. Tale condizione determina il blocco della via metabolica. Inibizione allostrerica In alcuni sistemi multienzimatici l'enzima regolatore viene inibito in modo specifico dal prodotto finale della via, quando tale prodotto si accumula oltre le necessità delle cellule. In genere l'enzima allosterico è il primo della via metabolica. Questa inibizione si chiama inibizione retroattiva o inibizione da prodotto (meccanismo a feedback). Nei batteri è attiva una via metabolica che converte, attraverso cinque reazioni, un aminoacido, la L-treonina in un altro aminoacido, la isoleucina. Il primo enzima di questa via metabolica è la treonina deidratasi (E 1 ) e viene inibito allostericamente, con meccanismo a feedback, dalla isoleucina. È ovvio che quando la Isoleucina, che funziona da effettore o modulatore, viene utilizzata dalla cellula e la sua concentrazione diminuisce, essa si stacca dall enzima allosterico che ritorna nella conformazione attivata e il sito attivo ritorna affine alla L-Treonina e la via metabolica riprende la sua attività. La cinetica enzimatica, con gli enzimi allosterici, ci fornisce curve di velocità con andamento sigmoide e non iperbolico. Il valore della V max non cambia mentre cambia quello della K m che diminuisce in caso di effettore positivo ed aumenta in caso di effettore negativo.
9 Altri meccanismi di regolazione enzimatica si hanno quando l enzima viene modificato covalentemente da alcuni gruppi chimici come il fosfato, l adenosina monofosfato, l uridina monofosfato e i gruppi metilici. Questi gruppi possono legarsi all enzima ed essere rimossi da altri enzimi. Un enzima appartenente a questa categoria è la glicogeno fosforilasi che regola nel muscolo e nel fegato il processo di demolizione del glicogeno. Un esempio interessante del meccanismo di regolazione enzimatica è dato da due effettori importanti come la calmodulina, in tutte le cellule, e la troponina nelle cellule muscolari. Essi sono attivati, all interno delle cellule, dalla presenza di ioni Ca 2+ che è normalmente bassa rispetto a quella dell ambiente extracellulare con un gradiente di circa volte. La cellula, in condizioni normali, non fa passare gli ioni Ca, opponendosi alla naturale tendenza mantenendo chiusi i canali proteici. Sappiamo che la contrazione muscolare avviene quando la cellula apre i canali proteici agli ioni Ca 2+ ; in queste condizioni la troponina viene attivata, altrimenti, vista la bassa concentrazione degli ioni Ca, essa è una molecola inattiva. Un segnale nervoso fa aprire i canali proteici, gli ioni Ca 2+ passano attraverso la membrana e si legano alla troponina che viene così attivata. La troponina, funziona da effettore attivando un enzima che determina la contrazione muscolare. In questo meccanismo è interessante notare la connessione che c è tra un segnale nervoso e la sua traduzione in attività chimica precisa. La concentrazione degli enzimi allosterici è generalmente molto bassa nelle cellule e la loro sintesi viene stimolata o inibita da specifici ormoni che operano a livello genico.
10 L insulina, ad esempio esplica la sua azione stimolando la sintesi degli enzimi glucochinasi, fosfofruttochinasi e glicogeno sintetasi, reprimendo quella degli enzimi della biosintesi del glucosio, rispettando il suo effetto ipoglicemizzante. È interessante osservare che le vie anaboliche e quelle cataboliche sono sempre localizzate in organelli e compartimenti cellulari diversi in modo che gli enzimi che controllano una via catabolica, non controllino contemporaneamente anche quella anabolica. La compartimentazione è un metodo efficiente della gestione dell attività cellulare.
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Regolazione del metabolismo del glucosio
 Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Attivitá e cinetica enzimatica
 Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
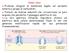 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
glicogeno Glucosio 6-P Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Il metabolismo del glicogeno e la gluconeogenesi. Copyright 2013 Zanichelli editore S.p.A.
 Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco.
 Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Il glicogeno (riserva di glucosio) è immagazzinato nel fegato e nei muscoli (con finalità diverse )
 Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti:
 Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono
 Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
L adattamento dei batteri. Strategie di adattamento
 L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA
 CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
ALIMENTAZIONE NELL UOMO
 ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
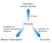 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Enzimi. Nomenclatura:
 Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
scaricato da www.sunhope.it
 Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
La catalasi: un enzima in azione
 Percorso di Didattica laboratoriale La catalasi: un enzima in azione Scuola Secondaria di Secondo Grado IISS - IPSIA E. Majorana Bari Classe IV B Docente: Miralma Serio Organizzatore cognitivo: Le trasformazioni
Percorso di Didattica laboratoriale La catalasi: un enzima in azione Scuola Secondaria di Secondo Grado IISS - IPSIA E. Majorana Bari Classe IV B Docente: Miralma Serio Organizzatore cognitivo: Le trasformazioni
V= R*I. LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro.
 LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
Mais, riso, patate, granozucchero di canna o barbabietola Latte da zucchero Polisaccaride Amido - - Disaccaride Maltosio Saccarosio Lattosio
 Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
FARMACODINAMICA RECETTORI ED EFFETTORI
 FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
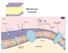 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Dal DNA all RNA. La trascrizione nei procarioti e negli eucarioti
 Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
Temperatura. V(t) = Vo (1+at) Strumento di misura: termometro
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
unità C2. Le trasformazioni energetiche nelle cellule
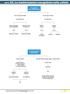 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
RNA polimerasi operone. L operatore è il tratto
 La regolazione genica nei procarioti Alcune proteine vengono prodotte dalla cellula ad un ritmo relativamente costante e l attività dei geni che codificano queste proteine non è regolata in modo sofisticato.
La regolazione genica nei procarioti Alcune proteine vengono prodotte dalla cellula ad un ritmo relativamente costante e l attività dei geni che codificano queste proteine non è regolata in modo sofisticato.
1) FIBRE ROSSE A CONTRAZIONE LENTA (Tipo I) 2) FIBRE BIANCHE INTERMEDIE (Tipo IIa) 3) FIBRE BIANCHE A CONTRAZIONE RAPIDA (Tipo IIb)
 LE FIBRE MUSCOLARI La fibra muscolare è considerata l' unità funzionale del muscolo scheletrico o, più semplicemente, una delle tante cellule che lo compongono. Ogni muscolo è infatti formato da un certo
LE FIBRE MUSCOLARI La fibra muscolare è considerata l' unità funzionale del muscolo scheletrico o, più semplicemente, una delle tante cellule che lo compongono. Ogni muscolo è infatti formato da un certo
ossigeno e ne facilita la diffusione dai capillari all ambiente intracellulare.
 Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
Il modello generale di commercio internazionale
 Capitolo 6 Il modello generale di commercio internazionale [a.a. 2013/14] adattamento italiano di Novella Bottini (ulteriore adattamento di Giovanni Anania) 6-1 Struttura della presentazione Domanda e
Capitolo 6 Il modello generale di commercio internazionale [a.a. 2013/14] adattamento italiano di Novella Bottini (ulteriore adattamento di Giovanni Anania) 6-1 Struttura della presentazione Domanda e
 forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Cinetica enzimatica Inibitori enzimatici
 Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Tecnologia e Tradizione nella produzione del vino
 Scuola secondaria di 1 grado A. Moro Mesagne Tecnologia e Tradizione nella produzione del vino BRINDISI DOC Vino rosso a denominazione di origine controllata prodotto nella zona di Mesagne e Brindisi A
Scuola secondaria di 1 grado A. Moro Mesagne Tecnologia e Tradizione nella produzione del vino BRINDISI DOC Vino rosso a denominazione di origine controllata prodotto nella zona di Mesagne e Brindisi A
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Il metabolismo dell RNA. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Laboratorio di Tecniche Microscopiche AA 2007-2008 Lezione 12 Marzo 2008 Ore 15-16
 Laboratorio di Tecniche Microscopiche AA 2007-2008 Lezione 12 Marzo 2008 Ore 15-16 L'immunoistochimica e' una tecnica ampiamente utilizzata per l'identificazione e la localizzazione di costituenti cellulari
Laboratorio di Tecniche Microscopiche AA 2007-2008 Lezione 12 Marzo 2008 Ore 15-16 L'immunoistochimica e' una tecnica ampiamente utilizzata per l'identificazione e la localizzazione di costituenti cellulari
Metabolismo degli amminoacidi. Ciclo dell urea
 Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Lo sviluppo del cancro è un processo complesso che coinvolge parecchi cambiamenti nella stessa cellula staminale. Poiché tutte le cellule staminali
 Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare.
 Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
La digestione degli alimenti
 La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali
 Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
Regolazione della trascrizione. Operoni catabolici nei procarioti (controllo negativo)
 Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
COS'E' UN IMPIANTO FOTOVOLTAICO E COME FUNZIONA
 COS'E' UN IMPIANTO FOTOVOLTAICO E COME FUNZIONA Il principio di funzionamento: la cella fotovoltaica Le celle fotovoltaiche consentono di trasformare direttamente la radiazione solare in energia elettrica,
COS'E' UN IMPIANTO FOTOVOLTAICO E COME FUNZIONA Il principio di funzionamento: la cella fotovoltaica Le celle fotovoltaiche consentono di trasformare direttamente la radiazione solare in energia elettrica,
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Lezione di oggi (Lunedì 19 Novembre)
 Lezione di oggi (Lunedì 19 Novembre) ADATTAMENTI METABOLICI INDOTTI DALL ALLENAMENTO Obiettivi della lezione Scoprire come l allenamento possa ottimizzare il rendimento dei sistemi energetici e sviluppare
Lezione di oggi (Lunedì 19 Novembre) ADATTAMENTI METABOLICI INDOTTI DALL ALLENAMENTO Obiettivi della lezione Scoprire come l allenamento possa ottimizzare il rendimento dei sistemi energetici e sviluppare
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Amplificatori Audio di Potenza
 Amplificatori Audio di Potenza Un amplificatore, semplificando al massimo, può essere visto come un oggetto in grado di aumentare il livello di un segnale. Ha quindi, generalmente, due porte: un ingresso
Amplificatori Audio di Potenza Un amplificatore, semplificando al massimo, può essere visto come un oggetto in grado di aumentare il livello di un segnale. Ha quindi, generalmente, due porte: un ingresso
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Genova 15 01 14 TIPOLOGIE DI LAMPADE
 Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
