Elisa Maria Platania
|
|
|
- Sara Catalano
- 8 anni fa
- Просмотров:
Транскрипт
1 UNIVERSITÀ DEGLI STUDI DI CATANIA DIPARTIMENTO DI SCIENZE DEL FARMACO Scuola di Specializzazione in Farmacia Ospedaliera Elisa Maria Platania Modello di Governo Clinico Integrato UFA-ONCO-EMA: Progetto Pilota Regionale presso l ARNAS Garibaldi di Catania TESI DI SPECIALIZZAZIONE Relatore: Chiar.mo Prof. Giovanni Puglisi Correlatore: Preg.ma Dott.ssa Giuseppina Fassari ANNO ACCADEMICO
2 INDICE 1. Introduzione... pag Quadro normativo 2.1 Gestione centralizzata... pag Raccomandazioni Ministeriali... pag Decreti assessoriali Regione Sicilia... pag Modello di governo clinico UFA-ONCO-EMA... pag Progetto pilota presso l ARNAS Garibaldi di Catania 4.1 Presupposti del progetto... pag Fasi del progetto... pag Modello integrato UFA-ONCO-EMA validato e certificato... pag Mission e politica di miglioramento... pag Gestione delle risorse umane e strumentali-tecnologiche... pag Processi di gestione del farmaco antitumorale... pag Strumenti di verifica e monitoraggio del modello... pag Procedura di gestione della terapia antitumorale 5.1 Approvvigionamento dei farmaci... pag Presa in carico del paziente... pag. 36 1
3 5.2.1 Indicatori presa in carico del paziente... pag Prescrizione... pag Indicatori prescrizione... pag Validazione della richiesta di allestimento... pag Elaborazione della documentazione... pag Preparazione... pag Operazioni preliminari all allestimento dei farmaci... pag Modalità di manipolazione e diluizione in cappa... pag Pulizia delle cappe di lavoro e smaltimento dei rifiuti... pag Indicatori preparazione... pag Distribuzione... pag Contenitori per trasporto dei chemioterapici... pag Compilazione bolla di accompagnamento... pag Indicatori distribuzione... pag Somministrazione... pag Procedure specifiche... pag Indicatori somministrazione... pag Dispensazione della terapia orale antitumorale... pag Indicatori dispensazione della terapia orale antitumorale... pag Immagazzinamento, conservazione e gestione scorte... pag. 67 2
4 6. Sezione sperimentale 6.1 Risultati indicatori di performance anno pag Risultati indicatori di performance anno pag Conclusioni... pag. 81 Bibliografia... pag. 83 Ringraziamenti... pag. 85 3
5 1. INTRODUZIONE Negli ultimi anni abbiamo assistito ad enormi progressi nell ambito della medicina oncologica. Questo dato è un segno inequivocabile del successo delle strategie messe in atto per il controllo del cancro quali la prevenzione primaria, la diagnosi precoce ed il trattamento della malattia. L incremento sempre maggiore della patologia oncologica la cui cura necessita di una terapia individuale con dosaggio personalizzato, in funzione delle diverse tipologie tumorali e delle condizioni fisiche del paziente, richiede un adeguata struttura ed organizzazione ospedaliera. Inoltre il basso indice terapeutico di questi farmaci, la necessità di contrastare la loro tossicità attraverso dosaggi personalizzati con somministrazione secondo sequenze predefinite e la contemporanea assunzione di altri farmaci specificatamente finalizzati al controllo e alla riduzione della tossicità sono elementi che generano serie probabilità di errore che, congiuntamente agli obblighi espressamente previsti dalle procedure tecnico-farmaceutiche di allestimento, richiedono l adozione di specifiche misure per garantire il contenimento del rischio. La centralizzazione della gestione dei farmaci antiblastici, oltre che un obbligo di legge, diventa una strategia efficace per garantire la qualità della preparazione, la salvaguardia dei lavoratori, la sicurezza per il paziente e la riduzione dei rischi di contaminazione ambientale. Nel corso degli ultimi anni la gestione della terapia antitumorale è passata dalla dimensione di 4
6 U.Ma.C.A. (Unità di Manipolazione Centralizzata Antiblastici) a quella di U.F.A. (Unità Farmaci Antitumorali) proprio perché la manipolazione non è l unica attività connessa alla gestione di questi farmaci. La Farmacopea Ufficiale (FU) XII edizione assimila l attività di manipolazione di farmaci antiblastici all attività di galenica magistrale e quindi prevede specifici requisiti di sicurezza e qualità che possono essere massimamente assicurati attraverso la realizzazione di un processo controllato e validato che un UFA deve garantire. La chemioterapia antiblastica richiede una stretta personalizzazione del dosaggio della terapia, infatti, per ottenere dose e forma di medicamento in oncologia occorre spesso modificare le dosi e la manipolazione che ne deriva trasforma le specialità medicinali in preparati galenici magistrali da preparare obbligatoriamente in farmacia 1. La riconduzione degli antiblastici personalizzati ai preparati di galenica clinica ha un risvolto molto importante sulla qualità del prodotto finito, dovendo questi essere allestiti, come tutti i preparati galenici, seguendo le condizioni operative indicate nelle Norme di Buona Preparazione (NBP) della FU e le Good Manufacturing Practice (GMP). 2 L attività di galenica clinica, tuttavia, non si esaurisce con la realizzazione di un prodotto sterile in cui la responsabilità del farmacista è limitata alla assicurazione della compatibilità e della correttezza del dosaggio ma presuppone azioni di governo clinico che rafforzino le sinergie tra i professionisti coinvolti nel processo terapeutico. 5
7 L erogazione dei trattamenti farmacologici antitumorali, infatti, è sottesa da un complesso processo che vede coinvolte numerose figure professionali afferenti a differenti discipline e che può configurarsi come una vera e propria articolazione funzionale interdipartimentale; come tale la gestione della terapia oncologica deve essere dotata di un sistema organizzativo sofisticato e di strumenti di controllo sensibili ed affidabili, concepiti al fine di garantire il rispetto dell appropriatezza clinica, prescrittiva e gestionale, livelli qualitativi ottimali del prodotto finale, sicurezza delle procedure e contenimento dei costi. Nel nuovo scenario che si viene a configurare, la figura del farmacista diventa centrale nell ambito del team multidisciplinare che si occupa della gestione della patologia tumorale grazie alle sue molteplici e specifiche conoscenze a garanzia e supporto dell appropriatezza delle cure. 3 6
8 2. QUADRO NORMATIVO 2.1 GESTIONE CENTRALIZZATA La gestione centralizzata dei farmaci antiblastici risponde a specifiche disposizioni di legge che si sono sviluppate nel corso degli anni. La legge 448 del 23 dicembre 1998 Misure di finanza pubblica per la stabilizzazione e lo sviluppo all articolo 68 (comma 6) sancisce che dal 1 gennaio 1999 i medicinali antiblastici iniettabili sono erogati a carico del Servizio Sanitario Nazionale (S.S.N.) esclusivamente attraverso le strutture ospedaliere o le altre strutture accreditate in regime di ricovero, dayhospital (DH) o assistenza domiciliare. 4 Successivamente nel decreto legislativo (D.Lgs.) 18 febbraio 1999 Modifica del regime di fornitura dei medicinali antiblastici iniettabili il Ministero della Sanità, sulla base di un riesame da parte della Commissione Unica del Farmaco, ha assoggettato i medicinali antiblastici iniettabili in medicinale utilizzabile esclusivamente in ambiente ospedaliero o in ambiente ad esso assimilabile", in ragione delle loro caratteristiche farmacologiche o per esigenze di tutela della salute dei pazienti. 5 Inoltre, il D.Lgs. 14 luglio 1999 Modalità di dispensazione dei medicinali antiblastici iniettabili stabilisce che i medicinali antiblastici iniettabili possono essere erogati a carico del S.S.N. soltanto mediante la loro somministrazione presso le strutture ospedaliere o le altre strutture 7
9 accreditate, in regime di ricovero o DH o trattamento ambulatoriale, o di ospedalizzazione domiciliare. 6 Dunque, il D.Lgs 18 febbraio 1999 ed il D.Lgs 14 luglio 1999 introducono la problematica sulla fornitura, dispensazione e manipolazione sicura dei farmaci antitumorali. I chemioterapici antiblastici iniettabili diventano a tutti gli effetti farmaci ospedalieri ovvero farmaci in fascia H cioè gestiti da sole aziende ospedaliere o strutture accreditate, in regime di ricovero o DH o trattamento ambulatoriale o di ospedalizzazione domiciliare. Le motivazioni che sono alla base della norma che colloca questi farmaci in fascia H sono molteplici e riguardano aspetti medico-scientifici e aspetti organizzativi. Dal punto di vista medico-scientifico è importante sottolineare che: la maggioranza dei protocolli terapeutici prevede la somministrazione di farmaci in combinazioni poli-chemioterapiche secondo precisi criteri di somministrazione, sequenze di erogazione, rispetto dei dosaggi e tempi di riciclo; i protocolli di terapia antiblastica sono stabiliti secondo piani terapeutici complessi, diversi da patologia a patologia, spesso multidisciplinari elaborati da competenze specialistiche di appartenenza ospedaliera; i singoli farmaci antiblastici e i diversi regimi di combinazione sono gravati da importanti e spesso pericolosi effetti collaterali talora immediati, più frequentemente dilazionati nel tempo, che debbono 8
10 essere tempestivamente riconosciuti e che richiedono appropriate misure preventive ed adeguati trattamenti di supporto, possibili solo in particolari condizioni di assistenza, quali il regime di ricovero ordinario, il DH, l ambulatorio divisionale e l ospedalizzazione domiciliare; sono anche frequenti i rischi di lesioni necrotico-ulcerative dei tessuti molli nella sede d inoculazione in seguito a stravaso del farmaco; durante tutto il programma terapeutico possono rendersi necessarie modifiche dei dosaggi e delle modalità di somministrazione dei chemioterapici conseguenti sia alla comparsa di effetti collaterali sfavorevoli, sia alla valutazione del grado di sensibilità della neoplasia al trattamento in atto, modifiche che sono di stretta competenza specialistica e quindi gestibili solo nell ambito di un adeguato programma terapeutico. Le motivazioni tecnico-gestionali riguardano: lo smaltimento dei chemioterapici; la protezione degli operatori sanitari addetti alla preparazione dei farmaci antiblastici. Proprio in riferimento a quest ultimo punto sono state emanate numerose norme al fine di contenere il rischio degli operatori professionalmente esposti agli antiblastici. Tali farmaci per quanto siano necessari a fini terapeutici, molto spesso risultano essere cancerogeni qualora fossero assorbiti da soggetti sani. Nonostante numerosi chemioterapici antiblastici 9
11 siano stati riconosciuti dalla IARC (International Agency for Research on Cancer) come cancerogeni o probabili cancerogeni per l uomo a queste sostanze non si applicava alcuna norma di prevenzione poiché farmaci utilizzati a scopo terapeutico. Solo nel 1995, la Commissione Consultiva Tossicologica Nazionale ha raccomandato l inclusione nel D.Lgs. 626 del 19 settembre 1994, che argomenta i problemi sulla tutela della salute dei lavoratori, delle attività di preparazione, impiego e smaltimento, dei farmaci antiblastici allo scopo di tutelare la salute del personale ospedaliero professionalmente esposto a sostanze cancerogene. Successivamente il Ministero della Sanità, nel Piano Sanitario Nazionale , pone tra gli obiettivi per la difesa e la tutela della salute pubblica, interventi atti a migliorare la sicurezza dei luoghi di lavoro, focalizzando l attenzione soprattutto sulle strutture sanitarie, sia pubbliche sia private, in base alle disposizioni di prevenzione stabilite dal D.Lgs. 626 del 19 settembre 1994 e successive modifiche ed integrazioni. 7 Tale decreto prevede, infatti, l effettuazione della preparazione degli antiblastici in ambiente protetto e con idonea aspirazione localizzata realizzata tramite cappe a flusso laminare verticale di classe ІІ B mediante filtro assoluto HEPA (High Efficiency Particulate Air filter) il quale rappresenta il sistema più efficiente per la captazione della contaminazione particellare garantendo la protezione dell operatore, l asetticità del prodotto e la conformità della preparazione alle NBP della FU. 10
12 Una seconda normativa mirata alla tutela dei lavoratori che manipolano i chemioterapici antiblastici è il Provvedimento Ministeriale del 5 agosto 1999 pubblicato nella Gazzetta Ufficiale n. 236 del 7 ottobre 1999, che individua le Linee Guida per la sicurezza e la salute dei lavoratori esposti a chemioterapici antiblastici in ambiente sanitario. In tali Linee Guida è affrontato il problema dell esposizione a miscele di chemioterapici, in quanto considerato uno dei rischi rilevanti per la salute dei lavoratori in ambiente sanitario; inoltre, vengono forniti gli indirizzi relativi alla valutazione dell esposizione, alla sorveglianza sanitaria, alle misure di prevenzione, alle modalità operative, ai carichi lavorativi, alla suscettibilità individuale, utili alla prevenzione del rischio medesimo, considerata la possibile cancerogenicità di alcuni farmaci antiblastici. Il provvedimento prevede che sia necessario il controllo di tutte le fasi della gestione del farmaco: della manipolazione, della somministrazione e dello smaltimento mediante il governo centralizzato attraverso l attivazione di un UFA a cui affidare l intero ciclo lavorativo. L UFA deve avere le seguenti caratteristiche ovvero deve essere: centralizzata: per impedire lo svolgimento senza controllo di attività a rischio, realizzando nel contempo un non trascurabile risparmio economico; isolata: in modo che, anche strutturalmente, risulti circoscritta e ben identificabile rispetto al restante ambiente sanitario; 11
13 chiusa: per cui i materiali utilizzati nella manipolazione possano essere depositati in un unico luogo, dal quale si possano recuperare con la garanzia di un rapido e totale smaltimento e del soddisfacimento dei criteri di prevenzione e di protezione ambientale; protetta: per consentire l accesso al solo personale sanitario autorizzato; segnalata: con appositi segnali di rischio. 8 In UFA è prevista la presenza di quattro aree (Fig.1): 1) Camera bianca 2) Zona filtro 3) Magazzino 4) Uffici Fig.1 Esempio di UFA 12
14 L accesso alla camera bianca prevede il passaggio attraverso una zona filtro nel quale sono presenti tutti i dispositivi di protezione individuale (DPI) ed in cui sono installati dei dispositivi sonori che segnalano l apertura contemporanea della porta fra la camera bianca (zona di allestimento) e il corridoio/filtro, e tra quella che da quest ultima comunica con la restante parte dell UFA. La camera bianca deve essere fornita di cappe biologiche di classe ІІ B a flusso laminare verticale, di un punto di decontaminazione dotato di una doccia a pedale, di un lava occhi di sicurezza e di un interfono a viva voce per la comunicazione con l esterno così da evitare qualsiasi tipo di contaminazione dei guanti dell operatore. Nel magazzino i farmaci antiblastici vengono conservati e disposti in sicurezza all interno di armadi chiusi sotto la responsabilità del personale autorizzato, mentre gli uffici sono dedicati a tutte le attività di natura organizzativa e gestionale connesse con la preparazione degli antiblastici. Dunque, attraverso la centralizzazione degli antiblastici, e soprattutto grazie al plus valore aggiunto dalla professionalità del farmacista, viene certificata la qualità delle terapie del paziente che rappresenta l obiettivo primario cui rivolgere l attenzione. L attivazione di un UFA, infatti, permette di perseguire i seguenti obiettivi: gestione del rischio clinico e riduzione del rischio di errore: la sicurezza per il paziente sottoposto a terapia con antiblastici è correlata al controllo della formulazione e della realizzazione di preparati particolarmente critici in funzione sia della loro tossicità e tecnica di 13
15 preparazione sia della necessità di garantirne l asetticità di allestimento; il farmacista garantisce ed è responsabile dell organizzazione di un valido sistema integrato di controllo che risponde all esigenza fondamentale di salvaguardare la salute del paziente; sicurezza per i lavoratori professionalmente esposti: implica particolari cautele di manipolazione di sostanze e principi attivi comunque pericolosi che solo locali e personale dedicato possono tutelare e garantire; correttezza gestionale: assicurata dal più efficace monitoraggio delle prestazioni erogate e della spesa farmaceutica; ottimizzazione dell uso delle risorse e risparmio: grazie alla riduzione degli sprechi, all annullamento delle scorte di reparto e riutilizzo dei residui, mediante la razionalizzazione nella gestione delle terapie; appropriatezza e aderenza alle indicazioni ministeriali: attraverso la realizzazione del principio della dose unitaria cioè con la preparazione di antiblastici monodose per ogni singolo paziente; il governo clinico: la gestione centralizzata delle terapie antiblastiche presuppone la creazione di un team multidiscliplinare e predispone quindi alla condivisione delle tematiche, delle criticità e all attuazione delle migliori condizioni di espletamento delle cure. Queste azioni di governo clinico rafforzano ulteriormente le sinergie tra i professionisti coinvolti nel processo terapeutico, in particolare tra il medico oncologo e i farmacisti. 9 14
16 2.2 RACCOMANDAZIONI MINISTERIALI Nel descrivere le misure che devono essere adottate per garantire la sicurezza del paziente nella terapia oncologica, il Ministero della Salute ribadisce la necessità di centralizzare e controllare attraverso un modello integrato la gestione di tali farmaci mediante l attuazione ed implementazione delle Raccomandazioni Ministeriali. La Raccomandazione n. 7 del Ministero della Salute emanata nel marzo 2008 Raccomandazione per la prevenzione della morte, coma o grave danno derivanti da errore nella terapia farmacologica enuncia che il paziente ha diritto a ricevere non solo terapie efficaci ma anche sicure e quindi ogni possibile danno deve essergli evitato. La sicurezza dei pazienti e la riduzione degli errori in terapia farmacologica rappresentano una priorità dell assistenza sanitaria. La Raccomandazione n. 7 si applica a tutti i farmaci usati in ospedale con particolare riferimento ai farmaci considerati ad alto rischio o ad alto livello di attenzione ovvero farmaci che richiedono particolare attenzione nella gestione ed uso a causa della loro potenziale tossicità, del basso indice terapeutico e dell alta possibilità di interazioni tra cui rientrano anche gli antineoplastici. Inoltre, viene sottolineato come gli errori in terapia farmacologica si possono verificare durante tutto il processo di gestione del farmaco in ospedale: approvvigionamento, immagazzinamento, conservazione, prescrizione, preparazione, distribuzione, somministrazione 15
17 e monitoraggio. Tale Raccomandazione rappresenta uno strumento a supporto degli operatori da implementare in tutte le strutture sanitarie per evitare o minimizzare il rischio dell insorgenza dell evento sentinella dovuto ad un uso non corretto dei farmaci nell ambito dell assistenza ospedaliera. Per raggiungere tale obiettivo le Aziende sanitarie devono dotarsi di strumenti ed acquisire metodologie di lavoro per impostare un trattamento terapeutico che risulti corretto e completo in tutti i suoi aspetti e che risponda a requisiti di sicurezza tra i quali l adozione di procedure o protocolli aziendali codificati e condivisi tra gli operatori. 10 Successivamente, al fine di ridurre il rischio di errore nella terapia farmacologica specificatamente per l utilizzo di farmaci antiblastici è stata elaborata nell ottobre 2012 la Raccomandazione Ministeriale n. 14. Proprio a causa della elevata tossicità dei farmaci antineoplastici e del loro basso indice terapeutico, gli errori in corso di terapia oncologica determinano danni molto gravi anche alle dosi approvate. Pertanto, è necessario avere a disposizione indicazioni, condivise ed uniformi su tutto il territorio nazionale, mirate alla prevenzione di tali errori. Questa Raccomandazione ha come obiettivo la prevenzione degli errori in terapia con farmaci antineoplastici ai fini della sicurezza del paziente. È indirizzata a: Regioni e Province Autonome, Direzioni sanitarie/aziendali, responsabili della funzione aziendale dedicata alla gestione del rischio clinico, operatori sanitari coinvolti nella gestione dei farmaci antineoplastici sia nei reparti che nella Farmacia ospedaliera e trova applicazione nelle 16
18 strutture sanitarie pubbliche (ospedaliere, universitarie, istituti di ricovero e cura a carattere scientifico) e private (accreditate e non) e, in particolare, nelle Unità operative di Oncologia medica e di Ematologia, nelle Farmacie ospedaliere e, per alcuni aspetti peculiari, presso il domicilio del paziente. La Raccomandazione è a tutela dei pazienti che necessitano di cure con farmaci antineoplastici. La Raccomandazione n. 14 ribadisce che la possibilità di errore è presente in tutto il processo di gestione dei farmaci antineoplastici (approvvigionamento, immagazzinamento, prescrizione, preparazione, distribuzione, somministrazione): per questo, le strutture sanitarie devono elaborare una procedura, condivisa con gli operatori sanitari, monitorata e aggiornata periodicamente, che riporti tutte le indicazioni necessarie per evitare errori in terapia e garantire sicurezza e qualità delle cure. E importante analizzare tutte le fasi della filiera del farmaco antineoplastico e in maniera particolare quelle nelle quali è più stretto il legame tra paziente, operatore sanitario e farmaco, vale a dire prescrizione, preparazione e somministrazione. Al riguardo, per ciascuna fase, l analisi deve essere condivisa, standardizzata e periodicamente aggiornata e le relative istruzioni devono essere scritte e risultare sempre disponibili per la consultazione di tutto il personale a cui sono destinate. Nella prevenzione degli errori in corso di terapia con farmaci antineoplastici, inoltre, è decisivo il ruolo della Direzione sanitaria/aziendale per accrescere il grado di consapevolezza tra gli 17
19 operatori sanitari e implementare azioni di miglioramento tra le quali risultano di notevole rilevanza l introduzione di tecnologie informatizzate e la garanzia di condizioni lavorative adeguate in termini sia di risorse strutturali sia gestionali DECRETI ASSESSORIALI REGIONE SICILIA L assessorato alla Salute della Regione Sicilia prendendo atto che il verificarsi di eventi sentinella scaturisce principalmente da una mancata centralizzazione delle attività di preparazione dei farmaci antiblastici, e che le indicazioni per la centralizzazione di tali farmaci risultano attualmente applicate in modo disomogeneo tra le varie strutture erogatrici del Servizio Sanitario Regionale, e considerato che questa tematica rappresenta un elemento significativo all interno del processo di cambiamento e miglioramento della qualità e della sicurezza dei pazienti, ha emanato il decreto assessoriale (DA) 10 ottobre 2012 Centralizzazione dei farmaci antiblastici. Questo decreto stabilisce che tutte le strutture sanitarie pubbliche e private accreditate che effettuino, a qualunque titolo, preparazioni di terapie farmacologiche oncologiche, oncoematologiche e/o qualunque altro tipo di terapia in cui sia previsto l utilizzo di farmaci antiblastici, devono dotarsi di un UFA presso la quale centralizzare le 18
20 procedure di conservazione, manipolazione, allestimento, distribuzione e smaltimento. Inoltre, le direzioni aziendali delle strutture sanitarie pubbliche e i rappresentanti legali delle strutture private accreditate devono verificare e certificare la piena corrispondenza dei requisiti posseduti dalle proprie UFA rispetto a quelli elencati nella linee guida ministeriali e a quanto previsto dalla FU XII edizione. 12 Nel corso dell anno 2013 un modello di governo clinico, in linea con i requisiti identificati nelle Raccomandazioni Ministeriali e con le disposizioni del DA per la centralizzazione dei farmaci antiblastici, che preveda l integrazione funzionale tra UFA-Oncologia-Ematologia è stato sviluppato e condotto a certificazione di qualità ISO 9001:2008 presso l ARNAS Garibaldi di Catania, che pertanto rappresenta un esperienza pilota unica e di riferimento per la nostra regione. Al fine di dare seguito ai sopraindicati provvedimenti normativi la Regione ha deciso di estendere alle altre aziende del Servizio Sanitario Regionale l esperienza dell ARNAS Garibaldi realizzando un programma di implementazione dedicato al miglioramento del percorso oncologico, all integrazione delle competenze tra farmacista-oncologo-ematologo e alla diffusione di un nuovo modello clinico integrato (Fig.2). 19
21 Fig.2 Modello UFA-ONCO-EMA su scala regionale Il DA n del 14 ottobre 2013 Approvazione del programma regionale per la sicurezza, appropriatezza e gestione complessiva della terapia antitumorale pubblicato nella Gazzetta Ufficiale della Regione Siciliana n. 50 dell 8 novembre 2013, approva il programma di implementazione del modello di governo clinico integrato UFA-ONCO-EMA e sancisce che le strutture pubbliche e private che effettuano preparazioni di terapie farmacologiche oncologiche e/o oncoematologiche sono tenute ad aderire al programma regionale attuando le azioni previste, che saranno anche oggetto di valutazione dei Direttori Generali. 13 Di seguito viene riportato l elenco delle strutture pubbliche e private accreditate coinvolte nel progetto aggiornate al DA del 14 aprile 2014 pubblicato nella Gazzetta Ufficiale della Regione Siciliana n. 20 del 16 maggio (Fig.3). 20
22 STRUTTURA DI APPARTENENZA CITTA' 1. ARNAS GARIBALDI CATANIA 2. AOU POLICLINICO FERRAROTTO CATANIA 3. AOU POLICLINICO VITTORIO EMANUELE CATANIA 4. AO CANNIZZARO CATANIA 5. ASP 3 CATANIA - P.O. CALTAGIRONE GRAVINA CATANIA 6. AOU POLICLINICO UNIVERSITARIO MESSINA 7. AOOR PAPARDO MESSINA 8. ASP MESSINA - P.O. TAORMINA MESSINA 9. ASP RAGUSA MARIA PATERNO AREZZO DI IBLA RAGUSA 10. ASP ENNA - P.O. UMBERTO I ENNA 11. ASP ENNA - P.O. LEONFORTE ENNA 12. ASP CALTANISSETTA P.O. S. ELIA CALTANISSETTA 13. ASP CALTANISSETTA P.O. V. EMANUELE GELA 14. ASP AGRIGENTO - P.O. SAN GIOVANNI DI DIO AGRIGENTO 15. ASP AGRIGENTO - P.O. SCIACCA AGRIGENTO 16. ASP AGRIGENTO - P.O. CANICATTI AGRIGENTO 17. ASP 9 TRAPANI - P.O. S. ANTONIO ABBATE TRAPANI 18. ASP TRAPANI - P.O. CASTELVETRANO TRAPANI 19. ARNAS CIVICO PALERMO 20. ASP SIRACUSA P.O. UMBERTO I SIRACUSA 21. ASP SIRACUSA P.O. AUGUSTA SIRACUSA 22. ASP SIRACUSA P.O. AVOLA SIRACUSA 23. AOU POLICLINICO PALERMO PALERMO 24. AOOR VILLA SOFIA CERVELLO PALERMO 25. FONDAZIONE GIGLIO CEFALU' 26. OSPEDALE BUCCHERI LAFERLA PALERMO 27. CASA DI CURA "G. B. MORGAGNI" CATANIA 28. CASA DI CURA MUSUMECI GECAS S.R.L. CATANIA 29. "HUMANITAS CENTRO CATANESE DI ONCOLOGIA" CATANIA 30. "ISTITUTO ONCOLOGICO DEL MEDITERRANEO" VIAGRANDE 31. CASA DI CURA"VILLA SALUS" MESSINA 32. CASA DI CURA CARMONA - ARCOBALENO S.R.L. MESSINA 33. CASA DI CURA VILLA DEI GERANI TRAPANI 34. CASA DI CURA "MACCHIARELLA S.P.A." PALERMO 35. CASA DI CURA "TORINA S.P.A." PALERMO 36. CASA DI CURA "LA MADDALENA" PALERMO 37. CASA DI CURA ORESTANO S.R.L. PALERMO Fig.3 Strutture coinvolte nel progetto UFA-ONCO-EMA 21
23 3. MODELLO DI GOVERNO CLINICO UFA ONCO EMA Il programma di implementazione del modello di governo clinico integrato UFA-ONCO-EMA si pone l obiettivo di migliorare la sicurezza, appropriatezza e gestione complessiva della terapia antitumorale. Con questo intervento la Regione intende garantire che la gestione della terapia antitumorale, prestazione sanitaria di alta complessità, avvenga attraverso un processo definito e controllato nei comportamenti, con tracciabilità delle attività svolte e delle relative responsabilità, a garanzia della sicurezza dei pazienti e degli operatori, dell'appropriatezza terapeutica e della efficace informazione al paziente riguardo gli stili di vita da adottare e i possibili effetti collaterali della terapia. Il programma integra l UFA con le Unità Operative (UU.OO.) di Oncologia ed Ematologia attraverso la condivisione di un processo di produzione e gestione farmaci antitumorali in grado di garantire una corretta gestione del rischio, una adeguata gestione delle risorse disponibili ed un focus importante sul livello qualitativo delle prestazioni erogate, come riportato nella Fig.4: 22
24 Fig.4 Programma UFA-ONCO-EMA La mission trova la propria esplicitazione e declinazione negli obiettivi di progetto quali: 1. Integrazione delle competenze tra farmacista, oncologo, ematologo, in ottica di una sempre più accurata, efficiente e personalizzata cura del paziente, con la realizzazione di documenti condivisi sulle interazioni, tossicità, stabilità dei preparati e schemi terapeutici; 2. Garantire la qualità della produzione nella UFA, condividendo protocolli e comportamenti mediante la standardizzazione di criteri tecnici ed organizzativi; 3. Attivare un sostenibile ed affidabile sistema di monitoraggio di specifici indicatori di performance del sistema integrato UFA-ONCO- EMA; 4. Progettare un sistema informativo per condivisione a livello regionale del modello UFA-ONCO-EMA e del sistema di monitoraggio degli indicatori. 23
25 Il risultato concreto delle attività di progetto sarà quello di definire protocolli e comportamenti nei seguenti ambiti: terapeutici per l appropriatezza prescrittiva; organizzativi per la gestione efficace delle criticità, degli incidenti e delle tossicità legate alla terapia antitumorale; controllo del rispetto dei requisiti legati all accreditamento regionale/ Joint Commission International (JCI), UNI-EN-ISO 9001:2008 e Raccomandazione Ministeriale n. 14. La realizzazione del modello di governo clinico garantisce la oggettività delle regole ed il raggiungimento di un profilo di conformità nelle varie strutture secondo i requisiti di JCI, attualmente vigenti nella nostra Regione, la Raccomandazione n. 14 del Ministero della Salute e della UNI-EN-ISO 9001: (Fig.5). Fig.5 Modello di governo clinico di gestione dei farmaci antiblastici 24
26 4. PROGETTO PILOTA PRESSO L ARNAS GARIBALDI DI CATANIA L ARNAS Garibaldi risponde concretamente ai requisiti del quadro regolatorio di riferimento in merito ad un utilizzo sicuro ed appropriato del farmaco antitumorale. Il progetto si basa sulla implementazione di un modello integrato tra i settori UFA, UU.OO. di Oncologia Medica e UU.OO. di Ematologia (UFA-ONCO-EMA) al fine di garantire sicurezza, appropriatezza ed utilizzo razionale delle risorse in merito al processo di gestione del farmaco antitumorale. 4.1 PRESUPPOSTI DEL PROGETTO Il team di progetto dell ARNAS Garibaldi, in collaborazione con la società di consulenza di direzione OPT, ha fornito una chiave di lettura concreta e pratica del concetto di clinical governance per il raggiungimento degli obiettivi di progetto quali: ottimizzare l interfaccia UFA Oncologia Ematologia con riferimento all intero processo di richiesta, consegna, somministrazione e accesso alle informazioni riguardo i farmaci antiblastici; favorire l integrazione di competenze tra Farmacista - Oncologo - Ematologo; garantire la qualità della produzione nell UFA; ottenere il raggiungimento della validazione attraverso la Certificazione di Qualità ISO 9001:2008 del Modello di Governo Clinico UFA-ONCO-EMA in linea con i requisiti delle Raccomandazioni Ministeriali ed in particolare della Raccomandazione n. 14 dell ottobre
27 4.2 FASI DEL PROGETTO 1) Formalizzazione del Gruppo di Lavoro interdisciplinare: Farmacista, Tecnico, Oncologo, Ematologo, Infermiere e condivisione fasi di progetto 2) Assessment iniziale in autovalutazione mediante predefinita e condivisa check-list 3) Audit iniziale di tipo documentale e in campo (UFA-Oncologia- Ematologia) 4) Analisi dei processi operativi, individuazione delle criticità e implementazione azioni di miglioramento: a) ambito UFA b) ambito ONCO-EMA c) interfaccia UFA-ONCO-EMA 5) Individuazione ed avvio monitoraggio degli indicatori di performance del processo di produzione e gestione farmaci antiblastici 6) Formalizzazione del Sistema Documentale per uso interno e per Ente di Certificazione 7) Ottimizzazione interfaccia Farmacia-Oncologia-Ematologia e integrazione delle competenze tra Farmacista e Clinico, in ottica di un accurata, efficiente e personalizzata cura del paziente 8) Audit preliminare alla visita dell Ente di Certificazione 9) Certificazione di Qualità del Processo di produzione e gestione Farmaci Antitumorali 26
28 L ARNAS Garibaldi ha ottenuto il 22 luglio 2013 la Certificazione di Qualità ISO 9001 dall Ente Certificatore Bureau Veritas, gruppo leader riconosciuto a livello mondiale nei servizi di ispezione, controllo e verifica dei sistemi di gestione della qualità specialmente in ambito sanitario (Fig.6). Fig.6 Certificazione ISO 9001 ottenuta dall ARNAS Garibaldi 4.3 MODELLO INTEGRATO UFA-ONCO-EMA VALIDATO E CERTIFICATO Il modello rappresenta un sistema semplice, fruibile ed in grado di dimostrare con le opportune evidenze oggettive il controllo nelle attività del processo di gestione del farmaco antitumorale in UFA, in ONCO ed EMA (Fig.7). Il modello è costituito da quattro ambiti principali: 1) Mission e politica di miglioramento 2) Gestione delle risorse umane e strumentali-tecnologiche 3) Processi di gestione del farmaco antitumorale 4) Strumenti di verifica e monitoraggio del modello 27
29 Fig.7 Logica del modello UFA-ONCO-EMA MISSION E POLITICA DI MIGLIORAMENTO La mission del progetto è garantire che la gestione della terapia antitumorale - prestazione sanitaria di alta complessità - avvenga attraverso un processo definito e controllato nei comportamenti, con tracciabilità delle attività svolte e delle relative responsabilità, nel rispetto della sicurezza dei pazienti e degli operatori ed assicurando un efficace informazione al paziente riguardo gli stili di vita da adottare e i possibili effetti collaterali della terapia. Importante è anche una politica di miglioramento definita dall esplicitazione degli obiettivi sottesi nella mission. Il processo strategico di individuazione degli obiettivi deve essere oggettivo, condiviso e misurato: Oggettivo: basato su dati e informazioni, nel rispetto delle direttive e normative di riferimento; 28
30 Condiviso: da tutti i portatori di interesse: Istituzioni ed Enti, Direzione Strategica Aziendale, UFA, ONCO ed EMA; Misurato: da un sistema di indicatori opportuni per il monitoraggio dell efficacia degli impegni attuati per il raggiungimento degli obiettivi prefissati GESTIONE DELLE RISORSE UMANE E STRUMENTALI- TECNOLOGICHE Per ciascun macro-processo operativo critico per la gestione del farmaco antitumorale viene rappresentato sottoforma di matrice la correlazione tra figura professionale e responsabilità. La condivisione e formalizzazione della matrice delle responsabilità rappresenta la base dell analisi delle attività e della definizione dei profili professionali delle risorse operanti nelle diverse fasi della gestione del farmaco antitumorale. Per quanto riguarda le risorse strumentali-tecnologiche, nei differenti settori (UFA, ONCO ed EMA) deputati alla gestione del farmaco antitumorale si hanno in dotazione numerosi apparecchi e strumenti informatici come software gestionali necessari per lo svolgimento delle attività. L uso delle tecnologie informatizzate migliora sicuramente la sicurezza in tutto il processo di gestione del farmaco antineoplastico perché consente la completa tracciabilità dei processi, elimina gli errori dovuti alla trascrizione e fornisce dati che possono essere utilizzati come strumento di audit clinico e di verifica. 29
31 Infatti, per la complessità delle azioni da svolgere è necessario dotarsi di un applicativo informatico che consenta di gestire in sicurezza tutte le operazioni previste in campo farmaceutico. La centralizzazione dell allestimento dei farmaci antiblastici presuppone la creazione dell anagrafica dei prodotti utilizzati e la proceduralizzazione dei comportamenti, delle regole di trasmissione dell informazione e, in particolare, della prescrizione. La dotazione di un software idoneo è importante perché contribuisce a creare un sistema di controllo che blocca l errore di prescrizione o di preparazione prima che si realizzi. Quindi è imprescindibile dotarsi di un programma informatico gestionale dedicato, che deve consentire il monitoraggio completo delle richieste dei reparti, dei protocolli terapeutici, delle terapie preparate, dei farmaci utilizzati e dei pazienti. Il programma individuato per l attivazione dell allestimento centralizzato delle terapie oncologiche dovrà consentire di: 1) creare l anagrafica dei prodotti utilizzati; 2) creare il prontuario informatizzato dei protocolli terapeutici; 3) gestire informaticamente la prescrizione; 4) gestire informaticamente il magazzino (foglio di prelievo, scarico automatizzato con lotti); 5) gestire informaticamente la documentazione a supporto della preparazione: foglio di preparazione, etichette con numerazione progressiva e codice a barre; 30
32 6) creare il registro elettronico delle preparazioni, in cui vengono registrati per ogni allestimento, il farmaco utilizzato, la dose, il diluente, il nome del paziente, il nome del medico richiedente, il reparto e la data; 7) creare il registro elettronico degli esposti in cui vengono riportati per ogni operatore, i tempi di esposizione e i farmaci; 8) creare l anagrafica dei pazienti e tenere la registrazione della storia clinica del malato, al fine di garantire la totale tracciabilità di tutti i trattamenti somministrati; 9) gestire informaticamente la somministrazione, per avere la completa tracciabilità non solo delle terapie somministrate, ma anche della modalità di somministrazione: sequenza, orario e durata PROCESSI DI GESTIONE DEL FARMACO ANTITUMORALE Il modello, alla luce dei principi della clinical governance, definisce le macro-attività e punti decisionali dei settori coinvolti (UFA, ONCO ed EMA) in tutte le sue fasi del suo percorso, come mostrato nel diagramma di flusso riportato in Fig.8. I protocolli operativi, in ottemperanza ai requisiti ministeriali della Raccomandazione n. 14, riguardano: Approvvigionamento Immagazzinamento, conservazione, gestione delle scorte Prescrizione Allestimento 31
33 Distribuzione Somministrazione Gestione della terapia orale Altri interventi: 1. Coinvolgimento del paziente e familiari nel processo di cura 2. Umanizzazione delle cure oncologiche 3. Strumenti di prevenzione e controllo La descrizione puntuale e opportunamente dettagliata delle attività e dei controlli del processo globale permette di far emergere eventuali criticità, definire univocamente responsabilità, figure coinvolte e settori interessati. Fig.8 Flow Chart Processo di Gestione del Farmaco Antitumorale 32
34 4.3.4 STRUMENTI DI VERIFICA E MONITORAGGIO DEL MODELLO Gli strumenti di verifica (autovalutazione e audit) traggono input da: Indicatori di processo e di risultato Customer satisfaction Registrazione delle anomalie per fornire come output il piano di azioni come strumento per attivare e garantire nel tempo un processo credibile, sostenibile e misurabile di miglioramento continuo. Infatti, la norma ISO 9001:2008 prevede che l organizzazione conduca ad intervalli pianificati audit interni per determinare se il sistema di gestione per la qualità è conforme ai requisiti della presente norma internazionale ed ai requisiti del sistema di gestione per la qualità stabiliti dall organizzazione stessa nonché per verificare se il sistema è efficacemente attuato e mantenuto. Inoltre come previsto dalla norma ISO 9001:2008 al punto 8.22, è stata predisposta una procedura documentata per definire le responsabilità ed i requisiti per la pianificazione e conduzione degli audit. 33
35 5. PROCEDURA DI GESTIONE DELLA TERAPIA ANTITUMORALE L adozione di procedure o protocolli aziendali codificati e condivisi tra gli operatori sanitari è uno strumento di prevenzione degli errori a garanzia della qualità e sicurezza delle cure e rappresenta un insostituibile metodo per la tracciabilità del percorso di gestione della terapia antitumorale. La seguente procedura, approvata dalla Direzione Sanitaria dell ARNAS Garibaldi di Catania, ha l obiettivo di definire le modalità operative relative all intero processo di gestione della terapia antitumorale, identificando la tracciabilità delle attività svolte e dei profili di responsabilità ad esse connesse, a tutela di tutti i pazienti che necessitano di terapie farmacologiche e degli operatori sanitari. Il campo di applicazione di questa procedura riguarda la Farmacia Ospedaliera dotata di UFA, l Unità Operativa Complessa (U.O.C.) di Oncologia e l U.O.C. di Ematologia. I Direttori dell UU.OO. di Oncologia, Ematologia e del Responsabile UFA, in collaborazione con la Direzione Sanitaria aziendale e di presidio, Risk Manager, l Ufficio Qualità devono verificare inizialmente e periodicamente la validità della procedura, mentre l applicazione è responsabilità del Farmacista Responsabile UFA, del Responsabile DH/Reparto Oncologia e del DH/Reparto Ematologia
36 5.1 APPROVVIGIONAMENTO DEI FARMACI Il responsabile della Farmacia Ospedaliera deve inserire nei capitolati di acquisto criteri o elementi finalizzati a garantire importanti requisiti di sicurezza dei farmaci, ad esempio: - la disponibilità di informazioni sulla ricostituzione dei farmaci, sulla compatibilità con i diluenti e sulla conservazione dei farmaci dopo la ricostituzione, per poterne informare gli utilizzatori; - l assenza di situazioni di rischio (lo stesso colore delle confezioni per dosaggi diversi della stessa forma farmaceutica o il nome simile, fiale trasparenti poco leggibili, etc.) ovvero la disponibilità a fornire etichette aggiuntive per la segnalazione/evidenza del rischio; - la presenza di dispositivi di sicurezza per la corretta preparazione e/o somministrazione dei farmaci; - ridurre le scelte delle opzioni disponibili dei farmaci, in particolare di quelli ad alto rischio: maggiore è il numero di opzioni disponibili (es. differenti concentrazioni e volumi), maggiore è la possibilità che si verifichi un errore; - verificare, per i farmaci equivalenti, la presenza di tutte le indicazioni terapeutiche, onde prevenire l eventuale uso off-label, ovvero opportunamente evidenziare le eventuali limitazioni d uso; - richiedere per i farmaci di origine biologica la garanzia del mantenimento di temperature particolari (cold chain) e il trasporto 35
37 con bassa vibrazione, ottenibili con sistemi certificati di imballaggio e di consegna idonea; - presenza per i farmaci antineoplastici iniettabili di sistema di protezione antirottura dei flaconi in vetro. 5.2 PRESA IN CARICO DEL PAZIENTE La presa in carico del paziente oncologico può avvenire in diversi contesti (ambulatorio divisionale, reparto di degenza) e può sfociare in un percorso diagnostico-terapeutico che si articola in uno o più dei seguenti setting assistenziali: - setting ambulatoriale (diagnostica non invasiva e terapia antitumorale orale); - setting di day-service e/o DH (diagnostica invasiva di bassa complessità e terapia iniettiva); - setting di degenza ordinaria (diagnostica invasiva di alta complessità, gestione delle complicanze della patologia tumorale e/o della terapia erogata, della somministrazione di terapia iniettiva di alta complessità). La presa in carico del paziente è competenza del dirigente medico oncologo o ematologo ed avviene sotto la responsabilità di questo. In tutti i contesti di cui sopra la procedura di presa in carico deve essere basata su: - identificazione del paziente; - apertura della cartella clinica; 36
38 - raccolta dell anamnesi familiare, fisiologica e patologica, dell anamnesi oncologica e dell esame fisico del paziente che devono essere riportati negli spazi appositamente dedicati nella cartella clinica adottata dalla Struttura Complessa di Oncologia Medica e dalla Struttura Complessa di Ematologia, datata e firmata dal dirigente medico che esegue la procedura; - Identificazione delle problematiche cliniche emergenti del paziente, qualora presenti; - eventuale prescrizione della terapia medica generale (non oncologica) richiesta dal quadro clinico (es: terapia del dolore). Segue la stesura della cartella infermieristica che è di competenza della figura dell infermiere professionale ed è sotto la sua responsabilità. La presa in carico del paziente è seguita quindi dalla delineazione della strategia assistenziale comprendente la programmazione delle eventuali procedure diagnostiche necessarie al completamento dello studio del caso clinico e l identificazione della strategia di cura (es: chemioterapia versus chemioterapia adiuvante versus terapia integrata chemio-radioterapica). La delineazione della strategia assistenziale è di competenza del dirigente medico oncologo o ematologo sotto la sua responsabilità. Una volta delineata la strategia terapeutica e debitamente informato il paziente, il dirigente medico ne otterrà il consenso alla erogazione delle procedure diagnostiche e/o terapeutiche compilato su apposito modulo che verrà 37
39 firmato dal paziente o dal legale rappresentante e controfirmato dal dirigente medico che lo raccoglie. L ottenimento da parte del paziente del consenso informato alle cure è attività di competenza del dirigente medico oncologo o ematologo ed avviene sotto la responsabilità di questi. In base alla strategia diagnostico-assistenziale delineata ed alle condizioni cliniche del paziente, il dirigente medico identificherà il regime assistenziale nel cui contesto verranno erogate le prestazioni sanitarie necessarie (es: ricovero in regime ordinario versus erogazione ambulatoriale della terapia). A tal fine il dirigente medico compilerà l apposito modulo; tale modulo verrà sottoposto per approvazione al Direttore della Struttura Complessa. La strategia diagnostico-terapeutica diverrà operativa una volta approvata dal Direttore della Struttura Complessa di Oncologia Medica e dal Direttore Struttura Complessa di Ematologia. L approvazione della strategia diagnostico-terapeutica è di competenza del Direttore della Struttura Complessa di Oncologia Medica e dal Direttore Struttura Complessa di Ematologia ed avviene sotto la propria responsabilità di questi. Una volta approvata la strategia diagnosticoterapeutica ed identificato il setting assistenziale in cui le prestazioni sanitarie inerenti verranno erogate, il dirigente medico provvederà alla compilazione della prescrizione della terapia antitumorale. La prescrizione dovrà contenere gli elementi essenziali indicati di seguito; verrà firmata dal 38
40 medico prescrittore e validata da un medico revisore che fungerà da secondo controllo di appropriatezza e qualità della prescrizione INDICATORI PRESA IN CARICO DEL PAZIENTE Titolo Attuale Atteso Target n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in ricoverato in Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Ematologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in ricoverato in Ematologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Oncologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Ematologia 39
41 5.3 PRESCRIZIONE La prescrizione della terapia antitumorale deve contenere i seguenti elementi essenziali al fine di garantire l appropriatezza prescrittiva e la sicurezza dei pazienti: - Data della prescrizione (che deve coincidere con la data in cui il paziente viene visto dal medico oncologo che prende visione degli eventuali accertamenti ematochimici e/o strumentali propedeutici alla somministrazione della terapia stessa); - Nome, cognome, data di nascita e sesso del paziente; - Altezza e peso del paziente; - Superficie corporea e/o altre variabili necessarie per il calcolo della dose di specifici farmaci (es. AUC); - Diagnosi; - Nome del regime di cura adottato cui corrisponda un numero cronologico preventivamente condiviso da parte della Struttura di Oncologia Medica, della Struttura di Ematologia e dell UFA; il nome del regime corrisponderà ad un acronimo noto e condiviso, rifacendosi ad un template standard custodito in reparto degenze, DH e UFA; - Numero cronologico del ciclo di trattamento; - Numero totale di cicli previsti nel contesto della strategia di cura stilata al momento della presa in carico del paziente, - Numero del giorno di terapia (nel caso di regimi di cura che prevedano multipli giorni di terapia, in sequenza e/o alternati); 40
42 - Nome e codice del protocollo del trattamento sperimentale (nel caso trattarsi di studio clinico controllato); - Denominazione dei principi attivi antitumorali e/o ancillari utilizzati; - Metodo di calcolo delle dosi dei principi attivi; - Dose dei singoli principi attivi componenti il regime di terapia (i valori dovranno essere espressi in milligrammi evitando, se possibile, le virgole e soprattutto gli zeri che seguano le virgole); - Eventuali riduzioni di dose adottate estemporaneamente per sopravvenute modifiche del quadro clinico e/o precedenti tossicità riferite e/o osservate; - Vie di somministrazione (es: I.V.), durata della somministrazione di ogni singolo principio attivo componente il regime di terapia, diluenti utilizzati (tipologie, volumi); - Intervalli intercorrenti tra le somministrazioni dei singoli principi attivi; - Sequenze di somministrazione dei singoli principi attivi; - Regime della terapia di supporto; - Firma del medico prescrittore. Allo scopo di soddisfare il requisito di possesso di questi elementi essenziali da parte delle prescrizioni emesse dalla Struttura Complessa di Oncologia Medica e della Struttura Complessa di Ematologia si è 41
43 provveduto a preparare ed adottare una scheda di prescrizione della terapia antitumorale condivisa con l UFA. La prescrizione della terapia antitumorale è di competenza del dirigente medico oncologo o ematologo ed avviene sotto la responsabilità di questi. Le principali azioni sulle quali si basa la procedura di prescrizione della terapia antitumorale riguardano i seguenti punti: a) Richiesta della terapia farmacologica. La richiesta deve essere sempre fatta dal medico prescrittore per iscritto o con la Convalida Informatica Certificata (CIC), qualora venisse resa disponibile da parte della Direzione Aziendale. Non saranno accettate in nessun caso prescrizioni verbali, eccetto che per l interruzione urgente della terapia che deve comunque essere trascritta quanto prima possibile. Anche le nuove prescrizioni o modifiche devono essere eseguite per iscritto. b) Modulistica. E adottata una modulistica standard, di facile compilazione in ogni parte, completa di ogni riferimento al paziente e ai farmaci, di immediata lettura e che permette la completa tracciabilità di ogni atto. Le correzioni manuali non sono permesse, ma, qualora fossero necessarie in particolari condizioni, saranno sempre controfirmate. Analogamente, nel caso di gestione informatica, sarà assicurata la tracciabilità di eventuali correzioni e degli operatori che vi hanno 42
44 provveduto. La modulistica in uso e la procedura di prescrizione sono note a tutti gli operatori coinvolti e alla Direzione sanitaria/aziendale. c) Schemi di terapia. Le decisioni terapeutiche sono riconducibili ad un numero elevato ma ben noto di schemi terapeutici standard, condivisi con la Farmacia ospedaliera per la valutazione degli aspetti tecnico farmaceutici, regolatori e logistici correlati alla preparazione, che vengono personalizzate dal medico oncologo o ematologo sulla base delle condizioni cliniche del paziente. La raccolta ordinata e dinamica degli schemi avviene tramite appositi template cartacei; nel momento in cui dovesse rendersi disponibile una cartella clinica informatizzata interfacciata con il programma di preparazione in uso all UFA l archiviazione avverrà sotto forma di template informatizzati (Prescrizione Elettronica Assistita = PEA). La richiesta compilata su template cartaceo (foglio di prescrizione dove sono riportate tutte le informazioni non variabili e dove quelle variabili vanno inserite in apposite caselle) evita di dover trascrivere manualmente la maggior parte di dati. La scheda di prescrizione della terapia antitumorale verrà inviata tramite fax all UFA sotto la responsabilità del dirigente medico prescrittore. d) Documentazione. I medici e gli infermieri, ad ogni trattamento chemioterapico, documenteranno in cartella clinica: la valutazione clinica e il performance status; la rilevazione dei parametri vitali e del peso; la verifica della presenza di allergie, precedenti reazioni e tossicità legate ai trattamenti; 43
45 la valutazione della tossicità della terapia prescritta: la documentazione necessaria alla valutazione della tossicità e della sostenibilità al trattamento successivo, deve essere disponibile per la programmazione di ogni ciclo di cura; la ricognizione e riconciliazione della terapia farmacologica in corso. L implementazione della prescrizione informatizzata permetterà di ridurre drasticamente gli errori di scrittura, lettura della trascrizione e calcolo; nel caso la Direzione aziendale dovesse rendere disponibile il programma informatizzato di prescrizione della terapia antitumorale sarà auspicabile che la scelta di tale programma venga guidata dal riscontro di caratteristiche idonee a garantire la sicurezza (es. non consentire inserimenti estemporanei di farmaci antineoplastici che possano modificare i protocolli concordati). Al fine di garantire la tracciabilità ed evitare il rischio di trascrizioni o cancellazioni, è opportuno predisporre un file per ogni ciclo di terapia. Tutti gli archivi informatici contenenti le informazioni relative ai farmaci e agli schemi di terapia vanno sottoposti a idonee procedure per la loro convalida e il loro corretto mantenimento. 44
46 5.3.1 INDICATORI PRESCRIZIONE Titolo Attuale Atteso Target n. prescrizione EMA non conformi/totale pervenute in UFA n. prescrizione ONCO non conformi/totale pervenute in UFA 5.4 VALIDAZIONE DELLA RICHIESTA DI ALLESTIMENTO Le UU.OO. fanno pervenire alla Farmacia ospedaliera la richiesta tramite fax di allestimento di medicinale personalizzato per terapia oncologica o le variazioni alla prescrizione per i pazienti già in trattamento. Le prescrizioni pervenute al centro dell UFA possono essere giornaliere o settimanali. La prescrizione medica deve contenere tutte le indicazioni necessarie alla valutazione dell allestimento nel rispetto della FU XII edizione (NBP, tabella 8) e ponendo particolare attenzione alle incompatibilità tra principi attivi ed eccipienti richiesti. Il farmacista verifica la correttezza e l accettabilità della prescrizione analizzandone la compatibilità quali-quantitativa tra il farmaco, il solvente e il diluente, la fotosensibilità e la stabilità chimico-fisica del farmaco, in relazione alla prescrizione stessa. 45
47 In caso di non conformità, il farmacista contatta il medico per le opportune considerazioni e richiede le correzioni controfirmate o l elaborazione di una nuova prescrizione medica ELABORAZIONE DELLA DOCUMENTAZIONE Elaborazione foglio di lavoro e della scheda di somministrazione della terapia allestita Il farmacista dopo aver valutato la conformità della prescrizione, elabora un foglio di lavorazione, con l ausilio di un applicativo informatico, che consente di gestire in sicurezza tutte le operazioni previste per garantire la tracciabilità dell intero processo. Nel foglio di lavoro è indicato: numero di protocollo; U.O. richiedente la terapia; nome, cognome e data di nascita del paziente; nome del protocollo; nome del principio attivo; volume in mg e in ml del farmaco da prelevare; tipo e volume del diluente utilizzato; 46
48 tutte le informazioni necessarie per eseguire una corretta tecnica di allestimento della terapia (volume di diluente da utilizzare per la ricostituzione del principio attivo, tipo di diluente da utilizzare, ecc.); data di allestimento; lotto e scadenza del farmaco utilizzato; modalità di conservazione dell eventuale residuo di farmaco; eventuali avvertenze per l infermiere o il tecnico preparatore; firma del farmacista; firma dell infermiere o del tecnico preparatore; copia dell etichetta. La scheda di somministrazione riporta: il nome e cognome e la data di nascita del paziente; il dosaggio del farmaco; il tipo e il volume del diluente utilizzato; il volume totale della preparazione espresso in ml; la data di preparazione; firma del farmacista; firma dell infermiere o del tecnico preparatore. Elaborazione dell etichetta Per ogni terapia allestita viene formulata un etichetta contenente le seguenti informazioni: 47
49 nome, cognome e data di nascita del paziente; composizione quali-quantitativa (principio attivo e dosaggio); volume finale; tempo previsto d infusione; ordine di somministrazione dei vari farmaci; lotto del farmaco utilizzato; scadenza e condizioni di conservazione della terapia fino all'uso (es. protezione dalla luce, conservazione in frigorifero); nome e cognome del medico prescrittore; nome e cognome del farmacista; avvertenze. 5.5 PREPARAZIONE Operazioni preliminari all allestimento dei farmaci L allestimento dei farmaci citotossici viene effettuata in cabina di sicurezza biologica di classe II, a flusso laminare verticale che, scendendo perpendicolarmente sul piano di lavoro, garantisce la protezione dell operatore, la sterilità del prodotto finito e la tutela dell ambiente. I locali devono essere a pressione negativa. Tramite la finestra/passaggio (SAS), vengono introdotti i fogli di lavoro, le schede di somministrazione, le etichette delle preparazioni da allestire, i farmaci privati delle scatole di cartone, e gli eventuali dispositivi da utilizzare per l allestimento. 48
50 Il personale (farmacista e infermiere e/o tecnico preparatore) prima di accedere ai locali sterili deve eseguire le seguenti norme igieniche e comportamentali: procedere al lavaggio delle mani con acqua corrente e sapone; accedere alla camera bianca tramite un corridoio/filtro dove indossa i DPI dedicati all allestimento di citotossici (camice, copriscarpe, mascherina, copricapo); accendere la cappa e controllare il funzionamento degli allarmi, lasciandola in funzione minuti prima di iniziare le manovre di diluizione; indossare un paio di guanti monouso in nitrile senza polvere; disinfettare la superficie di lavoro all interno della cappa con garze imbevute di soluzione alcolica 70 ; sistemare sul piano di lavoro il telino in tessuto non tessuto (TNT) con il lato assorbente volto verso l alto, da cambiare ogni volta si contamina e di dimensioni tali da non ostacolare il flusso laminare verticale nella zona grigliata della cappa stessa; introdurre all interno della cappa solo il materiale necessario per una preparazione (contenitore per lo smaltimento dei rifiuti, siringhe, tamponi sterili, disinfettate, ecc ) che deve essere accuratamente disinfettato con soluzione alcolica; 49
51 preparare su un carrello servitore tutto il materiale necessario per la diluizione dei farmaci (dispositivi per ricostituzione e diluizione, siringhe con raccordo luer-lock, fleboclisi, garze sterili e farmaci) Modalità di manipolazione e diluizione in cappa Nella zona controllata vi devono essere le persone strettamente necessarie, riducendo al minimo le attività al suo interno, per impedire che correnti d aria possano turbare la barriera frontale ed il flusso laminare. Gli operatori dedicati alle attività di manipolazione, ove possibile, dovrebbero essere almeno due: un operatore che allestisce e uno di supporto per assicurare un doppio controllo di tutte le attività svolte all interno dei locali sterili. Durante la fase di allestimento, che comporta il trasferimento del farmaco in soluzione di un flacone ad una siringa, il rischio di formazione di aerosol per nebulizzazione e di spandimenti durante la fase di preparazione è maggiormente elevato. Per tale motivo è necessario l utilizzo di sistemi di ricostituzione chiusi con equalizzatori di pressione dotati di valvola di sicurezza e attacco luer-lock femmina a garanzia dell operatore e del preparato. Inoltre all interno della cappa sono stati installati due sistemi per la manipolazione delle terapie antitumorali Diana Onco Plus, studiati appositamente per la miscelazione dei farmaci chemioterapici in modo sicuro, semplice, preciso e automatico. 50
52 Il sistema a circuito chiuso, è formato da due canali caratterizzati da pompe a siringa controllata da processore ad elevata precisione e velocità adatti a dosare in un recipiente di miscelazione delle soluzioni citostatiche prelevate in base al volume liberamente selezionabile da contenitori come flaconi, sacche, fiale. L utilizzo giornaliero del sistema evita l esposizione del personale sanitario a patologie correlate ai movimenti ripetuti da manipolazione del farmaco. Il sistema è dotato di display touchscreen con comandi facili e intuitivi, ed è inoltre interfacciato con una stampante che consente la stampa di report ed etichette per la documentazione del lavoro eseguito. Regole di base per un corretto allestimento dei chemioterapici antiblastici: - operare seduti sullo sgabello in posizione comoda e corretta e si devono evitare, sotto cappa, movimenti bruschi delle braccia; - lavorare sempre al centro della cappa evitando di frapporre oggetti che interrompono il flusso di aria sterile che va dall alto verso il basso; - in caso di spargimento accidentale bisogna rimuovere il telino e, se necessario, pulire il piano della cappa con un panno sterile imbevuto di soluzione ipoclorito al 5%; - togliere dalla confezione il connect set (set per la miscelazione e somministrazione di farmaci citotossici dotato di spike per una facile penetrazione nella sacca/flacone); 51
53 - perforare la membrana della sacca di diluente con lo spike del connet set; - aprire il tappo e la clamp a scorrimento riempire completamente il tubicino; - chiudere clamp a scorrimento sul connect set il più vicino possibile all adattatore; - rimuovere il cappuccio di protezione dal flacone del farmaco e disinfettare la membrana perforabile del tappo. Preparazione in sacca da infusione di farmaci antiblastici liofilizzati contenuti in flaconi: - perforare centralmente la membrana del flacone del farmaco (tenuto appoggiato sul piano di lavoro), con il chemoprotect spike avvolgendo una garza sterile attorno al collo dello stesso flacone; - prelevare con la siringa il volume del solvente richiesto per la ricostituzione del farmaco; - rimuovere il tappo di protezione dal chemoprotect spike e connettervi la siringa; - introdurre il solvente nel flacone dirigendo il diluente sulle pareti del flacone per garantire che tutta la polvere sia bagnata prima di agitarla in questo modo si minimizza la pressione all interno del flacone; - mantenere la siringa connessa al chemoprotect spike e agitare la fiala per sciogliere completamente il liofilizzato; 52
54 - prelevare con la siringa il volume del solvente richiesto per la ricostituzione del farmaco e sconnettere la siringa (non riempire la siringhe oltre i ¾ del suo volume), la membrana si chiude automaticamente con la sconnessione; - disconnettere la siringa dallo spike e riconnetterla all adattatore del connet set (l avvitamento della siringa permette l apertura della membrana nell adattatore del connect set) e introdurre il farmaco dosato nella sacca del diluente. Preparazione in sacca da infusione di farmaci antiblastici pronti per l uso contenuti in flaconi - perforare centralmente la membrana del flacone del farmaco (tenuto appoggiato sul piano di lavoro), con il chemoprotect spike avvolgendo una garza sterile attorno al collo dello stesso flacone; - capovolgere l insieme flacone-siringa (il flacone si troverà adesso in alto) e mantenendo la posizione aspirare il 20% della soluzione richiesta corrispondente al relativo dosaggio del farmaco e verificare la presenza di aria: se non c è l aria, terminare l aspirazione della quantità richiesta; se l aria è presente, reiniettare nel flacone quindi aspirare la quantità richiesta di soluzione; - disconnettere la siringa dallo spike e verificare il dosaggio prelevato, riconnetterla all adattatore del connet set iniettare il farmaco nella sacca del diluente; 53
55 - sconnettere la siringa, pulire l ingresso del farmaco nella sacca con della garza imbevuta di alcool 70% e riapplicare il tappo e la clip di protezione; - pulire la sacca con una garza umida per rimuovere eventuali contaminazioni accidentali; - apporre l etichetta contenente tutti i dati necessari all identificazione del preparato e del paziente destinatario; - coprire la sacca con involucro protettivo in caso di farmaco fotosensibile Pulizia delle cappe di lavoro e smaltimento dei rifiuti Alla fine della giornata lavorativa, si procede alla pulizia delle cappe e allo smaltimento dei rifiuti: tutti i rifiuti (siringhe, fiale, flaconi, etc), le rimanenze dei farmaci e il telino, andranno smaltiti in appositi contenitori per taglienti (rifiuti speciali ospedalieri) impermeabili, rigidi, a bocca larga e con chiusura ermetica; a sua volta questi vengono inseriti in un contenitore di rifiuti speciali ospedalieri più grande, munito di sacchetto di plastica asportabile nel quale vengono riposti anche tutti i dispositivi di sicurezza indossati dal personale. durante la fase di pulizia, la cabina deve essere tenuta in funzione prestando attenzione a non otturare i filtri con i panni, o la garza utilizzata; 54
56 la cappa viene ripulita dall infermiere che vi ha lavorato, con della garza imbevuta di alcool a 70 ; la pulizia viene effettuata sulla vetrata interna, sulla parete frontale, sulle pareti laterali, seguendo il flusso verticale (dall alto verso il basso), e sul piano di lavoro (dalla zona più esterna a quella più interna); alla fine della pulizia si accende la lampada U.V. della cappa. Questa, oltre ad assicurare un ambiente sterile, garantisce un sistema di degradazione molecolare dei chemioterapici in caso di residui accidentali in quanto molti di questi farmaci sono fotosensibili INDICATORI PREPARAZIONE Titolo Attuale Atteso Target n. di errori (near-miss) accaduti nell anno/totale preparazioni n. preparazioni conformi alla prescrizione/totale preparazioni 55
57 5.6 DISTRIBUZIONE Contenitori per trasporto dei chemioterapici Il contenitore per il trasporto dei farmaci antiblastici deve essere realizzato per garantire un elevato standard di sicurezza durante il trasferimento dei farmaci dalla centrale di preparazione ai locali di somministrazione. Il contenitore presenta le seguenti caratteristiche: completamente trasparente ed ispezionabile per verificare, prima dell apertura, la presenza di eventuali perdite dei farmaci trasportati; dotato di coperchio con guarnizione ermetica di sicurezza, tale da garantire il contenimento dei medicamenti antitumorali liquidi anche in caso di fuoriuscite; idoneo a trasportare flaconi di vetro, sacche in materiale plastico e siringhe pronte all uso; dotato di chiusura con quattro ganci di sicurezza che impediscono l apertura accidentale del contenitore in caso di caduta; dotato di idonea segnaletica per avvertire l utilizzatore della tipologia di prodotto trasportato Compilazione della bolla di accompagnamento Il farmacista compila la bolla di accompagnamento delle terapie che riporta le seguenti informazioni: data; U.O. a cui le terapie sono destinate; 56
58 nome, cognome dei pazienti e descrizione della preparazione; eventuali note; numero di contenitori per il trasporto; firma del farmacista, firma di chi ritira e firma di chi riceve le terapie. L operatore incaricato al ritiro presso UFA firma per presa in carico del contenitore per il trasporto dei chemioterapici. Giunto in reparto, l operatore consegna al personale della UOC di ONCO/EMA il contenitore che viene contestualmente svuotato del contenuto e viene validata la consegna mediante apposizione della firma/sigla dell operatore che riceve. Le bolle di accompagnamento con allegati i fogli di lavoro, sono archiviati e catalogati da parte dell UFA in ordine cronologico e per singolo reparto INDICATORI DISTRIBUZIONE Titolo Attuale Atteso Target Mediana/Media dal tempo che intercorre dalla presa in carico in UFA alla consegna ai reparti n. di bolle di accompagnamento che non seguono il contenitore sino ai reparti/totale bolle predisposte 57
59 5.7 SOMMINISTRAZIONE Il personale infermieristico del reparto degenze e del DH sono responsabili della preparazione della terapia ancillare, secondo gli schemi previsti nei protocolli di terapia approvati e condivisi dalla Direzione della Struttura Complessa di Oncologia Medica e l UFA, la conservazione delle cui copie validate persiste sotto la loro responsabilità. Le azioni che devono essere poste in essere da parte del personale infermieristico responsabile della somministrazione delle terapie antitumorali vengono suddivise, in rapporto alla relazione temporale intercorrente con l atto della somministrazione stessa, in: - azioni antecedenti la somministrazione; - azioni concomitanti alla somministrazione; - azioni successive alla somministrazione. Tutte le azioni in oggetto sono di competenza del personale infermieristico e avvengono sotto la responsabilità di questi. Le azioni antecedenti la somministrazione della terapia prevedono: - il ricevimento della scheda di somministrazione associata a copia della scheda di prescrizione inviata dall UFA; - l informazione ed il coinvolgimento attivo del paziente relativamente al piano di trattamento per il quale questi ha sottoscritto il consenso informato e su ogni eventuale problema o sintomo. Prima di iniziare la somministrazione della terapia antitumorale il personale infermieristico effettua delle verifiche puntuali circa la 58
60 corrispondenza tra il farmaco prescritto per lo specifico paziente e quello effettivamente pervenuto per la somministrazione. In caso di mancata corrispondenza, il farmaco deve essere somministrato solo dopo consultazione del medico prescrittore e modifica scritta della prescrizione stessa o dopo chiarimenti scritti da parte dei responsabili della preparazione. In particolare, due operatori sanitari, facenti parte del gruppo infermieristico operante nel DH e/o nel Reparto degenze della Struttura Complessa di Oncologia Medica e/o della Struttura Complessa di Ematologia abilitati alla somministrazione dei farmaci antineoplastici, verificano indipendentemente: nome del farmaco; dose del farmaco; via di somministrazione; velocità di somministrazione; data e ora di scadenza del farmaco rispetto a data e ora di preparazione; aspetto della preparazione (eventuali precipitati, limpidezza, colore) qualora il farmaco non arrivi schermato da parte della Farmacia ospedaliera; integrità dei contenitori; eventuale premedicazione. 59
61 Chi somministra il farmaco deve conoscerne l uso e le precauzioni necessarie per l impiego, le controindicazioni, le reazioni avverse da farmaco (ADR), le interazioni con altri farmaci. Le attività di cui sopra sono di competenza del personale infermieristico ed avvengono sotto la responsabilità di questi. Prima di iniziare l infusione l infermiere professionale dovrà essere protetto con gli idonei dispositivi: - guanti - camice Prima e dopo ogni somministrazione l operatore dovrà lavarsi accuratamente le mani. È, inoltre, indicato utilizzare rubinetti, con dispositivo luer-lock, per raccordare i deflussori a i vari tipi di ago utilizzati. Così facendo si rendono le operazioni più semplici e con minore possibilità di fuoriuscita del farmaco antiblastico. In caso di mal funzionamento del deflussore occorre staccarlo, portarlo nel locale di preparazione (UFA), e lavorando sotto cappa, inserirne uno nuovo. Per evitare spargimenti del farmaco, durante la somministrazione, è necessario posizionare un telino sotto il braccio del paziente. Le caratteristiche del telino dovranno essere: assorbente nella parte superiore, impermeabile su quella inferiore e non rilasciare particelle. Bisogna procedere al reperimento della vena rispettando le norme generali di asepsi. Occorre innanzitutto ispezionare ambedue le braccia, il vaso 60
62 venoso deve presentarsi morbido, elastico e di dimensioni adeguate a contenere il catetere o l'ago scelto per la somministrazione. E' meglio scegliere vasi di grosso calibro in zona lontana da plessi nervosi, tendini o grosse arterie; per ridurre il danno da stravaso bisogna scegliere la sede più idonea per l infusione evitando le vene piccole, sclerotiche e in genere quelle degli arti inferiori: Siti di elezione: - vene mediane dell avambraccio; - vena cefalica e basilica; - vene dorsali della mano. Siti da evitare: - fossa anticubitale (grossi vasi un danno da stravaso può essere gravissimo); - flessione del polso e della mano (rapporto diretto con nervi e tendini per una scarsa copertura cutanea); - vasi di piccolo calibro e fragili; - vene infiammate o sclerotiche; - vene degli arti inferiori (transito sanguineo rallentato con rischio di tromboflebiti); - zone con circolazione sanguigna e linfatica compromessa (arti immobilizzati, circolazione compromessa dal tumore, flebiti, ecc.); - zone che drenano in distretti precedentemente irradiati; - zone dove sono state praticate iniezioni sottocutanee. 61
63 5.7.1 Procedure specifiche Introdurre l ago o il catetere venoso nella vena prescelta; raccordare una fleboclisi contenente soluzione fisiologica sia per il lavaggio della vena che per l eventuale idratazione prevista dallo schema chemioterapico. Posizionare una garza sotto il raccordo. Rispettare il seguente ordine di infusione dei chemioterapici: prima il farmaco più vescicante o necrotizzante, poi l irritante ma non vescicante ed infine quello nè irritante nè vescicante; prima dell infusione, tra un farmaco e l altro, infondere sempre almeno 10 ml di soluzione fisiologica per lavare il lume dell accesso venoso ed evitare il depositarsi di piccole quantità di farmaco che potrebbero essere causa di irritazioni locali; alla fine dell infusione per lo stesso motivo, lavare il lume della vena con 100 ml di soluzione fisiologica. Per l estrazione dell ago e l infusione dei farmaci deve essere usato un tampone sterile imbevuto di alcool. Tutti i materiali contaminati devono essere eliminati con cautela in contenitori specifici e adeguatamente identificabili L infermiere che intraprende la somministrazione appunterà sulla scheda di somministrazione l ora di inizio delle infusioni e la controfirmerà. Le azioni concomitanti alla somministrazione prevedono che sia garantita la presenza di almeno un medico oncologo sia all interno del reparto di degenza ordinaria che del DH che sia prontamente disponibile per fronteggiare ogni eventuale evento improvviso connesso alla somministrazione della terapia. 62
64 La vigilanza medica sulle attività del reparto di degenza ordinaria e del DH sono di competenza dei dirigenti medici oncologi e avvengono sotto la loro responsabilità. Sarà inoltre garantita la pronta disponibilità di un medico e di personale infermieristico preparati secondo le modalità Basic Life Support (BLS) per le eventuali urgenze; La gestione dello stravaso da farmaco avverrà seguendo la procedura aziendale, stilata coerentemente con la letteratura e le linee guida più aggiornate. La gestione dello stravaso è di competenza sia del dirigente medico oncologo che dell infermiere professionale ed avviene sotto la responsabilità di entrambe le figure professionali. Gli antidoti e il materiale necessario per lo stravaso nonché la procedura scritta sono rese disponibili sia presso i locali del reparto degenze che presso i locali del DH. Nei locali del reparto di degenza ordinaria e nei locali del DH è garantita la presenza di un carrello adeguatamente attrezzato per far fronte alle emergenze/urgenze e la rapida reperibilità di un monitor per controllare i parametri vitali. La disponibilità degli antidoti e della procedura scritta, nonché del carrello d emergenza è sotto la responsabilità del coordinatore infermieristico. Ogni eventuale reazione avversa inattesa sarà documentata per iscritto da parte dell infermiere nella scheda di somministrazione; il medico che sia 63
65 intervenuto riporterà in diario clinico le informazioni inerenti la reazione verificatasi. Le azioni successive alla somministrazione della terapia antitumorale prevedono che il completamento della procedura di somministrazione, avvenuta secondo quanto previsto dalla scheda di terapia, sia adeguatamente documentata per iscritto dall operatore sanitario che vi ha provveduto; l infermiere che completa la somministrazione appunterà l ora di fine delle infusioni e la controfirmerà INDICATORI SOMMINISTRAZIONE Titolo Attuale Atteso Target n. stravasi/totale somministrazioni n. ADR/totale somministrazioni n. schede di somministrazioni correttamente formalizzate/totale somministrazioni 5.8 DISPENSAZIONE DELLA TERAPIA ORALE ANTITUMORALE La prescrizione della terapia antineoplastica orale avviene all interno dei locali del DH delle UU.OO. di Oncologia ed Ematologia. 64
66 Particolare attenzione viene dedicata dagli operatori sanitari nell informare il paziente in merito alla terapia da seguire, alle modalità e ai tempi di assunzione del farmaco, ai possibili effetti collaterali (verrà spiegato il modo di riconoscerli precocemente, le modalità di comunicazione e soprattutto i comportamenti da adottare come nel caso in cui il farmaco venisse emesso con il vomito), alle ADR, alle incompatibilità farmacologiche nonché ai possibili errori della posologia. Per la valutazione della compliance del paziente, viene compilato un diario in cui annotare il numero di dosi assunte, gli orari, gli effetti collaterali o le eventuali problematiche incontrate. Analogamente a quanto avviene per i farmaci antineoplastici somministrati per via parenterale, anche per i farmaci orali sono utilizzate schede di prescrizione condivise dall intera équipe (medico, farmacista, infermiere). Tali schede, viste le peculiarità gestionali connaturate alla terapia antineoplastica orale, recano le seguenti informazioni: dati anagrafici del paziente (nome, cognome, data e luogo di nascita, residenza); recapiti telefonici del paziente e dell eventuale caregiver; peso, altezza e superficie corporea del paziente; comorbosità; elenco completo dei farmaci assunti dal paziente; posologia del farmaco antineoplastico con indicazione delle dosi da assumere per ogni singola somministrazione, delle modalità di 65
67 assunzione in relazione ai pasti e dell orario di somministrazione. Le dosi totali ed il loro eventuale frazionamento in dosi multiple giornaliere devono essere chiaramente indicate. Sulla scorta del contenuto della scheda di prescrizione, il farmaco viene consegnato al paziente nel quantitativo corrispondente ad un ciclo di cura o altro, secondo indicazioni aziendali, da parte del farmacista dell UFA. Una copia della scheda sarà consegnata al medico curante dal paziente, il quale la esibirà in ogni situazione in cui riceverà una prestazione sanitaria (es. accesso al Pronto soccorso) INDICATORI DISPENSAZIONE DELLA TERAPIA ORALE ANTITUMORALE TITOLO Attuale Atteso Target n. di farmaci dispensati con indicazioni gestione ADR/totale dispensazioni n. di farmaci dispensati con indicazioni gestione dello smaltimento mediante apposito foglio esplicativo 66
68 5.9 IMMAGAZZINAMENTO, CONSERVAZIONE E GESTIONE SCORTE I chemioterapici antiblastici devono essere conservati in aree specifiche della farmacia, appositamente segnalate, non accessibili al personale non addetto, all interno di armadi fissi. Nelle zone di immagazzinamento e ricezione deve essere presente un kit per il contenimento degli spandimenti accidentali. Le scorte di magazzino richiedono una rotazione elevata, sia per la difficoltà di conservazione sia per i costi. Grazie alla presenza di un sistema informatico è possibile predisporre un inventario periodico per la verifica delle giacenze reali e per il riallineamento informatico di lotti e scadenze. 67
69 6. SEZIONE SPERIMENTALE Metodi Per la realizzazione del modello integrato sono stati condivisi e formalizzati da parte della Direzione Aziendale e dal Gruppo di Progetto i seguenti obiettivi: Mission e politica per il miglioramento Obiettivi - impegni e piani per il miglioramento Gestione dei processi (con descrizione e analisi delle criticità e formalizzazione delle buone pratiche clinico-organizzative) Gestione delle risorse umane e tecnologiche (con definizione dei profili professionali, delle schede individuali, del piano formativo e con il coinvolgimento della Ingegneria Clinica dell Ufficio Tecnico dei piani di manutenzione e taratura) Strumenti di verifica (audit) del modello attraverso l individuazione e il monitoraggio di opportuni indicatori di processo e di risultato per la misurazione delle performance del sistema. 68
70 6.1 INDICATORI DI PERFORMANCE ANNO INDICATORI PRESA IN CARICO DEL PAZIENTE Titolo Attuale Atteso Target n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Ematologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in Ematologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Oncologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Ematologia 100% 100% 100% 100% 100% 100% 80% 90% 100% 90% 100% 100% 100% 100% 100% 90% 100% 100% 69
71 5.3.1 INDICATORI PRESCRIZIONE Titolo Attuale Atteso Target n. prescrizione EMA non conformi/totale pervenute in UFA (16/1728 x 100) n. prescrizione ONCO non conformi/totale pervenute in UFA (112/9626 x 100) 0,92% 0,80% 0% 1,16% 0,80% 0% INDICATORI PREPARAZIONE Titolo Attuale Atteso Target n. di errori (near-miss) accaduti nell anno/totale preparazioni (128/19346 x100) n. preparazione conformi alla prescrizione/totale preparazioni (19346/19346 x 100) 0,66% 0,33% 0% 100% 100% 100% 70
72 5.6.3 INDICATORI DISTRIBUZIONE Titolo Attuale Atteso Target Mediana/Media dal tempo che intercorre dalla presa in carico in UFA alla consegna ai reparti n. di bolle di accompagnamento che non seguono il contenitore sino ai reparti/totale bolle predisposte 120 minuti 90 minuti 60 minuti 40% 20% 0% INDICATORI SOMMINISTRAZIONE Titolo Attuale Atteso Target n. stravasi/totale somministrazioni (2/19346 x 100) 0,01% 0% 0% n. ADR/totale somministrazioni (57/19346 x 100) 0,30% 0,60% 0,70% n. schede di prescrizione correttamente formalizzate/totale prescrizioni 100% 100% 100% 71
73 INDICATORI DISPENSAZIONE DELLA TERAPIA ORALE ANTITUMORALE Titolo Attuale Atteso Target n. di farmaci dispensati con indicazione gestione ADR/totale dispensazioni n. di farmaci dispensati con indicazioni gestione dello smaltimento mediante apposito foglio esplicativo 0% 80% 100% 0% 80% 100% 6. INDICATORI PROCEDURA DI GESTIONE DEGLI STRAVASI DI FARMACI CHEMIOTERAPICI ANTIBLASTICI IN ONCOLOGIA-EMATOLOGIA Titolo Attuale Atteso Target n. stravasi/totale procedure eseguite (DH) (2/19346 x 100) 0,01% 0% 0% n. stravasi/totale procedure eseguite (Ricovero) 0% 0% 0% n. stravasi per Dislocazione del reservoir (Port)/n. stravasi 0% 0% 0% (DH) Dislocazione del reservoir (Port)/n. stravasi (Ricovero) 0% 0% 0% 72
74 NEAR MISS ANNO 2013 Titolo Oncologia Ematologia Mancata/Errata Diagnosi 10 0 Firma del Medico (assente) 20 1 Dati del paziente assenti o errati (es. data di nascita/nome, altezza, peso, sup. corporea) Protocollo terapeutico indicato errato/schema terapeutico incompleto o farmaco prescritto errato Data di somministrazione/prescrizione errata (es. anticipata rispetto al protocollo) o assente Tipo di somministrazione indicato errato o assente Protocollo (dosaggio errato ) 21 4 Durata terapia errata o assente 4 0 Dosaggio farmaco assente 5 0 Totale near miss
75 6.2 INDICATORI DI PERFORMANCE ANNO INDICATORI PRESA IN CARICO DEL PAZIENTE Titolo Attuale Atteso Target n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in Oncologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati DH Ematologia n. schede di anamnesi correttamente compilate/totale pazienti ricoverati in Ematologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Oncologia n. consensi correttamente formalizzati/totale pazienti ricoverati in Ematologia 100% 100% 100% 100% 100% 100% 90% 100% 100% 95% 100% 100% 100% 100% 100% 100% 100% 100% 74
76 INDICATORI PRESCRIZIONE Titolo Attuale Atteso Target n. prescrizione EMA non conformi/totale pervenute in UFA (6/1256 x 100) n. prescrizione ONCO non conformi/totale pervenute in UFA (48/6998 x 100) 0,47% 0,40% 0% 0,69% 0,50% 0% INDICATORI PREPARAZIONE Titolo Attuale Atteso Target n. di errori (near-miss) accaduti nell anno/totale preparazioni (54/16338 x100) n. preparazione conformi alla prescrizione/totale preparazioni (16338/16338 x 100) 0,33% 0,23% 0% 100% 100% 100% 75
77 5.6.3 INDICATORI DISTRIBUZIONE Titolo Attuale Atteso Target Mediana/Media dal tempo che intercorre dalla presa in carico in UFA alla consegna ai reparti n. di bolle di accompagnamento che non seguono il contenitore sino ai reparti/totale bolle predisposte 100 minuti 90 minuti 60 minuti 30% 20% 0% INDICATORI SOMMINISTRAZIONE Titolo Attuale Atteso Target n. stravasi/totale somministrazioni (1/16338 x 100) 0,006% 0% 0% n. ADR/totale somministrazioni (110/16338 x 100) 0,67% 0,85% 0,87% n. schede di prescrizione correttamente formalizzate/totale prescrizioni 100% 100% 100% 76
78 5.8.1 INDICATORI DISPENSAZIONE DELLA TERAPIA ORALE ANTITUMORALE Titolo Attuale Atteso Target n. di farmaci dispensati con indicazione gestione ADR/totale dispensazioni 60% 80% 100% n. di farmaci dispensati con indicazioni gestione dello smaltimento mediante apposito foglio esplicativo 60% 80% 100% 6. INDICATORI PROCEDURA DI GESTIONE DEGLI STRAVASI DI FARMACI CHEMIOTERAPICI ANTIBLASTICI IN ONCOLOGIA-EMATOLOGIA Titolo Attuale Atteso Target n. stravasi/totale procedure eseguite (DH) (1/16338 x 100) 0,006% 0% 0% n. stravasi/totale procedure eseguite (Ricovero) 0% 0% 0% n. stravasi per Dislocazione del reservoir (Port)/n. stravasi 0% 0% 0% (DH) Dislocazione del reservoir (Port)/n. stravasi (Ricovero) 0% 0% 0% 77
79 NEAR MISS ANNO 2014 Titolo Oncologia Ematologia Mancata/Errata Diagnosi Firma del Medico (assente) Dati del paziente assenti o errati (es. data di nascita/nome) 10 1 Protocollo (data errata) 3 0 Protocollo (dosaggio errato o assente) 15 1 Protocollo (errato/incompleto o ciclo errato) 17 4 Totale near miss
80 Risultati Attraverso l analisi degli indicatori di performance ottenuti nell anno 2013 e ancor di più nel 2014 si evince come la maggior parte dei risultati ottenuti si avvicini al valore atteso ed in qualche processo anche al valore target. La migliore gestione del sistema di sorveglianza con riferimento agli errori evitati ovvero i near miss cioè agli errori riconosciuti in tempo prima che gli stessi possano provocare eventuali danni al paziente dimostra come il modello sviluppato sia di fondamentale supporto per la sicurezza e qualità delle cure. Inoltre, mediante l analisi organizzativa effettuata sui processi e sulle risorse impiegate è stato possibile declinare gli obiettivi con il piano delle azioni di miglioramento e con la successiva verifica dell efficacia mediante il monitoraggio di specifici indicatori. Il miglioramento misurato, quindi, diventa elemento di trasparenza verso i vari portatori di interesse e di attivazione di un processo di comunicazione all interno della struttura sanitaria basato sulla condivisione di obiettivi comuni, delle criticità riscontrate, dalle strategie da attuare e dei risultati ottenuti. Nella tabella seguente (Tab. 1) si riportano alcuni valori di indicatori di performance attesi per il 2015 ottenibili mediante azioni di miglioramento continuo al fine di ridurre ulteriormente gli errori nella fasi di prescrizione e somministrazione della terapia e limitare gli eventi avversi da farmaco. 79
81 Titolo attuale al 2014 atteso al 2015 n. totale degli errori prescrizione/n. totale terapie prescritte 1,16% 0,80% n. errori in fase di somministrazione/n. totale somministrazioni 0,01% 0% n. di errori accaduti nell'anno/n. totale preparazioni 0,66% 0,33% n. eventi avversi /n. totale somministrazioni 0,01% 0% Tab. 1 Valori di indicatori di performance attesi al
82 7. CONCLUSIONI La gestione centralizzata delle terapie oncologiche presuppone la creazione di un team multidiscliplinare e predispone quindi alla condivisione delle tematiche e delle criticità e all attuazione delle migliori condizioni di espletamento delle cure. Queste azioni di governo clinico rafforzano ulteriormente le sinergie tra i professionisti coinvolti nel processo terapeutico, in particolare tra il medico oncologo ed i farmacisti. Il modello integrato UFA-ONCO-EMA sviluppato dall ARNAS Garibaldi di Catania per la produzione e gestione del farmaco antitumorale ha rappresentato un esperienza pilota unica a livello regionale. Questo modello di governo clinico garantisce la sicurezza del paziente e assicura cure più opportune per la gestione della patologia ed è stato preso come riferimento da parte dell Assessorato della Salute per un progetto rivolto a tutte le strutture pubbliche e private della Regione Sicilia. Inoltre, la certificazione del processo di produzione e gestione del farmaco antitumorale pone l ARNAS Garibaldi in linea con la Raccomandazione n. 14 dell ottobre 2012 con la quale il Ministero della Salute ha invitato tutti gli operatori sanitari impegnati nell assistenza al paziente oncologico a porre particolare cure e attenzione alle criticità che inevitabilmente si incontrano nella presa in carico di soggetti affetti da patologie così invalidanti e a multipla compromissione. La validazione e l ottenimento della certificazione ISO 9001 del processo di produzione e gestione farmaci antiblastici da parte dell ARNAS Garibaldi 81
83 ha consentito di creare una cultura organizzativa capace di accrescere la credibilità con cui l organizzazione si autoresponsabilizza nel rispettare le regole stabilite e nella pragmaticità di misurare i risultati raggiunti. Il Gruppo di Progetto, pertanto, rimane attivamente impegnato nel completare e consolidare il modello organizzativo di governo clinico al fine di dimostrare nel tempo la propria capacità di migliorare i risultati in termini di rendimento dell intero processo di gestione del farmaco antitumorale. 82
84 BIBLIOGRAFIA [1] Farmacopea Ufficiale della Repubblica Italiana. XII edizione. Roma: Istituto Poligrafico dello Stato, [2] Good Manufacturing Practice European Commission (GMP). Vol. 4 all.1: Manufacture of sterile medicine products 25/11/2008 (rev.). [3] Medaglia, Pastori, Vimercati. Schede d informazione farmacologica per il paziente oncologico, 2001 pag 7-10 [4] Legge 448 del 23/12/1998 Misure di finanza pubblica per la stabilizzazione e lo sviluppo" (articolo 68; comma 6) [5] Decreto 18 febbraio 1999 Modifica del regime di fornitura dei medicinali antiblastici iniettabili (articolo 1) [6] D.Lgs. 14/07/1999 Modalità di dispensazione dei medicinali antiblastici iniettabili. (articolo 1) [7] D.Legs. del 19 settembre 1994 n 626 e 19 marzo 1996 n 242- Titolo VII Protezione da agenti cancerogeni (articolo 60-72) [8] Provvedimento 5 agosto 1999 (G.U. n 236 del 7 ottobre 1999 ) Documento di linee-guida per la sicurezza e la salute dei lavoratori esposti a chemioterapici antiblastici in ambiente sanitario. (articolo 4.2) [9] Ferderici, Farina, Mattioli. Il farmacista e l oncologia oggi: aspetti metodologici ed organizzativi di un team multidisciplinare. 2011, pag
85 [10] Raccomandazione n. 7 marzo 2008 Ministero della Salute Raccomandazione per la prevenzione della morte, coma o grave danno derivanti da errore nella terapia farmacologica [11] Raccomandazione n. 14 ottobre 2012 Ministero della Salute Raccomandazione per la prevenzione degli errori in terapia con farmaci antineoplastici [12] Decreto 10 ottobre 2012 Regione Sicilia Centralizzazione dei farmaci antiblastici (articolo 1, 4, 6) [13] Decreto 14 ottobre 2013 Regione Sicilia Implementazione del modello di governo clinico integrato U.F.A.-ONCO-EMA (articolo 2) [14] Decreto 14 aprile 2014 Regione Sicilia Approvazione del programma regionale per la sicurezza, appropriatezza e gestione complessiva della terapia antitumorale (allegato) [15] Decreto 14 ottobre 2013 Regione Sicilia Implementazione del modello di governo clinico integrato U.F.A.-ONCO-EMA (allegato) [16] Procedura approvata dalla Direzione Sanitaria dell ARNAS Garibaldi di Catania. Gestione della terapia antitumorale in UFA-ONCOLOGIA- EMATOLOGIA: approvvigionamento, prescrizione, preparazione, distribuzione, somministrazione, dispensazione terapia orale, immagazzinamento stoccaggio e conservazione, 2014, pag
86 RINGRAZIAMENTI Desidero ringraziare il mio relatore Prof. Giovanni Puglisi per la disponibilità dimostrata e per i preziosi insegnamenti profusi. Ringrazio il mio correlatore Dott.ssa Giuseppina Fassari per aver suscitato in me interesse ed entusiasmo verso questo settore della terapia oncologica ed i farmacisti dell ospedale ARNAS Garibaldi di Catania per essere stati punto di riferimento durante il percorso di tesi. Un ringraziamento all assistente di Progetto UFA-ONCO-EMA la Dott.ssa Desiree Caudullo ed a tutti i componenti del Gruppo di Progetto per la collaborazione ed il valido contributo nell analisi dei dati sperimentali. 85
Azienda sanitaria Provinciale Enna PROCESSO DI GESTIONE DELLA TERAPIA ANTITUMORALE IN UFA ONCOLOGIA EMATOLOGIA APPROVIGIONAMENTO
 Pagina 1 di 5 APPROVIGIONAMENTO Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott. Giuseppe Scollo Farmacista Borsista Dott.ssa Maria Teresa Verifica Perricone
Pagina 1 di 5 APPROVIGIONAMENTO Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott. Giuseppe Scollo Farmacista Borsista Dott.ssa Maria Teresa Verifica Perricone
Gestione dei Farmaci Off-Label
 Pagina 1 di 6 Gestione dei Farmaci Off-Label Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Verifica Approvazione Martino Responsabile UFA Dott.ssa Maria Teresa Perricone Direttore U.O.C.
Pagina 1 di 6 Gestione dei Farmaci Off-Label Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Verifica Approvazione Martino Responsabile UFA Dott.ssa Maria Teresa Perricone Direttore U.O.C.
La raccomandazione n. 14: il punto di vista dell Azienda Sanitaria
 PRORA Progetto Regionale in oncoematologia di assessment sulla raccomandazione per i farmaci antineoplastici presentazione degli esiti La gestione del rischio clinico nelle rete Oncoematologica Piemontese
PRORA Progetto Regionale in oncoematologia di assessment sulla raccomandazione per i farmaci antineoplastici presentazione degli esiti La gestione del rischio clinico nelle rete Oncoematologica Piemontese
LE PROCEDURE INFORMATICHE PER LA GESTIONE DEL PROCESSO TERAPEUTICO IN ONCOLOGIA
 La Rete delle Farmacie Oncologiche della Regione Emilia Romagna I Corso regionale per Farmacisti e Tecnici di Laboratorio dell'area Oncologica Bologna, 20-21 ottobre 2009 LE PROCEDURE INFORMATICHE PER
La Rete delle Farmacie Oncologiche della Regione Emilia Romagna I Corso regionale per Farmacisti e Tecnici di Laboratorio dell'area Oncologica Bologna, 20-21 ottobre 2009 LE PROCEDURE INFORMATICHE PER
RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI»
 RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI» Bologna 8 Aprile 2014 APPROVVIGIONAMENTO e STOCCAGGIO del FARMACO ANTINEOPLASTICO
RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI» Bologna 8 Aprile 2014 APPROVVIGIONAMENTO e STOCCAGGIO del FARMACO ANTINEOPLASTICO
Le relazioni tra i laboratori di Allestimento dei Farmaci Oncologici (UFA) e le Unità di Cura del paziente oncologico
 LA RETE DELLE FARMACIE ONCOLOGICHE DELLA REGIONE EMILIA ROMAGNA: 1 CORSO REGIONALE PER FARMACISTI E TECNICI DI LABORATORIO DELL AREA ONCOLOGICA Bologna, 20-21 ottobre 2009 Le relazioni tra i laboratori
LA RETE DELLE FARMACIE ONCOLOGICHE DELLA REGIONE EMILIA ROMAGNA: 1 CORSO REGIONALE PER FARMACISTI E TECNICI DI LABORATORIO DELL AREA ONCOLOGICA Bologna, 20-21 ottobre 2009 Le relazioni tra i laboratori
Sicurezza e salute del paziente oncologico
 Rischi e prevenzione nella manipolazione dei farmaci antiblastici Cagliari Maggio 2010 Sicurezza e salute del paziente oncologico riferimenti normativi e linee guida a garanzia della qualità e della sicurezza
Rischi e prevenzione nella manipolazione dei farmaci antiblastici Cagliari Maggio 2010 Sicurezza e salute del paziente oncologico riferimenti normativi e linee guida a garanzia della qualità e della sicurezza
Dr.ssa Cristiana Romanazzi
 LE MIGLIORI PRATICHE ORGANIZZATIVE NEI LABORATORI DI ALLESTIMENTO DEI FARMACI ONCOLOGICI (UFA) NELL OTTICA DELLA RETE OSPEDALIERA sviluppo di un progetto Dr.ssa Cristiana Romanazzi La rete delle farmacie
LE MIGLIORI PRATICHE ORGANIZZATIVE NEI LABORATORI DI ALLESTIMENTO DEI FARMACI ONCOLOGICI (UFA) NELL OTTICA DELLA RETE OSPEDALIERA sviluppo di un progetto Dr.ssa Cristiana Romanazzi La rete delle farmacie
Silla Antonelli Farmacia Ospedaliera Villa Scassi ASL3 Genovese Costanza Nurchis - Farmacia Ospedaliera Villa Scassi ASL3 Genovese
 APPROPRIATEZZA FARMACI ANTIBIOTICI RICHIESTA MOTIVATA INFORMATIZZATA Silla Antonelli Farmacia Ospedaliera Villa Scassi ASL3 Genovese Costanza Nurchis - Farmacia Ospedaliera Villa Scassi ASL3 Genovese FARMACI
APPROPRIATEZZA FARMACI ANTIBIOTICI RICHIESTA MOTIVATA INFORMATIZZATA Silla Antonelli Farmacia Ospedaliera Villa Scassi ASL3 Genovese Costanza Nurchis - Farmacia Ospedaliera Villa Scassi ASL3 Genovese FARMACI
Prescrizione (Racc. RER n.3: sez. 4.3)
 Direzione Generale Giunta Regionale Sanità e Politiche Sociali Direzione Servizio Generale Politica Sanitàdel e Politiche FarmacoSociali Raccomandazione Regionale per la sicurezza nella terapia farmacologica
Direzione Generale Giunta Regionale Sanità e Politiche Sociali Direzione Servizio Generale Politica Sanitàdel e Politiche FarmacoSociali Raccomandazione Regionale per la sicurezza nella terapia farmacologica
Chiara Volpone. I PDTA: A come Assistenziale
 Chiara Volpone I PDTA: A come Assistenziale in un contesto ad elevata complessità e con risorse limitate come quello del SSN, la Pianificazione e la Programmazione sono di estrema rilevanza ai fini del
Chiara Volpone I PDTA: A come Assistenziale in un contesto ad elevata complessità e con risorse limitate come quello del SSN, la Pianificazione e la Programmazione sono di estrema rilevanza ai fini del
Responsabile - AREA FARMACEUTICA OSPEDALIERA -ASP RAGUSA
 INFORMAZIONI PERSONALI Nome RIZZA GIUSEPPINA Data di nascita 18/11/1956 Qualifica Amministrazione Incarico attuale Numero telefonico dell ufficio FARMACISTA OSPEDALIERO ASL DI RAGUSA Responsabile - AREA
INFORMAZIONI PERSONALI Nome RIZZA GIUSEPPINA Data di nascita 18/11/1956 Qualifica Amministrazione Incarico attuale Numero telefonico dell ufficio FARMACISTA OSPEDALIERO ASL DI RAGUSA Responsabile - AREA
Standardizzazione e Informatizzazione delle prescrizioni delle terapie
 CENTRALIZZAZIONE TERAPIE ONCOLOGICHE IOV, 5 febbraio 2014 Standardizzazione e Informatizzazione delle prescrizioni delle terapie antitumorali Vittorina Zagonel Direttore U.O.C. Oncologia Medica 1 Istituto
CENTRALIZZAZIONE TERAPIE ONCOLOGICHE IOV, 5 febbraio 2014 Standardizzazione e Informatizzazione delle prescrizioni delle terapie antitumorali Vittorina Zagonel Direttore U.O.C. Oncologia Medica 1 Istituto
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Politiche del Farmaco e dei Dispositivi Medici Dott.ssa E.
 REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Politiche del Farmaco e dei Dispositivi Medici Dott.ssa E. Giordani PROCEDURA AUDIT ARMADIO FARMACEUTICO DI REPARTO Rev. 0 Del 22/02/2017
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Politiche del Farmaco e dei Dispositivi Medici Dott.ssa E. Giordani PROCEDURA AUDIT ARMADIO FARMACEUTICO DI REPARTO Rev. 0 Del 22/02/2017
LISTA DI RISCONTRO PER GLI AUDIT INTERNI
 INTEGRATI QUALITA E SICUREZZA Data: Unità Operativa: Cognome e Nome Auditor Firma Personale contattato: Cognome e Nome Ruolo Area/ processi auditati: Considerazioni Complessive Pagina 1 di 9 Modalità di
INTEGRATI QUALITA E SICUREZZA Data: Unità Operativa: Cognome e Nome Auditor Firma Personale contattato: Cognome e Nome Ruolo Area/ processi auditati: Considerazioni Complessive Pagina 1 di 9 Modalità di
Dalle Linee Guida ministeriali alla Raccomandazione ministeriale N.14, alla Raccomandazione regionale n. 3
 Giunta Regionale Direzione Generale Sanità e Politiche Sociali Servizio Politica del Farmaco Raccomandazione Regionale per la sicurezza nella terapia farmacologica n. 3 Gestione sicura dei farmaci antineoplastici
Giunta Regionale Direzione Generale Sanità e Politiche Sociali Servizio Politica del Farmaco Raccomandazione Regionale per la sicurezza nella terapia farmacologica n. 3 Gestione sicura dei farmaci antineoplastici
Redatta da : Condivisa da : Visionata da: Approvata da:
 AZIENDA OSPEDALIERA UNIVERSITARIA FEDERICO II FARMACIA CENTRALIZZATA U.F.A PROCEDURA OPERATIVA PER L ALLESTIMENTO PREPARAZIONI ANTIBLASTICHE IN U.F.A PER U.O.C ESTERNE AL DH DI ONCOEMATOLOGIA Redatta da
AZIENDA OSPEDALIERA UNIVERSITARIA FEDERICO II FARMACIA CENTRALIZZATA U.F.A PROCEDURA OPERATIVA PER L ALLESTIMENTO PREPARAZIONI ANTIBLASTICHE IN U.F.A PER U.O.C ESTERNE AL DH DI ONCOEMATOLOGIA Redatta da
Premessa. Responsabilità La responsabilità associata alla gestione della presente procedura è precisata nella Tabella 1 ( allegato 1)
 Premessa La somministrazione inappropriata endovenosa di sali di Potassio può comportare grave rischio per il paziente ed è una delle principali cause di incidenti ad effetto letale nelle unità operative
Premessa La somministrazione inappropriata endovenosa di sali di Potassio può comportare grave rischio per il paziente ed è una delle principali cause di incidenti ad effetto letale nelle unità operative
L ACCREDITAMENTO ISTITUZIONALE. Aspetti e requisiti generali Requisiti specifici dei Laboratori
 L ACCREDITAMENTO ISTITUZIONALE Aspetti e requisiti generali Requisiti specifici dei Laboratori Obiettivi della presentazione Approfondire il significato ed il modello di Accreditamento Istituzionale Analizzare
L ACCREDITAMENTO ISTITUZIONALE Aspetti e requisiti generali Requisiti specifici dei Laboratori Obiettivi della presentazione Approfondire il significato ed il modello di Accreditamento Istituzionale Analizzare
Prescrizione informatizzata e distribuzione dei farmaci in dose unitaria. Dr. Saverio Santachiara Direzione Assistenza Farmaceutica
 Prescrizione informatizzata e distribuzione dei farmaci in dose unitaria Dr. Saverio Santachiara Direzione Assistenza Farmaceutica Rischio clinico del farmaco: In Italia si stima che, ogni anno, su 8 milioni
Prescrizione informatizzata e distribuzione dei farmaci in dose unitaria Dr. Saverio Santachiara Direzione Assistenza Farmaceutica Rischio clinico del farmaco: In Italia si stima che, ogni anno, su 8 milioni
Dal 1 marzo 2015 a tutt oggi
 INFORMAZIONI PERSONALI Nome MARIA FELICITA LISSIA Data di nascita 9 novembre 1956 Nazionalità ITALIANA Numero telefonico 0677054493 E-mail [email protected] TITOLI DI STUDIO E PROFESSIONALI
INFORMAZIONI PERSONALI Nome MARIA FELICITA LISSIA Data di nascita 9 novembre 1956 Nazionalità ITALIANA Numero telefonico 0677054493 E-mail [email protected] TITOLI DI STUDIO E PROFESSIONALI
afferente al Dipartimento Qualità e Sicurezza dei percorsi di Diagnosi e Cura
 afferente al Dipartimento Qualità e Sicurezza dei percorsi di Diagnosi e Cura Direttore Struttura Complessa: Dott. Francesco CATTEL SEDE E CONTATTI Ospedale Molinette - Ubicazione: Corso Bramante, 88-10126
afferente al Dipartimento Qualità e Sicurezza dei percorsi di Diagnosi e Cura Direttore Struttura Complessa: Dott. Francesco CATTEL SEDE E CONTATTI Ospedale Molinette - Ubicazione: Corso Bramante, 88-10126
Cloruro Di Potassio 27/05/2005 (Livello 2)
 Cloruro Di Potassio 27/05/2005 (Livello 2) Ministero Della Salute Raccomandazioni Sul Corretto Utilizzo Delle Soluzioni Concentrate di Cloruro di Potassio E Altre Soluzioni Concentrate con Potassio Documento
Cloruro Di Potassio 27/05/2005 (Livello 2) Ministero Della Salute Raccomandazioni Sul Corretto Utilizzo Delle Soluzioni Concentrate di Cloruro di Potassio E Altre Soluzioni Concentrate con Potassio Documento
I piani terapeutici informatizzati in Regione Liguria. Dott.ssa Maria Susanna Rivetti
 I piani terapeutici informatizzati in Regione Liguria Dott.ssa Maria Susanna Rivetti 1 Note limitative Con il provvedimento 30 dicembre 1993 di riclassificazione dei medicinali sono state introdotte le
I piani terapeutici informatizzati in Regione Liguria Dott.ssa Maria Susanna Rivetti 1 Note limitative Con il provvedimento 30 dicembre 1993 di riclassificazione dei medicinali sono state introdotte le
Per un Ospedale Sicuro: l approccio del Policlinico di Modena
 Per un Ospedale Sicuro: l approccio del Policlinico di Modena Stefano Cencetti Direttore Generale Azienda ospedaliero-universitaria Policlinico Modena In collaborazione con Direzione Sanitaria Direzione
Per un Ospedale Sicuro: l approccio del Policlinico di Modena Stefano Cencetti Direttore Generale Azienda ospedaliero-universitaria Policlinico Modena In collaborazione con Direzione Sanitaria Direzione
Il Modello centralizzato degli acquisti in sanità
 Meeting Acquisti nella filiera della salute Strategie e Politiche di acquisto nella filiera della salute Il Modello centralizzato degli acquisti in sanità Dott. Giuseppe Laganga Senzio Direttore Dipartimento
Meeting Acquisti nella filiera della salute Strategie e Politiche di acquisto nella filiera della salute Il Modello centralizzato degli acquisti in sanità Dott. Giuseppe Laganga Senzio Direttore Dipartimento
REGIONE EMILIA ROMAGNA Cartella Clinica Integrata. Bologna 5 dicembre 2013
 REGIONE EMILIA ROMAGNA Cartella Clinica Integrata Bologna 5 dicembre 2013 L esperienza della Cartella Clinica Integrata Elettronica nell Azienda Ospedaliera di Desenzano del Garda Lorenzini A. Rovere A.
REGIONE EMILIA ROMAGNA Cartella Clinica Integrata Bologna 5 dicembre 2013 L esperienza della Cartella Clinica Integrata Elettronica nell Azienda Ospedaliera di Desenzano del Garda Lorenzini A. Rovere A.
IL POLICLINICO TOR VERGATA. Tiziana Frittelli 25/02/2015
 IL POLICLINICO TOR VERGATA Tiziana Frittelli 25/02/2015 Chi siamo La Fondazione PTV è stata costituita dalla Regione Lazio e dall Università di Roma-Tor Vergata in base alle previsioni del Protocollo d
IL POLICLINICO TOR VERGATA Tiziana Frittelli 25/02/2015 Chi siamo La Fondazione PTV è stata costituita dalla Regione Lazio e dall Università di Roma-Tor Vergata in base alle previsioni del Protocollo d
IL PROCESSO DI CERTIFICAZIONE UNI EN ISO 9001 DEI DIPARTIMENTI DI PREVENZIONE
 IL PROCESSO DI CERTIFICAZIONE UNI EN ISO 9001 DEI DIPARTIMENTI DI PREVENZIONE NORMATIVA UNI EN ISO 9001/2008 Disciplinare tecnico-normativo applicato per il rilascio della certificazione da parte degli
IL PROCESSO DI CERTIFICAZIONE UNI EN ISO 9001 DEI DIPARTIMENTI DI PREVENZIONE NORMATIVA UNI EN ISO 9001/2008 Disciplinare tecnico-normativo applicato per il rilascio della certificazione da parte degli
Modalità di pulizia della cappa, della S.A.S., materiali e del piano di lavoro
 Istruzione Operativa Modalità di pulizia della cappa, della S.A.S., materiali e del piano di lavoro I_ PGS-DSA-7-01_14 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
Istruzione Operativa Modalità di pulizia della cappa, della S.A.S., materiali e del piano di lavoro I_ PGS-DSA-7-01_14 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
La centralizzazione come elemento di sicurezza per i pazienti
 INCONTRO REGIONALE Istituto Oncologico Veneto IRCCS PADOVA Aula magna 5 febbraio 2013 La centralizzazione come elemento di sicurezza per i pazienti Maria Giacobbo Direttore Sanitario Istituto Oncologico
INCONTRO REGIONALE Istituto Oncologico Veneto IRCCS PADOVA Aula magna 5 febbraio 2013 La centralizzazione come elemento di sicurezza per i pazienti Maria Giacobbo Direttore Sanitario Istituto Oncologico
DIPARTIMENTO FARMACEUTICO
 DIPARTIMENTO FARMACEUTICO DIRETTORE UOC: Dott. Isodoro Mazzoni Tel. 0735 793524 0736 358856 Mail: [email protected] SEDE : Ascoli Piceno : via degli Iris, San Benedetto del Tronto : via
DIPARTIMENTO FARMACEUTICO DIRETTORE UOC: Dott. Isodoro Mazzoni Tel. 0735 793524 0736 358856 Mail: [email protected] SEDE : Ascoli Piceno : via degli Iris, San Benedetto del Tronto : via
SCUOLA DI FARMACIA OSPEDALIERA PIANO DEGLI STUDI NUOVO CICLO AA 2016/2017 Attività Formative
 SUDDIVISIONE DELLE DISCIPLINE I ANNO FA0107 ATTIVITA PROFESSIONALIZZANTI AREA GESTIONALE E DI GOVERNO CLINICO I SCUOLA DI FARMACIA OSPEDALIERA PIANO DEGLI STUDI NUOVO CICLO AA 2016/2017 Formative Professionalizzanti
SUDDIVISIONE DELLE DISCIPLINE I ANNO FA0107 ATTIVITA PROFESSIONALIZZANTI AREA GESTIONALE E DI GOVERNO CLINICO I SCUOLA DI FARMACIA OSPEDALIERA PIANO DEGLI STUDI NUOVO CICLO AA 2016/2017 Formative Professionalizzanti
PROCEDURA GESTIONE FARMACI AD ALTO RISCHIO
 Dipartimento del Ed. 0 Rev. 00 originale copia controllata copia non controllata bozza N. distribuzione interna a cura del RQ La presente procedura definisce le modalità di approvvigionamento, stoccaggio,
Dipartimento del Ed. 0 Rev. 00 originale copia controllata copia non controllata bozza N. distribuzione interna a cura del RQ La presente procedura definisce le modalità di approvvigionamento, stoccaggio,
Profilassi antibiotica in chirurgia La gestione del processo: dalla prescrizione alla verifica
 Profilassi antibiotica in chirurgia La gestione del processo: dalla prescrizione alla verifica Vicenza, 27 Febbraio 2009 Giovanna Scroccaro Dipartimento di Farmacia Azienda Ospedaliera di Verona Strategie
Profilassi antibiotica in chirurgia La gestione del processo: dalla prescrizione alla verifica Vicenza, 27 Febbraio 2009 Giovanna Scroccaro Dipartimento di Farmacia Azienda Ospedaliera di Verona Strategie
La continuità assistenziale
 Le reti oncologiche regionali Presente, problematiche e prospettive future La continuità assistenziale Giuseppe Nastasi U.O.C. Oncologia Medica A.O. Bolognini - Seriate (BG) Camera dei Deputati - Palazzo
Le reti oncologiche regionali Presente, problematiche e prospettive future La continuità assistenziale Giuseppe Nastasi U.O.C. Oncologia Medica A.O. Bolognini - Seriate (BG) Camera dei Deputati - Palazzo
2. STRUTTURA ORGANIZZATIVA
 42 2. STRUTTURA ORGANIZZATIVA 2.1 43 Questa sezione del D.A. 890/2002 comprende 7 requisiti identificati dalla sigla SROR1.1A, i cui contenuti essenzialmente rappresentati dalla richiesta di definire e
42 2. STRUTTURA ORGANIZZATIVA 2.1 43 Questa sezione del D.A. 890/2002 comprende 7 requisiti identificati dalla sigla SROR1.1A, i cui contenuti essenzialmente rappresentati dalla richiesta di definire e
Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3
 giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
BOLLETTINO UFFICIALE DELLA REGIONE CAMPANIA - N. 67 DEL 19 DICEMBRE 2005
 BOLLETTINO UFFICIALE DELLA REGIONE CAMPANIA - N. 67 DEL 19 DICEMBRE 2005 REGIONE CAMPANIA - Giunta Regionale - Seduta del 26 novembre 2005 - Deliberazione N. 1690 - Area Generale di Coordinamento N. 20
BOLLETTINO UFFICIALE DELLA REGIONE CAMPANIA - N. 67 DEL 19 DICEMBRE 2005 REGIONE CAMPANIA - Giunta Regionale - Seduta del 26 novembre 2005 - Deliberazione N. 1690 - Area Generale di Coordinamento N. 20
DAY HOSPITAL ONCOLOGICO REQUISITI MINIMI SPECIFICI
 Allegato n. 5 alla Delib.G.R. n. 29.9.2015 DAY HOSPITAL ONCOLOGICO REQUISITI MINIMI SPECIFICI Scheda Il Day Hospital Oncologico e/o Oncoematologico costituisce il ricovero diurno funzionale alla somministrazione
Allegato n. 5 alla Delib.G.R. n. 29.9.2015 DAY HOSPITAL ONCOLOGICO REQUISITI MINIMI SPECIFICI Scheda Il Day Hospital Oncologico e/o Oncoematologico costituisce il ricovero diurno funzionale alla somministrazione
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani
 REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani CHECK LIST AUTOCONTROLLO MAGAZZINO FARMACIA Allegato n. 2 Procedura Audit Armadio
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani CHECK LIST AUTOCONTROLLO MAGAZZINO FARMACIA Allegato n. 2 Procedura Audit Armadio
Le iniziative CIPOMO Gestione farmaci: risultati della Survey CIPOMO
 GIORGIO DE SIGNORIBUS Direttore U.O. di Oncologia Medica Ospedale Civile Madonna del Soccorso ASUR Marche AV5 Le iniziative CIPOMO Gestione farmaci: risultati della Survey CIPOMO Dove eravamo rimasti?
GIORGIO DE SIGNORIBUS Direttore U.O. di Oncologia Medica Ospedale Civile Madonna del Soccorso ASUR Marche AV5 Le iniziative CIPOMO Gestione farmaci: risultati della Survey CIPOMO Dove eravamo rimasti?
ASSESSORATO DELL IGIENE E SANITA E DELL ASSISTENZA SOCIALE CENTRO UNICO PREPARAZIONE FARMACI ANTITUMORALI
 Il Centro Unico di Preparazione Farmaci Antitumorali, risponde alla necessità di garantire un adeguato sistema di prevenzione, protezione e controllo per gli operatori che professionalmente manipolano
Il Centro Unico di Preparazione Farmaci Antitumorali, risponde alla necessità di garantire un adeguato sistema di prevenzione, protezione e controllo per gli operatori che professionalmente manipolano
Prescrizione e dispensazione di terapie oncologiche per via orale
 1 di 8 Allegato B: Prescrizione e dispensazione di terapie oncologiche per via LISTA DI DISTRIBUZIONE Farmacia ospedaliera Unità operative Direzione sanitaria 13.03.2015 Redazione Gruppo di studio Rapporti
1 di 8 Allegato B: Prescrizione e dispensazione di terapie oncologiche per via LISTA DI DISTRIBUZIONE Farmacia ospedaliera Unità operative Direzione sanitaria 13.03.2015 Redazione Gruppo di studio Rapporti
LA GESTIONE DEGLI ANTIBLASTICI:
 CORSO DI FORMAZIONE LA GESTIONE DEGLI ANTIBLASTICI: (le linee-guida per la sicurezza e la salute dei lavoratori esposti a chemioterapici antiblastici in ambiente sanitario) LA CENTRALIZZAZIONE DELLE STRUTTURE
CORSO DI FORMAZIONE LA GESTIONE DEGLI ANTIBLASTICI: (le linee-guida per la sicurezza e la salute dei lavoratori esposti a chemioterapici antiblastici in ambiente sanitario) LA CENTRALIZZAZIONE DELLE STRUTTURE
La gestione del dolore nell integrazione ospedale e territorio: il ruolo del Medico di Medicina Generale
 La gestione del dolore nell integrazione ospedale e territorio: il ruolo del Medico di Medicina Generale Ospedale senza dolore un percorso integrato in continuo miglioramento Daniele Govi Medico di Medicina
La gestione del dolore nell integrazione ospedale e territorio: il ruolo del Medico di Medicina Generale Ospedale senza dolore un percorso integrato in continuo miglioramento Daniele Govi Medico di Medicina
RAZIONALIZZAZIONE DEL SISTEMA INFORMATIVO OSPEDALIERO
 RAZIONALIZZAZIONE DEL SISTEMA INFORMATIVO OSPEDALIERO Premessa Nei moderni sistemi informativi sanitari il sempre maggior bisogno di informazioni è dovuto a nuovi cambiamenti l ingresso di nuovi attori
RAZIONALIZZAZIONE DEL SISTEMA INFORMATIVO OSPEDALIERO Premessa Nei moderni sistemi informativi sanitari il sempre maggior bisogno di informazioni è dovuto a nuovi cambiamenti l ingresso di nuovi attori
G. Italiano Dipartimento Farmaceutico ASP Palermo
 G. Italiano Dipartimento Farmaceutico ASP Palermo REGIONE SICILIA 1. La dispensazione dei medicinali necessari dovrà essere effettuata direttamente dalle Aziende sanitarie provinciali di residenza del
G. Italiano Dipartimento Farmaceutico ASP Palermo REGIONE SICILIA 1. La dispensazione dei medicinali necessari dovrà essere effettuata direttamente dalle Aziende sanitarie provinciali di residenza del
Emanuele Mognon. Dati anagrafici Luogo e data di nascita Padova, Titoli di studio. Coniugato. Azienda Ospedaliera di Padova
 Emanuele Mognon Dati anagrafici Luogo e data di nascita Padova, 1970 Stato civile Coniugato Domicilio Azienda Ospedaliera di Padova Recapito telefonico 049 8214602-4636 e-mail [email protected]
Emanuele Mognon Dati anagrafici Luogo e data di nascita Padova, 1970 Stato civile Coniugato Domicilio Azienda Ospedaliera di Padova Recapito telefonico 049 8214602-4636 e-mail [email protected]
Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione)
 Istruzione Operativa Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione) I_ PGS-DSA-7-01_08 ed. 0 rev. 00 17 giugno 2014 originale X informatica cartacea copia non controllata
Istruzione Operativa Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione) I_ PGS-DSA-7-01_08 ed. 0 rev. 00 17 giugno 2014 originale X informatica cartacea copia non controllata
REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A.
 Allegato n. 2 alla Delib.G.R. n. 47/15 del 29.9.2015 REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A. Scheda La preparazione dei farmaci antineoplastici per somministrazione parenterale,
Allegato n. 2 alla Delib.G.R. n. 47/15 del 29.9.2015 REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A. Scheda La preparazione dei farmaci antineoplastici per somministrazione parenterale,
Stato delle Attività di centralizzazione delle terapie oncologiche Regione Veneto
 Stato delle Attività di centralizzazione delle terapie oncologiche Regione Veneto Risultati Indagine conoscitiva Servizio Farmaceutico Regionale dr.ssa Valentina Fantelli e dr.ssa Silvia Adami Aula Magna
Stato delle Attività di centralizzazione delle terapie oncologiche Regione Veneto Risultati Indagine conoscitiva Servizio Farmaceutico Regionale dr.ssa Valentina Fantelli e dr.ssa Silvia Adami Aula Magna
ALLEGATO A. Raccomandazioni per la realizzazione di un programma di Antibiotic Stewardship in ospedale
 ALLEGATO A Raccomandazioni per la realizzazione di un programma di Antibiotic Stewardship in ospedale Premessa In Toscana, negli ospedali durante il 2014 sono stati consumati 88,9 DDD di antibiotici per
ALLEGATO A Raccomandazioni per la realizzazione di un programma di Antibiotic Stewardship in ospedale Premessa In Toscana, negli ospedali durante il 2014 sono stati consumati 88,9 DDD di antibiotici per
Il Ruolo della Direzione Sanitaria
 Il Ruolo della Direzione Sanitaria Agenda La rete ospedale territorio per la lotta al dolore La rete ospedale territorio per la lotta al dolore Impegno Istituzionale obiettivi alle aziende le norme e gli
Il Ruolo della Direzione Sanitaria Agenda La rete ospedale territorio per la lotta al dolore La rete ospedale territorio per la lotta al dolore Impegno Istituzionale obiettivi alle aziende le norme e gli
I PDTA in Medicina Fisica e Riabilitativa, una strategia per contemperare appropriatezza, efficacia ed efficienza della prestazione
 I PDTA in Medicina Fisica e Riabilitativa, una strategia per contemperare appropriatezza, efficacia ed efficienza della prestazione Dott. Lorenzo Antonio de Candia Direttore Dipartimento Medicina Fisica
I PDTA in Medicina Fisica e Riabilitativa, una strategia per contemperare appropriatezza, efficacia ed efficienza della prestazione Dott. Lorenzo Antonio de Candia Direttore Dipartimento Medicina Fisica
6. GESTIONE, VALUTAZIONE E MIGLIORAMENTO DELLA QUALITÀ
 176 6. GESTIONE, VALUTAZIONE E MIGLIORAMENTO DELLA QUALITÀ 6.1 177 Questa sezione del D.A. 890/2002 comprende 13 requisiti identificati dalla sigla SVQM.1.1A che richiedono: - la pianificazione dell attività
176 6. GESTIONE, VALUTAZIONE E MIGLIORAMENTO DELLA QUALITÀ 6.1 177 Questa sezione del D.A. 890/2002 comprende 13 requisiti identificati dalla sigla SVQM.1.1A che richiedono: - la pianificazione dell attività
Le buone pratiche. Sicurezza in sala operatoria: esperienze regionali a confronto - REGIONE SICILIA - Tommaso Mannone Risk manager
 Le buone pratiche. Sicurezza in sala operatoria: esperienze regionali a confronto - REGIONE SICILIA - Tommaso Mannone Risk manager Regione Siciliana - Assessorato della Salute D.A. 3181 del 23 dicembre
Le buone pratiche. Sicurezza in sala operatoria: esperienze regionali a confronto - REGIONE SICILIA - Tommaso Mannone Risk manager Regione Siciliana - Assessorato della Salute D.A. 3181 del 23 dicembre
L uso in sicurezza dei chemioterapici antiblastici: premesse e normative. Fabrizio Meliga
 Corso di accreditamento e aggiornamento per operatori sanitari dedicati alla preparazione di farmaci antiblastici presso le varie U.F.A. Piemonte e Valle d Aosta 15-22 settembre 2015 L uso in sicurezza
Corso di accreditamento e aggiornamento per operatori sanitari dedicati alla preparazione di farmaci antiblastici presso le varie U.F.A. Piemonte e Valle d Aosta 15-22 settembre 2015 L uso in sicurezza
I SESSIONE: FOCUS SULLE MALATTIE RARE
 CORSO DI FORMAZIONE SUL CAMPO A CURA DELL OSSERVATORIO NAZIONALE SIFO Torino, 5 Giugno 2015 I SESSIONE: FOCUS SULLE MALATTIE RARE Erica Daina Coordinamento Malattie Rare Regione Lombardia Centro di Ricerche
CORSO DI FORMAZIONE SUL CAMPO A CURA DELL OSSERVATORIO NAZIONALE SIFO Torino, 5 Giugno 2015 I SESSIONE: FOCUS SULLE MALATTIE RARE Erica Daina Coordinamento Malattie Rare Regione Lombardia Centro di Ricerche
Rete Regionale per la Gestione Terapeutica delle Malattie Infiammatorie Croniche dell Intestino in Sicilia
 Rete Regionale per la Gestione Terapeutica delle Malattie Infiammatorie Croniche dell Intestino in Sicilia Dott.ssa Sara Renna A.O. Ospedali riuniti Villa Sofia-Cervello Palermo Le IBD hanno una incidenza
Rete Regionale per la Gestione Terapeutica delle Malattie Infiammatorie Croniche dell Intestino in Sicilia Dott.ssa Sara Renna A.O. Ospedali riuniti Villa Sofia-Cervello Palermo Le IBD hanno una incidenza
PROGETTO INTERAZIENDALE PER LA GESTIONE DELLA PATOLOGIA UROLOGICA NELL AREA DEL NORD SARDEGNA
 PROGETTO INTERAZIENDALE PER LA GESTIONE DELLA PATOLOGIA UROLOGICA NELL AREA DEL NORD SARDEGNA (AOU SASSARI & ASL OLBIA) Avvio fase Sperimentale A cura di: AOU SS ASL 2 OLBIA (BOZZA) Febbraio 2016 1 Premessa:
PROGETTO INTERAZIENDALE PER LA GESTIONE DELLA PATOLOGIA UROLOGICA NELL AREA DEL NORD SARDEGNA (AOU SASSARI & ASL OLBIA) Avvio fase Sperimentale A cura di: AOU SS ASL 2 OLBIA (BOZZA) Febbraio 2016 1 Premessa:
Casa della Salute di San Secondo
 Casa della Salute di San Secondo PROGETTO: GESTIONE INTEGRATA DEL PAZIENTE CON BPCO NELLA CASA DELLA SALUTE DI SAN SECONDO Obiettivo generale è la presa in carico delle persone assistite affette da BPCO
Casa della Salute di San Secondo PROGETTO: GESTIONE INTEGRATA DEL PAZIENTE CON BPCO NELLA CASA DELLA SALUTE DI SAN SECONDO Obiettivo generale è la presa in carico delle persone assistite affette da BPCO
Regolamento Commissione Terapeutica Aziendale dell Azienda Ospedaliero - Universitaria di Sassari
 Regolamento Commissione Terapeutica Aziendale dell Azienda Ospedaliero - Universitaria di Sassari INDICE Art. 1 Definizione Art. 2 Composizione, nomina e decadenza Art. 3 Deleghe Art. 4 Funzioni della
Regolamento Commissione Terapeutica Aziendale dell Azienda Ospedaliero - Universitaria di Sassari INDICE Art. 1 Definizione Art. 2 Composizione, nomina e decadenza Art. 3 Deleghe Art. 4 Funzioni della
La Gestione del Rischio Clinico all interno dei servizi sanitari delle carceri toscane
 30/05/3013 Dr. Alessandro Cerri Lab Gestione Rischio Clinico Regione Toscana La Gestione del Rischio Clinico all interno dei servizi sanitari delle carceri toscane «La Sanità Penitenziaria dopo la Riforma»
30/05/3013 Dr. Alessandro Cerri Lab Gestione Rischio Clinico Regione Toscana La Gestione del Rischio Clinico all interno dei servizi sanitari delle carceri toscane «La Sanità Penitenziaria dopo la Riforma»
ASL PROVINCIA DI VARESE UNA VISIONE DI SISTEMA SULL INTEGRAZIONE SOCIO- SANITARIA NELLA NOSTRA PROVINCIA. 29 giugno 2011
 ASL PROVINCIA DI VARESE 29 giugno 2011 UNA VISIONE DI SISTEMA SULL INTEGRAZIONE SOCIO- SANITARIA NELLA NOSTRA PROVINCIA 1 PRINCIPALI PROVVEDIMENTI LEGISLATIVI RELATIVI ALL INTEGRAZIONE SOCIO-SANITARIA
ASL PROVINCIA DI VARESE 29 giugno 2011 UNA VISIONE DI SISTEMA SULL INTEGRAZIONE SOCIO- SANITARIA NELLA NOSTRA PROVINCIA 1 PRINCIPALI PROVVEDIMENTI LEGISLATIVI RELATIVI ALL INTEGRAZIONE SOCIO-SANITARIA
Raccomandazione 7, 7, Marzo Marzo derivati da da errori errori in in terapia terapia farmacologica
 . Committenza della Direzione Aziendale/Zonale per la prevenzione della morte, coma o grave danno derivati da errori in terapia farmacologica A La Direzione Aziendale/Zonale, anche sulla base delle indicazioni
. Committenza della Direzione Aziendale/Zonale per la prevenzione della morte, coma o grave danno derivati da errori in terapia farmacologica A La Direzione Aziendale/Zonale, anche sulla base delle indicazioni
LA RACCOMANDAZIONE MINISTERIALE PER LA RICONCILIAZIONE DELLA TERAPIA FARMACOLOGICA
 LA RACCOMANDAZIONE MINISTERIALE PER LA RICONCILIAZIONE DELLA TERAPIA FARMACOLOGICA Susanna Ciampalini Direzione generale della Programmazione sanitaria Ministero della Salute Rosamaria Congedo Area S.I.F.O.
LA RACCOMANDAZIONE MINISTERIALE PER LA RICONCILIAZIONE DELLA TERAPIA FARMACOLOGICA Susanna Ciampalini Direzione generale della Programmazione sanitaria Ministero della Salute Rosamaria Congedo Area S.I.F.O.
Misurare per decidere
 STRUMENTI PER LA VALUTAZIONE DEI SERVIZI TERRITORIALI Azienda Ulss n. 3 Bassano del Grappa Michela Piccinini Servizio Controllo di Gestione e Controllo Interno IL SISTEMA DI PROGRAMMAZIONE E CONTROLLO
STRUMENTI PER LA VALUTAZIONE DEI SERVIZI TERRITORIALI Azienda Ulss n. 3 Bassano del Grappa Michela Piccinini Servizio Controllo di Gestione e Controllo Interno IL SISTEMA DI PROGRAMMAZIONE E CONTROLLO
GESTIONE FARMACI E MATERIALE SANITARIO
 Ogni struttura sanitaria complessa deve disporre di spazi/locali per la ricezione, l immagazzinamento e la distribuzione dei farmaci, dei presidi medico-chirurgici e sanitari, del materiale di medicazione
Ogni struttura sanitaria complessa deve disporre di spazi/locali per la ricezione, l immagazzinamento e la distribuzione dei farmaci, dei presidi medico-chirurgici e sanitari, del materiale di medicazione
La responsabilità nelle attività ispettive e nelle Commissioni di appropriatezza prescrittiva
 La responsabilità nelle attività ispettive e nelle Commissioni di appropriatezza prescrittiva Direttore UOCC Area Assistenza Farmaceutica Convenzionata e Farmacovigilanza ASL Napoli 1 Scenario Efficacia
La responsabilità nelle attività ispettive e nelle Commissioni di appropriatezza prescrittiva Direttore UOCC Area Assistenza Farmaceutica Convenzionata e Farmacovigilanza ASL Napoli 1 Scenario Efficacia
Azienda USL Pescara IL FARMACISTA : UN RIFERIMENTO PER LA GOVERNANCE AZIENDALE
 Azienda USL Pescara IL FARMACISTA : UN RIFERIMENTO PER LA GOVERNANCE AZIENDALE Le scelte dell Asl di Pescara 2 - INTEGRAZIONE E TRASVERSALITA Agevolare forme di forte integrazione organizzativa tra: Stessa
Azienda USL Pescara IL FARMACISTA : UN RIFERIMENTO PER LA GOVERNANCE AZIENDALE Le scelte dell Asl di Pescara 2 - INTEGRAZIONE E TRASVERSALITA Agevolare forme di forte integrazione organizzativa tra: Stessa
AREA C: SISTEMI INTEGRATI
 AREA C: SISTEMI INTEGRATI Codice Titolo Ore C01 Formazione in merito al Sistema di Gestione per la Qualità UNI EN 28 ISO 9001 C02 Internal Auditing secondo la linea guida UNI EN ISO 19011:2012 28 C03 Formazione
AREA C: SISTEMI INTEGRATI Codice Titolo Ore C01 Formazione in merito al Sistema di Gestione per la Qualità UNI EN 28 ISO 9001 C02 Internal Auditing secondo la linea guida UNI EN ISO 19011:2012 28 C03 Formazione
CIRCOLARE 3: Flussi ASA e FED
 CIRCOLARE 3: Flussi ASA e FED 14 Luglio 2016 Francesca Francesconi e Sonia Gandolfi Delibera 463/2016: Linee di indirizzo per la conversione in regime ambulatoriale dei day hospital oncologici in Regione
CIRCOLARE 3: Flussi ASA e FED 14 Luglio 2016 Francesca Francesconi e Sonia Gandolfi Delibera 463/2016: Linee di indirizzo per la conversione in regime ambulatoriale dei day hospital oncologici in Regione
La qualità delle materie prime: implicazioni per il farmacista preparatore
 La qualità delle materie prime: implicazioni per il farmacista preparatore Prof. Paola Minghetti Presidente SIFAP Roma, 17.12.2004, Istituto Superiore di Sanità Cos è la SIFAP? La SIFAP è una associazione
La qualità delle materie prime: implicazioni per il farmacista preparatore Prof. Paola Minghetti Presidente SIFAP Roma, 17.12.2004, Istituto Superiore di Sanità Cos è la SIFAP? La SIFAP è una associazione
Corso per Progettisti dei Sistemi di Gestione per la Qualità UNI EN ISO 9001:2008 PROGRAMMA DEL CORSO 32 ORE
 Corso per Progettisti dei Sistemi di Gestione per la Qualità UNI EN ISO 9001:2008 PROGRAMMA DEL CORSO 32 ORE Responsabile del progetto formativo: Dott. Ing. Antonio Razionale Tutor: Dott. Ing. Massimo
Corso per Progettisti dei Sistemi di Gestione per la Qualità UNI EN ISO 9001:2008 PROGRAMMA DEL CORSO 32 ORE Responsabile del progetto formativo: Dott. Ing. Antonio Razionale Tutor: Dott. Ing. Massimo
Relatore: Dott.ssa Piera Sau Napoli 19-21 Maggio 2016 XIV Congresso Nazionale CARD ITALIA
 Procedura di dimissione ed ammissione protetta e continuità delle cure a domicilio. Asl n.2 di Olbia Relatore: Dott.ssa Piera Sau Napoli 19-21 Maggio 2016 XIV Congresso Nazionale CARD ITALIA La dimissione
Procedura di dimissione ed ammissione protetta e continuità delle cure a domicilio. Asl n.2 di Olbia Relatore: Dott.ssa Piera Sau Napoli 19-21 Maggio 2016 XIV Congresso Nazionale CARD ITALIA La dimissione
Scheda per la stesura dei piani attuativi aziendali ASL RMB Piano Regionale di Prevenzione e Proroga 2013
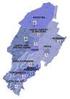 Scheda per la stesura dei piani attuativi aziendali ASL RMB Piano Regionale di Prevenzione 2010-12 e Proroga 2013 LINEA DI ATTIVITA E TITOLO DEL PROGETTO: 20-3.5.1 Prevenzione della progressione dell artrite
Scheda per la stesura dei piani attuativi aziendali ASL RMB Piano Regionale di Prevenzione 2010-12 e Proroga 2013 LINEA DI ATTIVITA E TITOLO DEL PROGETTO: 20-3.5.1 Prevenzione della progressione dell artrite
LA CONTINUITÀ ASSISTENZIALE: IL MODELLO PAI
 LA CONTINUITÀ ASSISTENZIALE: IL MODELLO PAI GIAMPIETRO GASPARINI U O C Oncologia Medica A.C.O. San Filippo Neri Roma RETE SANITARIA IN ONCOLOGIA:OBIETTIVI Presa in carico del paziente in modo globale Riconoscimento
LA CONTINUITÀ ASSISTENZIALE: IL MODELLO PAI GIAMPIETRO GASPARINI U O C Oncologia Medica A.C.O. San Filippo Neri Roma RETE SANITARIA IN ONCOLOGIA:OBIETTIVI Presa in carico del paziente in modo globale Riconoscimento
Ospedale Civile San Bortolo Vicenza. Unità operativa di Medicina Interna
 Ospedale Civile San Bortolo Vicenza Unità operativa di Medicina Interna Cartella Integrata medico - infermieristica La documentazione integrata Medico - Infermieristica: Strumento per migliorare la qualità
Ospedale Civile San Bortolo Vicenza Unità operativa di Medicina Interna Cartella Integrata medico - infermieristica La documentazione integrata Medico - Infermieristica: Strumento per migliorare la qualità
AVVISO PUBBLICO DIREZIONE DELLA STRUTTURA COMPLESSA OSPEDALIERA DI DIREZIONE OSPEDALIERA DELL ASSL DI ORISTANO
 Allegato A alla Deliberazione n.675_ del 02/08/2017 AVVISO PUBBLICO DIREZIONE DELLA STRUTTURA COMPLESSA OSPEDALIERA DI DIREZIONE OSPEDALIERA DELL ASSL DI ORISTANO DEFINIZIONE DEL FABBISOGNO/PROFILO OGGETTIVO
Allegato A alla Deliberazione n.675_ del 02/08/2017 AVVISO PUBBLICO DIREZIONE DELLA STRUTTURA COMPLESSA OSPEDALIERA DI DIREZIONE OSPEDALIERA DELL ASSL DI ORISTANO DEFINIZIONE DEL FABBISOGNO/PROFILO OGGETTIVO
I REQUISITI INNOVATIVI DELLA ISO Alessandra Peverini Perugia 23 ottobre 2015
 I REQUISITI INNOVATIVI DELLA ISO 9001 Alessandra Peverini Perugia 23 ottobre 2015 Le principali novità 1. Le relazioni fra l Organizzazione ed il contesto interno ed esterno 2. Le aspettative delle parti
I REQUISITI INNOVATIVI DELLA ISO 9001 Alessandra Peverini Perugia 23 ottobre 2015 Le principali novità 1. Le relazioni fra l Organizzazione ed il contesto interno ed esterno 2. Le aspettative delle parti
SCELTA ED ASSEGNAZIONE DEI DISPOSITIVI DI PROTEZIONE INDIVIDUALI
 Proc. Pagina 1 di 7 Rev. Data Motivazione della Redazione Verifica Approvazio revisione ne 0 24/10/2012 RSPP Proc. Pagina 2 di 7 INDICE 1 SCOPO...3 2 CAMPO DI APPLICAZIONE...3 3 RIFERIMENTI...3 4 DEFINIZIONI...3
Proc. Pagina 1 di 7 Rev. Data Motivazione della Redazione Verifica Approvazio revisione ne 0 24/10/2012 RSPP Proc. Pagina 2 di 7 INDICE 1 SCOPO...3 2 CAMPO DI APPLICAZIONE...3 3 RIFERIMENTI...3 4 DEFINIZIONI...3
La Geriatria: punto di incontro tra territorio e ospedale nella gestione della fragilità e della complessità di cura
 La Geriatria: punto di incontro tra territorio e ospedale nella gestione della fragilità e della complessità di cura L Organizzazione dell Assistenza territoriale agli Anziani nei sistemi sanitari regionali
La Geriatria: punto di incontro tra territorio e ospedale nella gestione della fragilità e della complessità di cura L Organizzazione dell Assistenza territoriale agli Anziani nei sistemi sanitari regionali
I SISTEMI DI GESTIONE PER IL MIGLIORAMENTO DELLE CONDIZIONI DI SALUTE E SICUREZZA
 Ecomondo 2016 - Rimini, 10 novembre 2016 Angelica Schneider Graziosi INAIL Contarp Centrale I SISTEMI DI GESTIONE PER IL MIGLIORAMENTO DELLE CONDIZIONI DI SALUTE E SICUREZZA Perché parlare di SGSL per
Ecomondo 2016 - Rimini, 10 novembre 2016 Angelica Schneider Graziosi INAIL Contarp Centrale I SISTEMI DI GESTIONE PER IL MIGLIORAMENTO DELLE CONDIZIONI DI SALUTE E SICUREZZA Perché parlare di SGSL per
Manuale Qualità. INCPLAST Group srl
 INCPLAST Group srl Ha iniziato tutti i processi per uniformandoci alle procedure di certificazione di gestione qualità secondo la norma ISO 9001 : 2008 per l ambito delle attività di stampa a caldo ( impressione
INCPLAST Group srl Ha iniziato tutti i processi per uniformandoci alle procedure di certificazione di gestione qualità secondo la norma ISO 9001 : 2008 per l ambito delle attività di stampa a caldo ( impressione
Allegato A Prescrizione, impiego ed erogazione di farmaci off-label
 Allegato A Prescrizione, impiego ed erogazione di farmaci off-label PREMESSA L'autorizzazione all'immissione in commercio (AIC) per un medicinale viene rilasciata, dagli enti regolatori preposti, a seguito
Allegato A Prescrizione, impiego ed erogazione di farmaci off-label PREMESSA L'autorizzazione all'immissione in commercio (AIC) per un medicinale viene rilasciata, dagli enti regolatori preposti, a seguito
Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate)
 Istruzione Operativa Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate) I_ PGS-DSA-7-01_04 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
Istruzione Operativa Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate) I_ PGS-DSA-7-01_04 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
Presentazione del Protocollo di intesa per la valorizzazione dei farmacisti e delle farmacie territoriali nell educazione terapeutica
 DIREZIONE GENERALE SERVIZIO ATTIVITA SPERIMENTALI E MALATTIE RARE U.O. Comunicazione viale Duca degli Abruzzi, 15 25124 Brescia Tel. 030/3838315 Fax 030/3838280 E-mail: [email protected] CONFERENZA
DIREZIONE GENERALE SERVIZIO ATTIVITA SPERIMENTALI E MALATTIE RARE U.O. Comunicazione viale Duca degli Abruzzi, 15 25124 Brescia Tel. 030/3838315 Fax 030/3838280 E-mail: [email protected] CONFERENZA
USL 7, Azienda Ospedaliera Senese Dipartimento Interaziendale di Programmazione Sanitaria Sistema integrato provinciale della diagnostica per immagini
 FORUMPA SANITA' 2001 Parte 1: Anagrafica USL 7, Azienda Ospedaliera Senese Dipartimento Interaziendale di Programmazione Sanitaria Sistema integrato provinciale della diagnostica per immagini Titolo del
FORUMPA SANITA' 2001 Parte 1: Anagrafica USL 7, Azienda Ospedaliera Senese Dipartimento Interaziendale di Programmazione Sanitaria Sistema integrato provinciale della diagnostica per immagini Titolo del
Valutazio ne dei rischi
 Valutazio ne dei rischi Il procedimento di valutazione dei rischi deve essere calato, in modo permanente, all interno della struttura di produzione, a livello individuale e di sistema, come uno strumento
Valutazio ne dei rischi Il procedimento di valutazione dei rischi deve essere calato, in modo permanente, all interno della struttura di produzione, a livello individuale e di sistema, come uno strumento
Tempi di attesa: DGR 272 del 15/02/2017
 Tempi di attesa: DGR 272 del 15/02/2017 Indice Stato dell arte Road map CAPITOLO 1 Stato dell arte GANTT 1 Nomina del RUA 2 Completamento del sistema unico informatizzato centralizzato 2 Monitoraggio volumi
Tempi di attesa: DGR 272 del 15/02/2017 Indice Stato dell arte Road map CAPITOLO 1 Stato dell arte GANTT 1 Nomina del RUA 2 Completamento del sistema unico informatizzato centralizzato 2 Monitoraggio volumi
Le Cure Palliative erogate in Rete
 Le Cure Palliative erogate in Rete La normativa nazionale e regionale Codigoro - 29 settembre 2012 Mauro Manfredini Focus sulla Rete No Terapia del dolore No Cure Palliative Pediatriche LEGGE n. 39 26
Le Cure Palliative erogate in Rete La normativa nazionale e regionale Codigoro - 29 settembre 2012 Mauro Manfredini Focus sulla Rete No Terapia del dolore No Cure Palliative Pediatriche LEGGE n. 39 26
