Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
|
|
|
- Agnello Motta
- 5 anni fa
- Visualizzazioni
Transcript
1 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu, disperato pilota, frangi ora fra gli scogli la mia barca già stanca e squassata per tante tempeste! A te accanto, mio amore! Oh schietto farmacista! Efficace è la tua droga. Con questo bacio io muoio. W. Shakespeare. Giulietta e Romeo, Atto 5, Scena 3. Ultima revisione: 11 novembre 2013 Lezione novembre 2013
2 Precipitazione e Acidità Precipitazione dei solfuri Poiché molti elementi formano solfuri poco solubili, in analisi si profitta di ciò per precipitarli mediante ioni S 2 (o anche HS ). GliioniS 2 necessari per la precipitazione sono forniti dal solfuro di idrogeno, H 2 S, che in soluzione acquosa è un acido molto debole, dissociandosi secondo l equazione complessiva: H 2 S 2H + +S 2 (KH 2 S ) Da questa relazione di equilibrio risulta che, diminuendo la concentrazione degli ioni H +, l equilibrio si sposta verso destra e quindi aumenta la concentrazione degli ioni S 2. 2/42
3 Precipitazione e Acidità Precipitazione dei solfuri In altri termini, quanto meno acida è la soluzione, tanto maggiore è la concentrazione degli ioni S 2. Il ph di precipitazione dei vari solfuri si può calcolare conoscendo la costante di dissociazione di H 2 S ed il prodotto di solubilità dei solfuri. Per un generico solfuro MeS il prodotto di solubilità è dato dalla relazione: Ps = [Me 2+ ][S 2 ] 3/42
4 Precipitazione e Acidità Precipitazione dei solfuri da cui si deduce: [S 2 ]= Ps [Me 2+ ] Dalla costante dell acido risulta che: [H + ] 2 [S 2 ] KH 2 S = = [H 2 S] 4/42
5 Precipitazione e Acidità Precipitazione dei solfuri Poiché una soluzione acquosa satura di H 2 S, a temperatura ambiente, ha una concentrazione ~0,1 M, si può scrivere: [H + ] 2 [S 2 ] = ( )(0,1) = [H + ] 2 = [S 2 ] sostituendo in questa espressione il valore di [S 2 ] ricavato sopra: [H + ] 2 = [Me 2+ ] [Ps] 5/42
6 Precipitazione e Acidità Precipitazione dei solfuri 6/42
7 Precipitazione e Acidità Precipitazione dei solfuri 7/42
8 Precipitazione e Acidità Precipitazione dei solfuri Aggiustando il ph della soluzione in maniera opportuna, cioè regolando la concentrazione degli ioni S 2, si può fare in modo di precipitare solo i solfuri meno solubili. In questo modo, i solfuri vengono separati dai cationi che formano solfuri più solubili e che quindi restano in soluzione. Ad esempio, a ph = 0,5 possono precipitare solo i solfuri di arsenico, antimonio, stagno, mercurio, rame, piombo, bismuto e cadmio, che hanno Ps < /42
9 Precipitazione e Acidità Precipitazione dei solfuri A ph = 0,5, infatti, lo zinco, il cobalto, il nichel ed il manganese restano in soluzione e vengono precipitati solo a ph più elevato. Bisogna, tuttavia, tenere presente che, dato il margine di sicurezza non molto largo, e data la possibilità di fenomeni di co-precipitazione e post-precipitazione, talvolta nella pratica analitica, si può avere la precipitazione del solfuro di zinco. 9/42
10 Precipitazione e Acidità Precipitazione dei solfuri: effetti sul ph Come una variazione del ph può portare alla formazione di precipitati, così la formazione di un precipitato può portare a variazioni del ph. Si consideri una soluzione di HCN 1N; essendo pk A =9,siha che ph = 4,5. Per aggiunta di nitrato di argento precipita il cianuro di argento, praticamente insolubile, secondo l equazione: HCN + Ag + AgCN + H + 10/42
11 Precipitazione e Acidità Precipitazione dei solfuri: effetti sul ph Se si aggiunge 1 equivalente di ioni Ag + si può dire che si forma una concentrazione di [H + ] = 1, e cioè il ph della soluzione diminuisce da 4,5 a 0. La variazione di ph è particolarmente importante nel caso della precipitazione analitica del solfuri. Infatti, durante la reazione di precipitazione l acido debole scompare mentre si forma l acido forte HCl. Ad esempio: CdCl 2 + H 2 S CdS + 2HCl 11/42
12 Precipitazione e Acidità Precipitazione dei solfuri: effetti sul ph Ciò porta ad un sensibile aumento dell acidità e quindi ad una variazione significativa del ph. Tale fenomeno può rendere incompleta la precipitazione di alcuni solfuri, specialmente quella del solfuro di cadmio. Di qui deriva la regola di controllare il ph della soluzione non solo prima della precipitazione con H 2 S, ma anche dopo. Se il ph risulta diminuito, conviene ripristinarlo diluendo la soluzione e trattare ancora con H 2 S per completare la precipitazione. 12/42
13 Precipitazione e Acidità Precipitazione dei solfuri: Zn, Co, Ni, Mn 13/42
14 Precipitazione e Acidità Precipitazione dei solfuri: Zn, Co, Ni, Mn A ph = 2,5, cioè in una soluzione tamponata con acido cloroacetico/cloroacetato sodico precipita solo il solfuro di zinco. A ph = 5, cioè in una soluzione tamponata con acido acetico/acetato sodico precipitano i solfuri di zinco, cobalto e nichel, mentre il manganese rimane in soluzione. A ph = 9, cioè in una soluzione tamponata con ammonio idrossido/ammonio cloruro, precipitano tutti assieme i solfuri di zinco, cobalto, nichel e manganese. 14/42
15 Precipitazione e Acidità Precipitazione dei solfuri: Zn, Co, Ni, Mn Quindi, aggiustando il ph della soluzione con opportuni successivi tamponamenti, si può precipitare in un primo tempo esclusivamente lo zinco. Successivamente si precipitano insieme il cobalto e il nichel e, infine, si precipita il manganese. In pratica, tale separazione si esegue solo in casi particolari; in genere si preferisce precipitare i quattro solfuri insieme a ph 9e successivamente si ricercano i singoli elementi. 15/42
16 Precipitazione e Acidità Precipitazione dei solfuri: ridissoluzione La dissoluzione dei solfuri negli acidi avviene generalmente in condizioni molto diverse da quelle di precipitazione. Infatti, nella precipitazione si opera in eccesso di H 2 S, mentre nella ridissoluzione, la concentrazione del catione è dello stesso ordine di quella dello ione S 2. Pertanto, i calcoli sul ph di ridissoluzione dei solfuri richiedono tante approssimazioni, che i risultati non sempre concordano con i valori sperimentali. 16/42
17 Precipitazione e Acidità Precipitazione dei solfuri: ridissoluzione Bisogna aggiungere che i solfuri subiscono in generale il fenomeno dell invecchiamento, per cui essi si ridisciolgono ad un ph talvolta notevolmente inferiore a quello di precipitazione o a quello che si potrebbe calcolare. Particolarmente notevole è l invecchiamento del solfuro di nichel e del solfuro di cobalto, i quali precipitano a ph 5, ma una volta precipitati non si ridisciolgono facilmente nemmeno in HCl concentrato. 17/42
18 Precipitazione e Acidità Precipitazione dei solfuri: ridissoluzione Le curve di ridissoluzione di CoS e NiS seguono un andamento molto diverso da quelle di precipitazione. Nel procedimento analitico si profitta di ciò per separare i solfuri di cobalto e di nichel dai solfuri di zinco e di manganese, i quali si ridisciolgono facilmente in acido cloridrico concentrato. Per ridisciogliere i solfuri di cobalto e nichel si ricorre all acido nitrico, che ossida gli ioni S 2 in modo da spostare l equilibrio di dissociazione verso destra fino alla completa dissoluzione del solfuro stesso (es., NiS Ni 2+ +S 2 ). 18/42
19 Ossidanti e riducenti Ossidazioni sono tutte le reazioni che avvengono con perdita di elettroni. Ad esempio, la reazione tra zinco e cloro, che dà cloruro di zinco secondo l equazione: Zn + Cl 2 ZnCl 2 è una reazione di ossidazione in quanto lo zinco, passando da Zn azn 2+ perde 2 elettroni: Zn Zn e 19/42
20 Ossidanti e riducenti Analogamente, riduzioni sono tutte le reazioni che avvengono con guadagno di elettroni. Ad esempio: Fe 3+ + e Fe 2+ Una sostanza per ossidarsi, cioè per cedere elettroni, richiede un reagente, detto ossidante, che acquisti quegli stessi elettroni, cioè che subisca una riduzione. 20/42
21 Ossidanti e riducenti Pertanto, ogni reazione di ossidazione avviene contemporaneamente ad una reazione di riduzione; la reazione complessiva si chiama reazione di ossido-riduzione. Gli elettroni assorbiti dall ossidante sono in numero eguale a quelli del riducente. Ciò appare chiaro se si scrive ogni reazione di ossido-riduzione separando le 2 equazioni parziali. Ad esempio, la reazione tra cloruro di stagno(ii) e cloro si può schematizzare come segue: 21/42
22 Ossidanti e riducenti Sn 2+ Sn e Cl 2 + 2e 2 Cl Sn 2+ + Cl 2 Sn Cl Dall esempio si evince che una perdita di elettroni equivale ad un aumento del numero di ossidazione e, analogamente, un acquisto di elettroni equivale ad una diminuzione del numero di ossidazione. 22/42
23 Ossidanti e riducenti In generale chiamando Ox la forma ossidata e Red la forma ridotta, si ha: Ox + ne riduzione ossidazione Red La forma ossidata e la forma ridotta che intervengono in ciascuno di tali equilibri costituiscono una coppia di ossidoriduzione o sistema redox. Le varie coppie redox si indicano scrivendo prima la forma ossidata e poi quella ridotta: Cl 2 /2Cl,Fe 3+ /Fe 2+, ecc. 23/42
24 Ossidanti e riducenti Se la forma ossidata di una coppia ha molta tendenza a prendere elettroni, si dice che è un ossidante forte. In tal caso, l equilibrio è molto spostato verso la forma ridotta, che risulta quindi la forma più stabile (es., Cl 2 2Cl ). Viceversa, se la forma ossidata ha poca tendenza a prendere elettroni, si tratta di un ossidante debole. In tal caso, l equilibrio è spostato verso la forma ossidata e la forma ridotta è poco stabile (es., I 2 2I ). 24/42
25 Ossidanti e riducenti Se la forma ridotta è molto poco stabile, cioè se ha molta tendenza ad ossidarsi, allora si parla di forte riducente. Ad esempio, la coppia Na + /Na è costituita da una forma ossidata molto stabile (Na + ) e da una forma ridotta facilmente ossidabile (Na); quindi il sodio è un forte riducente. 25/42
26 Serie dei potenziali normali Poiché l ossidazione consiste in un trasferimento di elettroni, il potere ossidante o riducente viene espresso con una grandezza fisica, nota come potenziale redox (E) espresso in volt (V). Il potenziale che ha una coppia quando la concentrazione della forma ossidata, [Ox], è uguale alla concentrazione della forma ridotta [Red], si chiama potenziale normale (E 0 ). Per le sostanze gassose la pressione deve essere pari a 1 atm; le sostanze poco solubili devono essere presenti come corpo di fondo. 26/42
27 Serie dei potenziali normali 27/42
28 Serie dei potenziali normali 28/42
29 Serie dei potenziali normali In chimica analitica, le reazioni di ossido-riduzione hanno una grande importanza. Inoltre, molte reazioni di ossido-riduzione avvengono con cambiamenti di colore caratteristici. Ad esempio, il manganese(ii) che è di colore rosa può ossidarsi a 2 ione MnO 4, che è verde, o anche a ione MnO 4, che è di colore 2 violetto; lo ione CrO 4 che è giallo, può essere ridotto a ione Cr 3+, che è di colore verde, ecc. 29/42
30 Variazione del potenziale con la concentrazione Il potenziale di ossido-riduzione varia con la concentrazione degli ioni secondo la relazione di Nernst: 0,06 E = E 0 + log n [Ox] [Red] dove n è il numero degli elettroni scambiati, E 0 normale di ossido-riduzione. il potenziale Dalla formula di Nernst si vede che anche variando notevolmente il rapporto [Ox]/[Red] il potenziale non varia molto. 30/42
31 Variazione del potenziale con la concentrazione 31/42
32 Tamponamento redox Le soluzioni che contengono contemporaneamente un ossidante ed il riducente coniugato permettono di fissare praticamente il potenziale di ossidoriduzione ad un valore determinato. Esiste del resto una evidente analogia fra la formula di Nernst 0,06 E = E 0 + log [Ox] n [Red] e la formula delle soluzioni tampone: ph = pk A + log Cs C A 32/42
33 Tamponamento redox Ad esempio, il bismuto(iii) reagisce con lo ioduro di potassio, formando un complesso arancione, secondo la reazione: Bi I BiI 4 Quando si ricerca il bismuto con questa reazione, tutti gli ossidanti degli ioduri interferiscono perché liberano iodio. Per evitare queste interferenze si esegue la reazione in ambiente riducente, cioè per esempio, in presenza di un eccesso di ipofosfito (E 0 H 3 PO 3 /H 3 PO 2 = 0,6 V). 33/42
34 Reazioni di ossidoriduzione Se il potenziale di un sistema 1) è superiore a quello di un sistema 2), si può costruire una pila in cui l ossidante 1) ossida il riducente 2). Ad esempio, per le coppie Ce 4+ /Ce 3+ efe 3+ /Fe 2+ i potenziali sono: [Ce 4+ ] ECe 4+ /Ce 3+ = 1,30 + 0,06 (1) [Ce 3+ ] [Fe 3+ ] EFe 3+ /Fe 2+ = 1,30 + 0,06 (2) [Fe 2+ ] 34/42
35 Reazioni di ossidoriduzione Si può quindi allestire una pila costituita da un recipiente (cella) diviso in 2 scomparti da un setto poroso, il quale permette il passaggio dell elettricità ma impedisce che le 2 soluzioni si possano mescolarsi. Nelle 2 soluzioni sono immersi 2 conduttori (elettrodi) di un metallo inerte (platino), collegati tra loro da un apparecchio di misura. Tale pila si indica: (Pt)/Fe 3+ /Fe 2+ / / Ce 4+ /Ce 3+ /(Pt) 35/42
36 Reazioni di ossidoriduzione In essa avviene la reazione: Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ cioè si ha l ossidazione del ferro (II) a ferro (III). Tale reazione procede sino a quando si ha: ECe 4+ /Ce 3+ = EFe 3+ /Fe 2+ 36/42
37 Reazioni di ossidoriduzione 37/42
38 Reazioni di miscele redox Quando una miscela di ossidanti viene trattata con un riducente, è l ossidante più forte quello che viene ridotto per primo. Analogamente, quando una miscela di più riducenti viene trattata con un ossidante, è il riducente più forte quello che viene ossidato per primo. In altri termini, la reazione che avviene per prima è quella che corrisponde alla più grande differenza di potenziale. 38/42
39 Reazioni di miscele redox 39/42
40 Reazioni di miscele redox Si considerino le coppie redox degli alogeni: Cl 2 /2Cl E 0 =1,36V Br 2 /2Br E 0 =1V I 2 /2I E 0 =0,5V Se una soluzione contenente ioduri e bromuri viene trattata lentamente con acqua di cloro, si ossida prima lo ioduro, che è il riducente più forte; poi si ossida il bromuro. 40/42
41 Reazioni di miscele redox Inizialmente lo ioduro si ossida a iodio secondo la reazione: 2I + Cl 2 I 2 + 2Cl In un secondo tempo lo iodio si ossida formando ICl 3 ehio 3 : I 2 + 3Cl 2 2ICl 3 ICl 3 + Cl 2 + 3H 2 O HIO 3 + 5HCl Continuando ad aggiungere acqua di cloro, il bromuro si ossida a bromo: 2Br + Cl 2 Br 2 + 2Cl 41/42
42 Reazioni di miscele redox Infine, se si aggiunge acqua di cloro in eccesso, si forma il composto BrCl. Se la reazione viene eseguita in presenza di un solvente organico (benzene, cloroformio), questo assume prima un colore violetto dovuto allo iodio formatosi, poi un colore giallastro dovuto al bromo. 42/42
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
1 Me Me (s) Me + (aq) + e -
 ELETTROCHIMICA 1 Me Me (s) Me + (aq) + e - Me + DOPPIO STRATO (+) (-) all interfaccia elettrodo-soluzione 2 Se inizialmente prevale la reazione 1, la lamina metallica si carica negativamente (eccesso di
ELETTROCHIMICA 1 Me Me (s) Me + (aq) + e - Me + DOPPIO STRATO (+) (-) all interfaccia elettrodo-soluzione 2 Se inizialmente prevale la reazione 1, la lamina metallica si carica negativamente (eccesso di
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
BaSO. BaSO 4 è una costante quindi: K ps = prodotto di solubilità
 Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Reazioni di ossido-riduzione (redox) - Come stabilire il verso di una redox? -
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche.
 Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
RNH 3 + OH - C 0 x x x
 Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2009/2010. Soluzioni prima
Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2009/2010. Soluzioni prima
Agente ossidante è la specie chimica che acquistando elettroni passa ad uno stato di ossidazione inferiore: Es. Ce +4 + e - Ce +3
 OSSIDIMETRIA Titolazioni di ossidoriduzione. Principi: Ossidazione = perdita di elettroni Riduzione = acquisto di elettroni Reazione redox in generale Oss 1 + Rid 2 Rid 1 + Oss 2 Agente ossidante è la
OSSIDIMETRIA Titolazioni di ossidoriduzione. Principi: Ossidazione = perdita di elettroni Riduzione = acquisto di elettroni Reazione redox in generale Oss 1 + Rid 2 Rid 1 + Oss 2 Agente ossidante è la
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2014/2015
 Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Reazioni di ossido-riduzione (redox) - Come stabilire il verso di una redox? -
 Reazioni di ossido-riduzione (redox) Reazioni in cui i reagenti si scambiano elettroni per formare i prodotti. Cu 2+ (aq) + Zn(s) Cu(s) + Zn 2+ (aq) Zn(s) Zn 2+ (aq) + 2 e - Cu 2+ (aq) + 2 e - Cu(s) ossidazione
Reazioni di ossido-riduzione (redox) Reazioni in cui i reagenti si scambiano elettroni per formare i prodotti. Cu 2+ (aq) + Zn(s) Cu(s) + Zn 2+ (aq) Zn(s) Zn 2+ (aq) + 2 e - Cu 2+ (aq) + 2 e - Cu(s) ossidazione
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Capitolo 22 L elettrochimica
 Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
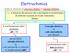 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
SOLUZIONE DEL COMPITO A DI CHIMICA DEL
 SOLUZIONE DEL COMPITO A DI CHIMICA DEL 05-07-13 1A) 33.5 g di ioduro di sodio e 33.0 g di iodio vengono sciolti in acqua trattati con 17.9 L (a c.n.) di cloro; si formano iodato di sodio, acido iodico
SOLUZIONE DEL COMPITO A DI CHIMICA DEL 05-07-13 1A) 33.5 g di ioduro di sodio e 33.0 g di iodio vengono sciolti in acqua trattati con 17.9 L (a c.n.) di cloro; si formano iodato di sodio, acido iodico
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Sommario della lezione 24. Equilibri di solubilità. Chimica Organica. Elettrochimica
 Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2015/2016
 Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
Solubilità dei sali Prodotto di solubilità
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
ELETTROCHIMICA 16/12/2015
 ELETTROCHIMICA Tratta delle trasformazioni tra energia chimica ed energia elettrica Alla base ci sono reazioni di ossidoriduzione, cioè con scambio di elettroni tra reagenti e prodotti della reazione Fe
ELETTROCHIMICA Tratta delle trasformazioni tra energia chimica ed energia elettrica Alla base ci sono reazioni di ossidoriduzione, cioè con scambio di elettroni tra reagenti e prodotti della reazione Fe
Bilanciamento delle reazioni chimiche
 Bilanciamento delle reazioni chimiche Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento
Bilanciamento delle reazioni chimiche Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento
II Gruppo: CH 3 - C + H 2 O CH 3 - C + H 2 S CH 3 - C + NH 4 OH TAA
 II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ESERCIZI Tabella dei potenziali
 ESERCIZI 1) Una pila chimica è un dispositivo in cui si ha trasformazione di: a. energia elettrica in energia chimica b. energia chimica in energia elettrica c. entalpia in energia elettrica d. entropia
ESERCIZI 1) Una pila chimica è un dispositivo in cui si ha trasformazione di: a. energia elettrica in energia chimica b. energia chimica in energia elettrica c. entalpia in energia elettrica d. entropia
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
Appunti di Stechiometria per Chimica. Elettrochimica
 Appunti di Stechiometria per Chimica Elettrochimica Celle Elettrochimiche Le reazioni d ossidoriduzione possono essere sfruttate per formare delle celle galvaniche o pile che trasformano l energia chimica
Appunti di Stechiometria per Chimica Elettrochimica Celle Elettrochimiche Le reazioni d ossidoriduzione possono essere sfruttate per formare delle celle galvaniche o pile che trasformano l energia chimica
Le celle elettrolitiche
 Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente.
 Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2017/2018
 Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente.
 Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
ELETTROCHIMICA. Consideriamo la reazione che si ha quando si aggiunge dello zinco ad una soluzione acquosa di acido cloridrico:
 ELETTROCHIMICA Alcune fra le più importanti reazioni chimiche di ossidoriduzione prevedono una modifica dei numeri di ossidazione dei vari elementi che compongono reagenti e prodotti. Consideriamo la reazione
ELETTROCHIMICA Alcune fra le più importanti reazioni chimiche di ossidoriduzione prevedono una modifica dei numeri di ossidazione dei vari elementi che compongono reagenti e prodotti. Consideriamo la reazione
red 1 + ox 2 ox 1 + red 2
 Reazioni Redox Ossidanti e Riducenti Ossidante: molecola o ione capace di strappare elettroni ad un riducente Riducente: molecola o ione capace di fornire elettroni ad un ossidante Reazione redox: trasferimento
Reazioni Redox Ossidanti e Riducenti Ossidante: molecola o ione capace di strappare elettroni ad un riducente Riducente: molecola o ione capace di fornire elettroni ad un ossidante Reazione redox: trasferimento
ELETTROCHIMICA. Zn(s) + Cu +2 Zn +2 + Cu. Ossidazione: perdita di elettroni Riduzione: acquisto di elettroni. +2e
 ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
Ossido Riduzione. Disproporzione: Processo di ossido-riduzione in cui la stessa sostanza si ossida e si riduce
 Ossido Riduzione 1. Il numero di ossidazione degli atomi in un qualsiasi elemento libero non combinato è zero. 2. Il numero di ossidazione di un elemento in uno ione monoatomico è uguale alla carica dello
Ossido Riduzione 1. Il numero di ossidazione degli atomi in un qualsiasi elemento libero non combinato è zero. 2. Il numero di ossidazione di un elemento in uno ione monoatomico è uguale alla carica dello
ESERCIZI POTENZIOMETRIA
 ESERCIZI POTENZIOMETRIA A. SPUNTI DI RIFLESSIONE 1. Quali sono i probabili fenomeni che permettono a un elettrodo al platino di assumere il potenziale di una soluzione contenente la coppia Fe 3+ /Fe 2+?
ESERCIZI POTENZIOMETRIA A. SPUNTI DI RIFLESSIONE 1. Quali sono i probabili fenomeni che permettono a un elettrodo al platino di assumere il potenziale di una soluzione contenente la coppia Fe 3+ /Fe 2+?
Dissoluzione dei Solidi
 Dissoluzione dei Solidi La capacità di un solvente di sciogliere un certo soluto non è illimitata Un solido si scioglie tanto più in un solvente quanto più gli è affine chimicamente; questo significa che
Dissoluzione dei Solidi La capacità di un solvente di sciogliere un certo soluto non è illimitata Un solido si scioglie tanto più in un solvente quanto più gli è affine chimicamente; questo significa che
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI. Dr. Francesco Musiani
 REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
Elettrochimica. Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s)
 2018 Elettrochimica 1 Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
2018 Elettrochimica 1 Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
3. Le Reazioni Chimiche
 . Le Reazioni Chimiche Equazioni Chimiche e Reazioni Chimiche il simbolismo delle reazioni chimiche il bilanciamento delle equazioni chimiche Reazioni di Precipitazione le soluzioni acquose le reazioni
. Le Reazioni Chimiche Equazioni Chimiche e Reazioni Chimiche il simbolismo delle reazioni chimiche il bilanciamento delle equazioni chimiche Reazioni di Precipitazione le soluzioni acquose le reazioni
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA. Prof. Antonino Mamo
 Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA Prof. Antonino Mamo 1) Scrivere le formule di struttura dei seguenti sali: a) permanganato di
Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA Prof. Antonino Mamo 1) Scrivere le formule di struttura dei seguenti sali: a) permanganato di
REAZIONI DI OSSIDORIDUZIONE. Rivista: «Didattica delle Scienze» 5/1991
 REAZIONI DI OSSIDORIDUZIONE G. Giacomo Guilizzoni Rivista: «Didattica delle Scienze» 5/1991 L Autore illustra un metodo che può essere impiegato con buoni risultati per introdurre gli allievi delle scuole
REAZIONI DI OSSIDORIDUZIONE G. Giacomo Guilizzoni Rivista: «Didattica delle Scienze» 5/1991 L Autore illustra un metodo che può essere impiegato con buoni risultati per introdurre gli allievi delle scuole
Esempi di calcolo del numero di ossidazione
 ESERCITAZIONE 3 1 Esempi di calcolo del numero di ossidazione 1) Calcolare il numero di ossidazione del Mn nel KMnO 4. K n.o. +1 O n.o. 2 La molecola è neutra per cui: n.o. Mn + n.o. K + 4 n.o. O = 0 Mn
ESERCITAZIONE 3 1 Esempi di calcolo del numero di ossidazione 1) Calcolare il numero di ossidazione del Mn nel KMnO 4. K n.o. +1 O n.o. 2 La molecola è neutra per cui: n.o. Mn + n.o. K + 4 n.o. O = 0 Mn
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
Studio delle trasformazioni dell energia chimica e dell energia elettrica
 ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
Il riducente si ossida cedendo elettroni all agente ossidante
 L ossidante si riduce acquistando elettroni dall agente riducente Il riducente si ossida cedendo elettroni all agente ossidante La conduzione dell elettricità Quando una sostanza è sottoposta ad una differenza
L ossidante si riduce acquistando elettroni dall agente riducente Il riducente si ossida cedendo elettroni all agente ossidante La conduzione dell elettricità Quando una sostanza è sottoposta ad una differenza
ELETTROCHIMICA. Elettricità per fare avvenire reazioni chimiche (processi elettrolitici)
 ELETTROCHIMICA Reazioni chimiche per produrre elettricità Elettricità per fare avvenire reazioni chimiche (processi elettrolitici) Esperimento: Nel tempo la sbarretta di Zn si consuma e si deposita Cu
ELETTROCHIMICA Reazioni chimiche per produrre elettricità Elettricità per fare avvenire reazioni chimiche (processi elettrolitici) Esperimento: Nel tempo la sbarretta di Zn si consuma e si deposita Cu
2- (aq) + Zn (s) Zn 2+ (aq) + SO 4. Semi-reazione di ossidazione: in cui una specie chimica perde elettroni
 Reazioni con trasferimento di elettroni Modifica della struttura elettronica attraverso uno scambio di elettroni: Una ossidazione può avvenire soltanto se avviene contemporaneamente una riduzione (reazioni
Reazioni con trasferimento di elettroni Modifica della struttura elettronica attraverso uno scambio di elettroni: Una ossidazione può avvenire soltanto se avviene contemporaneamente una riduzione (reazioni
Titolazioni Redox. Analisi volumetrica basata su una reazione di ossido-riduzione. La somma delle due coppie coniugate ossido-riduttive
 Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
Elettrochimica (parte I)
 Elettrochimica (parte I) Reazioni redox Le reazioni di ossidazione e di riduzione sono anche dette reazioni di ossidoriduzione e reazioni redox. In queste reazioni avviene uno scambio di elettroni tra
Elettrochimica (parte I) Reazioni redox Le reazioni di ossidazione e di riduzione sono anche dette reazioni di ossidoriduzione e reazioni redox. In queste reazioni avviene uno scambio di elettroni tra
LE PILE. La scala delle reattività redox. La scala delle reattività redox. La scala delle reattività redox. dall energia chimica a quella elettrica
 La scala delle reattività redox LE PILE dall energia chimica a quella elettrica E' possibile sapere a priori quale sarà il decorso di una reazione redox? La reazione Cu + Zn Cu + Zn avviene spontaneamente?...
La scala delle reattività redox LE PILE dall energia chimica a quella elettrica E' possibile sapere a priori quale sarà il decorso di una reazione redox? La reazione Cu + Zn Cu + Zn avviene spontaneamente?...
Acidi e basi di Lewis
 Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
+ MnO 4 + 8H + 5Fe 3+ + Mn H 2 O
 Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2008/2009. Prova scritta,
Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2008/2009. Prova scritta,
Gli equilibri di solubilità
 Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Elettrochimica. Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s)
 217 1 Elettrochimica Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
217 1 Elettrochimica Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA
 ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA L elettrolisi è una reazione non spontanea ( G>0) di ossidoriduzione provocata dal passaggio di corrente tra due elettrodi immersi in
ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA L elettrolisi è una reazione non spontanea ( G>0) di ossidoriduzione provocata dal passaggio di corrente tra due elettrodi immersi in
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2013/2014
 Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina I.
Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina I.
Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C. dove : R = costante dei gas T = 298,15 K F = Faraday
 A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 8: Elettrochimica: legge di Nernst e leggi di Faraday(4 h) Cella galvanica:
A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 8: Elettrochimica: legge di Nernst e leggi di Faraday(4 h) Cella galvanica:
Studenti L-P(2017/18) L-O(2018/19) (Prof.Giuliano Moretti) Risultati della prova scritta del 15 febbraio 2019
 Studenti LP(2017/18) LO(2018/19) (Prof.Giuliano Moretti) Risultati della prova scritta del 15 febbraio 2019 La prova orale si svolgerà secondo il calendario riportato di seguito Presentarsi presso la stanza
Studenti LP(2017/18) LO(2018/19) (Prof.Giuliano Moretti) Risultati della prova scritta del 15 febbraio 2019 La prova orale si svolgerà secondo il calendario riportato di seguito Presentarsi presso la stanza
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento elettronico
Reazioni di ossido-riduzione Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento elettronico
ESERCIZI DI RIEPILOGO GENERALE
 ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
LE REAZIONI DI OSSIDORIDUZIONE
 LE REAZIONI DI OSSIDORIDUZIONE Immergiamo una lamina di zinco metallico in una soluzione di solfato rameico : si osserva immediatamente la formazione di una sostanza solida che nel tempo diventa di color
LE REAZIONI DI OSSIDORIDUZIONE Immergiamo una lamina di zinco metallico in una soluzione di solfato rameico : si osserva immediatamente la formazione di una sostanza solida che nel tempo diventa di color
Una reazione chimica rappresenta un processo di trasformaczioni in cui si rompono e si formano legami chimici. γc + δd
 Una reazione chimica rappresenta un processo di trasformaczioni in cui si rompono e si formano legami chimici αa + βb γc + δd - A e B: reagenti - C e D: prodotti - α,β,γ e δ: coefficienti stechiometrici
Una reazione chimica rappresenta un processo di trasformaczioni in cui si rompono e si formano legami chimici αa + βb γc + δd - A e B: reagenti - C e D: prodotti - α,β,γ e δ: coefficienti stechiometrici
Processi ossido-riduttivi chimici ed elettrochimici
 Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
Soluzioni. B è spontanea nel senso opposto alla freccia. 12 Soluzione di HF in un contenitore di rame: C La soluzione rimane inalterata.
 Soluzioni capitolo 23 VERIFICA LE TUE CONOSCENZE LA PILA O CELLA GALVANICA 1 Una cella galvanica trasforma energia chimica in energia elettrica, utilizzando una redox spontanea. Una cella galvanica è formata
Soluzioni capitolo 23 VERIFICA LE TUE CONOSCENZE LA PILA O CELLA GALVANICA 1 Una cella galvanica trasforma energia chimica in energia elettrica, utilizzando una redox spontanea. Una cella galvanica è formata
Chimica A.A. 2017/2018
 Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 9 Calcolare la solubilità molare del solfato di bario in una soluzione 0.020 M di solfato di sodio. Il prodotto di solubilità del solfato di
Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 9 Calcolare la solubilità molare del solfato di bario in una soluzione 0.020 M di solfato di sodio. Il prodotto di solubilità del solfato di
INDICAZIONI DI LAVORO PER GLI STUDENTI CON GIUDIZIO DI SOSPENSIONE
 INDICAZIONI DI LAVORO PER GLI STUDENTI CON GIUDIZIO DI SOSPENSIONE Classi quarte SA: SCIENZE Anno scolastico 2015 2016 ANATOMIA E FISIOLOGIA: Gli esercizi dovranno essere svolti: o sul libro qualora riguardino
INDICAZIONI DI LAVORO PER GLI STUDENTI CON GIUDIZIO DI SOSPENSIONE Classi quarte SA: SCIENZE Anno scolastico 2015 2016 ANATOMIA E FISIOLOGIA: Gli esercizi dovranno essere svolti: o sul libro qualora riguardino
Elettrochimica. Studia la trasformazione dell energia chimica in energia elettrica e viceversa.
 lettrochimica Studia la trasformazione dell energia chimica in energia elettrica e viceversa. Ricordiamo che la corrente elettrica si origina grazie al movimento di cariche, elettroni, in un materiale
lettrochimica Studia la trasformazione dell energia chimica in energia elettrica e viceversa. Ricordiamo che la corrente elettrica si origina grazie al movimento di cariche, elettroni, in un materiale
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Solubilità dei sali Prodotto di solubilità
 Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
DETERMINAZIONE della COMPOSIZIONE di un MISCUGLIO METALLICO. OBIETTIVO: determinare la composizione di un miscuglio Cu-Zn ed esprimerla in % (m/m)
 DETERMINAZIONE della COMPOSIZIONE di un MISCUGLIO METALLICO OBIETTIVO: determinare la composizione di un miscuglio Cu-Zn ed esprimerla in % (m/m) Approccio al problema: 1) Zn (s) + Cl (aq) (g) + Zn ++
DETERMINAZIONE della COMPOSIZIONE di un MISCUGLIO METALLICO OBIETTIVO: determinare la composizione di un miscuglio Cu-Zn ed esprimerla in % (m/m) Approccio al problema: 1) Zn (s) + Cl (aq) (g) + Zn ++
COME CALCOLARE I NUMERI DI OSSIDAZIONE
 COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
15 aprile 2010 Prova scritta di Chimica Analitica 1 con Laboratorio
 15 aprile 2010 Prova scritta di Chimica Analitica 1 con Laboratorio 1. La concentrazione di ioni cloruro in una soluzione viene determinata con il metodo di olhard. Un aliquota di 25.0 ml della soluzione
15 aprile 2010 Prova scritta di Chimica Analitica 1 con Laboratorio 1. La concentrazione di ioni cloruro in una soluzione viene determinata con il metodo di olhard. Un aliquota di 25.0 ml della soluzione
III verifica 2005/06 (A) Colonna.. Riga...
 Sono riportate le soluzioni commentate del compito A. Per gli altri compiti sono riportate (a volte in maniera succinta) le soluzioni dei quesiti, 2,4,6,8,9. Per gli altri quesiti, potete ricavare il procedimento
Sono riportate le soluzioni commentate del compito A. Per gli altri compiti sono riportate (a volte in maniera succinta) le soluzioni dei quesiti, 2,4,6,8,9. Per gli altri quesiti, potete ricavare il procedimento
DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015
 A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015 COGNOME NOME MATRICOLA Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015 COGNOME NOME MATRICOLA Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A
 POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Seconda Prova in Itinere del 28 Gennaio 2008
 Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Sede di Ceccano Insegnamento di Chimica Generale e Laboratorio (A.A. 200708) Seconda Prova
Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Sede di Ceccano Insegnamento di Chimica Generale e Laboratorio (A.A. 200708) Seconda Prova
Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z. Testo A
 Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z Testo A 1) Una soluzione è ottenuta miscelando 15,00 ml di una soluzione di HCl (MM36,46) 0,360 M, 10,00 ml di una soluzione
Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z Testo A 1) Una soluzione è ottenuta miscelando 15,00 ml di una soluzione di HCl (MM36,46) 0,360 M, 10,00 ml di una soluzione
