La sorveglianza del mercato: modalità e strumenti
|
|
|
- Giorgiana Lupi
- 5 anni fa
- Visualizzazioni
Transcript
1 La sorveglianza del mercato: modalità e strumenti Ministero della salute Direttore ufficio 3 Direzione generale dei dispositivi medici e del servizio farmaceutico
2 Sorveglianza del mercato (44) Un aspetto fondamentale è la creazione di una banca dati centrale che integri diversi sistemi elettronici [...] al fine di raccogliere ed elaborare le informazioni riguardanti i dispositivi medici presenti sul mercato e gli operatori economici, taluni aspetti della valutazione della conformità, gli organismi notificati, i certificati, le indagini cliniche, la vigilanza e la sorveglianza del mercato. Gli obiettivi della banca dati sono migliorare la trasparenza generale, razionalizzare e facilitare il flusso di informazioni tra operatori economici, organismi notificati o sponsor e Stati membri, come pure tra gli stessi Stati membri e tra Stati membri e Commissione, evitare la moltiplicazione degli obblighi di informazione e rafforzare il coordinamento tra Stati membri. Nel mercato interno questi obiettivi possono essere realizzati in maniera efficace solo al livello dell'unione e la Commissione dovrebbe pertanto continuare a sviluppare e gestire la banca dati europea dei dispositivi medici (Eudamed), istituita dalla decisione 2010/227/UE della Commissione, del 19 aprile 2010, relativa alla banca dati europea dei dispositivi medici.
3 Sorveglianza del mercato (74) I fabbricanti dovrebbero svolgere un ruolo attivo nella fase successiva alla commercializzazione raccogliendo in modo sistematico e attivo informazioni relative ad esperienze maturate dopo l'immissione sul mercato dei loro dispositivi, allo scopo di aggiornare la relativa documentazione tecnica e di cooperare con le autorità nazionali competenti incaricate delle attività di vigilanza e sorveglianza del mercato. (80) Nel presente regolamento dovrebbero essere inserite regole sulla sorveglianza del mercato allo scopo di rafforzare i diritti e gli obblighi delle autorità nazionali competenti, garantire un coordinamento efficace delle loro attività di sorveglianza del mercato e precisare le procedure applicabili.
4 Sorveglianza del mercato (definizioni) 60) "sorveglianza post-commercializzazione": tutte le attività svolte dai fabbricanti in collaborazione con altri operatori economici volte a istituire e tenere aggiornata una procedura sistematica per raccogliere e analizzare in modo proattivo l'esperienza acquisita dai loro dispositivi immessi sul mercato, messi a disposizione o messi in servizio, al fine di identificare eventuali necessità di procedere immediatamente ad eventuali azioni correttive o preventive; 61) "sorveglianza del mercato": le attività svolte e i provvedimenti adottati dalle autorità pubbliche per verificare e garantire che i [...] dispositivi siano conformi ai requisiti stabiliti nella pertinente normativa di armonizzazione dell'unione e non pregiudichino la salute, la sicurezza o qualsiasi altro aspetto della protezione del pubblico interesse;
5 Capitolo VII Sezione 3 Attività di sorveglianza del mercato Art. 93 Attività di sorveglianza del mercato Art. 94 Art. 95 Art. 96 Art. 97 Valutazione di Dispositivi sospetti di presentare rischi inaccettabili o altre non conformità Procedure riguardante i dispositivi che presentano un rischio inaccettabile per la salute e sicurezza Procedura di valutazione delle misure nazionali a livello dell'unione Altre non conformità
6 Capitolo VII Sezione 3 Sorveglianza del mercato Art. 98 Art. 99 Art. 100 Misure preventive di protezione della salute Buone pratiche amministrative Sistema elettronico per la sorveglianza del mercato
7 Base legale normativa nazionale: art. 17 D. lgs. 46/1997 (MD) art. 8 D. lgs. 507/1992 (AIMD) Notifiche ex art. 13 D. lgs. 46/1997 (verifiche random banca dati dispositivi medici) Richieste certificati di libera vendita (Free Sale Certificate) Valutazioni contenuti tecnici messaggi pubblicitari Attività successive alle ispezioni ai fabbricanti (informative agli Organismi Notificati) Richieste dall Ufficio responsabile per la vigilanza Controllo all importazione da paesi terzi da parte degli Uffici di sanità marittima e aerea del Ministero (verifiche della notifica, della marcatura e dell etichettatura) Verifiche attività certificativa Organismi Notificati
8 Sorveglianza REattiva: Reports (DM singolo o multiplo) provenienti da: Altre Autorità Competenti (COEN Enquiry Gruppi europei) Organismi notificati Autorità giudiziaria, Carabinieri NAS Utilizzatori (società, operatori sanitari, pazienti/utenti)
9 Monitoraggio e verifica della conformità Compliance monitoring /enforcement activities 1/2 Gestione delle Banche dati Fabbricanti di dispositivi medici su misura Partecipazione alle attività comunitarie (CAMD, MDEG, COEN, NBOG, B&C, IMDRF coordination) Monitoraggio e verifica della conformità Compliance monitoring/ enforcement activities Notifiche di dispositivi medici Scambio di informazioni tra Autorità attraverso Enquiry e COEN form (uso appropriato degli strumenti e tempistica delle risposte) Questioni relative a Borderline & Classification
10 Monitoraggio e verifica della conformità Compliance monitoring /enforcement activities 2/2 Rapporti con altre Amministrazioni ed enti locali Certificati di libera vendita (attestazioni di conformità) Attività successiva alle ispezioni agli operatori economici e agli audit agli Organismi notificati Monitoraggio e verifica della conformità Compliance monitoring/ enforcement activities Pareri sui contenuti dei messaggi pubblicitari di dispositivi medici Quesiti dal pubblico, dagli operatori economici, dagli operatori sanitari,.. Aggiornamento del sito web
11 Azioni di sorveglianza
12 Azioni Sorveglianza ITALIA 2016 Azioni Sorveglianza EUROPA 2016
13 Sorveglianza UE
14 Focus sorveglianza UE coen to Italy
15 Organismi Notificati - Designazione, Sorveglianza e Rinnovo Cod. ON Denominazione ON Italcert S.r.l Certiquality S.r.l IMQ S.p.A Icim S.p.A Bureau Veritas Italia S.p.A Istituto di Ricerca e Collaudi M. Masini S.r.l Eurofins Product Testing Italy S.r.l Istituto Superiore Sanità Kiwa Cermet Italia S.p.A Tüv Rheinland Italia S.r.l. Tre nuove richieste di designazione Designazione e Rinnovo, a partire dal 2013 (Regolamento 920/2013) sono svolte insieme al Joint Assessment team. Le visite di sorveglianza sono previste ogni anno per gli Organismi con più di 100 clienti e ogni 18 mesi per gli Organismi con meno di 100 clienti e non prevedono il coinvolgimento della Commissione Europea e degli Stati Membri.
16 Organismi Notificati - Designazione e rinnovo Per ogni audit l Autorità Designante incarica almeno tre ispettori con competenze diverse (medici, ingegneri, farmacisti) Il Joint Assessment Team è composto da due ispettori della Commissione Europea (DG SANTE) e di due esperti nazionali degli Stati Membri. Anno JA Le due valutazioni sono svolte in maniera congiunta ma vengono preparati due diversi report. In caso di opinioni divergenti, queste vengono registrate nei report.
17 Stato dei lavori Domanda Joint Assessment Follow-up CIRCA BC
18 Attività 2016 Attività Ispettori DA Giorni Giorni Uomo Joint Assessment (5) Sorveglianza (5) Follow-up (3)
19 Sorveglianza certificazioni OONN italiani comunicazioni ai fabbricanti
20
21 Rilascio attestazioni di conformità (CLV = FSC)
22 Strumenti a supporto della sorveglianza Banca dati / Repertorio dei dispositivi medici IL SISTEMA INTEGRATO DEI DISPOSITIVI MEDICI Sorveglianza del mercato Indagini cliniche Pre-market Fabbricanti Dispositivi medici Certificati Market Vigilanza sugli incidenti Monitoraggio spesa SSN Consumi DM Contratti DM Apparecchiature Sanitarie Post-market
23 Banca Dati e Repertorio dei Dispositivi Medici Dispositivi di classe e Assemblati registrati Dispositivi di classe IVD TOTALE Assemblati Sistema BD/RDM 12/12/
24 Banca Dati e Repertorio dei Dispositivi Medici Focus Dispositivi di classe distribuzione dei DM per classi di rischio Classe Ilb 23% Classe III 11% Impiantabili attivi 1% Classe I non sterile e senza funzioni di misura 30% Classe I con funzioni di misura 0,5% Classe Ila 31% Classe I sterile con funzioni di misura 0,04% Classe I sterile 4% Sistema BD/RDM 12/12/
25 Dispositivi Medici registrati nella Nuova Banca Dati (Distribuzione per categoria CND) Sistema BD/RDM 12/12/
26 Distribuzione mondiale delle aziende fabbricanti rispetto alla Nazione della sede legale (riferita a soggetti giuridici - situazione al )
27 UE+EFTA - Distribuzione delle aziende fabbricanti rispetto alla Nazione della sede legale (riferita a soggetti giuridici - situazione al )
28 Banca Dati e Repertorio dei Dispositivi Medici Fotografia delle Aziende italiane presenti nel Sistema BD/RDM Fabbricanti/Assemblatori italiani di cui Fabbricanti DM di classe I (75%) Mandatari italiani 681 di cui Mandatari DM di classe I 386 (57%) Sistema BD/RDM 12/12/
29 Fabbricanti italiani di dispositivi medici su misura registrati nella specifica Banca dati Situazione al
30 Situazione al
31 Alessandra, Antonella, Dina, Danilo, Daniela, Edoardo, Elisabetta, Ennio, Franco, Gabriella, Giuseppe, Ivo, Lorella, Marco, Maria Grazia, Riccardo, Roberto, Roberta, Rossella. Direttore ufficio III Dispositivi Medici Tel GRAZIE PER L ATTENZIONE!
32 Dott.ssa
16 maggio 2014 Aula Gialla Torino Esposizioni
 UNIVERSITA DEGLI STUDI DI TORINO «Dispositivi medici: dalla siringa alle nuove frontiere diagnostico-terapeutiche. Prospettive di un settore in grande sviluppo» Il ruolo del Ministero della Salute, autorità
UNIVERSITA DEGLI STUDI DI TORINO «Dispositivi medici: dalla siringa alle nuove frontiere diagnostico-terapeutiche. Prospettive di un settore in grande sviluppo» Il ruolo del Ministero della Salute, autorità
NUOVO REGOLAMENTO UE SUI DISPOSITIVI MEDICI
 NUOVO REGOLAMENTO UE SUI DISPOSITIVI MEDICI Come prepararsi alla deadline 2020 Ramada Plaza Milano, Via Stamira d Ancona 27, Milano VIGILANZA E SORVEGLIANZA POST-COMMERCIALIZZAZIONE NEL NUOVO REGOLAMENTO
NUOVO REGOLAMENTO UE SUI DISPOSITIVI MEDICI Come prepararsi alla deadline 2020 Ramada Plaza Milano, Via Stamira d Ancona 27, Milano VIGILANZA E SORVEGLIANZA POST-COMMERCIALIZZAZIONE NEL NUOVO REGOLAMENTO
III CONGRESSO CONGIUNTO DI ORTOPEDIA TECNICA
 Il razionale del nuovo Regolamento III CONGRESSO CONGIUNTO DI ORTOPEDIA TECNICA Gian Luca Salerio, Dir. Area Normazione Internazionale UNI Sandro Storelli, Coordinatore Innovazione e ricerca CNA Padova
Il razionale del nuovo Regolamento III CONGRESSO CONGIUNTO DI ORTOPEDIA TECNICA Gian Luca Salerio, Dir. Area Normazione Internazionale UNI Sandro Storelli, Coordinatore Innovazione e ricerca CNA Padova
L'esperienza italiana all interno dell Unione Europea
 Regione Emilia-Romagna Direzione Generale Sanità e Politiche sociali SEMINARIO REGIONALE L'EVOLUZIONE DEL SISTEMA DISPOSITIVI MEDICI 25 giugno 2015 SALA 20 maggio 2012 Viale della Fiera 8 Bologna L'esperienza
Regione Emilia-Romagna Direzione Generale Sanità e Politiche sociali SEMINARIO REGIONALE L'EVOLUZIONE DEL SISTEMA DISPOSITIVI MEDICI 25 giugno 2015 SALA 20 maggio 2012 Viale della Fiera 8 Bologna L'esperienza
Ing. Giulia Abis PhD Student Università degli Studi di Sassari
 POTENZIALITÀ DEI FLUSSI REGIONALI AUTOMATIZZATI PER IL MONITORAGGIO DELL ASSISTENZA E LA GENERAZIONE DI EVIDENZE SCIENTIFICHE: UN MODELLO INNOVATIVO PER L APPROVVIGIONAMENTO DEI DISPOSITIVI MEDICI Ing.
POTENZIALITÀ DEI FLUSSI REGIONALI AUTOMATIZZATI PER IL MONITORAGGIO DELL ASSISTENZA E LA GENERAZIONE DI EVIDENZE SCIENTIFICHE: UN MODELLO INNOVATIVO PER L APPROVVIGIONAMENTO DEI DISPOSITIVI MEDICI Ing.
Opportunità offerte dall introduzione del Repertorio nel settore dei dispositivi medico-diagnostici in vitro
 Opportunità offerte dall introduzione del Repertorio nel settore dei dispositivi medico-diagnostici in vitro Pietro Calamea Direzione Generale dei Dispositivi Medici, del Servizio Farmaceutico e della
Opportunità offerte dall introduzione del Repertorio nel settore dei dispositivi medico-diagnostici in vitro Pietro Calamea Direzione Generale dei Dispositivi Medici, del Servizio Farmaceutico e della
Piani di lavoro in attesa della futura regolamentazione
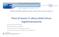 Evoluzione del quadro regolatorio: passato, presente, futuro del nuovo approccio Piani di lavoro in attesa della futura regolamentazione Dott.ssa Annamaria Donato Direttore Ufficio III ex DGFDM Direzione
Evoluzione del quadro regolatorio: passato, presente, futuro del nuovo approccio Piani di lavoro in attesa della futura regolamentazione Dott.ssa Annamaria Donato Direttore Ufficio III ex DGFDM Direzione
Vigilanza e Sorveglianza post-commercializzazione nel nuovo Regolamento
 Vigilanza e Sorveglianza post-commercializzazione nel nuovo Regolamento Rosaria Boldrini Direttore Ufficio V, Attività ispettiva e vigilanza Ministero della Salute D.G. Dispositivi medici e servizio farmaceutico
Vigilanza e Sorveglianza post-commercializzazione nel nuovo Regolamento Rosaria Boldrini Direttore Ufficio V, Attività ispettiva e vigilanza Ministero della Salute D.G. Dispositivi medici e servizio farmaceutico
Vigilanza e sorveglianza post-commercializzazione nel nuovo Regolamento (UE)
 Vigilanza e sorveglianza post-commercializzazione nel nuovo Regolamento (UE) Rosaria Boldrini Ministero della Salute D.G. Dispositivi medici e servizio farmaceutico Post-market surveillance e vigilanza
Vigilanza e sorveglianza post-commercializzazione nel nuovo Regolamento (UE) Rosaria Boldrini Ministero della Salute D.G. Dispositivi medici e servizio farmaceutico Post-market surveillance e vigilanza
Alessandro BERTI Vice Presidente ADM ARHEA Associazione nazionale delle imprese del settore ausili per disabilità motorie
 PRESTAZIONI DEGLI AUSILI ERGONOMIA E SICUREZZA Introduzione : ausili e nuovo regolamento MDR 745/2017 Alessandro BERTI Vice Presidente ADM ARHEA Associazione nazionale delle imprese del settore ausili
PRESTAZIONI DEGLI AUSILI ERGONOMIA E SICUREZZA Introduzione : ausili e nuovo regolamento MDR 745/2017 Alessandro BERTI Vice Presidente ADM ARHEA Associazione nazionale delle imprese del settore ausili
Dispositivi medici e nuovo Regolamento Europeo
 Società di Scienze Farmacologiche Applicate Society for Applied Pharmacological Sciences Seminario GdL Dispositivi Medici 15 Luglio 2013 Milano Dispositivi medici e nuovo Regolamento Europeo Principali
Società di Scienze Farmacologiche Applicate Society for Applied Pharmacological Sciences Seminario GdL Dispositivi Medici 15 Luglio 2013 Milano Dispositivi medici e nuovo Regolamento Europeo Principali
Presentazione del D. M. 23 dicembre 2013 Iscrizione dei dispositivi medico-diagnostici in vitro nel Repertorio dei dispositivi medici
 Presentazione del D. M. 23 dicembre 2013 Iscrizione dei dispositivi medico-diagnostici in vitro nel Repertorio dei dispositivi medici Direzione Generale del Sistema Informativo e Statistico Sanitario Direzione
Presentazione del D. M. 23 dicembre 2013 Iscrizione dei dispositivi medico-diagnostici in vitro nel Repertorio dei dispositivi medici Direzione Generale del Sistema Informativo e Statistico Sanitario Direzione
VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE
 VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE La vigilanza e la sorveglianza del mercato costituiscono una delle attività di fondamentale importanza per garantire prodotti sicuri e di alta qualità
VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE La vigilanza e la sorveglianza del mercato costituiscono una delle attività di fondamentale importanza per garantire prodotti sicuri e di alta qualità
Titolo PR.PART. ON/BED/D. Riferimento. Revisione e data entrata in vigore. Rev. 0 del 30/10/2017
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI PER DIRETTIVA N. 92/42/CEE (BED) concernente i requisiti di rendimento per le nuove caldaie ad acqua calda alimentate
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI PER DIRETTIVA N. 92/42/CEE (BED) concernente i requisiti di rendimento per le nuove caldaie ad acqua calda alimentate
Il Ministero della Salute e l applicazione del Regolamento 1223/2009
 "Il Regolamento (CE) n. 1223/2009 del Parlamento Europeo e del Consiglio del 30 novembre 2009 sui prodotti cosmetici" Roma, 6 giugno 2013 Il Ministero della Salute e l applicazione del Regolamento 1223/2009
"Il Regolamento (CE) n. 1223/2009 del Parlamento Europeo e del Consiglio del 30 novembre 2009 sui prodotti cosmetici" Roma, 6 giugno 2013 Il Ministero della Salute e l applicazione del Regolamento 1223/2009
Cosa cambia dal punto di vista dell industria
 Cosa cambia dal punto di vista dell industria Il nuovo regolamento Dispositivi Medici XVIII Convegno Nazionale AIIC -Genova, 8 Aprile 2017 1 Il testo finale dei regolamenti MD & IVD è stato votato! Il
Cosa cambia dal punto di vista dell industria Il nuovo regolamento Dispositivi Medici XVIII Convegno Nazionale AIIC -Genova, 8 Aprile 2017 1 Il testo finale dei regolamenti MD & IVD è stato votato! Il
Le attività del Forum dell agenzia e attività ispettive
 Le attività del Forum dell agenzia e attività ispettive Dott. Pietro Pistolese Min. del Lavoro, della Salute e delle politiche sociali DG prevenzione sanitaria Roma, 9/10 Giugno 2008 FORUM Articolo 76
Le attività del Forum dell agenzia e attività ispettive Dott. Pietro Pistolese Min. del Lavoro, della Salute e delle politiche sociali DG prevenzione sanitaria Roma, 9/10 Giugno 2008 FORUM Articolo 76
Il Rapporto sulla Spesa rilevata dalle strutture sanitarie pubbliche del SSN per l acquisto di dispositivi medici Anno 2015
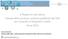 Il Rapporto sulla Spesa rilevata dalle strutture sanitarie pubbliche del SSN per l acquisto di dispositivi medici Anno 2015 Marcella Marletta Ministero della salute Direttore generale dei Dispositivi Medici
Il Rapporto sulla Spesa rilevata dalle strutture sanitarie pubbliche del SSN per l acquisto di dispositivi medici Anno 2015 Marcella Marletta Ministero della salute Direttore generale dei Dispositivi Medici
SCHEDA SINOTTICA DI CONSULTAZIONE DELLA NORMATIVA
 SCHEDA SINOTTICA DI CONSULTAZIONE DELLA NORMATIVA Normativa D. Legislativo n. 507 del 14/12/1992 Titolo Attuazione della direttiva 90/385/CEE concernente il ravvicinamento delle legislazioni degli Stati
SCHEDA SINOTTICA DI CONSULTAZIONE DELLA NORMATIVA Normativa D. Legislativo n. 507 del 14/12/1992 Titolo Attuazione della direttiva 90/385/CEE concernente il ravvicinamento delle legislazioni degli Stati
GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI
 GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI Linda Sanin UNIDI (Unione Nazionale Industrie Dentarie Italiane) EXPODENTAL MEETIING 17 Maggio 2018 DA DOVE NASCE L ESIGENZA
GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI Linda Sanin UNIDI (Unione Nazionale Industrie Dentarie Italiane) EXPODENTAL MEETIING 17 Maggio 2018 DA DOVE NASCE L ESIGENZA
L evoluzione della normativa nazionale e i risvolti applicativi
 SEMINARIO REGIONALE QUALE FUTURO PER IL SISTEMA DISPOSITIVI MEDICI L evoluzione della normativa nazionale e i risvolti applicativi Annamaria Donato Direttore ufficio III e Direttore Reggente Ufficio VI
SEMINARIO REGIONALE QUALE FUTURO PER IL SISTEMA DISPOSITIVI MEDICI L evoluzione della normativa nazionale e i risvolti applicativi Annamaria Donato Direttore ufficio III e Direttore Reggente Ufficio VI
Some views on the challenges for stakeholders on conformity assessment activities
 on Accreditation and Conformity Assessment Some views on the challenges for stakeholders on conformity assessment activities Rome, 28 June 2013 Mr Technologist INAIL INAIL L Istituto Nazionale per l'assicurazione
on Accreditation and Conformity Assessment Some views on the challenges for stakeholders on conformity assessment activities Rome, 28 June 2013 Mr Technologist INAIL INAIL L Istituto Nazionale per l'assicurazione
Vigilanza sui dispositivi medici
 Livorno 29 Aprile 2006 IL SISTEMA DI FARMACOVIGILANZA E IL PERCORSO DI SEGNALAZIONE DELL ADRs Vigilanza sui dispositivi medici DISPOSITIVI MEDICI Difetti di fabbricazione, Problemi occasionali, Errori
Livorno 29 Aprile 2006 IL SISTEMA DI FARMACOVIGILANZA E IL PERCORSO DI SEGNALAZIONE DELL ADRs Vigilanza sui dispositivi medici DISPOSITIVI MEDICI Difetti di fabbricazione, Problemi occasionali, Errori
PROCEDURA OPERATIVA PER LA SORVEGLIANZA
 26/01/2011 Pag. 1 di 6 PROCEDURA OPERATIVA PER LA SORVEGLIANZA POST- VENDITA 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Modulistica di riferimento... 3 4. RESPONSABILITÀ...
26/01/2011 Pag. 1 di 6 PROCEDURA OPERATIVA PER LA SORVEGLIANZA POST- VENDITA 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Modulistica di riferimento... 3 4. RESPONSABILITÀ...
Ministero del Lavoro, della Salute e delle Politiche Sociali
 Aspetti regolatori dei Dispositivi Medici applicati al Sistema Banca Dati e Repertorio Corso regionale di aggiornamento per la consultazione del Repertorio dei dispositivi medici Annamaria Donato Direzione
Aspetti regolatori dei Dispositivi Medici applicati al Sistema Banca Dati e Repertorio Corso regionale di aggiornamento per la consultazione del Repertorio dei dispositivi medici Annamaria Donato Direzione
Stato attuale della ricerca con dispositivi medici e scenari futuri
 Stato attuale della ricerca con dispositivi medici e scenari futuri Pietro Calamea Ministero della salute Direzione generale dei Dispositivi Medici e del Servizio Farmaceutico Ufficio 6 - Sperimentazione
Stato attuale della ricerca con dispositivi medici e scenari futuri Pietro Calamea Ministero della salute Direzione generale dei Dispositivi Medici e del Servizio Farmaceutico Ufficio 6 - Sperimentazione
Class. 3.5 Fasc. n. 917/2018
 PAT/RFSPGAS-13/07/2018-0412137 AGENZIA PROVINCIALE PER GLI APPALTI E CONTRATTI Servizio Procedure di Gara in Ambito Sanitario Via Dogana, 8 38122 Trento P +39 0461 496839 @ spgc-apss@pec.provincia.tn.it
PAT/RFSPGAS-13/07/2018-0412137 AGENZIA PROVINCIALE PER GLI APPALTI E CONTRATTI Servizio Procedure di Gara in Ambito Sanitario Via Dogana, 8 38122 Trento P +39 0461 496839 @ spgc-apss@pec.provincia.tn.it
Daniele Dondarini Segreteria ANTOI
 Daniele Dondarini Segreteria ANTOI 2017/745 5 APRILE 2017 Pubblicato sulla Gazzetta Ufficiale dell Unione Europea (L117/1) del 5 maggio 2017 REGOLAMENTO DISPOSITIVI MEDICI (UE) 2017/745 (MDR) 25 MAGGIO
Daniele Dondarini Segreteria ANTOI 2017/745 5 APRILE 2017 Pubblicato sulla Gazzetta Ufficiale dell Unione Europea (L117/1) del 5 maggio 2017 REGOLAMENTO DISPOSITIVI MEDICI (UE) 2017/745 (MDR) 25 MAGGIO
GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI
 GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI IDENTIFICAZIONE UNIVOCA DEI DISPOSITIVI MEDICI sistema UDI Cristina Bazzaro AIRMEDD KULZER srl EXPODENTAL MEETING 17 Maggio
GLI OPERATORI ECONOMICI NEL QUADRO DEI NUOVI REGOLAMENTI SUI DISPOSITIVI MEDICI IDENTIFICAZIONE UNIVOCA DEI DISPOSITIVI MEDICI sistema UDI Cristina Bazzaro AIRMEDD KULZER srl EXPODENTAL MEETING 17 Maggio
VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE
 VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE VIGILANZA E SORVEGLIANZA POST-COMMERCIALIZZAZIONE I nuovi obblighi degli operatori economici in ambito di vigilanza e sorveglianza post-commercializzazione
VIGILANZA E SORVEGLIANZA POST- COMMERCIALIZZAZIONE VIGILANZA E SORVEGLIANZA POST-COMMERCIALIZZAZIONE I nuovi obblighi degli operatori economici in ambito di vigilanza e sorveglianza post-commercializzazione
Garantire efficacia, sicurezza e innovazione per una crescita sostenibile
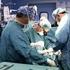 24 ottobre 2015 Sessione plenaria Sala Archimede DISPOSITIVI MEDICI: INNOVAZIONE, SOSTENIBILITÀ E SICUREZZA Garantire efficacia, sicurezza e innovazione per una crescita sostenibile Annamaria Donato -
24 ottobre 2015 Sessione plenaria Sala Archimede DISPOSITIVI MEDICI: INNOVAZIONE, SOSTENIBILITÀ E SICUREZZA Garantire efficacia, sicurezza e innovazione per una crescita sostenibile Annamaria Donato -
Ministero della Salute
 Ministero della Salute QUESTIONARIO INFORMATIVO Dati relativi alla ditta Data di compilazione Nome / Ragione sociale P. IVA / CF Indirizzo della sede legale C.A.P. Comune Provincia Prefisso Telefonico
Ministero della Salute QUESTIONARIO INFORMATIVO Dati relativi alla ditta Data di compilazione Nome / Ragione sociale P. IVA / CF Indirizzo della sede legale C.A.P. Comune Provincia Prefisso Telefonico
Regolamento UE 2016/679 in materia di protezione dei dati personali
 Regolamento UE 2016/679 in materia di protezione dei dati personali Entrata in vigore Pubblicazione nella Gazzetta Ufficiale dell Unione Europea n. 119/2016: 4 Maggio 2016. Entrata in vigore: 25 Maggio
Regolamento UE 2016/679 in materia di protezione dei dati personali Entrata in vigore Pubblicazione nella Gazzetta Ufficiale dell Unione Europea n. 119/2016: 4 Maggio 2016. Entrata in vigore: 25 Maggio
La sorveglianza sui dispositivi medici
 Corso Attività di Polizia Sanitaria ROMA, 21 giugno 2012 La sorveglianza sui dispositivi medici Dr. Franco Abbenda Ministero della Salute DGFDSC Ufficio 03 1 Origini regolatorie - Armamentario del medico
Corso Attività di Polizia Sanitaria ROMA, 21 giugno 2012 La sorveglianza sui dispositivi medici Dr. Franco Abbenda Ministero della Salute DGFDSC Ufficio 03 1 Origini regolatorie - Armamentario del medico
MANAGEMENT DEI CAMPIONI GRATUITI DI DISPOSITIVI MEDICI
 MANAGEMENT DEI CAMPIONI GRATUITI DI DISPOSITIVI MEDICI Tentativo di colmare un vuoto normativo Antonella Iudicello Azienda USL Modena DD - POLICLINICO 1 DISPOSITIVO MEDICO (DM) Definizione: qualsiasi strumento,
MANAGEMENT DEI CAMPIONI GRATUITI DI DISPOSITIVI MEDICI Tentativo di colmare un vuoto normativo Antonella Iudicello Azienda USL Modena DD - POLICLINICO 1 DISPOSITIVO MEDICO (DM) Definizione: qualsiasi strumento,
Nuovo Regolamento europeo sui dispositivi medici: aggiornamenti sulla discussione in corso al Consiglio UE
 SIMPOSIO AFI Le imprese farmaceutiche ed i settori collegati: quale futuro? DISPOSITIVI MEDICI BORDERLINE: ASPETTI DI QUALITÀ E SICUREZZA Nuovo Regolamento europeo sui dispositivi medici: aggiornamenti
SIMPOSIO AFI Le imprese farmaceutiche ed i settori collegati: quale futuro? DISPOSITIVI MEDICI BORDERLINE: ASPETTI DI QUALITÀ E SICUREZZA Nuovo Regolamento europeo sui dispositivi medici: aggiornamenti
LA GOVERNANCE DEL NUOVO SISTEMA E I TEMPI E LE FORME DELL IMPLEMENTAZIONE
 LA GOVERNANCE DEL NUOVO SISTEMA E I TEMPI E LE FORME DELL IMPLEMENTAZIONE Milano, 10 ottobre 2017 Salvatore Scalzo Health Technology and Cosmetics DG Internal Market, Industry, Entrepreneurship and SMEs
LA GOVERNANCE DEL NUOVO SISTEMA E I TEMPI E LE FORME DELL IMPLEMENTAZIONE Milano, 10 ottobre 2017 Salvatore Scalzo Health Technology and Cosmetics DG Internal Market, Industry, Entrepreneurship and SMEs
Cosa è cambiato per i fabbricanti di dispositivi medici in serie di Classe I. Alessandro BERTI
 Alessandro BERTI Vice Presidente ADM ARHEA Associazione nazionale delle imprese del settore ausili per disabilità motorie Il nuovo regolamento MDR 745/2017 rappresenta una grande sfida per tutto il comparto.
Alessandro BERTI Vice Presidente ADM ARHEA Associazione nazionale delle imprese del settore ausili per disabilità motorie Il nuovo regolamento MDR 745/2017 rappresenta una grande sfida per tutto il comparto.
Introduzione alla direttiva 2007/47/CE: le principali novità
 Introduzione alla direttiva 2007/47/CE: le principali novità Forum Sanità Futura Cernobbio, 18 marzo 2008 1 II Conferenza Nazionale La direttiva sui dispositivi 2007/47/CE medici dott. G. Ruocco Direttore
Introduzione alla direttiva 2007/47/CE: le principali novità Forum Sanità Futura Cernobbio, 18 marzo 2008 1 II Conferenza Nazionale La direttiva sui dispositivi 2007/47/CE medici dott. G. Ruocco Direttore
Fabbricanti di dispositivi medico -diagnostici in vitro
 Commissione europea Scheda informativa per Fabbricanti di dispositivi medico -diagnostici in vitro La presente scheda informativa si rivolge ai fabbricanti di dispositivi medico-diagnostici in vitro. Per
Commissione europea Scheda informativa per Fabbricanti di dispositivi medico -diagnostici in vitro La presente scheda informativa si rivolge ai fabbricanti di dispositivi medico-diagnostici in vitro. Per
Gare centralizzate e corretta classificazione dei dispositivi medici
 Gare centralizzate e corretta classificazione dei dispositivi medici Marcella Marletta Ministero della salute Direttore Generale dei Dispositivi Medici e del Servizio Farmaceutico I presupposti normativi
Gare centralizzate e corretta classificazione dei dispositivi medici Marcella Marletta Ministero della salute Direttore Generale dei Dispositivi Medici e del Servizio Farmaceutico I presupposti normativi
PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/34/UE
 Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/34/UE Apparecchi e sistemi di protezione per atmosfera potenzialmente esplosiva Allegato VI - MODULO C1 Conformità al Tipo basata sul controllo interno
Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/34/UE Apparecchi e sistemi di protezione per atmosfera potenzialmente esplosiva Allegato VI - MODULO C1 Conformità al Tipo basata sul controllo interno
La vigilanza sui dispositivi medici in Italia: il ruolo dell Autorità competente
 Dott.ssa Annamaria Donato Ministero della Salute Direzione Generale dei farmaci e dispositivi medici Direttore Ufficio V La vigilanza sui dispositivi medici in Italia: il ruolo dell Autorità competente
Dott.ssa Annamaria Donato Ministero della Salute Direzione Generale dei farmaci e dispositivi medici Direttore Ufficio V La vigilanza sui dispositivi medici in Italia: il ruolo dell Autorità competente
PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED)
 Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO B Esame UE del tipo tipo di produzione Riferimento Revisione e data entrata in vigore Approvato da PR PART ON/PED/B_PDZ
Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO B Esame UE del tipo tipo di produzione Riferimento Revisione e data entrata in vigore Approvato da PR PART ON/PED/B_PDZ
Le nuove disposizioni in materia didevicevigilance
 Le nuove disposizioni in materia didevicevigilance Marco Colombati Pharmacovigilance Department Bayer SSFA 09 Novembre 2017 GdL Dispositivi Medici Background Soluzione: Nuovi Regolamenti!! Medical Device
Le nuove disposizioni in materia didevicevigilance Marco Colombati Pharmacovigilance Department Bayer SSFA 09 Novembre 2017 GdL Dispositivi Medici Background Soluzione: Nuovi Regolamenti!! Medical Device
Articolazioni organizzative che si occupano di sicurezza alimentare auditate:
 SCHEDA AUDIT N : 05/2011 Azienda USL auditata: USL 1 Massa e Articolazioni alimentare auditate: Strutture organizzative dipartimentali U.F. Gestione Imprese Alimentari U.F. Igiene degli Allevamenti e delle
SCHEDA AUDIT N : 05/2011 Azienda USL auditata: USL 1 Massa e Articolazioni alimentare auditate: Strutture organizzative dipartimentali U.F. Gestione Imprese Alimentari U.F. Igiene degli Allevamenti e delle
Articolazioni organizzative che si occupano di sicurezza alimentare auditate:
 SCHEDA AUDIT N : 02/2010 Azienda USL auditata: USL 7 Siena Articolazioni organizzative che si occupano di sicurezza alimentare auditate: U.F. Igiene Alimenti e Nutrizione Zona Senese U.F. Igiene e Sanità
SCHEDA AUDIT N : 02/2010 Azienda USL auditata: USL 7 Siena Articolazioni organizzative che si occupano di sicurezza alimentare auditate: U.F. Igiene Alimenti e Nutrizione Zona Senese U.F. Igiene e Sanità
La Marcatura CE dei Dispositivi Medici
 La Marcatura CE dei Dispositivi Medici Il ruolo dell Organismo Notificato nel progetto di marcatura CE Author: Attilio Durantini (TUV Italia) Slide 1 Il contesto legislativo AIMDD: Direttiva Europea 90/385/CEE
La Marcatura CE dei Dispositivi Medici Il ruolo dell Organismo Notificato nel progetto di marcatura CE Author: Attilio Durantini (TUV Italia) Slide 1 Il contesto legislativo AIMDD: Direttiva Europea 90/385/CEE
Qualità e sicurezza dei dispositivi medici
 Qualità e sicurezza dei dispositivi medici 2 Aprile 2012 organizzato da ISTITUTO SUPERIORE DI SANITA Origine della manifestazione. I recenti casi di incidenti segnalati e il sempre più ampio fenomeno della
Qualità e sicurezza dei dispositivi medici 2 Aprile 2012 organizzato da ISTITUTO SUPERIORE DI SANITA Origine della manifestazione. I recenti casi di incidenti segnalati e il sempre più ampio fenomeno della
PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/32/UE
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/32/UE Messa a disposizione sul mercato di strumenti di misura Allegato II - MODULO B Esame UE
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/32/UE Messa a disposizione sul mercato di strumenti di misura Allegato II - MODULO B Esame UE
REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE
 L 320/8 Gazzetta ufficiale dell Unione europea 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono applicare
L 320/8 Gazzetta ufficiale dell Unione europea 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono applicare
Linee Guida per la gestione del Codice di Repertorio
 Linee Guida per la gestione del Codice di Repertorio Sottogruppo tecnico per la gestione del Codice di Repertorio Roma, 27 giugno g 2012 Premessa il Sottogruppo tecnico Nell incontro del 25 gennaio 2012
Linee Guida per la gestione del Codice di Repertorio Sottogruppo tecnico per la gestione del Codice di Repertorio Roma, 27 giugno g 2012 Premessa il Sottogruppo tecnico Nell incontro del 25 gennaio 2012
DISPOSITIVI MEDICI SICUREZZA D USOD
 DISPOSITIVI MEDICI e SICUREZZA D USOD DISPOSITIVI MEDICI Qualsiasi strumento, apparecchio, impianto, sostanza o altro prodotto, usato da solo o in combinazione, ma destinato dal fabbricante ad essere impiegato
DISPOSITIVI MEDICI e SICUREZZA D USOD DISPOSITIVI MEDICI Qualsiasi strumento, apparecchio, impianto, sostanza o altro prodotto, usato da solo o in combinazione, ma destinato dal fabbricante ad essere impiegato
Ministero delle politiche agricole alimentari e forestali
 Ministero delle politiche agricole alimentari e forestali DG PQAI - PQAI 01 - Prot. Interno N.0008283 del 06/02/2018 DIPARTIMENTO DELLE POLITICHE COMPETITIVE DELLA QUALITÀ AGROALIMENTARE IPPICHE E DELLA
Ministero delle politiche agricole alimentari e forestali DG PQAI - PQAI 01 - Prot. Interno N.0008283 del 06/02/2018 DIPARTIMENTO DELLE POLITICHE COMPETITIVE DELLA QUALITÀ AGROALIMENTARE IPPICHE E DELLA
PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED)
 Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO G - Conformità basata sulla verifica dell unità Riferimento Revisione e data entrata in vigore Approvato da PR PART
Titolo PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO G - Conformità basata sulla verifica dell unità Riferimento Revisione e data entrata in vigore Approvato da PR PART
DELIBERA DEL COMITATO SETTORIALE DI ACCREDITAMENTO CERTIFICAZIONE E ISPEZIONE (CSA CI) DEL 27 NOVEMBRE 2018
 DELIBERA DEL COMITATO SETTORIALE DI ACCREDITAMENTO CERTIFICAZIONE E ISPEZIONE (CSA CI) DEL 27 NOVEMBRE 2018 NUOVI ACCREDITAMENTI CERTI.S S.R.L. Ha ottenuto l accreditamento, nello schema PRS, per le seguenti
DELIBERA DEL COMITATO SETTORIALE DI ACCREDITAMENTO CERTIFICAZIONE E ISPEZIONE (CSA CI) DEL 27 NOVEMBRE 2018 NUOVI ACCREDITAMENTI CERTI.S S.R.L. Ha ottenuto l accreditamento, nello schema PRS, per le seguenti
PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XI Garanzia della Qualità del Prodotto per gli Ascensori
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XI Garanzia della Qualità del Prodotto per gli Ascensori PR.PART. ON/LIFT-XI Rev.
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XI Garanzia della Qualità del Prodotto per gli Ascensori PR.PART. ON/LIFT-XI Rev.
Impresa concorrente LOTTO. GARA n Prodotto
 ALLEGATO F4) SCHEDA TECNICA PRODOTTO MATERIALE PER OSTEOSINTESI DISTRETTO COLLO/FEMORE in conto deposito con strumentario in comodato d uso gratuito Impresa concorrente LOTTO GARA n. 4307622 Prodotto Codice
ALLEGATO F4) SCHEDA TECNICA PRODOTTO MATERIALE PER OSTEOSINTESI DISTRETTO COLLO/FEMORE in conto deposito con strumentario in comodato d uso gratuito Impresa concorrente LOTTO GARA n. 4307622 Prodotto Codice
Sicurezza e DM: Vigilanza, Tracciabilitàe progetti di verifica. Dott.ssa Monica Capasso DGFDM- Ufficio V
 Sicurezza e DM: Vigilanza, Tracciabilitàe progetti di verifica Dott.ssa Monica Capasso DGFDM- Ufficio V L obiettivo del sistema di vigilanza è quello di incrementare la protezione della salute e la sicurezza
Sicurezza e DM: Vigilanza, Tracciabilitàe progetti di verifica Dott.ssa Monica Capasso DGFDM- Ufficio V L obiettivo del sistema di vigilanza è quello di incrementare la protezione della salute e la sicurezza
FOCUS SUI PRINCIPALI ISTITUTI IN MATERIA DI TRATTAMENTO DEI DATI ALLA LUCE DEL GDPR REGOLAMENTO UE 2016/679
 FOCUS SUI UE 2016/679 1 25 MAGGIO 2018 QUADRO NORMATIVO Il 25 maggio 2018 diviene efficace il nuovo regolamento europeo in materia di trattamento dei dati personali General Data Protection Regulation (Regolamento
FOCUS SUI UE 2016/679 1 25 MAGGIO 2018 QUADRO NORMATIVO Il 25 maggio 2018 diviene efficace il nuovo regolamento europeo in materia di trattamento dei dati personali General Data Protection Regulation (Regolamento
Corso I.Re.F La sicurezza delle macchine
 Corso I.Re.F La sicurezza delle macchine ing. Giuliano Corbella UNI Ente Nazionale Italiano di Unificazione Concetto di Direttiva Nuovo Approccio Con la risoluzione del Consiglio del 1985 è stata istituita
Corso I.Re.F La sicurezza delle macchine ing. Giuliano Corbella UNI Ente Nazionale Italiano di Unificazione Concetto di Direttiva Nuovo Approccio Con la risoluzione del Consiglio del 1985 è stata istituita
PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED)
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO F Conformità al tipo basata sulla verifica delle attrezzature
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI PER LA DIRETTIVA 2014/68/UE (PED) Allegato III - MODULO F Conformità al tipo basata sulla verifica delle attrezzature
Il registro delle protesi impiantabili: aspetti normativi
 Il registro delle protesi impiantabili: aspetti normativi Stato attuale e prospettive Istituto Superiore di Sanità Roma, 23 marzo 2007 D. Lgs. 46/1997, art. 13 (come modificato da d. l.vo 332/2000) Registrazione
Il registro delle protesi impiantabili: aspetti normativi Stato attuale e prospettive Istituto Superiore di Sanità Roma, 23 marzo 2007 D. Lgs. 46/1997, art. 13 (come modificato da d. l.vo 332/2000) Registrazione
Consiglio dell'unione europea Bruxelles, 10 marzo 2017 (OR. en)
 Consiglio dell'unione europea Bruxelles, 10 marzo 2017 (OR. en) Fascicolo interistituzionale: 2012/0267 (COD) 7189/17 NOTA DI TRASMISSIONE Origine: Data: 9 marzo 2017 Destinatario: n. doc. Comm.: COM(2017)
Consiglio dell'unione europea Bruxelles, 10 marzo 2017 (OR. en) Fascicolo interistituzionale: 2012/0267 (COD) 7189/17 NOTA DI TRASMISSIONE Origine: Data: 9 marzo 2017 Destinatario: n. doc. Comm.: COM(2017)
Dispositivi medici: attività di sorveglianza in frontiera
 Polizia Sanitaria Roma, 20 Aprile 2011 Dispositivi medici: attività di sorveglianza in frontiera 1 dr. Franco Abbenda Ministero della Salute DGFDM Una precisazione Farmaco, cosmetico o dispositivo medico??
Polizia Sanitaria Roma, 20 Aprile 2011 Dispositivi medici: attività di sorveglianza in frontiera 1 dr. Franco Abbenda Ministero della Salute DGFDM Una precisazione Farmaco, cosmetico o dispositivo medico??
TÜV Rheinland Italia
 TÜV Rheinland Italia TÜV Rheinland Italia 1997 Founded to ensure the safety in the Italian market 2015 TÜV Rheinland Italy Business Stream 01 02 03 04 Business Stream Industrial Business Stream Mobility
TÜV Rheinland Italia TÜV Rheinland Italia 1997 Founded to ensure the safety in the Italian market 2015 TÜV Rheinland Italy Business Stream 01 02 03 04 Business Stream Industrial Business Stream Mobility
2 a CONFERENZA NAZIONALE SUL REGOLAMENTO REACH
 2 a CONFERENZA NAZIONALE SUL REGOLAMENTO REACH Armonizzazione delle procedure di vigilanza a livello comunitario Roma, 11 dicembre 2009 Dott. Mariano Alessi RUOLO DEL FORUM Obiettivi Diffondere buone pratiche,
2 a CONFERENZA NAZIONALE SUL REGOLAMENTO REACH Armonizzazione delle procedure di vigilanza a livello comunitario Roma, 11 dicembre 2009 Dott. Mariano Alessi RUOLO DEL FORUM Obiettivi Diffondere buone pratiche,
REGOLAMENTO (UE) 2017/745 PER I DISPOSITIVI MEDICI. Le novità normative per il trading, la tracciabilità e la supply chain per i dispositivi medici
 REGOLAMENTO (UE) 2017/745 PER I DISPOSITIVI MEDICI Le novità normative per il trading, la tracciabilità e la supply chain per i dispositivi medici Padova, 5 giugno 2017 dott. Riccardo Dainese Eumed s.r.l.
REGOLAMENTO (UE) 2017/745 PER I DISPOSITIVI MEDICI Le novità normative per il trading, la tracciabilità e la supply chain per i dispositivi medici Padova, 5 giugno 2017 dott. Riccardo Dainese Eumed s.r.l.
La Banca Dati ed il Repertorio dei DM
 La Banca Dati ed il Repertorio dei DM Claudia Biffoli Direzione generale del sistema informativo Ex Ministero della Salute XXIX Congresso nazionale SIFO Napoli, 14 Ottobre 2008 0 UDAMED Uropean DAtabase
La Banca Dati ed il Repertorio dei DM Claudia Biffoli Direzione generale del sistema informativo Ex Ministero della Salute XXIX Congresso nazionale SIFO Napoli, 14 Ottobre 2008 0 UDAMED Uropean DAtabase
UDI: ultime novità dalla Commissione e dal MS italiano
 UDI: ultime novità dalla Commissione e dal MS italiano Nel corso del Workshop UDI organizzato a Roma da Assobiomedica lo scorso 31 gennaio 2018 sono intervenuti rappresentanti delle istituzioni, del mondo
UDI: ultime novità dalla Commissione e dal MS italiano Nel corso del Workshop UDI organizzato a Roma da Assobiomedica lo scorso 31 gennaio 2018 sono intervenuti rappresentanti delle istituzioni, del mondo
ESEMPIO DI CONTRATTO DI DISTRIBUZIONE / IMPORTAZIONE 1
 ESEMPIO DI CONTRATTO DI DISTRIBUZIONE / IMPORTAZIONE 1 (di seguito ), una filiale interamente di proprietà di., entrambe le società interamente di proprietà di ASSICURAZIONE DEL CONTROLLO QUALITA, VIGILANZA
ESEMPIO DI CONTRATTO DI DISTRIBUZIONE / IMPORTAZIONE 1 (di seguito ), una filiale interamente di proprietà di., entrambe le società interamente di proprietà di ASSICURAZIONE DEL CONTROLLO QUALITA, VIGILANZA
MARCATURA CE DISPOSITIVI MEDICI OBL
 MARCATURA CE DISPOSITIVI MEDICI OBL Sara Pelizzoli Modena, 29/10/2014 - Copyright Bureau Veritas RIFERIMENTI NORMATIVI Direttiva 93/42/CEE del Consiglio del 14 Giugno 1993 concernente i dispositivi medici
MARCATURA CE DISPOSITIVI MEDICI OBL Sara Pelizzoli Modena, 29/10/2014 - Copyright Bureau Veritas RIFERIMENTI NORMATIVI Direttiva 93/42/CEE del Consiglio del 14 Giugno 1993 concernente i dispositivi medici
Titolo PR. PART. ON/GAR/F. Riferimento. Revisione e data entrata in vigore. Rev. 0 del 17/10/2017
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI REGOLAMENTO (UE) N. 2016/426 (GAR) sugli apparecchi che bruciano carburanti gassosi Allegato III - MODULO F Conformità
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI REGOLAMENTO (UE) N. 2016/426 (GAR) sugli apparecchi che bruciano carburanti gassosi Allegato III - MODULO F Conformità
PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO VI Garanzia della Qualità del Prodotto dei Componenti di Sicurezza per Ascensori
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO VI Garanzia della Qualità del Prodotto dei Componenti di Sicurezza per Ascensori
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO VI Garanzia della Qualità del Prodotto dei Componenti di Sicurezza per Ascensori
I nuovi Regolamenti Europei sui dispositivi medici: le novita principali per il settore e i tempi e le forme dell implementazione
 I nuovi Regolamenti Europei sui dispositivi medici: le novita principali per il settore e i tempi e le forme dell implementazione Seminario I nuovi regolamenti Europei sui dispositivi medici Trieste, 27
I nuovi Regolamenti Europei sui dispositivi medici: le novita principali per il settore e i tempi e le forme dell implementazione Seminario I nuovi regolamenti Europei sui dispositivi medici Trieste, 27
TBS Group. Roberto Belliato. Il Nuovo Regolamento MDR-IVD: Riflessi e impatto operativo per l Ingegneria Clinica
 TBS Group Roberto Belliato Il Nuovo Regolamento MDR-IVD: Riflessi e impatto operativo per l Ingegneria Clinica Trieste, 09/03/2018 Approccio Fase preliminare di studio del Nuovo Regolamento UE 746/2017
TBS Group Roberto Belliato Il Nuovo Regolamento MDR-IVD: Riflessi e impatto operativo per l Ingegneria Clinica Trieste, 09/03/2018 Approccio Fase preliminare di studio del Nuovo Regolamento UE 746/2017
«Obiettivi e contenuti. per gli Audit Committee»
 «Obiettivi e contenuti del questionario del CEAOB per gli Audit Committee» Elena Falsetti Roma, 1 febbraio 2019 Obiettivi e contenuti del questionario del CEAOB per gli Audit Committee L art. 27 del Reg.
«Obiettivi e contenuti del questionario del CEAOB per gli Audit Committee» Elena Falsetti Roma, 1 febbraio 2019 Obiettivi e contenuti del questionario del CEAOB per gli Audit Committee L art. 27 del Reg.
MINISTERO DELLE POLITICHE AGRICOLE ALIMENTARI E FORESTALI
 (PREF) allegato A Linea di attività Ufficio responsabile dell'attuazione Prodotto Indicatori di Prodotto Obiettivo Individuazione e implementazione di modelli per l analisi e la gestione del rischio di
(PREF) allegato A Linea di attività Ufficio responsabile dell'attuazione Prodotto Indicatori di Prodotto Obiettivo Individuazione e implementazione di modelli per l analisi e la gestione del rischio di
Il Ministro della Salute
 Il Ministro della Salute Nuove modalità per gli adempimenti previsti dall articolo 13 del decreto legislativo 24 febbraio 1997, n. 46 e successive modificazioni e per la registrazione dei dispositivi impiantabili
Il Ministro della Salute Nuove modalità per gli adempimenti previsti dall articolo 13 del decreto legislativo 24 febbraio 1997, n. 46 e successive modificazioni e per la registrazione dei dispositivi impiantabili
LA PERSONA RESPONSABILE DEL RISPETTO DELLA NORMATIVA
 LA PERSONA RESPONSABILE DEL RISPETTO DELLA NORMATIVA Alessandro Berti Vice Presidente AIRMEDD Article 15 Person responsible for regulatory compliance I fabbricanti, (.mandatari ) all'interno della loro
LA PERSONA RESPONSABILE DEL RISPETTO DELLA NORMATIVA Alessandro Berti Vice Presidente AIRMEDD Article 15 Person responsible for regulatory compliance I fabbricanti, (.mandatari ) all'interno della loro
RACCOMANDAZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO 1
 Raccomandazione 197 RACCOMANDAZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio
Raccomandazione 197 RACCOMANDAZIONE SUL QUADRO PROMOZIONALE PER LA SALUTE E LA SICUREZZA SUL LAVORO 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio
Protezione dei dati personali (c.d. Privacy ) ASL AL Progetto di attuazione di nuovi servizi privacy.
 Protezione dei dati personali (c.d. Privacy ) ASL AL Progetto di attuazione di nuovi servizi privacy. Alessandria, 21 febbraio 2017 Indice Argomenti oggetto della presentazione Introduzione: ambito, finalità
Protezione dei dati personali (c.d. Privacy ) ASL AL Progetto di attuazione di nuovi servizi privacy. Alessandria, 21 febbraio 2017 Indice Argomenti oggetto della presentazione Introduzione: ambito, finalità
Informativa in merito all Attività annuale di controllo - anno
 Informativa in merito all Attività annuale di controllo - anno 2011 - ai sensi dell art. 65 lett. e) del Reg. (Ce) 1083/06 Autorità di Audit (Gabriella Volpi) 1 Il Comitato di sorveglianza (art.65, lettera
Informativa in merito all Attività annuale di controllo - anno 2011 - ai sensi dell art. 65 lett. e) del Reg. (Ce) 1083/06 Autorità di Audit (Gabriella Volpi) 1 Il Comitato di sorveglianza (art.65, lettera
Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova
 Corso aggiornamento sezione regionale SIFO Liguria Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova Corso SIFO
Corso aggiornamento sezione regionale SIFO Liguria Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova Corso SIFO
Indice generale. Prefazione
 Indice generale Prefazione Autori XI XIII Capitolo 1: Contesto istituzionale e normativo dell Unione Europea 1 1 Trattati e Stati membri 1 2 Le istituzioni dell Unione Europea 3 2.1 Parlamento Europeo
Indice generale Prefazione Autori XI XIII Capitolo 1: Contesto istituzionale e normativo dell Unione Europea 1 1 Trattati e Stati membri 1 2 Le istituzioni dell Unione Europea 3 2.1 Parlamento Europeo
10AA.2018/D /3/2018
 PRESIDENTE DELLA GIUNTA UFFICIO CONTROLLO FONDI EUROPEI 10AA 10AA.2018/D.00008 29/3/2018 UFFICIO CONTROLLO FONDI EUROPEI: Programmazione Comunitaria 2014-2020 -Approvazione "Manuale di Audit"IV Versione
PRESIDENTE DELLA GIUNTA UFFICIO CONTROLLO FONDI EUROPEI 10AA 10AA.2018/D.00008 29/3/2018 UFFICIO CONTROLLO FONDI EUROPEI: Programmazione Comunitaria 2014-2020 -Approvazione "Manuale di Audit"IV Versione
ISO 14001:2015 NUOVI APPROCCI DELL AUDIT DI CERTIFICAZIONE
 NUOVI APPROCCI DELL AUDIT DI CERTIFICAZIONE Stefano Aldini Milano, 6 ottobre 2015 CONFORMA La mission Promuovere la qualità, la sicurezza e la protezione dell ambiente attraverso certificazioni, prove
NUOVI APPROCCI DELL AUDIT DI CERTIFICAZIONE Stefano Aldini Milano, 6 ottobre 2015 CONFORMA La mission Promuovere la qualità, la sicurezza e la protezione dell ambiente attraverso certificazioni, prove
L inventario ECHA delle classificazioni: modalità di notifica
 L inventario ECHA delle classificazioni: modalità di notifica Chiara Pozzi/Ilaria Malerba Servizio Sicurezza Prodotti Direzione Centrale Tecnico Scientifica Roma, 13 maggio 2010 Inventario C&L Titolo V,
L inventario ECHA delle classificazioni: modalità di notifica Chiara Pozzi/Ilaria Malerba Servizio Sicurezza Prodotti Direzione Centrale Tecnico Scientifica Roma, 13 maggio 2010 Inventario C&L Titolo V,
Il REACH questo (s)conosciuto: il quadro normativo. Udine, 27/11/2015
 Il REACH questo (s)conosciuto: il quadro normativo Udine, 27/11/2015 Che cos è il «REACH»? È un regolamento europeo, e precisamente: Reg. (CE) 18-12-2006 n. 1907/2006 «Regolamento del Parlamento Europeo
Il REACH questo (s)conosciuto: il quadro normativo Udine, 27/11/2015 Che cos è il «REACH»? È un regolamento europeo, e precisamente: Reg. (CE) 18-12-2006 n. 1907/2006 «Regolamento del Parlamento Europeo
L Ente Italiano di Accreditamento. Il ruolo dell accreditamento
 L Ente Italiano di Accreditamento Nuovi strumenti per la trasparenza e la qualificazione delle imprese della Green Economy Il Nuovo Codice Appalti e la ISO 37001 Il ruolo dell accreditamento Filippo Trifiletti
L Ente Italiano di Accreditamento Nuovi strumenti per la trasparenza e la qualificazione delle imprese della Green Economy Il Nuovo Codice Appalti e la ISO 37001 Il ruolo dell accreditamento Filippo Trifiletti
Utilizzare il presente modulo per notificare gli aiuti di Stato a favore della pubblicità dei prodotti di cui all allegato I del trattato CE.
 PARTE III.12.R. SCHEDA DI INFORMAZIONI SUPPLEMENTARI SUGLI AIUTI PER LA PROMOZIONE E LA PUBBLICITÀ DEI PRODOTTI AGRICOLI Utilizzare il presente modulo per notificare gli aiuti di Stato a favore della pubblicità
PARTE III.12.R. SCHEDA DI INFORMAZIONI SUPPLEMENTARI SUGLI AIUTI PER LA PROMOZIONE E LA PUBBLICITÀ DEI PRODOTTI AGRICOLI Utilizzare il presente modulo per notificare gli aiuti di Stato a favore della pubblicità
PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XII Garanzia della Qualità della Produzione degli Ascensori
 Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XII Garanzia della Qualità della Produzione degli Ascensori PR.PART. ON/LIFT-XII
Titolo Riferimento Revisione e data entrata in vigore Approvato da PRESCRIZIONI PARTICOLARI DIRETTIVA 2014/33/UE ALLEGATO XII Garanzia della Qualità della Produzione degli Ascensori PR.PART. ON/LIFT-XII
STRUMENTI PER IDENTIFICARE E CARATTERIZZARE I DISPOSITIVI IMPIANTABILI: LA PROSPETTIVA DELLA COLLABORAZIONE TRA IL RIAP E IL NJR
 STRUMENTI PER IDENTIFICARE E CARATTERIZZARE I DISPOSITIVI IMPIANTABILI: LA PROSPETTIVA DELLA COLLABORAZIONE TRA IL RIAP E IL NJR Flussi informativi RIAP per la tracciabilità del DM impiantato: il Dizionario
STRUMENTI PER IDENTIFICARE E CARATTERIZZARE I DISPOSITIVI IMPIANTABILI: LA PROSPETTIVA DELLA COLLABORAZIONE TRA IL RIAP E IL NJR Flussi informativi RIAP per la tracciabilità del DM impiantato: il Dizionario
Dispositivo-vigilanza: aspetti normativi e procedura aziendale per la segnalazione di incidenti o mancati incidenti da dispositivo
 Dispositivo-vigilanza: aspetti normativi e procedura aziendale per la segnalazione di incidenti o mancati incidenti da dispositivo medico Dr.ssa Liliana Ciannarella Dirigente Sanitario Farmacista A.O.Ospedale
Dispositivo-vigilanza: aspetti normativi e procedura aziendale per la segnalazione di incidenti o mancati incidenti da dispositivo medico Dr.ssa Liliana Ciannarella Dirigente Sanitario Farmacista A.O.Ospedale
Ministero dello Sviluppo Economico
 Ministero dello Sviluppo Economico DIREZIONE GENERALE PER IL MERCATO, LA CONCORRENZA, IL CONSUMATORE, LA VIGILANZA E LA NORMATIVA TECNICA IL DIRETTORE GENERALE VISTA la direttiva 94/9/CE relativa agli
Ministero dello Sviluppo Economico DIREZIONE GENERALE PER IL MERCATO, LA CONCORRENZA, IL CONSUMATORE, LA VIGILANZA E LA NORMATIVA TECNICA IL DIRETTORE GENERALE VISTA la direttiva 94/9/CE relativa agli
Sistema per la tracciabilità degli articoli pirotecnici - Direttiva di esecuzione 2014/58/UE della Commissione Europea del 16 aprile 2014
 Argomenti: Sistema per la tracciabilità degli articoli pirotecnici - Direttiva di esecuzione 2014/58/UE della Commissione Europea del 16 aprile 2014 DISCIPLINA ATTIVITA' COMMERCIALI POLITICHE E SERVIZI
Argomenti: Sistema per la tracciabilità degli articoli pirotecnici - Direttiva di esecuzione 2014/58/UE della Commissione Europea del 16 aprile 2014 DISCIPLINA ATTIVITA' COMMERCIALI POLITICHE E SERVIZI
DIREZIONE GENERALE DELLA VALUTAZIONE DEI MEDICINALI E DELLA FARMACOVIGILANZA Ufficio III
 DIREZIONE GENERALE DELLA VALUTAZIONE DEI MEDICINALI E DELLA FARMACOVIGILANZA Ufficio III Decreto Ministeriale 30 maggio 2001: Accertamenti ispettivi sulla osservanza delle norme di buona pratica di fabbricazione
DIREZIONE GENERALE DELLA VALUTAZIONE DEI MEDICINALI E DELLA FARMACOVIGILANZA Ufficio III Decreto Ministeriale 30 maggio 2001: Accertamenti ispettivi sulla osservanza delle norme di buona pratica di fabbricazione
Direttiva EMC 2014/30/EU: gli elementi di novità e le modalità di adeguamento
 Direttiva EMC 2014/30/EU: gli elementi di novità e le modalità di adeguamento Roberto Colombo - IMQ New Legislative Framework ll New Legislative Framework (NLF) è sostanzialmente composto dai seguenti
Direttiva EMC 2014/30/EU: gli elementi di novità e le modalità di adeguamento Roberto Colombo - IMQ New Legislative Framework ll New Legislative Framework (NLF) è sostanzialmente composto dai seguenti
