Prof. Maria Nicola GADALETA
|
|
|
- Giuditta Innocenti
- 9 anni fa
- Просмотров:
Транскрипт
1 Prof. Maria Nicola GADALETA Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA N. 1 T CENTRIFUGAZIONE
2 Centrifugazione Tecnica comunissima in biochimica, basilare per la separazione delle biomolecole e degli organuli cellulari. Permette la separazione meccanica in un mezzo liquido di materiali solidi dal liquido e di materiali solidi tra loro sottoponendoli ad una forza centrifuga. Materiali di FORMA, DIMENSIONI, DENSITA diversa, posti in un campo centrifugo, sedimentano con velocità diversa. cellule organuli subcellulari macromolecole
3 CENTRIFUGAZIONE Le tecniche centrifugative si possono suddividere in generale in: preparative e analitiche La centrifugazione preparativa permette di separare e purificare cellule intere, organuli subcellulari e macromolecole biologiche come acidi nucleici o proteine. La centrifugazione analitica permette invece di studiare le caratteristiche di sedimentazione del campione e di determinarne il grado di purezza o la massa molecolare. Questa centrifugazione richiede quantità minime di materiale e utilizza rotori e sistemi di rilevamento più sensibili e molto più costosi.
4 La forza centrifuga è la forza uguale e contraria che si oppone alla Forza Centripeta, cioè a quella forza che impedisce ad un corpo, animato di moto circolare uniforme, di sfuggire per inerzia nella direzione del moto (ossia nella direzione della tangente alla traiettoria). La Forza Centripeta è perpendicolare alla traiettoria e diretta verso il centro di rotazione mentre la Forza Centrifuga ha la stessa direzione, ma verso opposto.
5 Forza Centrifuga La Forza Centrifuga è perpendicolare all asse di rotazione e diretta verso l esterno F.C. = m ω 2 r m = massa della particella ω = velocità angolare del sistema r = raggio (distanza della particella dall asse di rotazione) ω 2 r m = grammi ω = rad/sec r = cm = accelerazione angolare che definisce il campo centrifugo. La F.C. dipende dal quadrato di ω 2 quindi per aumentare F.C. conviene aumentare questa piuttosto che r F.C. = Dine
6 rpm e RCF La Velocità Angolare ( omega ) può essere espressa anche in r.p.m. ω = 2π rpm 60 Per esprimere la F.C. è comodo definire il seguente rapporto: f.centrif m ω 2 r = f.gravità m g ω 2 r = = g R.C.F. Forza Centrifuga Relativa E improprio chiamarla forza: ci dice di quante volte l accelerazione a cui è sottoposta la particella è più grande della accelerazione di gravità Sostituendo: g=980cm s -2 R.C.F. 4π = 2 rpm 2 r cm/sec 2 R.C.F. = 1, rpm 2 r La R.C.F. è funzione della velocità di rotazione (rpm) e della distanza dall asse di rotazione (r), quindi se sottoposte alla stessa R.C.F., particelle di massa diversa sedimentano con velocità diversa che dipende in gran parte dalla loro massa.
7 Nomogramma Per descrivere le modalità di centrifugazione in maniera completa bisogna indicare: o la R.C.F (come multiplo della forza di gravità, cioè di g) o la velocità di rotazione (rpm) + il raggio del sistema (r=dipende dal rotore usato) N.B. rpm = revolution per minute= giri al min. Il nomogramma serve per convertire i g in rpm quando è noto il rotore che si deve adoperare e quindi si conosce r
8 Centrifugazione preparativa La centrifugazione preparativa comprende: centrifugazione differenziale, centrifugazione in gradiente di densità La centrifugazione differenziale si basa sulla diversa velocità di sedimentazione di particelle tra loro diverse per densità e dimensioni; la centrifugazione porterà inizialmente alla sedimentazione delle particelle di maggiori dimensioni. Se le particelle hanno la stessa massa ma densità diversa, quelle con densità maggiore sedimenteranno più rapidamente di quelle meno dense.
9 Centrifugazione differenziale (Pelleting):FRAZIONAMENTO CELLULARE Il materiale da frazionare viene separato in un certo numero di frazioni mediante centrifugazioni successive in cui aumenta di volta in volta la forza centrifuga applicata (CENTRIFUGAZIONE DIFFERENZIALE). Dopo ciascuna centrifugazione vi è la separazione in due distinte fasi: - Sovranatante - Sedimento (Pellet) La velocità di sedimentazione dipenderà dalle dimensioni e dalla densità della particella; L efficienza del Pelleting sarà proporzionale alla forza di gravità (RCF) applicata e al tempo di centrifugazione.
10 Frazionamento cellulare Il frazionamento cellulare ha lo scopo di isolare le strutture subcellulari per: Lo studio della morfologia, composizione e attività dei componenti La separazione di sostanze con caratteristica localizzazione subcellulare (DNA, Enzimi, CoEnzimi ecc) L integrazione delle attività di componenti subcellulari isolati Importante nel frazionamento cellulare è: La scelta del materiale di partenza (es fegato, cellule ecc) L omogeneizzazione (se si parte da tessuti) con Waring blendor, Potter ecc. L uso di opportuni tamponi, per es.isotonici con l ambiente cellulare in cui la struttura subcellulare si trova (es. una soluzione salina; una soluzione 0,25 M di saccarosio per l integrità dei mitocondri )
11 Centrifugazione differenziale Fr da Kleinsmith Fig 4-29
12 Marcatori di frazioni subcellulari Kleinsmith &Kish, tab 4-2
13 Marcatori di frazioni subcellulari Kleinsmith &Kish, fig 4-30
14 Centrifugazione in gradiente di densità Il gradiente di densità può considerarsi come una colonna di una soluzione la cui densità è crescente man mano che si raggiunge il fondo della provetta. Caratteristiche del gradiente di densità: riduce al minimo le perturbazioni dovute ai moti convettivi, evitando il rimescolamento permette la separazione di particelle con dimensioni simili e con diversa densità Realizzazione di gradienti Soluti usati sali di metalli pesanti (Cloruro di Cesio) molecole organiche (Glicerolo, Saccarosio), polimeri (Ficoll, destrano) sostanze ad alto peso molecolare Forma dei Continui (proteine, ac. nucleici ecc) mediante un Gradienti formatore di gradienti. Maggiore risoluzione Discontinui (ribosomi, virus ecc) mediante stratificazione successiva della soluzione a concentrazione e quindi a densità decrescente
15 Metodi di centrifugazione in gradiente di densità La centrifugazione su gradiente di densità può essere : ZONALE o ISOPCNICA La Centrifugazione Zonale Sfrutta le differenze di dimensione e forma delle particelle. Le particelle sono stratificate alla sommità del gradiente. Sotto l azione della F.C. le particelle si disporranno in zone del gradiente contenenti ciascuna particelle con stessa velocità di sedimentazione. La separazione dipende dal tempo (se si centrifuga per molto tempo le particelle si stratificano tutte sul fondo essendo la densità del gradiente inferiore alla densità delle componenti da separare). Esistono Gradienti continui preformati e apparecchietti per formarli. La densità delle particelle deve essere maggiore della densità di ogni specifica posizione del gradiente. La corsa deve essere terminata prima che ogni particella raggiunga il fondo del tubo se no si ha un rimescolamento delle frazioni stesse. Es. Separare rrna da altri RNA in gradiente di saccarosio.
16 Centrifugazione zonale A Z Campo centrifugo Campione Gradiente di densità Particelle piccole Particelle medie Particelle grandi All inizio le particelle sono stratificate al di sopra del gradiente (A), alla fine (Z) sono sedimentate in funzione delle loro dimensioni, della loro densità e della densità del mezzo.
17 La Centrifugazione Isopicnica (isodensità) o della densità all equilibrio Sfrutta la densità delle particelle (e non la forma o la dimensione) Il gradiente comprende tutti i valori di densità delle particelle da separare. La particella si arresterà nella zona del gradiente la cui densità è pari a quella della particella. È una separazione dipendente solo dalla differenza di densità e non dal tempo. A volte il gradiente non è preformato ma si forma per effetto della F.C. sulle molecole del soluto. Gradienti continui e discontinui. Es. Separazione diverse forme di DNA in base alla diversa densità specifica (esperimento di Meselson e Stahl).
18 Centrifugazione isopicnica con A gradiente Z Campo centrifugo Particelle piccole Particelle medie Particelle grandi All inizio le particelle sono disperse nel mezzo (A), durante la centrifugazione si forma il gradiente, alla fine (Z) le particelle galleggiano alla densità del gradiente uguale alla loro.
19 Ultracentrifugazione E una procedura in cui si utilizzano centrifughe capaci di imprimere al rotore regimi rotazionali estremamente elevati rpm. Il rotore gira in una camera blindata ove viene praticato il vuoto. Ultracentrifugazione preparativa: per separare particelle piccole: microsomi,ribosomi, batteri, virus, ac. nucleici e proteine. Ultracentrifugazione analitica: utilizza un sistema ottico che permette di visualizzare il processo di sedimentazione man mano che si verifica. E possibile caratterizzare: coef. sedimentazione, coef. diffusione, peso molecolare, densità, misura concentrazione e omogeneità di una soluzione.
20 La legge di Stokes esprime la relazione tra velocità di sedimentazione, dimensioni, forma e densità delle particelle e viscosità del mezzo. ν = 2 9 a 2 ( ρ ) p m 2 η ρ ω r 2/9 = coef. per particella sferica V= dx/dt; velocità percorsa dalla particella a = raggio particella (cm) η = viscosità del mezzo (poises) ρ = densità particella o del mezzo s = v/ω 2 r ω 2 r = campo centrifugo Il coefficiente di sedimentazione s esprime la velocità di sedimentazione di una particella per unità di campo centrifugo.
21 Centrifuga analitica Per la determinazione del coefficiente di sedimentazione si centrifuga in un solvente a bassa densità misurando in tempi diversi la velocità del movimento del boundary (cm/sec).
22 Coefficienti di sedimentazione delle principali strutture biologiche: Proteine 2-25 S Acidi nucleici S Virus S Lisosomi 4000 S Mitocondri 20 X X 10 3 S Membrane 100 X 10 3 S Nuclei 4000 X X 10 3 S Il coefficiente di sedimentazione è espresso in secondi e dipende dalla temperatura, dalla densità e dalla viscosità della soluzione. Poiché gli studi di velocità di sedimentazione vengono condotti impiegando svariati sistemi solutosolvente, per convenzione si usa correggere il coefficiente di sedimentazione trovato sperimentalmente in quel valore che si otterrebbe in un mezzo la cui densità e viscosità fosse pari a quello dell'acqua a 20 C:coefficiente di sedimentazione standard o s 20,w. S = Svedberg = sec.
23 Centrifughe Centrifughe da banco preparative analitiche separazioni rapide di sospensioni grossolane separazioni preparative di particelle diverse fra loro Analisi di particelle già pure per studiare le caratteristiche di sedimentazione delle macromolecole o strutture organiche che interessano
24 Centrifughe e rotori
25 Rotori Rotore ad angolo fisso I rotori ad angolo fisso hanno piccole differenze tra r max e r min Il tempo richiesto per la sedimentazione è minore per rotori ad angolo fisso I rotori ad angolo fisso sono più pesanti e necessitano di una maggiore energia per operare I rotori a bracci mobili (Swing out) sono da preferire per centrifugare cellule e particelle Per sedimentare macromolecole e particelle fini si usano rotori ad angolo fisso I rotori a bracci mobili sono da preferire per la centrifugazione su gradiente. r max - r min Rotore swing-out r max - r min
26 ESERCITAZIONE: Centrifugazione e frazionamento cellulare: isolamento di mitocondri. Isolamento di mitocondri da fegato di ratto mediante centrifugazione differenziale Preparare 50 ml di una soluzione composta da: Saccarosio 0,25 M, Tris 10 mm ph 7,4, EDTA 1 mm. Calcolare quanti grammi di saccarosio (PM 342,30)..., quanti ml di Tris a partire da una soluzione madre 1M..., quanti ml di EDTA a partire da una soluzione madre 0,1 M..., sono necessari per preparare la soluzione. Raffreddare la soluzione in ghiaccio. Omogeneizzare meccanicamente circa 2 g di fegato di ratto (prelevato da animale sacrificato in precedenza e congelato in azoto liquido) mediante pestello e mortaio in presenza di azoto liquido, così da mantenere il campione congelato durante la procedura. Raccogliere la polvere del campione, trasferirla in un potter e risospenderla in 10 ml della soluzione preparata in precedenza. Omogeneizzare a velocità media con 3-5 colpi di potter fino ad ottenere una sospensione omogenea all aspetto. Trasferire l omogenato in 1 tubo da 15 ml.
27 Centrifugare la sospensione a 500 x g, in rotore a 4 C per 5 min per far sedimentare nuclei e frammenti cellulari. Prelevare il sovranatante, trasferirlo in altri tubi e centrifugare a 6000 x g, in rotore JA-20, a 4 C per 10 min per far sedimentare i mitocondri. Risospendere ciascun pellet di mitocondri in 1 ml di soluzione di saccarosio, trasferirlo in eppendorf e omogenarlo a mano con un micropestello. Conservare i mitocondri a 20 C per il successivo dosaggio delle proteine.
Tecniche Centrifugative
 Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
TECNICHE CENTRIFUGATIVE
 TECNICHE CENTRIFUGATIVE Le tecniche di separazione mediante centrifugazione sfruttano il comportamento delle particelle all interno di un campo centrifugo applicato Lo scopo di tali metodiche e quello
TECNICHE CENTRIFUGATIVE Le tecniche di separazione mediante centrifugazione sfruttano il comportamento delle particelle all interno di un campo centrifugo applicato Lo scopo di tali metodiche e quello
Centrifugazione. Alle sospensioni viene applicato un campo gravitazionale artificiale attraverso la rotazione ad alta velocità (campo centrifugo).
 Centrifugazione Alle sospensioni viene applicato un campo gravitazionale artificiale attraverso la rotazione ad alta velocità (campo centrifugo). Viene sfruttata la differenza di densità tra le particelle
Centrifugazione Alle sospensioni viene applicato un campo gravitazionale artificiale attraverso la rotazione ad alta velocità (campo centrifugo). Viene sfruttata la differenza di densità tra le particelle
Acidi nucleici come materiale di studio. DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna
 Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA
 TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA TIPI DI CENTRIFUGHE CENTRIFUGHE PREPARATIVE Consentono la separazione, isolamento e purificazione
TECNICHE CENTRIFUGATIVE PRINCIPI DI BASE DELLA SEDIMENTAZIONE TIPI DI CENTRIFUGHE ULTRACENTRIFUGA ANALITICA TIPI DI CENTRIFUGHE CENTRIFUGHE PREPARATIVE Consentono la separazione, isolamento e purificazione
PURIFICAZIONE DELLE PROTEINE
 PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
TECNICHE CENTRIFUGATIVE
 TECNICHE CENTRIFUGATIVE Le tecniche di separazione mediante centrifugazione sfruttano il comportamento delle particelle all interno di un campo centrifugo applicato Lo scopo di tali metodiche e quello
TECNICHE CENTRIFUGATIVE Le tecniche di separazione mediante centrifugazione sfruttano il comportamento delle particelle all interno di un campo centrifugo applicato Lo scopo di tali metodiche e quello
da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri
 7.17. SEDIMENTAZIONE da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri Se si vogliono studiare le proprietà fisiche e chimiche dei componenti subcellulari (membrane, nuclei, mitocondri, ecc.)
7.17. SEDIMENTAZIONE da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri Se si vogliono studiare le proprietà fisiche e chimiche dei componenti subcellulari (membrane, nuclei, mitocondri, ecc.)
Metodi di studio delle proteine (o altre macromolecole)
 Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Applicazione equazione di Bernoulli: stenosi arteriosa(restringimento arteria)
 Applicazione equazione di Bernoulli: stenosi arteriosa(restringimento arteria) Applicazione equazione di Bernoulli: Aneurisma (dilatazione arteria) Liquidi reali attrito interno-viscosita' la velocita'
Applicazione equazione di Bernoulli: stenosi arteriosa(restringimento arteria) Applicazione equazione di Bernoulli: Aneurisma (dilatazione arteria) Liquidi reali attrito interno-viscosita' la velocita'
LEGGE DI STOKES. Fisica Applicata, Area Infermieristica, M. Ruspa
 LEGGE DI STOKES La forza di attrito viscoso che agisce su un corpo sfrerico di raggio r che si muove con velocita v non elevata in un fluido di viscosita η in quite si puo calcolare come: SEDIMENTAZIONE
LEGGE DI STOKES La forza di attrito viscoso che agisce su un corpo sfrerico di raggio r che si muove con velocita v non elevata in un fluido di viscosita η in quite si puo calcolare come: SEDIMENTAZIONE
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Il Corso di Fisica per Scienze Biologiche
 Il Corso di Fisica per Scienze Biologiche Ø Prof. Attilio Santocchia Ø Ufficio presso il Dipartimento di Fisica (Quinto Piano) Tel. 075-585 708 Ø E-mail: [email protected] Ø Web: http://www.fisica.unipg.it/~attilio.santocchia
Il Corso di Fisica per Scienze Biologiche Ø Prof. Attilio Santocchia Ø Ufficio presso il Dipartimento di Fisica (Quinto Piano) Tel. 075-585 708 Ø E-mail: [email protected] Ø Web: http://www.fisica.unipg.it/~attilio.santocchia
CENTRIFUGHE. Centrifughe da Laboratorio Ventilate
 CENTRIFUGHE Centrifughe da Laboratorio Ventilate Centrifuga R-8D Costruzione estremamente compatta Camera di centrifugazione in acciaio e di facile accessibilità Display digitale luminoso Interfaccia intuitiva
CENTRIFUGHE Centrifughe da Laboratorio Ventilate Centrifuga R-8D Costruzione estremamente compatta Camera di centrifugazione in acciaio e di facile accessibilità Display digitale luminoso Interfaccia intuitiva
Centrifughe da laboratorio
 3 R-5S Basic per scuole e lavori di routine R-16M R-8C+ R-9M per microprovette la classica per laboratorio per laboratorio con microprocessore Centrifuga R-5S Basic La centrifuga per l utilizzatore che
3 R-5S Basic per scuole e lavori di routine R-16M R-8C+ R-9M per microprovette la classica per laboratorio per laboratorio con microprocessore Centrifuga R-5S Basic La centrifuga per l utilizzatore che
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
10/03/16. Metodi vigorosi
 Metodi blandi Lisi cellulare con detergenti Metodi vigorosi 1 10/03/16 FRAZIONAMENTO CELLULARE 1. Centrifugazione preparativa Centrifugazione preparativa permette di separare i vari elementi di un omogenato
Metodi blandi Lisi cellulare con detergenti Metodi vigorosi 1 10/03/16 FRAZIONAMENTO CELLULARE 1. Centrifugazione preparativa Centrifugazione preparativa permette di separare i vari elementi di un omogenato
Teoria cellulare e Evoluzione biologica. f i l o g e n e s i. Batteri Funghi Alghe Protozoi. (aspetto morfologico e funzione) Microrganismi
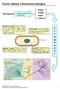 Teoria cellulare e Evoluzione biologica Microrganismi (aspetto morfologico e funzione) Batteri Funghi Alghe Protozoi f i l o g e n e s i Microbiologia, Perry, Staley and Lory, ZANICHELLI, http://www.zanichelli.it/f_universita.html
Teoria cellulare e Evoluzione biologica Microrganismi (aspetto morfologico e funzione) Batteri Funghi Alghe Protozoi f i l o g e n e s i Microbiologia, Perry, Staley and Lory, ZANICHELLI, http://www.zanichelli.it/f_universita.html
Calcolo idraulico. 8.1 Definizione di idraulica. 8.2 Proprietà dell acqua
 8 Calcolo idraulico 8.1 Definizione di idraulica è quella parte della meccanica dei mezzi continui che studia le leggi che regolano la statica o il moto dei fluidi. Generalmente si distingue in idrostatica
8 Calcolo idraulico 8.1 Definizione di idraulica è quella parte della meccanica dei mezzi continui che studia le leggi che regolano la statica o il moto dei fluidi. Generalmente si distingue in idrostatica
PROTOCOLLO RACCOLTA SANGUE PER ANALISI OMICHE
 PROTOCOLLO RACCOLTA SANGUE PER ANALISI OMICHE 00028 Autori Vittorio Sirolli Gianluigi Zaza Contenuti Premesse - Introduzione separazione del plasma Premesse - Introduzione separazione del plasma release
PROTOCOLLO RACCOLTA SANGUE PER ANALISI OMICHE 00028 Autori Vittorio Sirolli Gianluigi Zaza Contenuti Premesse - Introduzione separazione del plasma Premesse - Introduzione separazione del plasma release
TECNOLOGIE BIOMOLECOLARI
 TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
Magnete. Campo magnetico. Fenomeni magnetici. Esempio. Esempio. Che cos è un magnete? FENOMENI MAGNETICI
 Magnete FENOMENI MAGNETICI Che cos è un magnete? Un magnete è un materiale in grado di attrarre pezzi di ferro Prof. Crosetto Silvio 2 Prof. Crosetto Silvio Quando si avvicina ad un pezzo di magnetite
Magnete FENOMENI MAGNETICI Che cos è un magnete? Un magnete è un materiale in grado di attrarre pezzi di ferro Prof. Crosetto Silvio 2 Prof. Crosetto Silvio Quando si avvicina ad un pezzo di magnetite
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
MATERIALE DIDATTICO. A supporto sono rese disponibili le slides delle lezioni
 MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
G. Dehò, E. Galli Biologia dei Microrganismi Copyright 2012 C.E.A. Casa Editrice Ambrosiana
 G. Dehò, E. Galli Biologia dei Microrganismi Copyright 2012 C.E.A. Casa Editrice Ambrosiana Teoria cellulare e Evoluzione biologica Microrganismi (aspetto morfologico e funzione) Batteri Funghi Alghe Protozoi
G. Dehò, E. Galli Biologia dei Microrganismi Copyright 2012 C.E.A. Casa Editrice Ambrosiana Teoria cellulare e Evoluzione biologica Microrganismi (aspetto morfologico e funzione) Batteri Funghi Alghe Protozoi
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Acido 3,5-dinitrosalicilico Glucosio Acido 3-amino-5-nitrosalicilico Acido gluconico (Incolore-giallo leggero)
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
Terza prova parziale di Fisica Data: 15 Dicembre Fisica. 15 Dicembre Test a risposta singola
 Fisica 15 Dicembre 2011 Test a risposta singola ˆ Una forza si dice conservativa quando: Il lavoro compiuto dalla forza su un qualsiasi cammino chiuso è nullo Il lavoro compiuto dalla forza su un qualsiasi
Fisica 15 Dicembre 2011 Test a risposta singola ˆ Una forza si dice conservativa quando: Il lavoro compiuto dalla forza su un qualsiasi cammino chiuso è nullo Il lavoro compiuto dalla forza su un qualsiasi
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Esempi di esercizi per la preparazione al primo compito di esonero
 Esempi di esercizi per la preparazione al primo compito di esonero 1. Quanto sangue è approssimativamente presente in un essere umano? Esprimere il risultato in ml. 2. La densità dell etanolo e pare a
Esempi di esercizi per la preparazione al primo compito di esonero 1. Quanto sangue è approssimativamente presente in un essere umano? Esprimere il risultato in ml. 2. La densità dell etanolo e pare a
VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI
 VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI Laboratorio di Genetica dei Microrganismi (Responsabile attività: Prof. Giovanni Salzano; Tutor: Dr.ssa Maria Grazia
VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI Laboratorio di Genetica dei Microrganismi (Responsabile attività: Prof. Giovanni Salzano; Tutor: Dr.ssa Maria Grazia
La lezione di oggi. I fluidi reali La viscosità Flussi laminare e turbolento. La resistenza idrodinamica
 1 La lezione di oggi I fluidi reali La viscosità Flussi laminare e turbolento La resistenza idrodinamica 2 La lezione di oggi Forze di trascinamento nei fluidi La legge di Stokes La centrifuga 3 ! Viscosità!
1 La lezione di oggi I fluidi reali La viscosità Flussi laminare e turbolento La resistenza idrodinamica 2 La lezione di oggi Forze di trascinamento nei fluidi La legge di Stokes La centrifuga 3 ! Viscosità!
Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
5- Estrazione ed analisi di DNA
 5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
DNA ACIDI NUCLEICI. Le coppie di basi sono distanti 0.34 nm. Un giro completo (360 ) della doppia elica richiede 3.4 nm, cioè 10 coppie di basi.
 DNA ACIDI NUCLEICI La scoperta della struttura del DNA avvenne alla Cambridge University nel 1953, da parte dell americano James D. Watson, ed un inglese, Francis H. Crick. Il loro modello per la struttura
DNA ACIDI NUCLEICI La scoperta della struttura del DNA avvenne alla Cambridge University nel 1953, da parte dell americano James D. Watson, ed un inglese, Francis H. Crick. Il loro modello per la struttura
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
IL MATERIALE EREDITARIO. Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene
 IL MATERIALE EREDITARIO Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene Caratteristiche del materiale ereditario 1 Replicarsi accuratamente durante crescita e divisione
IL MATERIALE EREDITARIO Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Giovanna Attene Caratteristiche del materiale ereditario 1 Replicarsi accuratamente durante crescita e divisione
CAMPIONAMENTO fondamentale analisi campionamento omogenei stessa composizione variazione l abilità persona variabilità metodo analitico realtà
 CAMPIONAMENTO Un momento fondamentale di una analisi è rappresentato dal campionamento, generalmente si pensa che i campioni da analizzare siano omogenei e che abbiano in ogni punto la stessa composizione,
CAMPIONAMENTO Un momento fondamentale di una analisi è rappresentato dal campionamento, generalmente si pensa che i campioni da analizzare siano omogenei e che abbiano in ogni punto la stessa composizione,
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
GASCROMATOGRAFIA INTRODUZIONE
 GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
I MOTI NEL PIANO. Vettore posizione e vettore spostamento
 I MOTI NEL IANO Vettore posizione e vettore spostamento Si parla di moto in un piano quando lo spostamento non avviene lungo una retta, ma in un piano, e può essere descritto usando un sistema di riferimento
I MOTI NEL IANO Vettore posizione e vettore spostamento Si parla di moto in un piano quando lo spostamento non avviene lungo una retta, ma in un piano, e può essere descritto usando un sistema di riferimento
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Classe delle operazioni unitarie fondamentali di SEPARAZIONE MECCANICA 1. Definizione
 Classe delle operazioni unitarie fondamentali di SEPARAZIONE MECCANICA 1. Definizione Si opera un frazionamento basato su differenze di forma, dimensione o densità per separare o purificare frazioni utili
Classe delle operazioni unitarie fondamentali di SEPARAZIONE MECCANICA 1. Definizione Si opera un frazionamento basato su differenze di forma, dimensione o densità per separare o purificare frazioni utili
Rotazioni. Debora Botturi ALTAIR. Debora Botturi. Laboratorio di Sistemi e Segnali
 Rotazioni ALTAIR http://metropolis.sci.univr.it Argomenti Propietá di base della rotazione Argomenti Argomenti Propietá di base della rotazione Leggi base del moto Inerzia, molle, smorzatori, leve ed ingranaggi
Rotazioni ALTAIR http://metropolis.sci.univr.it Argomenti Propietá di base della rotazione Argomenti Argomenti Propietá di base della rotazione Leggi base del moto Inerzia, molle, smorzatori, leve ed ingranaggi
CARATTERISTICHE. In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee.
 In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
ISOLAMENTO E PURIFICAZIONE DEGLI ACIDI NUCLEICI prof.ssa Daniela Gallo
 ISOLAMENTO E PURIFICAZIONE DEGLI ACIDI NUCLEICI prof.ssa Daniela Gallo INTRODUZIONE Acidi nucleici Gli acidi nucleici sono una famiglia eterogenea di macromolecole distribuite all interno di tutte le cellule
ISOLAMENTO E PURIFICAZIONE DEGLI ACIDI NUCLEICI prof.ssa Daniela Gallo INTRODUZIONE Acidi nucleici Gli acidi nucleici sono una famiglia eterogenea di macromolecole distribuite all interno di tutte le cellule
Estrazione di proteine - Scelta della fonte biologica
 Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Dinamica dei fluidi. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 Dinamica dei fluidi Universita' di Udine 1 Caratteristiche di un fluido In generale: FLUIDO sostanza senza forma propria (assume la forma del recipiente che la contiene) liquido volume limitato dalla superficie
Dinamica dei fluidi Universita' di Udine 1 Caratteristiche di un fluido In generale: FLUIDO sostanza senza forma propria (assume la forma del recipiente che la contiene) liquido volume limitato dalla superficie
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
Test di vitalità cellulare
 Test di vitalità cellulare Per valutare, nell ambito di una popolazione cellulare, la percentuale di cellule vitali si possono effettuare diversi test, ad es.: 1. Cloruro di Trifeniltetrazolio (TTC) Formula
Test di vitalità cellulare Per valutare, nell ambito di una popolazione cellulare, la percentuale di cellule vitali si possono effettuare diversi test, ad es.: 1. Cloruro di Trifeniltetrazolio (TTC) Formula
Secondo Appello Estivo del corso di Fisica del
 Secondo Appello Estivo del corso di Fisica del 25.7.2012 Corso di laurea in Informatica A.A. 2011-2012 (Prof. Paolo Camarri) Cognome: Nome: Matricola: Anno di immatricolazione: Problema n.1 Una semisfera
Secondo Appello Estivo del corso di Fisica del 25.7.2012 Corso di laurea in Informatica A.A. 2011-2012 (Prof. Paolo Camarri) Cognome: Nome: Matricola: Anno di immatricolazione: Problema n.1 Una semisfera
CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING
 Largo Zecca, 4-16124 GENOVA Tel. 010/247.07.78 - Fax 010/251.29.60- E-mail [email protected] C.F. 95062410105 CLASSI PRIME: CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING Grandezze
Largo Zecca, 4-16124 GENOVA Tel. 010/247.07.78 - Fax 010/251.29.60- E-mail [email protected] C.F. 95062410105 CLASSI PRIME: CORSI DELL INDIRIZZO TECNICO AMMINISTRAZIONE FINANZA MARKETING Grandezze
Angolo polare, versori radiale e trasverso
 Angolo polare, versori radiale e trasverso Desideriamo descrivere il moto di un corpo puntiforme che ruota su una circonferenza attorno ad un asse fisso. Nella figura l asse di rotazione coincide con l
Angolo polare, versori radiale e trasverso Desideriamo descrivere il moto di un corpo puntiforme che ruota su una circonferenza attorno ad un asse fisso. Nella figura l asse di rotazione coincide con l
FISICA. MECCANICA: Principio conservazione momento angolare. Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica
 FISICA MECCANICA: Principio conservazione momento angolare Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica MOMENTO ANGOLARE Fino a questo punto abbiamo esaminato soltanto moti di traslazione.
FISICA MECCANICA: Principio conservazione momento angolare Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica MOMENTO ANGOLARE Fino a questo punto abbiamo esaminato soltanto moti di traslazione.
Elettroforesi di Tamara Benincasa
 Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
Modulo Biologia-Chimica-Fisica. Syllabus delle conoscenze di base cui fanno riferimento le 25 domande
 Modulo Biologia-Chimica-Fisica Syllabus delle conoscenze di base cui fanno riferimento le 25 domande Le conoscenze di base richieste per ciascun argomento sono limitate a quanto esposto nei testi delle
Modulo Biologia-Chimica-Fisica Syllabus delle conoscenze di base cui fanno riferimento le 25 domande Le conoscenze di base richieste per ciascun argomento sono limitate a quanto esposto nei testi delle
l'analisi dello spettro permette di individuare la natura della sostanza in esame
 L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
L ACQUA E LE CELLULE VEGETALI
 L ACQUA E LE CELLULE VEGETALI Importanza dell acqua per le cellule vegetali compromesso fotosintesi/traspirazione: la necessità fotosintetica espone le piante al rischio di disidratazione Il deficit idrico
L ACQUA E LE CELLULE VEGETALI Importanza dell acqua per le cellule vegetali compromesso fotosintesi/traspirazione: la necessità fotosintetica espone le piante al rischio di disidratazione Il deficit idrico
Distribuzione e Temperatura. Pressione di Vapore. Evaporazione
 Evaporazione Le molecole del Liquido hanno una distribuzione di energia cinetica. Una frazione di molecole della superficie del liquido ha energia cinetica sufficiente per sfuggire all attrazione attrazione
Evaporazione Le molecole del Liquido hanno una distribuzione di energia cinetica. Una frazione di molecole della superficie del liquido ha energia cinetica sufficiente per sfuggire all attrazione attrazione
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Prova scritta di FISICA 16 Febbraio 2016
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE Prova scritta di FISICA 16 Febbraio 016 1) Un corpo di massa M= kg si muove lungo una guida AB, liscia ed irregolare, partendo dal punto A a quota H = 9m, fino al
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Prova scritta di FISICA 16 Febbraio 016 1) Un corpo di massa M= kg si muove lungo una guida AB, liscia ed irregolare, partendo dal punto A a quota H = 9m, fino al
POTENZA METABOLICA. Fisica Applicata, Area Infermieristica, M. Ruspa
 POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
La separazione elettrolitica di un metallo. Scheda di Laboratorio
 La separazione elettrolitica di un metallo Scheda di Laboratorio Premessa Destinatari: classe seconda di un istituto tecnico commerciale, nell insegnamento di scienze della materia. Argomento proposto:
La separazione elettrolitica di un metallo Scheda di Laboratorio Premessa Destinatari: classe seconda di un istituto tecnico commerciale, nell insegnamento di scienze della materia. Argomento proposto:
CENTRIFUGAZIONE. Centrifugazione. Forza centrifuga e caratteristiche costruttive. Forza centrifuga e caratteristiche costruttive. (v =!
 CENTRIFUGAZIONE Prof.ssa Silvia Recchia Centrifugazione Alle sospensioni viene applicato un campo gravitazionale artificiale attraverso la rotazione ad alta velocità (campo centrifugo). Per la separazione
CENTRIFUGAZIONE Prof.ssa Silvia Recchia Centrifugazione Alle sospensioni viene applicato un campo gravitazionale artificiale attraverso la rotazione ad alta velocità (campo centrifugo). Per la separazione
