Promotore: Prof. Alessandro Gringeri. Sperimentatore principale:
|
|
|
- Ippolito Alessi
- 8 anni fa
- Просмотров:
Транскрипт
1 NOTA INFORMATIVA E CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST- NAÏVE (REScue Immunotolerance STudy in ITI-Naïve patients) PAZIENTE MINORE- ADOLESCENTE Studio randomizzato sulla induzione della Immunotolleranza per la prima volta in pazienti con severa emofilia di tipo A con inibitore ad alto rischio di fallimento: comparazione tra l induzione della immunotolleranza con concentrati di Fattore VIII (FVIII) con il Fattore di Von Willebrand (FVW)e quelli senza il fattore di Von Willebrand. Promotore: Prof. Alessandro Gringeri Sperimentatore principale: Ciao, vorrei invitarti a partecipare a una ricerca organizzata dal Centro Emofilia Angelo Bianchi Bonomi, Dipartimento di Medicina e Specialità Mediche, IRCCS Fondazione Ospedale Maggiore Policlinico Mangiagalli e Regina Elena, Via Pace, 9 Milano. Prima di decidere di dare il tuo consenso alla partecipazione allo studio è molto importante che tu capisca i motivi di questa ricerca. Leggi attentamente la seguente nota informativa e chiedi informazioni sui punti che non ti sono chiari. AMBITO DI INTERESSE DELLO STUDIO Il tuo medico vuole proporti di partecipare al presente studio in quanto sei è affetto da emofilia grave di tipo A con inibitore del fattore VIII. La presenza di questo inibitore è una complicanza seria dell Emofilia che deve essere trattata appena possibile per far sì che il sistema immunitario accetti nuovamente i trattamenti con concentrati di FVIII e tu possa controllare meglio le tue emorragie. OBIETTIVO DELLO STUDIO Il trattamento convenzionale dei pazienti che come te hanno inibitori del fattore VIII si chiama induzione della tolleranza immunologica o immunotolleranza. Tolleranza immunologica significa che il sistema immunitario dell organismo accetta e tollera il fattore VIII somministrato e che il paziente risponde di nuovo normalmente alle iniezioni di fattore VIII. La tolleranza immunologica si ottiene somministrando forti dosi di fattore VIII ogni giorno fino alla scomparsa dell inibitore. Esistono 2 tipi di concentrati di fattore VIII: i concentrati di fattore VIII di origine plasmatica umana che contengono il fattore Von Willebrand e i concentrati di fattore VIII ricombinante che non contengono quest altro fattore della coagulazione. 1
2 Si è ipotizzato che i concentrati contenenti il fattore Von Willebrand potrebbero essere più efficaci nell indurre l organismo ad accettare il fattore VIII (tolleranza immunologica). Ti verrà dato uno di questi due tipi di fattore VIII scelto dal caso (questa scelta casuale la chiamiamo randomizzazione ). Quindi, l obiettivo principale di questo studio sarà quello di verificare quale dei due tipi di concentrato funziona di più nell eliminare l inibitore. SVOLGIMENTO DELLO STUDIO Esistono diverse specialità commerciali di questi concentrati plasmatici contenenti fattore di von Willebrand. Sarà il tuo medico, in accordo con te, a decidere quella che ti verrà assegnata per tutta la durata dello studio. La durata massima del trattamento è di 33 mesi. Dopo l ottenimento della tolleranza immunologica, sarai sottoposto a un follow-up (un controllo) nei 12 mesi successivi per verificare il rischio di ricomparsa dell inibitore. Sarai seguito dal proprio medico presso il Centro di emofilia 1 volta al mese per tutta la durata dello studio; un campione di sangue (10 ml, circa 2 cucchiaini da te) sarà preso all inizio e alla fine dello studio, e un campione di 3.5 ml ogni mese. Inoltre, un prelievo di 5 ml sarà effettuato una volta durante il periodo di trattamento per i test genetici (per studiare i fattori che possono essere legati alla terapia che stai facendo). Se tutti questi concetti ti sembrano difficili da comprendere, chiedi chiarimenti al tuo medico di riferimento che saprà darti tutte le informazioni necessarie! RISCHI POTENZIALI Per poter effettuare quotidianamente l iniezione di fattore VIII per diversi mesi, è possibile che il tuo medico ti proponga l applicazione di un catetere venoso centrale. L applicazione di questo dispositivo è una procedura abituale. Questa applicazione è un intervento chirurgico semplice e realizzato in anestesia generale. Il rischio principale di questo catetere è una eventuale infezione, che richiederebbe il trattamento con antibiotici o l asportazione del catetere e la conseguente necessità di reinserire un dispositivo nuovo. TRATTAMENTO ALTERNATIVO L induzione della tolleranza immunologica è il trattamento abituale dei pazienti che hanno sviluppato un inibitore contro il fattore VIII. Nel caso in cui decidessi di non partecipare allo studio, verrai ugualmente sottoposto a un induzione dell Immunotolleranza in quanto si tratta del trattamento normale. 2
3 Sia che partecipi o meno allo studio, in caso di emorragia attiva, verrai trattato con altri fattori della coagulazione aventi un attività bypassante cioè capace di saltare l assenza di fattore VIII. POSSIBILI BENEFICI DELLO STUDIO Non è possibile garantirti o prometterti un beneficio diretto derivante dalla tua partecipazione. Tuttavia le informazioni che saranno fornite dallo studio consentiranno un progresso nelle modalità di trattamento dei pazienti che come te avranno bisogno di indurre la tolleranza immunologica al fattore VIII. COMUNICAZIONE DI NUOVE INFORMAZIONI Sarai informato di qualsiasi nuova informazione relativa al presente studio che potrebbe influenzare la tua decisione di proseguire o meno la partecipazione allo studio e dovrai firmare un nuovo modulo di consenso. Allo stesso modo, sarai informato dei risultati globali dello studio, una volta terminato. PARTECIPAZIONE La tua partecipazione al presente studio è completamente volontaria. Inoltre, hai il diritto di ritirarti dallo studio in qualsiasi momento e senza dover fornire spiegazioni. Il rifiuto o l interruzione della partecipazione allo studio non cambieranno i tuoi rapporti con il medico del Centro di emofilia, che continuerà a seguirti come sempre. DISPOSIZIONI LEGALI Ti informiamo che lo studio verrà condotto in accordo con le Norme di Buona Pratica Clinica definite a livello internazionale e nel rispetto dei principi etici stabiliti nella Dichiarazione di Helsinki. RISERVATEZZA DELLE INFORMAZIONI RACCOLTE Tutti i tuoi dati medici raccolti nel corso del presente studio saranno conservati in forma strettamente riservata. Per garantire l anonimato, nei documenti relativi allo studio tali dati saranno identificati dal tuo Centro di trattamento dell emofilia con un numero e con le tue iniziali. CONTATTI Per eventuali domande in merito allo studio o ai tuoi diritti, o in caso di problemi legati allo studio, contatta i medici responsabili della sperimentazione del tuo Centro di 3
4 trattamento dell emofilia: il Professor Alessandro Gringeri, al seguente n. di telefono : , Eventuali commenti, domande e qualsiasi forma di richiesta sono ben accetti. Per maggiori informazioni, non esitare a contattare il personale del centro di emofilia o il Professor Gring CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST-NAÏVE PAZIENTE MINORE ADOLESCENTE (REScue Immunotolerance STudy) Studio randomizzato sulla induzione della Immunotolleranza per la prima volta in pazienticon severa emofilia di tipo A con inibitore ad alto rischio di fallimento: comparazione tra l induzione della immunotolleranza con concentrati di Fattore VIII (FVIII) con il Fattore di Von Willebrand (FVW)e quelli senza il fattore di Von Willebrand. 1. Confermo di aver letto e compreso la nota informativa relativa allo studio sopra riportato e di aver avuto modo di porre domande al medico sperimentatore. 2. Ho capito che la mia partecipazione è volontaria e che sono libero di ritirare il mio consenso in qualsiasi momento presso il medico sperimentatore, per qualsivoglia ragione, senza che siano compromessi i miei trattamenti medici e i miei diritti legali. 3. Sono a conoscenza del fatto che i dati di carattere medico saranno trattati nel più totale anonimato sin dall inserimento nello studio. Autorizzo l accesso a tali dati a coloro che lavorano al presente studio. 4. Firmando il modulo di consenso, accetto di partecipare allo studio RESIST- Naïve 5. Sono d accordo/non sono d accordo (ti prego di scegliere l opzione desiderata) che i miei campioni di sangue potranno essere conservati e utilizzati per ricerche future compresi eventuali test genetici. Sarò sempre contattato per ogni futura ricerca che possa implicare l uso di un mio campione di sangue al fine di approvare l utilizzo di tale campione con il consenso informato CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST-NAÏVE PAZIENTE MINORE ADOLESCENTE (REScue Immunotolerance STudy Naïve Patients) IL PAZIENTE: COGNOME e NOME, di anni dichiara di accettare di partecipare liberamente e volontariamente allo studio denominato RESIST- Naïve.. [Luogo] Data (gg/mm/aa): 4
5 Firma del paziente: IL MEDICO SPERIMENTATORE: Io sottoscritto/a Dott/Dott.ssa (COGNOME e NOME), attesto di aver spiegato ai titolari della potestà genitoriale e il paziente firmatario lo scopo, le modalità e i potenziali rischi del presente studio e di aver risposto alle domande postemi. [Luogo] Data (gg/mm/aa): Firma del medico: 5
NOTA INFORMATIVA E CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST- EXPERIENCED PER I TITOLARI DELLA POTESTÀ GENITORIALE SU UN MINORE
 NOTA INFORMATIVA E CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST- EXPERIENCED PER I TITOLARI DELLA POTESTÀ GENITORIALE SU UN MINORE (REScue Immunotolerance STudy Experienced Patients) Studio
NOTA INFORMATIVA E CONSENSO INFORMATO PER LA PARTECIPAZIONE ALLO STUDIO RESIST- EXPERIENCED PER I TITOLARI DELLA POTESTÀ GENITORIALE SU UN MINORE (REScue Immunotolerance STudy Experienced Patients) Studio
L IMMUNOTOLLERANZA RESCUE NEL BAMBINO CON EMOFILIA. Padova 13/14 maggio Chiara Biasoli Centro Emofilia Cesena
 L IMMUNOTOLLERANZA RESCUE NEL BAMBINO CON EMOFILIA Padova 13/14 maggio Chiara Biasoli Centro Emofilia Cesena Raccomandazioni AICE Obiettivo primario eradicazione Bambini principali candidati Intrapresa
L IMMUNOTOLLERANZA RESCUE NEL BAMBINO CON EMOFILIA Padova 13/14 maggio Chiara Biasoli Centro Emofilia Cesena Raccomandazioni AICE Obiettivo primario eradicazione Bambini principali candidati Intrapresa
Facsimile. prelievo di sangue (per analisi cliniche di laboratorio e per l estrazione di DNA)
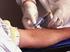 Consenso informato Dichiaro di aver preso visione del filmato informativo e di avere letto le informazioni inviatemi a casa. Mi è stato spiegato e mi è chiaro lo svolgimento, lo scopo e i rischi connessi
Consenso informato Dichiaro di aver preso visione del filmato informativo e di avere letto le informazioni inviatemi a casa. Mi è stato spiegato e mi è chiaro lo svolgimento, lo scopo e i rischi connessi
Informazione per il paziente. Raccolta di dati clinici di pazienti con tumore cerebrale per il gruppo cooperativo svizzero per lo studio del glioma
 Informazione per il paziente Raccolta di dati clinici di pazienti con tumore cerebrale per il gruppo cooperativo svizzero per lo studio del glioma Gentile Signora, gentile Signore, prenda il tempo necessario
Informazione per il paziente Raccolta di dati clinici di pazienti con tumore cerebrale per il gruppo cooperativo svizzero per lo studio del glioma Gentile Signora, gentile Signore, prenda il tempo necessario
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA.
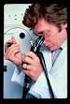 FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
Il processo del consenso informato
 Oncology Business Unit - GMO Il processo del consenso informato Alessandra Foietta GMO Training & Compliance Manager Negrar 21 Ottobre 2016 Definizione del consenso informato LINEE GUIDA PER LA BUONA PRATICA
Oncology Business Unit - GMO Il processo del consenso informato Alessandra Foietta GMO Training & Compliance Manager Negrar 21 Ottobre 2016 Definizione del consenso informato LINEE GUIDA PER LA BUONA PRATICA
MODULO DI CONSENSO INFORMATO ARMONIZZATO PER LE FORME AUTOSOMICHE DOMINANTI DI DEGENERAZIONE LOBARE FRONTOTEMPORALE
 Titolo del Progetto: NETWORK ITALIA PER LE FORME AUTOSOMICHE DOMINANTI DI MALATTIA DI ALZHEIMER E DI DEGENERAZIONE LOBARE FRONTOTEMPORALE MODULO DI CONSENSO INFORMATO ARMONIZZATO PER LE FORME AUTOSOMICHE
Titolo del Progetto: NETWORK ITALIA PER LE FORME AUTOSOMICHE DOMINANTI DI MALATTIA DI ALZHEIMER E DI DEGENERAZIONE LOBARE FRONTOTEMPORALE MODULO DI CONSENSO INFORMATO ARMONIZZATO PER LE FORME AUTOSOMICHE
PROCEDURE PER IL PRELIEVO BIOLOGICO
 Istituto di Ricerche Farmacologiche Mario Negri Milano 13 Aprile 2010 SOTTOPROGETTO ANALISI GENOME-WIDE PROCEDURE PER IL PRELIEVO BIOLOGICO 1 ORA CHE MI SONO CHIARI GLI OBIETTIVI COSA E COME CHE COSA DEVO
Istituto di Ricerche Farmacologiche Mario Negri Milano 13 Aprile 2010 SOTTOPROGETTO ANALISI GENOME-WIDE PROCEDURE PER IL PRELIEVO BIOLOGICO 1 ORA CHE MI SONO CHIARI GLI OBIETTIVI COSA E COME CHE COSA DEVO
SCHEDA INFORMATIVA INTERVENTO DI ASPORTAZIONE DI CALAZIO APPROVATA DALLA SOCIETA OFTALMOLOGICA ITALIANA NELL ANNO 2003
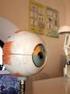 SCHEDA INFORMATIVA INTERVENTO DI ASPORTAZIONE DI CALAZIO APPROVATA DALLA SOCIETA OFTALMOLOGICA ITALIANA NELL ANNO 2003 Gentile Signora, Signore, Lei soffre di un calazio palpebrale. Questa scheda contiene
SCHEDA INFORMATIVA INTERVENTO DI ASPORTAZIONE DI CALAZIO APPROVATA DALLA SOCIETA OFTALMOLOGICA ITALIANA NELL ANNO 2003 Gentile Signora, Signore, Lei soffre di un calazio palpebrale. Questa scheda contiene
UNIVERSITÁ DEGLI STUDI MAGNA GRÆCIA DI CATANZARO
 SCHEDA INFORMATIVA E DICHIARAZIONE DI CONSENSO (per soggetti capace di fornire personalmente il consenso) SCHEDA INFORMATIVA Gentile Signora/e, In questa Azienda Ospedaliera è in programma una ricerca
SCHEDA INFORMATIVA E DICHIARAZIONE DI CONSENSO (per soggetti capace di fornire personalmente il consenso) SCHEDA INFORMATIVA Gentile Signora/e, In questa Azienda Ospedaliera è in programma una ricerca
INFORMATIVA AL PAZIENTE
 CEI FONDAZIONE PTV POLICLINICO TOR VERGATA SOP Procedure Operative Standard INFORMATIVA AL PAZIENTE Nessuna delle informazioni orali e scritte concernenti lo studio, compreso il modulo di consenso informato
CEI FONDAZIONE PTV POLICLINICO TOR VERGATA SOP Procedure Operative Standard INFORMATIVA AL PAZIENTE Nessuna delle informazioni orali e scritte concernenti lo studio, compreso il modulo di consenso informato
MODELLO INFORMATIVO. Informazioni relative all esame diagnostico HEAD-UP TILT TEST
 MODELLO INFORMATIVO Informazioni relative all esame diagnostico HEAD-UP TILT TEST Io sottoscritto/a nato/a. il. dichiaro di essere stato/a informato/a in data dal dr.. DI ESSERE AFFETTO DALLA SEGUENTE
MODELLO INFORMATIVO Informazioni relative all esame diagnostico HEAD-UP TILT TEST Io sottoscritto/a nato/a. il. dichiaro di essere stato/a informato/a in data dal dr.. DI ESSERE AFFETTO DALLA SEGUENTE
CONSENSO ALL ESECUZIONE DI TEST GENETICI
 CONSENSO ALL ESECUZIONE DI TEST GENETICI Io sottoscritto/a............................................................................ nato/a a.................................... (...... ) il....................................
CONSENSO ALL ESECUZIONE DI TEST GENETICI Io sottoscritto/a............................................................................ nato/a a.................................... (...... ) il....................................
SINOSSI. Titolo. Coordinatori e Promotori dello studio
 SINOSSI Titolo PLERIXAFOR (PLX) IN MODALITA ON DEMAND PER LA RACCOLTA DI CELLULE STAMINALI EMOPOIETICHE AUTOLOGHE IN PAZIENTI AFFETTI DA MIELOMA MULTIPLO DA LINFOMA CHE MOSTRINO POVERA MOBILIZZAZIONE DOPO
SINOSSI Titolo PLERIXAFOR (PLX) IN MODALITA ON DEMAND PER LA RACCOLTA DI CELLULE STAMINALI EMOPOIETICHE AUTOLOGHE IN PAZIENTI AFFETTI DA MIELOMA MULTIPLO DA LINFOMA CHE MOSTRINO POVERA MOBILIZZAZIONE DOPO
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE
 DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
INFORMATIVA PER IL PAZIENTE
 INFORMATIVA PER IL PAZIENTE (Mod. Versione 4 del 27 maggio 2013) 1) Finalità del trattamento dei dati personali Diagnosi e cura dei tumori rari. Ricerca retrospettiva e/o traslazionale sui tumori rari.
INFORMATIVA PER IL PAZIENTE (Mod. Versione 4 del 27 maggio 2013) 1) Finalità del trattamento dei dati personali Diagnosi e cura dei tumori rari. Ricerca retrospettiva e/o traslazionale sui tumori rari.
Altre patologie di rilievo :
 In data da parte del personale della U.O.C. di Diagnostica per Immagini di qeusto Istituto, mi è stata consegnata copia del presente modulo al fine di consentire un attenta lettura e valutazione di quanto
In data da parte del personale della U.O.C. di Diagnostica per Immagini di qeusto Istituto, mi è stata consegnata copia del presente modulo al fine di consentire un attenta lettura e valutazione di quanto
PLACEBO Aspetti etici e scientifici
 Aspetti etici e scientifici Definizione Placebo (dal latino, letteralmente piacerò) può essere definito ogni trattamento, o parte di esso, che viene deliberatamente impiegato per determinare un effetto
Aspetti etici e scientifici Definizione Placebo (dal latino, letteralmente piacerò) può essere definito ogni trattamento, o parte di esso, che viene deliberatamente impiegato per determinare un effetto
DESTINATARI TEMA CATEGORIE E SEZIONI DEL CONCORSO
 La Sezione Italiana di Amnesty International, in collaborazione con EGA Editore in occasione del 60 anniversario della Dichiarazione universale dei diritti umani bandisce il DESTINATARI Il Concorso è riservato
La Sezione Italiana di Amnesty International, in collaborazione con EGA Editore in occasione del 60 anniversario della Dichiarazione universale dei diritti umani bandisce il DESTINATARI Il Concorso è riservato
MODULO DI CONSENSO ALLA GASTROSCOPIA
 Ospedale San Donato - Arezzo Servizio di Endoscopia Digestiva MODULO DI CONSENSO ALLA GASTROSCOPIA Gentile Signore/a, attraverso l'opuscolo informativo che le è stato consegnato ha potuto conoscere le
Ospedale San Donato - Arezzo Servizio di Endoscopia Digestiva MODULO DI CONSENSO ALLA GASTROSCOPIA Gentile Signore/a, attraverso l'opuscolo informativo che le è stato consegnato ha potuto conoscere le
Classificazione clinica dell emofilia A e B
 Classificazione clinica dell emofilia A e B Gravità Grave Moderata Lieve Livello di FVIII/ IX < 1 % 1-5 % > 5 % < 40 % Caratteristiche cliniche Emorragie spontanee dalla prima infanzia; frequenti emartri
Classificazione clinica dell emofilia A e B Gravità Grave Moderata Lieve Livello di FVIII/ IX < 1 % 1-5 % > 5 % < 40 % Caratteristiche cliniche Emorragie spontanee dalla prima infanzia; frequenti emartri
Responsabile Centro Emofilia Sapienza Università di Roma; Associazione Italiana Centri Emofilia, AICE EMOFILIA: PERCORSI INTEGRATI DI CURA
 PROF.SSA MARIA GABRIELLA MAZZUCCONI Responsabile Centro Emofilia Sapienza Università di Roma; Associazione Italiana Centri Emofilia, AICE EMOFILIA: PERCORSI INTEGRATI DI CURA L emofilia, come le altre
PROF.SSA MARIA GABRIELLA MAZZUCCONI Responsabile Centro Emofilia Sapienza Università di Roma; Associazione Italiana Centri Emofilia, AICE EMOFILIA: PERCORSI INTEGRATI DI CURA L emofilia, come le altre
N cartella N ricovero Cognome Nome Data di nascita DICHIARAZIONE DI AVVENUTA INFORMAZIONE ED ESPRESSIONE DEL CONSENSO A TRATTAMENTO CHEMIOTERAPICO
 Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Direttore Sanitario: Dr.ssa Silvia Campagnari MAMMOGRAFIA
 Direttore Sanitario: Dr.ssa Silvia Campagnari MAMMOGRAFIA INFORMAZIONI COS E E un indagine che utilizza radiazioni ionizzanti (Raggi X), a basso dosaggio, per la diagnosi della patologia mammaria. Poiché
Direttore Sanitario: Dr.ssa Silvia Campagnari MAMMOGRAFIA INFORMAZIONI COS E E un indagine che utilizza radiazioni ionizzanti (Raggi X), a basso dosaggio, per la diagnosi della patologia mammaria. Poiché
Modulo di Consenso Informato
 Clinica Medica 4 DIPARTIMENTO DI MEDICINA - DIMED Università di Padova Direttore: Prof. GianPaolo Rossi Prospective Appraisal of the Prevalence of Primary Aldosteronism in HYpertensive Patients presenting
Clinica Medica 4 DIPARTIMENTO DI MEDICINA - DIMED Università di Padova Direttore: Prof. GianPaolo Rossi Prospective Appraisal of the Prevalence of Primary Aldosteronism in HYpertensive Patients presenting
Allegato IV. Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato IV Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 277 Conclusioni scientifiche Il CHMP ha preso in esame la raccomandazione del
Allegato IV Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 277 Conclusioni scientifiche Il CHMP ha preso in esame la raccomandazione del
INTERVENTO PER MORBO DI NOTTA
 INTERVENTO PER MORBO DI NOTTA 2 Nel pollice a scatto i tendini flessori sono compressi alla base del dito. L intervento consiste nella sezione della puleggia che li comprime (puleggia A1) Il morbo di Notta
INTERVENTO PER MORBO DI NOTTA 2 Nel pollice a scatto i tendini flessori sono compressi alla base del dito. L intervento consiste nella sezione della puleggia che li comprime (puleggia A1) Il morbo di Notta
ESAMI DI CITOGENETICA ISTRUZIONI OPERATIVE PER ESECUZIONE PRELIEVI
 ESAMI DI CITOGENETICA ISTRUZIONI OPERATIVE PER ESECUZIONE PRELIEVI CENTRO PRELIEVI LABORATORIO CENTRALE- VIA SAN MASSIMO 10 AZIENDA OSPEDALIERA DI PADOVA ESAMI DI CITOGENETICA Esecuzione del Prelievo:
ESAMI DI CITOGENETICA ISTRUZIONI OPERATIVE PER ESECUZIONE PRELIEVI CENTRO PRELIEVI LABORATORIO CENTRALE- VIA SAN MASSIMO 10 AZIENDA OSPEDALIERA DI PADOVA ESAMI DI CITOGENETICA Esecuzione del Prelievo:
Studio SOUND. Sentinel node vs. Observation after axillary UltrasouND
 Studio SOUND Sentinel node vs. Observation after axillary UltrasouND Lo IEO pubblica una collana di Booklets al fine di aiutare il paziente a gestire eventuali problematiche (quali ad esempio le terapie
Studio SOUND Sentinel node vs. Observation after axillary UltrasouND Lo IEO pubblica una collana di Booklets al fine di aiutare il paziente a gestire eventuali problematiche (quali ad esempio le terapie
MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1
 Appendice 6 MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1 Il presente parere del comitato etico è stato compilato e stampato dal sito internet dell
Appendice 6 MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1 Il presente parere del comitato etico è stato compilato e stampato dal sito internet dell
Domanda di conciliazione in ambito di responsabilità professionale medica
 Domanda di conciliazione in ambito di responsabilità professionale medica ai sensi dell art. 4/bis della legge provinciale 5 marzo 2001, n. 7, e successive modifiche, e del decreto del Presidente della
Domanda di conciliazione in ambito di responsabilità professionale medica ai sensi dell art. 4/bis della legge provinciale 5 marzo 2001, n. 7, e successive modifiche, e del decreto del Presidente della
INTERVENTO PER MORBO DI NOTTA
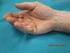 INTERVENTO PER MORBO DI NOTTA Nel pollice a scatto i tendini flessori sono compressi alla base del dito. L intervento consiste nella sezione della puleggia che li comprime (puleggia A1) 2 Il morbo di Notta
INTERVENTO PER MORBO DI NOTTA Nel pollice a scatto i tendini flessori sono compressi alla base del dito. L intervento consiste nella sezione della puleggia che li comprime (puleggia A1) 2 Il morbo di Notta
L EMOFILIA. Che cos è
 L EMOFILIA Che cos è L emofilia è una malattia rara di origine genetica che colpisce soprattutto i maschi. Se in un individuo sano la fuoriuscita di sangue dai vasi sanguigni si arresta rapidamente, chi
L EMOFILIA Che cos è L emofilia è una malattia rara di origine genetica che colpisce soprattutto i maschi. Se in un individuo sano la fuoriuscita di sangue dai vasi sanguigni si arresta rapidamente, chi
MODULO DI CONSENSO INFORMATO PER IL PAZIENTE
 Pagina 1 di 9 MODULO DI CONSENSO INFORMATO PER IL PAZIENTE Istruzioni per la compilazione del modulo: Prima di firmare il presente modulo, il paziente - o i genitori/tutori in caso di pazienti minori o
Pagina 1 di 9 MODULO DI CONSENSO INFORMATO PER IL PAZIENTE Istruzioni per la compilazione del modulo: Prima di firmare il presente modulo, il paziente - o i genitori/tutori in caso di pazienti minori o
Good Clinical Practice (ICH- GCP): principi generali. Alessandra Foietta GMO Training & Compliance Manager Negrar 21 Ottobre 2016
 Good Clinical Practice (ICH- GCP): principi generali Alessandra Foietta GMO Training & Compliance Manager Negrar 21 Ottobre 2016 Good Clinical Practice: cosa sono? Standard etico e di qualità internazionale
Good Clinical Practice (ICH- GCP): principi generali Alessandra Foietta GMO Training & Compliance Manager Negrar 21 Ottobre 2016 Good Clinical Practice: cosa sono? Standard etico e di qualità internazionale
CONSENSO INFORMATO. Giornate ANMDO Caterina Mineccia. aterina Mineccia
 CONSENSO INFORMATO Giornate ANMDO 2006 Caterina Mineccia CONSENSO Espressione della volontà del Paziente: l obbligo è sancito dalla Costituzione, da norme, dal codice deontologico medico, dalla Carta dei
CONSENSO INFORMATO Giornate ANMDO 2006 Caterina Mineccia CONSENSO Espressione della volontà del Paziente: l obbligo è sancito dalla Costituzione, da norme, dal codice deontologico medico, dalla Carta dei
RICHIESTA DI PARERE SU SPERIMENTAZIONE CLINICA DI DISPOSITIVO MEDICO
 COMITATO ETICO INTERAZIENDALE (istituito con Delibera n. 236 del 10/09/13 e successiva Delibera n. 267 del 25/10/13 ed iscritto al Registro Regionale al n. 2) Sede: Via Venezia n.16, 15121 tel.0131206974-6651
COMITATO ETICO INTERAZIENDALE (istituito con Delibera n. 236 del 10/09/13 e successiva Delibera n. 267 del 25/10/13 ed iscritto al Registro Regionale al n. 2) Sede: Via Venezia n.16, 15121 tel.0131206974-6651
Nota Informativa Importante. Guida alla Terapia per i Paziente. Guida alla Contraccezione. Modulo d'informazione e Consenso Informato
 AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
MODALITÀ DI ISCRIZIONE NUOVI SOCI A.I.S.F.
 Pag 1 di 5 MODALITÀ DI ISCRIZIONE NUOVI SOCI A.I.S.F. 1. La domanda di iscrizione deve essere corredata dal versamento della quota e può essere presentata dal 1 Gennaio di ciascun anno. All atto del versamento
Pag 1 di 5 MODALITÀ DI ISCRIZIONE NUOVI SOCI A.I.S.F. 1. La domanda di iscrizione deve essere corredata dal versamento della quota e può essere presentata dal 1 Gennaio di ciascun anno. All atto del versamento
INFORMAZIONI PRELIMINARI PER L ISCRIZIONE AL REGISTRO SCHEDA SBMA (Malattia di Kennedy)
 INFORMAZIONI PRELIMINARI PER L ISCRIZIONE AL REGISTRO SCHEDA SBMA (Malattia di Kennedy) Prima di iscriversi al presente Registro, è importante capire di cosa si tratta e come saranno utilizzati i dati
INFORMAZIONI PRELIMINARI PER L ISCRIZIONE AL REGISTRO SCHEDA SBMA (Malattia di Kennedy) Prima di iscriversi al presente Registro, è importante capire di cosa si tratta e come saranno utilizzati i dati
FedEmo Progetto Sa.Me.Da. L.I.F.E.
 FedEmo Progetto Sa.Me.Da. L.I.F.E. (Safety Medical Database - Local Informed For Emergency) Emofilia: la patologia L emofilia è una malattia rara di origine genetica dovuta ad un difetto della coagulazione
FedEmo Progetto Sa.Me.Da. L.I.F.E. (Safety Medical Database - Local Informed For Emergency) Emofilia: la patologia L emofilia è una malattia rara di origine genetica dovuta ad un difetto della coagulazione
Modello di proposta di inserimento di nuovo farmaco in P.T.O.U.
 ALLEGAT0 1 Modello di proposta di inserimento di nuovo farmaco in P.T.O.U. Alla Commissione Terapeutica Ospedaliera Unica Oggetto: Proposta di introduzione farmaco in P.T.O.U. Il sottoscritto Dott. Dirigente
ALLEGAT0 1 Modello di proposta di inserimento di nuovo farmaco in P.T.O.U. Alla Commissione Terapeutica Ospedaliera Unica Oggetto: Proposta di introduzione farmaco in P.T.O.U. Il sottoscritto Dott. Dirigente
Manuale per la somministrazione informatizzata del Questionario studente (CBT) 2016/2017
 Manuale per la somministrazione informatizzata del Questionario studente (CBT) 2016/2017 1 A.S. 2016-17 Manuale per la somministrazione informatizzata del Questionario studente (CBT) Data pubblicazione:
Manuale per la somministrazione informatizzata del Questionario studente (CBT) 2016/2017 1 A.S. 2016-17 Manuale per la somministrazione informatizzata del Questionario studente (CBT) Data pubblicazione:
U.O. Ortopedia e Traumatologia Direttore: Dott. Carlo Ranalletta. Consenso informato -chirurgia del piede-
 U.O. Ortopedia e Traumatologia Direttore: Dott. Carlo Ranalletta Consenso informato -chirurgia del piede- Casa di Cura Privata Di Lorenzo S.p.a. Via Veneto n. 37, 67051 Avezzano (AQ) Unità Operativa di
U.O. Ortopedia e Traumatologia Direttore: Dott. Carlo Ranalletta Consenso informato -chirurgia del piede- Casa di Cura Privata Di Lorenzo S.p.a. Via Veneto n. 37, 67051 Avezzano (AQ) Unità Operativa di
Diagnosi di laboratorio della malattia di Gaucher
 Diagnosi di laboratorio della malattia di Gaucher Studio delle alterazioni genetiche ed enzimatiche PROCEDURA PER L INVIO DEI DBS (Dried Blood Spot) Utilizzare un DBS uguale o simile all immagine e compilare
Diagnosi di laboratorio della malattia di Gaucher Studio delle alterazioni genetiche ed enzimatiche PROCEDURA PER L INVIO DEI DBS (Dried Blood Spot) Utilizzare un DBS uguale o simile all immagine e compilare
Lezione 16. Statistica. Alfonso Iodice D Enza Università degli studi di Cassino. Lezione 16. A. Iodice. Ipotesi statistiche
 Statistica Alfonso Iodice D Enza [email protected] Università degli studi di Cassino () Statistica 1 / 23 Outline 1 2 3 4 5 6 () Statistica 2 / 23 La verifica delle ipotesi Definizione Un ipotesi statistica
Statistica Alfonso Iodice D Enza [email protected] Università degli studi di Cassino () Statistica 1 / 23 Outline 1 2 3 4 5 6 () Statistica 2 / 23 La verifica delle ipotesi Definizione Un ipotesi statistica
CATETERISMO CARDIACO, CORONAROGRAFIA, ANGIOGRAFIA PERIFERICA CONSENSO INFORMATO CARDIOLOGIA INTERVENTISTICA PER EMODINAMICA E
 Dipartimento Cardio-Toraco-Vascolare e Area Critica Cardiologia Interventistica Dott. Antonio Manari - Direttore CONSENSO INFORMATO PER EMODINAMICA E CARDIOLOGIA INTERVENTISTICA CATETERISMO CARDIACO, CORONAROGRAFIA,
Dipartimento Cardio-Toraco-Vascolare e Area Critica Cardiologia Interventistica Dott. Antonio Manari - Direttore CONSENSO INFORMATO PER EMODINAMICA E CARDIOLOGIA INTERVENTISTICA CATETERISMO CARDIACO, CORONAROGRAFIA,
Dipartimento del Farmaco
 Dipartimento del Farmaco U. O. C. di Farmaceutica Ospedaliera VERBALE DI VERIFICA DEGLI ARMADI DI REPARTO (in collaborazione con la Direzione Sanitaria di Presidio, per valutare la corretta tenuta dei
Dipartimento del Farmaco U. O. C. di Farmaceutica Ospedaliera VERBALE DI VERIFICA DEGLI ARMADI DI REPARTO (in collaborazione con la Direzione Sanitaria di Presidio, per valutare la corretta tenuta dei
DOMANDA DI ACCOGLIMENTO
 DOMANDA DI ACCOGLIMENTO Nome: Residente a: Tipo ricovero: Permanente Temporaneo Diurno In convenzione Domanda Impegnativa S.VA.M.A. Notifica consenso trattamento dati Richiesta U.O.D. Soggetto autosufficiente
DOMANDA DI ACCOGLIMENTO Nome: Residente a: Tipo ricovero: Permanente Temporaneo Diurno In convenzione Domanda Impegnativa S.VA.M.A. Notifica consenso trattamento dati Richiesta U.O.D. Soggetto autosufficiente
PROCEDURA PER LA GESTIONE DEI PRODOTTI MEDICINALI SPERIMENTALI
 Modello 8 FARMACIA OSPEDALIERA PROCEDURA PER LA GESTIONE DEI PRODOTTI MEDICINALI SPERIMENTALI NORMATIVA DI RIFERIMENTO D.M. 27 aprile 1992 - Disposizioni sulle documentazioni tecniche da presentare a corredo
Modello 8 FARMACIA OSPEDALIERA PROCEDURA PER LA GESTIONE DEI PRODOTTI MEDICINALI SPERIMENTALI NORMATIVA DI RIFERIMENTO D.M. 27 aprile 1992 - Disposizioni sulle documentazioni tecniche da presentare a corredo
Modello di Cura (MdC) per le persone affette da Artrite Reumatoide
 Translation into: Completed by: Email: MdC 1 MdC 2 MdC 3 MdC 4 MdC 5 Italian Modello di Cura (MdC) per le persone affette da Artrite Reumatoide Annamaria Iuliano [email protected] Le persone
Translation into: Completed by: Email: MdC 1 MdC 2 MdC 3 MdC 4 MdC 5 Italian Modello di Cura (MdC) per le persone affette da Artrite Reumatoide Annamaria Iuliano [email protected] Le persone
La clinica delle sindromi emofiliche
 La clinica delle sindromi emofiliche MARIA ELISA MANCUSO Centro Emofilia e Trombosi Angelo Bianchi Bonomi Fondazione IRCCS Ca Granda, Ospedale Maggiore Policlinico Milano Siset Training Center: Corso Malattie
La clinica delle sindromi emofiliche MARIA ELISA MANCUSO Centro Emofilia e Trombosi Angelo Bianchi Bonomi Fondazione IRCCS Ca Granda, Ospedale Maggiore Policlinico Milano Siset Training Center: Corso Malattie
DOCUMENTO INFORMATIVO E DI CONSENSO INFORMATO PER I PARTECIPANTI ALLO STUDIO AFFETTI DA CMT E SOGGETTI DI CONTROLLO (VERSIONE 2 DEL 15/9/2014)
 DOCUMENTO INFORMATIVO E DI CONSENSO INFORMATO PER I PARTECIPANTI ALLO STUDIO AFFETTI DA CMT E SOGGETTI DI CONTROLLO (VERSIONE 2 DEL 15/9/2014) Titolo dello studio: REGISTRO NAZIONALE CMT: VERSO LA DEFINIZIONE
DOCUMENTO INFORMATIVO E DI CONSENSO INFORMATO PER I PARTECIPANTI ALLO STUDIO AFFETTI DA CMT E SOGGETTI DI CONTROLLO (VERSIONE 2 DEL 15/9/2014) Titolo dello studio: REGISTRO NAZIONALE CMT: VERSO LA DEFINIZIONE
1. Vorresti condividere qualcosa di te? Nickname. Nazionalità. Età. Nazione in cui risiedi attualmente. Sei una studentessa?
 INTRODUZIONE Perchè una indagine riguardante delle informazioni relative alla tua diagnosi? Per progettare un domani migliore per le ragazze e le donne con problemi emorragici e per valutare le migliori
INTRODUZIONE Perchè una indagine riguardante delle informazioni relative alla tua diagnosi? Per progettare un domani migliore per le ragazze e le donne con problemi emorragici e per valutare le migliori
INFORMAZIONI PER IL PAZIENTE CHE DEVE SOTTOPORSI A: IMPIANTO DI CONTROPULSATORE AORTICO
 INFORMAZIONI PER IL PAZIENTE CHE DEVE SOTTOPORSI A: IMPIANTO DI CONTROPULSATORE AORTICO 2 Per la diagnosi ed il trattamento delle seguenti patologie è indicato effettuare l impianto di un contropulsatore
INFORMAZIONI PER IL PAZIENTE CHE DEVE SOTTOPORSI A: IMPIANTO DI CONTROPULSATORE AORTICO 2 Per la diagnosi ed il trattamento delle seguenti patologie è indicato effettuare l impianto di un contropulsatore
I servizi coinvolti: I I Consultori il Presidio Ospedaliero di Pontedera e di Volterra
 Il Percorso IVG nella ASL 5 Procedura di Accoglienza e di presa in carico per il Percorso Interruzione Volontaria di Gravidanza (IVG) I servizi coinvolti: I I Consultori il Presidio Ospedaliero di Pontedera
Il Percorso IVG nella ASL 5 Procedura di Accoglienza e di presa in carico per il Percorso Interruzione Volontaria di Gravidanza (IVG) I servizi coinvolti: I I Consultori il Presidio Ospedaliero di Pontedera
E. O. Ospedali Galliera - Genova (L. 833/1978, art. 41; D. lgs n. 517/1993 art. 4 c. 12)
 E. O. Ospedali Galliera - Genova (L. 833/1978, art. 41; D. lgs n. 517/1993 art. 4 c. 12) Ospedale di rilievo nazionale e di alta specializzazione (D.P.C.M. 14 luglio 1995) Segreteria Amministrativa Comitato
E. O. Ospedali Galliera - Genova (L. 833/1978, art. 41; D. lgs n. 517/1993 art. 4 c. 12) Ospedale di rilievo nazionale e di alta specializzazione (D.P.C.M. 14 luglio 1995) Segreteria Amministrativa Comitato
TERAPIA CON DUODOPA. Biella, Ottobre D.S.Russo Mariangela Struttura Complessa di Neurologia
 TERAPIA CON DUODOPA Biella, Ottobre 2013 D.S.Russo Mariangela Struttura Complessa di Neurologia Terapia con DUODOPA Fase iniziale: terapia farmacologica convenzionale (L-Dopa in compresse) Fase avanzata:indicazione
TERAPIA CON DUODOPA Biella, Ottobre 2013 D.S.Russo Mariangela Struttura Complessa di Neurologia Terapia con DUODOPA Fase iniziale: terapia farmacologica convenzionale (L-Dopa in compresse) Fase avanzata:indicazione
Un esempio: CE Policlinico Gemelli
 Un esempio: CE Policlinico Gemelli Tipologia degli studi 32% 2% 3% 4% Farmacologici 41% 3% 9% 6% Diagnostici Chirurgici Anestesiologici Osservazionali Studi di laboratorio Dispositivi medici Radioterapia
Un esempio: CE Policlinico Gemelli Tipologia degli studi 32% 2% 3% 4% Farmacologici 41% 3% 9% 6% Diagnostici Chirurgici Anestesiologici Osservazionali Studi di laboratorio Dispositivi medici Radioterapia
residente a c.a.p. prov. n. MATRICOLA AZIENDALE QUALIFICA e CATEGORIA
 via n. Ricevuti lo Statuto e la nota informativa su COMETA DICHIARO DI ADERIRE al per i lavoratori dell Industria metalmeccanica, dell installazione Copia per COMETA via n. Ricevuti lo Statuto e la nota
via n. Ricevuti lo Statuto e la nota informativa su COMETA DICHIARO DI ADERIRE al per i lavoratori dell Industria metalmeccanica, dell installazione Copia per COMETA via n. Ricevuti lo Statuto e la nota
