Le vitamine sono sostanze organiche essenziali, molte di queste infatti non possono essere sintetizzate dall organismo
|
|
|
- Flavio Volpe
- 8 anni fa
- Visualizzazioni
Transcript
1
2 Le vitamine sono sostanze organiche essenziali, molte di queste infatti non possono essere sintetizzate dall organismo Sono precursori di molti coenzimi Il fabbisogno di queste sostanze dipende dalla vitamina ed è influenzato da età,, sesso, condizioni fisiologiche: allattamento gravidanza attività fisica ed alimentazione
3 con un alimentazione equilibrata, il fabbisogno giornaliero di vitamine è coperto; l alimentazione sbagliata (ad esempio poco variata) o anche disturbi nell assorbimento possono portare ad un apporto insufficiente di vitamine, la conseguenza è l ipovitaminosi che, in casi estremi sfocia nell avitaminosi il sovradosaggio di vitamine porta, solo nel caso delle vitamine A e D, ad ipervitaminosi con sintomi di intossicazioni
4 Le vitamine vengono classificate, in base alla loro solubilità,, in vitamine liposolubili e vitamine idrosolubili vitamine liposolubili: dal punto di vista chimico appartengono agli isoprenoidi,, tra queste ricordiamo le vitamine A, D, E, K ed F vitamine idrosolubili: classe variegata di vitamine formata da diversi tipi di molecole dal punto di vista chimico: B 1, B 2 (riboflavina, nicotinato, pantonenato), B 6, B 12, C ed H
5 Vitamine solubili in acqua
6 Vitamine solubili in acqua
7 Vitamine solubili in acqua
8 Le vitamine precursori di coenzimi
9 Vitamina B 1 La vitamina B 1, o tiamina, è formata da 2 sistemi ciclici un anello pirimidinico un anello tiazolico. N N N + S CH 3 H 3 C NH 2 OH
10 Vitamina B 1 La forma attiva della vitamina B 1 è la tiamina pirofosfato (TPP) Partecipa come coenzima gruppi aldeidici attivi per esempio di trasferimento di nella decarbossilazione ossidativa di α-chetoacidi nelle reazioni di transchetolasi nella via dell esosomonofosfato esosomonofosfato.
11 La transchetolasi trasferisce una unità bicarboniosa al sito dell anello tiazolico del coenzima, la tiamina pirofosfato l atomo di carbonio C-2 del TPP legato si ionizza facilmente per dare un carbanione Il risultante composto di addizione rilascia ilprodotto aldosico e si forma una unità di gliceraldeide attivata
12 Vitamina B 1 Una mancanza di questa vitamina causa il beriberi disturbi neurologici insufficienza cardiaca atrofia muscolare i cui sintomi sono
13 Vitamina B 2 La vitamina B 2, è un complesso di varie vitamine: O 1. Riboflavina 2. Folato 3. Nicotinato 4. Pantotenato O N N H H H N N CH 2 OH OH OH CH 2 OH CH 3 CH 3
14 Vitamina B 2 1. Riboflavina è un componente dei gruppi prostetici flavina mononucleotide (FMN)) e flavina adenina dinucleotide (FAD). FMN e FAD sono legati covalentemente a varie ossidoreduttasi e servono al trasferimento di elettroni e atomi di idrogeno. Avitaminosi specifiche non sono note
15 Vitamina B2 2. Folato (pteridina) è composto da 3 parti: H 2 N N OH N N N HN H O N COO- CH 2 H CH 2 COO- anello pteridinico gruppo dell acido para-ammino benzoico un residuo di glutammato Dopo riduzione a tetraidrofolato viene utilizzato come coenzima nel trasferimento di unità C1.
16 Vitamina B2 La mancanza di folato, che è abbastanza frequente, causa modificazioni nel quadro ematologico con: aumentata presenza di precursori anomali di megalociti (anemia megaloblastica), in quanto la sintesi degli acidi nucleici è alterata. In stadi avanzati della malattia si hanno ulteriori danni generali, in quanto anche la sintesi dei fosfolipidi e il metabolismo degli aminoacidi subiscono modificazioni
17 Vitamina B2 3. Nicotinato e nicotinammide: denominati anche niacina sono necessari per la biosintesi dei 2 coenzimi: nicotinammide adenina dinucleotide (NAD + ) nicotinammide adenina dinucleotide fosfato (NADP + ), Hanno la funzione di trasferire elettroni e atomi di idrogeno (ioni idruro o equivalenti riducenti). O COO- NH 2 N N
18 Vitamina B2 Gli animali sono in grado di trasformare il triptofano in nicotinato,, anche se con una resa bassa. Per questo motivo si riscontra avitaminosi solo quando nell alimentazione mancano contemporaneamente: nicotinato/nicotinammide e triptofano L avitaminosi si manifesta con disturbi della pelle pellagra) con disturbi della digestione depressione
19 Vitamina B2 Acido pantotenico C H 3 CH 3 O OH OH è l ammide acida di β-alanina e 2,4 diidrossi-3,3- dimetilbutirrato (pantoinato). Questa vitamina serve per la biosintesi del coenzima A (CoA) Partecipa al metabolismo di molti acidi carbossilici La proteina trasportatrice di acili (ACP) contiene pantotenato nel suo gruppo prostetico A causa dell ampia diffusione del pantotenato negli alimenti, le ipovitaminosi sono rare N H COO-
20 CH 3 B 1 H 3 C N N NH 2 N + S OH O N N CH 3 B 2 H H H CH 2 OH OH OH CH 2 OH O N N CH 3 Pteridina N OH N HN H O N COO- CH 2 H H 2 N N N CH 2 COO- Nicotina, Nicotinammide N COO- N O NH 2 Pantotenato C H 3 CH 3 O OH OH N H COO-
21 Vitamina B 6 La vitamina B 6, è costituita da un gruppo di 3 piridine sostituite: il piridossale il piridossolo O H la piridossamina HO CH 2 OH H 3 C N
22 Vitamina B 6 La forma attiva della vitamina B 6, il piridossalfosfato, coenzima importante nel metabolismo degli aminoacidi. Anche la glicogeno fosforilasi, l enzima della degradazione del glicogeno, contiene piridossalfosfato. L avitaminosi è rara
23 Vitamina B 12 Detta anche cobalamina, è un sistema ciclico complesso (corrina) contenente cobalto come atomo centrale. La vitamina viene sintetizzata esclusivamente dai microrganismi Si trova prevalentemente nel fegato ed anche nella carne, nelle uova e nel latte; non è invece presente nei prodotti di origine vegetale
24 Vitamina B 12 La vitamina viene assorbita solo se la mucosa gastrica secerne il cosiddetto fattore intriseco, una glicoproteina capace di legare la vitamina e la protegge così dalla degradazione. Anche nel sangue la vitamina è legata ad una proteina specifica, la transcobalamina. Il fegato può immagazzinare la vit. B 12.
25 La cobalamina partecipa al metabolismo dando reazioni di trasposizione Agisce come coenzima nella trasformazione di metilmalonil-coa in succinil- CoA Nella formazione di metionina ad omocisteina. I derivati della cobalamina partecipano anche nella riduzione di ribonucleotidi a deossiribonucleotidi. Avitaminosi o disturbi sono di solito causati dalla mancanza del fattore intrinseco e portano all anemia perniciosa
26 Vitamina C La vitamina C è l acido ascorbico. Solo gli esseri umani, le scimmie e i porcellini d India hanno bisogno di questa vitamina perché manca loro la l-gluconolattone ossidasi L enzima che catalizza l ultima reazione della trasformazione del glucosio in ascorbato La vitamina C si trova in particolare nella frutta e nella verdura fresca; a molte bevande rinfrescanti e alimenti viene aggiunto acido ascorbico sintetico. La bollitura distrugge lentamente la vitamina.
27 Nell organismo serve come riducente in varie reazioni, tra cui : HO O la sintesi del collageno la degradazione della tirosina la sintesi delle catecolamine la biosintesi degli acidi biliari HO HO Il fabbisogno giornaliero di vitamina C è di 60 mg ed è quindi relativamente alto per una vitamina. L ipovitaminosi C non è rara, si manifesta dopo alcuni mesi sotto forma di scorbuto, malattia caratterizzata da danni del tessuto connettivo, emorragie e perdita di denti O H CH 2 OH
28 O Vitamina H HN NH La vitamina H, o biotina, si trova nel fegato, nel tuorlo d uovo ed in altri alimenti e viene anche sintetizzata dalla flora intestinale. Nell organismo la biotina è legata covalentemente, attraverso una catena laterale della lisina, ad enzimi che catalizzano reazioni di carbossilazione, ad esempio la piruvato carbossilasi. S COO-
29 Vitamina H La biotina viene legata con alta specificità dall avidina, una proteina che si trova nel bianco d uovo. La bollitura denatura l avidina, quindi solo il consumo di albume crudo porta alla mancanza della vitamina.
30 O H B 6 HO CH 2 OH H 3 C N B 12 HO O C HO HO O H CH 2 OH O H HN NH S COO-
31 Coenzimi In molte reazioni catalizzate da enzimi vengono trasferiti elettroni o gruppi di atomi da un substrato donatore ad un accettore. A queste reazioni partecipano sempre altre molecole che legano temporaneamente il gruppo da trasferire. Queste molecole di assistenza vengono dette coenzimi
32 Sulla base dell'interazione con l'enzima, questi composti possono essere suddivisi in: (1) coenzimi solubili (2) gruppi prostetici (3) Coenzimi redox (1) I coenzimi solubili durante il ciclo catalitico, si legano all'enzima come substrati, vengono modificati chimicamente e poi rilasciati nella soluzione. La forma iniziale del coenzima viene rigenerata attraverso una seconda reazione indipendente.
33 (2) I coenzimi saldamente legati ad un enzima non si dissociano alla fine del ciclo catalitico e vengono chiamati gruppi prostetici Il gruppo legato dal coenzima viene poi trasferito ad un substrato accettore dello stesso enzima.
34 (3) Coenzimi redox Tutte le ossidoreduttasi coenzimi. utilizzano Nelle reazioni redox,, insieme agli elettroni,, vengono trasferiti da una molecola ad un'altra anche uno o due protoni. Per questo motivo si dice che vengono trasferiti equivalenti riducenti.
35 I nucleotidi piridinici NAD + e NADP + (1) sono i coenzimi di molte deidrogenasi. Essi trasportano ioni idruro (2e- e 1H + ) e agiscono sempre in forma solubile. NAD + trasporta equivalenti riducenti dalle vie cataboliche alla catena respiratoria e serve per il metabolismo energetico. NADP + invece raccoglie elettroni da utilizzare nelle più importanti biosintesi
36 Questi nucleotidi contengono adenosina legata ad un nucleotide nicotinamidico. Il NADP+ contiene un ulteriore gruppo fosforico sull ossidrile in posizione 2 dell adenosina
37 I coenzimi flavinici FMN e FAD (2) sono per lo più saldamente legati ad enzimi. Il gruppo redox attivo dei due coenzimi è costituito dalla flavina (isoallossazina), un sistema a tre anelli che può assumere nella forma ridotta due eletttoni e due protoni. FMN contiene il ribitolo un polialcol a cinque atomi di carbonio in forma fosforilata;
38 FAD si forma dall'fmn mediante legame con l'amp. I due coenzimi sono funzionalmente paragonabili e sono utilizzati dalle deidrogenasi ossidasi monoossigenasi
39 Flavina adenina dinucleotide (FAD). L adenosina è legata alla riboflaviva mediante due gruppi fosforici.
40 (3) Nell'acido lipoico il centro redox attivo è rappresentato da un ponte disolfuro intramolecolare. L'acido lipoico attivo è legato covalentemente ad un residuo di lisina (R') dell'enzima e partecipa soprattutto alla decarbossilazione ossidativa di 2-chetoacidi2 chetoacidi.
41 La funzione dell'ubichinone o coenzima Q è quella di trasportatore mobile di elettroni e protoni nell ambito della catena respiratoria. Con la riduzione, il chinone si trasforma nella forma aromatica di idrochinone.
42 Emogruppi che svolgono la funzione di cofattori redox sono presenti nella catena respiratoria fotosintesi monoossigenasi perossidasi. A differenza di quanto accade nell'emoglobina, in questi casi lo ione ferro cambia valenza.
43 Coenzimi per il trasferimento di gruppi I nucleosidi fosfato non sono solo i precursori della biosintesi degli acidi nucleici, ma possiedono anche funzioni coenzimatiche Essi servono per la conservazione dell'energia e rendono possibili processi endoergonici,, mediante accoppiamento energetico (CTP, GTP,UTP)
44 I metaboliti vengono spesso resi più reattivi (attivatti) mediante il trasferimento nella loro molecola di residui fosfatidici (fosforilazione). Il legame di zuccheri a nucleosidi difosfato genera molecole reattive che si comportano da precursori nella sintesi dei polisaccaridi e dei lipidi.
45 L energia presente nei nucleosidi trifosfato viene utilizzata nelle reazioni di formazione di legami chimici catalizzate dalle ligasi.
46 I residui acilici vengono attivati mediante il legame al coenzima A In questo composto, la pantoteina è legata al 3'-fosfo fosfo-adp mediante un legame estere. La pantoteina è formata da tre componenti uniti da legami ammidici: 1. una vitamina 2. la β-alanina che si forma dalla decarbossilazione dell'aspartato 3. la cisteammina, un'ammina che trae origine dalla decarbossilazione della cisteina.
47 Mediante la reazione del gruppo tiolico del residuo cisteamminico con un gruppo carbossilico si forma un tioestere, per esempio l'acetil-coa. Questa reazione è fortemente endoergonica e di conseguenza accoppiata a processi esoergonici.
48 I tioesteri rappresentano la forma attivata degli acidi organici, quando i residui acilici devono essere trasferiti da una molecola ad un'altra. Nel metabolismo, questo processo viene utilizzato frequentemente.
49 Questo derivato dell adenosina trasporta gruppi acilici uniti in modo covalente mediante legami tioesteri al suo gruppo sulfidrilico. CoA
50 La tiamina pirofosfato è in grado di attivare aldeidi o chetoni sotto forma di gruppi idrossialchilici e di donarli poi ad altre molecole. Questo tipo di trasferimento di gruppi è importante per esempio nella reazione della transchetolasi.
51 Residui idrossi-alchilici si formano anche nella decarbossilazione dei chetoacidi. Essi vengono liberati sotto forma di aldeidi o trasferiti al gruppo prostetico lipoammide, come nel caso delle 2- chetoacido deidrogenasi
52 Il piridossalfosfato E il coenzima più importante nel metabolismo degli amminoacidi. Il piridossalfosfato partecipa anche ad altre reazioni in cui sono coinvolti gli amminoacidi, come le loro decarbossilazioni o deidratazioni.
53 La forma aldeidica del piridossalfosfato non esiste in forma lineare. In assenza di substrati il gruppo aldeidico è legato, con formazione di aldimmina (base di Schiff protonata), al gruppo ε-amminico di un residuo di lisina dell'enzima.
54 Le carbossilasi Hanno come enzima la biotina unita all'enzima con un legame ammidico tra il gruppo carbossilico della sua catena laterale ed un residuo di lisina dell'enzima. La biotina reagisce con il bicarbonato (HCO 3- ) per formare N-carbossibiotina. La reazione richiede ATP. Questa forma attivata dell'anidride carbonica può essere trasferita ad altre molecole.
55 La sintesi di malonil-coa dall'acetil acetil-coa oppure la formazione di ossalacetato dal piruvato sono esempi di reazioni dipendenti dalla biotina
56 Il tetraidrofolato (THF) è un coenzima che può trasferire unità monocarboniose a vari livelli di ossidazione. Il THF deriva dalla vitamina acido folico, mediante duplice idratazione dell'anello pterinico.
57 Le unità monocarboniose possono essere Le unit possono essere legate agli atomi di azoto N-5N o N-1O o, in alcuni casi, ad entrambi. I derivati più importanti del THF sono: a.n formil-thf, in cui l'unità monocarboniosa ha lo stato di ossidazione di un gruppo carbossilico; b.n 5,N,N 10 -metilene-tfh in cui l'unità monocarboniosa ha lo stato di ossidazione di un gruppo aldeidico;
58 c. N5-metile metile-thf in cui l'unità monocarboniosa ha lo stato di ossidazione di un gruppo alcolico. Le unità monocarboniose che vengono trasferite dal THF servono nelle sintesi di nucleotidi purinici del dtmp della metionina.
-uno o più IONI INORGANICI
 Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
TIAMINA (vitamina B1, aneurina)
 TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
F. G. Hopkins, C. Eijkman: Scoperta della Vitamina B1 (tiamina) (Premio Nobel per la medicina nel 1929)
 VITAMINE Gruppo eterogeneo di composti chimici di natura organica indispensabili in piccole quantità (milligrammi o microgrammi) per consentire il funzionamento dell organismo e del metabolismo Non vengono
VITAMINE Gruppo eterogeneo di composti chimici di natura organica indispensabili in piccole quantità (milligrammi o microgrammi) per consentire il funzionamento dell organismo e del metabolismo Non vengono
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
Cofattori e vitamine
 Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Ruolo metabolico delle flavine
 Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Coenzimi. Ioni essenziali. Molti coenzimi hanno come precursori le vitamine.
 COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
VITAMINE. Classificazione Liposolubili e idrosolubili (la solubilità influenza il loro modo di essere assorbite, accumulate ed escrete).
 VITAMINE Definizione Composti organici che agiscono in piccolissime quantità nell organismo animale promuovendo e regolando numerose funzioni metaboliche. Classificazione Liposolubili e idrosolubili (la
VITAMINE Definizione Composti organici che agiscono in piccolissime quantità nell organismo animale promuovendo e regolando numerose funzioni metaboliche. Classificazione Liposolubili e idrosolubili (la
Metabolismo degli amminoacidi. Ciclo dell urea
 Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
VITAMINE IDROSOLUBILI
 VITAMINE IDROSOLUBILI VITAMINA B1 o TIAMINA formula di struttura Stabile in soluzione acida Sensibile al calore, alle basi e alla luce UV VITAMINA B1 assorbimento Sito di assorbimento: duodeno tramite
VITAMINE IDROSOLUBILI VITAMINA B1 o TIAMINA formula di struttura Stabile in soluzione acida Sensibile al calore, alle basi e alla luce UV VITAMINA B1 assorbimento Sito di assorbimento: duodeno tramite
Transferasi che hanno come coenzima FOSFOPANTOTEINA E COENZIMA A (derivati dalla VITAMINA B3 )
 Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 24
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
glicogeno Glucosio 6-P Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
Prof.ssa Maria Luisa Eliana Luisi
 Corso Integrato Scienze Tecniche Dietetiche Applicate MED/49 Scienze Tecniche Dietetiche Anno Accademico 2011-12 Le Vitamine Prof.ssa Maria Luisa Eliana Luisi Le Vitamine Conosciamo le vitamine dall 800;
Corso Integrato Scienze Tecniche Dietetiche Applicate MED/49 Scienze Tecniche Dietetiche Anno Accademico 2011-12 Le Vitamine Prof.ssa Maria Luisa Eliana Luisi Le Vitamine Conosciamo le vitamine dall 800;
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Da dove prendono energia le cellule animali?
 Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
METABOLISMO DEI LIPIDI
 METABOLISMO DEI LIPIDI Generalità I lipidi alimentari, per poter essere assorbiti dall organismo umano, devono essere preventivamente digeriti (ad eccezione del colesterolo), cioè, trasformati in molecole
METABOLISMO DEI LIPIDI Generalità I lipidi alimentari, per poter essere assorbiti dall organismo umano, devono essere preventivamente digeriti (ad eccezione del colesterolo), cioè, trasformati in molecole
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Si possono suddividere in:
 Si possono suddividere in: LIPIDI DI DEPOSITO: si accumulano nelle cellule del tessuto adiposo, sono una riserva energetica, mantengono costante la temperatura del corpo (termogenesi) LIPIDI STRUTTURALI:
Si possono suddividere in: LIPIDI DI DEPOSITO: si accumulano nelle cellule del tessuto adiposo, sono una riserva energetica, mantengono costante la temperatura del corpo (termogenesi) LIPIDI STRUTTURALI:
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 18
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 18 I meccanismi di catalisi Concetti chiave: Le catene laterali degli amminoacidi in grado di donare o accettare protoni possono
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 18 I meccanismi di catalisi Concetti chiave: Le catene laterali degli amminoacidi in grado di donare o accettare protoni possono
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
NIACINA (vitamina B3 o PellagraPreventing)
 NIACINA (vitamina B3 o PellagraPreventing) (vitameri: ACIDO NICOTINICO, NICOTINAMMIDE o NIACINAMMIDE) Fonti alimentari: carni, fegato, cereali, legumi, tè, caffè RDA: 18 (M)-14 (F) mg NE/die Coenzima:
NIACINA (vitamina B3 o PellagraPreventing) (vitameri: ACIDO NICOTINICO, NICOTINAMMIDE o NIACINAMMIDE) Fonti alimentari: carni, fegato, cereali, legumi, tè, caffè RDA: 18 (M)-14 (F) mg NE/die Coenzima:
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
Il metabolismo del glicogeno e la gluconeogenesi. Copyright 2013 Zanichelli editore S.p.A.
 Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
PROTEINA GREGGIA (P.G.)
 PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
Alimentazione (uomo)
 Alimentazione (uomo) Macronutrienti Decine di grammi Proteine Lipidi Carboidrati Micronutrienti < 1 g Per ciascun micronutriente è stata definita la RDA (Recommended Daily Allowance, razione giornaliera
Alimentazione (uomo) Macronutrienti Decine di grammi Proteine Lipidi Carboidrati Micronutrienti < 1 g Per ciascun micronutriente è stata definita la RDA (Recommended Daily Allowance, razione giornaliera
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare e energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare e energia. La quantità di energia
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
FUNZIONI DEI MITOCONDRI
 FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE)
 a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
Domande relative alla specializzazione in: Biochimica clinica
 Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
ALIMENTAZIONE NELL UOMO
 ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
Vitamine: generalità Vitamina C Vitamine del complesso B
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica Prof.ssa Luciana Avigliano 2014 Vitamine: generalità Vitamina C Vitamine del complesso B VITAMINE Micronutrienti organici, richiesti
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica Prof.ssa Luciana Avigliano 2014 Vitamine: generalità Vitamina C Vitamine del complesso B VITAMINE Micronutrienti organici, richiesti
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
ANTIOSSIDANTI Grassi IV LEZIONE
 ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
METABOLISMO DEL Glucosio
 METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
Catena di Trasporto degli elettroni
 Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Il flusso dell informazione genetica il ruolo dei polimeri di nucleotidi
 Il flusso dell informazione genetica il ruolo dei polimeri di nucleotidi trascrizione traduzione DNA RNA Proteina replicazione DNA replicazione: sintesi del DNA trascrizione: sintesi del RNA traduzione:
Il flusso dell informazione genetica il ruolo dei polimeri di nucleotidi trascrizione traduzione DNA RNA Proteina replicazione DNA replicazione: sintesi del DNA trascrizione: sintesi del RNA traduzione:
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
La digestione degli alimenti
 La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
ALLEGATO II COMPOSIZIONE ESSENZIALE DEGLI ALIMENTI DI PROSEGUIMENTO DOPO RICOSTITUZIONE SECONDO LE ISTRUZIONI DEL PRODUTTORE
 ALLEGATO II COMPOSIZIONE ESSENZIALE DEGLI ALIMENTI DI PROSEGUIMENTO DOPO RICOSTITUZIONE SECONDO LE ISTRUZIONI DEL PRODUTTORE I valori indicati nel presente allegato si riferiscono al prodotto finale pronto
ALLEGATO II COMPOSIZIONE ESSENZIALE DEGLI ALIMENTI DI PROSEGUIMENTO DOPO RICOSTITUZIONE SECONDO LE ISTRUZIONI DEL PRODUTTORE I valori indicati nel presente allegato si riferiscono al prodotto finale pronto
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono
 Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
unità C2. Le trasformazioni energetiche nelle cellule
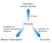
 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Dott.ssa Sara Pacchini
 Dott.ssa Sara Pacchini Radicali liberi Molecole o frammenti di molecole con uno o più e - spaiati negli orbitali esterni Per completare il loro ottetto sottraggono e - ad altre molecole Anione superossido
Dott.ssa Sara Pacchini Radicali liberi Molecole o frammenti di molecole con uno o più e - spaiati negli orbitali esterni Per completare il loro ottetto sottraggono e - ad altre molecole Anione superossido
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
Gli Alimenti Classificazione degli alimenti Alimenti semplici o principi alimentari o principi nutritivi o nutrienti inorganici organici
 Prof. Carlo Carrisi Gli Alimenti Classificazione degli alimenti Alimenti semplici o principi alimentari o principi nutritivi o nutrienti: servono a nutrire l organismo, derivano dalla digestione, vengono
Prof. Carlo Carrisi Gli Alimenti Classificazione degli alimenti Alimenti semplici o principi alimentari o principi nutritivi o nutrienti: servono a nutrire l organismo, derivano dalla digestione, vengono
Metabolismo dei composti azotati: aminoacidi e nucleotidi
 Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
FIACCHEZZA, STANCHEZZA, MALESSERE MORALE. Carenza di ferro molto diffusa e spesso sottovalutata
 FIACCHEZZA, STANCHEZZA, MALESSERE MORALE Carenza di ferro molto diffusa e spesso sottovalutata Cari pazienti! Vi sentite spesso fiacchi, stanchi, esauriti o giù di morale? Soffrite facilmente il freddo?
FIACCHEZZA, STANCHEZZA, MALESSERE MORALE Carenza di ferro molto diffusa e spesso sottovalutata Cari pazienti! Vi sentite spesso fiacchi, stanchi, esauriti o giù di morale? Soffrite facilmente il freddo?
A livello della loro struttura chimica, come i grassi, anche i carboidrati sono composti ternari, formati cioè da tre molecole:
 I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE. L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO
 GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
Nota dell editore Presentazione
 00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
Mais, riso, patate, granozucchero di canna o barbabietola Latte da zucchero Polisaccaride Amido - - Disaccaride Maltosio Saccarosio Lattosio
 Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
Amminoacidi e Proteine
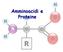 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
GLICOGENOLISI & GLICOGENOSINTESI
 GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
: : H-Cl + H-N: H-N-H + : Cl : H
 Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Fosforilazione ossidativa
 Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara
 Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Le proteine. Le proteine sono i mattoncini che costituiscono gli organismi viventi.
 Le proteine Le proteine sono i mattoncini che costituiscono gli organismi viventi. Per avere un idea più precisa, basti pensare che tutti i muscoli del nostro corpo sono composti da filamenti di proteine
Le proteine Le proteine sono i mattoncini che costituiscono gli organismi viventi. Per avere un idea più precisa, basti pensare che tutti i muscoli del nostro corpo sono composti da filamenti di proteine
DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY
 DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY Una reazione acido/base coinvolge un trasferimento di protone: l'acido è il donatore di protone e la base è l'accettore del protone. Questa definizione spiega
DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY Una reazione acido/base coinvolge un trasferimento di protone: l'acido è il donatore di protone e la base è l'accettore del protone. Questa definizione spiega
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I G L U C I D I ASPETTI GENERALI
 I G L U C I D I ASPETTI GENERALI I glucidi sono i costituenti più importanti dei vegetali e le sostanze organiche più diffuse nella biosfera. Rappresentano solo l 1% del corpo umano ma hanno una notevole
I G L U C I D I ASPETTI GENERALI I glucidi sono i costituenti più importanti dei vegetali e le sostanze organiche più diffuse nella biosfera. Rappresentano solo l 1% del corpo umano ma hanno una notevole
La fotosintesi: energia dal Sole
 La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
COENZIMI. Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica.
 COENZIMI Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
PROGRAMMA DI CHIMICA E SCIENZE DELLA TERRA CLASSE V SEZ. D. Liceo A. Labriola a.s. 2015/2016
 PROGRAMMA DI CHIMICA E SCIENZE DELLA TERRA CLASSE V SEZ. D Liceo A. Labriola a.s. 2015/2016 CHIMICA: Testo in adozione: J. E. Brady, F. Senese, N. Taddei, H. Kreuzer, A. Massey Dal carbonio al biotech.
PROGRAMMA DI CHIMICA E SCIENZE DELLA TERRA CLASSE V SEZ. D Liceo A. Labriola a.s. 2015/2016 CHIMICA: Testo in adozione: J. E. Brady, F. Senese, N. Taddei, H. Kreuzer, A. Massey Dal carbonio al biotech.
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
PIRIDOSSALE-FOSFATO (PLP)
 PIRIDOSSALE-FOSFATO (PLP) Deriva dalla famiglia delle Vitamine B 6 (piridossale, piridossina) Il PLP è il gruppo prostetico di enzimi che catalizzano transamminazione, decarbossilazione, racemizzazione
PIRIDOSSALE-FOSFATO (PLP) Deriva dalla famiglia delle Vitamine B 6 (piridossale, piridossina) Il PLP è il gruppo prostetico di enzimi che catalizzano transamminazione, decarbossilazione, racemizzazione
